文档内容
第二章能力提升检测卷
完卷时间:90分钟
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu 64 Ag 108
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2021·浙江金华市·高三一模)下列方程式不正确的是
A.硫代硫酸钠溶液中加入稀硝酸:
B.熟石膏加水变成生石膏:
C.金属钠与水反应:
D. 溶液与过量 溶液混合后共热:
2.(2021·浙江台州市·高三二模)已知: ,下列说法正确的是
A. 是氧化剂
B.HIO得电子,发生氧化反应
C.该反应的氧化产物与还原产物的物质的量之比为1:2
D.通过该反应可说明HIO的氧化性强于
3.(2021·广东深圳市·高三二模)下列有关物质分类的说法错误的是
A.SiO、PO 均为酸性氧化物 B.碘酒、水玻璃均为混合物
2 2 5
C.糖类、蛋白质均为高分子化合物 D.NaCl晶体、HCl气体均为电解质
4.(2021·上海浦东新区·高三二模)某新型氨氮去除技术中的含氮物质转化关系如图所示。下列说法
正确的是
A.过程Ⅰ还需要加入氧化剂B.过程Ⅱ反应后酸性减弱
C.过程Ⅲ中,参与反应的 与 的物质的量之比为4∶3
D.过程Ⅰ、Ⅱ、Ⅲ的总反应为:
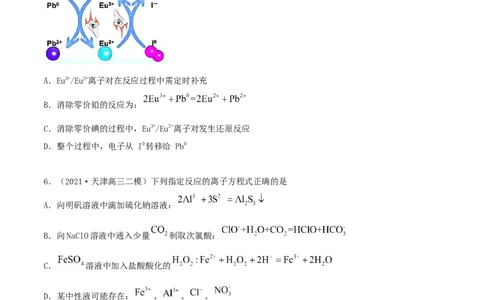
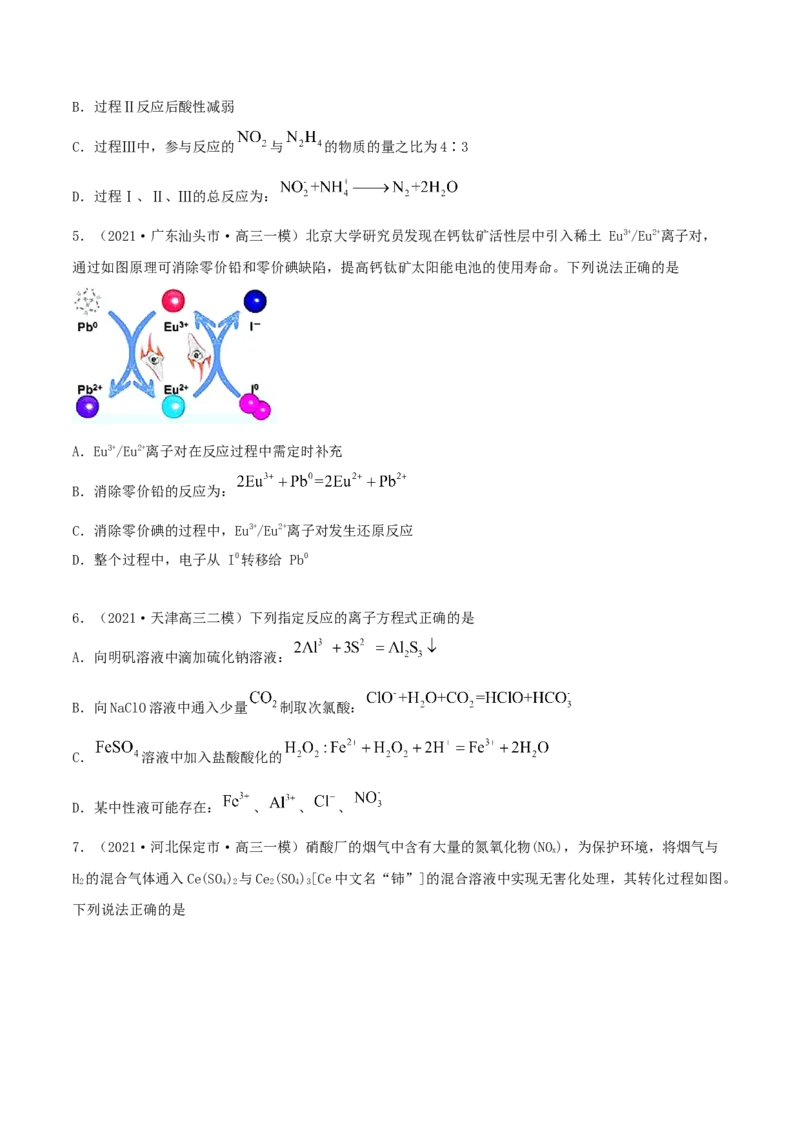
5.(2021·广东汕头市·高三一模)北京大学研究员发现在钙钛矿活性层中引入稀土 Eu3+/Eu2+离子对,
通过如图原理可消除零价铅和零价碘缺陷,提高钙钛矿太阳能电池的使用寿命。下列说法正确的是
A.Eu3+/Eu2+离子对在反应过程中需定时补充
B.消除零价铅的反应为:
C.消除零价碘的过程中,Eu3+/Eu2+离子对发生还原反应
D.整个过程中,电子从 I0转移给 Pb0
6.(2021·天津高三二模)下列指定反应的离子方程式正确的是
A.向明矾溶液中滴加硫化钠溶液:
B.向NaClO溶液中通入少量 制取次氯酸:
C. 溶液中加入盐酸酸化的
D.某中性液可能存在: 、 、 、
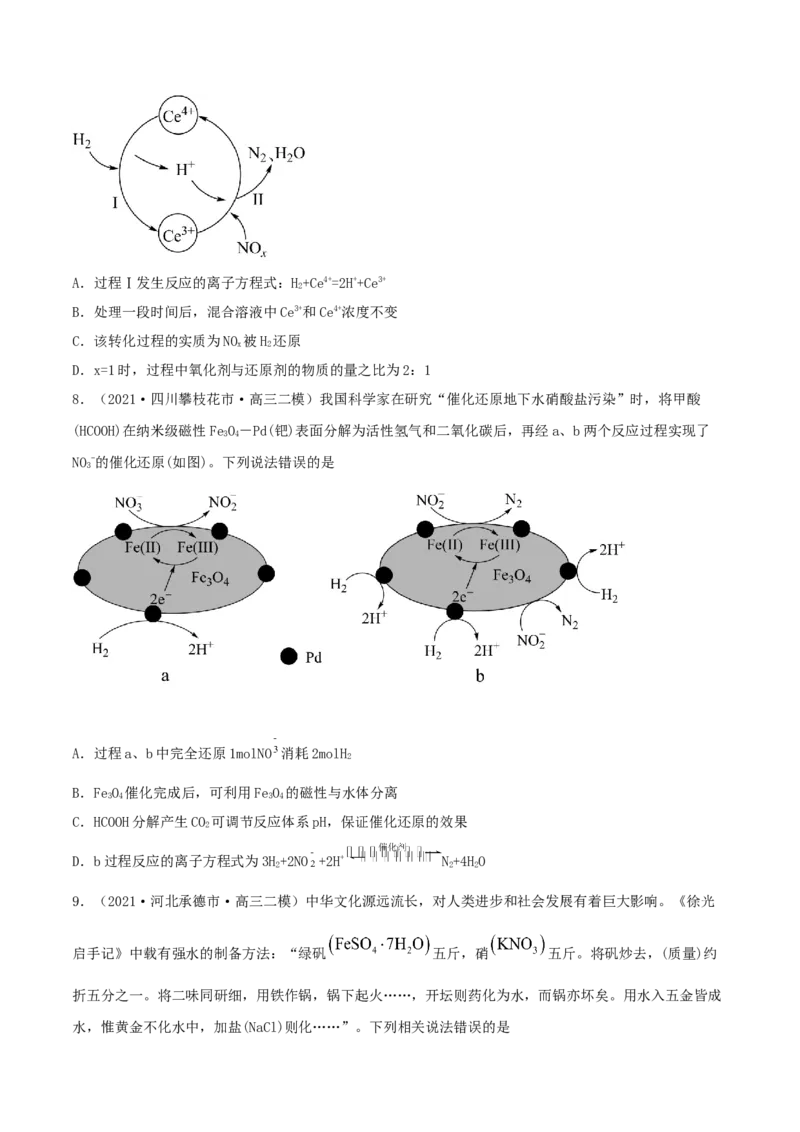
7.(2021·河北保定市·高三一模)硝酸厂的烟气中含有大量的氮氧化物(NO),为保护环境,将烟气与
x
H 的混合气体通入Ce(SO) 与Ce(SO)[Ce中文名“铈”]的混合溶液中实现无害化处理,其转化过程如图。
2 4 2 2 4 3
下列说法正确的是A.过程Ⅰ发生反应的离子方程式:H+Ce4+=2H++Ce3+
2
B.处理一段时间后,混合溶液中Ce3+和Ce4+浓度不变
C.该转化过程的实质为NO 被H 还原
x 2
D.x=1时,过程中氧化剂与还原剂的物质的量之比为2:1
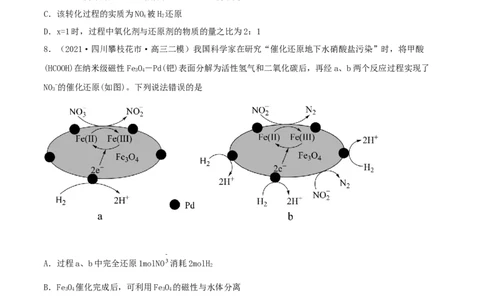
8.(2021·四川攀枝花市·高三二模)我国科学家在研究“催化还原地下水硝酸盐污染”时,将甲酸
(HCOOH)在纳米级磁性FeO-Pd(钯)表面分解为活性氢气和二氧化碳后,再经a、b两个反应过程实现了
3 4
NO-的催化还原(如图)。下列说法错误的是
3
A.过程a、b中完全还原1molNO 消耗2molH
2
B.FeO 催化完成后,可利用FeO 的磁性与水体分离
3 4 3 4
C.HCOOH分解产生CO 可调节反应体系pH,保证催化还原的效果
2
D.b过程反应的离子方程式为3H+2NO +2H+ N+4HO
2 2 2
9.(2021·河北承德市·高三二模)中华文化源远流长,对人类进步和社会发展有着巨大影响。《徐光
启手记》中载有强水的制备方法:“绿矾 五斤,硝 五斤。将矾炒去,(质量)约
折五分之一。将二味同研细,用铁作锅,锅下起火……,开坛则药化为水,而锅亦坏矣。用水入五金皆成
水,惟黄金不化水中,加盐(NaCl)则化……”。下列相关说法错误的是A.“炒”矾时绿矾失去全部结晶水
B.强水中加盐后形成王水能溶解金
C.硝的焰色试验中火焰呈紫色
D.制备强水过程中涉及氧化还原反应
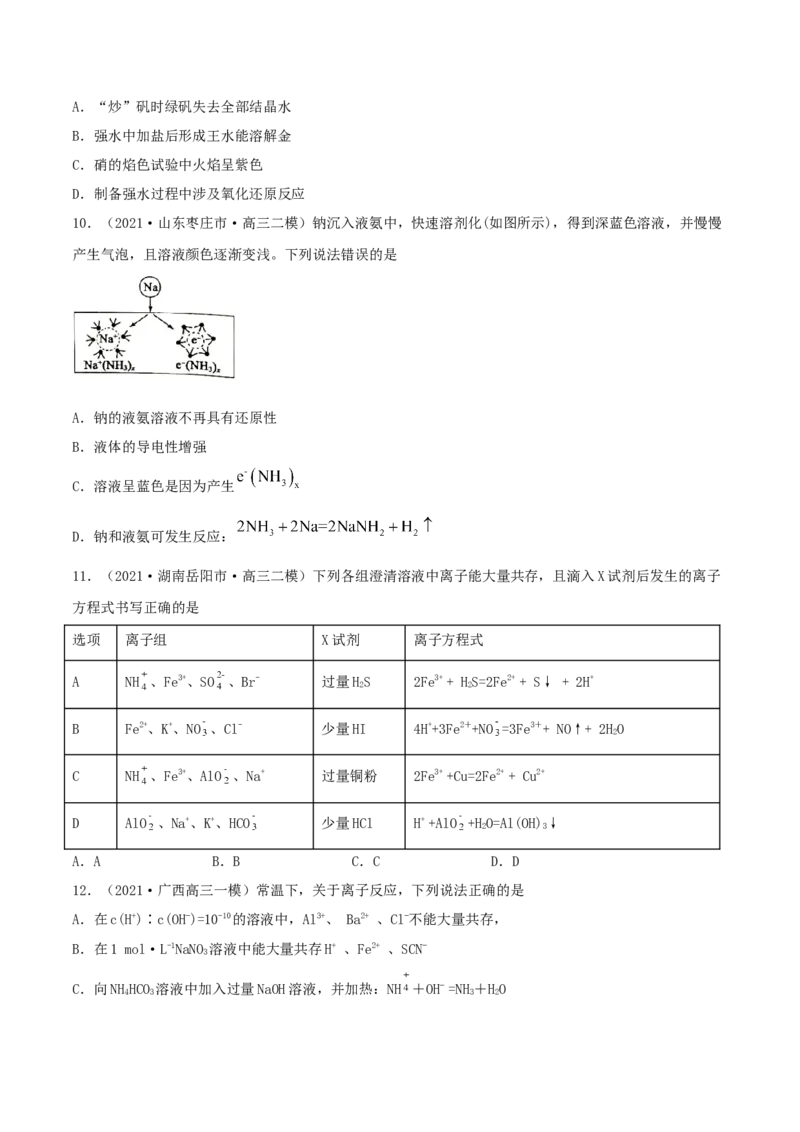
10.(2021·山东枣庄市·高三二模)钠沉入液氨中,快速溶剂化(如图所示),得到深蓝色溶液,并慢慢
产生气泡,且溶液颜色逐渐变浅。下列说法错误的是
A.钠的液氨溶液不再具有还原性
B.液体的导电性增强
C.溶液呈蓝色是因为产生
D.钠和液氨可发生反应:
11.(2021·湖南岳阳市·高三二模)下列各组澄清溶液中离子能大量共存,且滴入X试剂后发生的离子
方程式书写正确的是
选项 离子组 X试剂 离子方程式
A NH 、Fe3+、SO 、Br- 过量HS 2Fe3+ + HS=2Fe2+ + S↓ + 2H+
2 2
B Fe2+、K+、NO 、Cl- 少量HI 4H++3Fe2++NO =3Fe3++ NO↑+ 2HO
2
C NH 、Fe3+、AlO 、Na+ 过量铜粉 2Fe3+ +Cu=2Fe2+ + Cu2+
D AlO 、Na+、K+、HCO 少量HCl H+ +AlO +HO=Al(OH)↓
2 3
A.A B.B C.C D.D
12.(2021·广西高三一模)常温下,关于离子反应,下列说法正确的是
A.在c(H)∶c(OH)=10-10的溶液中,Al3、 Ba2 、Cl不能大量共存,
B.在1 mol·L-1NaNO 溶液中能大量共存H 、Fe2 、SCN
3
C.向NHHCO 溶液中加入过量NaOH溶液,并加热:NH +OH =NH+HO
4 3 3 2D.向1L0.5 mol·L-1FeBr 溶液中通入0.1molCl :2Fe2+4Br+3Cl = 2Fe3+2Br+6Cl
2 2 2 2
13.(2020·河北高三一模)由下列实验操作和现象能推出结论的是
选
实验操作 现象 结论
项
A 向黄色的Fe(NO) 溶液中滴加氢碘酸 溶液变为紫红色 氧化性:Fe3+>I
3 3 2
向10 mL 0.2 mol·L-1 ZnSO 溶液中加入10
4 先产生白色沉淀,然后 相同温度下,溶度积常
B mL 0.4 mol·L-1 NaS溶液,再滴加CuSO 溶
2 4 沉淀变黑 数:K (CuS)<K (ZnS)
液 sp sp
将CaCO 与盐酸反应得到的气体直接通入
C 3 产生白色沉淀 酸性:HCO>HSiO
NaSiO 溶液中 2 3 2 3
2 3
很快有气体产生,一段 Fe3+能催化HO 分解且该
D 向FeCl 溶液中滴入几滴30%的HO 溶液 2 2
3 2 2 时间后溶液变为红褐色 分解反应为放热反应
A.A B.B C.C D.D
14.(2020·河北张家口市·高三一模)C和CuO在高温下反应生成Cu、CuO、CO、CO。现将1 g碳粉跟
2 2
8 g CuO混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的
气体,测得溶液增加的质量为1.1 g,残余气体在标准状况下的体积为560 mL。下列说法不正确的是
A.反应后硬质试管中碳粉有剩余
B.反应后生成CuO为0.025 mol
2
C.该氧化还原反应共转移电子0.2 mol
D.反应后硬质试管中剩余的固体混合物的总质量为7.2 g
15.(2020·通榆县第一中学校高三月考)4.6 g铜镁合金完全溶解于100 mL密度为1.40 g/mL、质量分
数为63%的浓硝酸中,得到4480 mL NO 和336 mL NO 的混合气体(标准状况),向反应后的溶液中加入
2 2 4
1.0 mol/L NaOH溶液至离子恰好全部沉淀时,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2:3
B.该浓硝酸中HNO 的物质的量浓度是14.0 mol/L
3
C.产生沉淀8.51 g
D.离子恰好完全沉淀时,加入NaOH溶液的体积是230 mL
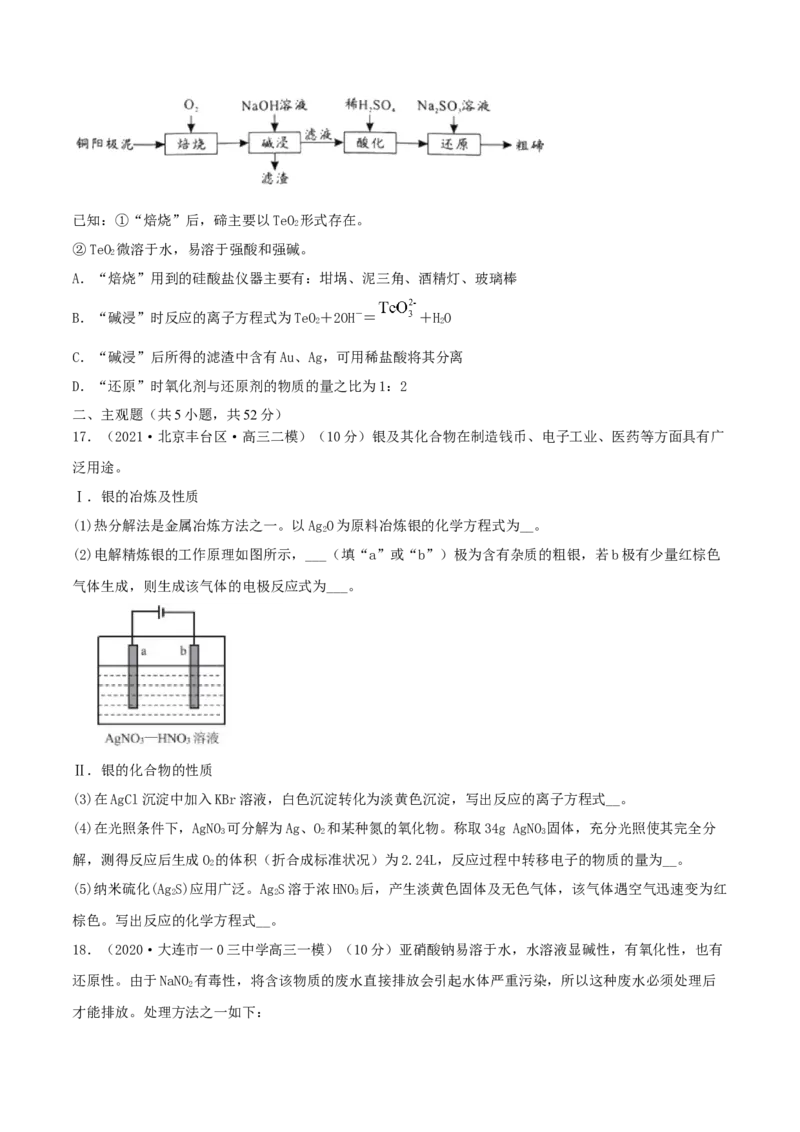
16.(2020·湖南永州市·高三三模)碲被誉为“现代工业的维生素”,它在地壳中丰度值很低,某科研
小组从粗铜精炼的阳极泥(主要含有CuTe)中提取粗碲工艺流程如图所示。下列有关说法不正确的是
2已知:①“焙烧”后,碲主要以TeO 形式存在。
2
②TeO 微溶于水,易溶于强酸和强碱。
2
A.“焙烧”用到的硅酸盐仪器主要有:坩埚、泥三角、酒精灯、玻璃棒
B.“碱浸”时反应的离子方程式为TeO+2OH-= +HO
2 2
C.“碱浸”后所得的滤渣中含有Au、Ag,可用稀盐酸将其分离
D.“还原”时氧化剂与还原剂的物质的量之比为1:2
二、主观题(共5小题,共52分)
17.(2021·北京丰台区·高三二模)(10分)银及其化合物在制造钱币、电子工业、医药等方面具有广
泛用途。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以AgO为原料冶炼银的化学方程式为__。
2
(2)电解精炼银的工作原理如图所示,___(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色
气体生成,则生成该气体的电极反应式为___。
Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式__。
(4)在光照条件下,AgNO 可分解为Ag、O 和某种氮的氧化物。称取34g AgNO 固体,充分光照使其完全分
3 2 3
解,测得反应后生成O 的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为__。
2
(5)纳米硫化(AgS)应用广泛。AgS溶于浓HNO 后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红
2 2 3
棕色。写出反应的化学方程式__。
18.(2020·大连市一0三中学高三一模)(10分)亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有
还原性。由于NaNO 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后
2
才能排放。处理方法之一如下:___NaNO+___KI+_____→___NO↑+___I+___KSO+___NaSO+______
2 2 2 4 2 4
(1)请完成该化学方程式并配平。
(2)将上述反应方程式改写为离子反应方程式:______________________;
(3)用上述反应来处理NaNO 并不是最佳方法,其原因是______________________。从环保角度来讲,要
2
处理NaNO,所用的物质的______(填“氧化性”或“还原性”)应该比KI更________(填“强”或
2
“弱”)。
(4)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式并用单线桥表示
其电子转移的方向和数目_____________________________。
19.(2020·上海青浦区·高三二模)(11分)Li-SOCl 电池采用LiAlCl 的SOCl 溶液为电解质溶液,是
2 4 2
目前比能量最高的化学电源,具有电压高.储存寿命长.工作温度范围宽.成本低等优点。
(1)该电池的工作原理为:4Li+2SOCl=4LiCl↓+SO↑+S↓,该反应的还原产物为__________,若生成标
2 2
准状况下气体11.2L,则转移电子的数目为_____________;
(2)SOCl 可用于AlCl·6HO制备无水AlCl,请结合离子方程式解释不采用直接加热晶体的方法除去结
2 3 2 3
晶水的原因_____________________________________________________________;
(3)解释Li-SOCl 电池组装必须在无水条件下的原因_______________________________;
2
(4)工业制硫酸中,SO 的催化氧化采用常压而不是高压的原因______________________;
2
(5)向NaOH溶液中缓慢通入SO 至过量,反应过程中某微粒X的物质的量浓度随着通入SO 体积的变化如
2 2
图所示,该微粒X为_____________,SO 过量时溶液仍然存在微粒X的原因
2
____________________________。
20.(2021·江苏盐城市·高三二模)(10分)氧化还原法、沉淀法等是常用于治理水体污染的重要化学
方法。
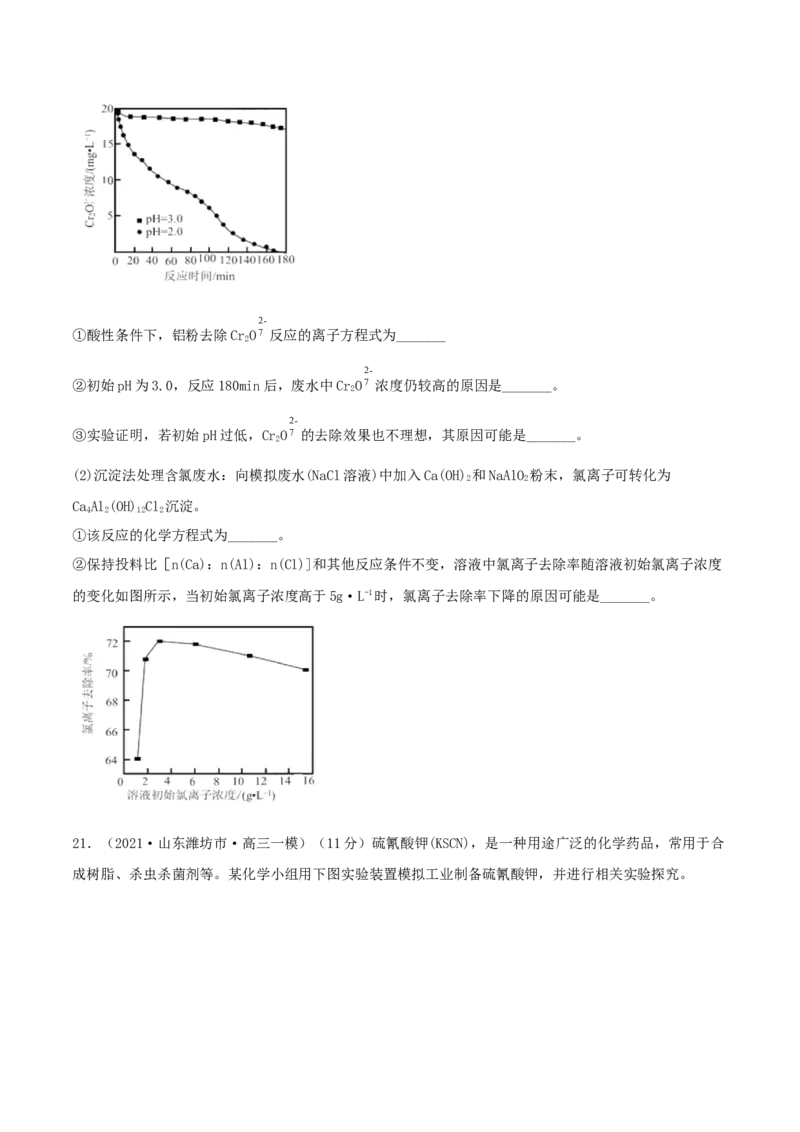
(1)还原法处理含铬废水:铝粉可将废水中的CrO 还原为Cr3+。如图所示,废水的不同初始pH对CrO
2 2
去除效果有重要影响。①酸性条件下,铝粉去除CrO 反应的离子方程式为_______
2
②初始pH为3.0,反应180min后,废水中CrO 浓度仍较高的原因是_______。
2
③实验证明,若初始pH过低,CrO 的去除效果也不理想,其原因可能是_______。
2
(2)沉淀法处理含氯废水:向模拟废水(NaCl溶液)中加入Ca(OH) 和NaAlO 粉末,氯离子可转化为
2 2
CaAl(OH) Cl 沉淀。
4 2 12 2
①该反应的化学方程式为_______。
②保持投料比[n(Ca):n(Al):n(Cl)]和其他反应条件不变,溶液中氯离子去除率随溶液初始氯离子浓度
的变化如图所示,当初始氯离子浓度高于5g·L-1时,氯离子去除率下降的原因可能是_______。
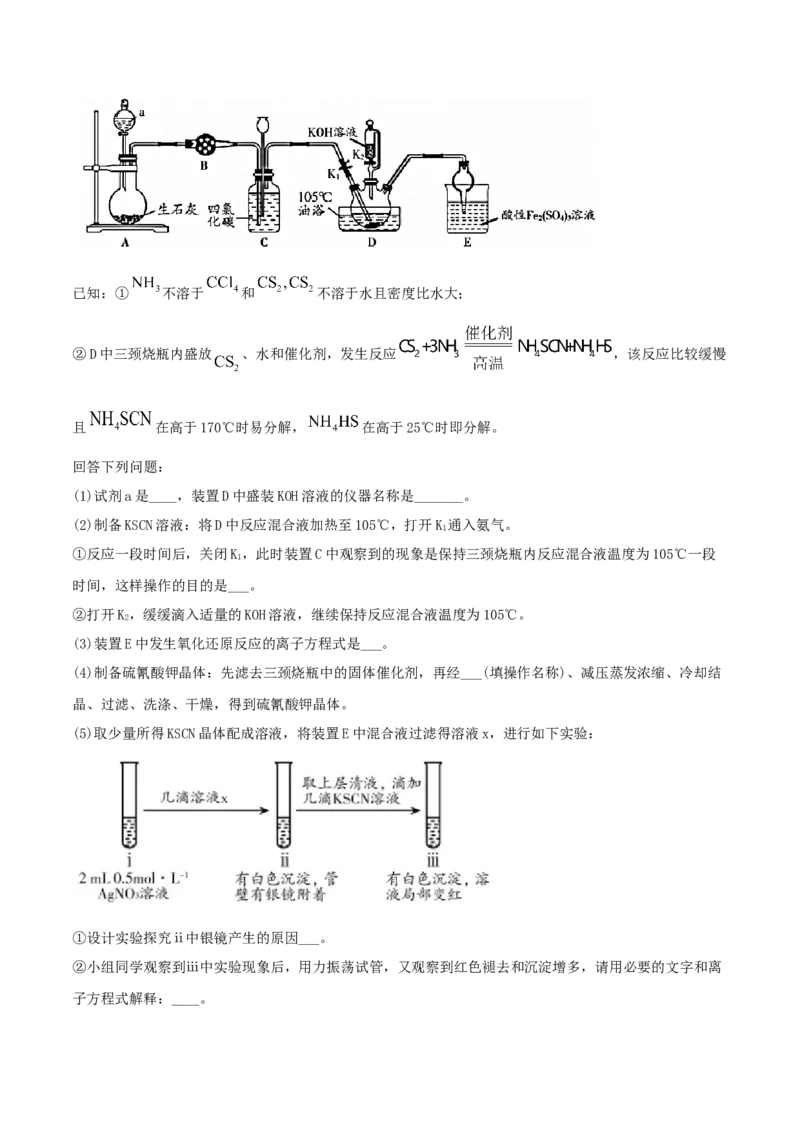
21.(2021·山东潍坊市·高三一模)(11分)硫氰酸钾(KSCN),是一种用途广泛的化学药品,常用于合
成树脂、杀虫杀菌剂等。某化学小组用下图实验装置模拟工业制备硫氰酸钾,并进行相关实验探究。已知:① 不溶于 和 不溶于水且密度比水大;
②D中三颈烧瓶内盛放 、水和催化剂,发生反应 ,该反应比较缓慢
且 在高于170℃时易分解, 在高于25℃时即分解。
回答下列问题:
(1)试剂a是____,装置D中盛装KOH溶液的仪器名称是_______。
(2)制备KSCN溶液:将D中反应混合液加热至105℃,打开K 通入氨气。
1
①反应一段时间后,关闭K,此时装置C中观察到的现象是保持三颈烧瓶内反应混合液温度为105℃一段
1
时间,这样操作的目的是___。
②打开K,缓缓滴入适量的KOH溶液,继续保持反应混合液温度为105℃。
2
(3)装置E中发生氧化还原反应的离子方程式是___。
(4)制备硫氰酸钾晶体:先滤去三颈烧瓶中的固体催化剂,再经___(填操作名称)、减压蒸发浓缩、冷却结
晶、过滤、洗涤、干燥,得到硫氰酸钾晶体。
(5)取少量所得KSCN晶体配成溶液,将装置E中混合液过滤得溶液x,进行如下实验:
①设计实验探究ⅱ中银镜产生的原因___。
②小组同学观察到ⅲ中实验现象后,用力振荡试管,又观察到红色褪去和沉淀增多,请用必要的文字和离
子方程式解释:____。