文档内容
第二章能力提升检测卷
完卷时间:90分钟
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu 64 Ag 108
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2021·浙江金华市·高三一模)下列方程式不正确的是
A.硫代硫酸钠溶液中加入稀硝酸:
B.熟石膏加水变成生石膏:
C.金属钠与水反应:
D. 溶液与过量 溶液混合后共热:
【答案】A
【解析】A.硝酸具有强氧化性能将二氧化硫氧化成硫酸,正确的方程式为:
,故A错误;B.熟石膏是 ,生石膏为
,两者转化的反应为 ,故B正确;C.金属钠与水
反应生成氢氧化钠和氢气,反应的离子方程式为: ,故C正确;D.
与过量的氢氧化钡反应生成硫酸钡,氨气和水,反应的离子方程式为:
,故D正确;故选:A。
2.(2021·浙江台州市·高三二模)已知: ,下列说法正确的是
A. 是氧化剂B.HIO得电子,发生氧化反应
C.该反应的氧化产物与还原产物的物质的量之比为1:2
D.通过该反应可说明HIO的氧化性强于
【答案】D
【解析】A.在反应 中,HO 中氧元素的化合价为-1价,反应后生成氧气,
2 2
氧元素的化合价为0价,化合价升高,HO 作还原剂,故A错误;B.HIO中的I为+1价,反应后降低到I
2 2 2
中的0价,得电子,HIO发生还原反应,故B错误;C.该反应中,O 为氧化产物,I 为还原产物,氧化产
2 2
物和还原产物的物质的量之比为1:1,故C错误;D.该反应中,HIO是氧化剂,O 为氧化产物,氧化剂的
2
氧化性强于氧化产物的氧化性,所以HIO的氧化性强于 ,故D正确;故选D。
3.(2021·广东深圳市·高三二模)下列有关物质分类的说法错误的是
A.SiO、PO 均为酸性氧化物 B.碘酒、水玻璃均为混合物
2 2 5
C.糖类、蛋白质均为高分子化合物 D.NaCl晶体、HCl气体均为电解质
【答案】C
【解析】A.SiO、PO 均能和碱反应生成盐和水,所以都是酸性氧化物,故A正确;B.碘酒是碘单质的酒
2 2 5
精溶液,水玻璃是硅酸钠水溶液,均为混合物,故B正确;C.蛋白质为高分子化合物,糖类中的二糖和单
糖都不是高分子化合物,故C错误;D.NaCl晶体和HCl气体的水溶液都能够导电,二者均为电解质,故D
正确;故选C。
4.(2021·上海浦东新区·高三二模)某新型氨氮去除技术中的含氮物质转化关系如图所示。下列说法
正确的是
A.过程Ⅰ还需要加入氧化剂
B.过程Ⅱ反应后酸性减弱
C.过程Ⅲ中,参与反应的 与 的物质的量之比为4∶3
D.过程Ⅰ、Ⅱ、Ⅲ的总反应为:【答案】C
【解析】A.过程Ⅰ中氮元素的化合价由+3价变为-1价,化合价降低,NO 做氧化剂被还原,所以过程Ⅰ
需加入还原剂,A错误;B.过程Ⅱ中NHOH与NH 反应生成NH,OH-被消耗,反应后碱性减弱,B错误;
2 2 4
C.由题分析可知,过程Ⅲ中的反应离子方程式为4 NO +3NH+4H+=5N +8HO,参与反应的NO 与NH 的
2 4 2 2 2 4
物质的量之比为4∶3,C正确;D.过程Ⅰ、Ⅱ、Ⅲ的总反应为NO 与NH 的反应,反应为4NO
2 4
+3NH+4H+=5N +8HO,D错误;故选C。
2 4 2 2
5.(2021·广东汕头市·高三一模)北京大学研究员发现在钙钛矿活性层中引入稀土 Eu3+/Eu2+离子对,
通过如图原理可消除零价铅和零价碘缺陷,提高钙钛矿太阳能电池的使用寿命。下列说法正确的是
A.Eu3+/Eu2+离子对在反应过程中需定时补充
B.消除零价铅的反应为:
C.消除零价碘的过程中,Eu3+/Eu2+离子对发生还原反应
D.整个过程中,电子从 I0转移给 Pb0
【答案】B
【解析】A.Eu3+/Eu2+离子对在反应过程中作催化剂,不需定时补充,A错误;B.消除零价铅,铅失电子生
成离子,Eu3+/Eu2+离子对得电子,反应为: 2Eu3++Pb0=2Eu2++Pb2+,B正确;C.消除零价碘的过程中,I0得
电子生成I-,Eu3+/Eu2+离子对失电子,发生氧化反应,C错误;D.整个过程中,电子从Pb0转移给I0,D错
误;答案为B。
6.(2021·天津高三二模)下列指定反应的离子方程式正确的是
A.向明矾溶液中滴加硫化钠溶液:B.向NaClO溶液中通入少量 制取次氯酸:
C. 溶液中加入盐酸酸化的
D.某中性液可能存在: 、 、 、
【答案】B
【解析】A.向明矾溶液中滴加硫化钠溶液,硫离子与铝离子双水解:
,故A错误;B.向NaClO溶液中通入少量 ,二氧化碳
通入水中形成碳酸,碳酸酸性强于次氯酸,可以制取次氯酸: ,故B正
确;C. 溶液中加入盐酸酸化的 : ,应保持电荷守恒,
故C错误;D.某中性液不可能存在 ,因为 会水解为氢氧化铁,故D错误;故选B。
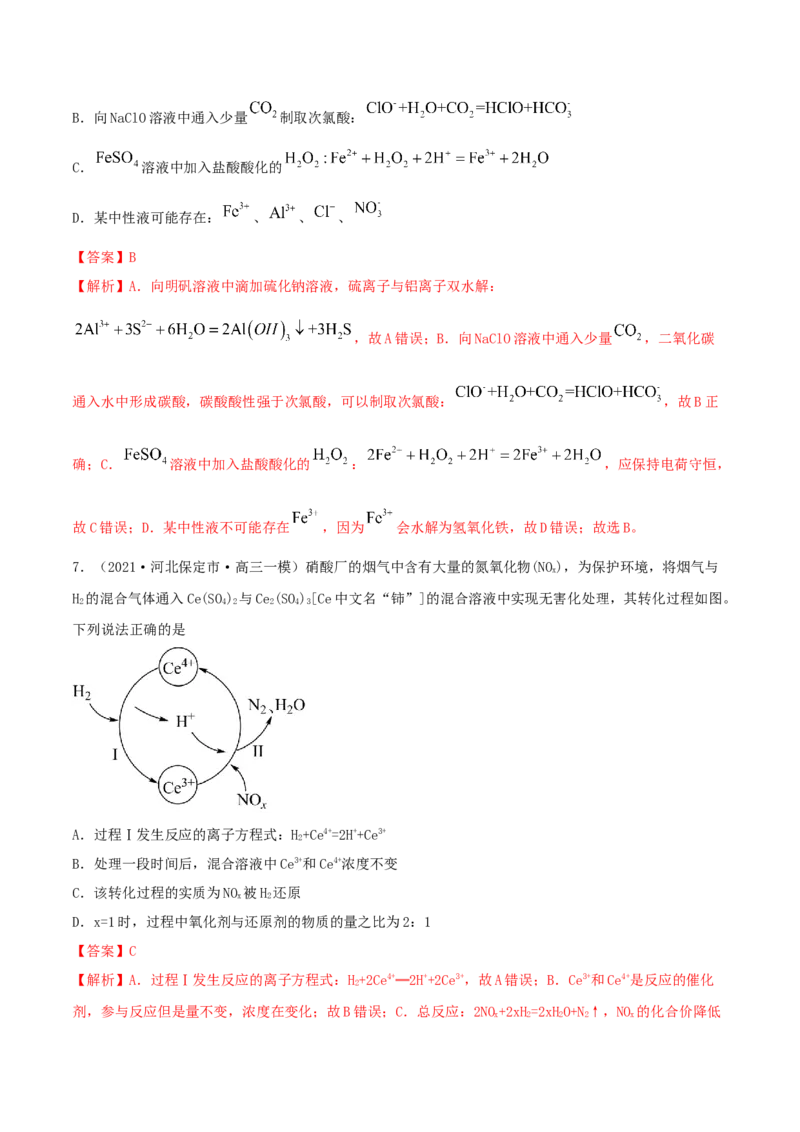
7.(2021·河北保定市·高三一模)硝酸厂的烟气中含有大量的氮氧化物(NO),为保护环境,将烟气与
x
H 的混合气体通入Ce(SO) 与Ce(SO)[Ce中文名“铈”]的混合溶液中实现无害化处理,其转化过程如图。
2 4 2 2 4 3
下列说法正确的是
A.过程Ⅰ发生反应的离子方程式:H+Ce4+=2H++Ce3+
2
B.处理一段时间后,混合溶液中Ce3+和Ce4+浓度不变
C.该转化过程的实质为NO 被H 还原
x 2
D.x=1时,过程中氧化剂与还原剂的物质的量之比为2:1
【答案】C
【解析】A.过程Ⅰ发生反应的离子方程式:H+2Ce4+═2H++2Ce3+,故A错误;B.Ce3+和Ce4+是反应的催化
2
剂,参与反应但是量不变,浓度在变化;故B错误;C.总反应:2NO+2xH=2xHO+N↑,NO 的化合价降低
x 2 2 2 x被还原,该转化过程的实质为NO 被H 还原,故C正确;D.总反应:2NO+2xH=2xHO+N↑,x=1时,过程
x 2 x 2 2 2
Ⅱ中氧化剂与还原剂的物质的量之比为1:1,故D错误;故选:C。
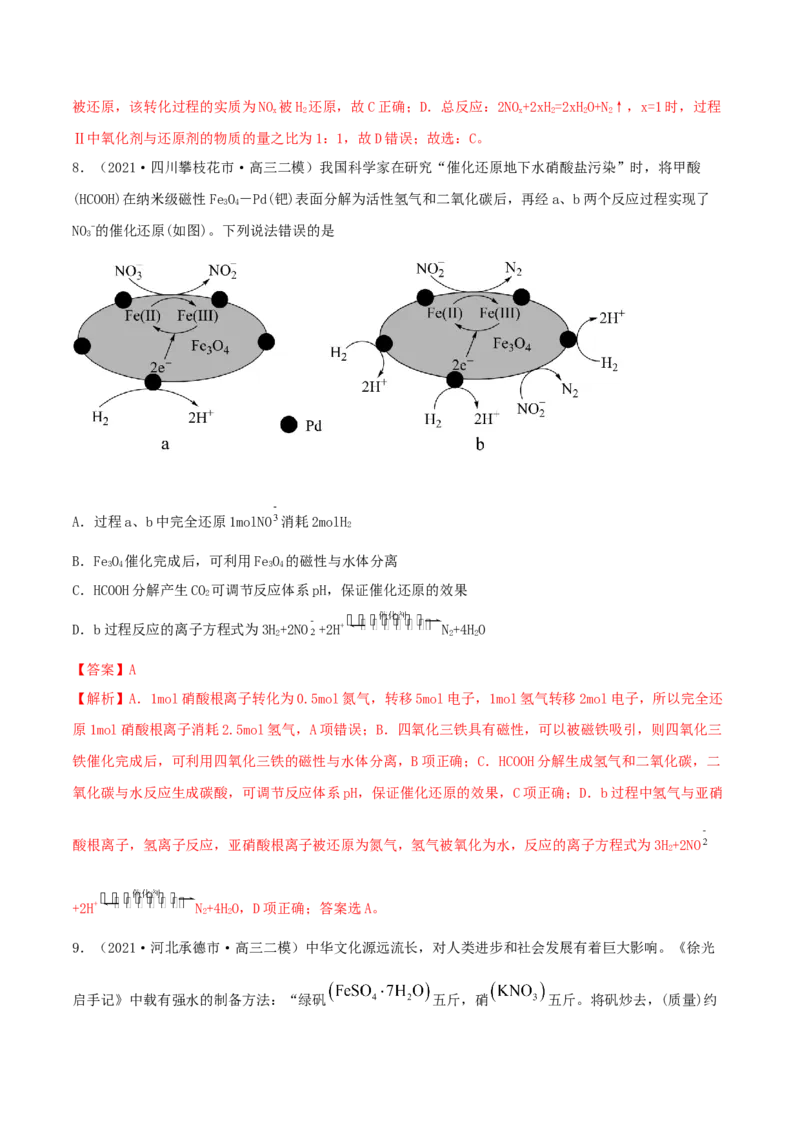
8.(2021·四川攀枝花市·高三二模)我国科学家在研究“催化还原地下水硝酸盐污染”时,将甲酸
(HCOOH)在纳米级磁性FeO-Pd(钯)表面分解为活性氢气和二氧化碳后,再经a、b两个反应过程实现了
3 4
NO-的催化还原(如图)。下列说法错误的是
3
A.过程a、b中完全还原1molNO 消耗2molH
2
B.FeO 催化完成后,可利用FeO 的磁性与水体分离
3 4 3 4
C.HCOOH分解产生CO 可调节反应体系pH,保证催化还原的效果
2
D.b过程反应的离子方程式为3H+2NO +2H+ N+4HO
2 2 2
【答案】A
【解析】A.1mol硝酸根离子转化为0.5mol氮气,转移5mol电子,1mol氢气转移2mol电子,所以完全还
原1mol硝酸根离子消耗2.5mol氢气,A项错误;B.四氧化三铁具有磁性,可以被磁铁吸引,则四氧化三
铁催化完成后,可利用四氧化三铁的磁性与水体分离,B项正确;C.HCOOH分解生成氢气和二氧化碳,二
氧化碳与水反应生成碳酸,可调节反应体系pH,保证催化还原的效果,C项正确;D.b过程中氢气与亚硝
酸根离子,氢离子反应,亚硝酸根离子被还原为氮气,氢气被氧化为水,反应的离子方程式为3H+2NO
2
+2H+ N+4HO,D项正确;答案选A。
2 2
9.(2021·河北承德市·高三二模)中华文化源远流长,对人类进步和社会发展有着巨大影响。《徐光
启手记》中载有强水的制备方法:“绿矾 五斤,硝 五斤。将矾炒去,(质量)约折五分之一。将二味同研细,用铁作锅,锅下起火……,开坛则药化为水,而锅亦坏矣。用水入五金皆成
水,惟黄金不化水中,加盐(NaCl)则化……”。下列相关说法错误的是
A.“炒”矾时绿矾失去全部结晶水
B.强水中加盐后形成王水能溶解金
C.硝的焰色试验中火焰呈紫色
D.制备强水过程中涉及氧化还原反应
【答案】A
【解析】A.1mol 的质量为296g,失去全部结晶水,质量减少 ,
,所以“炒”矾时绿矾没有失去全部结晶水,A项错误;B.强水是指硝酸,加入盐后形
成王水,金能溶于王水,B项正确;C.硝是KNO,含有K+,K+的焰色试验中火焰呈紫色,C项正确;D.开
3
坛则药化为水,而锅亦坏矣,铁被硝酸氧化为Fe3+,是氧化还原反应,D项正确;答案选A。
10.(2021·山东枣庄市·高三二模)钠沉入液氨中,快速溶剂化(如图所示),得到深蓝色溶液,并慢慢
产生气泡,且溶液颜色逐渐变浅。下列说法错误的是
A.钠的液氨溶液不再具有还原性
B.液体的导电性增强
C.溶液呈蓝色是因为产生
D.钠和液氨可发生反应:
【答案】A
【解析】A.钠的液氨溶液中含有钠单质,具有还原性,故A错误;B.液氨中没有自由移动的带电子粒子,
不导电,而钠投入液氨中生成蓝色的溶剂合电子,能导电,即溶液的导电性增强,故B正确;C.溶液呈蓝
色是因为钠单质的自由电子与氨气结合产生 ,随着反应进行, 不断减小,故蓝色变浅,故C正确;D.Na和液氨反应生成NaNH 和H,则发生反应的化学方程式为2NH+2Na=2NaNH+H↑,故
2 2 3 2 2
D正确。
故选A。
11.(2021·湖南岳阳市·高三二模)下列各组澄清溶液中离子能大量共存,且滴入X试剂后发生的离子
方程式书写正确的是
选项 离子组 X试剂 离子方程式
A NH 、Fe3+、SO 、Br- 过量HS 2Fe3+ + HS=2Fe2+ + S↓ + 2H+
2 2
B Fe2+、K+、NO 、Cl- 少量HI 4H++3Fe2++NO =3Fe3++ NO↑+ 2HO
2
C NH 、Fe3+、AlO 、Na+ 过量铜粉 2Fe3+ +Cu=2Fe2+ + Cu2+
D AlO 、Na+、K+、HCO 少量HCl H+ +AlO +HO=Al(OH)↓
2 3
A.A B.B C.C D.D
【答案】A
【解析】A.四种离子相互不反应,能够共存,三价铁离子能氧化硫离子生成硫单质,硫化氢过量反应的
离子方程式为Fe3+ + HS=2Fe2+ + S↓ + 2H+,A项正确;B.碘离子的还原性强于二价铁离子,碘离子和氢
2
离子先和硝酸根离子进行反应,反应方程式为8H++6I-+2NO =3I +2NO↑+ 4HO,B项错误;C.三价铁离
2 2
子能够与偏铝酸根离子发生双水解反应生成氢氧化铝和氢氧化铁沉淀,二者不共存,C项错误;D.碳酸氢
根离子与偏铝酸根离子反应生成碳酸根离子和氢氧化铝沉淀,二者不共存,D项错误;答案选A。
12.(2021·广西高三一模)常温下,关于离子反应,下列说法正确的是
A.在c(H)∶c(OH)=10-10的溶液中,Al3、 Ba2 、Cl不能大量共存,
B.在1 mol·L-1NaNO 溶液中能大量共存H 、Fe2 、SCN
3
C.向NHHCO 溶液中加入过量NaOH溶液,并加热:NH +OH =NH+HO
4 3 3 2
D.向1L0.5 mol·L-1FeBr 溶液中通入0.1molCl :2Fe2+4Br+3Cl = 2Fe3+2Br+6Cl
2 2 2 2
【答案】A
【解析】A.c(H)∶c(OH)=10-10的溶液中,溶液c(H)