文档内容
1.(2023·昆明高三检测)氯气是一种黄绿色的非金属单质,下列叙述不正确的是( )
A.红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟
B.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
C.光照H 和Cl 的混合气体时,因迅速化合而爆炸
2 2
D.铁丝在Cl 中燃烧,反应生成FeCl
2 2
2.下列关于氯及其化合物的性质与用途具有对应关系的是( )
A.Cl 易液化,可用于生产盐酸
2
B.ClO 有强氧化性,可用于自来水消毒
2
C.CCl 难溶于水,可用作灭火剂
4
D.HCl极易溶于水,可用于检验NH
3
3.化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述正确的是( )
A.氯气和活性炭均可作漂白剂,若同时使用,漂白效果会明显加强
B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH,测定结果无影响
D.通常状况下氯气能和Fe反应,氯气的储存不能用铁制容器
4.某化学教师为“氯气与金属钠反应”设计了如图装置的实验。实验操作:先给钠预热至钠
熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是(
)
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉花球是用于吸收过量的氯气,以免其污染空气
C.钠着火燃烧产生苍白色火焰
D.发生的反应为2Na+Cl=====2NaCl
2
5.(2023·广东揭阳高三期末)某实验小组利用以下装置制备少量的氯气,并检验氯气的性质。
实验过程中 ,下列说法正确的是( )
A.参与反应的HCl全部被氧化为Cl
2
B.发生的所有反应均是氧化还原反应C.观察到淀粉-KI试纸变蓝,说明Cl 具有氧化性
2
D.湿润的pH试纸变红,干燥的pH试纸不变色
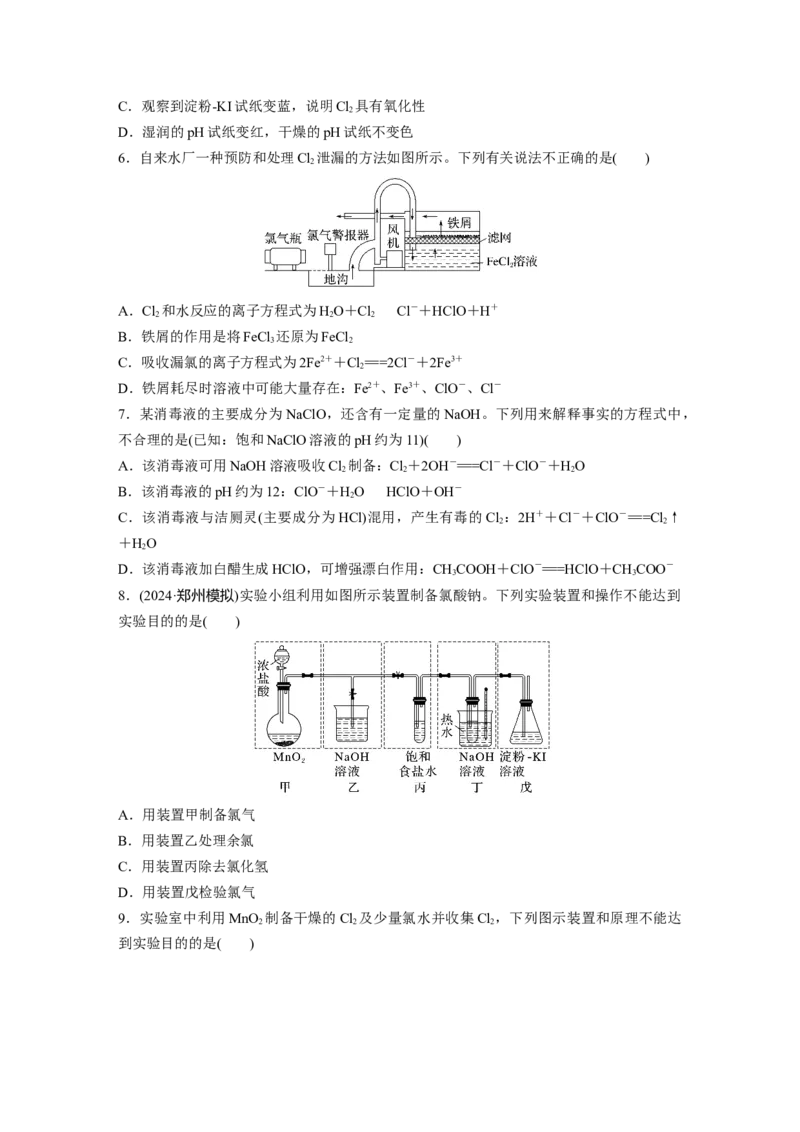
6.自来水厂一种预防和处理Cl 泄漏的方法如图所示。下列有关说法不正确的是( )
2
A.Cl 和水反应的离子方程式为HO+ClCl-+HClO+H+
2 2 2
B.铁屑的作用是将FeCl 还原为FeCl
3 2
C.吸收漏氯的离子方程式为2Fe2++Cl===2Cl-+2Fe3+
2
D.铁屑耗尽时溶液中可能大量存在:Fe2+、Fe3+、ClO-、Cl-
7.某消毒液的主要成分为NaClO,还含有一定量的NaOH。下列用来解释事实的方程式中,
不合理的是(已知:饱和NaClO溶液的pH约为11)( )
A.该消毒液可用NaOH溶液吸收Cl 制备:Cl+2OH-===Cl-+ClO-+HO
2 2 2
B.该消毒液的pH约为12:ClO-+HOHClO+OH-
2
C.该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒的Cl :2H++Cl-+ClO-===Cl↑
2 2
+HO
2
D.该消毒液加白醋生成HClO,可增强漂白作用:CHCOOH+ClO-===HClO+CHCOO-
3 3
8.(2024·郑州模拟)实验小组利用如图所示装置制备氯酸钠。下列实验装置和操作不能达到
实验目的的是( )
A.用装置甲制备氯气
B.用装置乙处理余氯
C.用装置丙除去氯化氢
D.用装置戊检验氯气
9.实验室中利用MnO 制备干燥的Cl 及少量氯水并收集Cl ,下列图示装置和原理不能达
2 2 2
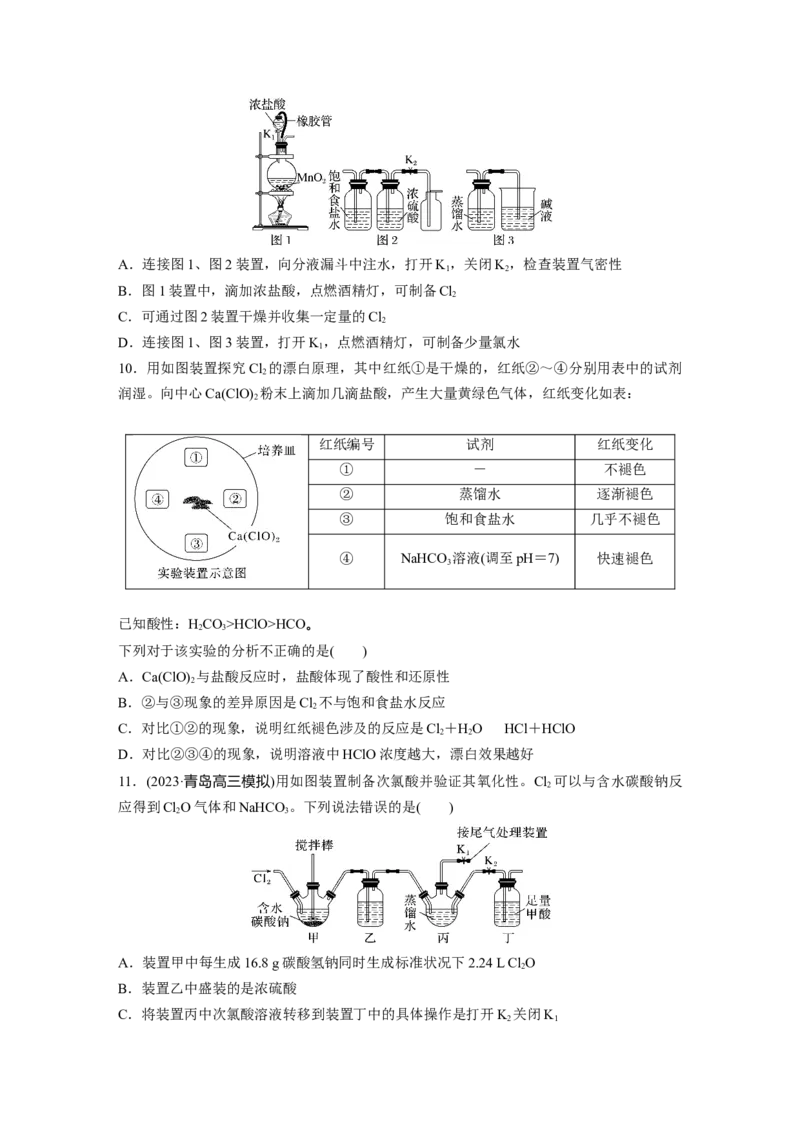
到实验目的的是( )A.连接图1、图2装置,向分液漏斗中注水,打开K,关闭K,检查装置气密性
1 2
B.图1装置中,滴加浓盐酸,点燃酒精灯,可制备Cl
2
C.可通过图2装置干燥并收集一定量的Cl
2
D.连接图1、图3装置,打开K,点燃酒精灯,可制备少量氯水
1
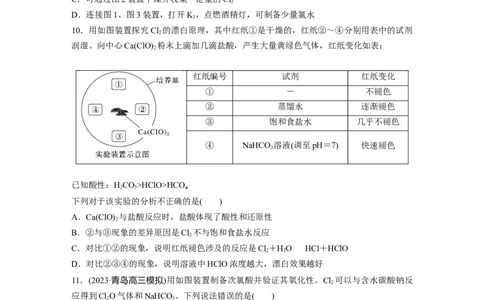
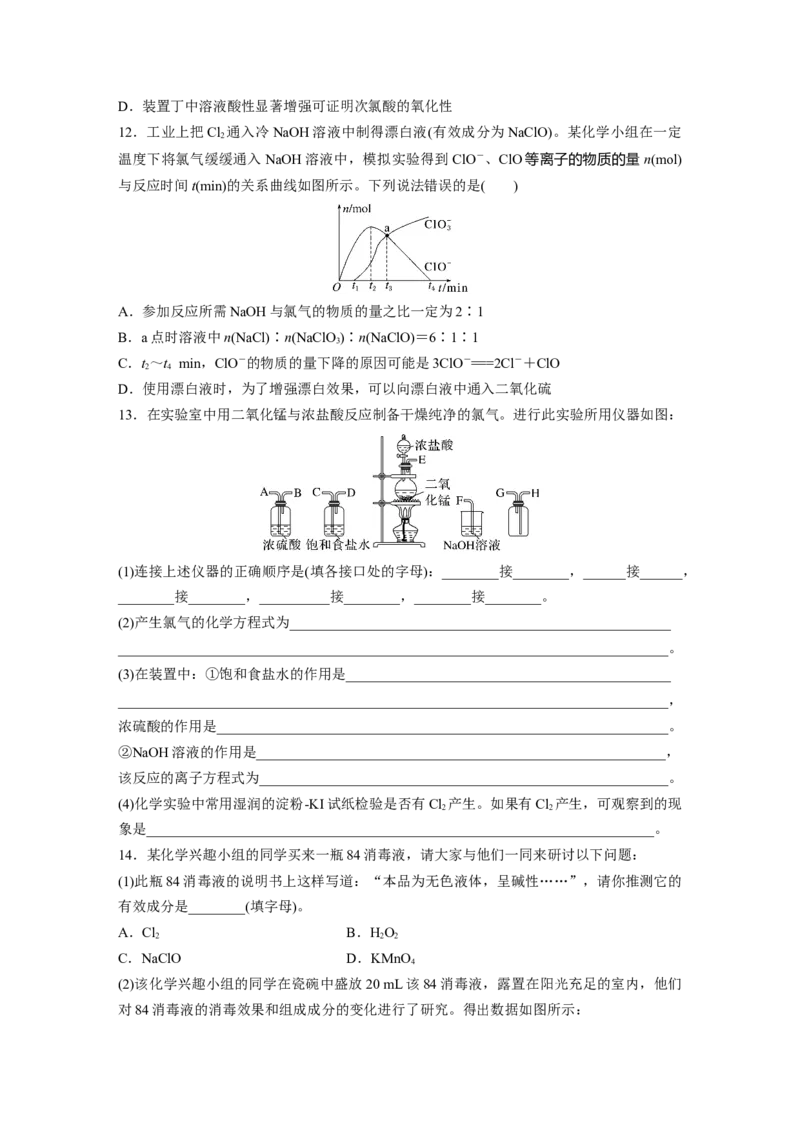
10.用如图装置探究Cl 的漂白原理,其中红纸①是干燥的,红纸②~④分别用表中的试剂
2
润湿。向中心Ca(ClO) 粉末上滴加几滴盐酸,产生大量黄绿色气体,红纸变化如表:
2
红纸编号 试剂 红纸变化
① - 不褪色
② 蒸馏水 逐渐褪色
③ 饱和食盐水 几乎不褪色
④ NaHCO 溶液(调至pH=7) 快速褪色
3
已知酸性:HCO>HClO>HCO。
2 3
下列对于该实验的分析不正确的是( )
A.Ca(ClO) 与盐酸反应时,盐酸体现了酸性和还原性
2
B.②与③现象的差异原因是Cl 不与饱和食盐水反应
2
C.对比①②的现象,说明红纸褪色涉及的反应是Cl+HOHCl+HClO
2 2
D.对比②③④的现象,说明溶液中HClO浓度越大,漂白效果越好
11.(2023·青岛高三模拟)用如图装置制备次氯酸并验证其氧化性。Cl 可以与含水碳酸钠反
2
应得到ClO气体和NaHCO 。下列说法错误的是( )
2 3
A.装置甲中每生成16.8 g碳酸氢钠同时生成标准状况下2.24 L Cl O
2
B.装置乙中盛装的是浓硫酸
C.将装置丙中次氯酸溶液转移到装置丁中的具体操作是打开K 关闭K
2 1D.装置丁中溶液酸性显著增强可证明次氯酸的氧化性
12.工业上把Cl 通入冷NaOH溶液中制得漂白液(有效成分为NaClO)。某化学小组在一定
2
温度下将氯气缓缓通入NaOH溶液中,模拟实验得到ClO-、ClO等离子的物质的量n(mol)
与反应时间t(min)的关系曲线如图所示。下列说法错误的是( )
A.参加反应所需NaOH与氯气的物质的量之比一定为2∶1
B.a点时溶液中n(NaCl)∶n(NaClO)∶n(NaClO)=6∶1∶1
3
C.t~t min,ClO-的物质的量下降的原因可能是3ClO-===2Cl-+ClO
2 4
D.使用漂白液时,为了增强漂白效果,可以向漂白液中通入二氧化硫
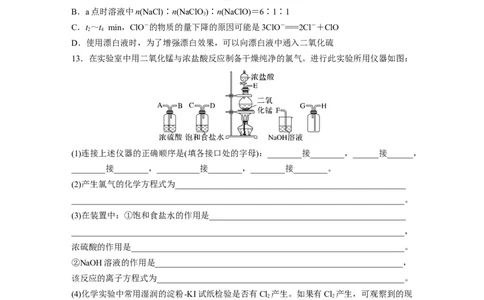
13.在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验所用仪器如图:
(1)连接上述仪器的正确顺序是(填各接口处的字母):________接________,______接______,
________接________,__________接________,________接________。
(2)产生氯气的化学方程式为______________________________________________________
______________________________________________________________________________。
(3)在装置中:①饱和食盐水的作用是______________________________________________
______________________________________________________________________________,
浓硫酸的作用是________________________________________________________________。
②NaOH溶液的作用是__________________________________________________________,
该反应的离子方程式为__________________________________________________________。
(4)化学实验中常用湿润的淀粉-KI试纸检验是否有Cl 产生。如果有Cl 产生,可观察到的现
2 2
象是________________________________________________________________________。
14.某化学兴趣小组的同学买来一瓶84消毒液,请大家与他们一同来研讨以下问题:
(1)此瓶84消毒液的说明书上这样写道:“本品为无色液体,呈碱性……”,请你推测它的
有效成分是________(填字母)。
A.Cl B.HO
2 2 2
C.NaClO D.KMnO
4
(2)该化学兴趣小组的同学在瓷碗中盛放20 mL该84消毒液,露置在阳光充足的室内,他们
对84消毒液的消毒效果和组成成分的变化进行了研究。得出数据如图所示:从图1和图2中数据可得知84消毒液暴露在空气中半小时后,其主要溶质是__________,
用化学方程式表示其中变化的主要原因:NaClO+CO +HO===HClO+NaHCO 、
2 2 3
_____________________________________________________________________________ 、
________________________________________________________________________。
(3)该化学兴趣小组的同学选择紫色石蕊溶液对84消毒液的性质进行实验探究,请你帮助他
们完成实验报告:
实验操作 预期现象 结论
(4)该化学兴趣小组的同学上网查询有关84消毒液的信息时 ,发现这样一则消息:有一家
庭主妇把84消毒液和清洁剂(呈酸性、含Cl-)倒在一起,进行刷洗。一会儿,她就晕倒在房
间里。这几位同学感到迷惑不解。请你用离子方程式帮助他们解开这一悬念:
_______________________________________________________________________________
_______________________________________________________________________________
。