文档内容
第五章 物质结构与性质 元素周期律
测试卷
时间:90分钟 分值:100分
可能用到的相对原子质量:C 12 N 14 F19 Na 23 Al 27 S 32 Ni 59 Cu 64 La 139
一、选择题(每小题只有一个正确选项,共16×3分)
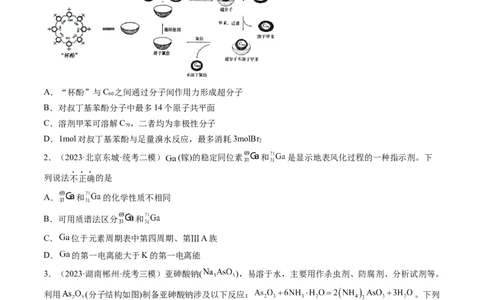
1.(2023·山西临汾·统考二模)某“杯酚”是对叔丁基苯酚与甲醛反应得到的一种环状缩合物,我国科学
家将C 、C 混合物加入该“杯酚”中进行分离的流程如图。下列说法正确的是
60 70
A.“杯酚”与C 之间通过分子间作用力形成超分子
60
B.对叔丁基苯酚分子中最多14个原子共平面
C.溶剂甲苯可溶解C ,二者均为非极性分子
70
D.1mol对叔丁基苯酚与足量溴水反应,最多消耗3molBr
2
2.(2023·北京东城·统考二模) (镓)的稳定同位素 和 是显示地表风化过程的一种指示剂。下
列说法不正确的是
A. 和 的化学性质不相同
B.可用质谱法区分 和
C. 位于元素周期表中第四周期、第ⅢA族
D. 的第一电离能大于K的第一电离能
3.(2023·湖南郴州·统考三模)亚砷酸钠( ),易溶于水,主要用作杀虫剂、防腐剂、分析试剂等。
利用 (分子结构如图)制备亚砷酸钠涉及以下反应: 。下列
说法错误的是
A. 的电子式为
B.砷的原子结构示意图为
1 / 7
学科网(北京)股份有限公司C. 中所含元素的电负性由大到小的顺序为N>O>H>As
D. 中阳离子的空间结构为正四面体形
4.(2023·山东聊城·校联考三模)为纪念元素周期表诞生150周年,IUPAC向世界介绍了118位优秀青年
化学家,并形成张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“ 、 、
”元素的代言人。下列围绕这些元素的相关说法正确的是
A. 是一种化合物 B. 与 的化学性质相同
C. 与 的电子数之比为 D. 中含有非极性键
5.(2023·湖北·校联考模拟预测)硫的下列4种微粒,若失去一个电子所需要能量最多的是
A.[Ne] B.[Ne] C.[Ne] D.[Ne]
6.(2023·湖南岳阳·统考三模)由铁及其化合物可制得FeSO ·7H O、FeCl 、KFeO 等化工产品,它们在
4 2 3 2 4
生产、生活中具有广泛应用。已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO 。高炉炼铁的反
4 2 5 4
应为 Fe O(s)+3CO(g)=2Fe(s)+3CO(g) ΔH=-23.5 kJ· mol-1。下列有关说法不正确的是
2 3 2
A.如图所示γFe的晶胞中,铁原子的配位数为12
B.配离子为[Fe(NO)(H O) ]2+,配位数为6
2 5
C.基态铁原子的核外电子排布式为1s22s22p63s23p63d74s1
D.该配合物中阴离子空间结构为正四面体形
7.(2023·上海·统考模拟预测)2022年6月,由来自德国、日本、美国和中国等国的科学家组成的国际科
研团队在《自然》杂志发表论文证实“四中子态”物质的存在。该物质只由四个中子组成,则其质量数是
A.1 B.2 C.3 D.4
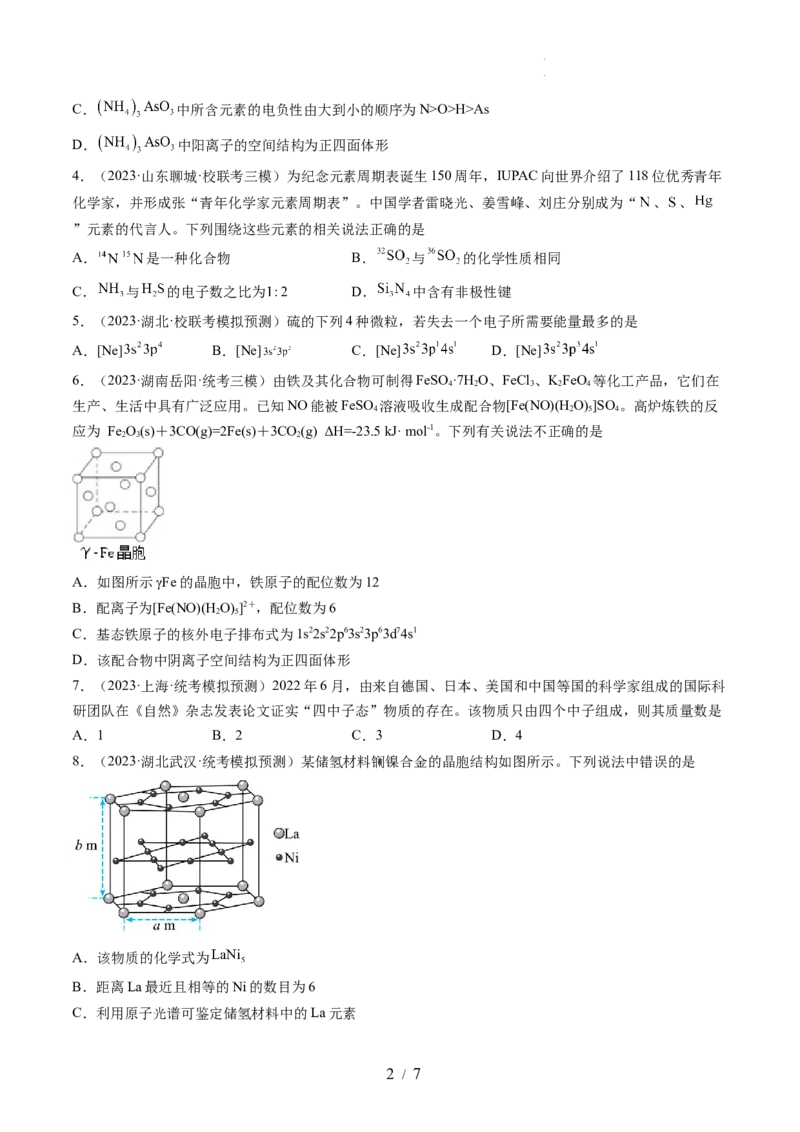
8.(2023·湖北武汉·统考模拟预测)某储氢材料镧镍合金的晶胞结构如图所示。下列说法中错误的是
A.该物质的化学式为
B.距离La最近且相等的Ni的数目为6
C.利用原子光谱可鉴定储氢材料中的La元素
2 / 7
学科网(北京)股份有限公司D.晶体密度:
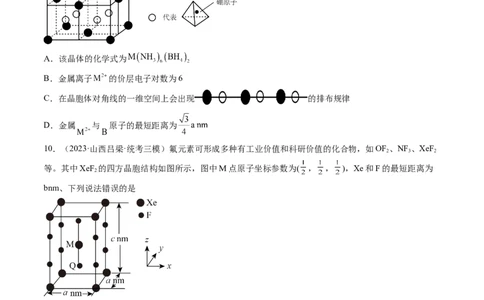
9.(2023·山东·沂水县第一中学校联考模拟预测)某新型储氢材料的晶胞如图。八面体中心为 ,顶点
均为 配体;四面体中心为硼原子,顶点均为氢原子。该晶体属于立方晶系,晶胞边长为anm其摩尔质
量为188g/mol。下列说法错误的是
A.该晶体的化学式为
B.金属离子 的价层电子对数为6
C.在晶胞体对角线的一维空间上会出现 的排布规律
D.金属 与 原子的最短距离为
10.(2023·山西吕梁·统考三模)氟元素可形成多种有工业价值和科研价值的化合物,如OF 、NF 、XeF
2 3 2
等。其中XeF 的四方晶胞结构如图所示,图中M点原子坐标参数为( , , ),Xe和F的最短距离为
2
bnm、下列说法错误的是
A. OF 分子中键角小于 分子中的
2
B. 中Xe的杂化方式为sp
C.基态N、F原子核外电子均有5种空间运动状态
D.Q点原子坐标参数为 [ ]
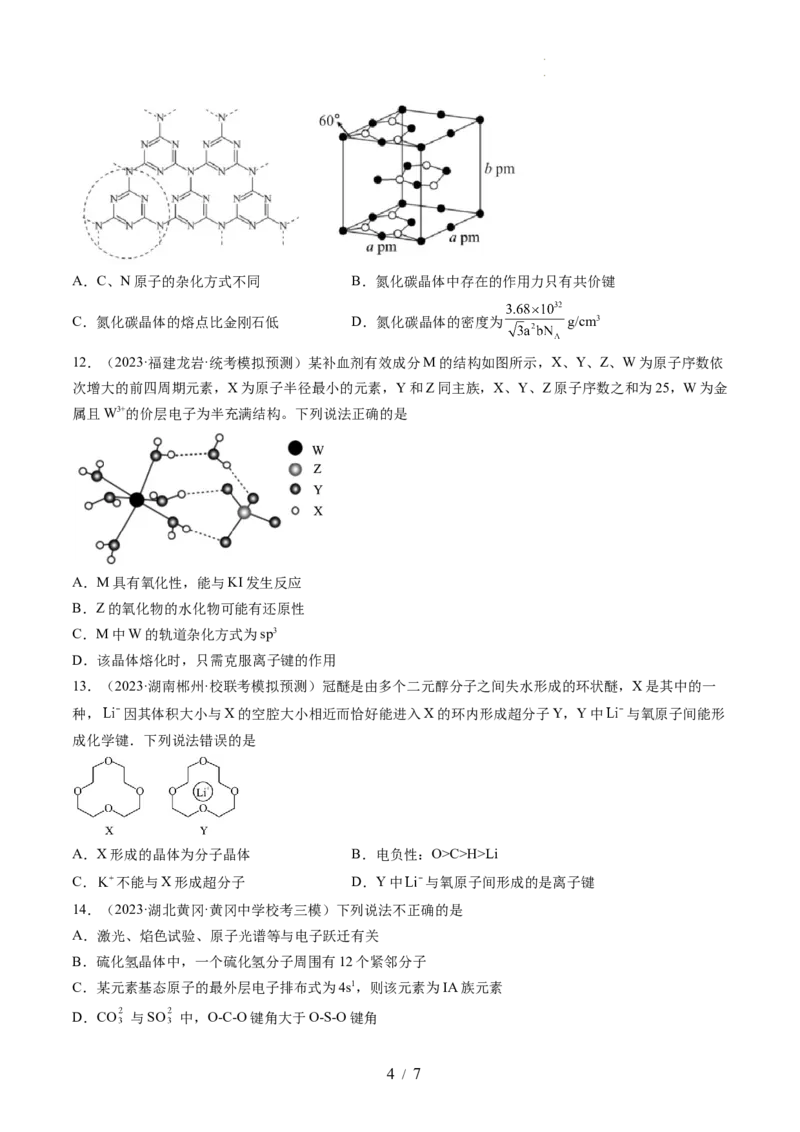
11.(2023·湖北荆门·荆门市龙泉中学校联考二模)石墨相氮化碳是一种光催化剂,类似于石墨层状结构,
其结构单元及晶胞结构如图所示。设N 为阿伏加德罗常数的值,下列说法正确的是
A
3 / 7
学科网(北京)股份有限公司A.C、N原子的杂化方式不同 B.氮化碳晶体中存在的作用力只有共价键
C.氮化碳晶体的熔点比金刚石低 D.氮化碳晶体的密度为 g/cm3
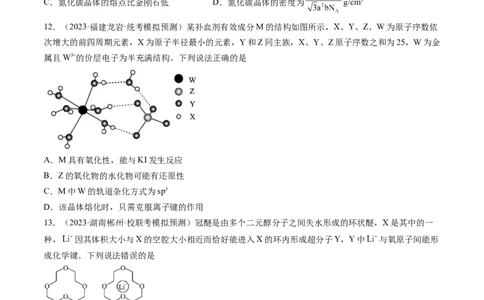
12.(2023·福建龙岩·统考模拟预测)某补血剂有效成分M的结构如图所示,X、Y、Z、W为原子序数依
次增大的前四周期元素,X为原子半径最小的元素,Y和Z同主族,X、Y、Z原子序数之和为25,W为金
属且W3+的价层电子为半充满结构。下列说法正确的是
A.M具有氧化性,能与KI发生反应
B.Z的氧化物的水化物可能有还原性
C.M中W的轨道杂化方式为sp3
D.该晶体熔化时,只需克服离子键的作用
13.(2023·湖南郴州·校联考模拟预测)冠醚是由多个二元醇分子之间失水形成的环状醚,X是其中的一
种, 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原子间能形
成化学键.下列说法错误的是
A.X形成的晶体为分子晶体 B.电负性:O>C>H>Li
C. 不能与X形成超分子 D.Y中 与氧原子间形成的是离子键
14.(2023·湖北黄冈·黄冈中学校考三模)下列说法不正确的是
A.激光、焰色试验、原子光谱等与电子跃迁有关
B.硫化氢晶体中,一个硫化氢分子周围有12个紧邻分子
C.某元素基态原子的最外层电子排布式为4s1,则该元素为IA族元素
D.CO 与SO 中,O-C-O键角大于O-S-O键角
4 / 7
学科网(北京)股份有限公司15.(2023·北京西城·北师大实验中学校考三模)下列图示或化学用语表示正确的是
A. 的电子 B.基态 的价层电子轨道表 C. 的结构示意 D. 的轨道的电子云轮
式 示式 图 廓图
16.(2023·海南海口·统考模拟预测)实验室利用CoCl 制备 的原理是
2
。下列有关说法错误的是
A.基态Co3+的价层电子排布式为3d6
B.HO 的电子式为
2 2
C.NH Cl在水中的电离方程式为
4
D.NH 的空间填充模型为
3
二、主观题(共5小题,共52分)
17.(11分)(2023·上海金山·统考二模)白云石的化学组成是CaCO ·MgCO ,500℃以下分解成二氧化
3 3
碳、金属氧化物和碳酸盐,800℃以上则彻底分解成氧化物。
(1)镁和钙在元素周期表中位于___________族,它们的价电子轨道式表示式为___________(用n表示电子层
数)。
(2)白云石500℃以下分解的化学方程式为___________。
(3)从物质结构角度分析、比较白云石分解生成的MgO和CaO的热稳定性。___________ 。
(4)白云石分解得到的CO 是氨碱法制备纯碱的基本原料之一,写出氨碱法制纯碱主要反应的化学方程式
2
___________、___________;向氨碱法的母液中加入生石灰可实现___________(填化学式)的循环利用。处
理后的母液经蒸发、浓缩、冷却、固化可得CaCl 。以质量比为1.44∶1的CaCl ·6H O与冰水混合,可获
2 2 2
得-55℃的低温,配制该制冷剂时不使用无水CaCl 的原因是___________。
2
18.(10分)(2023·天津·校联考一模)近日,我国研究人员利用硫氰酸甲基铵{[CH NH ]+[SCN]-}气相辅
3 3
助生长技术,成功制得稳定的钙钛矿型甲脒铅碘(FAPbI )。请回答下列问题:
3
(1)基态S原子的价电子排布图为___________。
(2)甲脒(FA)的结构简式为
①其组成元素的电负性由小到大的排序为___________,其中碳原子的杂化方式为___________。
②甲脒比丙烷的熔点更高的原因是___________。
(3)FAPbI 的晶体结构单元如图所示,图中Y表示Pb,位于八面体中心,则甲脒的碘配位数为___________。
3
5 / 7
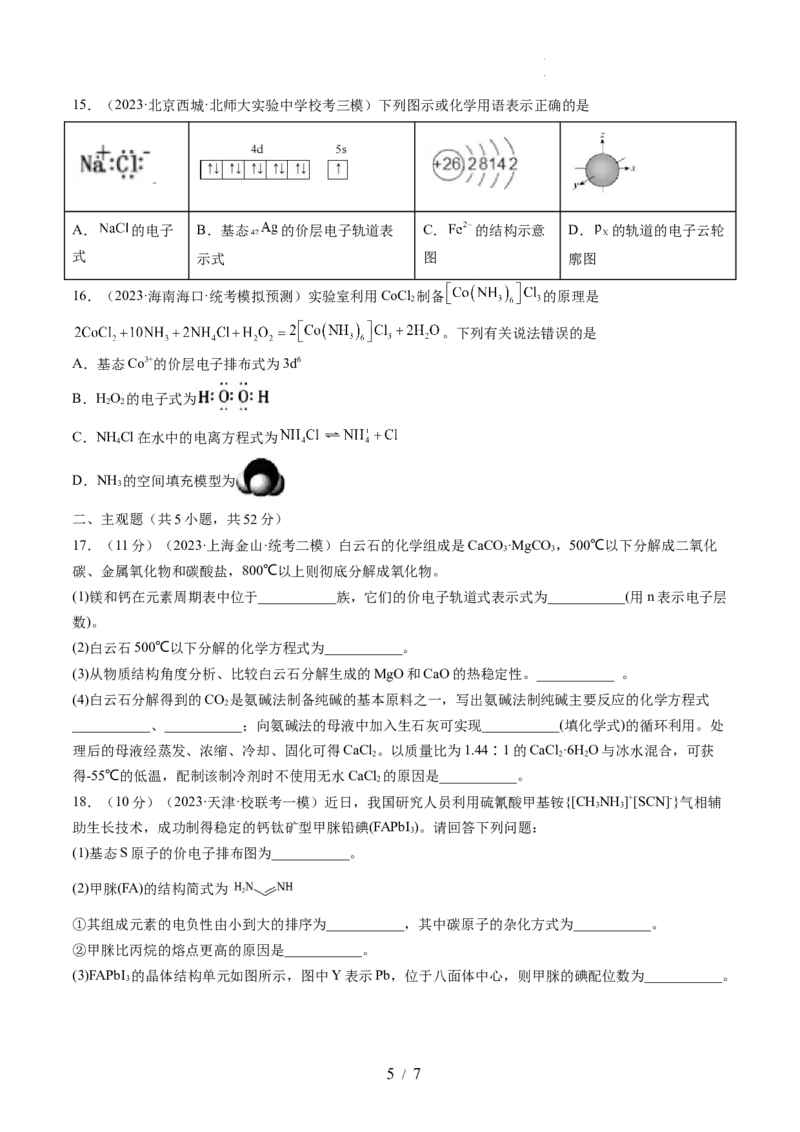
学科网(北京)股份有限公司19.(10分)(2023·海南海口·海南华侨中学校考二模)冰晶石的主要成分为六氟合铝酸钠 。工
业上制备冰晶石的化学方程式为 。
回答下列问题:
(1)Al激发态的电子排布式有________,其中能量较高的是________。(填字母)
a. b. c. d.
(2)HF的沸点比 的________(填“高”或“低”),其原因是________________。
(3)气态氯化铝是以双聚分子 的形式存在的,其结构式为________________。
(4)冰晶石的结构单元如图所示,该结构单元中 的数目为________;已知晶胞参数 、
、 、 ,阿伏加德罗常数的值为 ,则 晶体的密度 ________
(列出计算式即可)。
20.(11分)(2023·江西赣州·统考二模)CuO、Cu S等含铜化合物可以催化合成HCOOH.回答下列问
2
题:
(1)基态铜原子的价电子排布式为___________。
(2)HCOOH中碳原子的轨道杂化类型为___________,元素电负性从大到小的顺序为___________。
(3)催化过程中可能产生 , 的空间构型为___________,碳氧键的平均键长 比CHOH要
3
___________(填“长”或“短”)。
(4)在有机溶剂中,HSO 的电离平衡常数K (H SO )比HCO 的电离平衡常数K (H CO)大,除S的非金属
2 4 a1 2 4 2 3 a1 2 3
性比C强外,在分子结构上还存在的原因是___________。
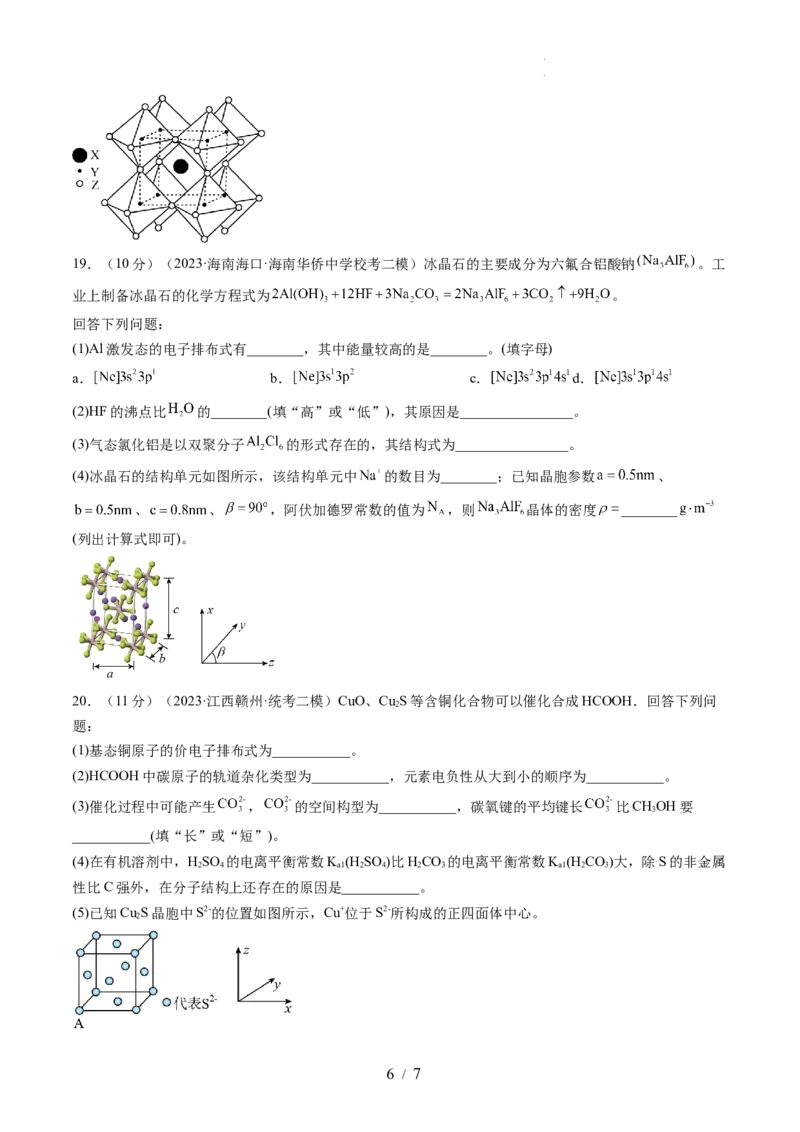
(5)已知Cu S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。
2
6 / 7
学科网(北京)股份有限公司S2-配位数为______________________;已知图中A处(S2-)的原子分数坐标为(0,0,0),则晶胞中与A距离
最近的为Cu+原子分数坐标为___________;若晶胞参数anm,晶体的密度为dg·cm-3),则阿佛伽德罗常数
的值为___________(用含a和d的式子表示)。
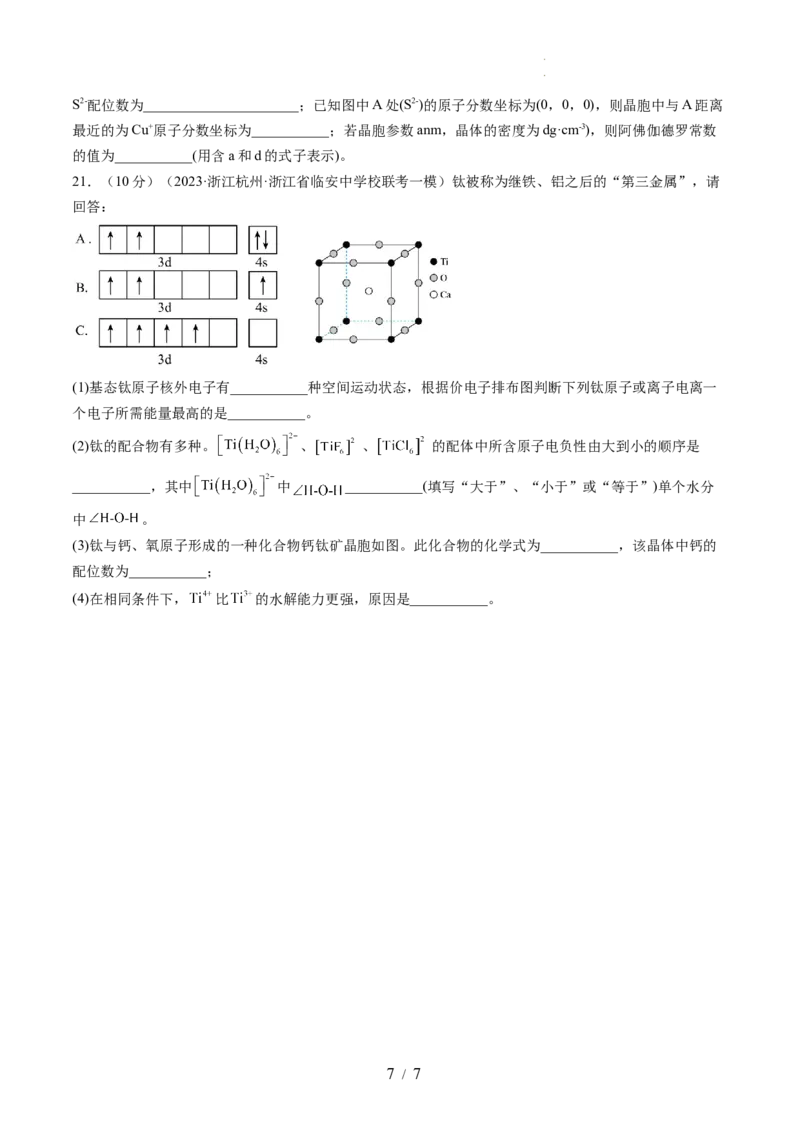
21.(10分)(2023·浙江杭州·浙江省临安中学校联考一模)钛被称为继铁、铝之后的“第三金属”,请
回答:
(1)基态钛原子核外电子有___________种空间运动状态,根据价电子排布图判断下列钛原子或离子电离一
个电子所需能量最高的是___________。
(2)钛的配合物有多种。 、 、 的配体中所含原子电负性由大到小的顺序是
___________,其中 中 ___________(填写“大于”、“小于”或“等于”)单个水分
中 。
(3)钛与钙、氧原子形成的一种化合物钙钛矿晶胞如图。此化合物的化学式为___________,该晶体中钙的
配位数为___________;
(4)在相同条件下, 比 的水解能力更强,原因是___________。
7 / 7
学科网(北京)股份有限公司