文档内容
考前速记01
教材方程式集萃
1.无机方程式
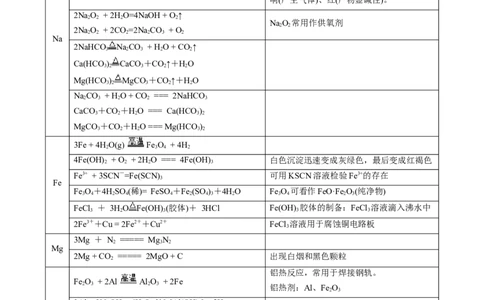
4Na + O=2NaO 钠在空气中放置,表面迅速变暗
2 2
2Na + O NaO 钠燃烧,产生黄色火焰,生成淡黄色固体
2 2 2
浮(密度小于水)、熔(放热、熔点低)、游、
2Na + 2HO=2NaOH + H ↑
2 2 响(产生气体)、红(产物显碱性)。
2NaO + 2H O=4NaOH + O ↑
2 2 2 2
NaO 常用作供氧剂
2 2
2NaO + 2CO=2NaCO + O
2 2 2 2 3 2
Na
2NaHCO NaCO + H O + CO ↑
3 2 3 2 2
Ca(HCO ) CaCO +CO↑+HO
3 2 3 2 2
Mg(HCO ) MgCO +CO↑+HO
3 2 3 2 2
NaCO + H O + CO === 2NaHCO
2 3 2 2 3
CaCO +CO+HO === Ca(HCO )
3 2 2 3 2
MgCO +CO+HO === Mg(HCO )
3 2 2 3 2
3Fe + 4H O(g) Fe O + 4H
2 3 4 2
4Fe(OH) + O + 2H O === 4Fe(OH) 白色沉淀迅速变成灰绿色,最后变成红褐色
2 2 2 3
Fe3+ + 3SCN-=Fe(SCN) 可用KSCN溶液检验Fe3+的存在
3
Fe
Fe O+4HSO (稀)= FeSO +Fe (SO )+4HO Fe O 可看作FeO·Fe O(纯净物)
3 4 2 4 4 2 4 3 2 3 4 2 3
FeCl + 3HO Fe(OH) (胶体)+ 3HCl Fe(OH) 胶体的制备:FeCl 溶液滴入沸水中
3 2 3 3 3
2Fe3++Cu = 2Fe2++Cu2+ FeCl 溶液用于腐蚀铜电路板
3
3Mg + N ===== Mg N
2 3 2
Mg
2Mg + CO ===== 2MgO + C 出现白烟和黑色颗粒
2
铝热反应,常用于焊接钢轨。
Fe O + 2Al Al O + 2Fe
2 3 2 3 铝热剂:Al、Fe O
2 3
2Al + 2NaOH + 6H O=2Na[Al(OH)] + 3H ↑
2 4 2
Al O 属于两性氧化物
2 3
Al Al O+2NaOH+3HO=2Na[Al(OH)]
2 3 2 4
Al(OH) 属于两性氢氧化物
3
Al(OH) +NaOH =Na[Al(OH) ]
3 4
AlCl + 3NH ·H O= Al(OH) ↓ + 3NHCl
3 3 2 3 4
用弱酸/弱碱制取Al(OH) ,过量也不溶解
3
Na[Al(OH)] + CO =Al(OH) ↓ + NaHCO
4 2 3 3
2Cu + O + H O + CO =Cu (OH) CO 铜生锈(铜绿)
2 2 2 2 2 3
Cu
4CuO 2Cu O + O↑ 黑色固体变红
2 2
C CO + C 2CO
2C+H 2 O CO+H 2 制水煤气(CO、H 2 )
Si + O SiO
2 2
SiO + 2C Si + 2CO↑ 工业制硅
2
SiO + 2NaOH === NaSiO + H O
2 2 3 2
SiO 属于酸性氧化物
2
Si SiO + CaO CaSiO
2 3
SiO + 4HF === SiF↑ + 2H O 此反应常被用来刻蚀玻璃
2 4 2
SiO + CaCO CaSiO + CO↑
2 3 3 2
工业制玻璃
SiO + Na CO NaSiO + CO↑
2 2 3 2 3 2
棕色的烟
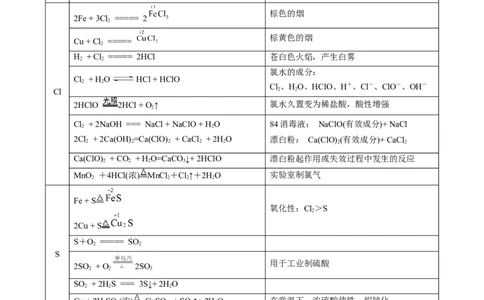
2Fe + 3Cl ===== 2
2
棕黄色的烟
Cu + Cl =====
2
H + Cl ===== 2HCl 苍白色火焰,产生白雾
2 2
氯水的成分:
Cl + H O HCl + HClO
2 2
Cl、HO、HClO、H+、Cl-、ClO-、OH-
Cl 2 2
2HClO 2HCl + O ↑ 氯水久置变为稀盐酸,酸性增强
2
Cl + 2NaOH === NaCl + NaClO + H O 84消毒液: NaClO(有效成分)+ NaCl
2 2
2Cl + 2Ca(OH) =Ca(ClO) + CaCl + 2H O 漂白粉: Ca(ClO) (有效成分)+ CaCl
2 2 2 2 2 2 2
Ca(ClO) + CO + H O=CaCO ↓+ 2HClO 漂白粉起作用或失效过程中发生的反应
2 2 2 3
MnO +4HCl(浓) MnCl +Cl↑+2HO 实验室制氯气
2 2 2 2
Fe + S
氧化性:Cl>S
2
2Cu + S
S+O ===== SO
2 2
S
用于工业制硫酸
2SO + O 2SO
2 2 3
SO + 2H S === 3S↓+ 2H O
2 2 2
Cu + 2H SO (浓) CuSO + SO ↑+ 2H O 在常温下,浓硫酸使铁、铝钝化
2 4 4 2 2
C + 2H SO (浓) CO↑+ 2SO ↑+ 2H O
2 4 2 2 2
N + O ===== 2NO 自然固氮
2 2
2NO + O =2NO
2 2
3NO + H O= 2HNO + NO
2 2 3
N
工业合成氨,人工固氮
N + 3H 2NH
2 2 3
NH +H O =NH·H O 氨水的成分:
3 2 3 2
NH ·H O NH + + OH- NH 、HO、NH ·H O、NH +、OH-、H+
3 2 4 3 2 3 2 4NH + HCl= NH Cl 浓氨水和浓盐酸靠近,产生白烟
3 4
4NH + 5O ===== 4NO + 6H O 氨的催化氧化,用于工业制硝酸
3 2 2
NH HCO NH ↑ + H O + CO ↑
4 3 3 2 2
NH Cl NH ↑ + HCl↑ 固体逐渐消失,试管口得到白色固体
4 3
2NH Cl+Ca(OH) CaCl +2NH ↑+2HO 实验室制氨气
4 2 2 3 2
4HNO ====== 4NO ↑ + O ↑ + 2H O 浓硝酸久置显黄色
3 2 2 2
Cu + 4HNO (浓=Cu(NO) + 2NO ↑ + 2H O
3 3 2 2 2
3Cu + 8HNO (稀)=3Cu(NO) + 2NO↑+ 4H O 在常温下,浓硝酸使铁、铝钝化
3 3 2 2
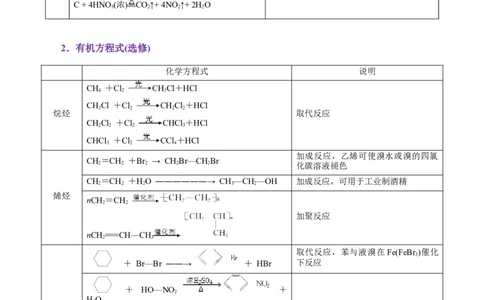
C + 4HNO (浓) CO↑+ 4NO ↑+ 2H O
3 2 2 2
2.有机方程式(选修)
化学方程式 说明
CH +Cl CHCl+HCl
4 2 3
CHCl +Cl CHCl+HCl
3 2 2 2
烷烃 取代反应
CHCl +Cl CHCl +HCl
2 2 2 3
CHCl +Cl CCl +HCl
3 2 4
加成反应,乙烯可使溴水或溴的四氯
CH=CH +Br → CHBr—CHBr
2 2 2 2 2 化碳溶液褪色
CH=CH +HO ――――――→ CH—CH—OH 加成反应,可用于工业制酒精
2 2 2 3 2
烯烃
nCH=CH
2 2
加聚反应
nCH===CH—CH
2 3
取代反应,苯与液溴在Fe(FeBr)催化
3
+ Br—Br ――→ + HBr 下反应
+ HO—NO +
2
HO
2
芳香烃
硝化反应/取代反应
加成反应
+3H
2
水解反应/取代反应
卤代烃
消去反应2CHCHOH+2Na → 2CHCHONa+H↑
3 2 3 2 2
2CHCHOH+O ――――→ 2CHCHO+2HO 氧化反应
3 2 2 3 2
CHCHOH+HBr――→C HBr+HO 取代反应
3 2 2 5 2
醇
CHCHOH――→CH==CH ↑+HO 消去反应,分子内脱水
3 2 2 2 2
2CHCHOH――→CHCHOCH CH+HO 取代反应,分子间脱水
3 2 3 2 2 3 2
CHCHOH + CHCOOH CHCOOCH CH +
3 2 3 3 2 3 酯化反应/取代反应,酸脱羟基醇脱氢
HO
2
酸性:HCO> >HCO -
2 3 3
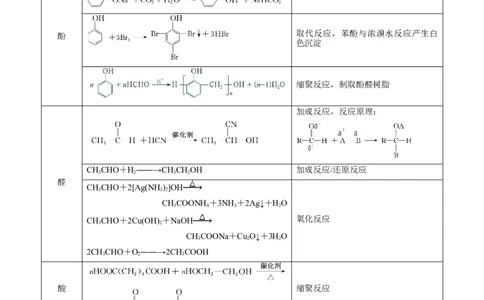
取代反应,苯酚与浓溴水反应产生白
酚
色沉淀
缩聚反应,制取酚醛树脂
加成反应,反应原理:
CHCHO+H――→CHCHOH 加成反应/还原反应
3 2 3 2
醛
CHCHO+2[Ag(NH)]OH
3 3 2
CHCOONH+3NH +2Ag↓+HO
3 4 3 2
CHCHO+2Cu(OH) +NaOH 氧化反应
3 2
CHCOONa+Cu O↓+3HO
3 2 2
2CHCHO+O――→2CHCOOH
3 2 3
酸 缩聚反应
CHCOOC H+HO CHCOOH+C HOH
酯 3 2 5 2 3 2 5 水解反应/取代反应
CHCOOC H+NaOH CHCOONa+ C HOH
3 2 5 3 2 5
2NH CHCOOH→NH CHCO-NHCH COOH+HO 取代反应,酸脱-OH氨脱-H
2 2 2 2 2 2
氨基酸
nNH -CH-COOH→ NH-CH-CO +nHO 缩聚反应
2 2 2 2
3.与工业生产相关的重要反应工业制漂白粉 2Ca(OH) +2Cl===Ca(ClO) +CaCl +2HO
2 2 2 2 2
NaCl+NH +CO+HO===NaHCO+NH Cl、2NaHCO NaCO+
3 2 2 3 4 3 2 3
工业制纯碱
CO↑+HO
2 2
合成氨工业
N+3H 2NH
2 2 3
工业制盐酸 H+Cl=====2HCl
2 2
4FeS+11O 2Fe O+8SO 、2SO +O 2SO 、SO +
硫酸工业 2 2 2 3 2 2 2 3 3
HO===H SO
2 2 4
4NH +5O 4NO+6HO、2NO+O===2NO、3NO +
硝酸工业 3 2 2 2 2 2
HO===2HNO +NO
2 3
氯碱工业 2NaCl+2HO 2NaOH+H↑+Cl↑
2 2 2
工业制玻璃 NaCO+SiO NaSiO+CO↑、CaCO +SiO CaSiO +CO↑
2 3 2 2 3 2 3 2 3 2
高炉炼铁 Fe O+3CO 2Fe+3CO
2 3 2