文档内容
考前速记02
常见元素及其化合物知识集萃
(一)物质的性质
1.钠
(1)钠的取用方法:用镊子夹取一小块钠,用滤纸吸干表面的煤油,在玻璃片上用小刀切取黄豆粒大小
的钠,剩余的钠放回原试剂瓶。
(2)钠与氧气反应的产物与反应温度有关,加热或点燃产物是过氧化钠。
(3)不管生成氧化钠还是过氧化钠,金属钠失电子均变为+1价的阳离子,因而等量的钠完全反应失去
的电子数相同。
(4)钠与水、酸、盐溶液反应的本质与顺序:本质上均是与 H+的反应,反应顺序是“有酸酸在前,无
酸水为先”。
(5)钠与水、酸反应的实质都是与H+的反应。钠与乙醇反应,钠块先沉在液面下,后上下浮动、能看
到表面冒出气泡,并不能熔化成小球。
(6) 金 属 钠 暴 露 在 空 气 中 会 发 生 一 系 列 变 化 , 最 终 生 成 NaCO : 银 白 色 金 属
2 3
钠――→NaO――→NaOH――→表面形成NaOH浓溶液――→NaCO·10H O――→NaCO。
2 2 3 2 2 3
(7)钠、钾、镁等活泼金属着火后,不能用水或泡沫灭火器灭火,应用干沙土扑灭。
(8) Na O、NaO 结构中阳离子和阴离子的个数之比均为2:1;
2 2 2
(9)1 mol Na O 与足量CO 或HO发生反应时转移电子数是1 mol;
2 2 2 2
(10)Na O 不是碱性氧化物。
2 2
(11)同温、同浓度的NaCO 和NaHCO 溶液的碱性是NaCO>NaHCO;因此,向两溶液中分别滴入酚
2 3 3 2 3 3
酞溶液,NaCO 溶液呈红色而NaHCO 溶液呈浅红色。
2 3 3
(12)Na CO 溶液中混有少量NaHCO 时,理论上加入适量NaOH可以除去,但实际上无法操作,因为
2 3 3
无法准确控制NaOH的用量。
(13)当NaCO、NaHCO 溶液的浓度不同时,一般不用气体法来鉴别。
2 3 3
(14)不能用Ca(OH) 或Ba(OH) 溶液鉴别NaCO 和NaHCO ,因为二者都能产生白色沉淀。
2 2 2 3 3
(15)焰色试验属于物理变化,焰色属于元素的性质,即同种元素的单质或化合物,固体或相应的溶液
均会产生同样的焰色。
(16)用稀盐酸而不用稀硫酸清洗铂丝的原因:铂丝表面的杂质与盐酸反应生成的氯化物沸点较低,易
汽化挥发,而硫酸盐的沸点较高,不易汽化挥发。
(17)并不是所有金属及其化合物灼烧时火焰均有颜色。
(18)碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。(19)碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
2.铁
(1)自然界中有少量游离态的铁(陨石中),纯净的铁块是银白色的,而铁粉是黑色的。
(1)Fe分别与O(点燃)、HO(g)(高温)反应的产物都是Fe O 而不是Fe O。
2 2 3 4 2 3
(2)Fe在Cl 中燃烧,无论Cl 过量还是不足均生成FeCl ;铁与硫蒸气反应生成的是FeS而不是Fe S ;
2 2 3 2 3
铁与碘蒸气反应生成的是FeI 而不是FeI。
2 3
(3)常温下,Fe、Al在冷的浓硫酸和浓硝酸中发生钝化,但加热后继续反应。
(4)铁在潮湿的空气中生成的铁锈的主要成分是Fe O,而铁在纯氧中燃烧的产物是Fe O。
2 3 3 4
(5)Fe O 的组成可理解为FeO·Fe O ,与非氧化性酸如盐酸、稀硫酸反应时生成Fe2+和Fe3+;与氧
3 4 2 3
化性酸如HNO 反应时生成Fe3+;与还原性酸如HI反应时生成Fe2+。
3
(6)Fe2+主要表现为还原性,Fe2+与NO可共存,但有H+存在时不共存。
(7)向含Fe2+的溶液中加入硝酸、KMnO 溶液、氯水等具有氧化性的物质时,溶液会出现浅绿色棕黄
4
色的颜色变化,该现象可用于Fe2+的检验。
(8)Fe3+的检验方法较多,如观察溶液颜色法(棕黄色)、NaOH溶液法(生成红褐色沉淀)、KSCN溶液法
(生成血红色溶液),前面两种方法需溶液中Fe3+浓度较大时才适用,最好也最灵敏的方法是KSCN溶液法。
Fe2+的检验可采用先加入KSCN溶液后加入氧化剂的方法。
3.铝
(1)Mg、Al在常温下均易在其表面形成致密的氧化膜。
(2)活泼金属与酸反应是金属的通性,而铝不仅能与酸(H+)反应,还能够与碱溶液反应,表现出特殊性:
2Al+2OH-+2HO===2AlO+3H↑。
2 2
(3)常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、
浓硝酸不反应。
(4)铝制品不宜长时间盛放咸菜等腌制食品,原因是氯化钠溶液中的氯离子会破坏氧化膜的结构。
(5)铝与稀硝酸反应时生成的气体是NO而不是H。
2
(6)用铝箔包裹的钠与HO反应时既考虑Na与HO的反应,又考虑Al与NaOH溶液的反应。
2 2
(7)铝热剂(发生铝热反应)。铝热剂是铝与金属氧化物的混合物,铝热反应本质上是金属之间的置换反
应,所以要遵循金属活动性顺序。例如:CuO与Al能发生铝热反应,而Al与MgO的混合物不能发生铝热
反应。
(8)制取Al(OH) ,一般不用强酸或强碱溶液,因为强酸、强碱能溶解生成的Al(OH) ,而又无法控制酸
3 3
碱的用量,一般使用氨水或CO 制取。
2
4.卤素
(1)氯气与水、强碱的反应中,氯气既做氧化剂又作还原剂。
(2)常温下干燥的氯气或液氯均不与铁反应,故液氯通常储存在钢瓶中。(3)氯气具有强氧化性,与变价金属反应时均生成高价态的金属氯化物,如 FeCl 不能由两种单质化合
2
生成。
(4)氯气没有漂白性,不能使干燥的有色布条褪色,但可使湿润的有色布条褪色,起漂白作用的物质是
HClO。
(5)Cl 可使湿润石蕊试纸先变红后褪色,原因是Cl 与水反应生成的酸使石蕊先变红,HClO使变色后
2 2
的石蕊褪色。
(6)HClO不稳定,不能单独存在,只存在于氯水、次氯酸盐溶液或次氯酸盐与酸反应的混合物中。
(7)久置氯水成分与性质分析:氯水中存在Cl +HO HCl+HClO,久置氯水中因HClO见光分解,
2 2
随着HClO的消耗,最后成为盐酸,久置氯水酸性增强,无漂白性。
(8)氯水的保存:密封保存在棕色试剂瓶中,并放在阴暗处。
(9)氯水能导电,但氯水是混合物,液氯是单质,它们既不是电解质,也不是非电解质。
(10)不能用pH试纸测量氯水的pH,原因是氯水中的HClO具有漂白性。
(11)工业上制取漂白粉是用氯气与石灰乳反应制得,而不是用氯气与石灰水反应。
(12)“84”消毒液的主要成分为NaClO,漂粉精的有效成分为Ca(ClO) 。“84”消毒液和洁厕灵不能混合
2
使用,其原因是ClO-+Cl-+2H+===Cl↑+HO。
2 2
(13)Br 在常温下呈液态,是唯一的液态非金属单质。液态 Br 有剧毒,易挥发,故保存Br 时在试剂瓶
2 2 2
中Br 液面上需用水封,磨口的玻璃塞用蜡封。
2
(14)淀粉遇I 显蓝色,这是碘单质的特殊性质,该性质可用于检验Cl 。Cl 可使湿润的淀粉KI试纸变
2 2 2
蓝,其实质是Cl+2I-===2Cl-+I。此外碘单质易升华,是常温下固体单质中唯一的双原子分子。
2 2
(15)Br 和I 都可被某些有机溶剂(如四氯化碳、苯)萃取。
2 2
(16)氟元素无正价,F 与HO发生置换反应生成O:2F+2HO===4HF+O。
2 2 2 2 2 2
(17)F 不能从NaX溶液中置换出X(X代表Cl、Br、I)。
2 2
(18)卤族元素的单质F、Cl、Br 均能将Fe氧化为Fe3+,而I 只能把Fe氧化为Fe2+,即:I 与Fe反应
2 2 2 2 2
产生FeI,Fe与其他卤素单质生成FeX。
2 3
(19)加碘食盐中的碘是KIO 而不是I 或KI。
3 2
5.硅
(1)自然界中无游离态的硅,通常原子晶体不导电,但硅是很好的半导体材料,是制作光电池的材料。
SiO 不导电,是制作光导纤维的材料。
2
(2)不要混淆硅和二氧化硅的用途:用作半导体材料的是晶体硅而不是SiO ,用于制作光导纤维的是
2
SiO 而不是硅。
2
(3)工业上制备粗硅,是用过量的C和SiO 高温下反应,由于C过量,生成的是CO而不是CO ,该反
2 2
应必须在隔绝空气的条件下进行。
(4)氢氟酸不能用玻璃容器盛放;NaOH溶液能用玻璃试剂瓶盛放,但不能用玻璃塞。(5)酸性氧化物一般能与水反应生成酸,但SiO 不溶于水;酸性氧化物一般不与酸作用,但SiO 能与
2 2
HF反应。
(6)不要混淆常见含硅物质的成分:①计算机芯片的成分是晶体硅而不是SiO ;②水晶、石英、玛瑙等
2
主要成分是SiO,而不是硅酸盐;③传统无机非金属材料陶瓷、水泥、玻璃的主要成分是硅酸盐。
2
6.硫
(1)实验室中,残留在试管内壁上的硫可用CS 溶解除去,也可用热的NaOH溶液除去,反应化学方程
2
式为3S+6NaOH 2NaS+NaSO +3HO。
2 2 3 2
(2)硫单质的氧化性较弱,与变价金属反应时一般生成低价态金属硫化物(和Cl 与变价金属的反应情况
2
相反),如FeS、Cu S等。
2
(3)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
(4)硫在空气中燃烧发出淡蓝色火焰,在纯氧中燃烧发出蓝紫色火焰,产物只能是SO ,无论O 的量是
2 2
否充足,均不会生成SO 。
3
(5)SO 使品红溶液褪色表现的是SO 的漂白性,加热后溶液颜色复原;SO 使酸性高锰酸钾溶液、溴水、
2 2 2
氯水、碘水褪色表现的是SO 的还原性,加热后溶液颜色不复原。
2
(6)SO 不能漂白酸碱指示剂,如只能使紫色的石蕊试液变红,但不能使之褪色。
2
(7)SO 能使溴水、酸性KMnO 溶液褪色,体现了SO 的还原性,而不是漂白性。
2 4 2
(8)浓硫酸能氧化(必要时加热)除Au、Pt以外的所有金属,其还原产物是SO 而不是H。
2 2
(9)常温下,浓硫酸与Fe、Al并不是不反应,而是发生了“钝化”,“钝化”是浓硫酸将Fe、Al氧化
而在其表面形成一层致密的氧化物薄膜,阻止了浓硫酸与Fe、Al的继续反应,体现了浓硫酸的强氧化性。
(10)注意“量变”引起的“质变”。在理解浓硫酸与铜、锌、铁、铝以及与碳、硫等反应时,要动态
地看待反应过程,如在浓硫酸与铜的反应中,开始是浓硫酸,但随着反应的进行硫酸的浓度逐渐减小,最
后变成了稀硫酸,稀硫酸与铜不反应。
(11)工业制硫酸过程中,为了提高SO 的吸收率,防止形成酸雾,常用浓硫酸来吸收SO 得到发烟硫酸。
3 3
7.氮
(1)因为水溶液中发生反应3NO +H O 2HNO+NO,所以无论何种情况下水溶液中不会剩余NO 。
2 2 3 2
(2)氮的氧化物都有毒,其中NO 与NO 存在下列平衡:2NO NO,因此实验测得NO 的平均
2 2 4 2 2 4 2
相对分子质量大于46。
(3)NO只能用排水法收集,不能用排空气法收集;而NO 只能用向上排空气法收集,不能用排水法收
2
集。
(4)验证某无色气体是NO的方法是向无色气体中通入O(或空气),无色气体变为红棕色。
2
(5)NO 既有氧化性又有还原性,以氧化性为主。NO 能使湿润的淀粉KI试纸变蓝。
2 2
(6)氨气极易溶于水,直接通入水中会引起倒吸。氨水的成分主要是NH ·H O,但在计算浓度时,溶质
3 2
应为NH ,且氨水的浓度越大,密度越小。
3(2)固体中NH的检验方法是取样溶解,加入浓氢氧化钠溶液并加热,用湿润的红色石蕊试纸检验产生
的气体,若试纸变蓝说明原固体含有NH。
(7)液氨是由氨气液化而得到的纯净物,所含粒子只有 NH 分子;氨水是由NH 溶于水而形成的混合物,
3 3
所含粒子有三种分子:NH 、NH ·H O、HO,三种离子:NH、OH-、H+。
3 3 2 2
(8)实验室用固体铵盐与碱共热制 NH 时,不能使用 NH HCO 、NH NO 及 NaOH 固体,因为
3 4 3 4 3
NH HCO 受热分解产生CO ,使制得的NH 不纯;NH NO 受热时易发生爆炸;NaOH容易吸水结块,不
4 3 2 3 4 3
利于NH 的产生和逸出,且加热条件下NaOH容易腐蚀玻璃。
3
(9)干燥氨气时不能选用酸性干燥剂,如浓硫酸、PO 等,也不能选用无水CaCl ,因为它们均能与
2 5 2
NH 发生反应,通常选用碱石灰。
3
(10)吸收氨气(或HCl)时要注意防止倒吸。
(二)常见物质的用途
N:合成氨,填充灯泡(与氩气),保存粮食。
2
稀有气体:保护气,霓虹灯,激光。
H:探空气球,氢氧焰,冶金,合成氨,高能无害燃料。
2
CO:灭火剂,制纯碱,制尿素,人工降雨(干冰)。
2
C:金刚石:制钻头;石墨:制电极,坩埚,铅笔芯,高温润滑剂;木炭:制黑火药;焦炭:冶金;炭
黑:制油黑、颜料、橡胶耐磨添加剂。
CaCO :建筑石料,混凝土,炼铁熔剂,制水泥,制玻璃,制石灰。
3
Cl :氯气是一种重要的化工原料,在生活和生产中的应用十分广泛。自来水的消毒、农药的生产、药
2
物的合成等都需要用到氯气。
ClO :二氧化氯的应用十分广泛,除用于一般的杀菌、消毒外,还广泛地用于环保、灭藻、漂白、保
2
鲜、除臭等方面。
Br :溴可用于生产多种药剂,如熏蒸剂、杀虫剂、抗爆剂等。
2
AgBr:溴化银是一种重要的感光材料,是胶卷中必不可少的成分。
I:碘是一种重要的药用元素,含碘食品的生产也需要碘元素。
2
AgI:可用于人工降雨。
S:制硫酸,硫化橡胶,制黑火药,制农药石硫合剂,制硫磺软膏治疗皮肤病。
P:白磷制高纯度磷酸],红磷[制农药,制火柴,制烟幕弹。
Si:制合金,制半导体。
SiO:制光导纤维,石英玻璃,普通玻璃]
2
NaO:过氧化钠可用作漂白剂和呼吸面具中的供氧剂。
2 2
Na:钠除了可用来制取一些钠的化合物外,还可用于从钛、锆、铌、钽等金属的氯化物中置换出金属
单质。充有钠蒸气的高压钠灯发出的黄光射程远,透雾能力强,常用于道路和广场的照明。Na、K:钠和钾的合金在常温下是液体,可用于快中子反应堆作热交换剂。
NaCO :碳酸钠的水溶液呈碱性,因而被称为“纯碱”。热的纯碱溶液可以去除物品表面的油污。纯
2 3
碱是一种非常重要的化工原料,在玻璃、肥皂、合成洗涤剂、造纸、纺织、石油、冶金、食品等工业中有
着广泛的应用。
NaHCO :碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一;在医疗上,它是治疗胃酸过多的一种药
3
剂。
Mg:镁能与铜、铝、锡、锰、钛等形成许多合金,镁合金的密度较小,但硬度和强度都较大,因此被
大量用于制造火箭、导弹和飞机的部件等。由于镁燃烧会发出耀眼的白光,因此常用来制造信号弹和焰火。
MgO:氧化镁的熔点高达2 800 ℃,是优质的耐高温材料。
FeCl :在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。
3
FeCl 、FeSO :氯化铁、硫酸亚铁是优良的净水剂。(说明:Fe3+、Fe2+可水解生成胶体)
3 4
Fe O:氧化铁红颜料跟某些油料混合,可以制成防锈油漆。
2 3
Fe:磁性材料大多数是含铁的化合物。人体中的铁元素大部分存在于血红蛋白内,血红蛋白起着运输
氧气、二氧化碳的作用。铁的化合物还在人体内发生的氧化还原反应中起传递电子的作用。人体缺铁会引
起贫血等疾病。
Cu2+:由于铜盐能杀死某些细菌,并能抑制藻类生长,因此游泳场馆常用硫酸铜作池水消毒剂。稀的
硫酸铜溶液还可用于杀灭鱼体上的寄生虫,治疗鱼类皮肤病和鳃病等。
NaSiO :硅酸钠是极少数可溶于水的硅酸盐中的一种,硅酸钠的水溶液俗称“水玻璃”,是建筑行业
2 3
经常使用的一种黏合剂。人们也经常把具有特殊用途的木材、纺织品等用水玻璃浸泡,这样加工的产品既
耐腐蚀又不易着火。
分子筛(具有多孔结构的硅酸盐):常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、
催化剂及催化剂载体等。
SiO :二氧化硅除可用于制作光学镜片、石英坩埚外,还可用于制造光导纤维。光导纤维非常细,导
2
光能力很强,一条光缆由上万条光导纤维组成,因此利用光缆通讯能同时传输大量的信息。
Si:硅晶体的导电性介于导体和绝缘体之间,是一种重要的半导体材料,广泛应用于电子工业的各个
领域。
SO :在工业上,二氧化硫可用于漂白纸浆以及草帽等编织物。
2
HSO :硫酸在生产中具有广泛的应用。化肥、医药、农药的生产,金属矿石的处理,金属材料的表面
2 4
清洗等都要用到硫酸。
明矾:净水剂。
CaSO :人们常用它制作各种模型和医疗上用的石膏绷带。在水泥生产中,可用石膏调节水泥的凝结
4
时间。在石膏资源丰富的地方也可以用它来制硫酸。
BaSO :硫酸钡不容易被X射线透过,在医疗上可用作检查肠胃的内服药剂,俗称“钡餐”。硫酸钡
4还可用作白色颜料,并可作高档油漆、油墨、造纸、塑料、橡胶的原料及填充剂。
FeSO :在医疗上硫酸亚铁可用于生产防治缺铁性贫血的药剂,在工业上硫酸亚铁还是生产铁系列净水
4
剂和颜料氧化铁红(主要成分为Fe O)的原料。
2 3
皓矾:医疗收敛剂,木材防腐剂,媒染剂,制颜料。
乙烯:果实催熟剂。
(三)常见物质的颜色
有色气体单质:F、Cl、O
2 2 3
其他有色单质:Br (深红色液体)、I(紫黑色固体)、S(淡黄色固体)、Cu(紫红色固体)、Au(金黄色固体)、
2 2
Si(灰黑色晶体)、C(黑色粉未)
无色气体单质:N、O、H
2 2 2
有色气体化合物:NO
2
黄色固体:S、NaO、Ag PO 、AgBr、AgI
2 2 3 4
黑色固体:FeO、Fe O、MnO 、C、CuS、CuO
3 4 2
红色固体:Fe(OH) 、Fe O、Cu O、Cu
3 2 3 2
蓝色固体:五水合硫酸铜(胆矾或蓝矾)
绿色固体:七水合硫酸亚铁(绿矾)
紫黑色固体:KMnO 、碘单质。
4
白色[Fe(OH) 、CaCO 、BaSO、AgCl、BaSO]
2 3 4 3
有色离子(溶液)Cu2+、Fe2+、Fe3+、MnO -、Fe(SCN) (血红色)
4 3
不溶于稀酸的白色沉淀:AgCl、BaSO
4
不溶于稀酸的黄色沉淀:S、AgBr、AgI
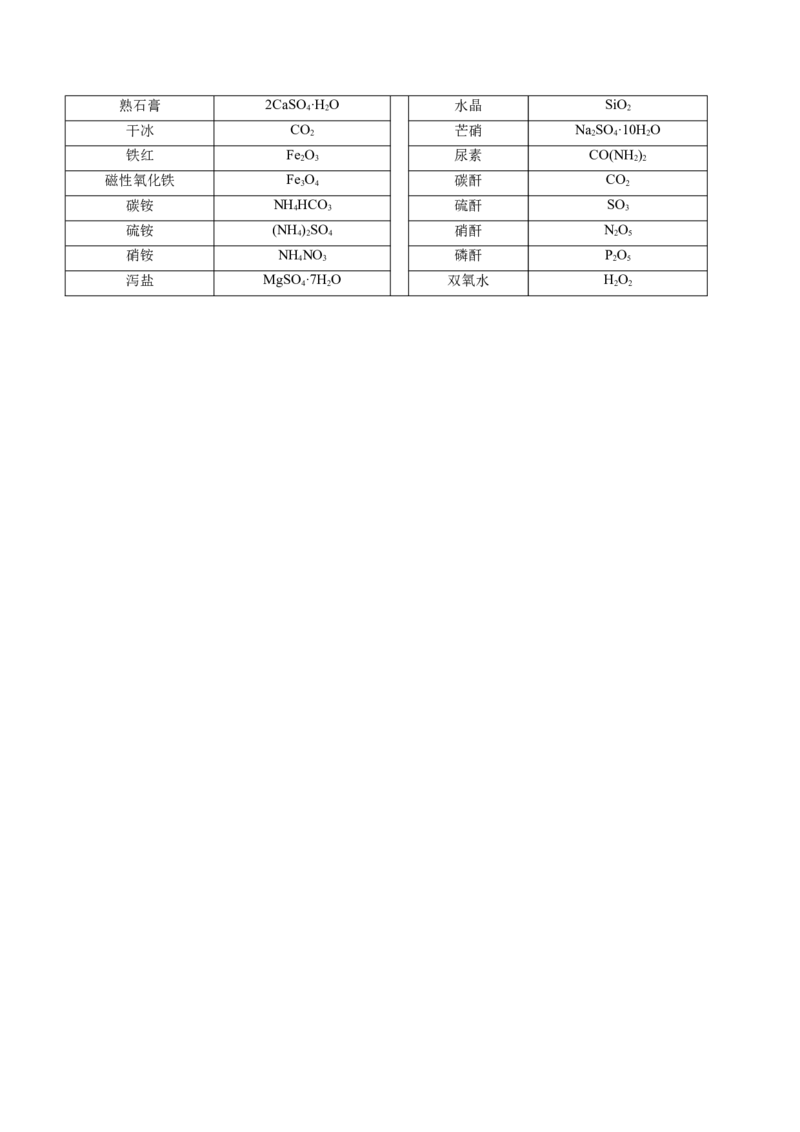
(四)常见物质的名称和化学式
名 称 主要成分的化学式 名 称 主要成分的化学式
漂白粉 Ca(ClO) 、CaCl 液氨 NH
2 2 3
面碱、洗涤碱 NaCO·10H O 铜 绿 Cu (OH) CO
2 3 2 2 2 3
纯碱(苏打) NaCO 硫铁矿 FeS
2 3 2
烧(火)碱 NaOH 蓝(胆)矾 CuSO ·5H O
4 2
硫 磺 S 绿矾 FeSO ·7H O
4 2
小苏打 NaHCO 明(白)矾 KAl(SO )·12H O
3 4 2 2
大苏打(海波) NaSO·5H O 皓矾 ZnSO·7H O
2 2 3 2 4 2
生石灰 CaO 金刚石 C
消(熟)石灰 Ca(OH) 石墨 C
2
石膏 CaSO·2H O 水银 Hg
4 2熟石膏 2CaSO·H O 水晶 SiO
4 2 2
干冰 CO 芒硝 NaSO ·10H O
2 2 4 2
铁红 Fe O 尿素 CO(NH)
2 3 2 2
磁性氧化铁 Fe O 碳酐 CO
3 4 2
碳铵 NH HCO 硫酐 SO
4 3 3
硫铵 (NH )SO 硝酐 NO
4 2 4 2 5
硝铵 NH NO 磷酐 PO
4 3 2 5
泻盐 MgSO ·7H O 双氧水 HO
4 2 2 2