文档内容
考向 20 原电池 化学电源
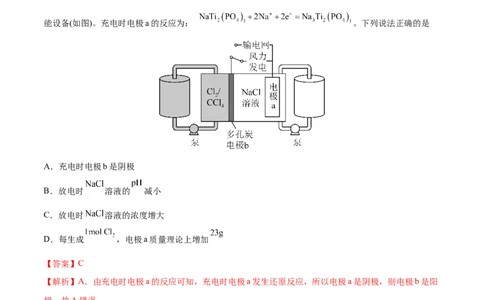
【2022·广东卷】科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电池,可作储
能设备(如图)。充电时电极a的反应为: 。下列说法正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
【答案】C
【解析】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳
极,故A错误;
B.放电时电极反应和充电时相反,则由放电时电极a的反应为 可
知,NaCl溶液的pH不变,故B错误;
C.放电时负极反应为 ,正极反应为 ,反应后
Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确;D.充电时阳极反应为 ,阴极反应为 ,由得失电
子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol 2mol=46g,故D错误;
2
答案选C。
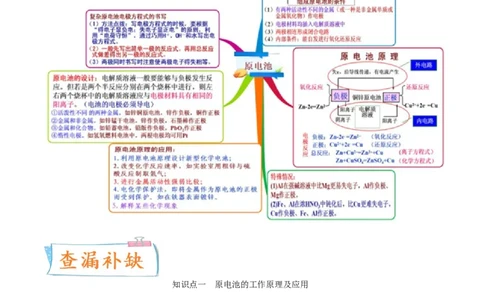
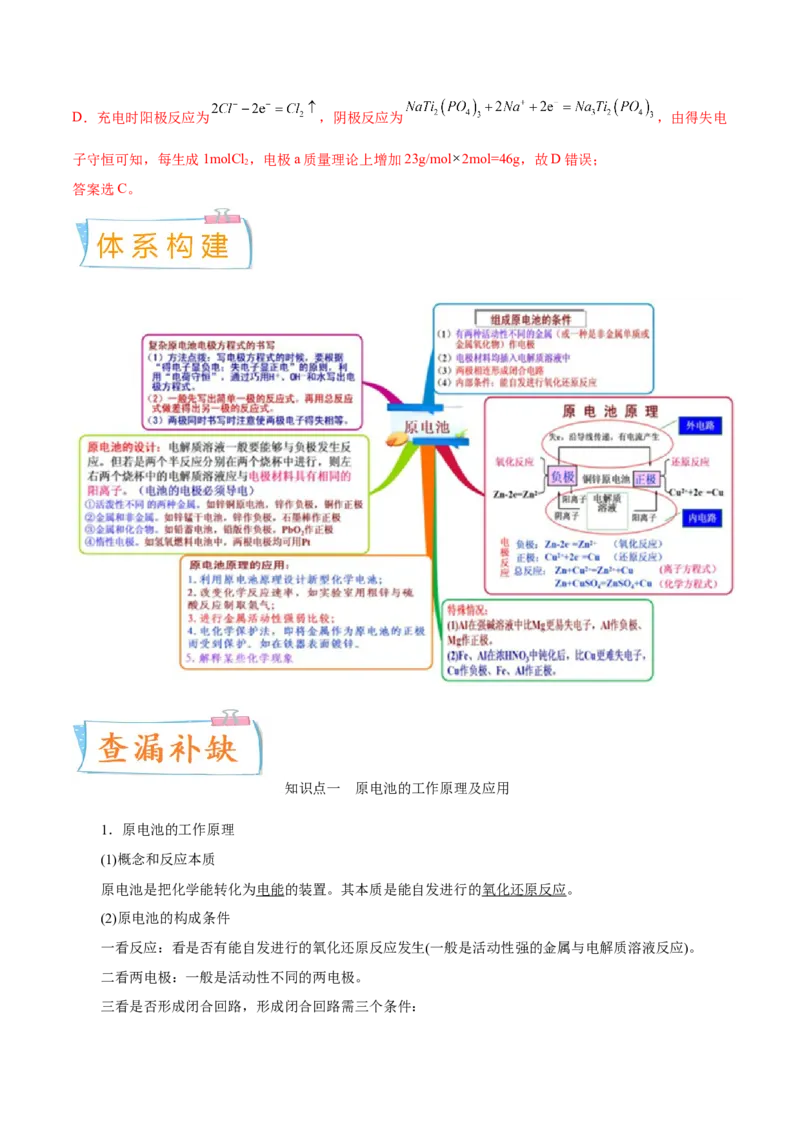
知识点一 原电池的工作原理及应用
1.原电池的工作原理
(1)概念和反应本质
原电池是把化学能转化为电能的装置。其本质是能自发进行的氧化还原反应。
(2)原电池的构成条件
一看反应:看是否有能自发进行的氧化还原反应发生(一般是活动性强的金属与电解质溶液反应)。
二看两电极:一般是活动性不同的两电极。
三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;
②两电极直接或间接接触;
③两电极插入电解质溶液中。
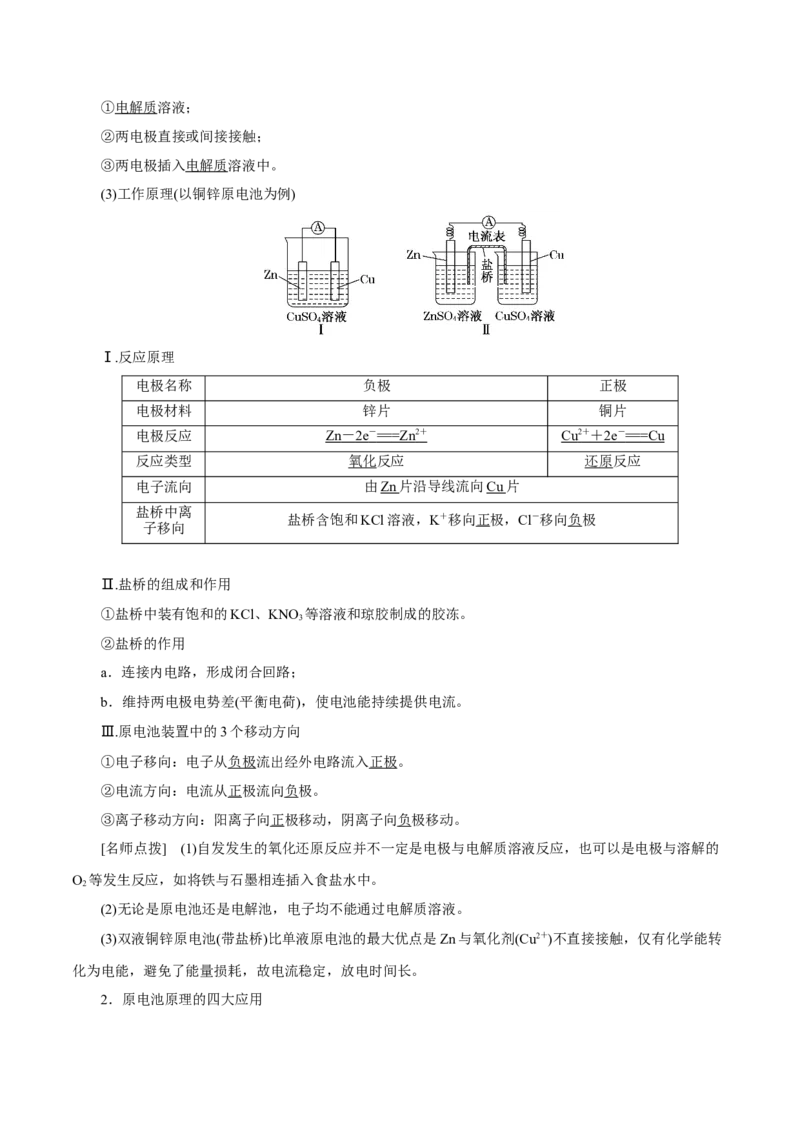
(3)工作原理(以铜锌原电池为例)
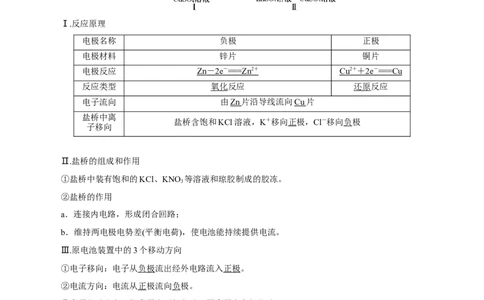
Ⅰ.反应原理
电极名称 负极 正极
电极材料 锌片 铜片
电极反应 Zn - 2e - == =Zn 2 + Cu 2 + + 2e - == =Cu
反应类型 氧化反应 还原反应
电子流向 由Zn 片沿导线流向Cu 片
盐桥中离
盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极
子移向
Ⅱ.盐桥的组成和作用
①盐桥中装有饱和的KCl、KNO 等溶液和琼胶制成的胶冻。
3
②盐桥的作用
a.连接内电路,形成闭合回路;
b.维持两电极电势差(平衡电荷),使电池能持续提供电流。
Ⅲ.原电池装置中的3个移动方向
①电子移向:电子从负极流出经外电路流入正极。
②电流方向:电流从正极流向负极。
③离子移动方向:阳离子向正极移动,阴离子向负极移动。
[名师点拨] (1)自发发生的氧化还原反应并不一定是电极与电解质溶液反应,也可以是电极与溶解的
O 等发生反应,如将铁与石墨相连插入食盐水中。
2
(2)无论是原电池还是电解池,电子均不能通过电解质溶液。
(3)双液铜锌原电池(带盐桥)比单液原电池的最大优点是Zn与氧化剂(Cu2+)不直接接触,仅有化学能转
化为电能,避免了能量损耗,故电流稳定,放电时间长。
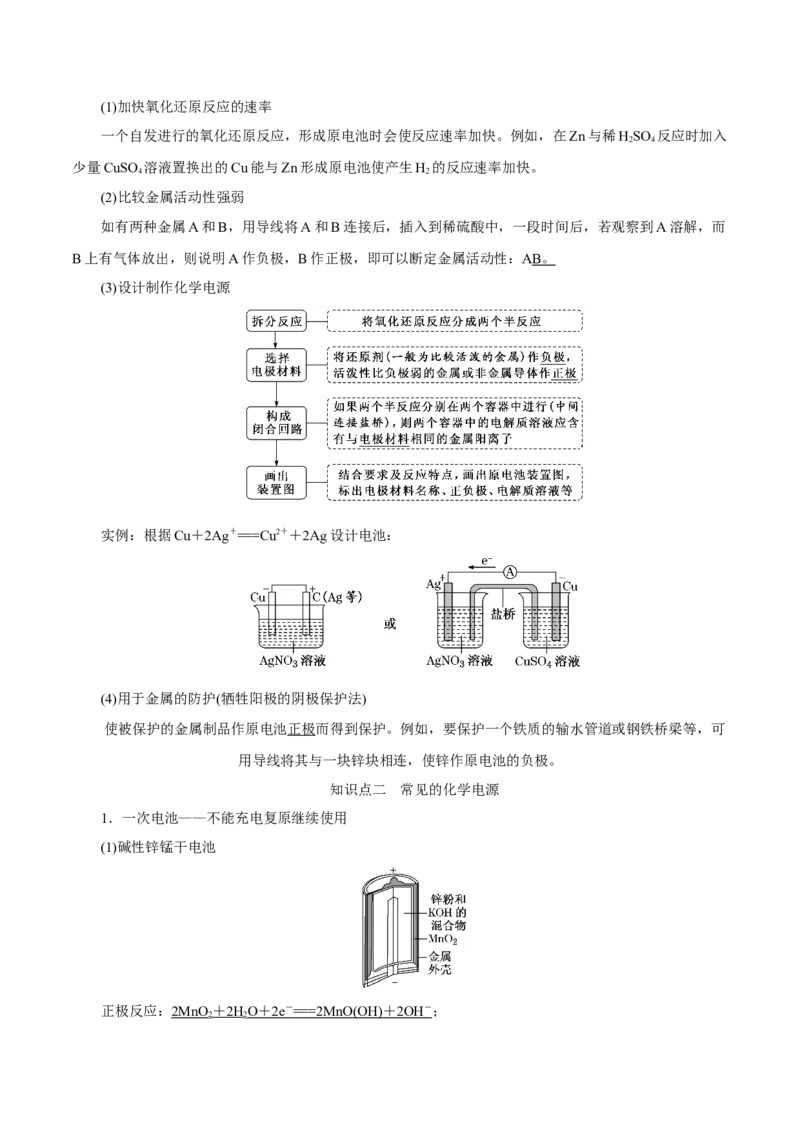
2.原电池原理的四大应用(1)加快氧化还原反应的速率
一个自发进行的氧化还原反应,形成原电池时会使反应速率加快。例如,在Zn与稀HSO 反应时加入
2 4
少量CuSO 溶液置换出的Cu能与Zn形成原电池使产生H 的反应速率加快。
4 2
(2)比较金属活动性强弱
如有两种金属A和B,用导线将A和B连接后,插入到稀硫酸中,一段时间后,若观察到A溶解,而
B上有气体放出,则说明A作负极,B作正极,即可以断定金属活动性:A B 。
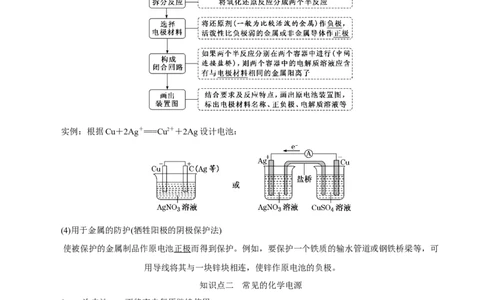
(3)设计制作化学电源
实例:根据Cu+2Ag+===Cu2++2Ag设计电池:
(4)用于金属的防护(牺牲阳极的阴极保护法)
使被保护的金属制品作原电池正极而得到保护。例如,要保护一个铁质的输水管道或钢铁桥梁等,可
用导线将其与一块锌块相连,使锌作原电池的负极。
知识点二 常见的化学电源
1.一次电池——不能充电复原继续使用
(1)碱性锌锰干电池
正极反应:2MnO + 2H O + 2e - == =2MnO(OH) + 2OH - ;
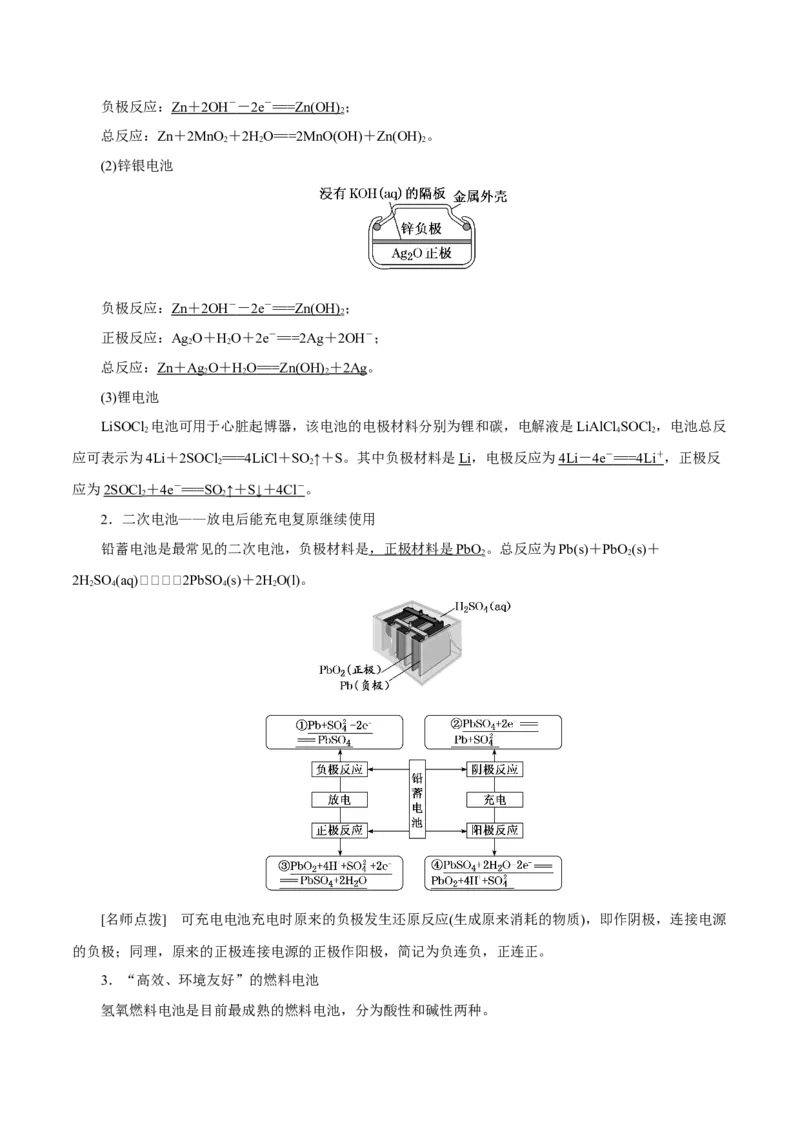
2 2负极反应: Zn + 2OH - - 2e - == =Zn(OH) ;
2
总反应:Zn+2MnO +2HO===2MnO(OH)+Zn(OH) 。
2 2 2
(2)锌银电池
负极反应: Zn + 2OH - - 2e - == =Zn(OH) ;
2
正极反应:Ag O+HO+2e-===2Ag+2OH-;
2 2
总反应: Zn + Ag O + H O == =Zn(OH) + 2A g。
2 2 2
(3)锂电池
LiSOCl 电池可用于心脏起博器,该电池的电极材料分别为锂和碳,电解液是LiAlCl SOCl ,电池总反
2 4 2
应可表示为4Li+2SOCl ===4LiCl+SO ↑+S。其中负极材料是Li,电极反应为 4Li - 4e - == =4Li + ,正极反
2 2
应为2SOCl + 4 e - == =SO ↑ + S↓ + 4Cl - 。
2 2
2.二次电池——放电后能充电复原继续使用
铅蓄电池是最常见的二次电池,负极材料是 ,正极材料是 PbO 。总反应为Pb(s)+PbO (s)+
2 2
2HSO (aq)2PbSO (s)+2HO(l)。
2 4 4 2
[名师点拨] 可充电电池充电时原来的负极发生还原反应(生成原来消耗的物质),即作阴极,连接电源
的负极;同理,原来的正极连接电源的正极作阳极,简记为负连负,正连正。
3.“高效、环境友好”的燃料电池
氢氧燃料电池是目前最成熟的燃料电池,分为酸性和碱性两种。种类 酸性 碱性
2H + 4OH - - 4 e -
2
负极反应式 2H - 4 e - == =4H +
2
== =4H O
2
O + 4H + + 4 e - 2H O + O + 4 e -
2 2 2
正极反应式
== =2H O == =4OH -
2
电池总反应 2H+O===2H O
2 2 2
[名师点拨] (1)燃料电池的电极不参与反应,有很强的催化活性,起导电作用。
(2)书写燃料电池的电极反应时,要注意溶液的酸、碱性,介质的酸碱性对半反应及总反应书写的影响。
知识点三 电极反应式的书写
1.原电池电极反应式的书写
书写电极反应式时,首先要根据原电池的工作原理准确判断正、负极,然后结合电解质溶液的环境确
定电极产物,最后再根据质量守恒和电荷守恒写出电极反应式。
(1)书写步骤
(2)书写方法
①拆分法
a.写出原电池的总反应,如2Fe3++Cu===2Fe2++Cu2+。
b.把总反应按氧化反应和还原反应拆分为两个半反应,注明正、负极,并依据质量守恒、电荷守恒
及电子得失守恒配平两个半反应:
正极:2Fe3++2e-===2Fe2+
负极:Cu-2e-===Cu2+
②加减法
a.写出总反应,如Li+LiMn O===Li MnO。
2 4 2 2 4
b.写出其中容易写出的一个半反应(正极或负极),如Li-e-===Li+(负极)。
c.利用总反应式与上述的一极反应式相减,即得另一个电极的反应式,即LiMn O+Li++e-
2 4
===Li MnO(正极)。
2 2 42.燃料电池电极反应式的书写
第一步:写出燃料电池反应的总反应式
燃料电池的总反应与燃料的燃烧反应一致,若产物能和电解质反应则总反应为加和后的反应。
如甲烷燃料电池(电解质为NaOH溶液)的反应式为
CH+2O===CO +2HO①
4 2 2 2
CO+2NaOH===Na CO+HO②
2 2 3 2
①式+②式得燃料电池总反应式为
CH+2O+2NaOH===Na CO+3HO。
4 2 2 3 2
第二步:写出电池的正极反应式
根据燃料电池的特点,一般在正极上发生还原反应的物质是O,随着电解质溶液的不同,其电极反应
2
式有所不同,大致有以下四种情况:
①酸性电解质溶液环境下电极反应式:
O+4H++4e-===2H O;
2 2
②碱性电解质溶液环境下电极反应式:
O+2HO+4e-===4OH-;
2 2
③固体电解质(高温下能传导O2-)环境下电极反应式:O+4e-===2O2-;
2
④熔融碳酸盐(如熔融KCO)环境下电极反应式:
2 3
O+2CO+4e-===2CO。
2 2
第三步:根据电池总反应式和正极反应式,写出负极反应式,电池反应的总反应式-电池正极反应式
=电池负极反应式。因为O 不是负极反应物,因此两个反应式相减时要彻底消除O。
2 2
[名师点拨] 燃料电池中产物的判断:
碱性介质:C―→CO,其余介质:C―→CO;
2
酸性介质:H―→H+,其余介质:H―→HO。
2
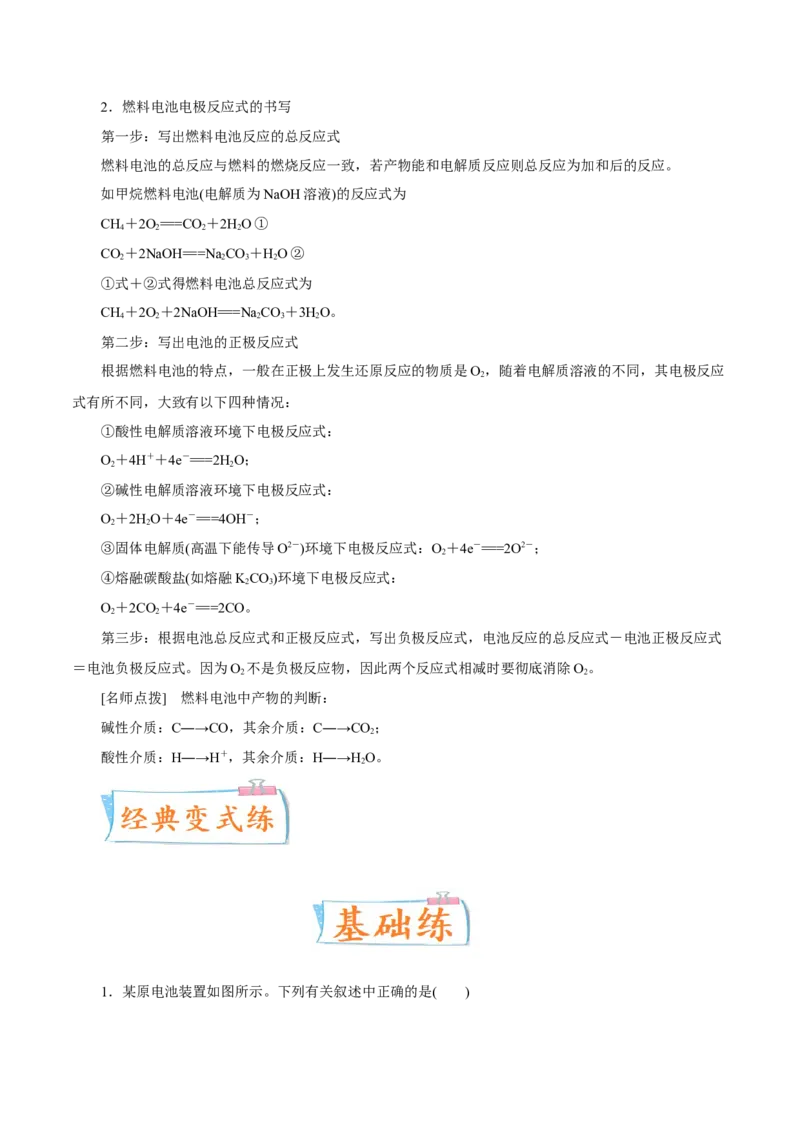
1.某原电池装置如图所示。下列有关叙述中正确的是( )A.电池工作时,盐桥中的Cl-向负极移动
B.负极反应式:2H++2e-===H ↑
2
C.工作一段时间后,两烧杯中溶液pH均不变
D.Fe作正极,发生氧化反应
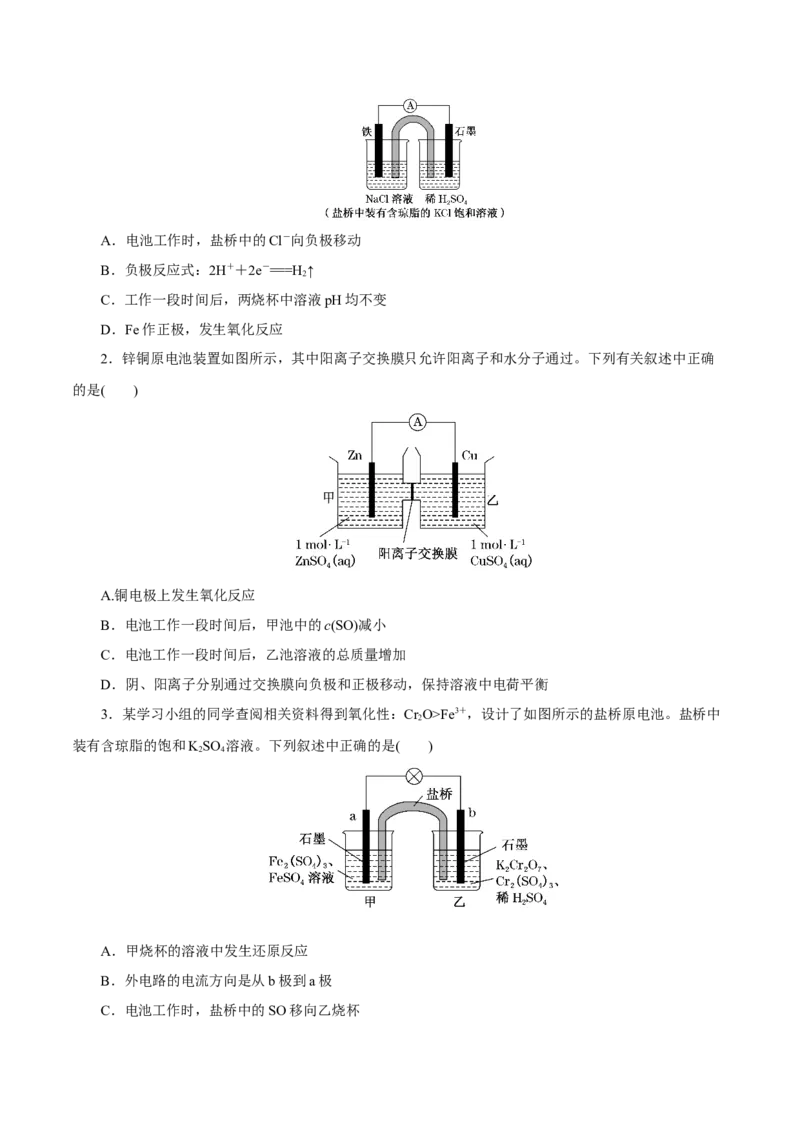
2.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述中正确
的是( )
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池中的c(SO)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
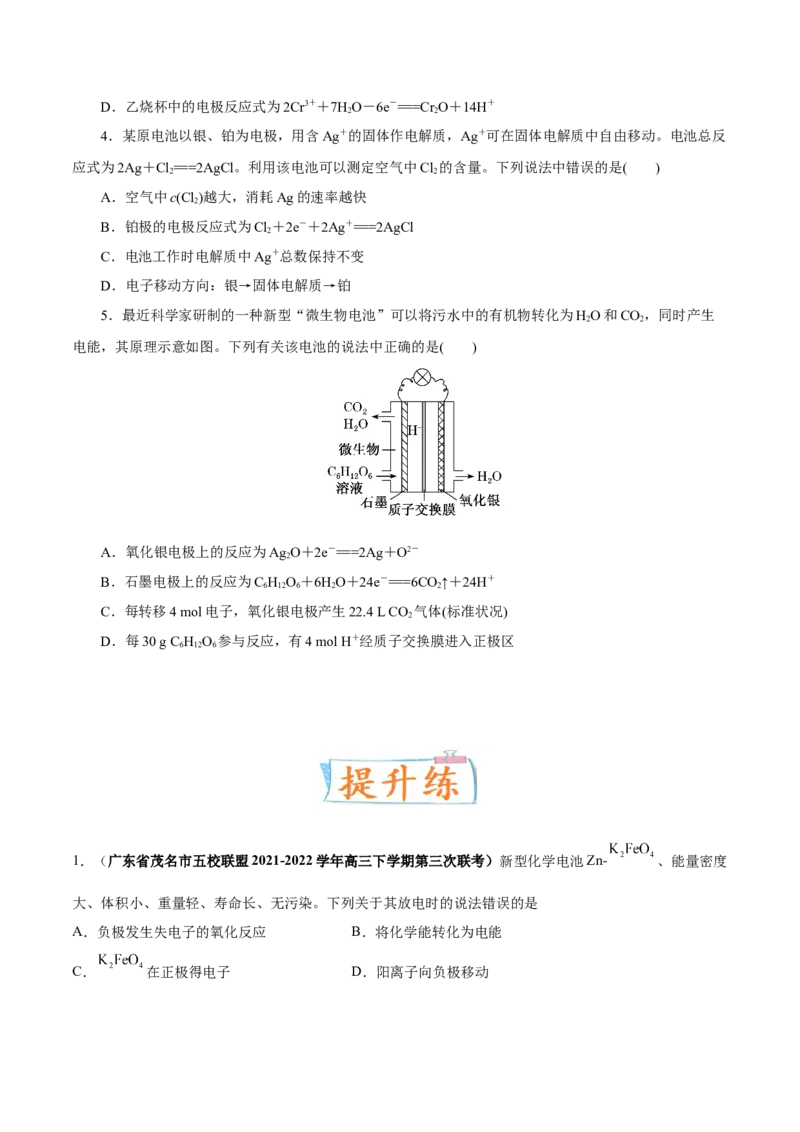
3.某学习小组的同学查阅相关资料得到氧化性:Cr O>Fe3+,设计了如图所示的盐桥原电池。盐桥中
2
装有含琼脂的饱和KSO 溶液。下列叙述中正确的是( )
2 4
A.甲烧杯的溶液中发生还原反应
B.外电路的电流方向是从b极到a极
C.电池工作时,盐桥中的SO移向乙烧杯D.乙烧杯中的电极反应式为2Cr3++7HO-6e-===Cr O+14H+
2 2
4.某原电池以银、铂为电极,用含Ag+的固体作电解质,Ag+可在固体电解质中自由移动。电池总反
应式为2Ag+Cl===2AgCl。利用该电池可以测定空气中Cl 的含量。下列说法中错误的是( )
2 2
A.空气中c(Cl )越大,消耗Ag的速率越快
2
B.铂极的电极反应式为Cl+2e-+2Ag+===2AgCl
2
C.电池工作时电解质中Ag+总数保持不变
D.电子移动方向:银→固体电解质→铂
5.最近科学家研制的一种新型“微生物电池”可以将污水中的有机物转化为HO和CO,同时产生
2 2
电能,其原理示意如图。下列有关该电池的说法中正确的是( )
A.氧化银电极上的反应为Ag O+2e-===2Ag+O2-
2
B.石墨电极上的反应为C H O+6HO+24e-===6CO ↑+24H+
6 12 6 2 2
C.每转移4 mol电子,氧化银电极产生22.4 L CO 气体(标准状况)
2
D.每30 g C H O 参与反应,有4 mol H+经质子交换膜进入正极区
6 12 6
1.(广东省茂名市五校联盟2021-2022学年高三下学期第三次联考)新型化学电池Zn- 、能量密度
大、体积小、重量轻、寿命长、无污染。下列关于其放电时的说法错误的是
A.负极发生失电子的氧化反应 B.将化学能转化为电能
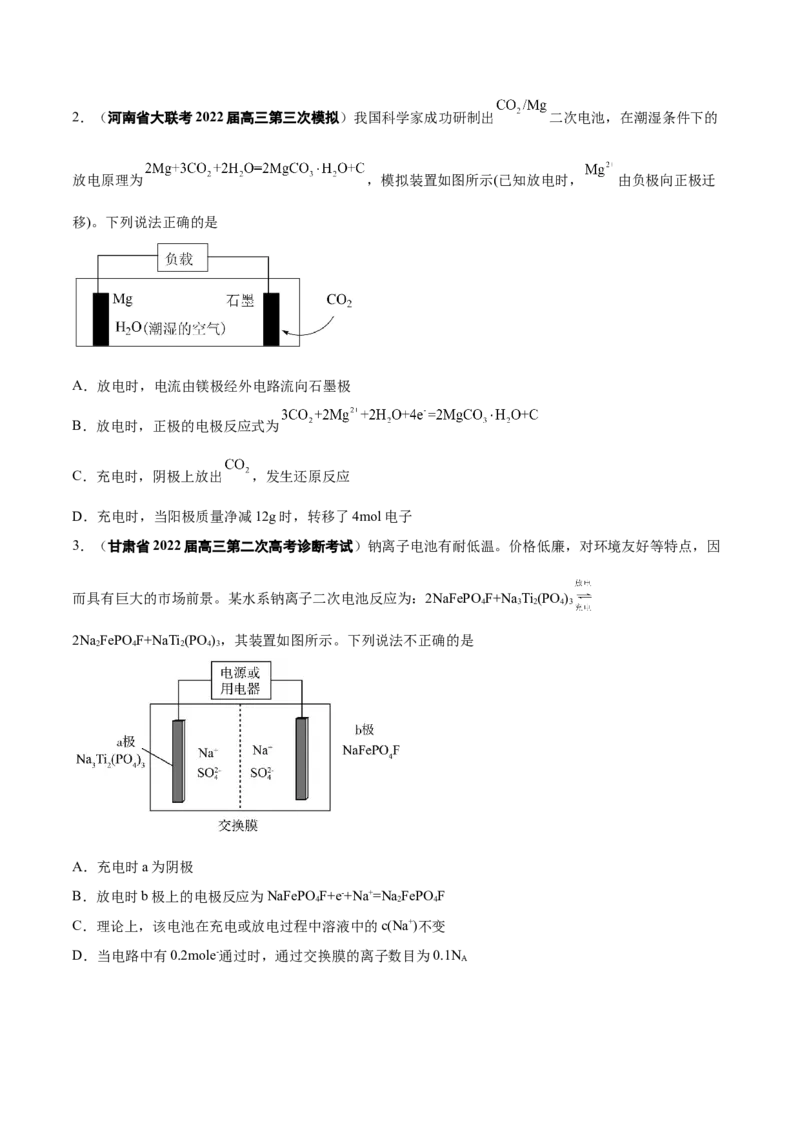
C. 在正极得电子 D.阳离子向负极移动2.(河南省大联考2022届高三第三次模拟)我国科学家成功研制出 二次电池,在潮湿条件下的
放电原理为 ,模拟装置如图所示(已知放电时, 由负极向正极迁
移)。下列说法正确的是
A.放电时,电流由镁极经外电路流向石墨极
B.放电时,正极的电极反应式为
C.充电时,阴极上放出 ,发生还原反应
D.充电时,当阳极质量净减12g时,转移了4mol电子
3.(甘肃省2022届高三第二次高考诊断考试)钠离子电池有耐低温。价格低廉,对环境友好等特点,因
而具有巨大的市场前景。某水系钠离子二次电池反应为:2NaFePO F+Na Ti (PO )
4 3 2 4 3
2NaFePO F+NaTi (PO ),其装置如图所示。下列说法不正确的是
2 4 2 4 3
A.充电时a为阴极
B.放电时b极上的电极反应为NaFePO F+e-+Na+=Na FePO F
4 2 4
C.理论上,该电池在充电或放电过程中溶液中的c(Na+)不变
D.当电路中有0.2mole-通过时,通过交换膜的离子数目为0.1N
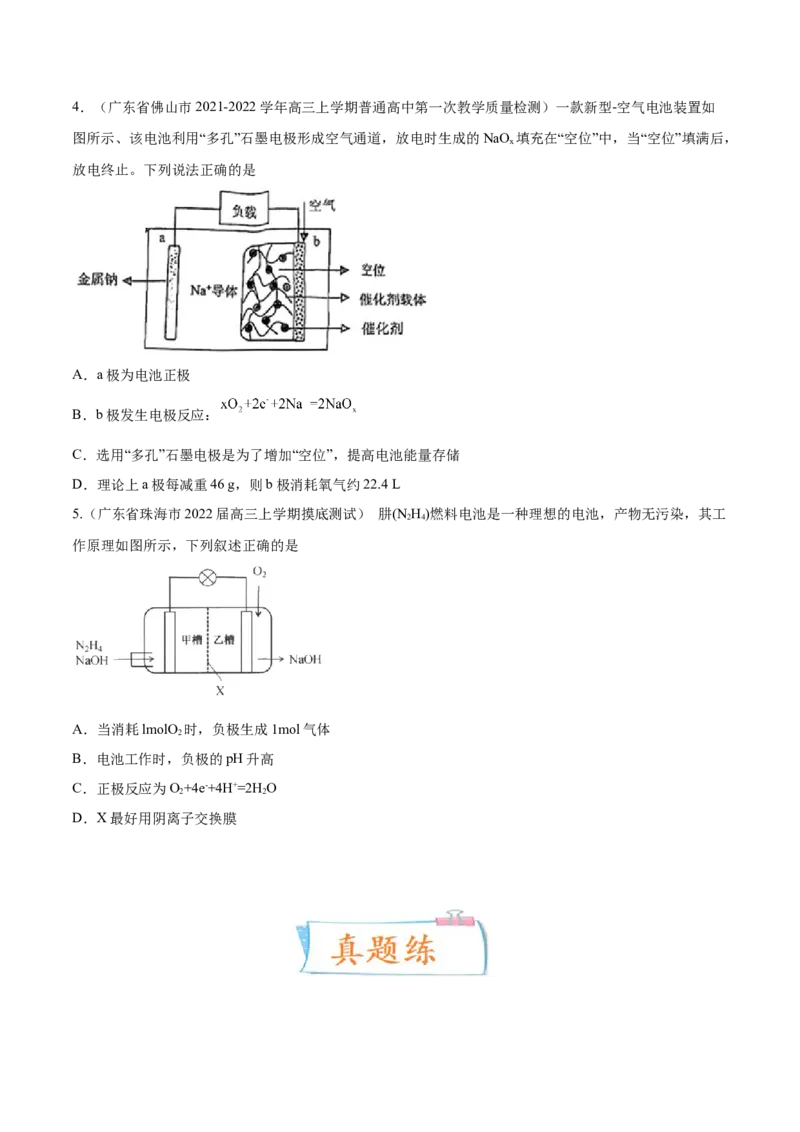
A4.(广东省佛山市2021-2022学年高三上学期普通高中第一次教学质量检测)一款新型-空气电池装置如
图所示、该电池利用“多孔”石墨电极形成空气通道,放电时生成的NaO 填充在“空位”中,当“空位”填满后,
x
放电终止。下列说法正确的是
A.a极为电池正极
B.b极发生电极反应:
C.选用“多孔”石墨电极是为了增加“空位”,提高电池能量存储
D.理论上a极每减重46 g,则b极消耗氧气约22.4 L
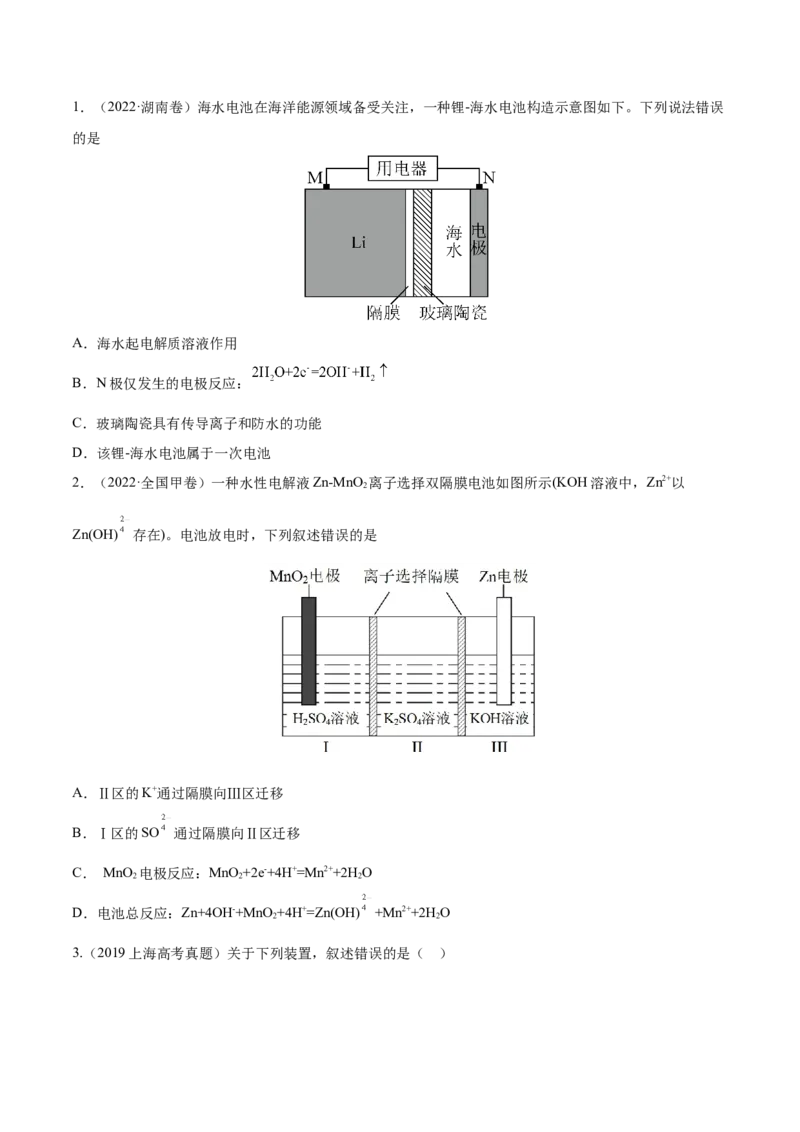
5.(广东省珠海市2022届高三上学期摸底测试) 肼(N H)燃料电池是一种理想的电池,产物无污染,其工
2 4
作原理如图所示,下列叙述正确的是
A.当消耗lmolO 时,负极生成1mol气体
2
B.电池工作时,负极的pH升高
C.正极反应为O+4e-+4H+=2H O
2 2
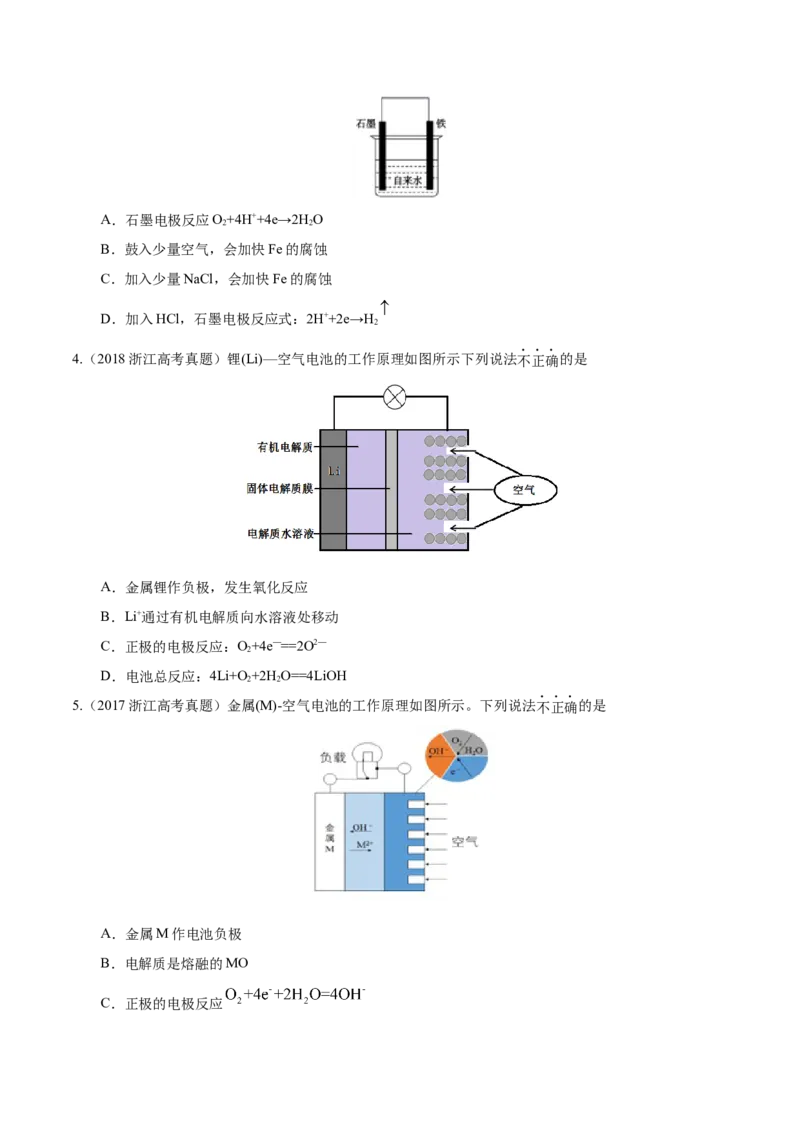
D.X最好用阴离子交换膜1.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误
的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
2.(2022·全国甲卷)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O
2 2
3.(2019上海高考真题)关于下列装置,叙述错误的是( )A.石墨电极反应O+4H++4e→2H O
2 2
B.鼓入少量空气,会加快Fe的腐蚀
C.加入少量NaCl,会加快Fe的腐蚀
D.加入HCl,石墨电极反应式:2H++2e→H
2
4.(2018浙江高考真题)锂(Li)—空气电池的工作原理如图所示下列说法不正确的是
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O+4e—==2O2—
2
D.电池总反应:4Li+O+2H O==4LiOH
2 2
5.(2017浙江高考真题)金属(M)-空气电池的工作原理如图所示。下列说法不正确的是
A.金属M作电池负极
B.电解质是熔融的MO
C.正极的电极反应D.电池反应
1. 【答案】A
【解析】根据原电池工作原理,阳离子向正极移动,阴离子向负极移动,盐桥的作用是构成闭合回路
和平衡两烧杯中的电荷,所以Cl-向负极移动,故A正确;铁作负极,负极反应式为Fe-2e-===Fe2+,正
极反应式为2H++2e-===H ↑,故B错误;左烧杯中pH基本不变,右烧杯中消耗H+,c(H+)减小,pH增
2
大,故C错误;电池总反应式为Fe+2H+===Fe2++H↑,铁作负极,发生氧化反应,故D错误。
2
2. 【答案】C
【解析】活泼金属锌作负极,铜作正极,铜电极上发生还原反应,故A错误;电池工作一段时间后,
甲池中的c(SO)不变,故B错误;铜电极上发生电极反应:Cu2++2e-===Cu,同时Zn2+通过阳离子交换膜
从甲池移向乙池,由电荷守恒可知,乙池中每析出1 mol Cu,则有1 mol Zn2+从甲池移向乙池,因为
M(Zn)>M(Cu),所以乙池溶液的总质量增加,故C正确;阳离子交换膜只允许阳离子和水分子通过,阴离
子不能通过阳离子交换膜,故D错误。
3. 【答案】B
【解析】由于氧化性:Cr O>Fe3+,即Cr O可以将Fe2+氧化为Fe3+,故在原电池中,Fe2+失电子被氧
2 2
化,则a极为负极;Cr O得电子被还原,则b极为正极。Fe2+失电子被氧化,即甲烧杯的溶液中发生氧化
2
反应,A错误;外电路中电流由正极流向负极,即由b极流向a极,B正确;原电池中,阴离子移向负极,
则SO移向甲烧杯,C错误;乙烧杯中Cr O得电子被还原,则电极反应式为Cr O+6e-+14H+===2Cr3++
2 2
7HO,D错误。
2
4. 【答案】D
【解析】c(Cl )越大,反应速率越快,则消耗银的速率也越快,A正确;银比铂活泼,铂作正极,Cl
2 2
在铂上得到电子发生还原反应生成Cl-,再与电解质中的Ag+结合,电极反应式为Cl+2e-+2Ag+
2
===2AgCl,B正确;根据电池总反应式可知,电解质中Ag+总数保持不变,C正确;原电池中,电子从负
极经过外电路的导线流向正极,电子不能通过电解质,故电子移动方向应是银→外电路导线→铂,D错误。
5. 【答案】D【解析】C H O 在微生物作用下转化为CO 和HO,C H O 被氧化,即石墨电极为负极,氧化银电
6 12 6 2 2 6 12 6
极为正极,Ag O发生得电子的还原反应,电极反应式为Ag O+2H++2e-===2Ag+HO,故A错误;石墨
2 2 2
电极为负极,C H O 在负极发生失电子的氧化反应:C H O+6HO-24e-===6CO ↑+24H+,故B错误;
6 12 6 6 12 6 2 2
根据负极的电极反应式可知,每转移4 mol电子,石墨电极产生22.4 L CO(标准状况),故C错误;30 g
2
C H O 的物质的量为= mol,根据B项负极的电极反应式可知,每30 g C H O 参与反应,有4 mol H+经
6 12 6 6 12 6
质子交换膜进入正极区,故D正确。
1. 【答案】D
【详解】
A.原电池放电时,负极发生失电子的氧化反应,A正确;
B.原电池放电过程是将化学能转化为电能,B正确;
C.新型化学电池Zn- 中,Zn作负极, 在正极得电子,C正确;
D.原电池放电时,电解质中的阳离子向正极移动,D错误;
故答案为:D。
2. 【答案】B
【分析】
该装置为电池装置,根据放电原理,Mg的化合价升高,Mg电极为负极,石墨为正极,据此分析;
【详解】
A.放电属于原电池,电流的方向是由正极经外电路流向负极,即电流由石墨经外电路流向镁极,故A错
误;
B.放电时,Mg2+由负极向正极迁移,根据在潮湿条件下的放电原理,正极反应式为3CO+2Mg2++2HO
2 2
+4e-=2MgCO·H O+C,故B正确;
3 2
C.充电时,电池的正极接电源的正极,电池的负极接电源的负极,充电时,石墨为阳极,阳极电极反应
式为2MgCO ·H O+C-4e-=3CO +2Mg2++2HO,故C错误;
3 2 2 2
D.根据C选项分析,充电时,阳极上质量减少的是2[MgCO ·H O]和C,即当阳极质量净减(2×102+
3 2
12)g=216g时,转移电子物质的量为4mol,故D错误;
答案为B。
3.【答案】D【分析】
由2NaFePO F+Na Ti (PO ) 2NaFePO F+NaTi (PO ) 可知Ti元素化合价由+3价变为+4价、Fe元素化合
4 3 2 4 3 2 4 2 4 3
价由+3价变为+2价,所以放电过程中NaFePO F得电子发生还原反应,电极反应为:NaFePO F+e-
4 4
+Na+=Na FePO F,NaTi (PO ) 失电子发生氧化反应,电极反应为:NaTi (PO )-2e-= Na Ti (PO )+2Na+,所
2 4 3 2 4 3 3 2 4 3 3 2 4 3
以左侧电极a为负极、右侧电极b为正极,充电时原来的负极为阴极、原来的正极作阳极,据此分析解题。
【详解】
A.由分析可知,充电时a与电源负极相连为阴极,A正确;
B.由分析可知,放电时b极为正极极,发生还原反应,其电极反应为NaFePO F+e-+Na+=Na FePO F,B正
4 2 4
确;
C.由分析可知,正、负极上有Na+的结合和释放,则交换膜为阳离子交换膜,Na+可以自由通过,电路上
通过1mol电子,则有1mol的Na+经过交换膜,则理论上,该电池在充电或放电过程中溶液中的c(Na+)不变,
C正确;
D.由C项分析可知,交换膜为阳离子交换膜,Na+可以自由通过,则当电路中有0.2mole-通过时,通过交
换膜的离子数目为0.2N ,D错误;
A
故答案为:D。
4.【答案】B
【详解】
A.在a电极上Na失去电子变为Na+,发生氧化反应,所以a电极为负极,A错误;
B.在b电极上O 得到电子,与Na+结合形成NaO ,所以b电极为正极,电极反应式为:
2 x
,B正确;
C.选用“多孔”石墨电极是为了增加“空位”,增大电势差,而与电池能量存储大小无关,C错误;
D.理论上a极每减重46 g,反应消耗2 mol Na,反应过程中转移2 mol电子,但b电极上未指明通入的O
2
所处的外界条件,因此不能确定消耗的O 的体积大小,D错误;
2
故合理选项是B。
5. 【答案】A
【详解】
A.负极NH 失电子生成N,当消耗lmolO 时转移4mol电子,根据电子守恒,负极生成1molN ,故A正
2 4 2 2 2
确;
B.电池工作时,负极反应式是 ,负极的pH降低,故B错误;C.根据图示,正极生成氢氧化钠,正极反应为O+4e-+2H O =4OH-,故C错误;
2 2
D.负极通入氢氧化钠,正极流出氢氧化钠,X最好用阳离子交换膜,故D错误;
选A。
1. 【答案】B
【解析】锂海水电池的总反应为2Li+2HO═2LiOH+H ↑, M极上Li失去电子发生氧化反应,则M电极为
2 2
负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2HO+2e-=2OH-+H ↑,同时氧气也可以在N极得电
2 2
子,电极反应为O+4e-+2H O=4OH-。
2 2
A.海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;
B.由上述分析可知,N为正极,电极反应为2HO+2e-=2OH-+H ↑,和反应O+4e-+2H O=4OH-,故B错误;
2 2 2 2
C.Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;
D.该电池不可充电,属于一次电池,故D正确;
答案选B。
2.【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于
2 2 2
两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此
可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 向Ⅱ区移动,Ⅲ区消耗OH-,生成
Zn(OH) ,Ⅱ区的SO 向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;
C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O,D正确;
2 2
故答案选A。3.【答案】A
【解析】该装置为原电池,铁为负极,石墨为正极。A.石墨电极为正极,溶液为中性,空气中的氧气得
到电子,电极反应为O+2H O +4e-=4OH-,错误;B.鼓入少量空气,增加氧气的浓度,加快反应速率,
2 2
正确;C.加入少量氯化钠,溶液导电能力增强,能加快铁的腐蚀,正确;D.加入氯化氢,发生析氢
腐蚀,石墨电极上氢离子得到电子生成氢气,电极反应式为:2H++2e→H ,正确;答案选A。
2
4.【答案】C
【解析】A.在锂空气电池中,金属锂失去电子,发生氧化反应,为负极,正确;B.Li在负极失去电子
变成了Li+,会通过有机电解质向水溶液处(正极)移动,正确;C.正极氧气得到了电子后与氢结合
形成氢氧根,电极方程式为O+4e-+2H O=4OH-,错误;D.负极的反应式为Li-e-= Li+,正极反应式为
2 2
O+4e-+2H O=4OH-,电池的总反应则为4Li+O+2H O==4LiOH,正确。综上所述,本题的正确答案为
2 2 2 2
C。
5.【答案】B
【解析】根据图示,金属M为负极,通入空气的电极为正极。A.金属M作电池负极,正确;B.根据图
示,电解质是熔融的M(OH) ,错误;C.正极发生还原反应,电极反应 ,正确;
2
D.负极M失去电子生成M2+,结合C的分析,电池反应 ,正确;答案选
B。