文档内容
考向 21 电解池 金属的腐蚀与防护
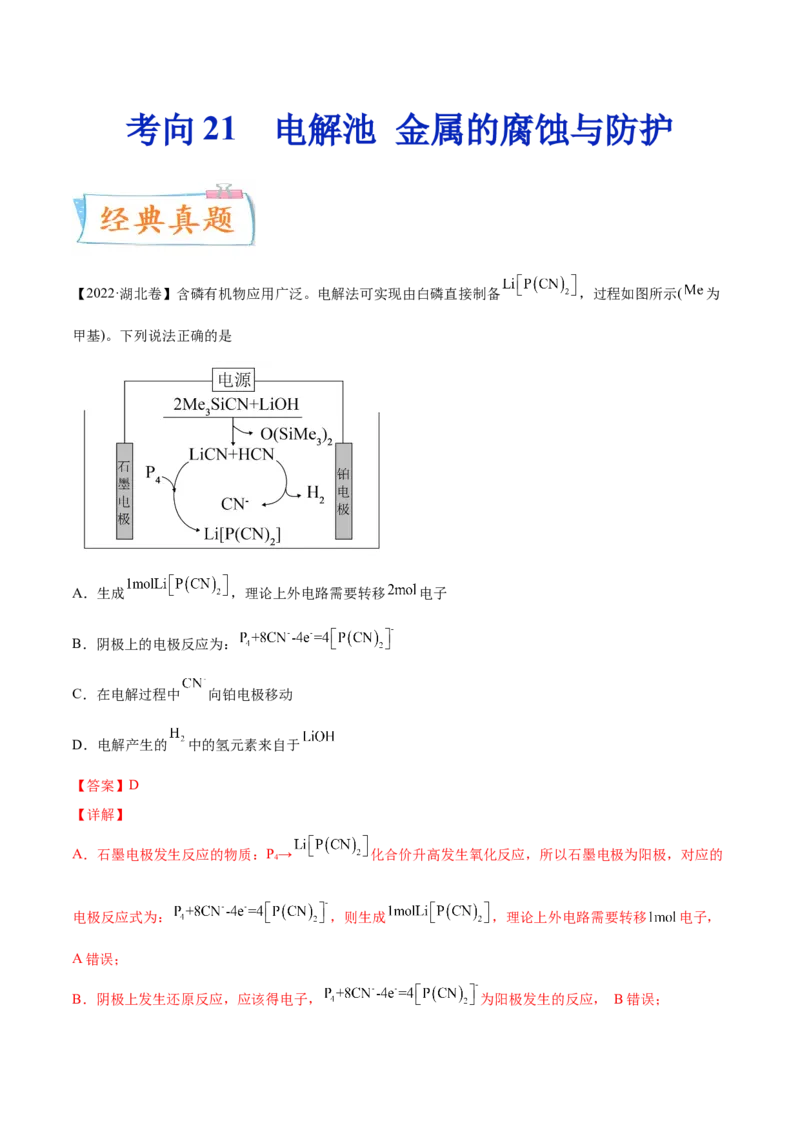
【2022·湖北卷】含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程如图所示( 为
甲基)。下列说法正确的是
A.生成 ,理论上外电路需要转移 电子
B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
D.电解产生的 中的氢元素来自于
【答案】D
【详解】
A.石墨电极发生反应的物质:P→ 化合价升高发生氧化反应,所以石墨电极为阳极,对应的
4
电极反应式为: ,则生成 ,理论上外电路需要转移 电子,
A错误;
B.阴极上发生还原反应,应该得电子, 为阳极发生的反应, B错误;C.石墨电极:P→ 发生氧化反应,为阳极,铂电极为阴极, 应该向阳极移动,即移向石
4
墨电极,C错误;
D.由所给图示可知HCN在阴极放电,产生 和 ,而HCN中的H来自 ,则电解产生的 中的
氢元素来自于 ,D正确;
故选D。
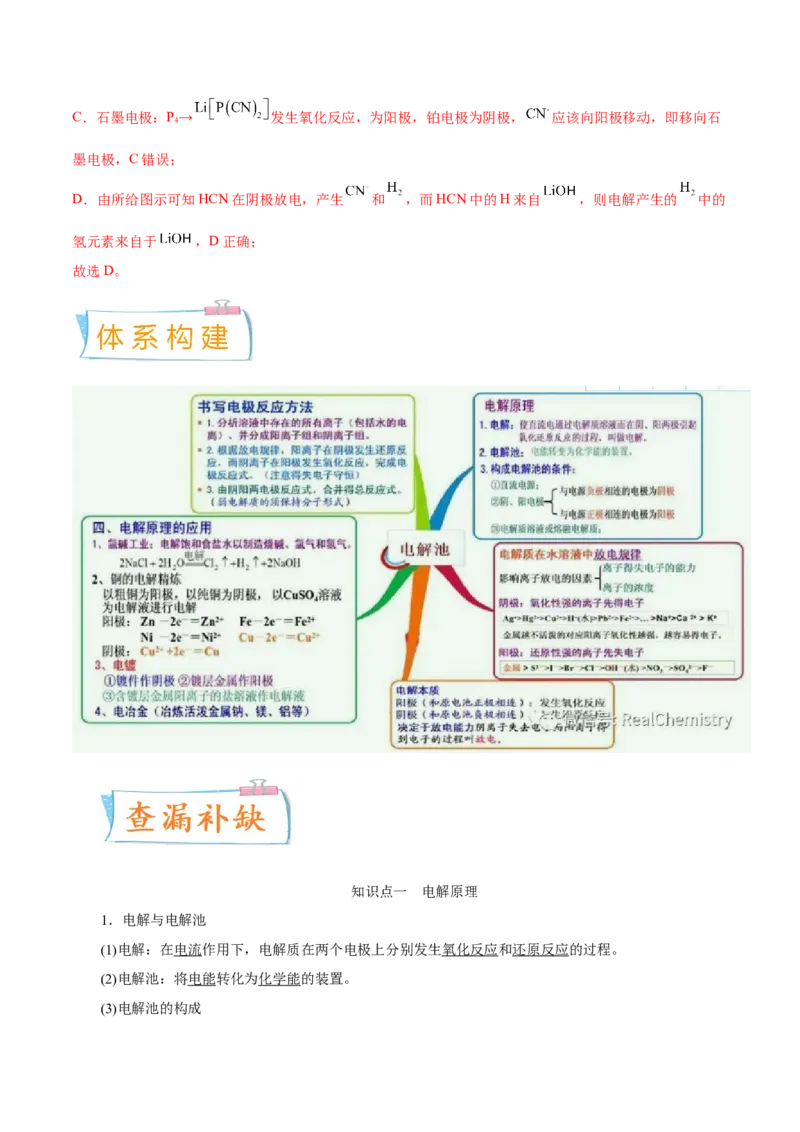
知识点一 电解原理
1.电解与电解池
(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
(2)电解池:将电能转化为化学能的装置。
(3)电解池的构成①有与直流电源相连的两个电极;
②电解质溶液(或熔融盐);
③形成闭合回路。
2.电解池的工作原理
(1)工作原理
[示例] 用惰性电极电解CuCl 溶液
2
阳极反应式: 2Cl - - 2e - == =Cl ↑;
2
阴极反应式: Cu 2 + + 2e - == =Cu ;
总反应式:CuCl ===== Cu + Cl ↑。
2 2
(2)电子和离子的移动方向(惰性电极)
3.阴、阳两极上的放电顺序
(1)阴极(与电极材料无关)
氧化性强的先放电,放电顺序:
――――――――――――――――――――――――――→
(2)阳极(与电极材料有关)
①活性电极作阳极(除Au、Pt以外的金属),则活性电极本身失去电子,发生氧化反应。如Cu-2e-
===Cu2+,Fe-2e-===Fe2+。
②惰性电极作阳极(Pt、Au、石墨碳棒)
离子的放电顺序为
――――――――――――――――――――――――――――――――――――――――――――
―→
4.分析电解的思维流程5.惰性电极电解电解质溶液的产物判断(图示)
[示例] 用惰性电极电解CuSO 溶液(放O 生酸型)
4 2
阳极反应式:2HO-4e-===O ↑+4H+(或4OH--4e-===2H O+O↑)
2 2 2 2
阴极反应式:2Cu2++4e-===2Cu
电池反应式:2CuSO +2HO=====2Cu+O↑+2HSO
4 2 2 2 4
[名师点拨] (1)阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放
电。
(2)电解水溶液时,K+~Al3+不可能在阴极放电,即不可能用电解水溶液的方法得到K、Ca、Na、
Mg、Al等金属。
(3)电解时,在外电路中有电子通过,而在溶液中是靠离子移动导电。因此,电子和离子的移动遵循
“电子不下水,离子不上线”。
(4)书写电解池的电极反应式时,可以用实际放电的离子表示,但书写电解池的总反应时,HO要写成
2
分子式。如用惰性电极电解食盐水时,阴极反应式为2H++2e-===H ↑(或2HO+2e-===H ↑+2OH-),总
2 2 2
反应式为2Cl-+2HO=====2OH-+H↑+Cl↑。
2 2 2
知识点二 电解原理的应用
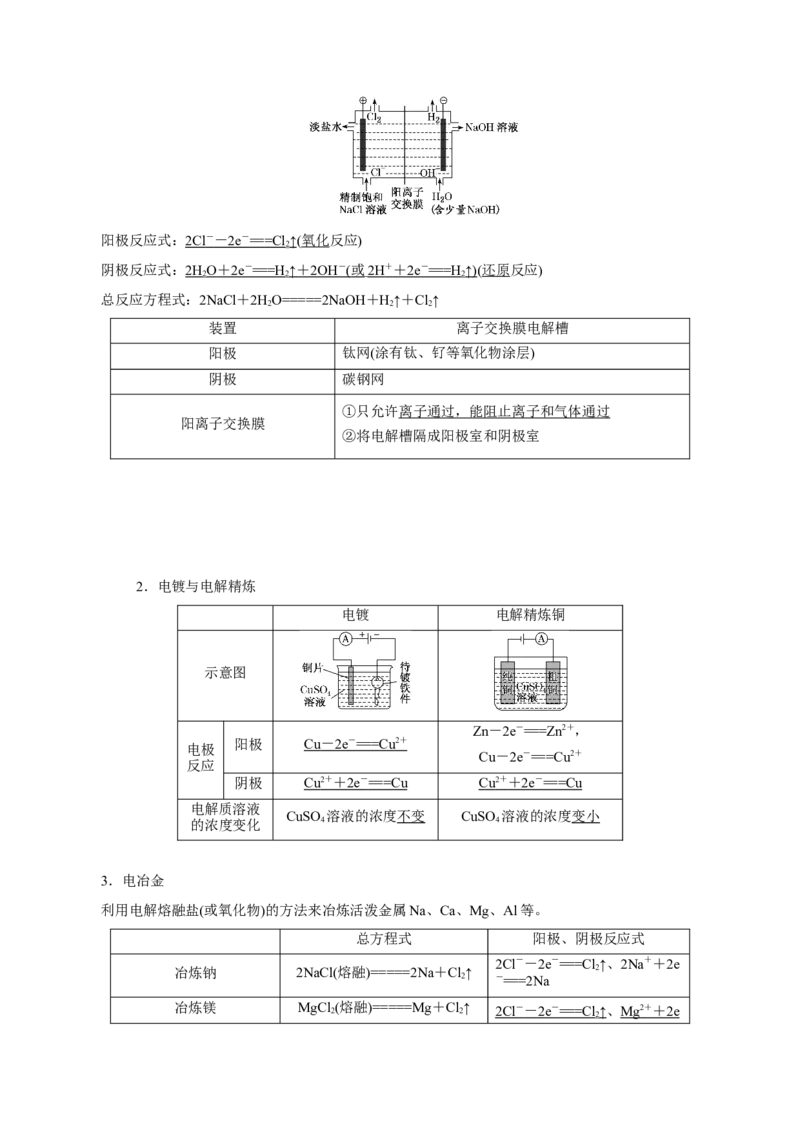
1.氯碱工业阳极反应式: 2Cl - - 2e - == =Cl ↑(氧化反应)
2
阴极反应式:2H O + 2e - == =H ↑ + 2OH - ( 或 2H + + 2e - == =H ↑)(还原反应)
2 2 2
总反应方程式:2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
装置 离子交换膜电解槽
阳极 钛网(涂有钛、钌等氧化物涂层)
阴极 碳钢网
①只允许离子通过,能阻止离子和气体通过
阳离子交换膜
②将电解槽隔成阳极室和阴极室
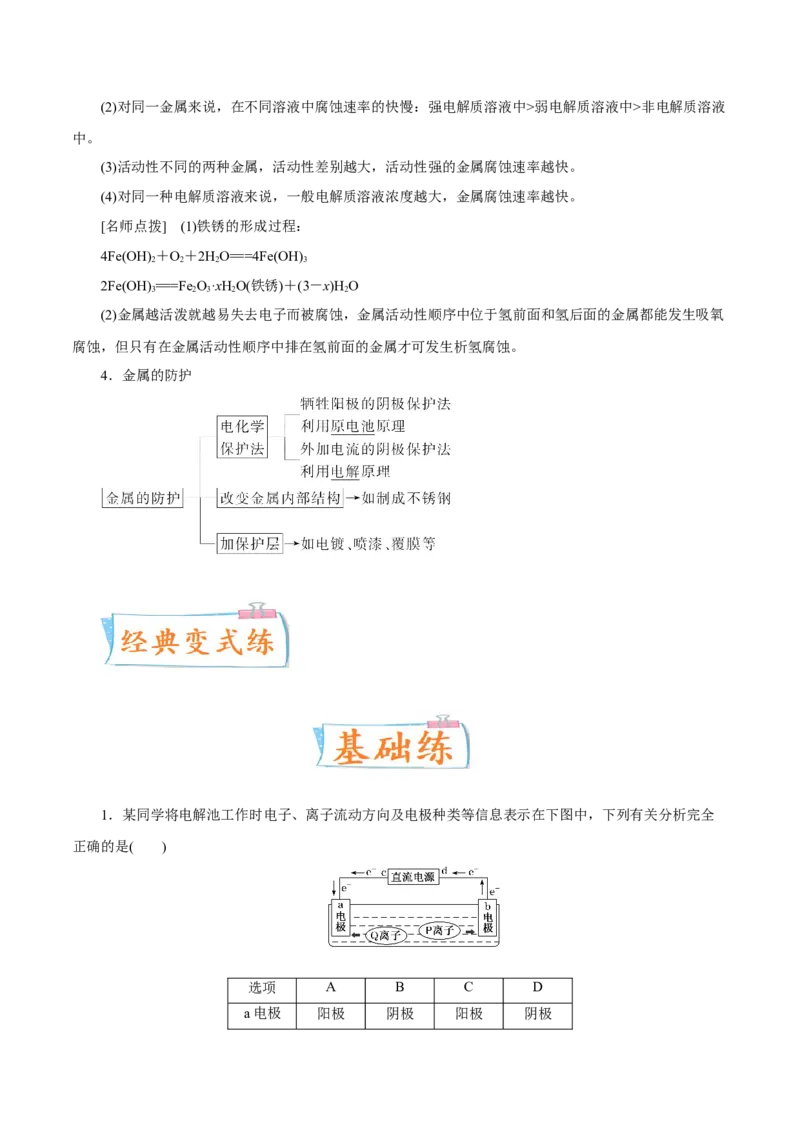
2.电镀与电解精炼
电镀 电解精炼铜
示意图
Zn-2e-===Zn2+,
阳极 Cu - 2e - == =Cu 2 +
电极
Cu-2e-===Cu2+
反应
阴极 Cu 2 + + 2e - == =Cu Cu 2 + + 2e - == =Cu
电解质溶液
CuSO 溶液的浓度不变 CuSO 溶液的浓度变小
的浓度变化 4 4
3.电冶金
利用电解熔融盐(或氧化物)的方法来冶炼活泼金属Na、Ca、Mg、Al等。
总方程式 阳极、阴极反应式
2Cl--2e-===Cl↑、2Na++2e
冶炼钠 2NaCl(熔融)=====2Na+Cl↑ 2
2 -===2Na
冶炼镁 MgCl 2 (熔融)=====Mg+Cl 2 ↑ 2Cl - - 2e - == =Cl 2 ↑、 Mg 2 + + 2e- == =M g
6O 2 - - 12e - == =3O ↑、 4Al 3 + +
冶炼铝 2Al O(熔融)=====4Al+3O↑ 2
2 3 2 12e - == =4Al
[名师点拨] (1)电解精炼铜时,阳极减少的质量与阴极增加的质量不相等,电解质溶液的浓度减小。
(2)粗铜中不活泼的杂质(金属活动性顺序中位于铜之后的银、金等),在阳极难以失去电子,当阳极上
的铜失去电子变成离子之后,它们以金属单质的形式沉积于电解槽的底部,成为阳极泥。
(3)由于AlCl 为共价化合物,熔融状态下不导电,所以电解冶炼铝时,电解的为熔点很高的氧化铝,
3
为降低熔化温度,加入了助熔剂冰晶石(Na AlF);而且电解过程中,阳极生成的氧气会与石墨电极反应,
3 6
所以石墨电极需不断补充。
知识点三 金属的腐蚀与防护
1.金属腐蚀的本质
金属原子失去电子变成金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀和电化学腐蚀
类型 化学腐蚀 电化学腐蚀
金属与接触到的物质直接发生 不纯的金属接触到电解质溶液
条件
反应 发生原电池反应
①实质都是金属原子失去电子
被氧化而损耗;
实质与联系 ②化学腐蚀与电化学腐蚀往往
同时发生,但电化学腐蚀更普
遍
(2)钢铁的析氢腐蚀与吸氧腐蚀
类型 析氢腐蚀 吸氧腐蚀
水膜性质 酸性 酸性很弱或者呈中性
负极反应 ① Fe - 2e - == =Fe 2 +
正极反应 ② 2H + + 2e - == =H ↑ ③ 2H O + O + 4 e - == =4OH -
2 2 2
总反应 ④ Fe + 2H + == =Fe 2 + + H ↑ ⑤ 2Fe + 2H O + O == =2Fe(OH)
2 2 2 2
3.金属腐蚀的快慢规律
(1)对同一电解质溶液来说,腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀
>有防腐措施的腐蚀。(2)对同一金属来说,在不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液
中。
(3)活动性不同的两种金属,活动性差别越大,活动性强的金属腐蚀速率越快。
(4)对同一种电解质溶液来说,一般电解质溶液浓度越大,金属腐蚀速率越快。
[名师点拨] (1)铁锈的形成过程:
4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
2Fe(OH) ===Fe O·xHO(铁锈)+(3-x)H O
3 2 3 2 2
(2)金属越活泼就越易失去电子而被腐蚀,金属活动性顺序中位于氢前面和氢后面的金属都能发生吸氧
腐蚀,但只有在金属活动性顺序中排在氢前面的金属才可发生析氢腐蚀。
4.金属的防护
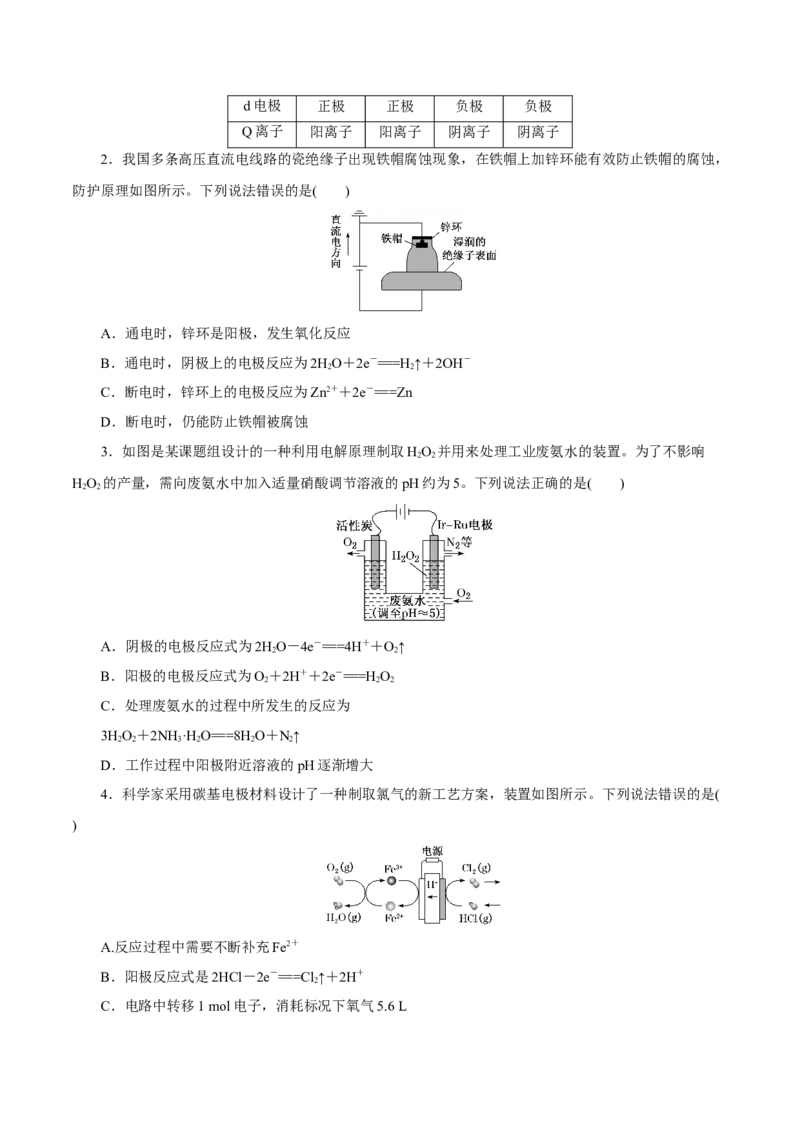
1.某同学将电解池工作时电子、离子流动方向及电极种类等信息表示在下图中,下列有关分析完全
正确的是( )
选项 A B C D
a电极 阳极 阴极 阳极 阴极d电极 正极 正极 负极 负极
Q离子 阳离子 阳离子 阴离子 阴离子
2.我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐蚀,
防护原理如图所示。下列说法错误的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为2HO+2e-===H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn2++2e-===Zn
D.断电时,仍能防止铁帽被腐蚀
3.如图是某课题组设计的一种利用电解原理制取HO 并用来处理工业废氨水的装置。为了不影响
2 2
HO 的产量,需向废氨水中加入适量硝酸调节溶液的pH约为5。下列说法正确的是( )
2 2
A.阴极的电极反应式为2HO-4e-===4H++O↑
2 2
B.阳极的电极反应式为O+2H++2e-===H O
2 2 2
C.处理废氨水的过程中所发生的反应为
3HO+2NH ·H O===8H O+N↑
2 2 3 2 2 2
D.工作过程中阳极附近溶液的pH逐渐增大
4.科学家采用碳基电极材料设计了一种制取氯气的新工艺方案,装置如图所示。下列说法错误的是(
)
A.反应过程中需要不断补充Fe2+
B.阳极反应式是2HCl-2e-===Cl↑+2H+
2
C.电路中转移1 mol电子,消耗标况下氧气5.6 LD.电解总反应可看作是4HCl(g)+O(g)=====2Cl(g)+2HO(g)
2 2 2
5.我国研制出非贵金属镍钼基高效电催化剂,实现电解富尿素废水低能耗制H(装置如图)。总反应为
2
CO(NH)+HO===3H ↑+N↑+CO↑。下列说法中错误的是( )
2 2 2 2 2 2
A.a为阳极,CO(NH) 发生氧化反应
2 2
B.b电极反应为2HO+2e-===H ↑+2OH-
2 2
C.每转移6 mol电子,a电极产生1 mol N
2
D.电解一段时间,a极区溶液pH升高
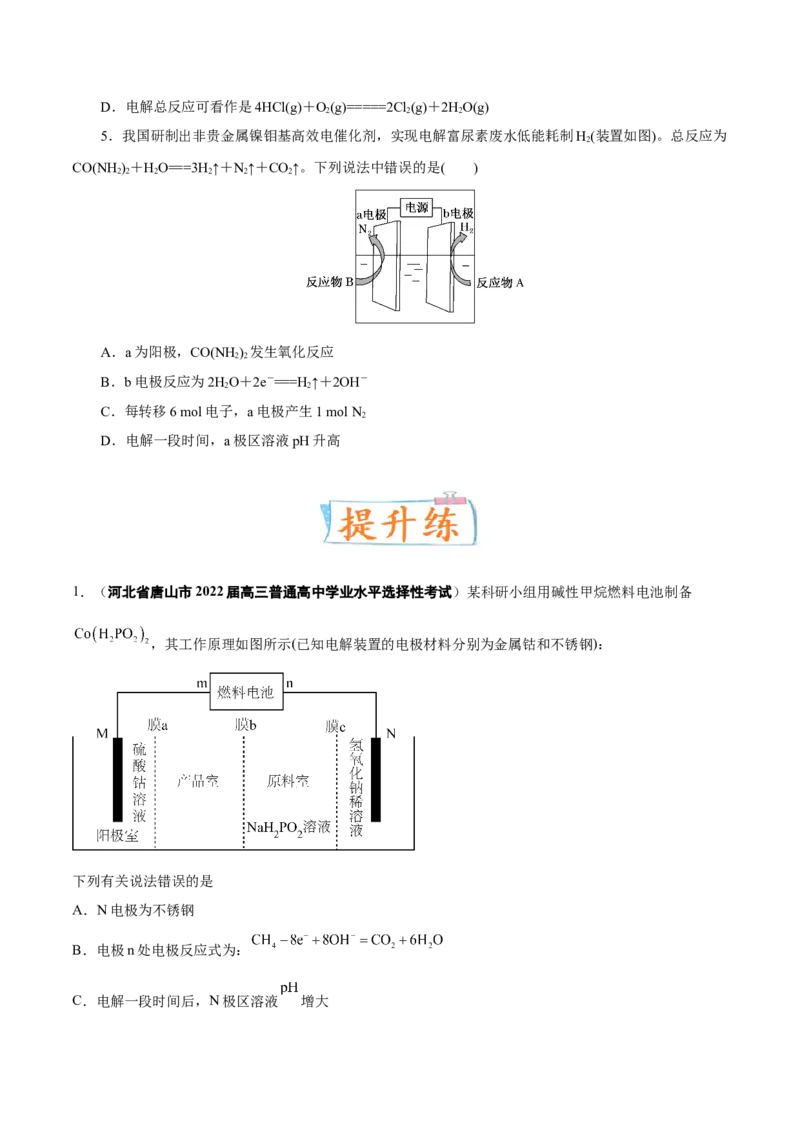
1.(河北省唐山市2022届高三普通高中学业水平选择性考试)某科研小组用碱性甲烷燃料电池制备
,其工作原理如图所示(已知电解装置的电极材料分别为金属钴和不锈钢):
下列有关说法错误的是
A.N电极为不锈钢
B.电极n处电极反应式为:
C.电解一段时间后,N极区溶液 增大D.膜a、膜c均为阳离子交换膜
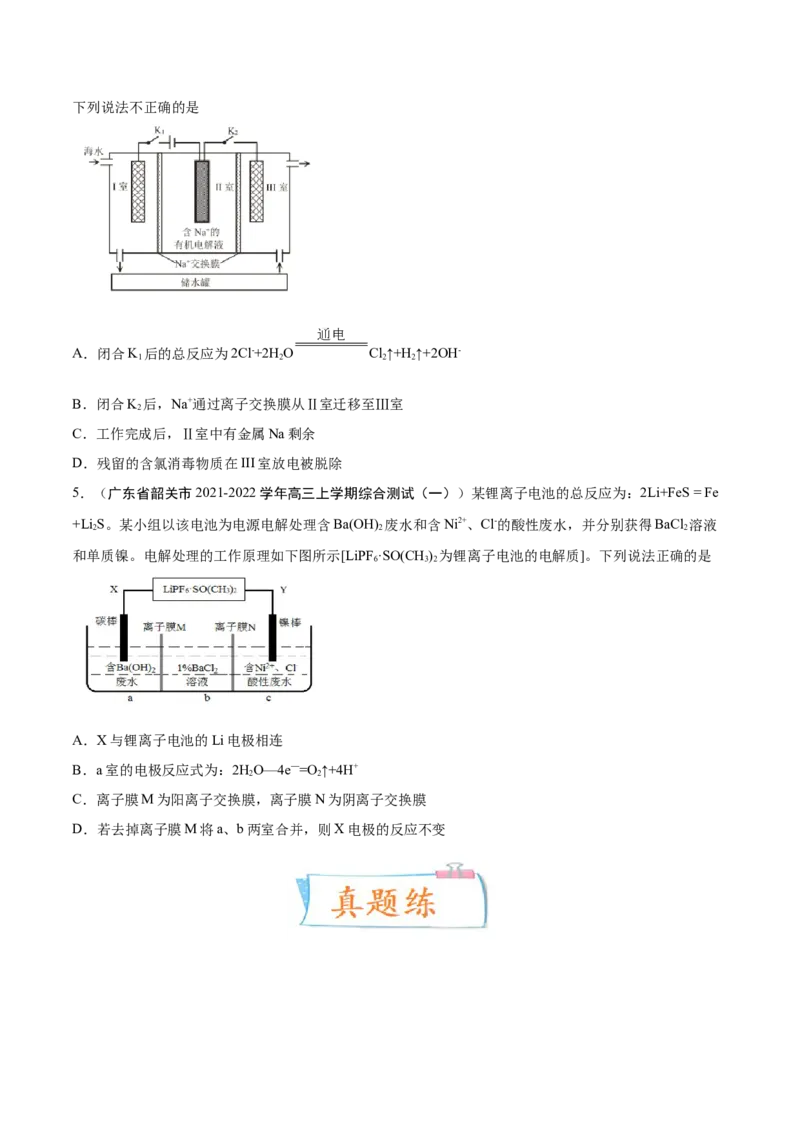
2.(江西省新余市2022届高三第二次模拟考试)科学家采用碳基电极材料设计了一种新的电解氯化氢回
收氯气的工艺方案,原理如图所示。下列说法错误的是
A.b极是电源的正极
B.阴极的电极反应式为:Fe3++e-=Fe2+
C.电路中每转移1mol e-理论上可以回收氯气11.2L(标准状况)
D.该工艺涉及的总反应为4HCl+O 2Cl+2H O
2 2 2
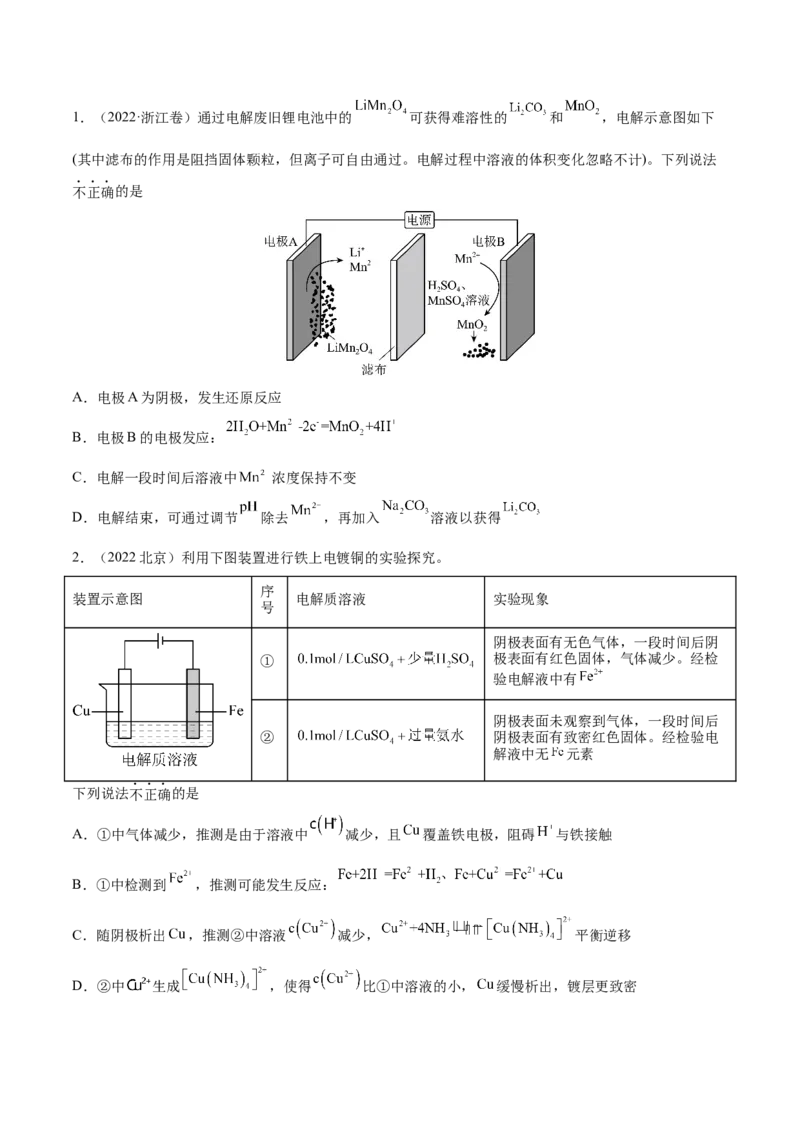
3.(辽宁省辽南协作体2022届高三第二次模拟考试)目前可采用“双极膜组"电渗析法淡化海水,同时获
得副产品A和B。其模拟工作原理如图所示。M和N为离子交换膜,在直流电作用下,双极阴阳膜(BP)复
合层间的HO解离成H+和OH-,作为H+和OH-的离子源。下列说法正确的是
2
A.X电极为阴极,电极反应式为2HO+2e-=2OH-+H ↑
2 2
B.M为阳离子交换膜,N为阴离子交换膜,BP膜作用是选择性通过Cl-和Na+
C.电路中每生成标况5.6 L气体a,理论上获得副产品A和B各1 mol
D.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)
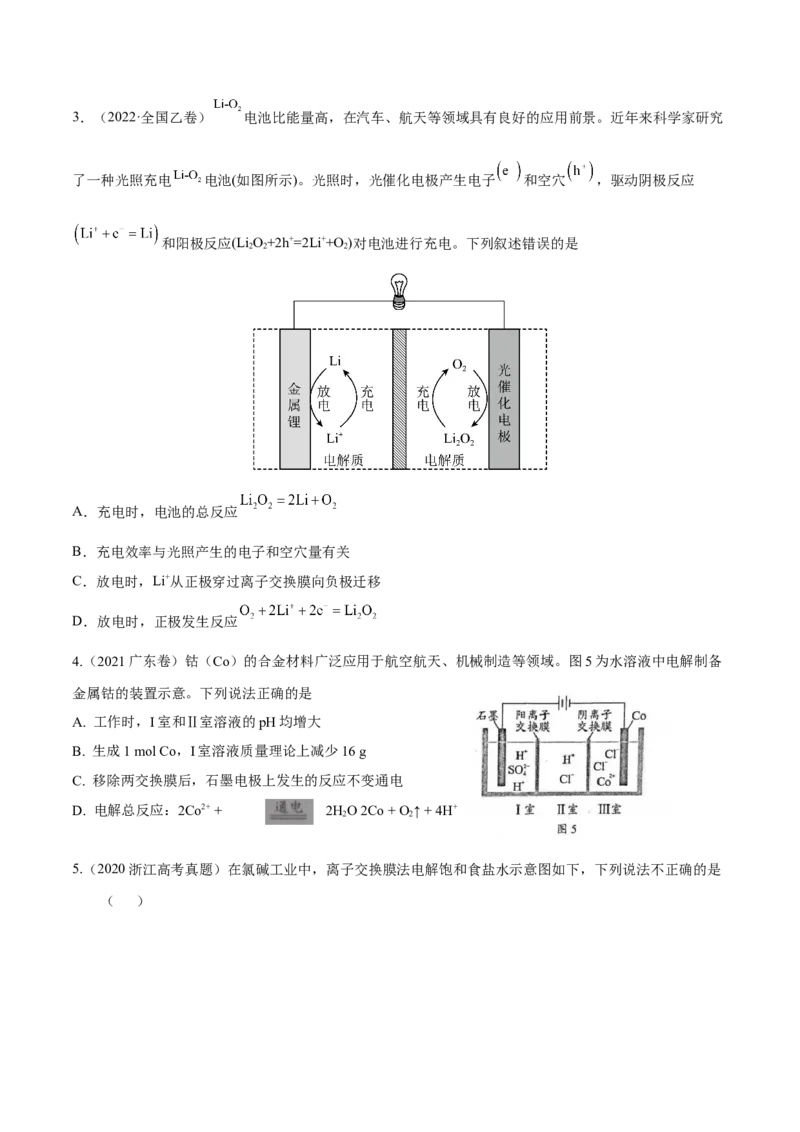
4.(广东省深圳市普通高中2022届高三下学期第一次调研)利用电化学原理可对海水(主要成分NaCl和
HO,还含有少量微生物)进行消毒,并能清除残留的含氯消毒物质(工作原理如图,其中电极均为惰性电
2
极)。
已知:工作时,先断开K,闭合K,一段时间后,断开K,闭合K
2 1 1 2下列说法不正确的是
A.闭合K 后的总反应为2Cl-+2H O Cl↑+H ↑+2OH-
1 2 2 2
B.闭合K 后,Na+通过离子交换膜从Ⅱ室迁移至Ⅲ室
2
C.工作完成后,Ⅱ室中有金属Na剩余
D.残留的含氯消毒物质在III室放电被脱除
5.(广东省韶关市2021-2022学年高三上学期综合测试(一))某锂离子电池的总反应为:2Li+FeS = Fe
+Li S。某小组以该电池为电源电解处理含Ba(OH) 废水和含Ni2+、Cl-的酸性废水,并分别获得BaCl 溶液
2 2 2
和单质镍。电解处理的工作原理如下图所示[LiPF ·SO(CH ) 为锂离子电池的电解质]。下列说法正确的是
6 3 2
A.X与锂离子电池的Li电极相连
B.a室的电极反应式为:2HO—4e—=O ↑+4H+
2 2
C.离子膜M为阳离子交换膜,离子膜N为阴离子交换膜
D.若去掉离子膜M将a、b两室合并,则X电极的反应不变1.(2022·浙江卷)通过电解废旧锂电池中的 可获得难溶性的 和 ,电解示意图如下
(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法
不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
2.(2022北京)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
阴极表面有无色气体,一段时间后阴
① 极表面有红色固体,气体减少。经检
验电解液中有
阴极表面未观察到气体,一段时间后
② 阴极表面有致密红色固体。经检验电
解液中无 元素
下列说法不正确的是
A.①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B.①中检测到 ,推测可能发生反应:
C.随阴极析出 ,推测②中溶液 减少, 平衡逆移
D.②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密3.(2022·全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究
了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴极反应
和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
4.(2021广东卷)钴(Co)的合金材料广泛应用于航空航天、机械制造等领域。图5为水溶液中电解制备
金属钴的装置示意。下列说法正确的是
A. 工作时,I室和Ⅱ室溶液的pH均增大
B. 生成1 mol Co,I室溶液质量理论上减少16 g
C. 移除两交换膜后,石墨电极上发生的反应不变通电
D. 电解总反应:2Co2+ + 2HO 2Co + O ↑ + 4H+
2 2
5.(2020浙江高考真题)在氯碱工业中,离子交换膜法电解饱和食盐水示意图如下,下列说法不正确的是
( )离子交换膜
A.电极A为阳极,发生氧化反应生成氯气
B.离子交换膜为阳离子交换膜
C.饱和NaCl从a处进,NaOH溶液从d处出
D.OH-迁移的数量等于导线上通过电子的数量
1.【答案】B
【解析】电子从电源的负极流出,故a是阴极,d是正极,溶液中的阳离子Q移向阴极a。
2.【答案】C
【解析】锌环与电源的正极相连,为阳极,发生氧化反应,A项正确;断电时,Zn比铁活泼,作负极,
电极反应为Zn-2e-===Zn2+,C项错误。
3.【答案】C
【解析】根据题给装置图可知,阳极的电极反应式为2HO-4e-===4H++O↑,阴极的电极反应式为
2 2
O+2H++2e-===H O,故A、B项错误。根据题图可知,HO 可将NH ·H O氧化为N,C项正确。根据
2 2 2 2 2 3 2 2
电极反应式可知,工作过程中阳极上生成氢离子,所以阳极附近溶液的pH逐渐减小,D项错误。
4.【答案】A
【解析】HCl在阳极失电子,发生氧化反应,生成Cl 和H+,Fe3+在阴极得电子,还原成Fe2+,Fe2
2
+、H+、O 反应生成Fe3+和HO,Fe2+、Fe3+在阴极循环,A错误;HCl在阳极失电子生成Cl 和H+,电
2 2 2
极反应式为2HCl-2e-===Cl↑+2H+,B正确;根据电子得失守恒有O~4e-,电路中转移1 mol电子,消
2 2
耗0.25 mol氧气,标准状况下体积为5.6 L,C正确;由图可知,反应物为HCl(g)和O(g),生成物为
2
HO(g)和Cl(g),故电解总反应可看作是4HCl(g)+O(g)=====2Cl(g)+2HO(g),D正确。
2 2 2 2 25.【答案】D
【解析】 电解池工作时,CO(NH) 失去电子,a为阳极,发生氧化反应,A正确;阴极水得电子生
2 2
成H,则阴极反应式为2HO+2e-===2OH-+H↑,B正确;阳极的电极反应式为CO(NH)-6e-+
2 2 2 2 2
HO===CO ↑+N↑+6H+,若电路中通过6 mol电子,阳极产生N 的物质的量为n(N )=6 mol×=1 mol,C
2 2 2 2 2
正确;a极反应式为CO(NH)-6e-+HO===CO ↑+N↑+6H+,则a极区溶液中氢离子浓度增大,溶液的
2 2 2 2 2
pH降低,D错误。
1.【答案】B
【分析】
根据图示,M电极所在为阳极室,M电极为阳极,N电极为阴极,则碱性甲烷燃料电池中m电极为正极,
n电极为负极;据此分析作答。
【详解】
A.该装置用于制备Co(HPO ),M电极为阳极,则M电极为金属Co,M电极的电极反应为Co-2e-
2 2 2
=Co2+,N电极为不锈钢,A正确;
B.n电极为碱性甲烷燃料电池的负极,n电极通入CH,电极反应式为CH-8e-+10OH-= +7H O,B错
4 4 2
误;
C.N电极为阴极,N电极电极反应为2HO+2e-=H ↑+2OH-,电解一段时间后,N极区碱性增强,溶液的
2 2
pH增大,C正确;
D.阳极室中的Co2+通过膜a进入产品室,膜a为阳离子交换膜,原料室中 通过膜b进入产品室,膜
b为阴离子交换膜,则原料室中Na+通过膜c进入阴极室,膜c为阳离子交换膜,D正确;
答案选B。
2.【答案】A
【分析】
HCl(g)→Cl(g),Cl元素失电子发生氧化反应,则与a电极相连的电极为电解池的阳极,从而得出a极为正
2
极。
【详解】
A.由分析可知,a极是电源的正极,则b极是电源的负极,A错误;
B.在阴极,Fe3+得电子生成Fe2+,则电极反应式为:Fe3++e-=Fe2+,B正确;C.阳极发生的电极反应为2HCl-2e-=Cl+2H+,则电路中每转移1mol e-,理论上可以回收氯气(标准状况)的
2
体积为0.5mol×22.4L/mol=11.2L,C正确;
D.该工艺涉及的反应为4HCl-4e-=2Cl+4H+、4Fe3++4e-=4Fe2+、4Fe2++O +4H+=4Fe3++2H O,总反应为
2 2 2
4HCl+O 2Cl+2H O,D正确;
2 2 2
故选A。
3.【答案】D
【分析】
由BP双极膜中H+、OH-移动方向可知:X电极为电解池的阳极,电极反应式为:2C1--2e-=Cl↑;Y电极为
2
阴极,电极反应式为:2H++2e-=H ↑,电解总反应为2HO+2Cl- Cl↑+H ↑+2OH-。精制盐水中Na+经过M
2 2 2 2
离子交换膜移向产品A室,与BP双极膜中转移过来的OH-结合生成NaOH,所以M膜为阳离子交换膜,
盐室中Cl-经过N离子交换膜移向产品B室,与BP双极膜中转移过来的H+结合生成HC1,所以N膜为阴
离子交换膜,据此分析解答。
【详解】
A.由以上分析知,X电极为电解池的阳极,电极反应式为:2C1--2e-=Cl↑;Y电极为阴极,电极反应式为:
2
2H++2e-=H ↑,A错误;
2
B.由题意可知:精制盐水中Na+经过M离子交换膜移向产品A室,与BP双极膜中转移过来的OH-结合生
成NaOH,所以M膜为阳离子交换膜,盐室中Cl-经过N离子交换膜移向产品B室,与BP双极膜中转移过
来的H+结合生成HC1,所以N膜为阴离子交换膜,BP膜作用是选择性通过H+和OH-,B错误;
C.阳极反应式为电极反应式为:2C1--2e-=Cl↑,电路中每生成标况5.6 L气体Cl,其物质的量是0.25
2 2
mol,转移电子0.5 mol,理论上获得副产品A (NaOH溶液)和B (HCl溶液)各0.5 mol,C错误;
D.“双极膜组”电渗析法从NaCl溶液获得酸( HCl )和碱( NaOH ),由此推知:也可从MX溶液制备相应
的酸( HX )和碱( MOH),D正确;
故合理选项是D。
4.【答案】A
【详解】A.闭合K 后为电解池,阳极海水中的Cl-被氧化为氯气,阴极为含Na+的有机电解液,所以应是Na+被还
1
原生成Na单质,总反应为2Cl-+2Na+ Cl↑+Na,A错误;
2
B.闭合K 后为原电池,Ⅱ室中Na单质被氧化为Na+,所以为负极,Ⅲ室为正极,原电池中阳离子流向正
2
极,所以Na+通过离子交换膜从Ⅱ室迁移至Ⅲ室,B正确;
C.闭合K 时在Ⅰ室生成的氯气与水反应生成HClO(含氯消毒物质),假设此过程生成1mol氯气,则生成
1
1molHClO,根据电子守恒可知生成2mol钠单质;HClO可以氧化微生物,进行消毒,未反应的HClO在闭
合K 后的Ⅲ室中被还原,由于部分HClO是被微生物还原,所以在Ⅲ室中被还原的HClO的物质的量小于
2
1mol,则消耗的钠单质小于2mol,所以有金属Na剩余,C正确;
D.闭合K 时在Ⅰ室生成的氯气与水反应生成含氯消毒物质,含氯消毒物质可以氧化微生物,进行消毒,
1
闭合K 后Ⅲ室为正极,剩余的氯消毒物质被还原,D正确;
2
综上所述答案为A。
5.【答案】C
【分析】
由方程式可知,锂为锂离子电池的负极,FeS为正极,由图可知,X电极与FeS电极相连,为电解池的阳
极,氢氧根离子在阳极失去电子发生氧化反应生成氧气和水,电极反应式为4OH——4e—=O ↑+2H O,a室
2 2
中溶液中钡离子通过阳离子交换膜进入b室;Y电极与锂电极相连,为电解池的阴极,镍离子在阴极得到
电子发生还原反应生成镍,电极反应式为Ni2++2 e—=Ni,c室中氯离子通过阳离子交换膜进入b室,则离子
膜M为阳离子交换膜,离子膜N为阴离子交换膜。
【详解】
A.由分析可知,X电极与FeS电极相连,为电解池的阳极,故A错误;
B.由分析可知,X电极与FeS电极相连,为电解池的阳极,氢氧根离子在阳极失去电子发生氧化反应生
成氧气和水,a室的电极反应式为4OH——4e—=O ↑+2H O,故B错误;
2 2
C.由分析可知,离子膜M为阳离子交换膜,离子膜N为阴离子交换膜,故C正确;
D.若去掉离子膜M将a、b两室合并,放电能力强于氢氧根离子的氯离子会在阳极失去电子发生氧化反应
生成氯气,电极反应式为2Cl——2e—=Cl↑,故D错误;
2
故选C。1.【答案】C
【解析】A.由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B
2
为阳极,电极A为阴极,得电子,发生还原反应,A正确;
B.由电解示意图可知,电极B上Mn2+失电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-
2 2
=MnO+4H+,B正确;
2
C.电极A为阴极, LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失
2 4 2 4 2
电子守恒,电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,
2 4 2 2
C错误;
D.电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离
2 4 2 2
子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;
答案选C。
2.【答案】C
【分析】
由实验现象可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚铁离子、
氢气和铜,一段时间后,铜离子在阴极失去电子发生还原反应生成铜;实验②中铜离子与过量氨水反应生
成四氨合铜离子,四氨合铜离子在阴极得到电子缓慢发生还原反应生成铜,在铁表面得到比实验①更致密
的镀层。
【详解】
A.由分析可知,实验①时,铁会先与溶液中的氢离子、铜离子反应,当溶液中氢离子浓度减小,反应和
放电生成的铜覆盖铁电极,阻碍氢离子与铁接触,导致产生的气体减少,故A正确;
B.由分析可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚铁离子、
氢气和铜,可能发生的反应为 ,故B正确;
C.由分析可知,四氨合铜离子在阴极得到电子缓慢发生还原反应生成铜,随阴极析出铜,四氨合铜离子
浓度减小, 平衡向正反应方向移动,故C错误;
D.由分析可知,实验②中铜离子与过量氨水反应生成四氨合铜离子,四氨合铜离子在阴极得到电子缓慢
发生还原反应生成铜,在铁表面得到比实验①更致密的镀层,故D正确;故选C。
3.【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(LiO+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化
2 2 2 2 2 2
电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。
A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳
极反应,充电时电池的总反应为LiO=2Li+O ,A正确;
2 2 2
B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率
与光照产生的电子和空穴量有关,B正确;
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
D.放电时总反应为2Li+O=Li O,正极反应为O+2Li++2e-=Li O,D正确;
2 2 2 2 2 2
答案选C。
4.【答案】D
【解析】
由图可知,石墨电极为阳极,得电子,阳极的反应式为2HO-4e- = O ↑+4H+, Co电极为阴极,得电子,电
2 2
极反应为Co2+ +2e- = Co, 则总的电解反应为 。
A项,由上述分析可知,在I室中产生H+,通过阳极交换膜进入II室,则I室和II室的pH减小,故A项
错误;
B、生成1 mol Co,同时转移2 mole-,需要消耗1 mol的水,则I室溶液质量理论上减少18g,B错误;
C、移除两交换膜后,溶液中的CI-更容易失去电子生成Cl,石墨电极发生的反应改变,C错误;
2
D、由上述分析可知,电解总反应为 。
故答案为D。
5.【答案】D
【解析】氯碱工业中的总反应为2Cl-+2H O 2OH-+H ↑+Cl↑;电解池中阳极失电子发生氧化反应,
2 2 2
氯碱工业中Cl 为氧化产物,所以电极A为阳极,电极B为阴极,据此作答。A.根据分析可知电极A
2
为阳极,发生氧化反应生成氯气,正确;B.阳极发生的方程式为:2Cl--2e-═Cl ↑,阴极:HO+2e-
2 2
═H ↑+2OH-;为了防止生成的氯气与氢氧化钠发生反应,氢氧化钠要从d口流出,所以要防止OH-流
2
向阳极即电极A,该离子交换膜为阳离子交换膜,正确;C.根据B选项的分析可知饱和NaCl从a处进,NaOH溶液从d处出,正确;D.因为有离子交换膜的存在,OH-不发生迁移,错误;故答案为
D。