文档内容
第四章 物质结构 元素周期律
单元测试卷
(考试时间:90分钟 试卷满分:100分)
第Ⅰ卷(选择题 44 分)
一、选择题:本题包括22小题,每小题只有以个选项符合题意,每小题2分,共44分。
1.Cl 与水发生反应Cl+H O=HCl+HClO,下列表示相关微粒的化学用语正确的是( )
2 2 2
A.C1-的结构示意图: B.HO的结构式:H-O-H
2
C.HCl的电子式: D.中子数为18的氯原子:18C1
【答案】B
【解析】A.Cl原子最外层有7个电子,获得一个电子变为Cl-,故Cl-的结构示意图: ,A错
误;B.水分子中O原子与2个H原子形成2个共用电子对,结构式为H—O—H,B正确 ,C.HCl中
H、Cl原子以共价键结合,C错误;D.中子数为18的氯原子,质量数为35 ,故可表示为 ,D错误;
故选B。
2.某微粒的结构示意图为 。下列关于该微粒的说法中,不正确的是( )
A.元素符号是 B.原子核外有3个电子层
C.元素非金属性比 强 D.元素属于短周期元素
【答案】C
【解析】A.由图可知,为14号元素硅元素,元素符号是,A正确;B.由图可知原子核外有3个电子
层,B正确;C.同周期从左到右,金属性减弱,非金属性变强;元素非金属性比P弱,C错误;D.硅元
素属于短周期元素,D正确;故选C。
3.下列有关 、 、 的说法正确的是( )
A.三者与 互为同素异形体 B.三者是碳元素的三种不同的核素C.三者物理性质相同 D. 和 所含的中子数相等
【答案】B
【解析】A.同素异形体是指同种元素形成的具有不同化学性质的单质, 是单质, 、 、 为核
素,A错误;B.一种原子就是一种核素,故题中三者接是碳元素的三种不同核素,B正确;C. 、
、 互为同位素,物理性质不同,化学性质基本相同,C错误;D. 含的中子数为14-6=8, 含的
中子数为14-7=7,D错误;故选B。
4.下列关于元素周期表的说法正确的是( )
A.第IA族的所有元素都是碱金属元素
B.同周期主族元素中,第ⅦA族元素原子半径最小
C.原子的最外层电子数为2的元素,一定是第ⅡA族元素
D.元素周期表共有7个周期,18个族
【答案】B
【解析】A.第IA族除H之外的所有元素即Li、Na、K、Rb、Cs、Fr都是碱金属元素,A错误;B.同周
期主族元素中从左往右原子半径依次减小,故第ⅦA族元素原子半径最小,B正确;C.He的最外层上2
个电子,其位于0族,故原子的最外层电子数为2的元素,不一定是第ⅡA族元素,C错误;D.元素周
期表共有7个横行,每个横行为一个周期,共有7个周期,18个纵行,除第8、9、10三纵行合为Ⅷ族,其
余各纵行自成一族,共有16个族,D错误;故选B。
5.关于元素周期律的应用,下列推测合理的是( )
A.根据硝酸属于强酸,预测磷酸也属于强酸
B.根据氯的非金属性强于硫,预测盐酸的酸性强于硫酸
C.根据钾的金属性强于钠,预测钾与水的反应比钠与水的反应更容易
D.根据溴水能和碘化钾溶液发生反应,预测溴水也能和氯化钾溶液反应
【答案】C
【解析】A.同主族元素从上至下非金属性逐渐减弱,元素的非金属性越强,其最高价氧化物的水化物的
酸性越强,氮的非金属性强于磷,则硝酸的酸性强于磷酸,硝酸属于强酸,磷酸属于中强酸,故A错误;
B.元素的非金属性越强,其最高价氧化物的水化物的酸性越强,根据氯的非金属性强于硫,预测高氯酸
的酸性强于硫酸,故B错误;C.元素的金属性越强,越容易和水(或酸)反应,根据钾的金属性强于钠,预测钾与水的反应比钠与水的反应更容易,故C正确;D.同主族元素从上至下非金属性逐渐减弱,
氯的非金属性强于溴,所以溴水不能和氯化钾溶液反应,故D错误,故选C。
6.元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是( )
A.元素原子的最外层电子数等于元素的最高化合价
B.元素核外电子排布时,先排满K层,再排L层,先排满M层,再排N层
C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
【答案】C
【解析】A.第二周期的元素 O、F无正价,故A错误;B.多电子原子中,在离核较近的区域内运动的
电子能量较低,元素核外电子排布时,先排满 K层,再排L层,L层排满后、再排M层,但N层有些电
子能量较低,所以M层排了8个电子、没有排满时会先有2个电子排N层,故B错误;C. P、S、Cl同
周期,且原子序数依次增大,非金属性递增,得电子能力和最高价氧化物对应水化物的酸性均依次增
强,故C正确;D.位于金属和非金属分界线附近的元素,表现一定的金属性与非金属性,而过渡元素包
含副族元素与第Ⅷ族元素,故D错误;答案选C。
7.如图为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素原子的核电荷数为X元素的2
倍。下列说法正确的是( )
X
Y Z W
T
A.简单氢化物的沸点:X<W
B.Y、Z、W元素的氧化物对应的水化物的酸性依次增强
C.简单离子半径:Z<W
D.根据元素周期律,推测T元素的单质具有半导体特性,TX 具有氧化性和还原性
2 3
【答案】D
【解析】X、Y、Z、W为短周期元素,W元素原子的核电荷数为X元素的2倍,W为第三周期元素,
W、X同主族,可知X为O、W为S元素;结合图中位置可知Y为Si、Z为P、T为As元素,以此来解
答。由分析可知,X为O,W为S,由于HO分子中存在分子间氢键,导致HO的沸点远远高于HS,即
2 2 2
简单氢化物的沸点:X>W,A错误;根据同一周期从左往右元素的非金属性依次增强,则其元素的最高
价氧化物对应水化物的酸性强弱顺序为 HSiO <HPO <HSO ,则Y、Z、W元素的最高价氧化物对应水
2 3 3 4 2 4
化物的酸性依次增强,若不是最高价氧化物对应水化物,则不好比较酸性强弱,B错误;Z为P,W为S,
则简单离子半径:Z>W,C错误;T为As,位于金属元素与非金属元素的交界处,故根据元素周期律,
推测T元素的单质具有半导体特性,TX 中As的化合价为中间价态,则具有氧化性和还原性,D正确。
2 3
8.应用元素周期律分析下列推断,其中正确的组合是( )①碱金属元素的最高价氧化物对应水化物的碱性随原子序数的增大而增强
②85号砹(At)是第ⅥA族元素,其氢化物的稳定性弱于HCl
③硒(Se)与氧同主族,它的最高价氧化物对应水化物酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤81号铊(Tl)与铝同主族,其单质不能与氢氧化钠溶液反应
⑥第三周期非金属元素的氧化物对应水化物的酸性随原子序数的增大而增加
A.①③⑥ B.①③⑤ C.②③⑤ D.②④⑥
【答案】B
【解析】①同主族元素从上到下金属性逐渐增强,则碱金属元素的最高价氧化物对应的水化物的碱性随原
子序数的增大而增强,①正确;②同主族元素从上到下非金属性逐渐减弱,氢化物的稳定性逐渐减弱,砹
(At)是第ⅦA族元素而不是第ⅥA族,其氢化物的稳定性弱于HCl,②错误;③同主族元素从上到下非金
属性逐渐减弱,最高价含氧酸的酸性逐渐减弱,硒(Se)与氧同主族,它的最高价氧化物对应水化物的酸性
比硫酸弱,③正确;④第二周期非金属元素的气态氢化物溶于水后,水溶液不一定均为酸性,如NH 溶于
3
水后,水溶液呈碱性,④错误;⑤同主族元素从上到下金属性逐渐增强,铊(Tl)与铝同主族,金属性强于
铝,其单质能与盐酸反应,不能与氢氧化钠溶液反应,⑤正确;⑥同周期元素自左向右非金属性逐渐增
强,则第三周期非金属元素的最高价氧化物对应水化物的酸性随原子序数的增大而增强,⑥错误,故B正
确;答案选B。
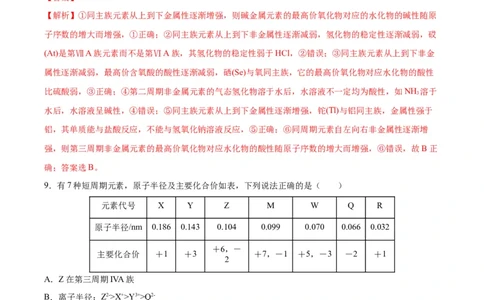
9.有7种短周期元素,原子半径及主要化合价如表,下列说法正确的是( )
元素代号 X Y Z M W Q R
原子半径/nm 0.186 0.143 0.104 0.099 0.070 0.066 0.032
+6,-
主要化合价 +1 +3 +7,-1 +5,-3 -2 +1
2
A.Z在第三周期IVA族
B.离子半径:Z2->X+>Y3+>Q2-
C.Z、W、Q、R四种元素形成的化合物一定不含离子键
D.M元素的非金属性比Z强
【答案】D
【分析】结合原子半径及主要化合价,X为Na,Y为Al,Z为S,M为Cl,W为N,Q为O,R为H。
A.Z为S,在第三周期第ⅥA族,A错误;B.X为Na,Y为Al,Z为S,Q为O,根据电子层数越多半
径越大,具有相同电子层数的阴离子半径大于阳离子半径,阳离子所带电荷越多,半径越小,故离子半
径:Z2->Q2->X+>Y3+,B错误;C.Z为S,W为N,Q为O,R为H,Z、W、Q、R四种元素形成的化合物可能含离子键,如硫酸铵,C错误;D.Z为S,M为Cl,同周期元素,非金属性从左往右逐渐增强,则
M元素的非金属性比Z强,D正确;故选D。
10.下列说法正确的是( )
A.NaOH和MgCl 中的化学键类型相同,都属于离子化合物
2
B.N、H、O三种元素组成的化合物一定只含共价键
C.由于固态水中水分子以氢键结合成排列规整的晶体,所以冰的密度比水小
D.CCl 和PCl 分子中,各原子均满足最外层8电子的稳定结构
4 5
【答案】C
【解析】A.NaOH中含有离子键和共价键,MgCl 中只含有离子键,化学键类型不同,A选项错误;B.
2
NH NO 中含有共价键和离子键,B选项错误;C.固态水中水分子间以氢键结合成规整排列的晶体,空隙
4 3
较大,所以密度小于液态水,C选项正确;D.PCl 中含有5个P-Cl键,P原子最外层有10个电子,D选
5
项错误;故选C。
11.室温下,大小相同的A、B两集气瓶中,分别装有0.01 mol氨气和0.01 mol氯化氢,抽去如图所示装
置中的玻璃片,使两种气体充分反应。下列说法正确的是( )
A.0.01 mol氨气中含0.03N 个共价键,0.01 mol氯化氢含0.03N 个离子键
A A
B.气体反应物的总体积为0.448 L
C.当玻璃片抽走后,可观察到集气瓶内出现白烟
D.该反应发生过程中,同时有共价键和离子键的断裂和生成
【答案】C
【解析】氨气为共价化合物,0.01 mol氨气中含0.03N 个共价键,但氯化氢为共价化合物,分子中不含离
A
子键,故A错误;题干并未告知是否为标准状况,无法使用V =22.4 L·mol-1计算气体体积,故B错误;
m
当玻璃片抽走后,NH 与HCl混合发生反应:NH +HCl===NHCl,可观察到集气瓶内出现白烟,故C正
3 3 4
确;该反应过程中没有离子键的断裂,故D错误。
12. X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充满,Y的s能级电子数量是
p能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法不正确的是( )
A. 电负性:
B. 最高正价:
C. Q与M的化合物中可能含有非极性共价键
D. 最高价氧化物对应水化物的酸性:【答案】B
【解析】Y的s能级电子数量是p能级的两倍,Y为C,X的2s轨道全充满,原子序数XX,A正确;B.N最高正价为+5
价,O无最高正价,最高正价N大于O,B错误;C.Na和O形成的过氧化钠中含有非极性共价键,C正
确;D.非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性 N大于C,硝酸酸性强于碳酸,
D正确;故选B。
13.现有4种短周期主族元素X、Y、Z和Q,原子序数依次增大。相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 在地壳中含量居第三位
Z 单质为淡黄色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是( )
A.常温时,X单质能与水发生剧烈反应
B.工业上常用电解熔融的YQ 来制备Y
3
C.因为Q元素的氢化物酸性比Z强,所以非金属性:Q>Z
D.第5周期且与Q同主族元素的单质在常温常压下呈固态
【答案】D
【分析】短周期主族元素X、Y、Z和Q,原子序数依次增大。其中X最外层电子数是核外电子总数的一
半,则X核外电子排布是2、2,则X是Be;Y在地壳中含量居第三位,则Y是Al;Z单质为淡黄色固
体,常存在于火山喷口附近,则Z是S元素;Q是同周期元素中原子半径最小的元素,则Q是Cl元素,然
后根据问题逐一分析解答。根据上述分析可知X是Be,Y是Al,Z是S,Q是Cl元素。A.X是Be,其金
属性比较弱,在常温时,X单质不能与水发生剧烈反应,A错误;B.AlCl 是共价化合物,在熔融状态下
3
不能导电,工业上常用电解熔融的Al O 来制备Al,B错误;C.元素最高价氧化物对应的水化物的酸性:
2 3
HClO>HSO ,所以元素的非金属性:Cl>S,而不能根据氢化物酸性强弱判断元素非金属性的强弱,C
4 2 4
错误;D.第5周期且与Q同主族元素是碘元素,其单质I2在常温常压下呈固态,D正确;故选D。
14.W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与
其K层电子数相等,WX 是形成酸雨的物质之一。下列说法正确的是( )
2A. 原子半径: B. 简单氢化物的沸点:
C. 与 可形成离子化合物 D. 的最高价含氧酸是弱酸
【答案】C
【解析】W、X、Y、Z为短周期主族元素,原子序数依次增大,WX 是形成酸雨的物质之一,根据原子序
2
数的规律,则W为N,X为O,Y的最外层电子数与其K层电子数相等,又因为Y的原子序数大于氧的,
则Y电子层为3层,最外层电子数为2,所以Y为Mg,四种元素最外层电子数之和为19,则Z的最外层
为
电子数为6,Z为S,据此解答。A.X O,W为N,同周期从左往右,原子半径依次减小,所以半径大
小为W>X,A错误;B.X为O,Z为S,X的简单氢化物为HO,含有分子间氢键,Z的简单氢化物为
2
HS,没有氢键,所以简单氢化物的沸点为X>Z,B错误;C.Y为Mg,X为O,他们可形成MgO,为离
2
子化合物,C正确;D.Z为S,硫的最高价含氧酸为硫酸,是强酸,D错误;故选C。
15.X、Y、Z、M、Q、R是前20号元素,其原子半径与主要化合价的关系如图所示。下列说法正确的是
( )
A.简单气态氢化物稳定性:
B.简单离子半径:
C.X、Y、Z三种元素组成的化合物可能是酸、碱或盐
D.Q元素的碳酸盐,进行焰色反应,火焰为黄色
【答案】C
【解析】X、Y、Z、M、Q、R是前20号元素,由原子半径与主要化合价的关系图可知,X为+1价,且原
子半径最小,X为H元素;Y只有-2价,Y为O元素;Z有+5、-3价,且原子半径比Y大,Z为N元素;
M有+7、-1价,M为Cl元素;Q为+1价,且原子半径大于M,则Q为Na;R为+2价,且原子半径最
大,R为Ca,以此来解答。由上述分析可知,X为H元素、Y为O元素、Z为N元素、M为Cl元素、Q为
Na元素、R为Ca元素,A.同周期主族元素从左向右非金属性增强,非金属性O>N,则简单气态氢化物稳定性:Y>Z,故A错误;B.一般来说,离子的电子层数越多、离子半径越大,且具有相同电子排布的
离子中原子序数大的离子半径小,则简单离子半径:M(Cl-)>Q(Ca2+)>R(Na+),故B错误;C.X为H元
素、Y为O元素、Z为N元素,H、O、N三种元素组成的化合物为硝酸、一水合氨、硝酸铵,分别为酸、
碱、盐,故C正确;D.Q为Na元素,碳酸钠溶液中含有钠元素,其焰色试验火焰呈黄色,颜色反应为物
理变化,故D错误;故选C。
16.几种短周期元素的原子半径及某些化合价见表:
元素代号 A B D E G H I J
+4、-
化合价 -1 -2 -1 +5、-3 +3 +2 +1
4
原子半径/nm 0.071 0.074 0.077 0.099 0.110 0.143 0.160 0.186
分析判断下列说法不正确的是( )
A.A、H、J的简单离子半径由大到小的顺序是A>J>H
B.D、H、J的氧化物分别为酸性氧化物、两性氧化物、碱性氧化物
C.D元素的单质存在多种同素异形体
D.I在DB 中燃烧会生成一种非金属单质
2
【答案】B
【解析】由表可知:A、E有-1价,B有-2价,且A的原子半径与B相差不大,则A、E处于第ⅦA
族,B处于第ⅥA族,A原子半径小于E,可推知A为F,E为Cl,B为O;D有-4、+4价,处于第ⅣA
族,原子半径与O原子相差不大,可推知D为C元素;G有-3、+5价,处于第ⅤA族,原子半径大于C
原子,应处于第三周期,则G为P元素;H、I、J的化合价分别为+3、+2、+1,分别处于第ⅢA族、第
ⅡA族、第ⅠA族,原子半径依次增大,且都大于P原子半径,应处于第三周期,可推知H为Al、I为
Mg、J为Na。A、H、J分别为F、Al、Na,Na+、Al3+、F-的核外电子层数相等,核电荷数越大离子半径
越小,则离子半径大小顺序为F->Na+>Al3+,即A>J>H,故A正确;CO不是酸性氧化物,三氧化二
铝是两性氧化物,过氧化钠不是碱性氧化物,故B错误;D为碳元素,碳的单质有石墨、金刚石和足球烯
等,故C正确;Mg在CO 中燃烧生成氧化镁和碳,故D正确。
2
17.X、Y、Z、M、W为五种短周期元素,它们的原子序数与其某种常见化合价的关系如图所示,对应坐
标分别为(a,+5)、(b,-2)、(c,+1)、(d,+3)、(e,+7)。下列说法不正确的是( )
A.最高价含氧酸的酸性:
B.气态氢化物的稳定性:
C.简单离子半径大小:
D.Y与X或W均可形成两种以上的二元化合物
【答案】B
【解析】X原子序数最小,常见化合价为+5价,X为N,Y原子序数大于N,常见化合价为-2价,Y为
O,Z原子序数大于O,常见化合价为+1价,Z为Na,M原子序数大于Na,常见化合价为+3价,M为
Al,W原子序数大于Al,常见化合价为+7价,W为Al。A.Cl的非金属性强于N,则最高价含氧酸的酸
性HClO>HNO ,A正确;B.非金属性O>Cl>N,则气态氢化物的稳定性HO>HCl>NH ,B错误;C.离
4 3 2 3
子的电子层数越多,离子半径越大,电子层结构相同时,核电荷数越大离子半径越小,则离子半径Cl->N3-
>O2->Na+>Al3+,C正确;D.O可与N形成NO、NO 、NO,可与Cl形成ClO、ClO 、ClO 等,D正
2 2 5 2 2 2 3
确;故选B。
18.X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数
之和为15,X与Z可形成XZ 分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质
2
子数是X、Y、Z、M四种元素质子数之和的二分之一。下列说法正确的是( )
A.Y的简单气态氢化物的热稳定性要强于X,是因为Y的简单气态氢化物分子间存在氢键
B.XZ、WZ 均为直线形的共价化合物
2 2 2
C.由X元素形成的单质在自然条件下有多种同素异形体存在
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
【答案】C
【解析】X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电
子数之和为15,X与Z可形成XZ 分子,先令XZ 为CO,C、N、O最外层电子数之和恰好为15,假设成
2 2 2
立,X、Y、Z分别为C、N、O;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1,则其相对分
子质量为0.76×22.4≈17,则M为H元素;W的质子数是X、Y、Z、M四种元素质子数之和的,则×(6+7
+8+1)=11,则W为Na元素。N的简单气态氢化物的热稳定性要强于C,是因为N元素的非金属性强,
与氢键无关,A错误;CO 为直线形的共价化合物,NaO 属于离子化合物,B错误;由C元素形成的单质
2 2 2
在自然条件下有多种同素异形体存在,如金刚石、石墨等,C正确;由C、N、O、H四种元素形成的化合
物不一定既有离子键又有共价键,如CO(NH) 只含有共价键,D错误。
2 2
19.U、V、W、X、Y、Z是原子序数依次增大的前四周期常见元素。Y的单质在 中燃烧的产物可使品
红溶液褪色。Z和W元素形成的化合物 具有磁性。U的单质在 中燃烧可生成UW和 两种气体。X原子半径同周期最大。下列说法正确的是( )
A.V元素位于第二周期第V主族 B. 的电子式为:
C. 是离子化合物 D. 溶于水只破坏了离子键
【答案】B
【解析】U、V、W、X、Y、Z是原子序数依次增大的前四周期常见元素。Y的单质在 中燃烧的产物可
使品红溶液褪色,则Y为S,W为O。Z和W元素形成的化合物 具有磁性,则Z为Fe。U的单质在
中燃烧可生成UW和 两种气体,则U为C,则V为N。X原子半径同周期最大,则X为Na。A.
V元素为氮元素,位于第二周期第VA族,故A错误;B. 为二氧化碳,其电子式为: ,
故B正确;C. 是二硫化碳,属于共价化合物,故C错误;D. 溶于水生成了氢氧化钠和氧气,
破坏了离子键和共价键,故D错误。故选B。
20.短周期主族元素A、B、C、D的原子序数依次增大;B、D元素同主族;C元素的电子层数等于最外
层电子数;甲是D元素的最高价氧化物对应的水化物;M、N分别是C、B元素的单质;乙、丙、戊是由
这些元素组成的二元化合物。上述物质的转化关系如下图所示。
下列说法正确的是( )
A.常温下,甲的浓溶液与M不发生反应
B.在丙转化为戊的反应中,消耗1mol N转移
C.气态氢化物的还原性:B>D
D.丙、戊均能使品红溶液褪色
【答案】B
【解析】结合题意和流程图可知,C元素的电子层数等于最外层电子数,C为Al元素,M为Al单质,B为O元素,N为O,B、D元素同主族,D为S元素,甲是D元素的最高价氧化物对应的水化物,甲为
2
H2SO4,浓硫酸与金属Al在加热条件下反应生成硫酸铝、SO 、H2O,乙、丙、戊是由这些元素组成的二
2
元化合物,则A为H元素,丁为硫酸铝,乙为HO,丙为SO ,戊为SO 。A.常温下,浓硫酸与金属Al
2 2 3
会发生钝化,在金属Al表面生成一层致密的氧化膜,发生了反应,A错误;B.SO 与O 在催化剂、加热
2 2
条件下生成SO 为可逆反应,但消耗1mol O 转移电子数等于4mole-,B正确;C.O元素的氧化性大于S
3 2
元素,则气态氢化物的还原性:D>B,C错误;D.SO 能使品红溶液褪色,而SO 不能使品红溶液褪色,
2 3
D错误;故选B。21.化合物甲是一种常见无机物,其结构如下图所示(图中的“—”为单键或双键),
其中W、X、Y、Z为元素周期表中的短周期主族元素,且原子序数依次增大,W和Y、X和Z分别为同主
族元素,其四种元素原子的最外层电子数之和为14.下列叙述正确的是( )
A.W分别与X、Z形成的简单分子均为10电子微粒
B.X、Y形成的离子化合物只含离子键
C.X、Y、Z三种元素的简单离子半径大小顺序为Z>X>Y
D.等物质的量Y和Z的最高价氧化物对应的水化物反应生成甲
【答案】C
【解析】由化合物甲中X能形成2个共价键可知,X为O元素、W为H元素,由W、X、Y、Z为元素周
期表中的短周期主族元素,且原子序数依次增大,W和Y、X和Z分别为同主族元素可知,Y为Na元
素、Z为S元素,H、O、Na、S四种元素原子的最外层电子数之和为14。A.硫元素位于第三周期,硫化氢
分子中含有的电子数为18,故A错误;B.氧元素和钠元素形成的过氧化钠为离子化合物,化合物中含有离
子键和共价键,故B错误;C.同主族元素,从上到下离子半径依次增大,电子层结构相同的离子,核电荷
数越大,离子半径越小,则X、Y、Z三种元素的简单离子半径大小顺序为Z>X>Y,故C正确;D.化合物
甲为亚硫酸氢钠,硫元素为+4价,而硫酸氢钠中硫元素化合价为+6价;氢氧化钠与硫酸等物质的量反应
生成硫酸氢钠,不能生成亚硫酸氢钠,故D错误;故选C。
22.X、Y、Z、W四种主族元素,原子序数依次增大,且均不大于20,四种元素核电荷数之和为46,X、
Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。Z元素是一种重要的“成盐元
素”,其形成的一种盐在海水中含量最高,其单质通过电解该盐溶液获得。下列关于四种元素说法错误的
是( )
A.XY、ZY、 W(ZY) 均是常见的杀菌消毒剂,三者作用原理相同
2 2 2 2B.WX 中X元素的检验方法可以将WX 固体置于氧气流中灼烧并将产物通过无水硫酸铜
2 2
C.WZ、WY 两种化合物中阴阳离子个数比均为1 : 2
2 2
D.可以通过XZY、ZY 等物质中的元素化合价来比较Y、Z两种元素的非金属性强弱
2
【答案】C
【解析】X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。则X、Y分别为H、
O。Z形成的一种盐在海水中含量最高,Z为Cl。四种元素核电荷数之和为46,则W为20号元素Ca。
A.三种物质分别为HO、ClO 、Ca(ClO) ,三者均具有较强的氧化性,可利用氧化性进行消毒杀菌,A
2 2 2 2
项正确;B.CaH 与O 反应变为HO遇CuSO 溶液变蓝,说明X为H元素,B项正确;C.WZ、WY 分
2 2 2 4 2 2
别为CaCl 和CaO,前者是由Ca2+和2个Cl-组成阴阳离子之比为1:2,而后者是由Ca2+和O2-阴阳离子之比
2 2 2
为1:1,C项错误;D.XZY、ZY 为HClO和ClO 中Cl均呈现出了正价而O均呈现出负价,说明O的电
2 2
子能力强于Cl,所以O的非金属性强于Cl,D项正确;故选C。
第 II 卷(非选择题 共 56 分)
二、非选择题:本题共5个小题,共56分。
23.下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素回答下列问题:
(1)h与f原子序数相差______________。
(2)b、c、f的简单离子半径最小的是______________________________(填离子符号)
(3)e、f、g三种元素的气态氢化物最不稳定的是______________________(用化学式表示)。
(4)写出h原子的结构示意图______________________________。
(5)b元素的最高价氧化物对应水化物与g元素最高价氧化物对应水化物反应的离子方程式为:
________________________________________________。
【答案】(1)18 (2)Mg2+ (3)PH (4) (5)H++OH- == HO
3 2
【分析】根据元素在周期表中的位置可以确定各符号代表的元素。a是氮,b是钠,c是镁,d是铝,e是
磷,f是硫,g是氯,h是硒。
(1)f、h为第VIA族元素,分别位于第三、四周期,原子序数相差18。(2)b、c简单离子有两个电子层,且电子层结构相同,核电荷数大,离子半径小,离子半径大小为b>c,
f简单离子有三个电子层,离子半径比b、c大。因此半径最小的离子是Mg2+。
(3)e、f、g在同一周期,从左到右非金属性增强,气态氢化物稳定性增强,故最不稳定的是 e的氢化物
PH 。
3
(4)h是硒元素,位于周期表第四周期第VIA族,原子结构示意图为: 。
(5)b、g元素最高价氧化物对应水化物分别为NaOH,HClO ,分别是强碱和强酸,两者反应的离子方程
4
式为: 。
24.某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。
I.甲同学验证同一周期从左到右元素的金属性强弱。实验药品有小块钠,表面积相同的镁、铝,稀盐酸,
蒸馏水。
(1)请填写实验操作。
实验目的 实验操作 实验结论
比较钠、镁金属性强弱 Na>Mg
比较镁、铝金属性强弱 Mg>A1
Ⅱ.乙同学利用如图所示装置可以验证非金属性的变化规律,实验室中药品有NaS溶液、KMnO 、浓盐
2 4
酸、MnO 。
2
(2)干燥管D的作用是 _______ _ 设计实验来验证氯的非金属性强于硫,装置A、B、C中所装药
品分别为 、 、 ,装置C中的实验现象为 ___________ _。
(3)用上述装置证明非金属性:S>C>Si,则装置A、B、C中所装药品分别为 、 、
。
【答案】(1) 取钠、镁投入到等量的蒸馏水中 取表面积相同的铝、镁投入到等量的稀盐酸中
(2) 防止倒吸 浓盐酸 KMnO Na S溶液 有黄色沉淀生成
4 2(3) 稀硫酸 碳酸钠 NaSiO 溶液
2 3
【解析】验证氯的非金属性强于硫,证明氯气将NaS中的S置换出来即可。该装置没有加热装置,故选用
2
浓盐酸与高锰酸钾制备氯气,A中放浓盐酸,B中放高锰酸钾,C中放NaS溶液,D的作用是防倒吸。
2
(1)钠与镁与水反应速率不同,比较金属性的实验操作是:取钠、镁投入到等量的蒸馏水中;镁、铝与
酸反应产生气泡的速率不同,比较金属性的实验操作是:取表面积相同的铝、镁投入到等量的稀盐酸中;
(2)根据分析,干燥管D的作用是:防止倒吸;A、B、C中所装药品分别为浓盐酸、KMnO 、NaS溶
4 2
液;C中观察到的现象是:有黄色沉淀生成;
(3)用上述装置证明非金属性:S>C>Si,需要证明酸性:硫酸>碳酸>硅酸,故A中盛放稀硫酸,B中盛
放碳酸钠,C中盛放NaSiO 溶液,故选稀硫酸、碳酸钠、NaSiO 溶液。
2 3 2 3
25.现有部分短周期元素的性质或原子结构如表:
元素编号 元素的性质或原子结构
T M层上有6个电子
X 最外层电子数是次外层电子数的2倍
Y 常温下单质为双原子分子,其氢化物的水溶液呈碱性
Z 元素的最高正化合价是+7价
(1)元素X的一种核素可用于测定文物年代,这种核素的符号是________________。
(2) 元 素 Y 与 氢 元 素 形 成 一 种 离 子 YH , 写 出 某 溶 液 中 含 该 微 粒 的 检 验 方 法 :
___________________________。
(3)元素Z与元素T相比,原子得电子能力较强的是________________(用元素符号表示),下列表述中能证
明这一事实的是______________(填序号)。
①常温下Z的单质和T的单质状态不同 ;
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中
化 学 性 质 明 显 不 同 于 其 他 三 种 的 是 ______________( 填 化 学 式 ) , 理 由 是
_______________________________。
【答案】(1) C
(2)在溶液中加入 NaOH 溶液然后加热,用湿润的红色石蕊试纸检验产生的气体,如果试纸变蓝,证明溶
液中含NH + (3) Cl ② (4) HCO HCO 是弱酸,HSO 、HNO 和HClO 都是强酸
4 2 3 2 3 2 4 3 4
【解析】T的M层上有6个电子,根据电子排布规律,M是第三层,故一共有16个电子,T为S,X的最
外层电子数是次外层电子数的2倍,推出X为C,Y常温下单质为双原子分子,其氢化物水溶液呈碱性,
推出Y为N,Z元素最高正价是+7价,位于第ⅦA族,即Z为Cl,据此分析。(1)元素C的一种同位素可测定文物年代,这种同位素的符号是 ;故答案为 ;
(2)N与H形成的一种离子为NH ,检验该离子的方法是在溶液中加入NaOH溶液然后加热,用湿润的
红色石蕊试纸检验产生的气体,如果试纸变蓝,证明溶液中含NH ;
(3)同周期从左向右主族元素的非金属性逐渐增强,得电子能力即为非金属能力,故 Cl的得电子能力强
于S;①物质的状态不能判断非金属性的强弱,故①不符合题意;②氢化物越稳定,其非金属性越强,Z
的氢化物比T的氢化物稳定,说明Cl的非金属性强于S,故②符合题意;③都与NaOH溶液反应,不能说
明它们非金属性强弱,故③不符合题意;故答案为Cl;②;
(4)三种最高价含氧酸分别为HSO 、HCO、HNO、HClO,其中碳酸是弱酸,其余都是强酸。
2 4 2 3 3 4
26.元素周期律反映了元素性质的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化
物中,碱性最弱的是__________________(填化学式)。
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,Al、O、N三种元素的简单离子半径由大到小的排
列顺序是_________________________________________。
(3)锡为主族元素,其原子结构示意图: 。锡在元素周期表中的位置是
______________________,SnO 能与NaOH溶液反应生成钠盐(Na SnO )和水,写出发生反应的化学方程
2 2 3
式:________________________。
(4)硒( Sn)是与人类的健康密切相关的一种元素,工业上用浓HSO 焙烧CuSe的方法提取硒(其中Cu转化
34 2 4
为CuSO ),且有SO 、HO和SeO(固体)生成,写出发生反应的化学方程式:
4 2 2 2
_____________________________。理论上该反应每转移1mol电子,可得到的SeO 的质量为
2
_____________________g。
【答案】(1)Al(OH)
3
(2)N3->O2->Al3+
(3) 第五周期第IVA族 SnO +2NaOH=Na SnO +H O
2 2 3 2
(4) CuSe+4H SO =====CuSO +SeO +3SO↑+4H O 18.5
2 4 4 3 2 2
【解析】(1)金属性越弱,最高价氧化物的水化物碱性越弱,故碱性最弱的是Al(OH)3。
(2)核外电子数相同时质子数越大半径越小,故离子半径由大到小的顺序为N3->O2->Al3+。
(3)锡原子核外含有5个电子层,最外层含有4个电子,则Sn在周期表中的位置为第五周期第IVA族,
锡和C同一主族,氧化物的性质相似,类比CO2与NaOH的反应可知SnO2与NaOH的反应生成Na2SnO3
和H2O,反应的化学方程式为 SnO +2NaOH=Na SnO +H O。
2 2 3 2
(4)CuSe和浓硫酸反应生成CuSO )、SO 和SeO,化学方程式
4 2 2CuSe+4H SO =====CuSO +SeO +3SO↑+4H O。存在关系式:SeO2~6e-,则理论上该反应每转移1mol电
2 4 4 3 2 2
子,可得到SeO2的质量为1/6mol×(79+32)g/mol=18.5g。
27.实验室加热液体时,常加入沸石,其主要成分为 Na(AlSi O )·2H O,根据其组成元素完成下列填
2 2 3 10 2
空:
(1)Al元素在周期表中的位置:_______________________。
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常做强还原剂,化合
物甲的电子式为______________________;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是
____________(填化学式),化合物乙中存在的化学键类型为_______________________。
(3)O元素和其同周期相邻的两种元素分别形成的简单气态氢化物中最稳定的是_______________(填化学
式)。
(4)已知硅酸(H SiO)为白色胶状沉淀。
2 3
实验室中现有药品:①稀盐酸、②稀硫酸、③ NaHCO 固体、④CaCO 固体、⑤NaSiO 溶液,请选择合
3 3 2 3
适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分
别为____________、____________、__________________(填序号)。但有同学认为该实验所得现象无法充
分证明C、Si的非金属性强弱,如何改进?
________________________________________________________________________。
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子
核中有180个中子,则Uue中A=____________、Z=____________。
【答案】 (1)第三周期第ⅢA族 (2)Na+[H]- NaO 离子键、非极性共价键 (3)HF
2 2
(4)① ④ ⑤ 在A、B之间加装盛有饱和NaHCO 溶液的洗气瓶 (5)299 119
3
【解析】 (1)铝的原子序数为13,位于元素周期表第三周期第ⅢA族。(2)原子半径最小的元素为H,Na
与H组成的化合物为NaH,其电子式为Na+[H]-,化合物乙可作为呼吸面具或潜艇氧气的来源,乙是
NaO ,NaO 为离子化合物,含离子键和非极性共价键。(3)O元素和其同周期相邻的两种元素分别形成的
2 2 2 2
简单气态氢化物为NH 、HO、HF,而F的非金属性比O、N强,因此HF的稳定性最强。(4)为验证C、Si
3 2
的非金属性的变化规律,A装置用于制取二氧化碳,B装置中盛放硅酸钠溶液,因此X、Y、Z处所盛装或
放置的药品分别为稀盐酸、CaCO 固体、NaSiO 溶液,但稀盐酸有挥发性,制得的二氧化碳中会混有
3 2 3
HCl,HCl也能和硅酸钠溶液反应生成硅酸沉淀,无法证明是二氧化碳和硅酸钠溶液反应生成硅酸,因此
应在A、B之间加装盛有饱和NaHCO 溶液的洗气瓶,用于除去氯化氢,防止干扰实验。(5)钠位于第ⅠA
3
族,Uue与Na同主族,位于第八周期,原子序数为119,即质子数为119,其一种可能存在的核素原子核
中有180个中子,质量数为119+180=299,因此Uue中A=299,Z=119。