文档内容
第四章 物质结构 元素周期律
过关测试 提高卷
(时间:90分钟)
一、选择题(每小题3分,共54分)
1.铁60同位素的现身,揭秘了超新星爆炸历史真相。下列说法中正确的是 ( )
A.铁元素的质量数为60
B. 的核内质子数比中子数多8
C. 与 的核外电子数相同,属于同一种核素
D. 与 的化学性质相似,互为同位素
2.下列物质中,含共价键的离子化合物是( )
A.MgCl B.N C.HCl D.NaO
2 2 2 2
3.关于化学键的各种叙述中,下列说法中正确的是( )
A.在离子晶体里,只存在离子键
B.共价化合物里,一定不存在离子键
C.仅由非金属元素形成的化合物中不可能有离子键
D.由不同种元素组成的多原子分子里,一定只存在极性键
4.下列说法中正确的是( )
A.某元素的阳离子与同种阴离子可形成多种化合物
B.阳离子中肯定含有金属元素,但含有金属元素的离子不一定是阳离子
C.某物质经科学测定只含有一种元素,则可断定该物质一定是纯净物
D.1 molNa和1 molAl各自发生化学反应时钠失去的电子少,则钠单质的还原性弱于铝单质
5.关于氢键,下列说法正确的是( )
A.所有含氢元素的化合物中都存在氢键,氢键比分子间作用力强
B.HO是一种非常稳定的化合物,就是由于水分子间形成氢键所致
2
C.氢原子和非金属性很强的元素原子(F、O、N)形成的共价键,称为氢键
D.分子间形成的氢键使相应物质的熔点和沸点升高
6.科学家制得一种新型分子O。关于O 和O 的说法不正确的是( )
4 4 2
A.互为同素异形体 B.等质量的O 和O 所含原子数相同
4 2
C.它们的摩尔质量相同 D.等物质的量的O 和O 所含原子数之比为2:1
4 2
7.已知3.0g 中核外电子数比质子数多6.02×1022个,下列说法中正确的是( )
A.A元素的相对原子质量为12 B.AO 的摩尔质量为60C.3.0gAO 的物质的量是0.02mol D.A原子的摩尔质量32g/mol
8.N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.22.4L(标准状况)氮气中含有7N 个中子
A
B.1mol重水比1mol水多N 个质子
A
C.若N 的数值变为原来的两倍,则O 的摩尔质量变为64g/mol
A 2
D.12C在自然界中的丰度为98.892%,因此碳元素的质量数为12
9.HRO 中共有x个电子,R原子的质量数为A,则a克HRO 中含有质子的物质的量为( )
n 3 n 3
A. B.
C.(x-n-24)mol D.
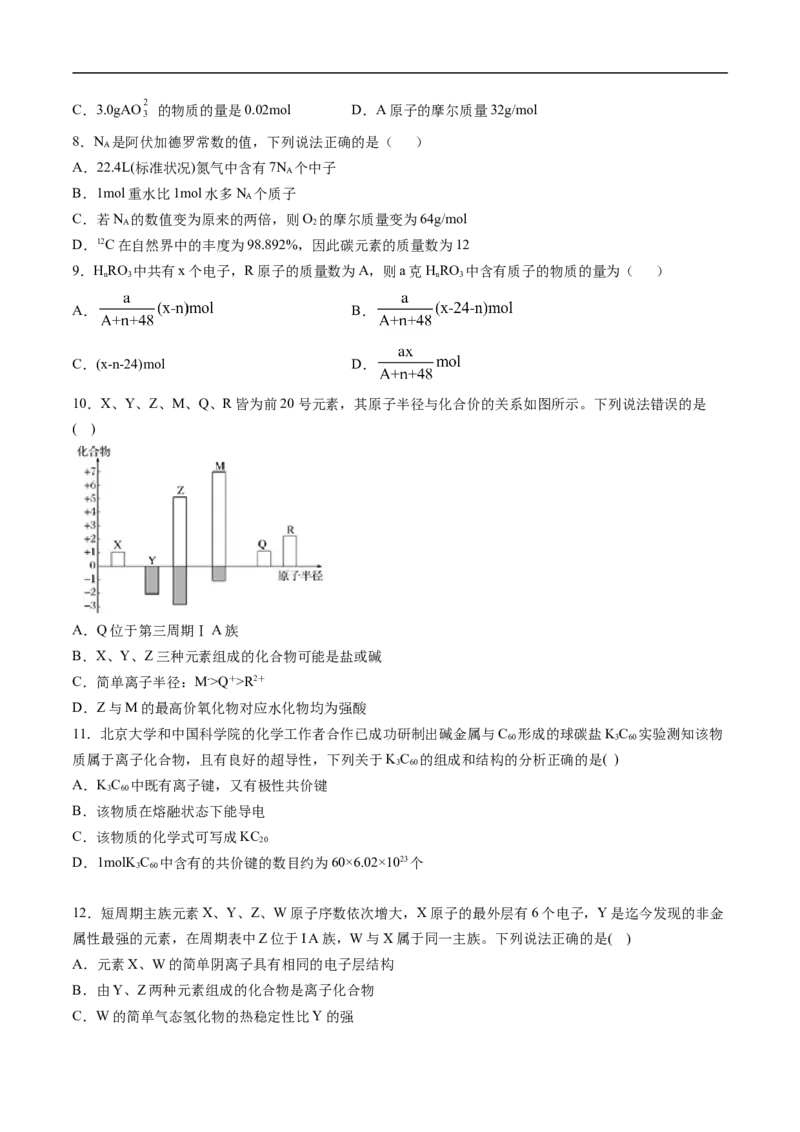
10.X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法错误的是
( )
A.Q位于第三周期ⅠA族
B.X、Y、Z三种元素组成的化合物可能是盐或碱
C.简单离子半径:M->Q+>R2+
D.Z与M的最高价氧化物对应水化物均为强酸
11.北京大学和中国科学院的化学工作者合作已成功研制出碱金属与C 形成的球碳盐KC 实验测知该物
60 3 60
质属于离子化合物,且有良好的超导性,下列关于KC 的组成和结构的分析正确的是( )
3 60
A.KC 中既有离子键,又有极性共价键
3 60
B.该物质在熔融状态下能导电
C.该物质的化学式可写成KC
20
D.1molK C 中含有的共价键的数目约为60×6.02×1023个
3 60
12.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金
属性最强的元素,在周期表中Z位于I A族,W与X属于同一主族。下列说法正确的是( )
A.元素X、W的简单阴离子具有相同的电子层结构
B.由Y、Z两种元素组成的化合物是离子化合物
C.W的简单气态氢化物的热稳定性比Y的强D.原子半径:r(X)<r(Y)<r(Z)<r(W)
13.砷(As)为第四周期第ⅤA族元素,根据元素周期表和元素周期律的知识,下列有关推测不正确的是
( )
A.砷有-3、+3、+5等多种化合价
B.原子半径:As>P
C.酸性:HAsO >HSO
3 4 2 4
D.热稳定性:HBr>AsH
3
14.元素周期表可以指导人们进行规律性的推测和判断,下列说法不正确的是( )
A.若 X2+和 Y-的核外电子层结构相同,则原子序数:a=b+3
a b
B.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F
C.锗与硅位于金属与非金属的交界处,都能作半导体材料
D.S和Se分别位于第ⅥA族的第三、四周期,则氢化物的稳定性:HS>HSe
2 2
15.下列说法中正确的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高
B.熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物
C.NCl 分子中所有的原子均为8电子稳定结构
3
D.NaHSO 溶于水时发生NaHSO=Na++H++ ,此时破坏的只有离子键
4 4
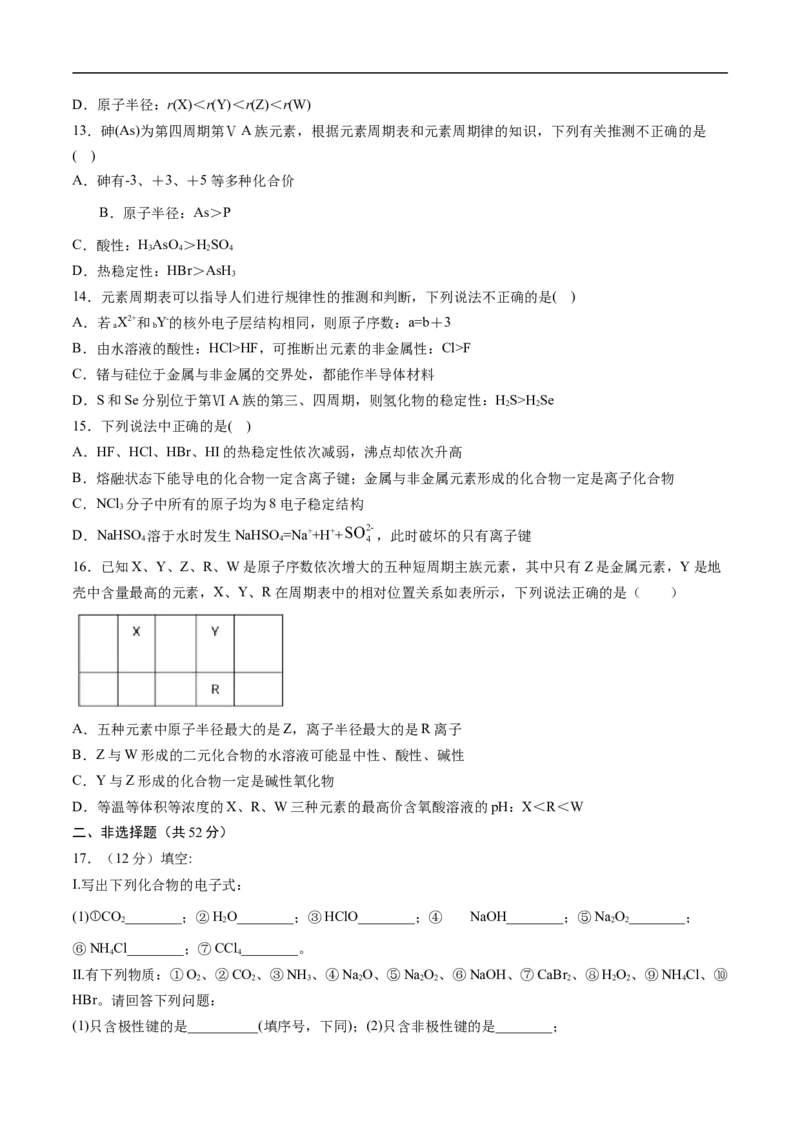
16.已知X、Y、Z、R、W是原子序数依次增大的五种短周期主族元素,其中只有Z是金属元素,Y是地
壳中含量最高的元素,X、Y、R在周期表中的相对位置关系如表所示,下列说法正确的是( )
A.五种元素中原子半径最大的是Z,离子半径最大的是R离子
B.Z与W形成的二元化合物的水溶液可能显中性、酸性、碱性
C.Y与Z形成的化合物一定是碱性氧化物
D.等温等体积等浓度的X、R、W三种元素的最高价含氧酸溶液的pH:X<R<W
二、非选择题(共52分)
17.(12分)填空:
I.写出下列化合物的电子式:
(1)①CO________;②HO________;③HClO________;④ NaOH________;⑤NaO________;
2 2 2 2
⑥NH Cl________;⑦CCl ________。
4 4
Ⅱ.有下列物质:①O、②CO、③NH 、④NaO、⑤NaO、⑥NaOH、⑦CaBr 、⑧HO、⑨NH Cl、⑩
2 2 3 2 2 2 2 2 2 4
HBr。请回答下列问题:
(1)只含极性键的是__________(填序号,下同);(2)只含非极性键的是________;(3)含有极性键和非极性键的是________;(4)含有极性键的离子化合物是________;
(5)含有非极性键的离子化合物是________。
18.(10分)A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A
与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排
布相同。由以上元素组成的物质BE和D 具有相同的电子数。请回答以下问题:
2
(1)F位于第_____周期第_____族。
(2)G的离子结构示意图为_____。
(3)用电子式表示D 的形成过程:______。
2
(4)由A、E、F三种元素形成的化合物的化学式为____,含有的化学键有_____(填化学键类型),属于_____
化合物。
(5)B的最高价是_____,由A、B组成的化合物中,含A量最高的物质的结构式是_____。
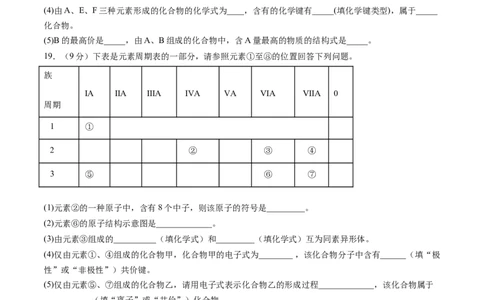
19.(9分)下表是元素周期表的一部分,请参照元素①至⑧的位置回答下列问题。
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦
(1)元素②的一种原子中,含有8个中子,则该原子的符号是_________。
(2)元素⑥的原子结构示意图是_____________。
(3)由元素③组成的__________(填化学式)和_________(填化学式)互为同素异形体。
(4)仅由元素①、④组成的化合物甲,化合物甲的电子式为________ ,该化合物分子中含有______(填“极
性”或“非极性”)共价键。
(5)仅由元素⑤、⑦组成的化合物乙,请用电子式表示化合物乙的形成过程_____________,该化合物属于
___________(填“离子”或“共价”)化合物。
20.(11分)为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答
下列问题:(原理:MnO +4HCl(浓) MnCl +Cl↑+2HO)
2 2 2 2(1)装置B中盛放的试剂是___(填选项),实验现象为___,化学反应方程式是___。
A.NaS溶液 B.NaSO 溶液 C.NaSO 溶液
2 2 3 2 4
(2)装置C中盛放烧碱稀溶液,目的是______。反应的离子方程式是______________________。
(3)不能证明氯元素比硫元素非金属性强的依据为_____。(填序号)
①氯原子比硫原子更容易获得电子形成离子
②S2-比Cl-还原性强
③次氯酸的氧化性比稀硫酸强
④HCl比HS酸性强
2
(4)若B瓶中盛放KI溶液和CCl 试剂,实验后,振荡、静置,会出现分层,下层呈紫红色的实验现象,若
4
B瓶中通入标准状况下44.8L氯气全部参加反应,则转移的电子数目是___。
21.(10分)现有部分短周期主族元素的性质或原子结构如表所示:
元素编号 元素性质或原子结构
X 周期序数=主族序数=原子序数
Y 原子最外层电子数为a,次外层电子数为b
Z 原子L层电子数为a+b,M层电子数为a-b
M 单质在自然界中的硬度最大
N 位于第三周期,最外层电子数是电子层数的2倍
L 其最高价氧化物水化物酸性最强
(1)写出Y、Z、N、L四种元素的名称:Y________,Z________,N________,L________。
(2)Y、Z、N氢化物稳定性由大到小的顺序________(用化学式回答)。
(3)证明用M单质与Z的氧化物反应制取单质Z的化学方程式__________。
(4)写出由X和Y组成的10e-和18e-物质的分子式_________、________。
(5)写出ML 的电子式_______;其化学键的类型是_______(极性键或者非极性键或者既有极性键又有非极
4
性键)。