文档内容
考点 05 氧化还原反应方程式的配平与计算
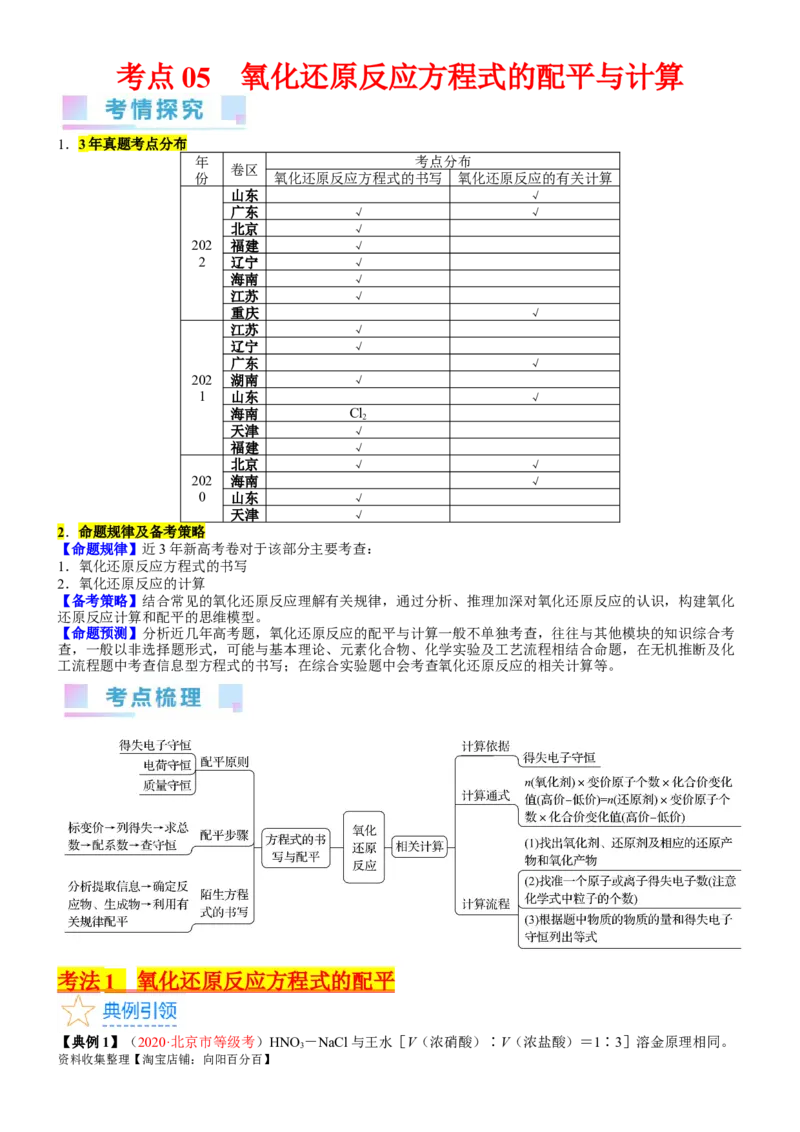
1.3年真题考点分布
年 考点分布
卷区
份 氧化还原反应方程式的书写 氧化还原反应的有关计算
山东 √
广东 √ √
北京 √
202 福建 √
2 辽宁 √
海南 √
江苏 √
重庆 √
江苏 √
辽宁 √
广东 √
202 湖南 √
1 山东 √
海南 Cl
2
天津 √
福建 √
北京 √ √
202 海南 √
0 山东 √
天津 √
2.命题规律及备考策略
【命题规律】近3年新高考卷对于该部分主要考查:
1.氧化还原反应方程式的书写
2.氧化还原反应的计算
【备考策略】结合常见的氧化还原反应理解有关规律,通过分析、推理加深对氧化还原反应的认识,构建氧化
还原反应计算和配平的思维模型。
【命题预测】分析近几年高考题,氧化还原反应的配平与计算一般不单独考查,往往与其他模块的知识综合考
查,一般以非选择题形式,可能与基本理论、元素化合物、化学实验及工艺流程相结合命题,在无机推断及化
工流程题中考查信息型方程式的书写;在综合实验题中会考查氧化还原反应的相关计算等。
考法 1 氧化还原反应方程式的配平
【典例1】(2020·北京市等级考)HNO-NaCl与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
3
资料收集整理【淘宝店铺:向阳百分百】将溶金反应的化学方程式补充完整:
___Au+____NaCl+____HNO HAuCl +____+____+____NaNO 。
3 4 3
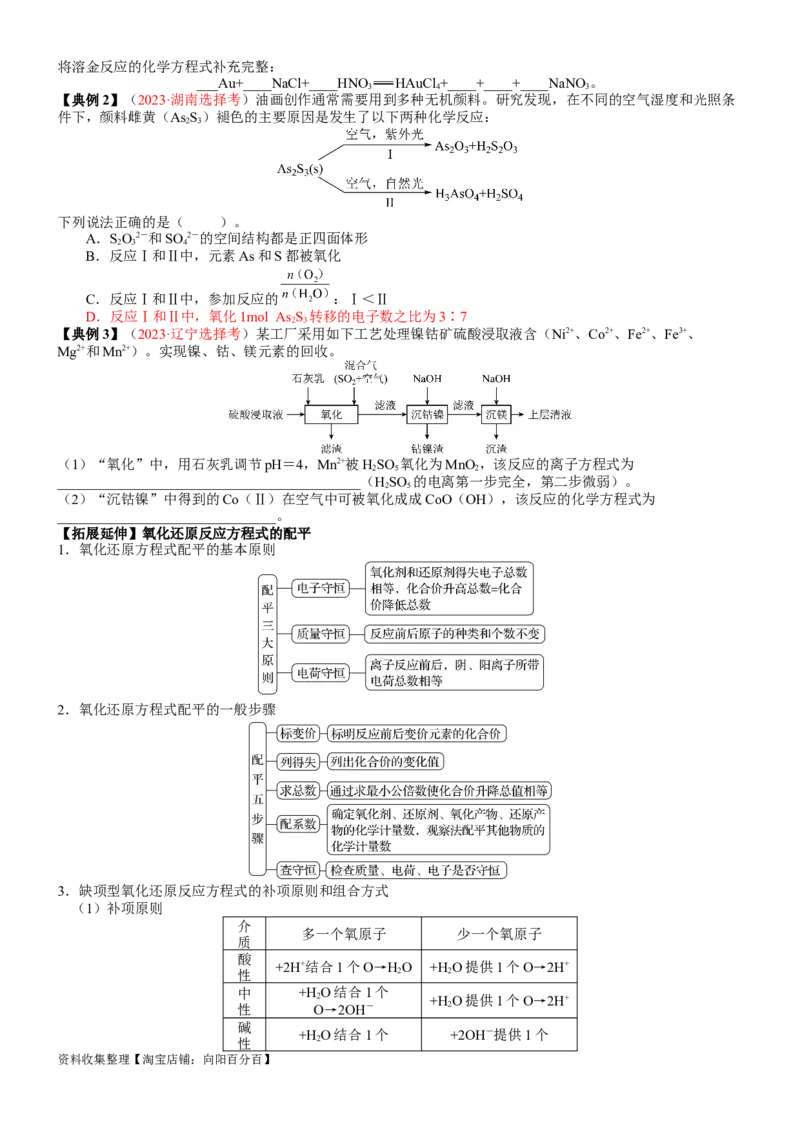
【典例2】(2023·湖南选择考)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条
件下,颜料雌黄(As S)褪色的主要原因是发生了以下两种化学反应:
2 3
下列说法正确的是( )。
A.SO2-和SO 2-的空间结构都是正四面体形
2 3 4
B.反应Ⅰ和Ⅱ中,元素As和S都被氧化
C.反应Ⅰ和Ⅱ中,参加反应的 :Ⅰ<Ⅱ
D.反应Ⅰ和Ⅱ中,氧化1mol As S 转移的电子数之比为3∶7
2 3
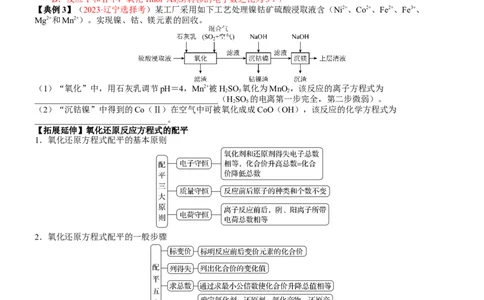
【典例3】(2023·辽宁选择考)某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、Fe3+、
Mg2+和Mn2+)。实现镍、钴、镁元素的回收。
(1)“氧化”中,用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO,该反应的离子方程式为
2 5 2
___________________________________________(HSO 的电离第一步完全,第二步微弱)。
2 5
(2)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成成CoO(OH),该反应的化学方程式为
_______________________________。
【拓展延伸】氧化还原反应方程式的配平
1.氧化还原方程式配平的基本原则
2.氧化还原方程式配平的一般步骤
3.缺项型氧化还原反应方程式的补项原则和组合方式
(1)补项原则
介
多一个氧原子 少一个氧原子
质
酸
+2H+结合1个O→HO +H O提供1个O→2H+
性 2 2
中 +H O结合1个
2 +H O提供1个O→2H+
性 O→2OH- 2
碱
+H O结合1个 +2OH-提供1个
性 2
资料收集整理【淘宝店铺:向阳百分百】O→2OH- O→HO
2
(2)组合方式
项目 反应物 生成物 使用条件
组合一 H+ HO 酸性溶液
2
组合二 HO H+ 酸性或中性溶液
2
组合三 OH- HO 碱性溶液
2
组合四 HO OH- 碱性或中性溶液
2
1.(2022·广东省等级考)催化剂Cr O 可由(NH )Cr O 加热分解制备,反应同时生成无污染气体。完成化
2 3 4 2 2 7
学方程式:(NH )Cr O Cr O+_______+_______。
4 2 2 7 2 3
2.(2023·山东选择考)已知电负性Cl>H>Si, SiHCl 在浓NaOH溶液中发生反应的化学方程式为
3
_________________________________________。
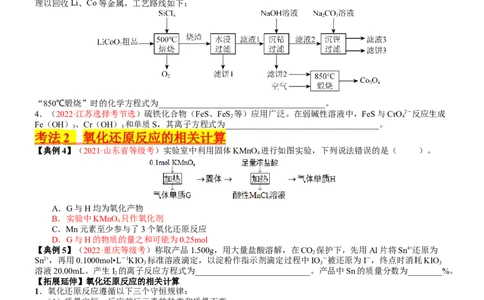
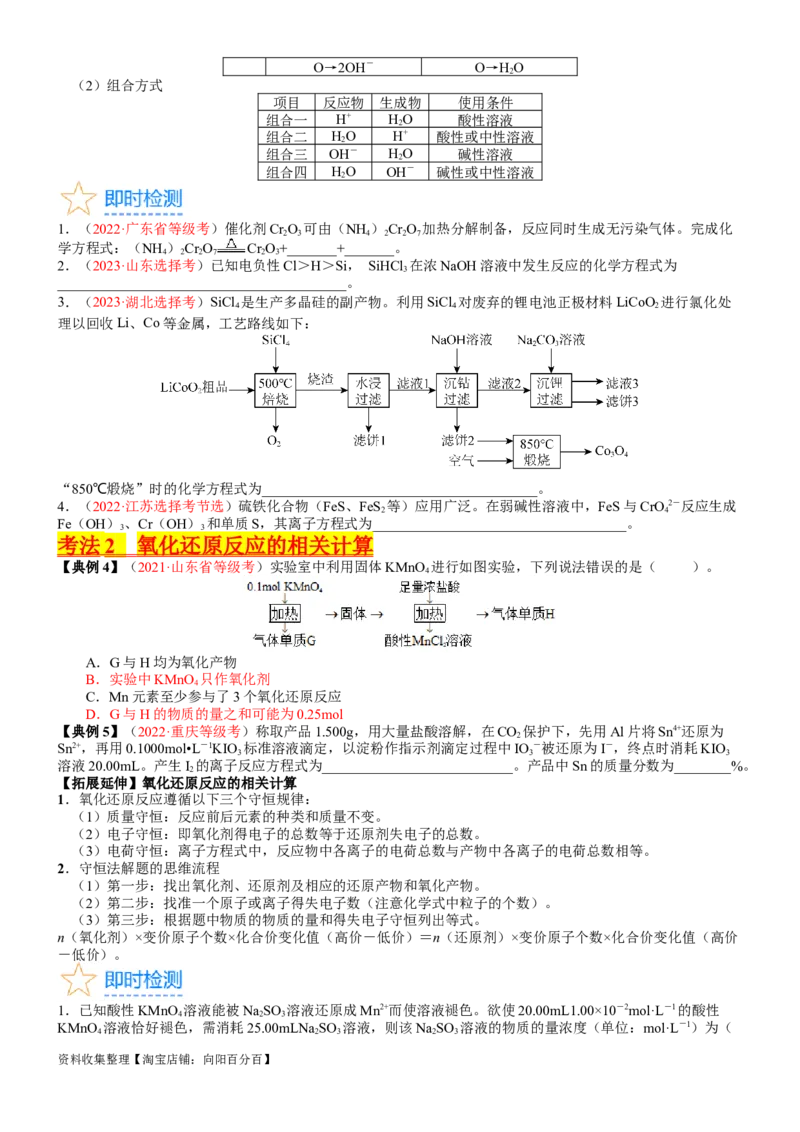
3.(2023·湖北选择考)SiCl 是生产多晶硅的副产物。利用SiCl 对废弃的锂电池正极材料LiCoO 进行氯化处
4 4 2
理以回收Li、Co等金属,工艺路线如下:
“850℃煅烧”时的化学方程式为_______________________________________。
4.(2022·江苏选择考节选)硫铁化合物(FeS、FeS 等)应用广泛。在弱碱性溶液中,FeS与CrO2-反应生成
2 4
Fe(OH)、Cr(OH) 和单质S,其离子方程式为____________________________________。
3 3
考法 2 氧化还原反应的相关计算
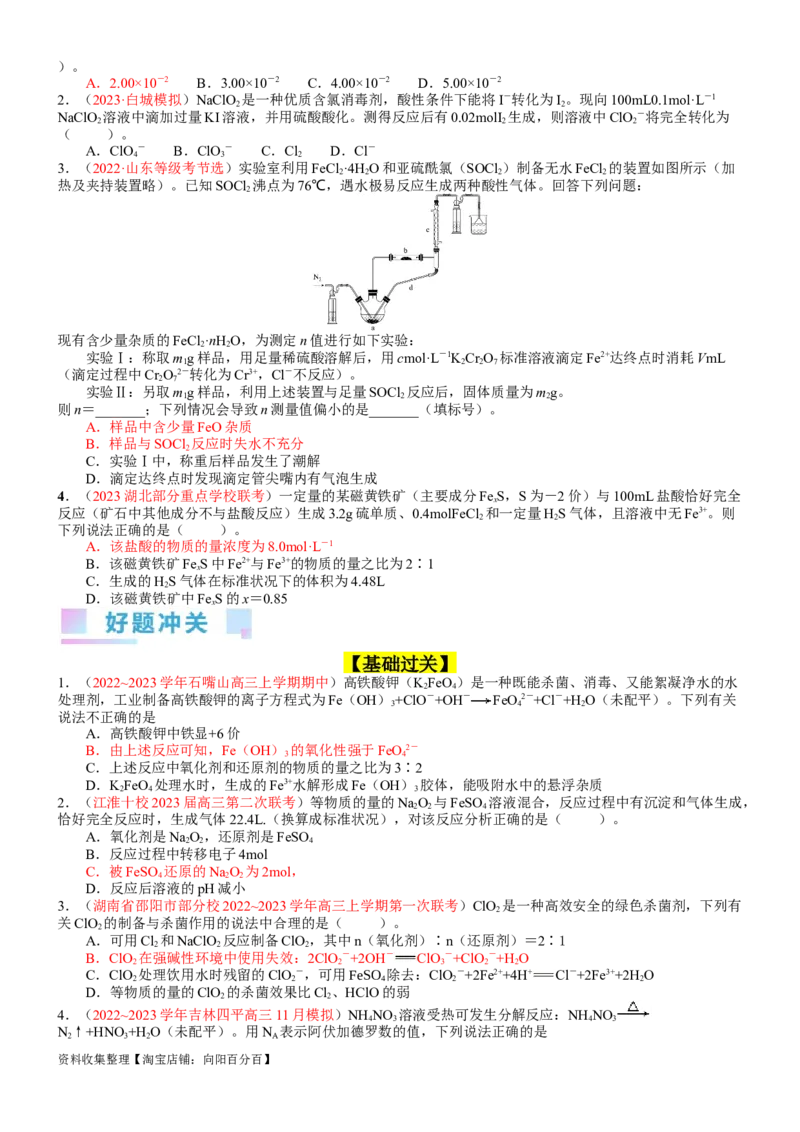
【典例4】(2021·山东省等级考)实验室中利用固体KMnO 进行如图实验,下列说法错误的是( )。
4
A.G与H均为氧化产物
B.实验中KMnO 只作氧化剂
4
C.Mn元素至少参与了3个氧化还原反应
D.G与H的物质的量之和可能为0.25mol
【典例5】(2022·重庆等级考)称取产品1.500g,用大量盐酸溶解,在CO 保护下,先用Al片将Sn4+还原为
2
Sn2+,再用0.1000mol•L-1KIO 标准溶液滴定,以淀粉作指示剂滴定过程中IO -被还原为I-,终点时消耗KIO
3 3 3
溶液20.00mL。产生I 的离子反应方程式为___________________________。产品中Sn的质量分数为________%。
2
【拓展延伸】氧化还原反应的相关计算
1.氧化还原反应遵循以下三个守恒规律:
(1)质量守恒:反应前后元素的种类和质量不变。
(2)电子守恒:即氧化剂得电子的总数等于还原剂失电子的总数。
(3)电荷守恒:离子方程式中,反应物中各离子的电荷总数与产物中各离子的电荷总数相等。
2.守恒法解题的思维流程
(1)第一步:找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)第二步:找准一个原子或离子得失电子数(注意化学式中粒子的个数)。
(3)第三步:根据题中物质的物质的量和得失电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值(高价-低价)=n(还原剂)×变价原子个数×化合价变化值(高价
-低价)。
1.已知酸性KMnO 溶液能被NaSO 溶液还原成Mn2+而使溶液褪色。欲使20.00mL1.00×10-2mol·L-1的酸性
4 2 3
KMnO 溶液恰好褪色,需消耗25.00mLNa SO 溶液,则该NaSO 溶液的物质的量浓度(单位:mol·L-1)为(
4 2 3 2 3
资料收集整理【淘宝店铺:向阳百分百】)。
A.2.00×10-2 B.3.00×10-2 C.4.00×10-2 D.5.00×10-2
2.(2023·白城模拟)NaClO 是一种优质含氯消毒剂,酸性条件下能将I-转化为I。现向100mL0.1mol·L-1
2 2
NaClO 溶液中滴加过量KI溶液,并用硫酸酸化。测得反应后有0.02molI 生成,则溶液中ClO -将完全转化为
2 2 2
( )。
A.ClO - B.ClO - C.Cl D.Cl-
4 3 2
3.(2022·山东等级考节选)实验室利用FeCl ·4HO和亚硫酰氯(SOCl )制备无水FeCl 的装置如图所示(加
2 2 2 2
热及夹持装置略)。已知SOCl 沸点为76℃,遇水极易反应生成两种酸性气体。回答下列问题:
2
现有含少量杂质的FeCl ·nHO,为测定n值进行如下实验:
2 2
实验Ⅰ:称取mg样品,用足量稀硫酸溶解后,用cmol·L-1KCr O 标准溶液滴定Fe2+达终点时消耗VmL
1 2 2 7
(滴定过程中Cr O2-转化为Cr3+,Cl-不反应)。
2 7
实验Ⅱ:另取mg样品,利用上述装置与足量SOCl 反应后,固体质量为mg。
1 2 2
则n=_______;下列情况会导致n测量值偏小的是_______(填标号)。
A.样品中含少量FeO杂质
B.样品与SOCl 反应时失水不充分
2
C.实验Ⅰ中,称重后样品发生了潮解
D.滴定达终点时发现滴定管尖嘴内有气泡生成
4.(2023湖北部分重点学校联考)一定量的某磁黄铁矿(主要成分FeS,S为-2价)与100mL盐酸恰好完全
x
反应(矿石中其他成分不与盐酸反应)生成3.2g硫单质、0.4molFeCl 和一定量HS气体,且溶液中无Fe3+。则
2 2
下列说法正确的是( )。
A.该盐酸的物质的量浓度为8.0mol·L-1
B.该磁黄铁矿FeS中Fe2+与Fe3+的物质的量之比为2∶1
x
C.生成的HS气体在标准状况下的体积为4.48L
2
D.该磁黄铁矿中FeS的x=0.85
x
【基础过关】
1.(2022~2023学年石嘴山高三上学期期中)高铁酸钾(KFeO)是一种既能杀菌、消毒、又能絮凝净水的水
2 4
处理剂,工业制备高铁酸钾的离子方程式为Fe(OH)+ClO-+OH- FeO2-+Cl-+H O(未配平)。下列有关
3 4 2
说法不正确的是
A.高铁酸钾中铁显+6价
B.由上述反应可知,Fe(OH) 的氧化性强于FeO2-
3 4
C.上述反应中氧化剂和还原剂的物质的量之比为3∶2
D.KFeO 处理水时,生成的Fe3+水解形成Fe(OH) 胶体,能吸附水中的悬浮杂质
2 4 3
2.(江淮十校2023届高三第二次联考)等物质的量的NaO 与FeSO 溶液混合,反应过程中有沉淀和气体生成,
2 2 4
恰好完全反应时,生成气体22.4L.(换算成标准状况),对该反应分析正确的是( )。
A.氧化剂是NaO,还原剂是FeSO
2 2 4
B.反应过程中转移电子4mol
C.被FeSO 还原的NaO 为2mol,
4 2 2
D.反应后溶液的pH减小
3.(湖南省邵阳市部分校2022~2023学年高三上学期第一次联考)ClO 是一种高效安全的绿色杀菌剂,下列有
2
关ClO 的制备与杀菌作用的说法中合理的是( )。
2
A.可用Cl 和NaClO 反应制备ClO ,其中n(氧化剂)∶n(还原剂)=2∶1
2 2 2
B.ClO 在强碱性环境中使用失效:2ClO -+2OH- ClO -+ClO -+H O
2 2 3 2 2
C.ClO 处理饮用水时残留的ClO -,可用FeSO 除去:ClO -+2Fe2++4H+ Cl-+2Fe3++2H O
2 2 4 2 2
D.等物质的量的ClO 的杀菌效果比Cl、HClO的弱
2 2
4.(2022~2023学年吉林四平高三11月模拟)NH NO 溶液受热可发生分解反应:NH NO
4 3 4 3
N↑+HNO+HO(未配平)。用N 表示阿伏加德罗数的值,下列说法正确的是
2 3 2 A
资料收集整理【淘宝店铺:向阳百分百】A.分解时每生成2.24L(标准状况)N,转移电子的数目为0.6N
2 A
B.2.8gN 中含有共用电子对的数目为0.3N
2 A
C.56gFe与足量稀硝酸反应生成NO 分子的数目为3N
2 A
D.0.1mol·L-1NH NO 溶液中,NH +的数目小于0.1N
4 3 4 A
5.(河北石家庄2022~2023学年高三3月模拟)用酸性KMnO 溶液处理硫化亚铜(Cu S)和二硫化亚铁
4 2
(FeS)的混合物时,发生反应I:MnO -+Cu S+H+ Cu2++SO 2-+Mn2++H O(未配平)和反应II:MnO -
2 4 2 4 2 4
+FeS +H+ Fe3++SO 2-+Mn2++H O(未配平)。下列说法正确的是( )。
2 4 2
A.反应I中Cu S既是氧化剂又是还原剂
2
B.反应I中每生成1molSO 2-,转移电子的物质的量为10mol
4
C.反应II中氧化剂与还原剂的物质的量之比为1∶3
D.若反应I和反应II中消耗的KMnO 的物质的量相同,则反应I和反应II中消耗的还原剂的物质的量之
4
比为2∶3
6.(天津市和平区2022~2023学年高三3月模拟)在特定碱性条件下,过量HO 可将Cr(Ⅲ)完全氧化成Cr
2 2
(Ⅵ),其反应为HO+CrO-+2OH- W+Y(未配平),下列有关说法错误的是( )。
2 2 2
A.W为OH-
B.上述反应中氧化剂和还原剂的物质的量之比为3∶2
C.1mol HO 参加反应时,转移电子的物质的量为2mol
2 2
D.在酸性条件下Cr O2-可以转化为CrO2-
2 7 4
7.(2023·南阳模拟)含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co O+6ClF
3 4 3
6CoF+3Cl+4X。下列有关该反应的说法正确的是( )。
3 2
A.X是还原产物
B.ClF 中氯元素为-3价
3
C.反应生成3molCl 时转移18mol电子
2
D.Co O 在反应中作氧化剂
3 4
8.(2023·芜湖高三模拟)测定某溶液中甲醇含量的部分过程如下:①KMnO 溶液处理:CHOH+MnO -
4 3 4
+X→CO2-+MnO 2-+H O(未配平,下同)②酸化处理:MnO 2-+H+→MnO ↓+MnO -+H O下列说法错误的是
3 4 2 4 2 4 2
( )。
A.“反应①”中X为OH-,配平后计量系数为8
B.“反应①”中氧化性:MnO ->CO2-
4 3
C.“反应②”中,可用盐酸进行酸化
D.“反应②”消耗71.4g MnO 2-时,反应中转移0.4mole-
4
9.(2023·芜湖高三模拟)测定某溶液中甲醇含量的部分过程如下:①KMnO 溶液处理:CHOH+MnO -
4 3 4
+X→CO2-+MnO 2-+H O(未配平,下同)②酸化处理:MnO 2-+H+→MnO ↓+MnO -+H O下列说法错误的是
3 4 2 4 2 4 2
( )。
A.“反应①”中X为OH-,配平后计量系数为8
B.“反应①”中氧化性:MnO ->CO2-
4 3
C.“反应②”中,可用盐酸进行酸化
D.“反应②”消耗71.4g MnO 2-时,反应中转移0.4mole-
4
10.把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平)。
对该氧化还原反应型离子方程式,说法不正确的是( )。
A.IO -作氧化剂具有氧化性
4
B.氧化剂和还原剂的物质的量之比为5∶2
C.若有2molMn2+参加反应时则转移10mol电子
D.氧化性:MnO ->IO -
4 4
11.氧化还原反应在工业生产、环保及科研中有广泛的应用,请根据以上信息,结合自己所掌握的化学知识,
回答下列问题:
Ⅰ.氢化亚铜(CuH)是一种难溶物质,用CuSO 溶液和“另一物质”在40~50℃时反应可生成CuH。CuH具
4
有的性质:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是
2Cu+ Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学方程式:_________________________。
(2)CuH溶解在稀盐酸中生成的气体是__________(填化学式)。
资料收集整理【淘宝店铺:向阳百分百】(3)将CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
____________________。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(4)将废钒催化剂(主要成分VO)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的
2 5
化学方程式是_______________。
(5)VO 能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与NaSO 溶液反应而被吸收,则SO 2-、Cl-、
2 5 2 3 3
VO2+还原性由强到弱的顺序是_______________。
12.酸性KMnO 、HO 在生活、卫生医疗中常用作消毒剂,其中HO 还可用于漂白,是化学实验室里必备的
4 2 2 2 2
重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(HC O)去除,Fe(NO ) 也是重要的氧化试剂,下
2 2 4 3 3
面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入HO 后,铜片溶解,写出该反应的离子方程式
2 2
_______________________,氧化产物与还原产物的物质的量之比为______。
(2)取300mL0.2mol·L-1的KI溶液与一定量的酸性KMnO 溶液恰好反应,生成等物质的量的I 和KIO ,则转
4 2 3
移电子的物质的量是_____mol。
(3)在Fe(NO ) 溶液中加入NaSO 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为
3 3 2 3
浅绿色的原因是_______________________________(用文字表达),又变为棕黄色的离子方程式是
____________________________。
(4)测定KMnO 样品的纯度可用标准NaSO 溶液进行滴定,取0.474gKMnO 样品溶解酸化后,用
4 2 2 3 4
0.100mol·L-1标准NaSO 溶液进行滴定,标准NaSO 溶液应盛装在____________(填“酸式”或“碱式”)
2 2 3 2 2 3
滴定管中。配平上述反应的离子方程式:
___MnO -+___SO2-+____H+=____Mn2++_____SO 2-+____HO
4 2 3 4 2
实验中,滴定至终点时消耗NaSO 溶液12.00mL,则该样品中KMnO 的物质的量是_________________。
2 2 3 4
【能力提升】
1.(2023·宁德模拟)SO 气体与足量Fe (SO ) 溶液完全反应后,再加入KCr O 溶液,发生如下化学反应:
2 2 4 3 2 2 7
①SO +2Fe3++2H O SO 2-+2Fe2++4H+;②Cr O2-+6Fe2++14H+ 2Cr3++6Fe3++7H O。则下列有关说法不正确
2 2 4 2 7 2
的是( )。
A.氧化性:Cr O2->Fe3+
2 7
B.标准状况下,若有6.72LSO 参加反应,则最终消耗0.2molKCr O
2 2 2 7
C.反应②中,每有1molK Cr O 参加反应,转移电子6mol
2 2 7
D.由上述反应原理推断,KCr O 可以将NaSO 氧化成NaSO
2 2 7 2 3 2 4
2.(2023·张家口模拟)黄铁矿(FeS)中-1价硫元素在酸性条件下可以与ClO -发生反应,其离子方程式如
2 3
下(未配平):
__ClO -+__FeS +___H+ __ClO ↑+__Fe3++__SO2-+__H O
3 2 2 4 2
下列说法正确的是( )。
A.ClO -是氧化剂,Fe3+是还原产物
3
B.ClO -的氧化性强于Fe3+
3
C.生成lmolSO 2-时,转移7mol电子
4
D.向反应后的溶液加KSCN溶液,可观察到有红色沉淀产生
3.(2022~2023学年太原高三上学期模拟)处理含氰(CN-)废水可以用以下两种方法:
Ⅰ:ClO-+CN-+OH- CO2-+A+Cl-+H O(未配平),其中A为参与大气循环的气体
3 2
Ⅱ:①CN-+OH-+Cl OCN-+Cl-+H O(未配平)
2 2
②2OCN-+4OH-+3Cl 2CO+N +6Cl-+2H O
2 2 2 2
下列说法正确的是( )。
A.ClO-和CN-的电子式分别为 、
B.方法Ⅰ中,每生成1mol A,转移6N 个电子
A
C.方法Ⅱ中,CO 是反应②的氧化产物
2
D.方法Ⅱ的反应①中,CN-与Cl 的物质的量之比为1∶1
2
4.(2022~2023学年河南三门峡12月模拟)已知:
Ⅰ.高锰酸钾在不同条件下发生的反应如下:
MnO ﹣+5e-+8H+ Mn2++4H O
4 2
MnO ﹣+3e-+2H O MnO ↓+4OH-
4 2 2
MnO ﹣+e- MnO 2﹣(溶液呈绿色)
4 4
Ⅱ.在下列反应中,产物KSO 和S的物质的量之比为3∶2
2 4
____KMnO +____K S+____ ____KMnO +____K SO +____S↓+____
4 2 2 4 2 4
下列说法不正确的是( )。
A.高锰酸根离子被还原的产物受溶液酸碱性的影响
B.化学方程式中反应物缺项为HSO ,配平后系数为12
2 4
资料收集整理【淘宝店铺:向阳百分百】C.化学方程式中产物缺项为HO,配平后系数为12
2
D.用石墨电极电解中性高锰酸钾溶液,在阴极可以得到MnO
2
5.(湖湘教育三新探索协作体2022年11月期中联考)已知反应:
①5V2++MnO-+8H+=Mn2++5V3++4H O
4 2
②5V3++MnO-+H O=Mn2++5VO2++2H+
4 2
③5VO2++MnO-+H O=Mn2++5VO++2H+
4 2 2
现向5L,c(V2+)=amol·L-1的溶液中不断加入一定浓度的酸性KMnO 溶液,溶液中某些离子的物质的量变化
4
如图所示,下列说法不正确的是( )。
A.AB段对应的离子为V2+
B.BC段、EF段分别对应反应②、反应③
C.原溶液中c(V2+)=2mol·L-1
D.乙点时:n(VO2+)∶n(VO +)∶n(Mn2+)=1∶1∶5
2
6.(2022年湖南衡阳高三3月模拟)一定温度下,PbO 完全分解为Pb O、PbO混合物(Pb O 中Pb为+2、+4
2 3 4 3 4
价)和O,向所得固体混合物中加入足量浓盐酸加热生成Cl,同时得到酸性PbCl 溶液。下列说法错误的是(
2 2 2
)。
A.氧化性:PbO >PbO>Cl
2 2
B.O 与Cl 的物质的量可能相等
2 2
2
C.受热分解过程中,超过3的PbO 表现氧化性
2
D.若生成1mol Cl,则参加反应的PbO 大于3mol
2 2
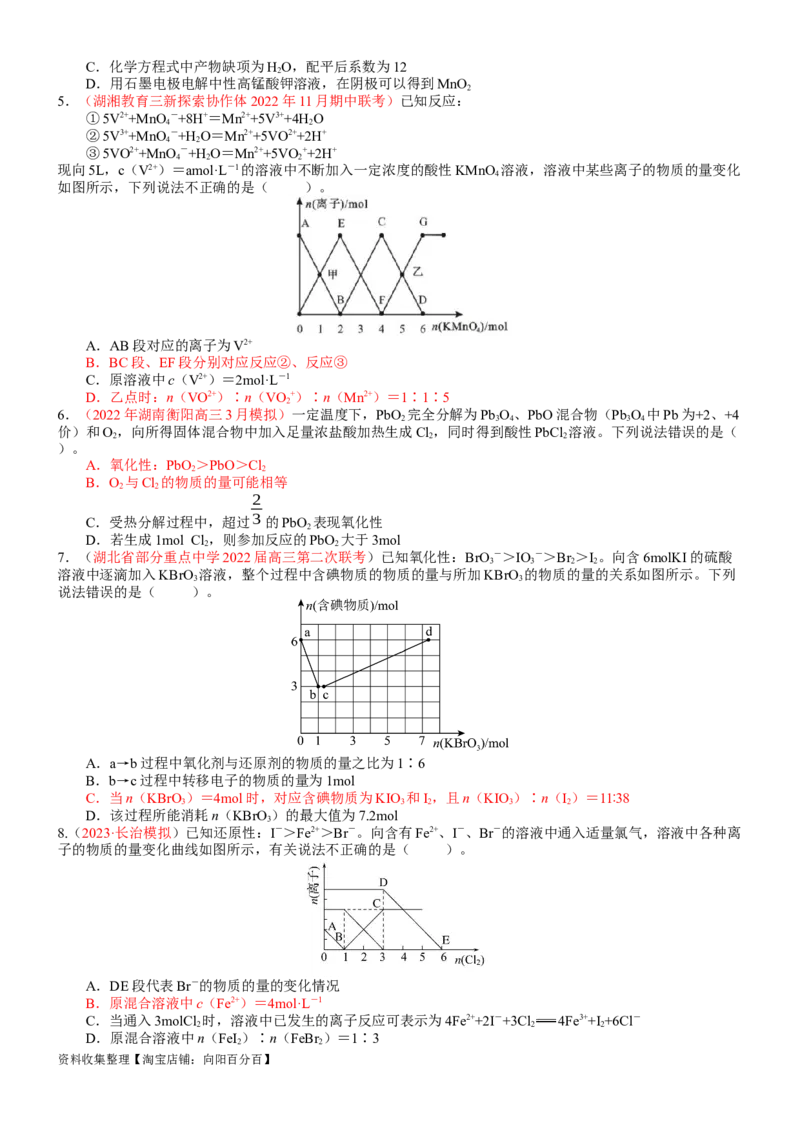
7.(湖北省部分重点中学2022届高三第二次联考)已知氧化性:BrO->IO ->Br >I。向含6molKI的硫酸
3 3 2 2
溶液中逐滴加入KBrO 溶液,整个过程中含碘物质的物质的量与所加KBrO 的物质的量的关系如图所示。下列
3 3
说法错误的是( )。
A.a→b过程中氧化剂与还原剂的物质的量之比为1∶6
B.b→c过程中转移电子的物质的量为1mol
C.当n(KBrO)=4mol时,对应含碘物质为KIO 和I,且n(KIO)∶n(I)=11∶38
3 3 2 3 2
D.该过程所能消耗n(KBrO)的最大值为7.2mol
3
8.(2023·长治模拟)已知还原性:I->Fe2+>Br-。向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离
子的物质的量变化曲线如图所示,有关说法不正确的是( )。
A.DE段代表Br-的物质的量的变化情况
B.原混合溶液中c(Fe2+)=4mol·L-1
C.当通入3molCl 时,溶液中已发生的离子反应可表示为4Fe2++2I-+3Cl 4Fe3++I +6Cl-
2 2 2
D.原混合溶液中n(FeI)∶n(FeBr )=1∶3
2 2
资料收集整理【淘宝店铺:向阳百分百】