文档内容
考点 05 氧化还原反应
(核心考点精讲)
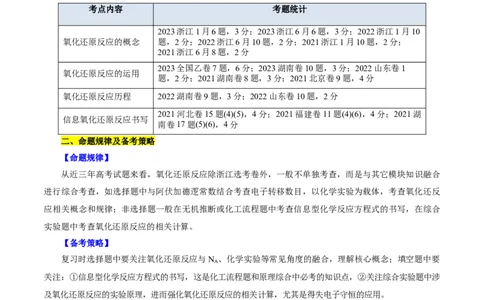
一、3年真题考点分布
考点内容 考题统计
2023浙江1月6题,3分;2023浙江6月6题,3分;2022浙江1月10
氧化还原反应的概念 题,2分;2022浙江6月10题,2分;2021浙江1月10题,2分;
2021浙江6月8题,2分
2023全国乙卷7题,6分;2023湖南卷10题,3分;2022山东卷1
氧化还原反应的运用
题,2分;2021湖南卷8题,3分;2021北京卷9题,4分
氧化还原反应历程 2022湖南卷9题,3分;2022山东卷10题,2分
2021河北卷15题(4)(5),4分;2021福建卷11题(4)(6),4分;2021湖
信息氧化还原反应书写
南卷17题(5)(6),4分
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,氧化还原反应除浙江选考卷外,一般不单独考查,而是与其它模块知识融合
进行综合考查,如选择题中与阿伏加德逻常数结合考查电子转移数目,以化学实验为载体,考查氧化还反
应相关概念和规律;非选择题一般在无机推断或化工流程题中考查信息型化学反应方程式的书写,在综合
实验题中考查氧化还原反应的相关计算。
【备考策略】
复习时选择题中要关注氧化还原反应与N 、化学实验等常见角度的融合,理解核心概念;填空题中要
A
关注:①信息型化学反应方程式的书写,这是化工流程题和原理综合中必考的知识点,②关注综合实验题中涉
及氧化还原反应的实验原理,进而强化氧化还原反应的相关计算,尤其是得失电子守恒的应用。
【命题预测】
预测2024年高考中,氧化还原反应在高考中考查形式有:(1)出现在阿伏伽德罗常数的正误判断中;
(2)出现在离子共存问题中;(3)出现在离子方程式的正误判断中;(4)出现在简答题中根据信息书写化学方
程式,能力要求高,难度较大。
考法 1 氧化还原反应的概念
资料收集整理【淘宝店铺:向阳百分百】1.氧化还原反应的本质和特征
2.基于双线桥理解氧化还原反应概念之间的关系
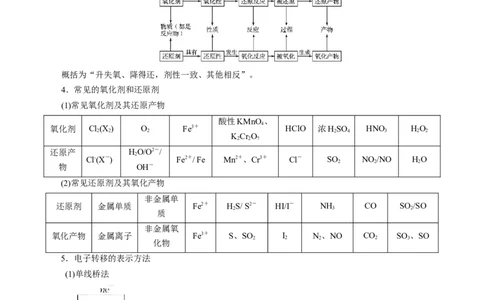
概括为“升失氧、降得还,剂性一致、其他相反”。
4.常见的氧化剂和还原剂
(1)常见氧化剂及其还原产物
酸性KMnO 、
4
氧化剂 Cl(X ) O Fe3+ HClO 浓HSO HNO HO
2 2 2 2 4 3 2 2
KCr O
2 2 7
还原产 HO/O2-/
2
Cl-(X-) Fe2+/ Fe Mn2+、Cr3+ Cl- SO NO /NO HO
2 2 2
物 OH-
(2)常见还原剂及其氧化产物
非金属单
还原剂 金属单质 Fe2+ HS/ S2- HI/I- NH CO SO /SO
2 3 2
质
非金属氧
氧化产物 金属离子 Fe3+ S、SO I N、NO CO SO 、SO
2 2 2 2 3
化物
5.电子转移的表示方法
(1)单线桥法
如:
(2)双线桥法
资料收集整理【淘宝店铺:向阳百分百】如:
1.常见元素的化合价可以借助化合价口诀来记忆:
一价氢、钾、钠、氟、氯、溴、碘、银;二价氧、钙、钡、镁、锌;三铝、四硅、五价磷;说变价也
不难,二三铁、二四碳、二四六硫都齐全;铜汞二价最常见。
2.近几年高考中一些特殊物质中元素化合价判断
CuFeS Cu + 2 Fe + 2 S - 2 KFeO Fe + 6
2 2 4
LiNH N - 3 LiNH N - 3 AlN N - 3
2 2
NaSO S + 2 MO M + 5 C O C + 3
2 2 3 2
HCN C + 2 N - 3 CuH Cu + 1 H - 1
FeO Fe + ( 8 - n ) Si N Si + 4 N - 3
3 4
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)有单质参加或有单质生成的化学反应一定是氧化还原反应( )
(2)金属阳离子一定只具有氧化性( )
(3)氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原( )
(4)氧化还原反应中的反应物,不是氧化剂就是还原剂( )
(5)某元素从游离态变为化合态,该元素可能被氧化也可能被还原( )
(6)水做还原剂时,产物中一般有O( )
2
(7)NO 溶于水发生氧化还原反应( )
2
(8)硝酸铜的分解产物可能是CuO、NO、NO ( )
2
(9)NaHCO +H===HCOONa+HO的反应中,NaHCO 被氧化( )
3 2 2 3
(10)Na O 与水的反应中,水是还原剂( )
2 2
(11)有单质参加的化合反应或有单质生成的分解反应一定是氧化还原反应( )
(12)在氧化还原反应中,还原剂失去电子的总数等于氧化剂得到电子的总数( )
(13)生产生活中使用的非金属单质都是通过氧化还原反应制得的( )
(14)在化学反应中,得电子越多的氧化剂,其氧化性就越强( )
答案:(1)× (2)× (3)× (4)× (5) √ (6) √ (7) √ (8)× (9)× (10)× (11) √ (12) √ (13)× (14)×
例1 (2023·浙江省天域全国名校协作体高三联考)火箭推进发生反应的化学方程式为:
资料收集整理【淘宝店铺:向阳百分百】C NH+2N O=2CO ↑+3N ↑+4H O (偏二甲肼中C、N元素的化合价相等)。下列说法正确的是( )
2 2 8 2 4 2 2 2
A.C NH 是氧化剂 B.NO 被氧化
2 2 8 2 4
C.氧化产物与还原产物之比为3∶2 D.NO 完全反应,有8N 个电子转移
2 4 A
【答案】C
【解析】A项,反应过程中C NH 中碳元素化合价升高,反应氧化反应,C NH 为还原剂,A错误;
2 2 8 2 2 8
B项,NO 中氮元素化合价降低得到氮气,发生还原反应被还原,B错误;C项,1分子C NH 中碳、氮
2 4 2 2 8
被氧化生成2分子二氧化碳和1分子氮气,NO 中氮元素化合价降低被还原生成2分子氮气,故氧化产物
2 4
与还原产物之比为3∶C正确;D项,反应中不确定NO 反应的量,故无法判断电子转移的量,D错误;
2 4
故选C。
例2 (2023·上海市宝山区一模)氨基钠(NaNH )是重要的化学试剂,其与氧气的反应如下:4
2
NaNH +3O = 2NaOH+2 NaNO +2NH。下列说法正确的是( )
2 2 2 3
A.n(氧化剂):n(还原剂)=3:4
B.每消耗0.3molO,转移电子数是2.4 N
2 A
C.NH 是氧化产物
3
D.NaNH 中N的化合价部分发生变化
2
【答案】D
【解析】A项,由化学方程式可知,3molO 中所含氧元素化合价降低,作氧化剂,4mol NaNH 中,只
2 2
有2mol NaNH 所含氮元素化合价升高,作还原剂,则n(氧化剂):n(还原剂)=3:2,A错误;B项,由化学
2
方程式可知,每消耗3molO ,反应转移12mol电子,则每消耗0.3molO,转移1.2mol电子,转移电子数是
2 2
1.2N ,B错误;C项,生成物NH 中的N和H元素,反应前后化合价无变化,则NH 既不是氧化产物也
A 3 3
不是还原产物,C错误;D项,NaNH →NaNO ,N元素化合价升高,NaNH →NH ,N元素化合价不变,
2 2 2 3
即NaNH 中N的化合价部分发生变化,D正确;故选D。
2
对点1 高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,反应方程式如下:KMnO +FeSO+H SO
4 4 2 4
KSO +MnSO +Fe (SO )+H O(未配平)。下列说法正确的是( )。
2 4 4 2 4 3 2
A.Fe2+的还原性强于Mn2+
B.MnO -是氧化剂,Fe3+是还原产物
4
C.氧化剂和还原剂物质的量之比为5∶1
D.生成1 mol水时,转移2.5 mol电子
【答案】A
【解析】Fe2+化合价升高,是还原剂,Mn2+是还原产物,还原性:还原剂>还原产物,A项正确;
MnO -中Mn元素的化合价降低,是氧化剂,Fe3+是氧化产物,B项错误;锰元素由+7价降至+2价,铁元素
4
资料收集整理【淘宝店铺:向阳百分百】由+2价升至+3价,根据得失电子守恒可知,MnO -、Mn2+的系数为1,Fe2+、Fe3+的系数为5,由电荷守恒
4
得H+的系数为8,则HO的系数为4,所以离子方程式为MnO -+5Fe2++8H+=Mn2++5Fe3++4H O,由此可知氧
2 4 2
化剂和还原剂物质的量之比为1∶5,C项错误;根据离子方程式MnO -+5Fe2++8H+=Mn2++5Fe3++4H O可知,
4 2
生成4 mol水时转移5 mol电子,则生成1 mol水时,转移1.25 mol电子,D项错误。
对点2 过氧化钠具有强氧化性,遇亚铁离子可将其氧化为一种常见的高效水处理剂,化学方程式为
2FeSO +6Na O=2Na FeO+2Na O+2Na SO +O ↑。下列说法中不正确的是( )。
4 2 2 2 4 2 2 4 2
A.氧化性:NaO>Na FeO>FeSO
2 2 2 4 4
B.FeSO 只作还原剂,NaO 既作氧化剂,又作还原剂
4 2 2
C.由反应可知每3 mol FeSO 完全反应时,反应中共转移12 mol电子
4
D.NaFeO 处理水时,不仅能杀菌消毒,还能起到净水的作用
2 4
【答案】C
【解析】由氧化剂的氧化性强于氧化产物可知,氧化性 NaO>Na FeO>FeSO ,A 项正确;
2 2 2 4 4
2FeSO +6Na O=2Na FeO+2Na O+2Na SO +O ↑,Fe元素的化合价由+2升高为+6,O元素的化合价部分
4 2 2 2 4 2 2 4 2
由-1降低为-2,部分由-1升高为0,所以FeSO 只作还原剂,NaO 既作氧化剂又作还原剂,B项正确;
4 2 2
2FeSO ~10e-,所以每3 mol FeSO 完全反应时,反应中共转移15 mol电子,C项错误;NaFeO 处理水时,
4 4 2 4
NaFeO 可以氧化杀死微生物,生成的还原产物氢氧化铁又具有吸附作用,可以起到净水的作用,D项正
2 4
确。
考法 2 氧化还原反应强弱规律
氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。如:Na-e-
===Na+,Al-3e-===Al3+,但根据金属活动性顺序表,Na比Al活泼,更易失去电子,所以Na比Al的还
原性强。
1.依据氧化还原反应方程式判断
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
口诀:比什么“性”找什么“剂”,“产物”之“性”小于“剂”。
2.依据反应条件及反应的剧烈程度判断
当不同的氧化剂(或还原剂)与同一还原剂(或氧化剂)反应时,反应越易进行,则对应的氧化剂(或还原
剂)的氧化性(或还原性)越强,反之越弱。如:
MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
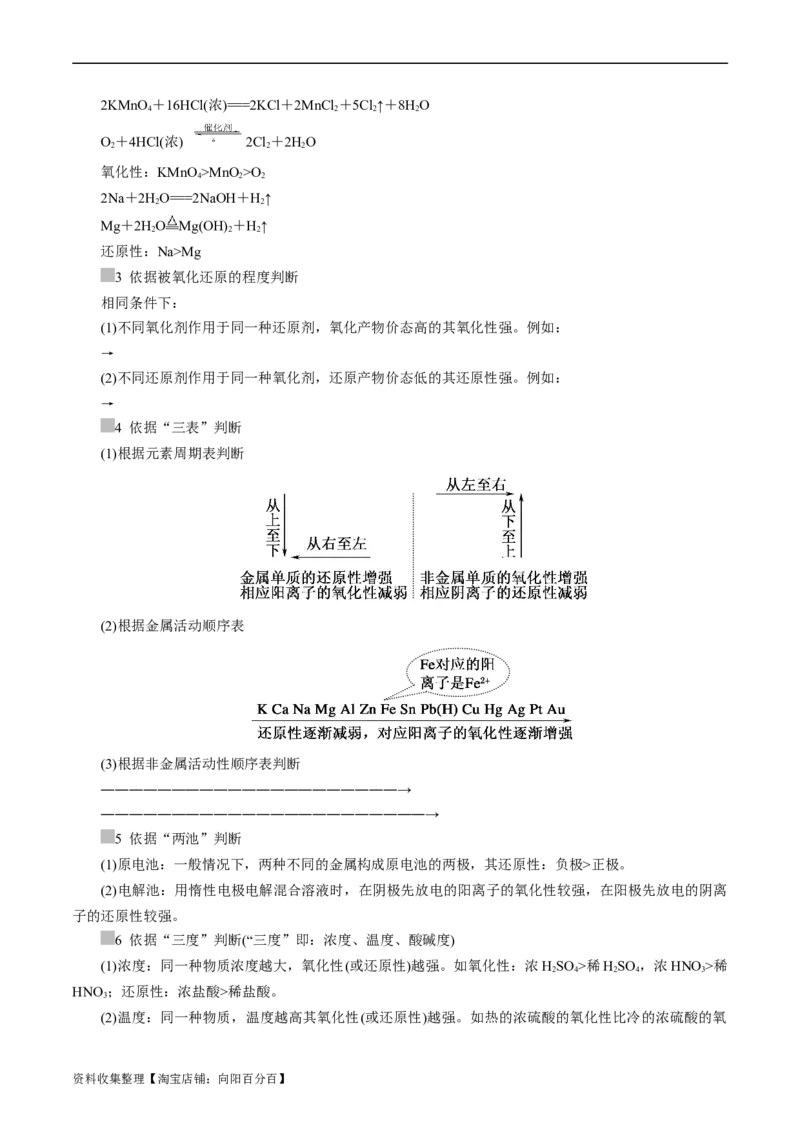
资料收集整理【淘宝店铺:向阳百分百】2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
O+4HCl(浓) 2Cl+2HO
2 2 2
氧化性:KMnO >MnO>O
4 2 2
2Na+2HO===2NaOH+H↑
2 2
Mg+2HO Mg(OH) +H↑
2 2 2
还原性:Na>Mg
3 依据被氧化还原的程度判断
相同条件下:
(1)不同氧化剂作用于同一种还原剂,氧化产物价态高的其氧化性强。例如:
→
(2)不同还原剂作用于同一种氧化剂,还原产物价态低的其还原性强。例如:
→
4 依据“三表”判断
(1)根据元素周期表判断
(2)根据金属活动顺序表
(3)根据非金属活动性顺序表判断
―――――――――――――――――――――→
―――――――――――――――――――――――→
5 依据“两池”判断
(1)原电池:一般情况下,两种不同的金属构成原电池的两极,其还原性:负极>正极。
(2)电解池:用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电的阴离
子的还原性较强。
6 依据“三度”判断(“三度”即:浓度、温度、酸碱度)
(1)浓度:同一种物质浓度越大,氧化性(或还原性)越强。如氧化性:浓HSO >稀HSO ,浓HNO>稀
2 4 2 4 3
HNO;还原性:浓盐酸>稀盐酸。
3
(2)温度:同一种物质,温度越高其氧化性(或还原性)越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧
资料收集整理【淘宝店铺:向阳百分百】化性强。
(3)酸碱度:同一种物质,所处环境酸(碱)性越强其氧化性(或还原性)越强。如KMnO 溶液的氧化性随
4
溶液酸性的增强而增强。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)强氧化剂与强还原剂混合不一定能发生氧化还原反应( )
(2)阳离子只有氧化性,阴离子只有还原性( )
(3)元素的非金属性越强,其氧化性越强,相应单质越活泼( )
(4)难失电子的物质一定易得电子( )
(5)含有最高价元素的化合物一定具有强氧化性( )
(6)MnO 不与稀盐酸反应是因为H+浓度小( )
2
(7)V 可以防止亚铁离子转化成三价铁离子,主要原因是V 具有较强的还原性( )
C C
(8)向FeSO 溶液中先滴入KSCN溶液,再滴加HO 溶液,加入HO 后溶液变成红色,则Fe2+既有氧
4 2 2 2 2
化性又有还原性( )
(9)在CO 中,Mg燃烧生成MgO和C,在该反应条件下,Mg的还原性强于C的还原性( )
2
答案:(1) √ (2)× (3)× (4)× (5) × (6) × (7) √ (8)× (9) √
资料收集整理【淘宝店铺:向阳百分百】