考点 25 化学反应速率与平衡图象
识图是化学反应速率和化学平衡的难点,图像、数据信息是高考考查难点和区分点,高考通过信息给
予多样化,往往根据工业生产实际,并结合陌生图象,分析投料比、转化率、产率的变化,考查接受、加
工、同化新信息能力。
预计2023年的高考仍然会以考查化学平衡图象为切入点。从近几年高考看,选择有机反应、溶液中进
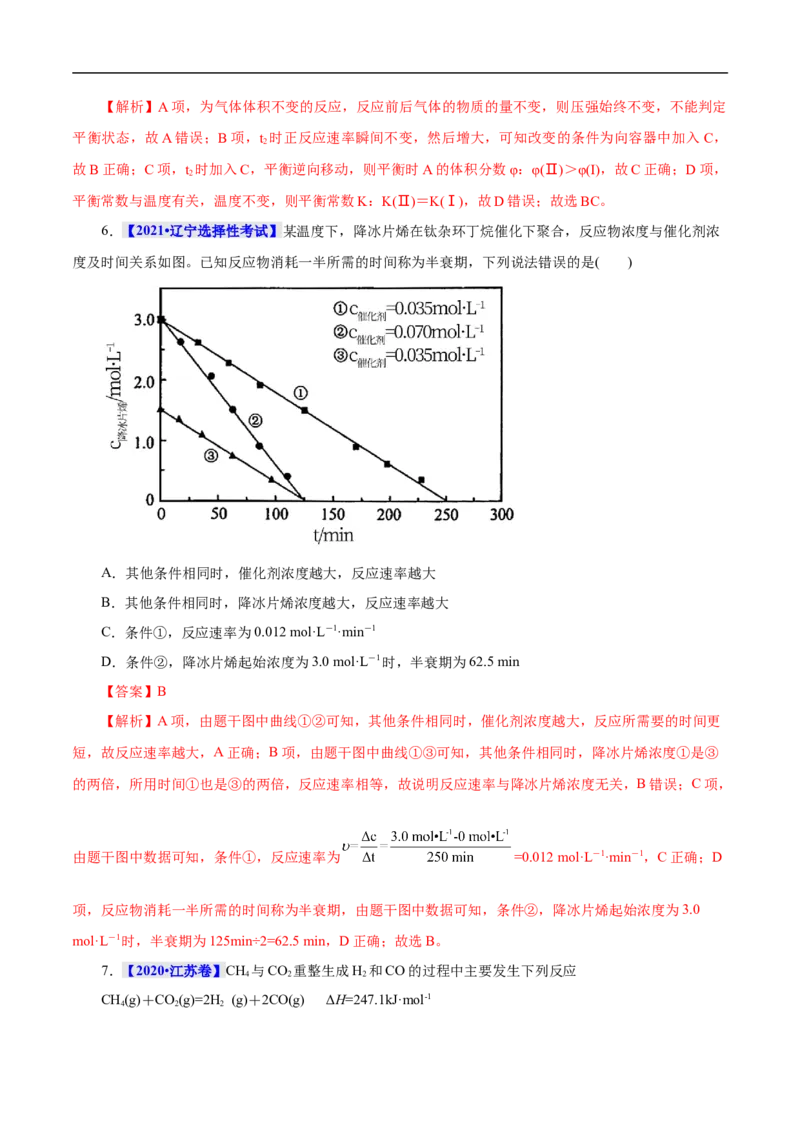
行的反应考查化学平衡问题成为命题热点,尤其是化学平衡图象的绘制,应此起关注。
一、化学反应速率图象
二、化学平衡图象
化学反应速率图象
化学反应速率图像
以反应mA(g)+nB(g) pC(g)+qD(g) ΔH>0为例。反应速率-时间(v-t)图像中,在平衡后的某时刻t 改
1
变某一条件后,v(正)与v(逆)的变化有两种情况:
(1)v(正)、v(逆)同时突变(2)v(正)、v(逆)之一渐变
【典例】
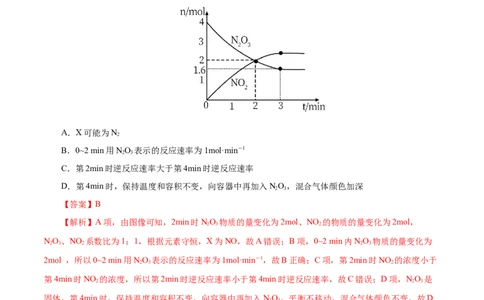
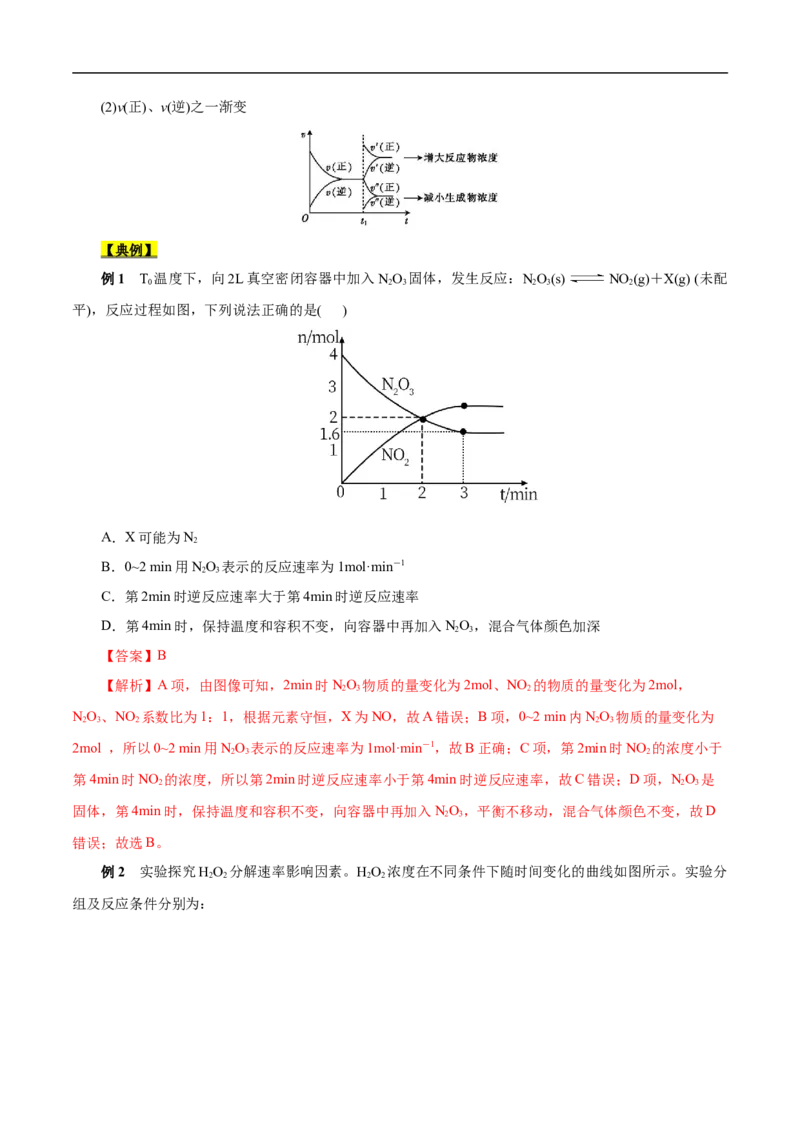
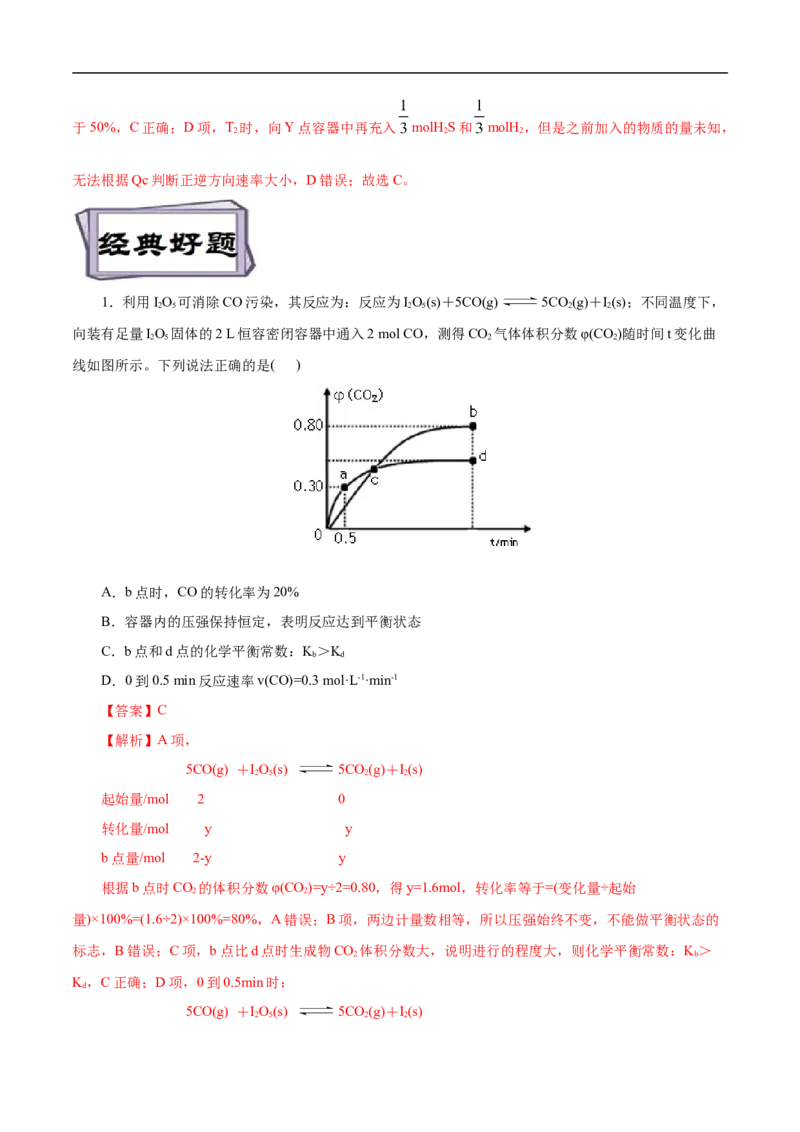
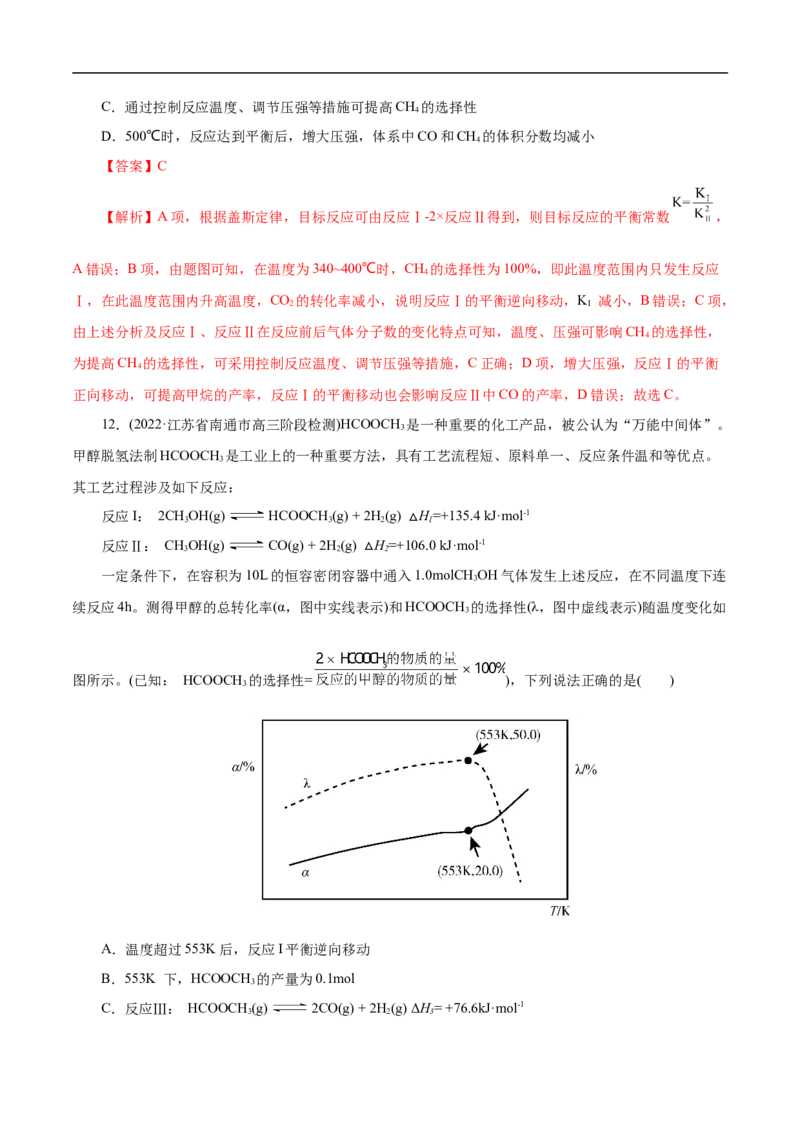
例1 T 温度下,向2L真空密闭容器中加入NO 固体,发生反应:NO(s) NO (g)+X(g) (未配
0 2 3 2 3 2
平),反应过程如图,下列说法正确的是( )
A.X可能为N
2
B.0~2 min用NO 表示的反应速率为1mol·min-1
2 3
C.第2min时逆反应速率大于第4min时逆反应速率
D.第4min时,保持温度和容积不变,向容器中再加入NO,混合气体颜色加深
2 3
【答案】B
【解析】A项,由图像可知,2min时NO 物质的量变化为2mol、NO 的物质的量变化为2mol,
2 3 2
NO、NO 系数比为1:1,根据元素守恒,X为NO,故A错误;B项,0~2 min内NO 物质的量变化为
2 3 2 2 3
2mol ,所以0~2 min用NO 表示的反应速率为1mol·min-1,故B正确;C项,第2min时NO 的浓度小于
2 3 2
第4min时NO 的浓度,所以第2min时逆反应速率小于第4min时逆反应速率,故C错误;D项,NO 是
2 2 3
固体,第4min时,保持温度和容积不变,向容器中再加入NO,平衡不移动,混合气体颜色不变,故D
2 3
错误;故选B。
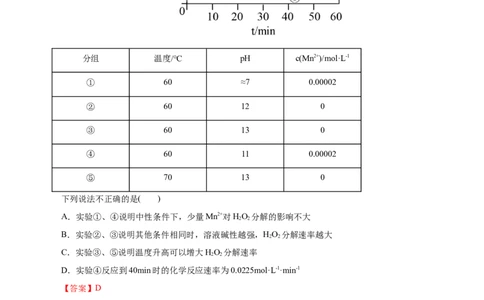
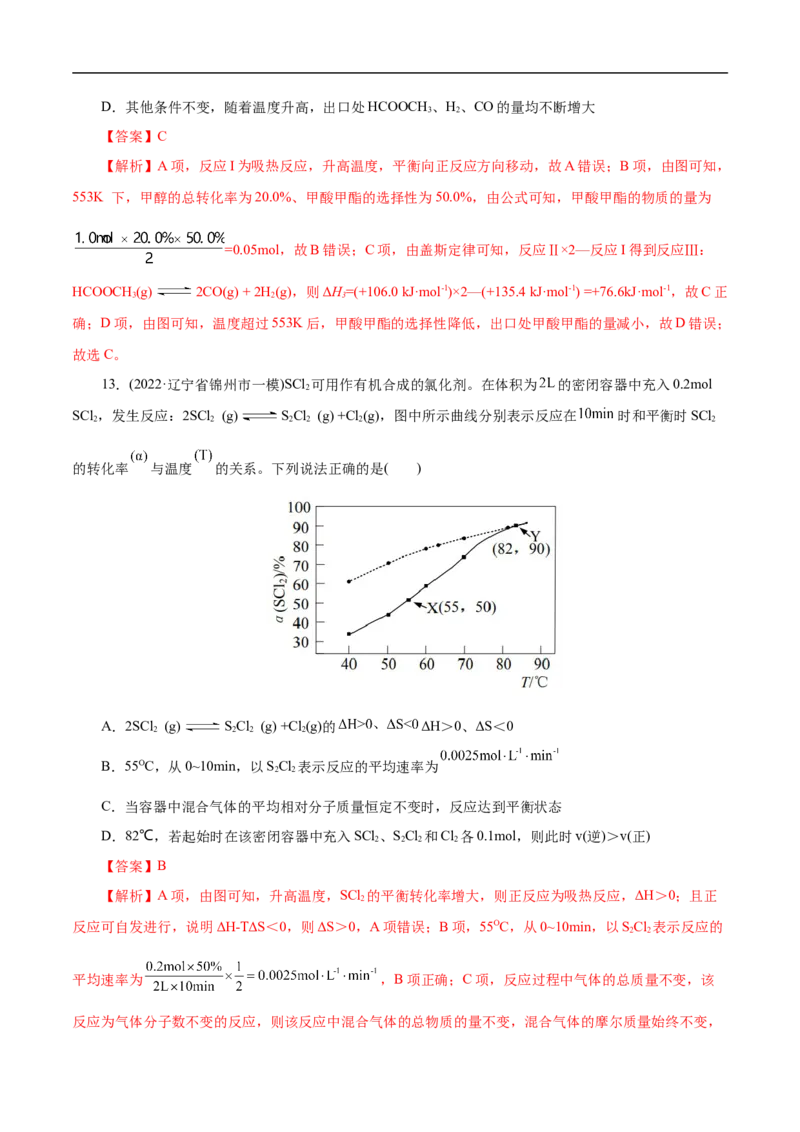
例2 实验探究HO 分解速率影响因素。HO 浓度在不同条件下随时间变化的曲线如图所示。实验分
2 2 2 2
组及反应条件分别为:分组 温度/°C pH c(Mn2+)/mol·L-1
① 60 ≈7 0.00002
② 60 12 0
③ 60 13 0
④ 60 11 0.00002
⑤ 70 13 0
下列说法不正确的是( )
A.实验①、④说明中性条件下,少量Mn2+对HO 分解的影响不大
2 2
B.实验②、③说明其他条件相同时,溶液碱性越强,HO 分解速率越大
2 2
C.实验③、⑤说明温度升高可以增大HO 分解速率
2 2
D.实验④反应到40min时的化学反应速率为0.0225mol·L-1·min-1
【答案】D
【解析】A项,实验①、④除pH外其他条件均相同,但①几乎不反应,说明中性条件下,少量
Mn2+对HO 分解的影响不大,A正确;B项,实验②、③除pH外其他条件均相同,都不添加催化剂,而
2 2
③的分解速率大于②,说明溶液碱性越强,HO 分解速率越大,B正确;C项,实验⑤中浓度低于实验③,
2 2
而温度高于③,分解速率大于③,说明温度升高可以增大HO 分解速率,C正确;D项,实验④反应到
2 2
40min时的平均速率为 =0.0225mol·L-1·min-1,由于随着反应进行,反应速率变慢,所以
40min时的瞬时速率应小于0.0225mol·L-1·min-1,D错误;故选D。【对点提升】
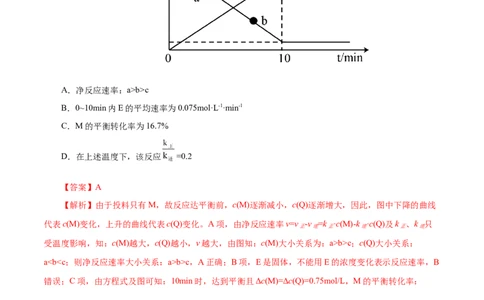
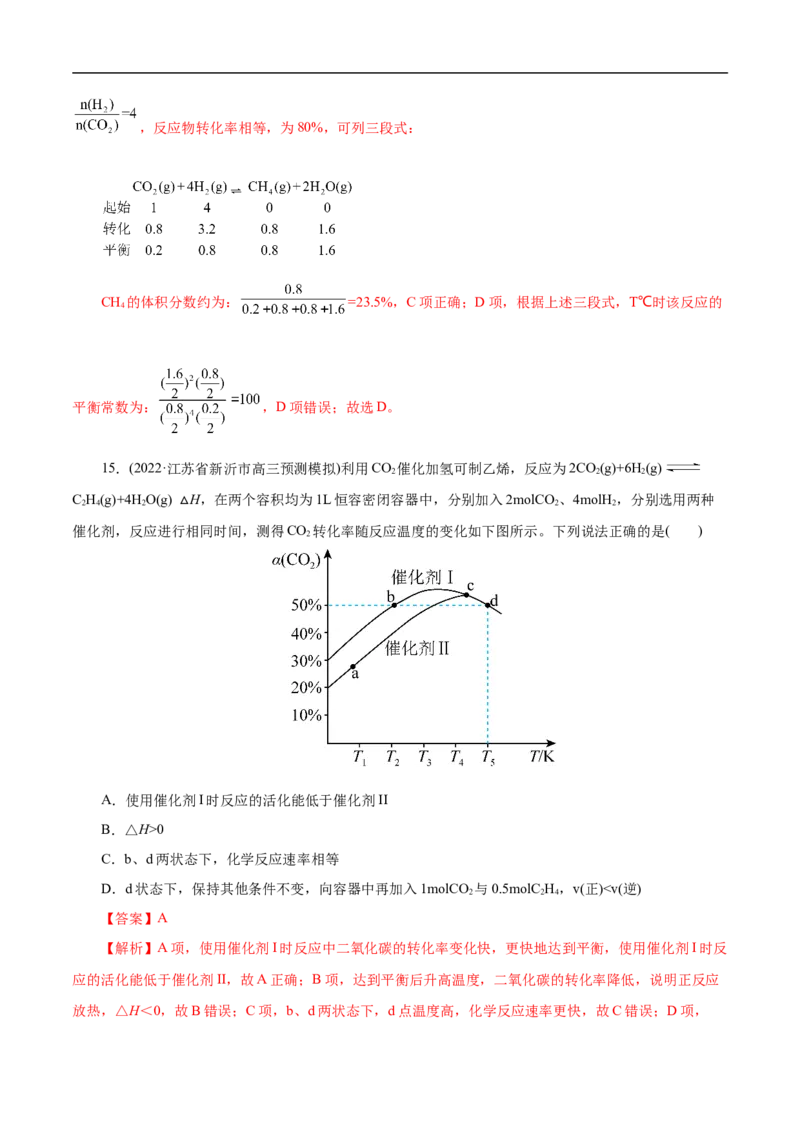
对点1 在一定温度下,在刚性密闭容器中充入一定量M发生反应:M(g) Q(g)+E(s),测得M、
Q的浓度与时间关系如图所示。已知:生成Q净反应速率v=v -v =k ·c(M)-k ·c(Q)。下列说法正确的是(
正 逆 正 逆
)
A.净反应速率:a>b>c
B.0~10min内E的平均速率为0.075mol·L-1·min-1
C.M的平衡转化率为16.7%
D.在上述温度下,该反应 =0.2
【答案】A
【解析】由于投料只有M,故反应达平衡前,c(M)逐渐减小,c(Q)逐渐增大,因此,图中下降的曲线
代表c(M)变化,上升的曲线代表c(Q)变化。A项,由净反应速率v=v -v =k ·c(M)-k ·c(Q)及k 、k 只
正 逆 正 逆 正 逆
受温度影响,知:c(M)越大,c(Q)越小,v越大,由图知:c(M)大小关系为:a>b>c;c(Q)大小关系:
a
b>c,A正确;B项,E是固体,不能用E的浓度变化表示反应速率,B
错误;C项,由方程式及图可知:10min时,达到平衡且Δc(M)=Δc(Q)=0.75mol/L,M的平衡转化率:
α(M)= ×100% = ×100%=83.3%,C错误;D项,平衡时:c(Q)=0.75mol/L,
c(M)=0.90mol/L-0.75mol/L=0.15mol/L,又平衡时,净反应速率v=0,故k ×0.15mol/L=k ×0.75mol/L,则
正 逆
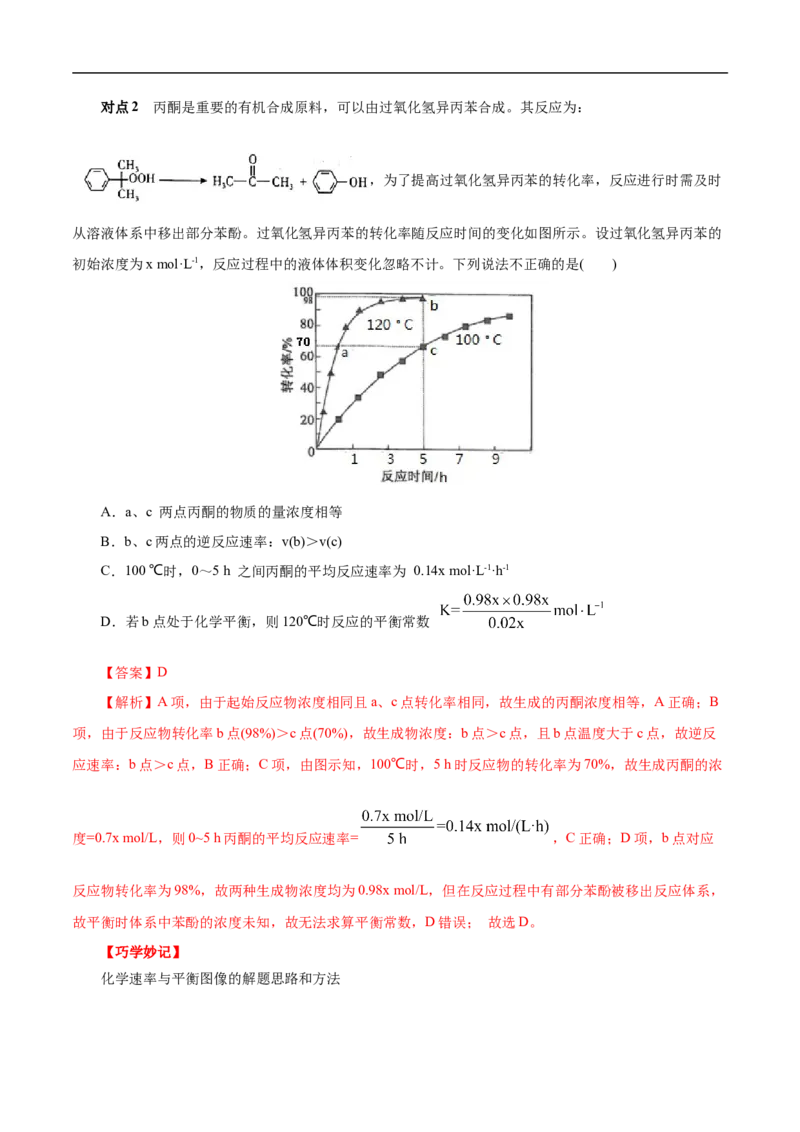
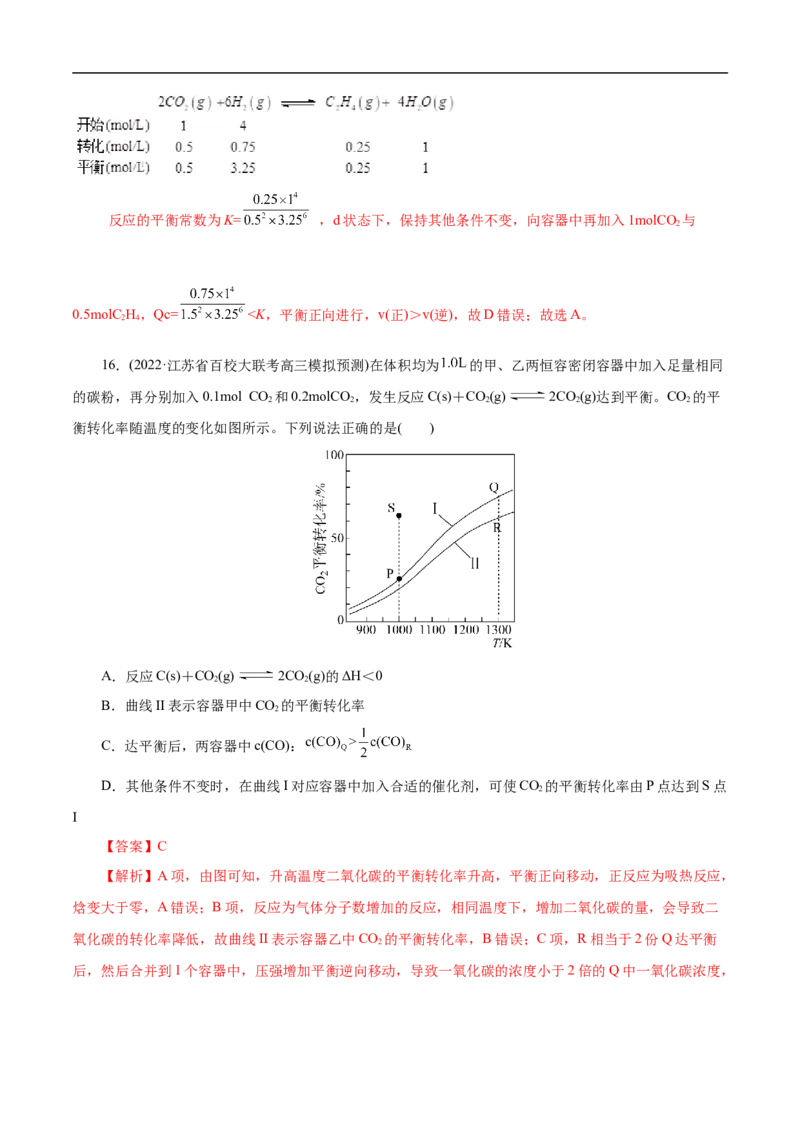
= =5,D错误;故选A。对点2 丙酮是重要的有机合成原料,可以由过氧化氢异丙苯合成。其反应为:
,为了提高过氧化氢异丙苯的转化率,反应进行时需及时
从溶液体系中移出部分苯酚。过氧化氢异丙苯的转化率随反应时间的变化如图所示。设过氧化氢异丙苯的
初始浓度为x mol·L-1,反应过程中的液体体积变化忽略不计。下列说法不正确的是( )
A.a、c 两点丙酮的物质的量浓度相等
B.b、c两点的逆反应速率:v(b)>v(c)
C.100 ℃时,0~5 h 之间丙酮的平均反应速率为 0.14x mol·L-1·h-1
D.若b点处于化学平衡,则120℃时反应的平衡常数
【答案】D
【解析】A项,由于起始反应物浓度相同且a、c点转化率相同,故生成的丙酮浓度相等,A正确;B
项,由于反应物转化率b点(98%)>c点(70%),故生成物浓度:b点>c点,且b点温度大于c点,故逆反
应速率:b点>c点,B正确;C项,由图示知,100℃时,5 h时反应物的转化率为70%,故生成丙酮的浓
度=0.7x mol/L,则0~5 h丙酮的平均反应速率= ,C正确;D项,b点对应
反应物转化率为98%,故两种生成物浓度均为0.98x mol/L,但在反应过程中有部分苯酚被移出反应体系,
故平衡时体系中苯酚的浓度未知,故无法求算平衡常数,D错误; 故选D。
【巧学妙记】
化学速率与平衡图像的解题思路和方法化学平衡图象
化学平衡图像的三种类型
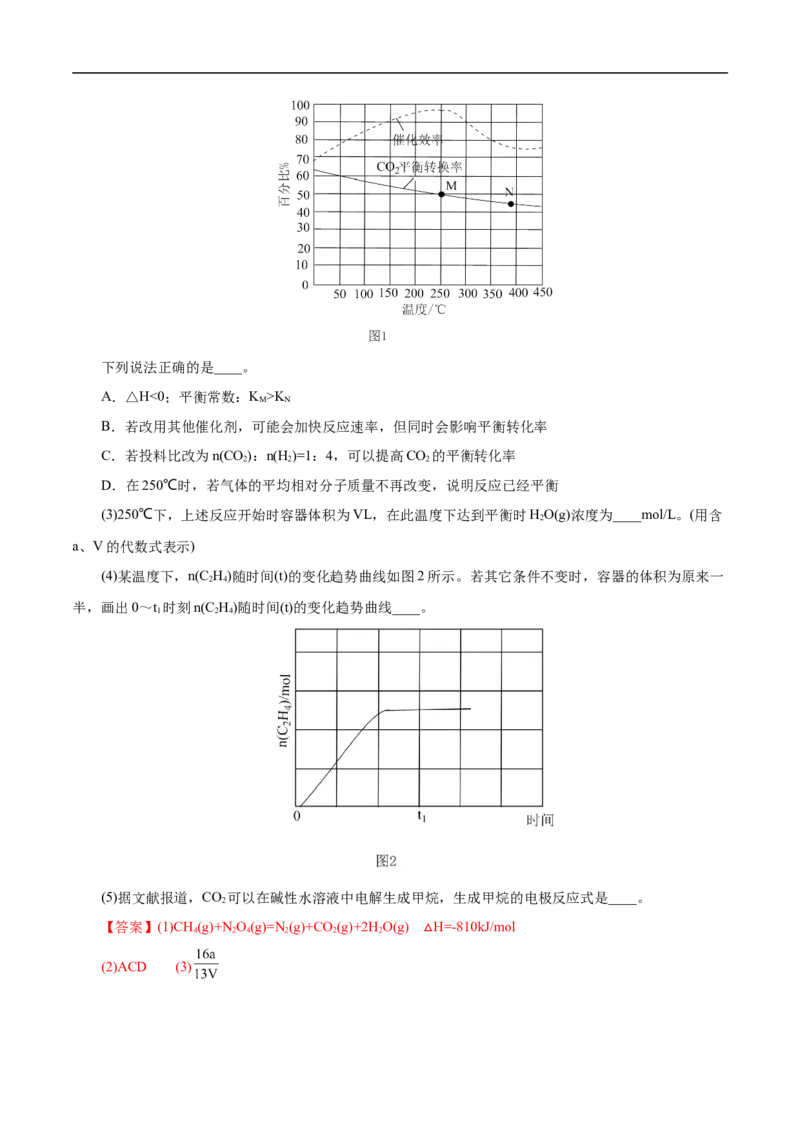
对于反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0。
(1)速率-时间图像
t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;t 时升高温度,
1 2
对任何反应,正反应和逆反应速率均增大,吸热反应的正反应速率增大较快;t 时减小压强,正反应速率
3
和逆反应速率均减小;t 时使用催化剂,正反应速率和逆反应速率同等程度增大。
4
(2)转化率(或含量)-时间图像
甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和
的反应,压强越大,反应物的转化率越大;乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,
反应物的转化率越大;丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变平
衡时反应物的转化率。(3)恒压(温)曲线
分析时可在横坐标上作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反
应的影响。
【典例】
例1 2SO (g)+O(g) 2SO (g)是工业制备硫酸的重要反应,恒温恒容条件下c(SO )随时间的变化
2 2 3 3
如图中曲线Ⅰ所示。下列说法正确的是( )
A.t~tmin,v(SO ) = mol·L-1·min-1
1 2 3 正
B.曲线Ⅱ对应的条件改变可能是增大了压强
C.工业上采用高温高压的反应条件以提高SO 的转化率
2
D.相同条件下,t 时再充入与起始投料等量的反应物,达到平衡后,SO 转化率增大
3 2
【答案】D
【解析】A项,由图中曲线Ⅰ,t~tmin内,三氧化硫的浓度变化量为(c—c),反应速率v(SO ) =
1 2 1 2 3 正
mol·L-1·min-1,故A错误;B项,若曲线Ⅱ对应的条件改变是增大了压强,则平衡正向移动,即曲线
Ⅱ条件下反应达到平衡时,三氧化硫的浓度应大于曲线Ⅰ,与题给图示不符,故B错误;C项,该反应是
放热反应,升高温度,平衡向逆反应方向移动,二氧化硫的转化率减小,故C错误;D项,相同条件下,
t 时再充入与起始投料等量的反应物相当于增大混合气体的压强,该反应是气体体积减小的反应,增大压
3
强,平衡向正反应方向移动,二氧化硫的转化率增大,故D正确;故选D。
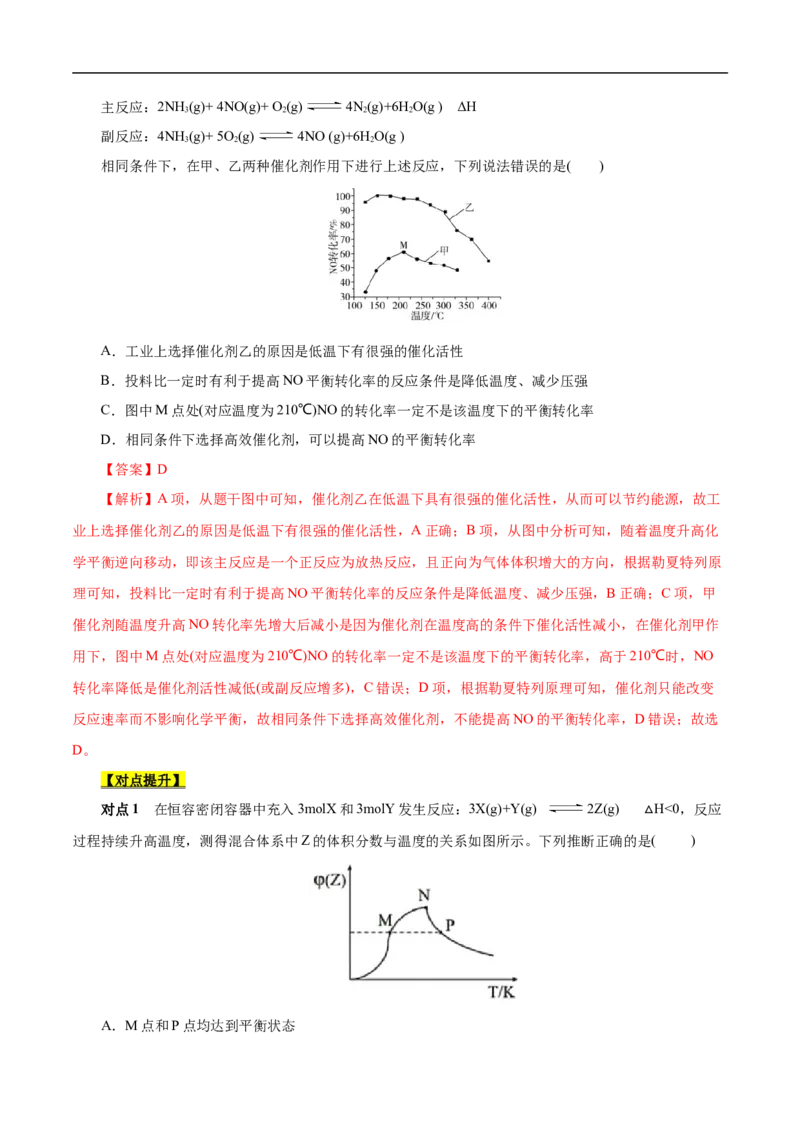
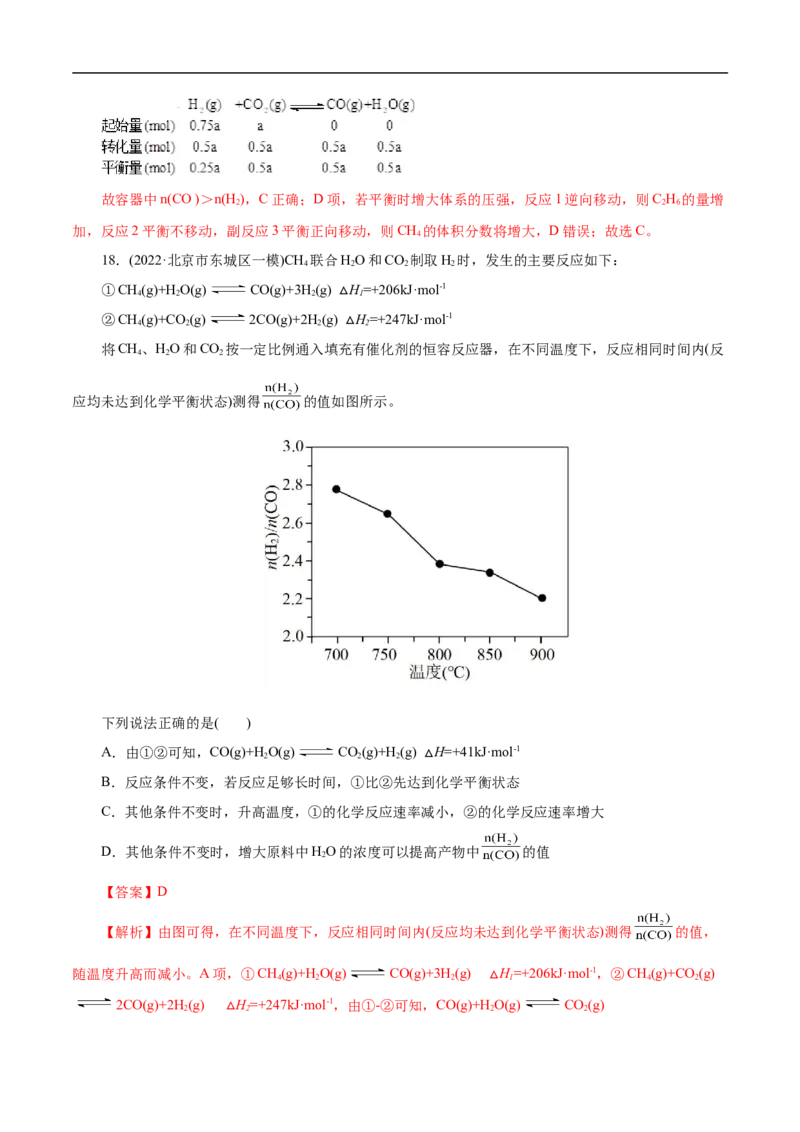
例2 SCR法是工业上消除氮氧化物的常用方法,反应如下:主反应:2NH (g)+ 4NO(g)+ O (g) 4N(g)+6HO(g ) ΔH
3 2 2 2
副反应:4NH (g)+ 5O (g) 4NO (g)+6HO(g )
3 2 2
相同条件下,在甲、乙两种催化剂作用下进行上述反应,下列说法错误的是( )
A.工业上选择催化剂乙的原因是低温下有很强的催化活性
B.投料比一定时有利于提高NO平衡转化率的反应条件是降低温度、减少压强
C.图中M点处(对应温度为210℃)NO的转化率一定不是该温度下的平衡转化率
D.相同条件下选择高效催化剂,可以提高NO的平衡转化率
【答案】D
【解析】A项,从题干图中可知,催化剂乙在低温下具有很强的催化活性,从而可以节约能源,故工
业上选择催化剂乙的原因是低温下有很强的催化活性,A正确;B项,从图中分析可知,随着温度升高化
学平衡逆向移动,即该主反应是一个正反应为放热反应,且正向为气体体积增大的方向,根据勒夏特列原
理可知,投料比一定时有利于提高NO平衡转化率的反应条件是降低温度、减少压强,B正确;C项,甲
催化剂随温度升高NO转化率先增大后减小是因为催化剂在温度高的条件下催化活性减小,在催化剂甲作
用下,图中M点处(对应温度为210℃)NO的转化率一定不是该温度下的平衡转化率,高于210℃时,NO
转化率降低是催化剂活性减低(或副反应增多),C错误;D项,根据勒夏特列原理可知,催化剂只能改变
反应速率而不影响化学平衡,故相同条件下选择高效催化剂,不能提高NO的平衡转化率,D错误;故选
D。
【对点提升】
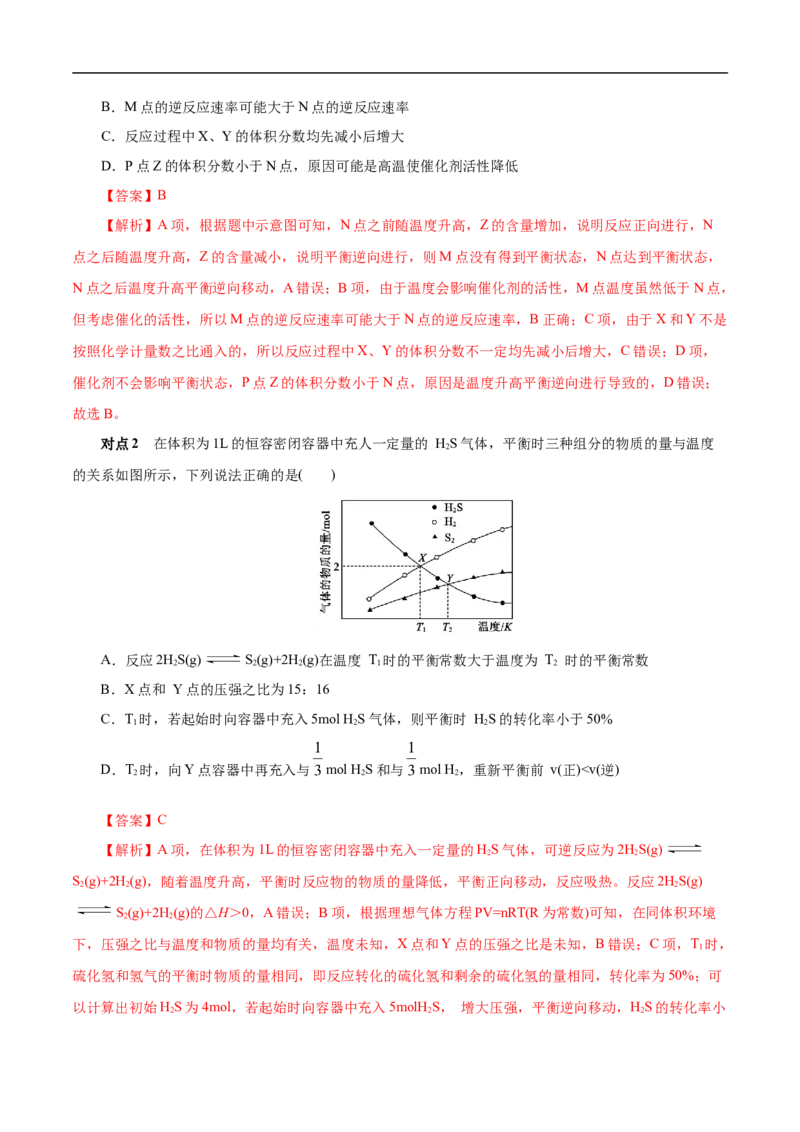
对点1 在恒容密闭容器中充入3molX和3molY发生反应:3X(g)+Y(g) 2Z(g) H<0,反应
过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示。下列推断正确的是△( )
A.M点和P点均达到平衡状态B.M点的逆反应速率可能大于N点的逆反应速率
C.反应过程中X、Y的体积分数均先减小后增大
D.P点Z的体积分数小于N点,原因可能是高温使催化剂活性降低
【答案】B
【解析】A项,根据题中示意图可知,N点之前随温度升高,Z的含量增加,说明反应正向进行,N
点之后随温度升高,Z的含量减小,说明平衡逆向进行,则M点没有得到平衡状态,N点达到平衡状态,
N点之后温度升高平衡逆向移动,A错误;B项,由于温度会影响催化剂的活性,M点温度虽然低于N点,
但考虑催化的活性,所以M点的逆反应速率可能大于N点的逆反应速率,B正确;C项,由于X和Y不是
按照化学计量数之比通入的,所以反应过程中X、Y的体积分数不一定均先减小后增大,C错误;D项,
催化剂不会影响平衡状态,P点Z的体积分数小于N点,原因是温度升高平衡逆向进行导致的,D错误;
故选B。
对点2 在体积为1L的恒容密闭容器中充人一定量的 HS气体,平衡时三种组分的物质的量与温度
2
的关系如图所示,下列说法正确的是( )
A.反应2HS(g) S(g)+2H(g)在温度 T 时的平衡常数大于温度为 T 时的平衡常数
2 2 2 1 2
B.X点和 Y点的压强之比为15:16
C.T 时,若起始时向容器中充入5mol HS气体,则平衡时 HS的转化率小于50%
1 2 2
D.T 时,向Y点容器中再充入与 mol HS和与 mol H,重新平衡前 v(正)0
B.若该反应在T、T 时的平衡常数分别为K、K,则KK ,故
1 2
B错误;C项,根据图像可知,由状态D到平衡点B,需要减小NO的浓度,所以反应正向进行,则v >v
正
,故C错误;D项,由于反应物碳是固体,所以在反应进行过程中,气体的总质量一直在变,V一定,
逆
气体的密度也就一直在变,当若混合气体的密度不再变化,则可以判断反应达到平衡状态C,故D正确;
答案D。
3.某科研团队研究将磷钨酸(H PW O ,以下简称HPW)代替浓硫酸作为酯化反应的催化剂,但HPW
3 12 40
自身存在比表面积小、易溶于有机溶剂而难以重复使用等缺点,将其负载在多孔载体(如硅藻土、C等)上
则能有效克服以上不足,提高其催化活性。用HPW负载在硅藻土上催化制取乙酸正丁酯的酯化率与HPW
负载量的关系(温度:120℃,时间:2h)如图所示,下列说法不正确的是( )A.与HPW相比,HPW/硅藻土比表面积显著增加,有助于提高其催化性能
B.当HPW负载量为40%时达到饱和,酯化率最高
C.用HPW/硅藻土代替传统催化剂,可减少设备腐蚀等不足
D.不同催化剂对酯化率的影响程度主要取决于化学反应正向进行的程度
【答案】D
【解析】A项,HPW自身存在比表面积小、易溶于有机溶剂而难以重复使用等缺点,将其负载在多孔
载体(如硅藻土、C等)上则能有效克服以上不足,提高其催化活性,A正确;B项,根据图中曲线可知,当
HPW负载量为40%时达到饱和,酯化率最高,B正确;C项,用HPW/硅藻土代替传统催化剂浓硫酸,可
减少设备腐蚀等不足,C正确;D项,催化剂不能使平衡移动,不能改变反应正向进行的程度,D不正确。
故选D。
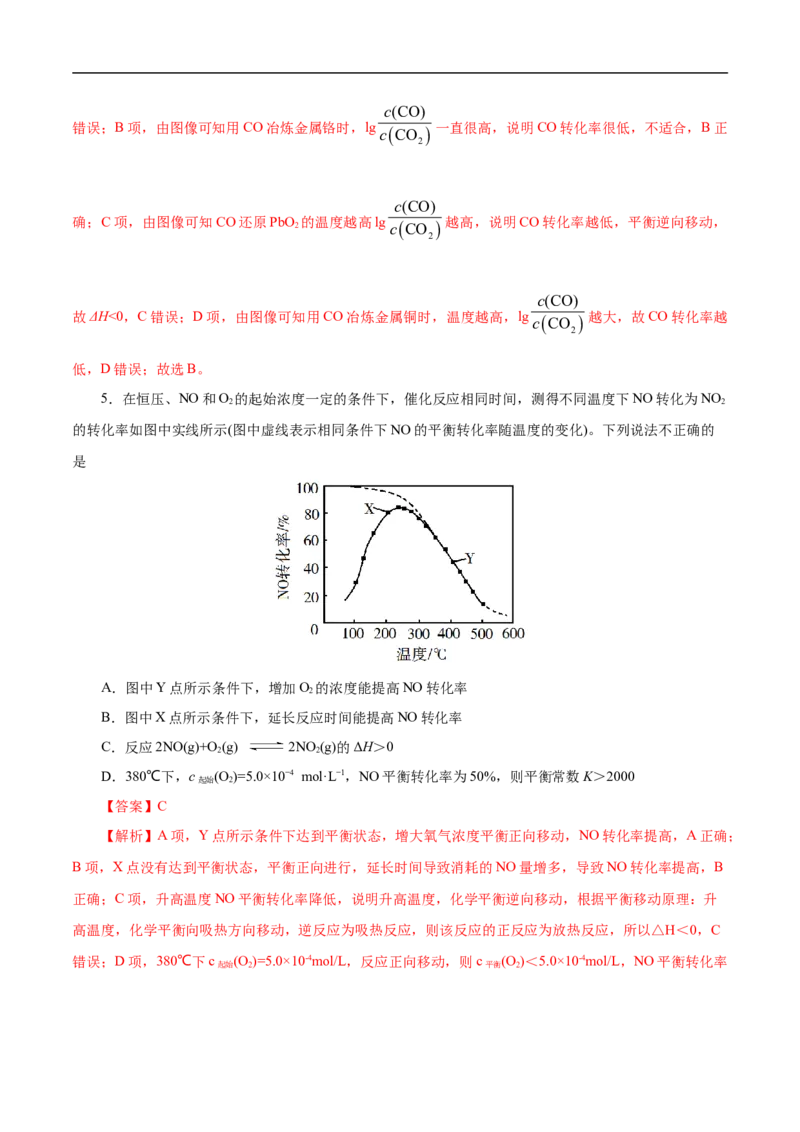
cCO
4.CO常用于工业冶炼金属。在不同温度下CO还原四种金属氧化物达平衡后气体中lgcCO 与温
2
度(t)的关系曲线如右图。下列说法正确的是( )
A. 通过增高反应炉的高度,延长矿石和CO接触的时间,能减少尾气中CO的含量
B. CO不适宜用于工业冶炼金属Cr
的
C. CO还原PbO 反应△H>0
2
D. 工业冶炼金属Cu时,高温有利于提高CO的转化率
【答案】B
【解析】A项,增高炉的高度,增大CO与铁矿石的接触,不能影响平衡移动,CO的利用率不变,Ac(CO)
错误;B项,由图像可知用CO冶炼金属铬时,lg cCO 一直很高,说明CO转化率很低,不适合,B正
2
c(CO)
确;C项,由图像可知CO还原PbO 2 的温度越高lg cCO 越高,说明CO转化率越低,平衡逆向移动,
2
c(CO)
故ΔH<0,C错误;D项,由图像可知用CO冶炼金属铜时,温度越高,lg cCO 越大,故CO转化率越
2
低,D错误;故选B。
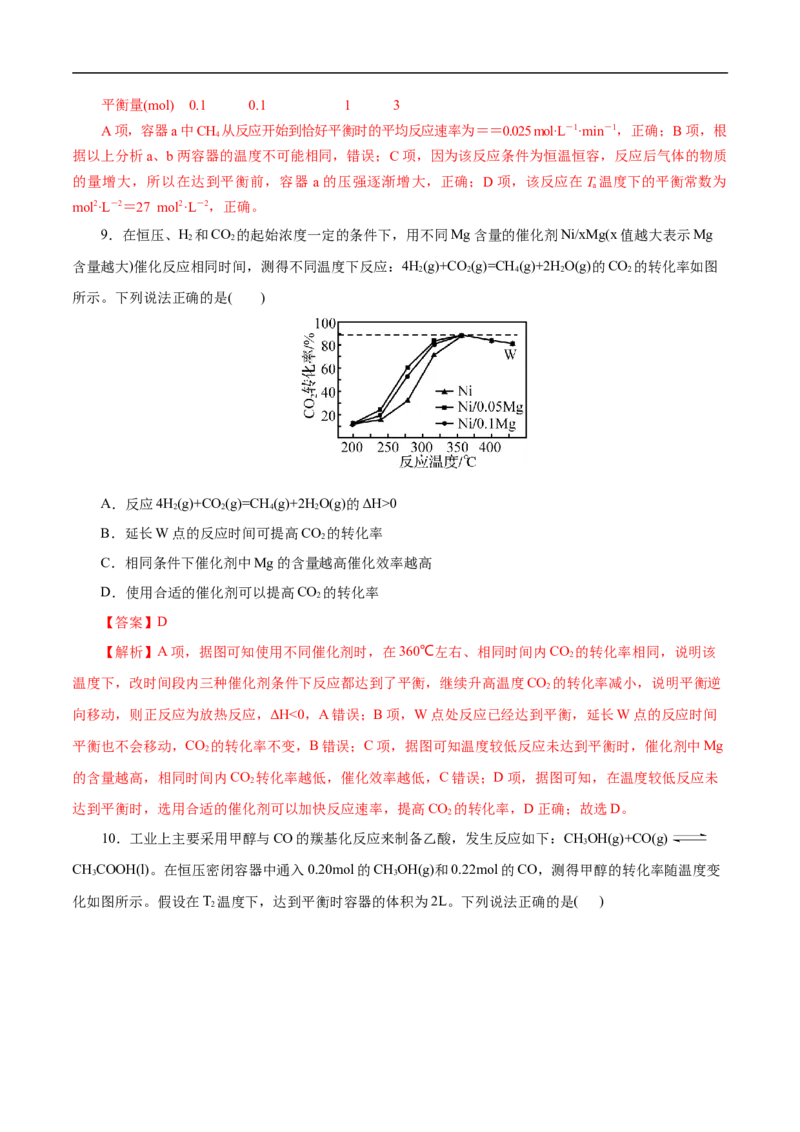
5.在恒压、NO和O 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO
2 2
的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法不正确的
是
A.图中Y点所示条件下,增加O 的浓度能提高NO转化率
2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.反应2NO(g)+O (g) 2NO (g)的ΔH>0
2 2
D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
【答案】C
【解析】A项,Y点所示条件下达到平衡状态,增大氧气浓度平衡正向移动,NO转化率提高,A正确;
B项,X点没有达到平衡状态,平衡正向进行,延长时间导致消耗的NO量增多,导致NO转化率提高,B
正确;C项,升高温度NO平衡转化率降低,说明升高温度,化学平衡逆向移动,根据平衡移动原理:升
高温度,化学平衡向吸热方向移动,逆反应为吸热反应,则该反应的正反应为放热反应,所以△H<0,C
错误;D项,380℃下c (O )=5.0×10-4mol/L,反应正向移动,则c (O )<5.0×10-4mol/L,NO平衡转化率
起始 2 平衡 2为50%,则平衡时c(NO)=c(NO ),化学平衡常数K= =2000,D正确。
2
6.在425 ℃时,在1 L密闭容器中充入下列气体物质进行的反应达到平衡,分析下图所示示意图,不
能从示意图中读出相关信息的选项是( )
A.同温同压下,只要投入物质比例适当,从正、逆方向都可以建立同一平衡状态
B.图(1)表示的反应为H(g)+I(g) 2HI(g)
2 2
C.图(1)中H 的转化率+图(2)中HI的转化率=100%
2
D.相同条件下,分别从正、逆方向建立等同的平衡状态,所需时间相同
【答案】D
【解析】比较图(1)和图(2)可知,两平衡状态的c(HI)、c(H )、c(I)相同,图(1)表示的化学反应方程式
2 2
为H(g)+I(g) 2HI(g),图(1)中H 的转化率为×100%=79%,图(2)中HI的转化率为×100%=21%,
2 2 2
故A、B、C正确。故选D。
7.一定温度下,向三个容积不等的恒容密闭容器(a<b<c)中分别投入2 mol NOCl,发生反应:
2NOCl(g) 2NO(g)+Cl(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述
2
正确的是( )
A.A点延长反应时间,可以提高NOCl的转化率
B.A、B两点的压强之比为25︰28
C.A点的平均反应速率大于C点的平均反应速率
D.容积为a L的容器达到平衡后再投入1 mol NOCl、1 mol NO,平衡不移动
【答案】D【解析】A项,容器体积越大,反应速率越小,容积为a L的容器反应速率大于容积为b L的容器,t
min后, A点的转化率小于B,说明A点达到平衡状态,A点延长反应时间,NOCl的转化率不变,故A
错误;B项,A、B两点的气体物质的量比为25︰28,容器的体积不同,所以压强之比不是25︰28,故B
错误;C项,A为平衡点,A点的平均反应速率为0,C没有达到平衡,C点的平均反应速率大于0,故C
错误;D项,A点为平衡点,根据A点数据,K= ,再投入1 mol NOCl、1 mol NO,Q=
,Q=K,平衡不移动,故D正确;故选D。
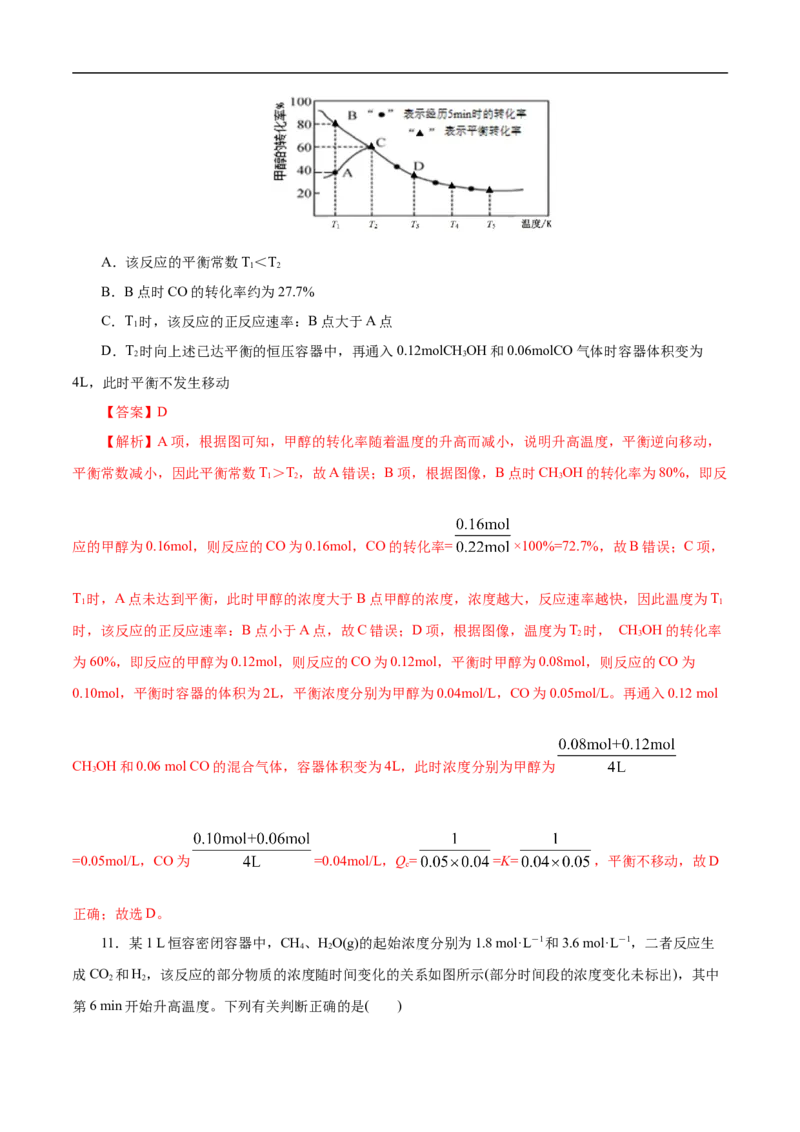
8.工业上以CH 为原料制备H 的原理为CH(g)+HO(g) CO(g)+3H(g)。在一定条件下a、b两
4 2 4 2 2
个恒温恒容的密闭容器中均通入1.1 mol CH (g)和1.1 mol H O(g),测得两容器中CO的物质的量随时间的
4 2
变化曲线分别为a和b。已知容器a的体积为10 L,温度为T,下列说法不正确的是( )
a
A.容器a中CH 从反应开始到恰好平衡时的平均反应速率为0.025 mol·L-1·min-1
4
B.a、b两容器的温度可能相同
C.在达到平衡前,容器a的压强逐渐增大
D.该反应在T温度下的平衡常数为27
a
【答案】B
【解析】观察两容器中CO的物质的量随时间的变化曲线a和b可知,当CO的物质的量保持不变时便
达到平衡状态,a容器用了4 min,b容器用了6.5 min,两个容器中反应快慢不同,因此温度肯定不同。用
三段式分析a容器中各物质的相关量:
CH(g)+HO(g) CO(g)+3H(g)
4 2 2
起始量(mol) 1.1 1.1 0 0
转化量(mol) 1 1 1 3平衡量(mol) 0.1 0.1 1 3
A项,容器a中CH 从反应开始到恰好平衡时的平均反应速率为==0.025 mol·L-1·min-1,正确;B项,根
4
据以上分析a、b两容器的温度不可能相同,错误;C项,因为该反应条件为恒温恒容,反应后气体的物质
的量增大,所以在达到平衡前,容器 a的压强逐渐增大,正确;D项,该反应在T 温度下的平衡常数为
a
mol2·L-2=27 mol2·L-2,正确。
9.在恒压、H 和CO 的起始浓度一定的条件下,用不同Mg含量的催化剂Ni/xMg(x值越大表示Mg
2 2
含量越大)催化反应相同时间,测得不同温度下反应:4H(g)+CO (g)=CH (g)+2HO(g)的CO 的转化率如图
2 2 4 2 2
所示。下列说法正确的是( )
A.反应4H(g)+CO (g)=CH (g)+2HO(g)的ΔH>0
2 2 4 2
B.延长W点的反应时间可提高CO 的转化率
2
C.相同条件下催化剂中Mg的含量越高催化效率越高
D.使用合适的催化剂可以提高CO 的转化率
2
【答案】D
【解析】A项,据图可知使用不同催化剂时,在360℃左右、相同时间内CO 的转化率相同,说明该
2
温度下,改时间段内三种催化剂条件下反应都达到了平衡,继续升高温度CO 的转化率减小,说明平衡逆
2
向移动,则正反应为放热反应,ΔH<0,A错误;B项,W点处反应已经达到平衡,延长W点的反应时间
平衡也不会移动,CO 的转化率不变,B错误;C项,据图可知温度较低反应未达到平衡时,催化剂中Mg
2
的含量越高,相同时间内CO 转化率越低,催化效率越低,C错误;D项,据图可知,在温度较低反应未
2
达到平衡时,选用合适的催化剂可以加快反应速率,提高CO 的转化率,D正确;故选D。
2
10.工业上主要采用甲醇与CO的羰基化反应来制备乙酸,发生反应如下:CHOH(g)+CO(g)
3
CHCOOH(l)。在恒压密闭容器中通入0.20mol的CHOH(g)和0.22mol的CO,测得甲醇的转化率随温度变
3 3
化如图所示。假设在T 温度下,达到平衡时容器的体积为2L。下列说法正确的是( )
2A.该反应的平衡常数T<T
1 2
B.B点时CO的转化率约为27.7%
C.T 时,该反应的正反应速率:B点大于A点
1
D.T 时向上述已达平衡的恒压容器中,再通入0.12molCHOH和0.06molCO气体时容器体积变为
2 3
4L,此时平衡不发生移动
【答案】D
【解析】A项,根据图可知,甲醇的转化率随着温度的升高而减小,说明升高温度,平衡逆向移动,
平衡常数减小,因此平衡常数T>T,故A错误;B项,根据图像,B点时CHOH的转化率为80%,即反
1 2 3
应的甲醇为0.16mol,则反应的CO为0.16mol,CO的转化率= ×100%=72.7%,故B错误;C项,
T 时,A点未达到平衡,此时甲醇的浓度大于B点甲醇的浓度,浓度越大,反应速率越快,因此温度为T
1 1
时,该反应的正反应速率:B点小于A点,故C错误;D项,根据图像,温度为T 时, CHOH的转化率
2 3
为60%,即反应的甲醇为0.12mol,则反应的CO为0.12mol,平衡时甲醇为0.08mol,则反应的CO为
0.10mol,平衡时容器的体积为2L,平衡浓度分别为甲醇为0.04mol/L,CO为0.05mol/L。再通入0.12 mol
CHOH和0.06 mol CO的混合气体,容器体积变为4L,此时浓度分别为甲醇为
3
=0.05mol/L,CO为 =0.04mol/L,Q= =K= ,平衡不移动,故D
c
正确;故选D。
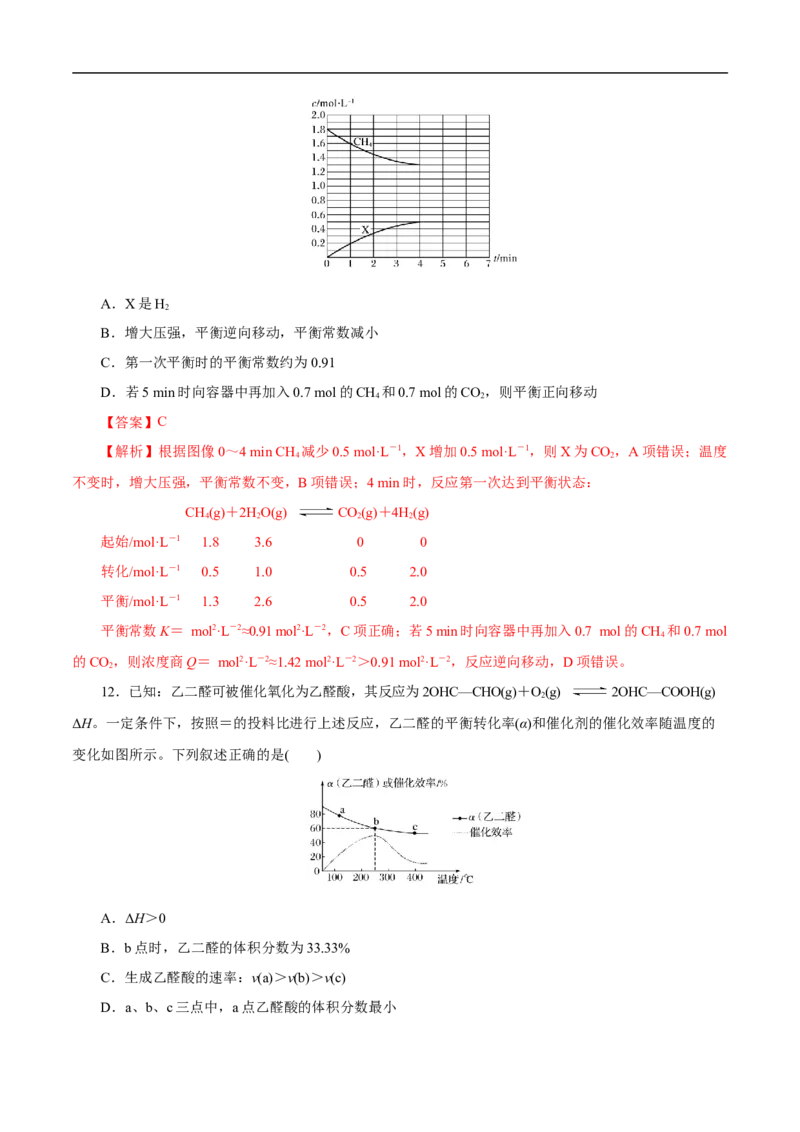
11.某1 L恒容密闭容器中,CH、HO(g)的起始浓度分别为1.8 mol·L-1和3.6 mol·L-1,二者反应生
4 2
成CO 和H,该反应的部分物质的浓度随时间变化的关系如图所示(部分时间段的浓度变化未标出),其中
2 2
第6 min开始升高温度。下列有关判断正确的是( )A.X是H
2
B.增大压强,平衡逆向移动,平衡常数减小
C.第一次平衡时的平衡常数约为0.91
D.若5 min时向容器中再加入0.7 mol的CH 和0.7 mol的CO,则平衡正向移动
4 2
【答案】C
【解析】根据图像0~4 min CH 减少0.5 mol·L-1,X增加0.5 mol·L-1,则X为CO ,A项错误;温度
4 2
不变时,增大压强,平衡常数不变,B项错误;4 min时,反应第一次达到平衡状态:
CH(g)+2HO(g) CO(g)+4H(g)
4 2 2 2
起始/mol·L-1 1.8 3.6 0 0
转化/mol·L-1 0.5 1.0 0.5 2.0
平衡/mol·L-1 1.3 2.6 0.5 2.0
平衡常数K= mol2·L-2≈0.91 mol2·L-2,C项正确;若5 min时向容器中再加入0.7 mol的CH 和0.7 mol
4
的CO,则浓度商Q= mol2·L-2≈1.42 mol2·L-2>0.91 mol2·L-2,反应逆向移动,D项错误。
2
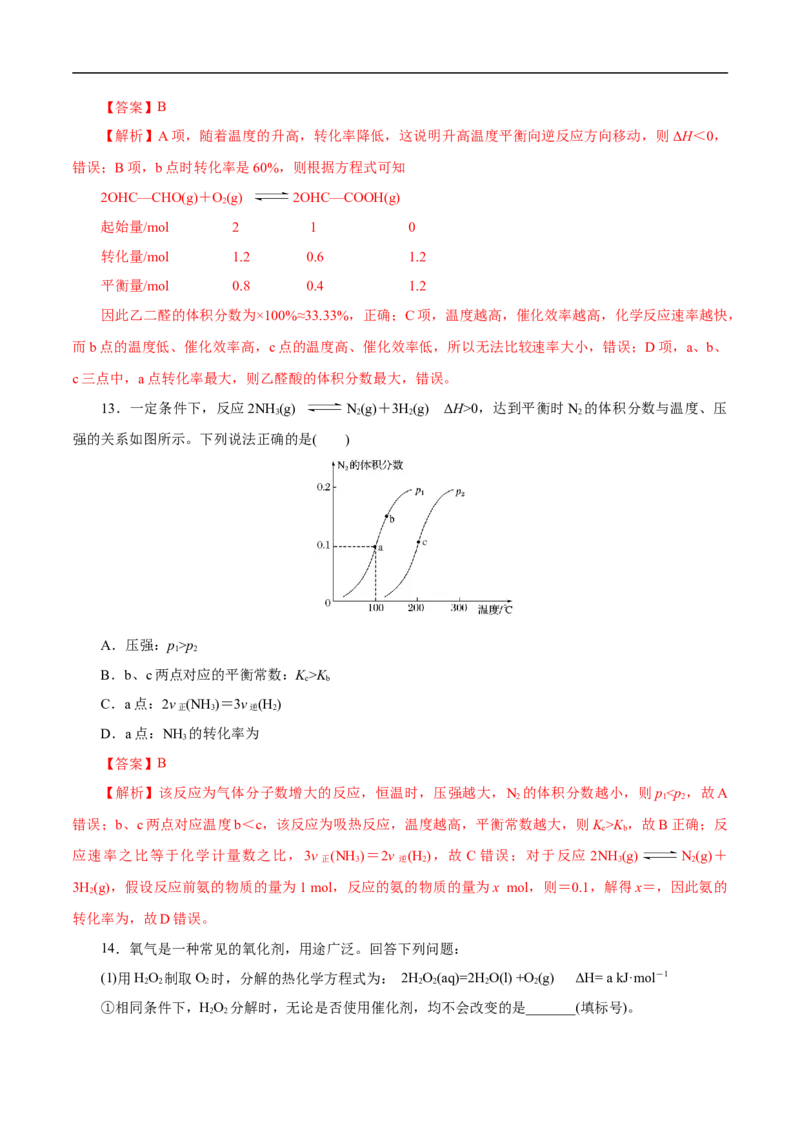
12.已知:乙二醛可被催化氧化为乙醛酸,其反应为2OHC—CHO(g)+O(g) 2OHC—COOH(g)
2
ΔH。一定条件下,按照=的投料比进行上述反应,乙二醛的平衡转化率(α)和催化剂的催化效率随温度的
变化如图所示。下列叙述正确的是( )
A.ΔH>0
B.b点时,乙二醛的体积分数为33.33%
C.生成乙醛酸的速率:v(a)>v(b)>v(c)
D.a、b、c三点中,a点乙醛酸的体积分数最小【答案】B
【解析】A项,随着温度的升高,转化率降低,这说明升高温度平衡向逆反应方向移动,则ΔH<0,
错误;B项,b点时转化率是60%,则根据方程式可知
2OHC—CHO(g)+O(g) 2OHC—COOH(g)
2
起始量/mol 2 1 0
转化量/mol 1.2 0.6 1.2
平衡量/mol 0.8 0.4 1.2
因此乙二醛的体积分数为×100%≈33.33%,正确;C项,温度越高,催化效率越高,化学反应速率越快,
而b点的温度低、催化效率高,c点的温度高、催化效率低,所以无法比较速率大小,错误;D项,a、b、
c三点中,a点转化率最大,则乙醛酸的体积分数最大,错误。
13.一定条件下,反应2NH (g) N(g)+3H(g) ΔH>0,达到平衡时N 的体积分数与温度、压
3 2 2 2
强的关系如图所示。下列说法正确的是( )
A.压强:p>p
1 2
B.b、c两点对应的平衡常数:K>K
c b
C.a点:2v (NH )=3v (H )
正 3 逆 2
D.a点:NH 的转化率为
3
【答案】B
【解析】该反应为气体分子数增大的反应,恒温时,压强越大,N 的体积分数越小,则pK ,故B正确;反
c b
应速率之比等于化学计量数之比,3v (NH )=2v (H ),故 C 错误;对于反应 2NH (g) N(g)+
正 3 逆 2 3 2
3H(g),假设反应前氨的物质的量为1 mol,反应的氨的物质的量为x mol,则=0.1,解得x=,因此氨的
2
转化率为,故D错误。
14.氧气是一种常见的氧化剂,用途广泛。回答下列问题:
(1)用HO 制取O 时,分解的热化学方程式为: 2HO(aq)=2H O(l) +O (g) ΔH= a kJ·mol-1
2 2 2 2 2 2 2
①相同条件下,HO 分解时,无论是否使用催化剂,均不会改变的是_______(填标号)。
2 2A 反应速率 B 反应热 C 活化能 D 生成物
②以Fe3+作催化剂时,HO 的分解反应分两步进行,第一步反应为: HO(aq) + 2Fe3+ (aq)=2Fe2+
2 2 2 2
(aq) +O(g) +2H+ (aq)ΔH=b kJ·mol-1
2
第二步反应的热化学方程式为____________。
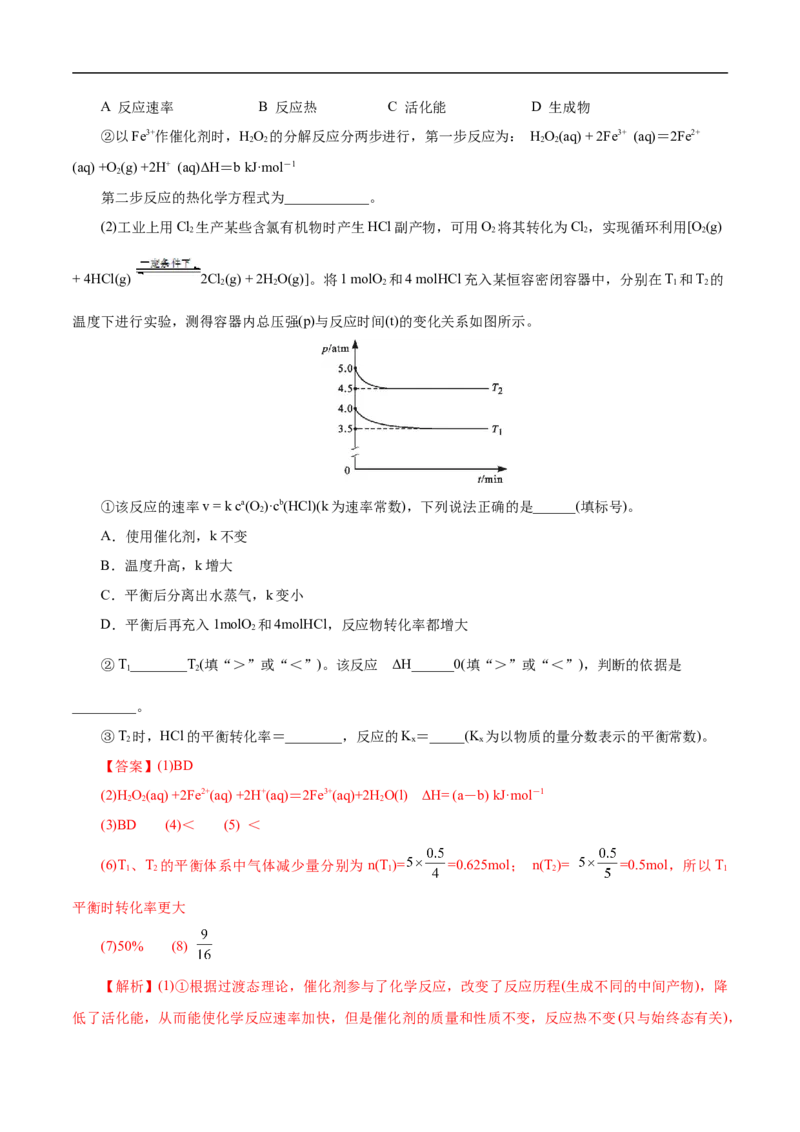
(2)工业上用Cl 生产某些含氯有机物时产生HCl副产物,可用O 将其转化为Cl,实现循环利用[O (g)
2 2 2 2
+ 4HCl(g) 2Cl(g) + 2HO(g)]。将1 molO 和4 molHCl充入某恒容密闭容器中,分别在T 和T 的
2 2 2 1 2
温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
①该反应的速率v = k ca(O )·cb(HCl)(k为速率常数),下列说法正确的是______(填标号)。
2
A.使用催化剂,k不变
B.温度升高,k增大
C.平衡后分离出水蒸气,k变小
D.平衡后再充入1molO 和4molHCl,反应物转化率都增大
2
的
②T________T(填“>”或“<”)。该反应 ΔH______0(填“>”或“<”),判断的依据是
1 2
_________。
③T 时,HCl的平衡转化率=________,反应的K=_____(K 为以物质的量分数表示的平衡常数)。
2 x x
【答案】(1)BD
(2)H O(aq) +2Fe2+(aq) +2H+(aq)=2Fe3+(aq)+2H O(l) ΔH= (a-b) kJ·mol-1
2 2 2
(3)BD (4)< (5) <
(6)T 、T 的平衡体系中气体减少量分别为 n(T )= =0.625mol; n(T )= =0.5mol,所以T
1 2 1 2 1
平衡时转化率更大
(7)50% (8)
【解析】(1)①根据过渡态理论,催化剂参与了化学反应,改变了反应历程(生成不同的中间产物),降
低了活化能,从而能使化学反应速率加快,但是催化剂的质量和性质不变,反应热不变(只与始终态有关),B D正确,故选BD;②Fe3+作为催化剂,在反应前后质量和性质不变,根据盖斯定律总反应=第一步反应
+第二步反应,故第二步反应为 HO(aq)+2Fe2+(aq)+2H+(aq)=2Fe3+(aq)+2H O(l) H=(a−b)kJmol−1;(2)①A
2 2 2
项,催化剂降低了反应的活化能,使反应的速率常数k增大,根据速率方程v=k△ca(O )cb(HC⋅l),反应速率随
2
之增大,A错误;B项,温度改变瞬间,浓度没有影响,即通过增大k从而改变了速⋅率,使平衡发生移动,
故B正确;C项,从速率方程可知,平衡后分离出水蒸气,降低了c(HO),使平衡正向移动,从而改变了
2
c(O)和c(HCl),但对k没有影响,故C错误;D项,化学平衡的建立与途径无关,所以“平衡后再充入
2
1molO 和4molHCl”,相当于增大反应体系的压强,反应有利于向气体分子数减小的方向进行,故D正确;
2
故选BD;②从图象可知,T 温度下,容器中压强大,达到平衡所需要的时间短,所以温度T>T ;T 、T
2 2 1 1 2
温度下,气体物质的量的减少量分别为n(T )=5× =0.625mol、n(T )=5× =0.5mol,即T 平衡时转化率
1 2 1
更大,且因为T>T ,所以△H<0,故答案为:<;<;T 、T 的平衡体系中气体减少量分别为n(T )=5×
2 1 1 2 1
=0.625mol、n(T )=5× =0.5mol,所以T 平衡时转化率更大;③对于气相反应,经验平衡常数常见的有
2 1
K、K、K 等,三种平衡常数的表示式相似,只是K、K、K 分别用平衡时物质的量浓度、分压、物质的
c p x c p x
量分数表示。
则HCl的平衡转化率为 ×100%=50%, = 。
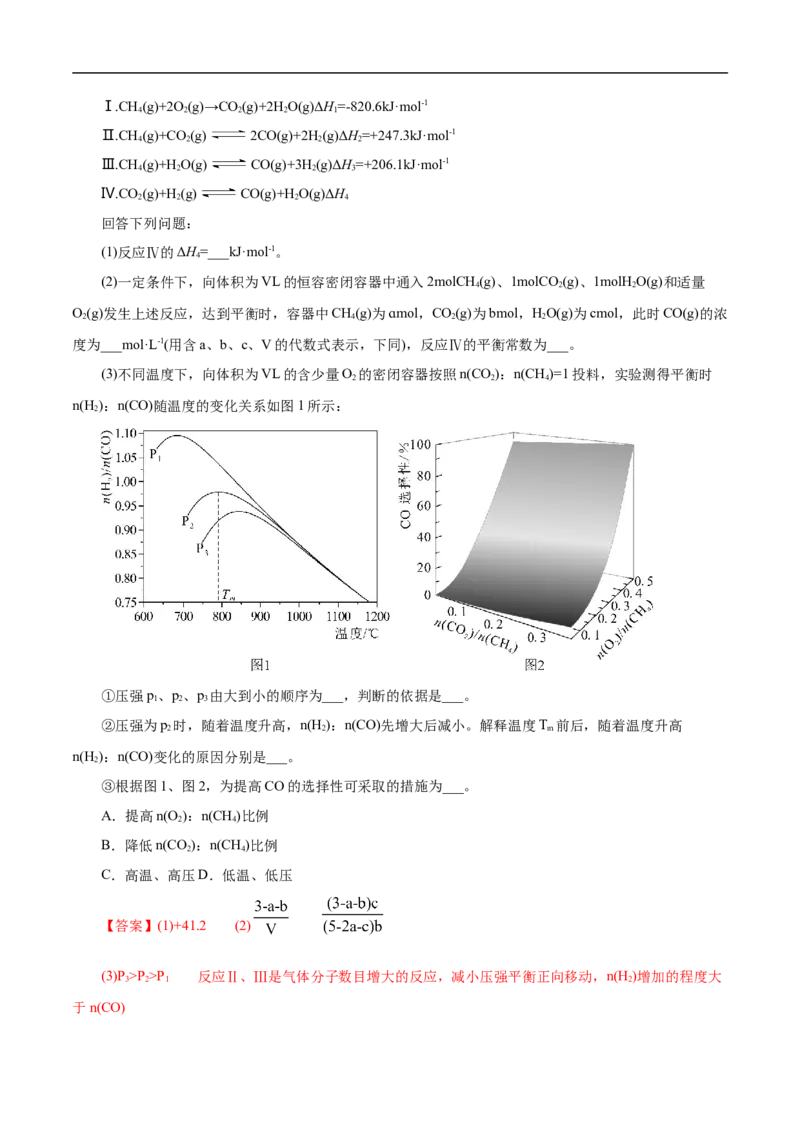
15.合成气是一种重要的化工原料气,可以合成甲醇、甲酸甲酯、二甲醚等化工产品。甲烷、二氧化
碳自热重整制合成气的主要反应有:Ⅰ.CH (g)+2O(g)→CO (g)+2HO(g)ΔH=-820.6kJ·mol-1
4 2 2 2 1
Ⅱ.CH (g)+CO (g) 2CO(g)+2H(g)ΔH=+247.3kJ·mol-1
4 2 2 2
Ⅲ.CH (g)+HO(g) CO(g)+3H(g)ΔH=+206.1kJ·mol-1
4 2 2 3
Ⅳ.CO (g)+H(g) CO(g)+HO(g)ΔH
2 2 2 4
回答下列问题:
(1)反应Ⅳ的ΔH=___kJ·mol-1。
4
(2)一定条件下,向体积为VL的恒容密闭容器中通入2molCH (g)、1molCO (g)、1molH O(g)和适量
4 2 2
O(g)发生上述反应,达到平衡时,容器中CH(g)为ɑmol,CO(g)为bmol,HO(g)为cmol,此时CO(g)的浓
2 4 2 2
度为___mol·L-1(用含a、b、c、V的代数式表示,下同),反应Ⅳ的平衡常数为___。
(3)不同温度下,向体积为VL的含少量O 的密闭容器按照n(CO):n(CH)=1投料,实验测得平衡时
2 2 4
n(H ):n(CO)随温度的变化关系如图1所示:
2
①压强p、p、p 由大到小的顺序为___,判断的依据是___。
1 2 3
②压强为p 时,随着温度升高,n(H ):n(CO)先增大后减小。解释温度T 前后,随着温度升高
2 2 m
n(H ):n(CO)变化的原因分别是___。
2
③根据图1、图2,为提高CO的选择性可采取的措施为___。
A.提高n(O ):n(CH)比例
2 4
B.降低n(CO):n(CH)比例
2 4
C.高温、高压D.低温、低压
【答案】(1)+41.2 (2)
(3)P >P >P 反应Ⅱ、Ⅲ是气体分子数目增大的反应,减小压强平衡正向移动,n(H )增加的程度大
3 2 1 2
于n(CO)②升高温度平衡Ⅱ、Ⅲ、Ⅳ均正向移动,TT 后,对反应Ⅳ的促进作用更大,n(CO)增加的更多
2 m
③AC
【解析】(1)根据盖斯定律,反应Ⅳ=Ⅱ-Ⅲ,则ΔH=ΔH-ΔH=+247.3kJ·mol-1-
4 2 3
206.1kJ·mol-1=+41.2kJ·mol-1;(2)通入2molCH (g)、1molCO (g)、1molH O(g)和适量O(g),达到平衡时,容
4 2 2 2
器中CH(g)为ɑmol,CO(g)为bmol,HO(g)为cmol,设H(g)的物质的量为x,CO(g)的物质的量为y,由
4 2 2 2
C、H原子守恒有:{ ,解得x=5-2a-c,y=3-a-b,即n(H )=( 5-2a-
2
c)mol,n(CO)=( 3-a-b)mol,此时c(CO)= = mol·L-1;
则K= = ;(3)①由反应可知,反应Ⅱ、Ⅲ是气体分子数目增大的反应,减小
压强平衡正向移动,n(H )增加的程度大于n(CO),则压强p、p、p 由大到小的顺序为P>P >P ,故答案为:
2 1 2 3 3 2 1
P>P >P ;反应Ⅱ、Ⅲ是气体分子数目增大的反应,减小压强平衡正向移动,n(H )增加的程度大于
3 2 1 2
n(CO); ②由图1可知,压强为p 时,随着温度升高,n(H ):n(CO)先增大后减小,原因是反应Ⅱ、Ⅲ、
2 2
Ⅳ均为吸热反应,升高温度平衡Ⅱ、Ⅲ、Ⅳ均正向移动,TT 后,对反应Ⅳ的促进作用更大,n(CO)增加的更多,故答案为:升高温度
2 m
平衡Ⅱ、Ⅲ、Ⅳ均正向移动,TT 后,对反应Ⅳ的促进作用更大,n(CO)增加的更多;③A项,根据图2,提高n(O ):n(CH)比例,可
m 2 4
提高CO的选择性,故A符合题意;B项,根据图2,降低n(CO):n(CH)比例,不能提高CO的选择性,
2 4
故B不符合题意;C项,根据图1,升高温度、增大压强时n(H ):n(CO)比例减小,即CO的选择性提高,
2
故C符合题意;D项,根据C项分析,低温、低压时CO的选择性降低,故D不符合题意;故选AC。
16.异丁烯为重要的化工原料,工业上可采用叔丁醇(TBA)气相脱水法制备高纯异丁烯产品,主要涉
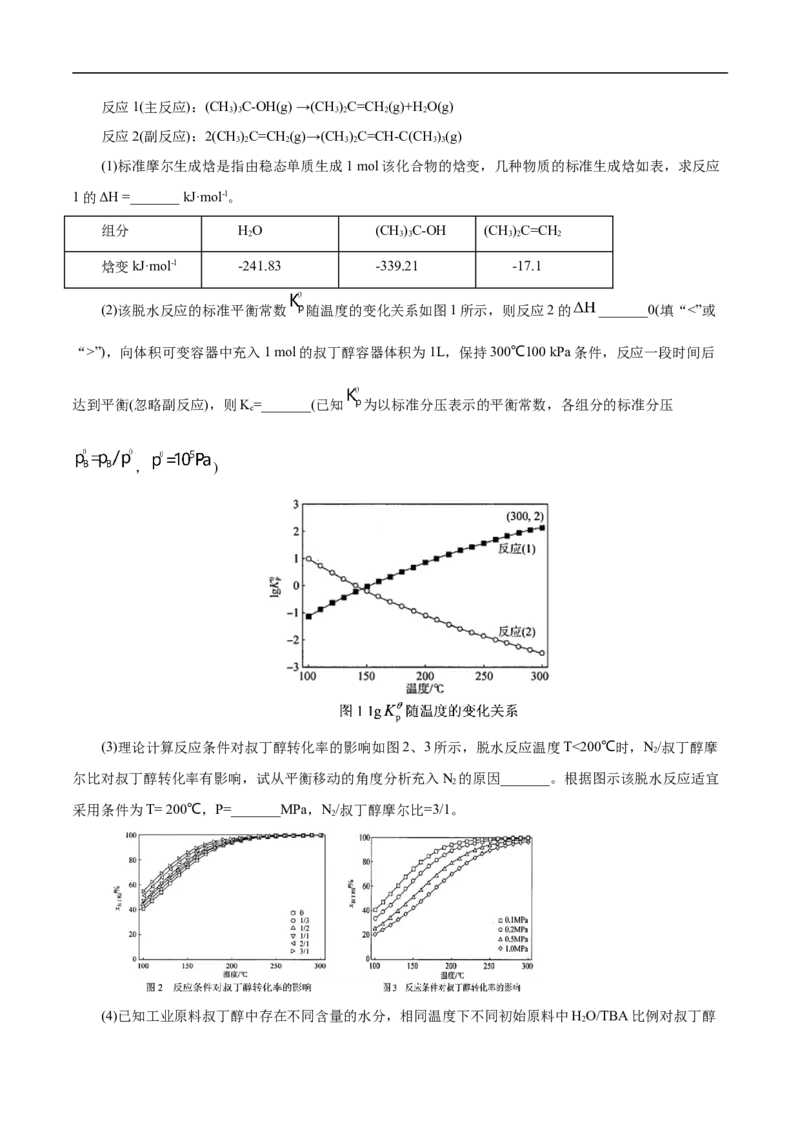
及以下反应:反应1(主反应):(CH)C-OH(g) →(CH )C=CH (g)+HO(g)
3 3 3 2 2 2
反应2(副反应):2(CH)C=CH (g)→(CH )C=CH-C(CH )(g)
3 2 2 3 2 3 3
(1)标准摩尔生成焓是指由稳态单质生成1 mol该化合物的焓变,几种物质的标准生成焓如表,求反应
1的ΔH =_______ kJ·mol-l。
组分 HO (CH)C-OH (CH)C=CH
2 3 3 3 2 2
焓变kJ·mol-l -241.83 -339.21 -17.1
(2)该脱水反应的标准平衡常数 随温度的变化关系如图1所示,则反应2的 _______0(填“<”或
“>”),向体积可变容器中充入1 mol的叔丁醇容器体积为1L,保持300℃100 kPa条件,反应一段时间后
达到平衡(忽略副反应),则K=_______(已知 为以标准分压表示的平衡常数,各组分的标准分压
c
, )
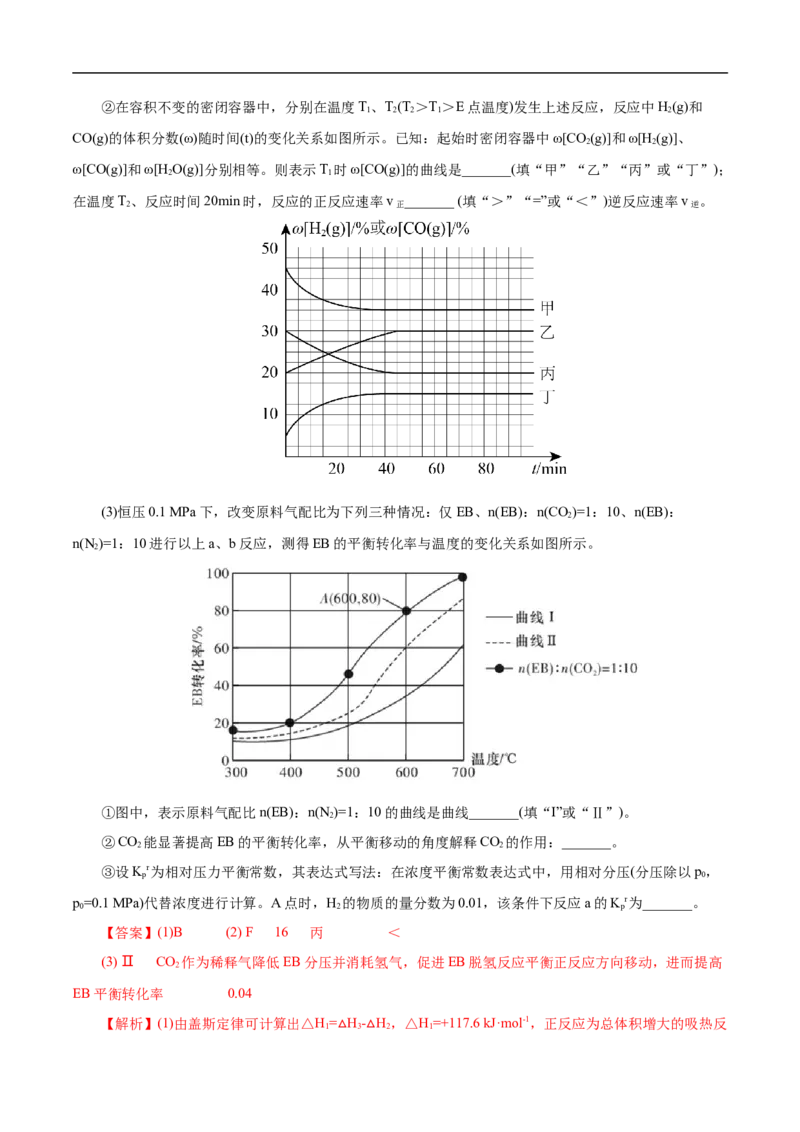
(3)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度T<200℃时,N/叔丁醇摩
2
尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N 的原因_______。根据图示该脱水反应适宜
2
采用条件为T= 200℃,P=_______MPa,N/叔丁醇摩尔比=3/1。
2
(4)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中HO/TBA比例对叔丁醇
2平衡转化率的影响如图4所示,实际生产最佳工艺条件为T=204~426℃,请从HO/TBA比例角度分析该条
2
件下的优点_______。
【答案】(1)+80.28
(2)< 100
(3)叔丁醇脱水反应是分子数增加的反应,而副反应是分子数降低的反应,N 为稀释剂,降低反应原料
2
的分压,有利于主反应正向进行,抑制副反应正向进行 0.1
(4)该条件下叔丁醇脱水法平衡转化率不受HO/TBA比例的影响,故工业上可忽略水对叔丁醇转化率
2
的影响,无需对原料进行烘干处理
【解析】(1)根据标准摩尔生成焓的定义,结合盖斯定律可知ΔH=生成物的标准摩尔生成焓-反应物的
标准摩尔生成焓 ;(2)由图像分析,反应2的 随温
度的升高逐渐降低,说明该反应为放热反应,ΔH<0;由图像信息知
,由题干信息各组分的标准分压 , ,可得
, ,列三段式:
平衡时总物质的量为(1+x)mol,体系反应前气体总物质的量为1 mol,体积为1L,根据PV=nRT,恒压体系,平衡时体系的体积为(1+x)L,各组分的浓度及物质的量分数分别为 ,
, , ,
, ,则 。
(3)脱水反应温度T<2000C时,N/叔丁醇摩尔比对叔丁醇转化率有影响,叔丁醇脱水反应是分子数增加的
2
反应,而副反应是分子数降低的反应,N 为稀释剂,降低反应的反应原料的分压,减小压强有利于促进主
2
反应和抑制副反应进行。由图像2、3可知叔丁醇转化率随温度升高逐渐增大,随压强增大而减小,随
N/叔丁醇摩尔比值增大而增大,故该脱水反应适宜采用条件为T=2000C, ,N/叔丁醇摩尔比
2 2
=3/1。(4)由图像4可知在T<2000C,叔丁醇平衡转化率随着HO/TBA比例的增加有一定程度的降低,即
2
反应时需要除去原料中包含的水,T>2000C,HO对叔丁醇平衡转化率影响可以忽略不计,该条件下叔丁
2
醇脱水法平衡转化率不受HO/TBA比例的影响,故工业上可忽略水对叔丁醇转化率的影响,无需对原料进
2
行烘干处理。
17.控制CO 的排放是防止温室效应等不良气候现象产生的有效途径。
2
(1)高炉炼铁会排放大量的CO 和烟尘,必须进行严格的控制。
2
已知:①3CO(g)+Fe O(s) 2Fe(s)+3CO (g) H=+a kJ/mol
2 3 2
②3C(石墨,s)+Fe
2
O
3
(s)=2Fe(s)+3CO(g) H=+48△9.0 kJ/mol
③C(石墨,s)+CO
2
(g)=2CO(g) H=+172.5△ kJ/mol
则a=____。若在恒温恒容密闭容△器中发生反应①,当达到平衡后,充入CO
2
,则达到新平衡后CO的
体积分数____(填“增大”、“减小”或“不变”,下同),其转化率_____。
(2)炼铁时需要用石灰石除去铁矿石中的脉石,该过程中涉及反应: CaCO(s) CaO(g)+CO(g)
3
ΔH>0。若在恒温恒容的密闭容器中进行上述反应达到平衡状态,在t 时刻向平衡体系中充入1 mol CO ,
1 2
t 时刻反应重新达到平衡,画出t 时刻后的正逆反应速率随时间变化的图像_____。
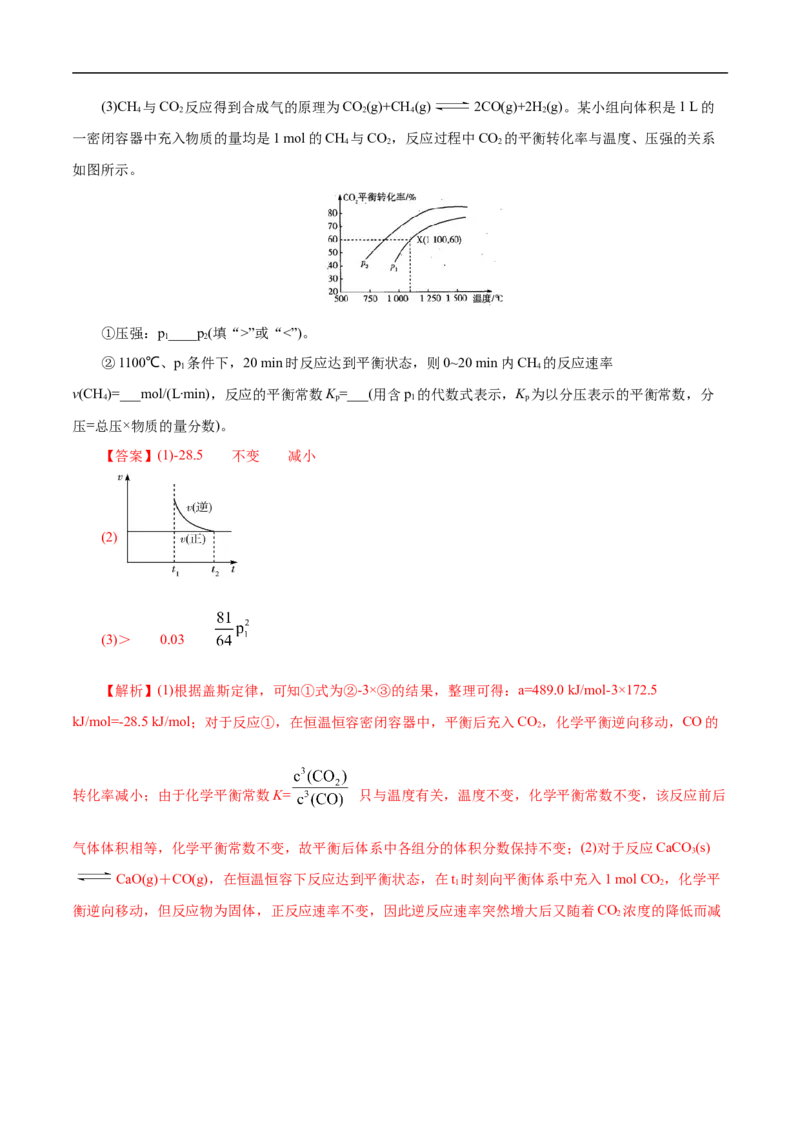
2 1(3)CH 与CO 反应得到合成气的原理为CO(g)+CH (g) 2CO(g)+2H(g)。某小组向体积是1 L的
4 2 2 4 2
一密闭容器中充入物质的量均是1 mol的CH 与CO,反应过程中CO 的平衡转化率与温度、压强的关系
4 2 2
如图所示。
①压强:p____p(填“>”或“<”)。
1 2
②1100℃、p 条件下,20 min时反应达到平衡状态,则0~20 min内CH 的反应速率
1 4
v(CH)=___mol/(L∙min),反应的平衡常数K =___(用含p 的代数式表示,K 为以分压表示的平衡常数,分
4 p 1 p
压=总压×物质的量分数)。
【答案】(1)-28.5 不变 减小
(2)
(3)> 0.03
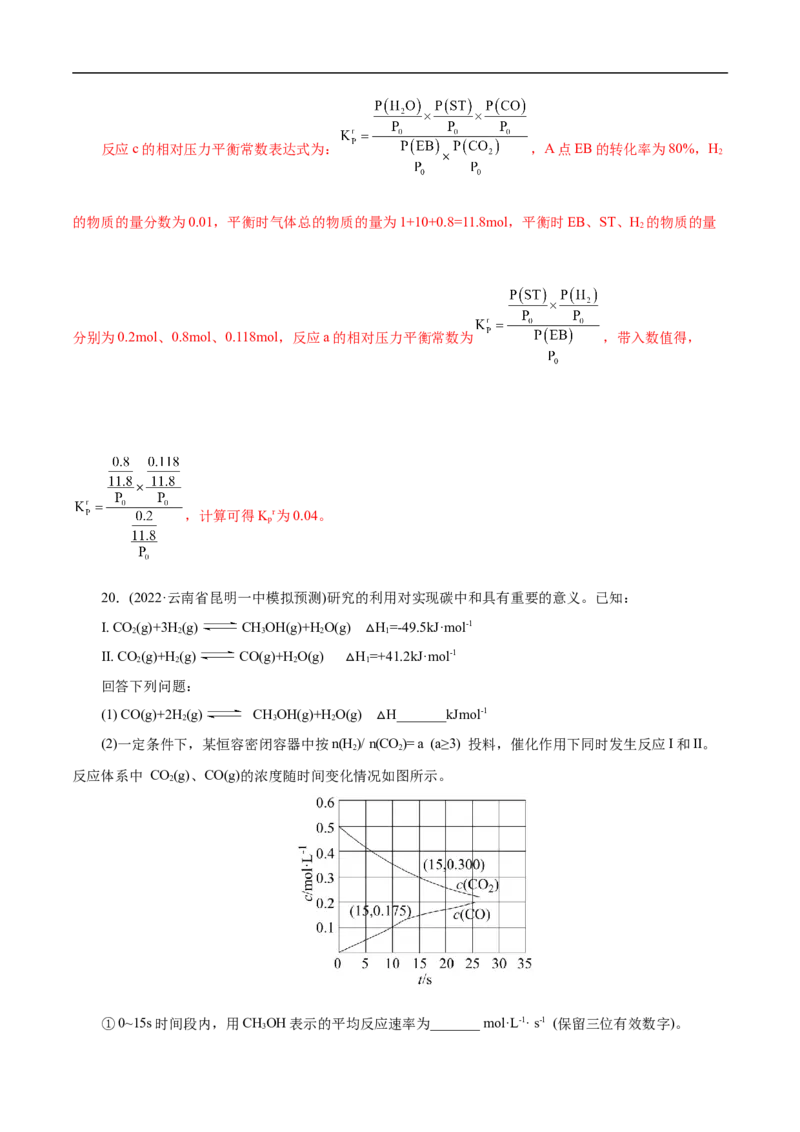
【解析】(1)根据盖斯定律,可知①式为②-3×③的结果,整理可得:a=489.0 kJ/mol-3×172.5
kJ/mol=-28.5 kJ/mol;对于反应①,在恒温恒容密闭容器中,平衡后充入CO,化学平衡逆向移动,CO的
2
转化率减小;由于化学平衡常数K= 只与温度有关,温度不变,化学平衡常数不变,该反应前后
气体体积相等,化学平衡常数不变,故平衡后体系中各组分的体积分数保持不变;(2)对于反应CaCO (s)
3
CaO(g)+CO(g),在恒温恒容下反应达到平衡状态,在t 时刻向平衡体系中充入1 mol CO ,化学平
1 2
衡逆向移动,但反应物为固体,正反应速率不变,因此逆反应速率突然增大后又随着CO 浓度的降低而减
2小直至不变。用图象表示为: ;(3)①对于反应CO(g)+CH (g) 2CO(g)+2H(g),
2 4 2
在温度不变时,减小压强,化学平衡向气体体积增大的正反应方向移动,使CO 的转化率增大,根据图象
2
可知CO 的转化率:p>p,说明压强p >p ;②在温度为1100℃、压强为p 条件下,20 min时反应达
2 2 1 1 2 1
到平衡状态时,CO 的转化率为60%,即平衡时△n(CO)=1 mol×60%=0.6 mol,由于容器的容积是1 L,则
2 2
v(CO)= =0.03 mol·L-1·min-1,由于同一反应用不同物质表示反应速率时,速率比等于方程式
2
中相应物质的化学计量数的比,所以v(CH)= v(CO)=0.03 mol/(L·min );反应中CO、CH 是按1:1关系
4 2 2 4
反应的,开始时加入的物质的量都是1 mol,则反应达到平衡时,n(CH)= n(CO)=0.4 mol,n(CO)=
4 2
n(H )=2×0.6mol= 1.2 mol,n(总)=0.4 mol+0.4 mol+1.2 mol+1.2 mol=3.2 mol,则用压强分数表示是化学平衡
2
常数表示为 。
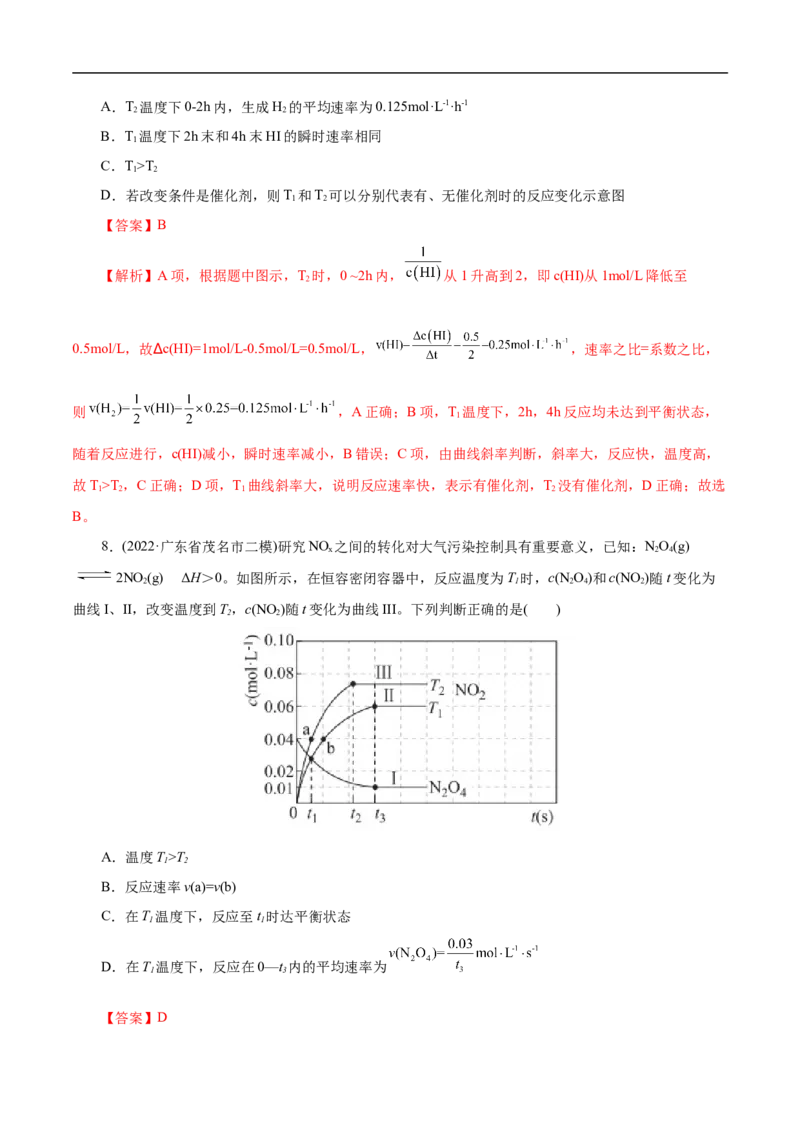
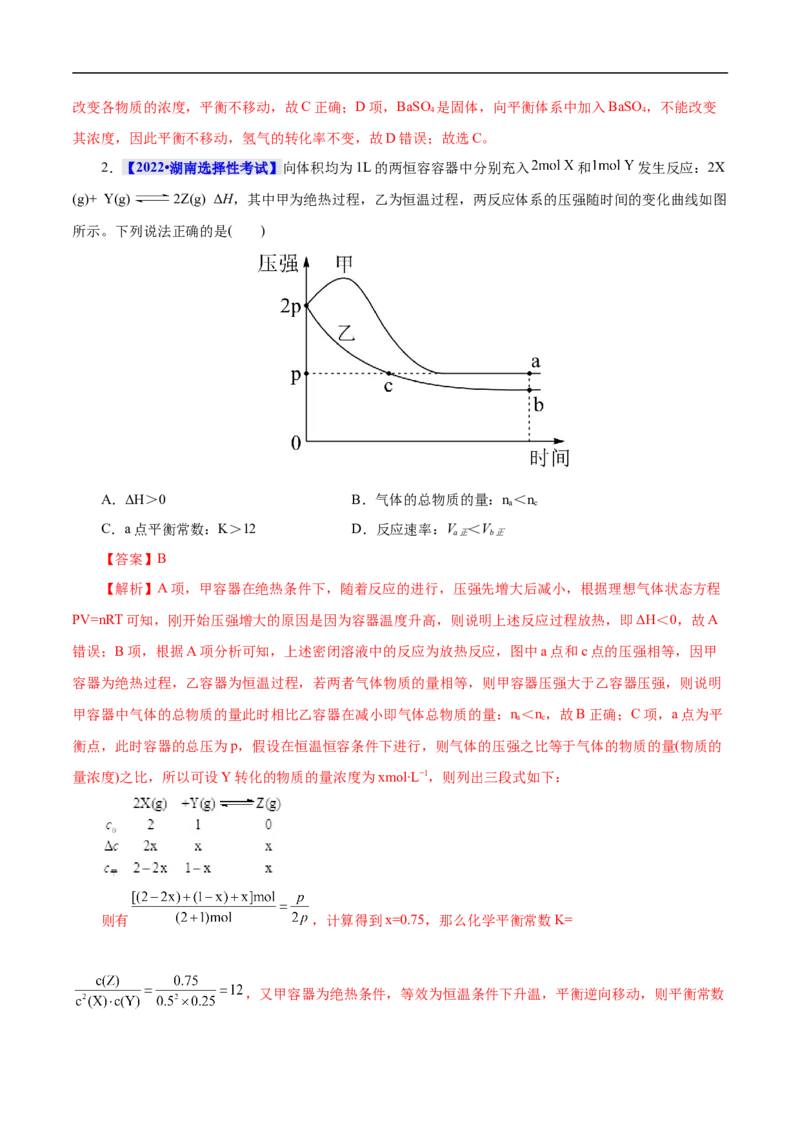
1.(2022·重庆市高三模拟预测)绿水青山是习总书记构建美丽中国的伟大构想,因此国家加大了对氮
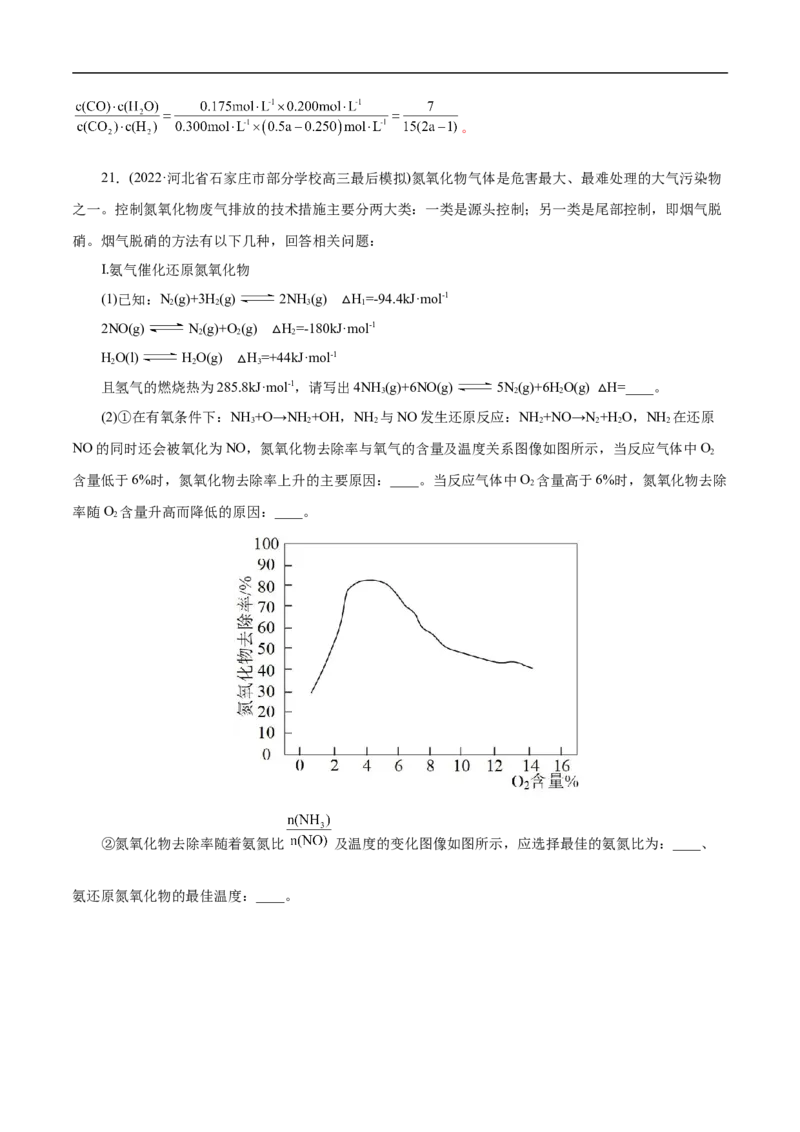
氧化物排放的控制力度。用活性炭还原处理氮氧化物的有关反应为C(s)+2NO(g) N(g)+CO (g) ΔH
2 2
<0。向容积可变的密闭容器中加入(足量的)活性炭和NO,在t 时刻改变某一条件,其反应的速率时间图
2
象如下图所示。下列说法正确的是( )A.给该反应升温, 减小, 增大
B.t 时刻改变的条件是向密闭容器中加NO
2
C.t 时刻的 大于t 时刻的
1 2
D.若气体的密度不变,不能说明该反应达到平衡
【答案】B
【解析】A项,升高温度,任何反应的反应速率均增大,故给该反应升温, 增大, 增大,A错
误;B项,由图像可知,压强一定条件下,t 时刻改变条件以后,逆反应速率突然减小,达到新平衡时,
2
与原反应速率相同,故改变的条件是向密闭容器中加NO,B正确;C项,由B项分析可知,t2时刻改变的
条件是向密闭容器中加NO,正反应速率增大,逆反应速率减小,则t 时刻的 小于t 时刻的 ,C错误;
1 2
D项,由题干反应方程式可知,反应前后气体的物质的量保持不变,即恒温下容器的体积保持不变,反应
正向气体质量增加,故若气体的密度不变,则气体质量不变,说明该反应达到平衡,D错误;故选B。
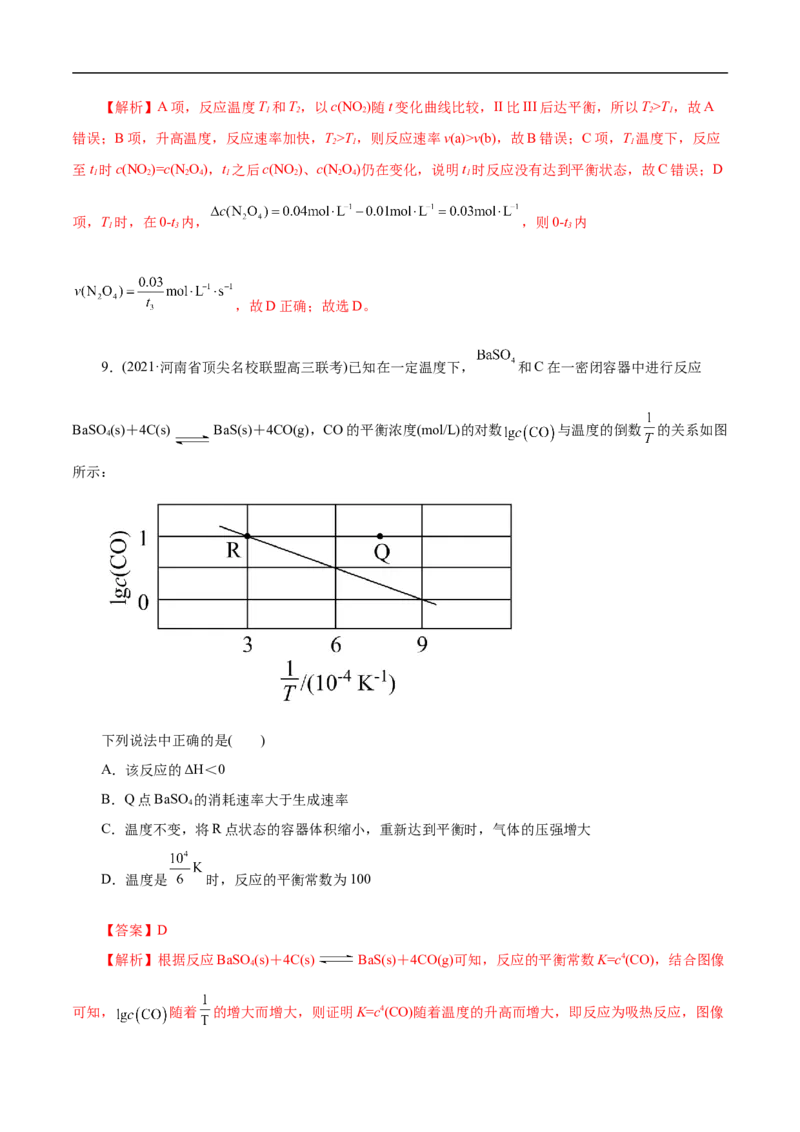
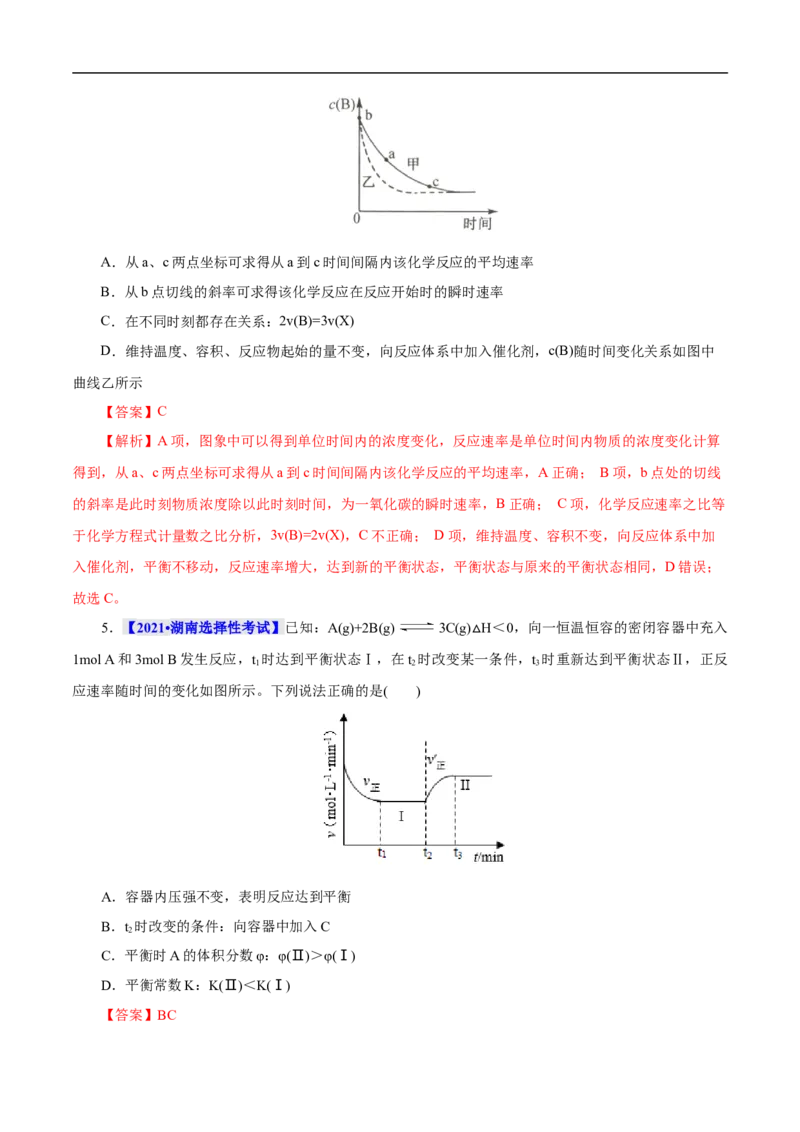
2.(2022·河南省郑州市四中第三次调研)T ℃时,向容积为2L的恒容密闭容器中充入SO 和O 发生反
1 2 2
应2SO (g)+O(g) 2SO (g),容器中各组分的物质的量随时间变化如图所示。下列说法正确的是( )
2 2 3
A.a、b两点反应速率υ<υ
a bB.0~t 时间段,反应速率υ(SO )= mol∙L−1∙min−1
2 3
C.t 时刻,向容器中充入一定体积的气体氦,使容器中气体总的压强增大,则υ 、υ 均增大
2 正 逆
D.若反应在T℃进行(T <T),反应进行t 分钟后,n(SO )<0.8mol
2 2 1 1 2
【答案】B
【解析】A项,根据浓度越大,反应速率越大,因此a、b两点反应速率υ<υ,故A错误;B项,根
b a
据图中改变量之比等于计量系数之比得到0~t 时间段SO 物质的量改变量为0.8mol,则0~t 时间段,反
2 3 2
应速率υ(SO )= mol∙L−1∙min−1,故B正确;C项,t 时刻,向容器中充入一定体积的气体氦,
3 2
使容器中气体总的压强增大,但反应各物质浓度没有改变,因此υ 、υ 均不变,故C错误;D项,若反
正 逆
应在T℃进行(T <T),根据温度越高,反应速率越快,T℃的速率比T℃的速率慢,因此反应进行t 分钟
2 2 1 2 1 1
后,SO 物质的量改变量小于0.2mol,因此n(SO ) >0.8mol,故D错误。故选B。
2 2
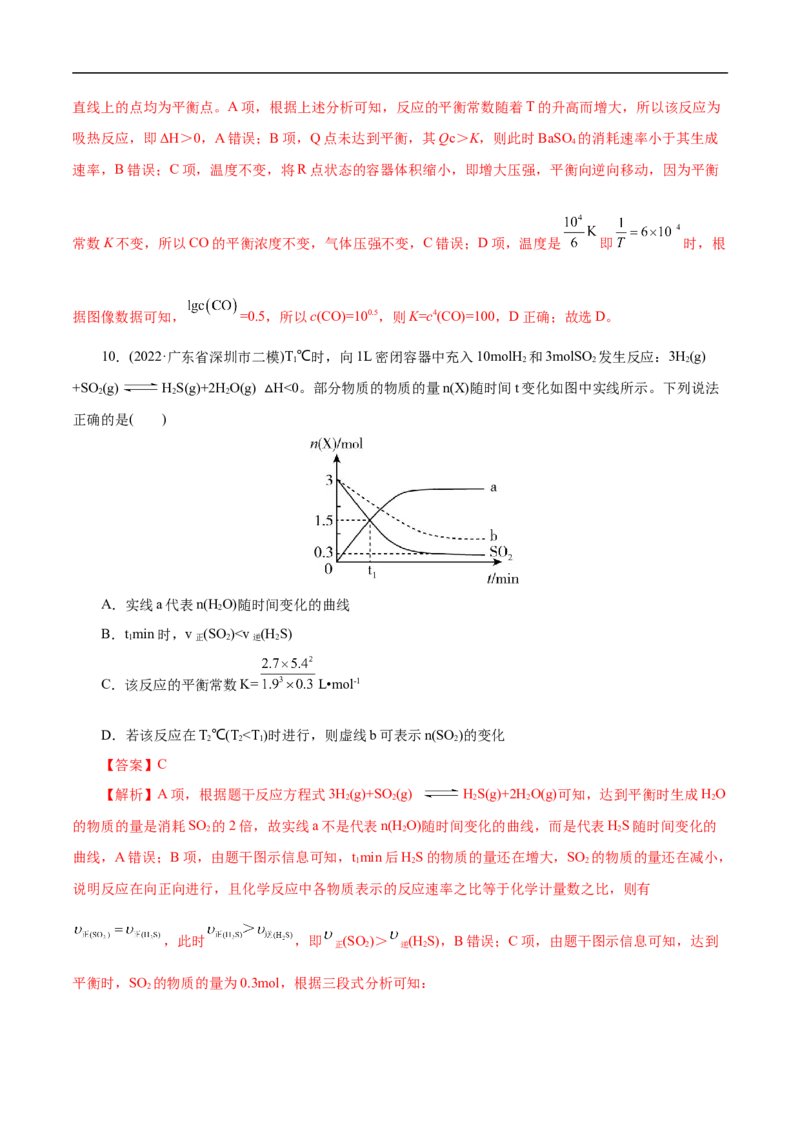
3.(2022·浙江省稽阳联谊学校高三下学期4月联考)25℃时,将20mL3x mol·L-1NaAsO、20mL3x
3 3
mol·L-1I 和20mL NaOH溶液混合,发生反应:AsO3−(aq)+I(aq)+ 2OH−(aq)= AsO3−(aq)+2I(aq)+
2 3 2 4 -
HO(l)。溶液中c(AsO3−)与反应时间(t)的关系如图所示。下列说法正确的是
2 4
A.0~ t min用HO表示的平均反应速率为
1 2
B.当2v (AsO3−)=v (I-)时,反应达到平衡状态
正 3 逆
C.a点的逆反应速率小于b点的正反应速率
D.平衡时溶液的pH=13,则该反应的平衡常数
【答案】C
【解析】A项,一般不用纯固体、纯液体表示反应速率,不能用HO表示该反应的平均反应速率,故
2A错误;B项,依据反应速率之比等于化学计量数之比,当2v (AsO3−)=v (I-)时,正逆反应速率相等,反
正 3 逆
应达到平衡状态,故B错误;C项,由图可知,a到b的过程中,反应一直正向进行,正反应速率一直减
小,逆反应速率一直增大,直到增大到与正反应速率相等,反应达到平衡状态,在反应达到平衡前,逆反
应速率均小于正反应速率,a点和b点均未达到平衡状态,且a到b反应逐渐趋于平衡,a点的逆反应速率
小于b点的正反应速率,故C正确;D项,根据题意,溶液混合后起始时,c(AsO3−)= c(I-)= x mol·L-1,由
3
图可知, 平衡时c(AsO3−)=y mol·L-1,c(I)= 2y mol·L-1,c(AsO3−)= c(I)=(x- y) mol·L-1,平衡时溶液的
4 2 3 2
pH=13,则c(OH-)=0.1mol·L-1,反应的平衡常数 ,故D错误;故选
C。
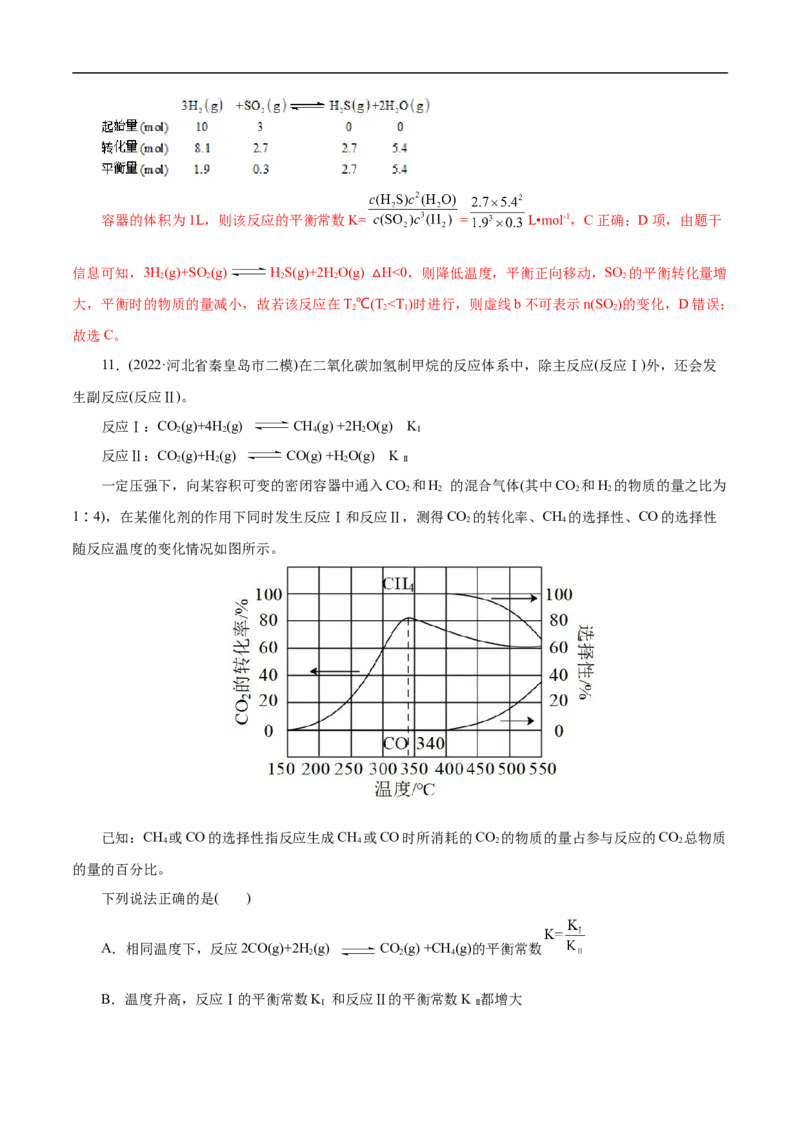
4.(2022·广东省惠州市高三第三次调研考试)已知:N(g)+3H(g) 2NH (g) ΔH= -m kJ·mol-1.在 2
2 2 3
L 容积不变的密闭容器中通入 1 mol N 和3 molH ,在温度分别为T T 下,测得NH 的产率随时间变
2 2 1 、 2 3
化如图。下列说法正确的是( )
A.T﹥T,ΔH﹥0
2 1
B.a,b两点的反应速率: >
a b
C.平衡时,通入氩气平衡正向移动
D.达到平衡时,放出热量为 m kJ
【答案】B
【解析】A项,由题干图示信息可知,T 条件下先达到平衡,说明T 时反应速率快,故有T﹥T,温
2 2 2 1
度越高,NH 的百分含量越小,说明升高温度,平衡逆向移动,故ΔH<0,A错误;B项,a,b两点对应
3
的温度分别是T、T,由A项分析可知,T﹥T,故反应速率:v >v ,B正确;C项,由题干信息可知,
2 1 2 1 a b
容器为恒温恒容,故平衡时,通入氩气反应体系各物质的浓度均不改变,正逆反应速率仍然相等,故平衡
不移动,C错误;D项,由于该反应是一个可逆反应,在 2 L 容积不变的密闭容器中通入 1 mol N 和3
2
molH ,达到平衡时,不可能完全进行,则放出热量小于 m kJ,D错误;故选B。
2
5.(2022·重庆市一中高三考前适应性考试)已知:2NO(g)+CO(g) 2NO (g)的反应历程分两步:
2 2第1步:2NO(g) NO(g) (快) ΔH<0
2 2 1
第2步:NO(g)+O(g) 2NO (g) (慢) ΔH<0
2 2 2 2 2
在固定容积的容器中充入一定量NO和O 发生上述反应,测得体系中部分物质的物质的量(n)随温度
2
(T)的变化如图所示。下列说法错误的是( )
A.第1步、第2步正反应活化能分别为E、E,则E<E
1 2 1 2
B.a点后,n(N O)迅速减小的原因是第1步平衡逆向移动,第2步速率加快
2 2
C.b点后,n(N O)增加的原因是第2步平衡逆向移动的程度比第1步的大
2 2
D.若其他条件不变,仅将容器变为恒压状态,则体系建立平衡的时间不变
【答案】D
【解析】A项,第2步是慢反应,由活化能越大反应速率越慢,可知第2步正反应活化能较大,则E
1
<E,A正确;B项,总反应速率由慢反应即第2步反应决定,a点后,n(N O)迅速减小说明第2步速率加
2 2 2
快,且第1步平衡逆向移动,B正确;C项,b点后,n(N O)增加说明第2步平衡逆向移动,生成的
2 2
n(N O)比第1步平衡逆向移动消耗的速率快,则原因是第2步平衡逆向移动的程度比第1步的大,C正确;
2 2
D项,若其他条件不变,仅将容器变为恒压状态,由于反应前后气体分子数不相等,恒压下会导致容器体
积变化,进而导致物质的浓度发生变化,反应速率发生变化,则体系建立平衡的时间改变,D错误;故选
D。
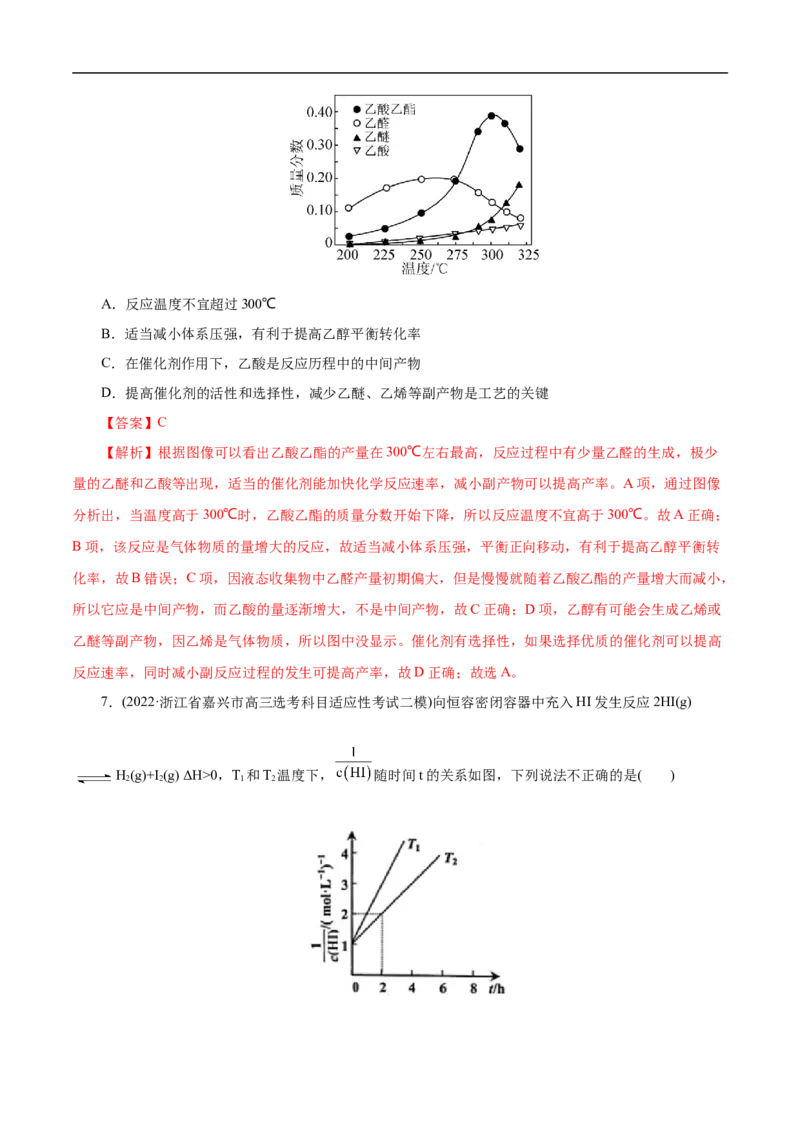
6.(2022·江苏省南京师大附中高三模拟)科学家研究了乙醇催化合成乙酸乙酯的新方法:2C HOH(g)
2 5
CHCOOC H(g) +2H (g),在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分
3 2 5 2
数如图所示。关于该方法,下列推测不合理的是( )A.反应温度不宜超过300℃
B.适当减小体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙酸是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
【答案】C
【解析】根据图像可以看出乙酸乙酯的产量在300℃左右最高,反应过程中有少量乙醛的生成,极少
量的乙醚和乙酸等出现,适当的催化剂能加快化学反应速率,减小副产物可以提高产率。A项,通过图像
分析出,当温度高于300℃时,乙酸乙酯的质量分数开始下降,所以反应温度不宜高于300℃。故A正确;
B项,该反应是气体物质的量增大的反应,故适当减小体系压强,平衡正向移动,有利于提高乙醇平衡转
化率,故B错误;C项,因液态收集物中乙醛产量初期偏大,但是慢慢就随着乙酸乙酯的产量增大而减小,
所以它应是中间产物,而乙酸的量逐渐增大,不是中间产物,故C正确;D项,乙醇有可能会生成乙烯或
乙醚等副产物,因乙烯是气体物质,所以图中没显示。催化剂有选择性,如果选择优质的催化剂可以提高
反应速率,同时减小副反应过程的发生可提高产率,故D正确;故选A。
7.(2022·浙江省嘉兴市高三选考科目适应性考试二模)向恒容密闭容器中充入HI发生反应2HI(g)
H(g)+I (g) ΔH>0,T 和T 温度下, 随时间t的关系如图,下列说法不正确的是( )
2 2 1 2A.T 温度下0-2h内,生成H 的平均速率为0.125mol·L-1·h-1
2 2
B.T 温度下2h末和4h末HI的瞬时速率相同
1
C.T>T
1 2
D.若改变条件是催化剂,则T 和T 可以分别代表有、无催化剂时的反应变化示意图
1 2
【答案】B
【解析】A项,根据题中图示,T 时,0 ~2h内, 从1升高到2,即c(HI)从1mol/L降低至
2
0.5mol/L,故∆c(HI)=1mol/L-0.5mol/L=0.5mol/L, ,速率之比=系数之比,
则 ,A正确;B项,T 温度下,2h,4h反应均未达到平衡状态,
1
随着反应进行,c(HI)减小,瞬时速率减小,B错误;C项,由曲线斜率判断,斜率大,反应快,温度高,
故T>T,C正确;D项,T 曲线斜率大,说明反应速率快,表示有催化剂,T 没有催化剂,D正确;故选
1 2 1 2
B。
8.(2022·广东省茂名市二模)研究NO 之间的转化对大气污染控制具有重要意义,已知:NO(g)
x 2 4
2NO (g) ΔH>0。如图所示,在恒容密闭容器中,反应温度为T 时,c(N O)和c(NO )随t变化为
2 1 2 4 2
曲线I、II,改变温度到T,c(NO )随t变化为曲线III。下列判断正确的是( )
2 2
A.温度T>T
1 2
B.反应速率v(a)=v(b)
C.在T 温度下,反应至t 时达平衡状态
1 1
D.在T 温度下,反应在0—t 内的平均速率为
1 3
【答案】D【解析】A项,反应温度T 和T,以c(NO )随t变化曲线比较,II比III后达平衡,所以T>T,故A
1 2 2 2 1
错误;B项,升高温度,反应速率加快,T>T,则反应速率v(a)>v(b),故B错误;C项,T 温度下,反应
2 1 1
至t 时c(NO )=c(N O),t 之后c(NO )、c(N O)仍在变化,说明t 时反应没有达到平衡状态,故C错误;D
1 2 2 4 1 2 2 4 1
项,T 时,在0-t 内, ,则0-t 内
1 3 3
,故D正确;故选D。
9.(2021·河南省顶尖名校联盟高三联考)已知在一定温度下, 和C在一密闭容器中进行反应
BaSO(s)+4C(s) BaS(s)+4CO(g),CO的平衡浓度(mol/L)的对数 与温度的倒数 的关系如图
4
所示:
下列说法中正确的是( )
A.该反应的ΔH<0
B.Q点BaSO 的消耗速率大于生成速率
4
C.温度不变,将R点状态的容器体积缩小,重新达到平衡时,气体的压强增大
D.温度是 时,反应的平衡常数为100
【答案】D
【解析】根据反应BaSO(s)+4C(s) BaS(s)+4CO(g)可知,反应的平衡常数K=c4(CO),结合图像
4
可知, 随着 的增大而增大,则证明K=c4(CO)随着温度的升高而增大,即反应为吸热反应,图像直线上的点均为平衡点。A项,根据上述分析可知,反应的平衡常数随着T的升高而增大,所以该反应为
吸热反应,即ΔH>0,A错误;B项,Q点未达到平衡,其Qc>K,则此时BaSO 的消耗速率小于其生成
4
速率,B错误;C项,温度不变,将R点状态的容器体积缩小,即增大压强,平衡向逆向移动,因为平衡
常数K不变,所以CO的平衡浓度不变,气体压强不变,C错误;D项,温度是 即 时,根
据图像数据可知, =0.5,所以c(CO)=100.5,则K=c4(CO)=100,D正确;故选D。
10.(2022·广东省深圳市二模)T ℃时,向1L密闭容器中充入10molH 和3molSO 发生反应:3H(g)
1 2 2 2
+SO(g) HS(g)+2HO(g) H<0。部分物质的物质的量n(X)随时间t变化如图中实线所示。下列说法
2 2 2
正确的是( ) △
A.实线a代表n(H O)随时间变化的曲线
2
B.tmin时,v (SO )0
C.b、d两状态下,化学反应速率相等
D.d状态下,保持其他条件不变,向容器中再加入1molCO 与0.5molC H,v(正) p > p > p 4p 2/9
4 3 2 1 4
(4) ④ ③
(5)CO +H O+2e-=HCOO-+OH-
2 2
【解析】(1)①CH(g)+2O(g)=CO (g)+2HO(g) ΔH=a kJ•mol-1;②CO(g)+H(g)=CO(g)
4 2 2 2 1 2 2
+H O(g) ΔH=b kJ•mol-1;③2CO(g)+O(g)=2CO (g) ΔH=c kJ•mol-1;根据盖斯定律①-②×2-③×2得
2 2 2 2 3
CO(g)+CH (g) 2CO(g)+2H(g)的ΔH= akJ•mol-1 -2b kJ•mol-1-2c kJ•mol-1=(a-2b-2c)kJ/mol;(2)温度超
2 4 2 4过250℃,催化剂的催化效率降低,所以250~300℃时,温度升高而乙酸的生成速率降低。(3)①正反应气
体物质的量增大,增大压强,平衡逆向移动,甲烷转化率降低,由图可知,p、p、p、p 由大到小的顺序
1 2 3 4
为p > p > p > p 。②在压强为p、投料比n(CH)/n(CO)为1、950℃的条件下,甲烷的转化率为50%;
4 3 2 1 4 4 2
则:
X点平衡常数K= ;(4)若反应CO(g)+H(g) CO(g)
p 2 2
+H O(g) ΔH=+41.17kJ•mol-1 的正、逆反应速率分别可表示为v =k c(CO)•c(H )、v =k
2 2 正 正 2 2 逆 逆
c(CO)•c(H O),升高温度,反应速率加快,k 、k 都增大,pk减小;反应达到平衡,k c(CO)•c(H )=k
2 正 逆 正 2 2 逆
c(CO)•c(H O), ,正反应吸热,升高温度,平衡正向移动,K增大,即 增大,
2
温度对k 影响更大,①②③④四条斜线中,能表示pk 随T变化关系的是斜线④,能表示pk 随T变化
正 正 逆
关系的是斜线③。(5)根据图示,二氧化碳在阴极得电子被还原为甲酸根离子,阴极的电极反应方程式
CO+H O+2e-=HCOO-+OH-。
2 2
23.(2022·重庆市缙云教育联盟高三第二次诊断性检测)工业生产中硫、氮、碳的氧化物排放都会导致
严重环境问题,对这些物质需要进行综合利用。
(1)用CH 催化还原煤燃烧产生的氮氧化物,可以消除污染。已知:
4
CH(g)+2NO (g)=N(g)+CO (g)+2HO(g) H=-867.0kJ•mol-1。
4 2 2 2 2 1
△
NO (g)= NO(g) H=-28.5kJ•mol-1。
2 2 4 2
△
写出CH 催化还原NO(g)生成CO、N 和HO(g)的热化学方程式____。
4 2 4 2 2 2
(2)以CO、H 为原料合成乙烯的方程式为:2CO(g)+6H(g) C H(g)+4HO(g) H。在常压下,按
2 2 2 2 2 4 2
n(CO):n(H )=1:3(总物质的量为4amol)的投料比充入恒压密闭容器中发生反应。测得△温度对CO 的平衡
2 2 2
转化率和催化剂催化效率影响情况如图1所示。下列说法正确的是____。
A.△H<0;平衡常数:K >K
M N
B.若改用其他催化剂,可能会加快反应速率,但同时会影响平衡转化率
C.若投料比改为n(CO):n(H )=1:4,可以提高CO 的平衡转化率
2 2 2
D.在250℃时,若气体的平均相对分子质量不再改变,说明反应已经平衡
(3)250℃下,上述反应开始时容器体积为VL,在此温度下达到平衡时HO(g)浓度为____mol/L。(用含
2
a、V的代数式表示)
(4)某温度下,n(C H)随时间(t)的变化趋势曲线如图2所示。若其它条件不变时,容器的体积为原来一
2 4
半,画出0~t 时刻n(C H)随时间(t)的变化趋势曲线____。
1 2 4
(5)据文献报道,CO 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是____。
2
【答案】(1)CH (g)+NO(g)=N(g)+CO (g)+2HO(g) H=-810kJ/mol
4 2 4 2 2 2
△
(2)ACD (3)(4)
(5)CO +8e-+6H O=CH+8OH-
2 2 4
【解析】(1)CH 催化还原NO(g)生成CO、N 和HO(g)的化学方程式为CH(g)+NO(g)=N(g)+CO (g)
4 2 4 2 2 2 4 2 4 2 2
+2H O(g),①CH(g)+2NO (g)=N(g)+CO (g)+2HO(g) H=-867.0kJ•mol-1,NO (g)=
2 4 2 2 2 2 1 2
△
NO(g) H=-28.5kJ•mol-1,根据盖斯定律 计算CH(g)+NO(g)=N(g)+CO (g)+2HO(g)的
2 4 2 4 2 4 2 2 2
△
△H=-867kJ/mol-(-28.5kJ/mol)×2=-810kJ/mol,即热化学方程式为CH(g)+NO(g)=N(g)+CO (g)+2HO(g)
4 2 4 2 2 2
H=-810kJ/mol;(2)A项,由图可知,CO 的平衡转化率随温度的升高而降低,则升高温度平衡逆向移动,
2
△即ΔH<0,温度越高该反应的平衡常数K越小,所以K >K ,故A正确;B项,催化剂能加快反应速率,
M N
但不改变化学平衡移动方向,不会影响转化率,故B错误;C项,若投料比改为n(CO):n(H )=1:4,相
2 2
当增大c(H ),可使平衡正向移动,提高CO 的平衡转化率,故C正确;D项,该反应正向是气体体积减小
2 2
的反应,容器中气体的质量不变,若气体的平均相对分子质量不再改变,则气体的总物质的量不变,说明
反应已经平衡,故D正确;故选ACD;(3)图中250℃时CO 的平衡转化率为50%,反应三段式:
2
恒温恒压条件下,气体的体积之比等于物质的量之比,平衡时气体的总体积 ,
所以平衡时HO(g)浓度为 ;(4)其它条件不变时,容器的体积为原来一半,相当增大压
2强一倍,反应速率加快、达到平衡的时间缩短,图象如图 ;(5)CO 可
2
以在碱性水溶液中电解生成甲烷,则CO 在阴极发生还原反应生成CH,阴极反应式为CO+8e-
2 4 2
+6H O=CH+8OH-。
2 4
1.【2022•广东选择性考试】恒容密闭容器中,BaSO(s)+4H(g) BaS(s)+4HO(g)在不同温度下
4 2 2
达平衡时,各组分的物质的量(n)如图所示。下列说法正确的是( )
A.该反应的ΔH<0
B.a为n(H O)随温度的变化曲线
2
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入BaSO,H 的平衡转化率增大
4 2
【答案】C
【解析】A项,从图示可以看出,平衡时升高温度,氢气的物质的量减少,则平衡正向移动,说明该
反应的正反应是吸热反应,即ΔH>0,故A错误; B项,从图示可以看出,在恒容密闭容器中,随着温
度升高氢气的平衡时的物质的量减少,则平衡随着温度升高正向移动,水蒸气的物质的量增加,而a曲线
表示的是物质的量不随温度变化而变化,故B错误;C项,容器体积固定,向容器中充入惰性气体,没有改变各物质的浓度,平衡不移动,故C正确;D项,BaSO 是固体,向平衡体系中加入BaSO,不能改变
4 4
其浓度,因此平衡不移动,氢气的转化率不变,故D错误;故选C。
2.【2022•湖南选择性考试】向体积均为1L的两恒容容器中分别充入 和 发生反应:2X
(g)+ Y(g) 2Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图
所示。下列说法正确的是( )
A.ΔH>0 B.气体的总物质的量:n<n
a c
C.a点平衡常数:K>12 D.反应速率:V <V
a正 b正
【答案】B
【解析】A项,甲容器在绝热条件下,随着反应的进行,压强先增大后减小,根据理想气体状态方程
PV=nRT可知,刚开始压强增大的原因是因为容器温度升高,则说明上述反应过程放热,即ΔH<0,故A
错误;B项,根据A项分析可知,上述密闭溶液中的反应为放热反应,图中a点和c点的压强相等,因甲
容器为绝热过程,乙容器为恒温过程,若两者气体物质的量相等,则甲容器压强大于乙容器压强,则说明
甲容器中气体的总物质的量此时相比乙容器在减小即气体总物质的量:n<n,故B正确;C项,a点为平
a c
衡点,此时容器的总压为p,假设在恒温恒容条件下进行,则气体的压强之比等于气体的物质的量(物质的
量浓度)之比,所以可设Y转化的物质的量浓度为xmol∙L−1,则列出三段式如下:
则有 ,计算得到x=0.75,那么化学平衡常数K=
,又甲容器为绝热条件,等效为恒温条件下升温,平衡逆向移动,则平衡常数减小即平衡常数K<12,故C错误;D项,根据图像可知,甲容器达到平衡的时间短,温度高,所以达到
平衡的速率相对乙容器的快,即V >V ,故D错误。故选B。
a正 b正
3.【2022•广东选择性考试】在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随
反应时间t的部分变化曲线如图,则( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1
【答案】D
【解析】A项,由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故
A错误;B项,由图可知,催化剂I比催化剂II催化效果好,说明催化剂I使反应活化能更低,反应更快,
故B错误;C项,由图可知,使用催化剂II时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的
X的浓度变化了2.0mol/L,二者变化量之比不等于化学计量数之比,所以a曲线不表示使用催化剂II时X
浓度随时间t的变化,故C错误;D项,使用催化剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则v
(Y) = = =2.0 mol·L-1·min-1,v (X) = (Y) = 2.0 mol·L-1·min-1=1.0 mol·L-1·min-1,故
D正确;故选D。
4.【2022·浙江省1月选考】在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变
化如图中曲线甲所示。下列说法不正确的是( )A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中
曲线乙所示
【答案】C
【解析】A项,图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算
得到,从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率,A正确; B项,b点处的切线
的斜率是此时刻物质浓度除以此时刻时间,为一氧化碳的瞬时速率,B正确; C项,化学反应速率之比等
于化学方程式计量数之比分析,3v(B)=2v(X),C不正确; D项,维持温度、容积不变,向反应体系中加
入催化剂,平衡不移动,反应速率增大,达到新的平衡状态,平衡状态与原来的平衡状态相同,D错误;
故选C。
5.【2021•湖南选择性考试】已知:A(g)+2B(g) 3C(g) H<0,向一恒温恒容的密闭容器中充入
1mol A和3mol B发生反应,t 时达到平衡状态Ⅰ,在t 时改变某△一条件,t 时重新达到平衡状态Ⅱ,正反
1 2 3
应速率随时间的变化如图所示。下列说法正确的是( )
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(Ⅱ)>φ(Ⅰ)
D.平衡常数K:K(Ⅱ)<K(Ⅰ)
【答案】BC【解析】A项,为气体体积不变的反应,反应前后气体的物质的量不变,则压强始终不变,不能判定
平衡状态,故A错误;B项,t 时正反应速率瞬间不变,然后增大,可知改变的条件为向容器中加入C,
2
故B正确;C项,t 时加入C,平衡逆向移动,则平衡时A的体积分数φ:φ(Ⅱ)>φ(I),故C正确;D项,
2
平衡常数与温度有关,温度不变,则平衡常数K:K(Ⅱ)=K(Ⅰ),故D错误;故选BC。
6.【2021•辽宁选择性考试】某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓
度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
【答案】B
【解析】A项,由题干图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间更
短,故反应速率越大,A正确;B项,由题干图中曲线①③可知,其他条件相同时,降冰片烯浓度①是③
的两倍,所用时间①也是③的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,B错误;C项,
由题干图中数据可知,条件①,反应速率为 =0.012 mol·L-1·min-1,C正确;D
项,反应物消耗一半所需的时间称为半衰期,由题干图中数据可知,条件②,降冰片烯起始浓度为3.0
mol·L-1时,半衰期为125min÷2=62.5 min,D正确;故选B。
7.【2020•江苏卷】CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
CH(g)+CO(g)=2H (g)+2CO(g) ΔH=247.1kJ·mol-1
4 2 2H(g)+CO(g)=HO (g)+CO(g) ΔH=41.2kJ·mol-1
2 2 2
在恒压、反应物起始物质的量比n(CH):n(CO)=1:1条件下,CH 和CO 的平衡转化率随温度变化的
4 2 4 2
曲线如图所示。下列有关说法正确的是( )
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线B表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800K、n(CH):n(CO)=1:1条件下,反应至CH 转化率达到X点的值,改变除温度外的
4 2 4
特定条件继续反应,CH 转化率能达到Y点的值
4
【答案】BD
【解析】A项,甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应即正向移动,甲烷转化
率增大,甲烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,故A错误;
B项,根据两个反应得到总反应为CH(g)+2CO(g) == H (g)+3CO(g) +HO (g),加入的CH 与CO 物质
4 2 2 2 4 2
的量相等,CO 消耗量大于CH,因此CO 的转化率大于CH,因此曲线B表示CH 的平衡转化率随温度
2 4 2 4 4
变化,故B正确;C项,使用高效催化剂,只能提高反应速率,但不能改变平衡转化率,故C错误;D项,
800K时甲烷的转化率为X点,可以通过改变二氧化碳的量来提高甲烷的转化率达到Y点的值,故D正确。
故选BD。
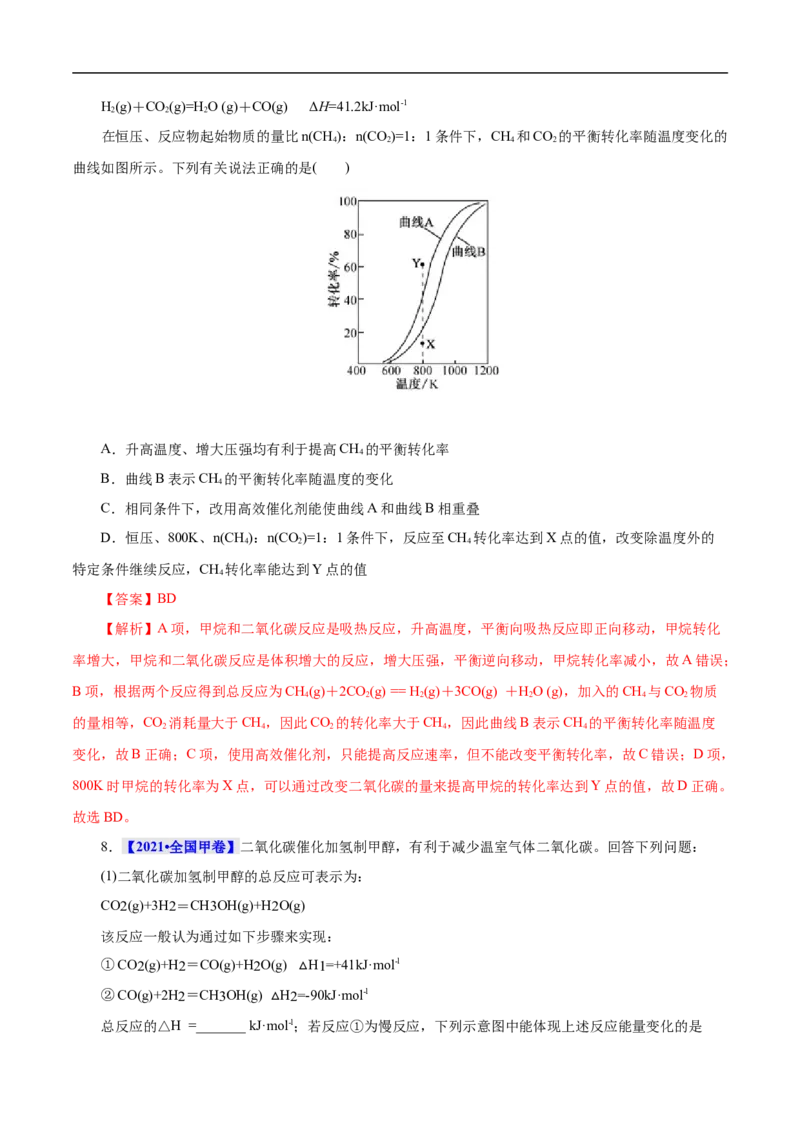
8.【2021•全国甲卷】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
CO2(g)+3H2=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2=CO(g)+H2O(g) H1=+41kJ·mol-l
②CO(g)+2H2=CH3OH(g) H2=△-90kJ·mol-l
总反应的△H =_______ kJ·m△ol-l;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是_______(填标号),判断的理由是_______。
A. B.
C. D.
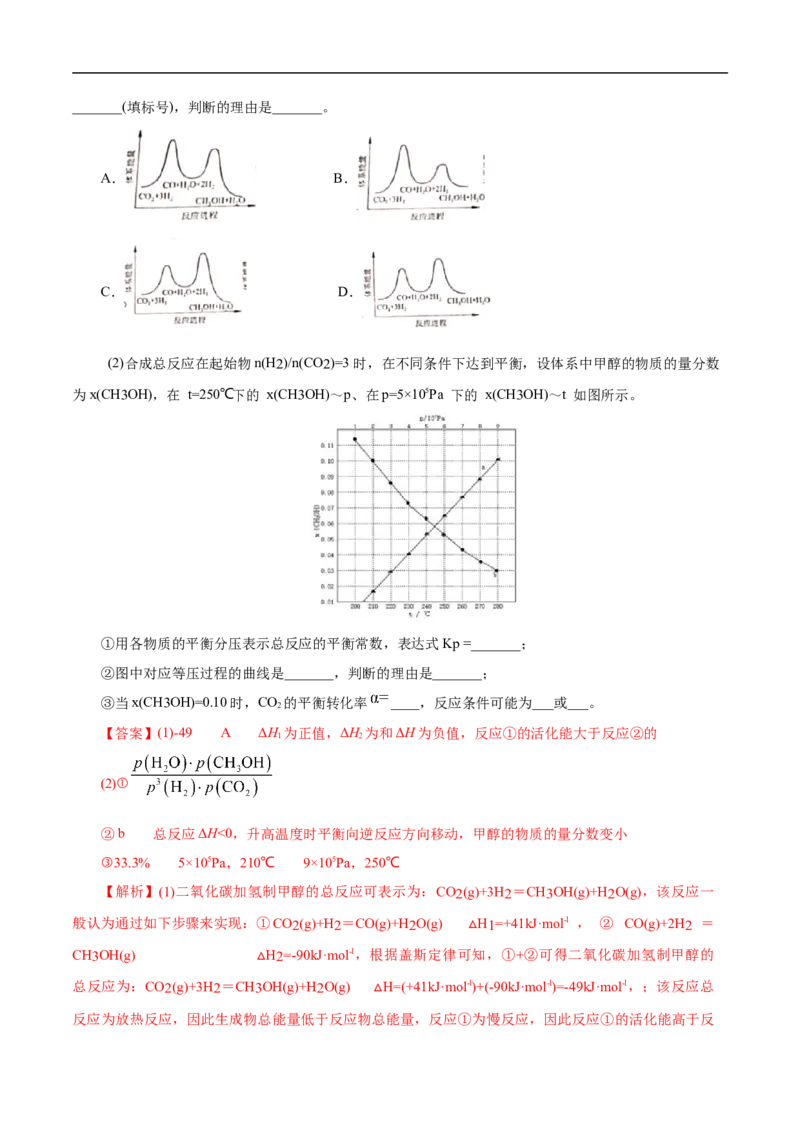
(2)合成总反应在起始物n(H2)/n(CO2)=3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数
为x(CH3OH),在 t=250℃下的 x(CH3OH)~p、在p=5×105Pa 下的 x(CH3OH)~t 如图所示。
①用各物质的平衡分压表示总反应的平衡常数,表达式Kp =_______;
②图中对应等压过程的曲线是_______,判断的理由是_______;
③当x(CH3OH)=0.10时,CO 的平衡转化率 ____,反应条件可能为___或___。
2
【答案】(1)-49 A ΔH 为正值,ΔH 为和ΔH为负值,反应①的活化能大于反应②的
1 2
(2)①
②b 总反应ΔH<0,升高温度时平衡向逆反应方向移动,甲醇的物质的量分数变小
③33.3% 5×105Pa,210℃ 9×105Pa,250℃
【解析】(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2=CH3OH(g)+H2O(g),该反应一
般认为通过如下步骤来实现:①CO2(g)+H2=CO(g)+H2O(g) H1=+41kJ·mol-l , ② CO(g)+2H2 =
CH3OH(g) H2=-90kJ·mol-l,根据盖斯定律可△知,①+②可得二氧化碳加氢制甲醇的
总反应为:CO2(g)+3H2=CH3△OH(g)+H2O(g) H=(+41kJ·mol-l)+(-90kJ·mol-l)=-49kJ·mol-l,;该反应总
反应为放热反应,因此生成物总能量低于反应物总△能量,反应①为慢反应,因此反应①的活化能高于反应②,同时反应①的反应物总能量低于生成物总能量,反应②的反应物总能量高于生成物总能量,因此
示意图中能体现反应能量变化的是A项。(2)①二氧化碳加氢制甲醇的总反应为CO2(g)+3H2=CH3OH(g)
+H2O(g),因此利用各物质的平衡分压表示总反应的平衡常数,表达式K = ;②
p
该反应正向为放热反应,升高温度时平衡逆向移动,体系中x(CH3OH)将减小,因此图中对应等压过程
的曲线是b;③设起始n(CO)=1mol,n(H )=3mol,则:
2 2
当平衡时x(CH3OH)=0.10时, =0.1,解得x=1/3mol,平衡时CO 的转化率α=
2
=33.3%;由图可知,满足平衡时x(CH3OH)=0.10的条件有:5×105Pa,210℃或9×105Pa,
250℃。
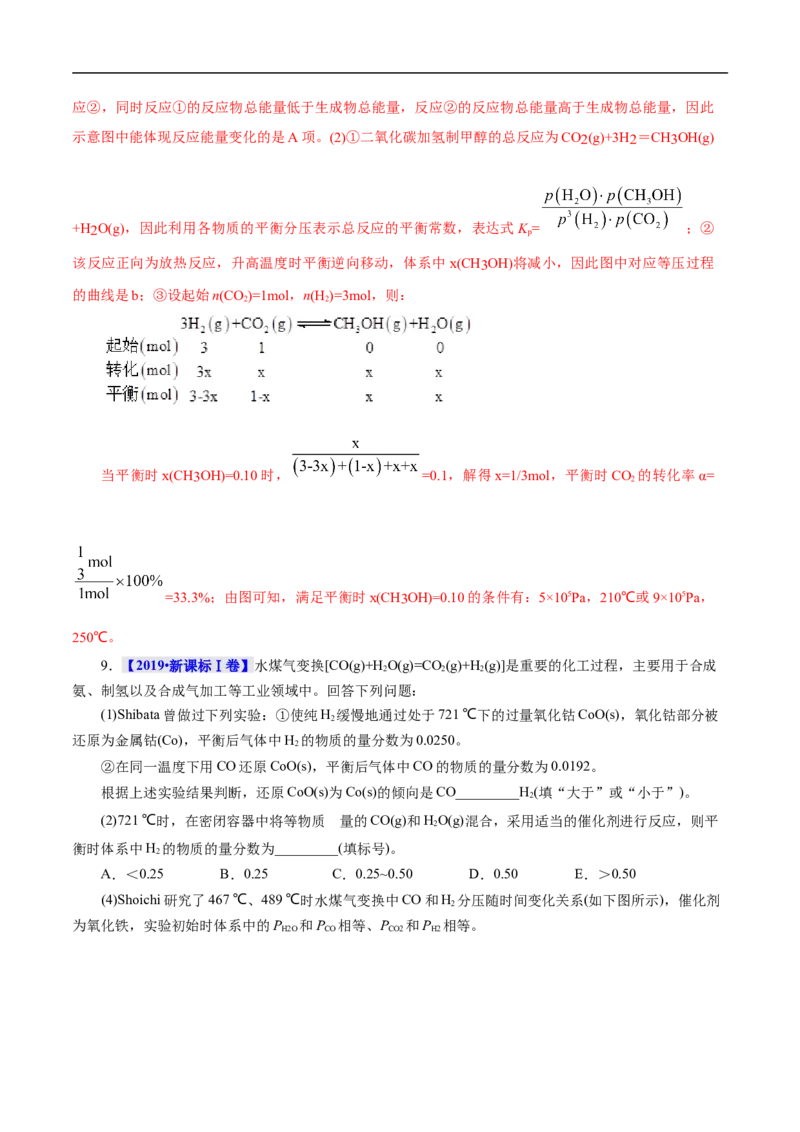
9.【2019•新课标Ⅰ卷】水煤气变换[CO(g)+H O(g)=CO(g)+H(g)]是重要的化工过程,主要用于合成
2 2 2
氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H 缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被
2
还原为金属钴(Co),平衡后气体中H 的物质的量分数为0.0250。
2
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H (填“大于”或“小于”)。
2
(2)721 ℃时,在密闭容器中将等物质 量的CO(g)和HO(g)混合,采用适当的催化剂进行反应,则平
2
衡时体系中H 的物质的量分数为_________(填标号)。
2
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H 分压随时间变化关系(如下图所示),催化剂
2
为氧化铁,实验初始时体系中的P 和P 相等、P 和P 相等。
H2O CO CO2 H2计算曲线a的反应在30~90 min内的平均速率 (a)=___________kPa·min−1。467 ℃时P 和P 随时间
H2 CO
变化关系的曲线分别是___________、___________。489 ℃时P 和P 随时间变化关系的曲线分别是
H2 CO
___________、___________。
【答案】 (1)大于 (2)C (4)0.0047 b c a d
【解析】(1)H 还原氧化钴的方程式为:H(g)+CoO(s)=Co(s)+HO(g);CO还原氧化钴的方程式为:
2 2 2
CO(g)+CoO(s)=Co(s)+CO(g),平衡时H 还原体系中H 的物质的量分数( )高于CO还原
2 2 2
体系中CO的物质的量分数( ),故还原CoO(s)为Co(s)的倾向是CO大于H;
2
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和HO(g)混合,可设其物质的量为1mol,则
2
CO(g)+HO(g) CO(g)+H(g)
2 2 2
起始(mol) 1 1 0 0
转化(mol) x x x x
平衡(mol) 1-x 1-x x x
则平衡时体系中H 的物质的量分数= ,因该反应为可逆反应,
2
故x<1,可假设二者的还原倾向相等,则x=0.5,由(1)可知CO的还原倾向大于H,所以CO更易转化为
2
H,故x>0.5,由此可判断最终平衡时体系中H 的物质的量分数介于0.25~0.50,故答案为C;(4)由图可知,
2 2
30~90 min内a曲线对应物质的分压变化量Δp=(4.08-3.80)kPa=0.28 kPa,故曲线a的反应在30~90 min内的
平均速率 (a)= =0.0047 kPa·min−1;由(2)中分析得出H 的物质的量分数介于0.25~0.5,CO的物
2
质的量分数介于0~0.25,即H 的分压始终高于CO的分压,据此可将图分成两部分:
2由此可知,A项,b表示的是H 的分压,C项,d表示的是CO的分压,该反应为放热反应,故升高温
2
度,平衡逆向移动,CO分压增加,H 分压降低,故467 ℃时P 和P 随时间变化关系的曲线分别是B项,
2 H2 CO
c;489 ℃时P 和P 随时间变化关系的曲线分别是A项,d。
H2 CO
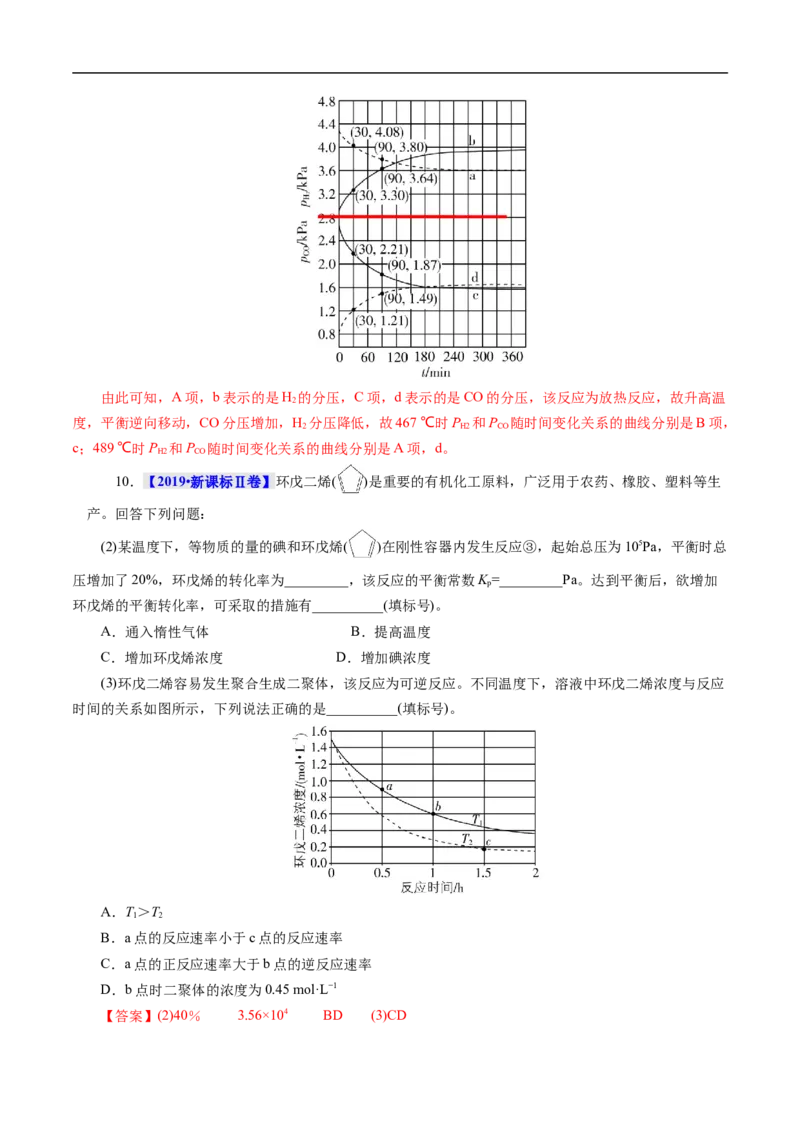
10.【2019•新课标Ⅱ卷】环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生
产。回答下列问题:
(2)某温度下,等物质的量的碘和环戊烯( )在刚性容器内发生反应③,起始总压为105Pa,平衡时总
压增加了20%,环戊烯的转化率为_________,该反应的平衡常数K =_________Pa。达到平衡后,欲增加
p
环戊烯的平衡转化率,可采取的措施有__________(填标号)。
A.通入惰性气体 B.提高温度
C.增加环戊烯浓度 D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应
时间的关系如图所示,下列说法正确的是__________(填标号)。
A.T>T
1 2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L−1
【答案】(2)40% 3.56×104 BD (3)CD【解析】(2)假设反应前碘单质与环戊烯均为nmol,平衡时环戊烯反应了xmol,根据题意可知:
(g)+I (g)= (g)+2HI(g) 增加的物质的量
2
1mol 1mol 1mol 2mol 1mol
xmol 2n×20%
得x=0.4nmol,转化率为0.4n/n×100%=40%;
(g) + I (g) = (g)+ 2HI(g)
2
P(初) 0.5×105 0.5×105 0 0
ΔP 0.5×105×40% 0.5×105×40% 0.5×105×40% 1×105×40%
P(平) 0.3×105 0.3×105 0.2×105 0.4×105
K= =3.56×104;A项,T、V一定,通入惰性气体,由于对反应物和生成物浓
p
度无影响,速率不变,平衡不移动,故A错误;B项,升高温度,平衡向吸热方向移动,环戊烯转化率升
高,故B正确;C项,增加环戊烯的浓度平衡正向移动,但环戊烯转化率降低;D项,增加I 的浓度,平
2
衡正向移动,环戊烯转化率升高,故D正确;(3)A项,温度越高,反应速率越快,其浓度下降的也越快。
因此Tv(逆),
a点反应物浓度大于b点,故a点正反应速率大于b点,因此v(正a)>v(逆b),故C正确;D项,.b点时环
戊二烯浓度由1.5mol/L减小到0.6mol/L,减少了0.9mol/L,因此生成二聚体0.45mol/L,故D正确;故选
CD