文档内容
考点 25 化学反应速率及其影响因素
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 化学反应速率及其计算...............................................................................................................2
考法02 影响化学反应速率的因素...........................................................................................................5
考法03 基元反应与反应机理...................................................................................................................8
...........................................................................................................................................11
1.高考真题考点分布
考点内容 考点分布
化学反应速率的 2024·河北卷,3分;2024·安徽卷,3分;2023·河北卷,3分;2022辽宁卷12题,3
概念及计算 分;2022浙江1月选考19题,2分;2022浙江6月选考20题,2分;
2024·甘肃卷,3分; 2024·安徽卷,3分;2023辽宁卷12题,3分;2022湖南卷12
影响化学反应速
题,4分;2022湖南卷14题,4分;2022北京卷14题,3分;2022河北卷11题,4
率的因素
分;
2024·北京卷,3分;2024·贵州卷,3分;2024·广东卷,3分;2024·甘肃卷,3分;
催化剂与反应机
2024·安徽卷,3分;2023·广东卷,3分;2023·湖南卷,3分;2023·新课标卷,3
理
分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,化学反应速率的计算和外界条件对化学反应速率的影响仍是高考命
题的热点。
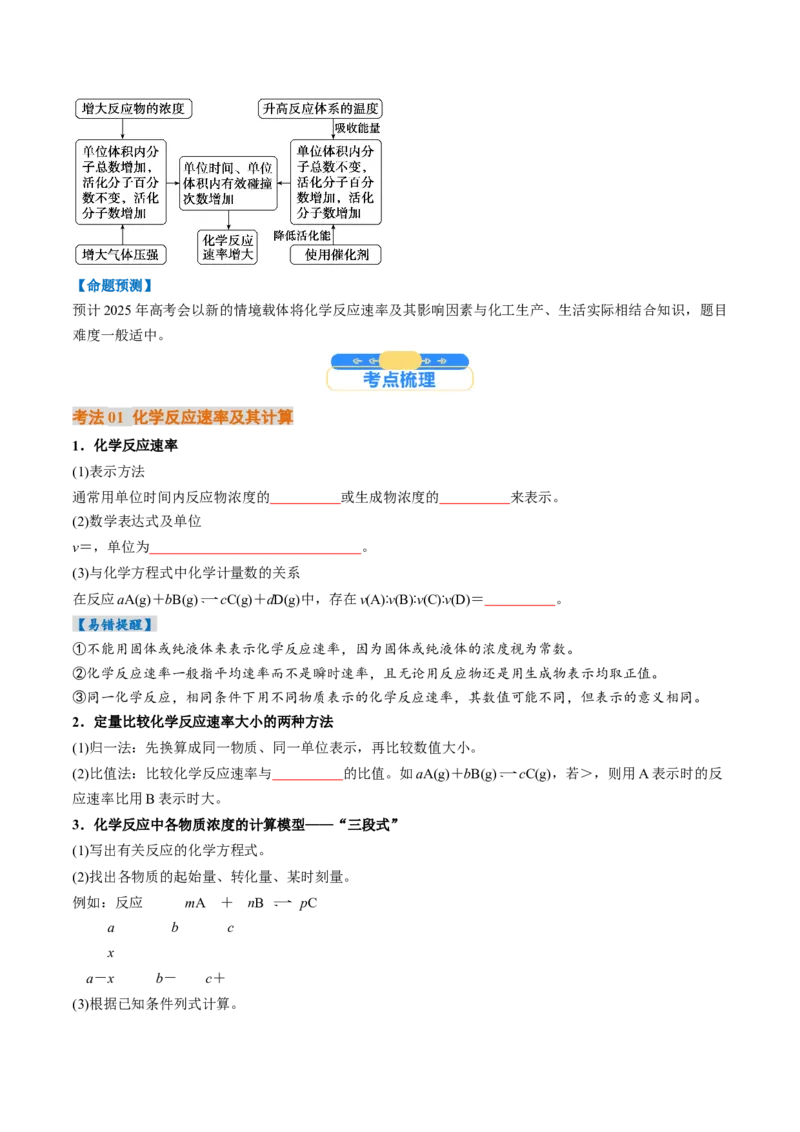
【备考策略】活化分子、有效碰撞与反应速率的关系【命题预测】
预计2025年高考会以新的情境载体将化学反应速率及其影响因素与化工生产、生活实际相结合知识,题目
难度一般适中。
考法01 化学反应速率及其计算
1.化学反应速率
(1)表示方法
通常用单位时间内反应物浓度的 或生成物浓度的 来表示。
(2)数学表达式及单位
v=,单位为 。
(3)与化学方程式中化学计量数的关系
在反应aA(g)+bB(g) cC(g)+dD(g)中,存在v(A)∶v(B)∶v(C)∶v(D)= 。
【易错提醒】
①不能用固体或纯液体来表示化学反应速率,因为固体或纯液体的浓度视为常数。
②化学反应速率一般指平均速率而不是瞬时速率,且无论用反应物还是用生成物表示均取正值。
③同一化学反应,相同条件下用不同物质表示的化学反应速率,其数值可能不同,但表示的意义相同。
2.定量比较化学反应速率大小的两种方法
(1)归一法:先换算成同一物质、同一单位表示,再比较数值大小。
(2)比值法:比较化学反应速率与 的比值。如aA(g)+bB(g) cC(g),若>,则用A表示时的反
应速率比用B表示时大。
3.化学反应中各物质浓度的计算模型——“三段式”
(1)写出有关反应的化学方程式。
(2)找出各物质的起始量、转化量、某时刻量。
例如:反应 mA + nB pC
a b c
x
a-x b- c+
(3)根据已知条件列式计算。请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1( )
(2)由v=计算平均速率,用反应物表示为正值,用生成物表示为负值( )
(3)同一化学反应,相同条件下用不同物质表示的反应速率,其数值可能不同,但表示的意义相同( )
(4)有时也可以用单位时间内某物质质量的变化量来表示化学反应速率( )
(5)同一化学反应,相同条件下用不同物质表示的反应速率,数值越大,表示化学反应速率越快( )
(6)对于任何化学反应来说,都必须用单位时间内反应物或生成物浓度的变化量来表示化学反应速率( )
(7)单位时间内反应物浓度的变化量表示正反应速率,生成物浓度的变化量表示逆反应速率( )
考向01 考查化学反应速率的计算
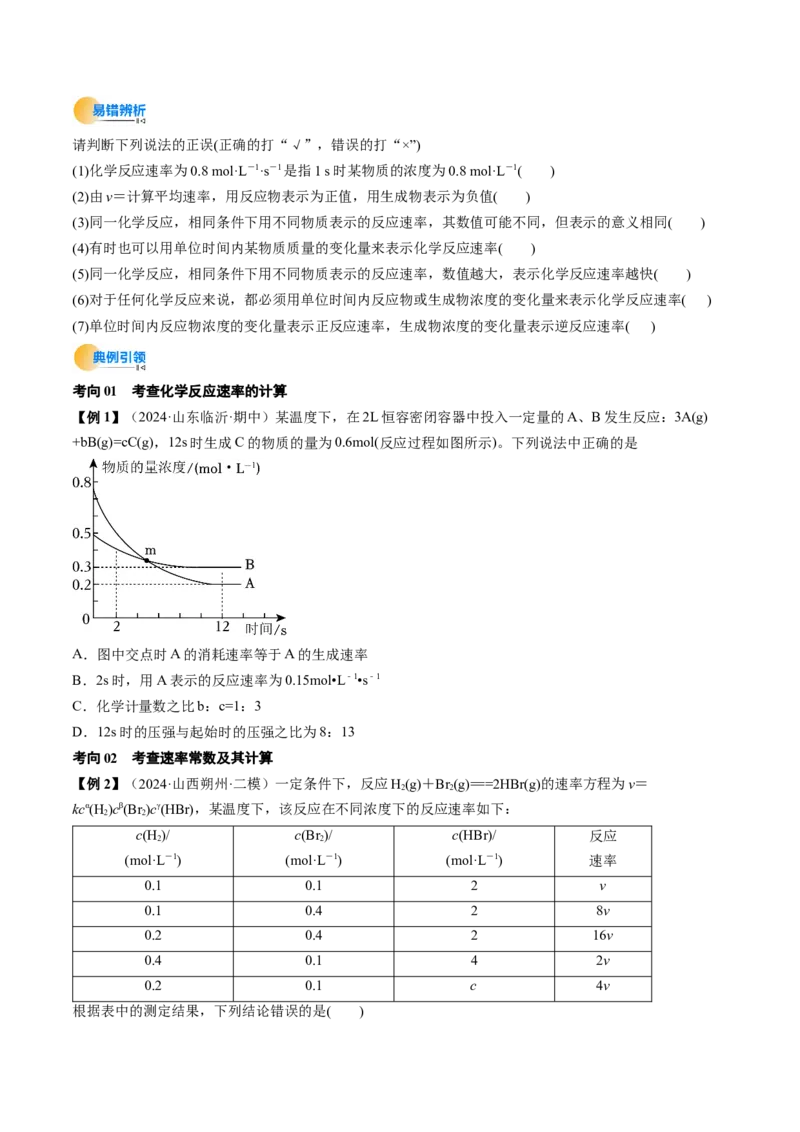
【例1】(2024·山东临沂·期中)某温度下,在2L恒容密闭容器中投入一定量的A、B发生反应:3A(g)
+bB(g)=cC(g),12s时生成C的物质的量为0.6mol(反应过程如图所示)。下列说法中正确的是
A.图中交点时A的消耗速率等于A的生成速率
B.2s时,用A表示的反应速率为0.15mol•L﹣1•s﹣1
C.化学计量数之比b:c=1:3
D.12s时的压强与起始时的压强之比为8:13
考向02 考查速率常数及其计算
【例2】(2024·山西朔州·二模)一定条件下,反应H(g)+Br (g)===2HBr(g)的速率方程为v=
2 2
kcα(H )cβ(Br)cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下:
2 2
c(H )/ c(Br)/ c(HBr)/ 反应
2 2
(mol·L-1) (mol·L-1) (mol·L-1) 速率
0.1 0.1 2 v
0.1 0.4 2 8v
0.2 0.4 2 16v
0.4 0.1 4 2v
0.2 0.1 c 4v
根据表中的测定结果,下列结论错误的是( )A.表中c的值为1
B.α、β、γ的值分别为1、2、-1
C.反应体系的三种物质中,Br (g)的浓度对反应速率影响最大
2
D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低
【思维建模】
1.速率常数:假设基元反应(能够一步完成的反应)为aA(g)+bB(g) cC(g)+dD(g),其速率可表示为v=
kca(A)cb(B),式中的k称为反应速率常数或速率常数。
2.正、逆反应的速率常数与平衡常数的关系:对于基元反应 aA(g)+bB(g) cC(g)+dD(g),v =k
正
·ca(A)·cb(B),v =k ·cc(C)·cd(D),平衡常数K=,反应达到平衡时v =v ,故K=。
正 逆 逆 正 逆
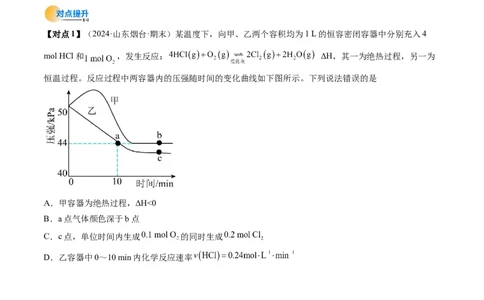
【对点1】(2024·山东烟台·期末)某温度下,向甲、乙两个容积均为1 L的恒容密闭容器中分别充入4
mol HCl和 ,发生反应: ΔH,其一为绝热过程,另一为
恒温过程。反应过程中两容器内的压强随时间的变化曲线如下图所示。下列说法错误的是
A.甲容器为绝热过程,ΔH<0
B.a点气体颜色深于b点
C.c点,单位时间内生成 的同时生成
D.乙容器中0~10 min内化学反应速率
【对点2】(2024·黑龙江哈尔滨·模拟)工业上利用CH(混有CO和H)与水蒸气在一定条件下制取H,原
4 2 2
理为CH(g)+HO(g) CO(g)+3H(g)该反应的逆反应速率表达式为v =k·c(CO)·c3(H ),k为速率常数,
4 2 2 逆 2
在某温度下测得实验数据如表所示:
CO浓度/(mol·L-1) H 浓度/(mol·L-1) 逆反应速率/(mol·L-1·min-1)
2
0.1 c 8.0
1
c c 16.0
2 1
c 0.15 6.75
2
由上述数据可得该温度下,c= mol·L-1,该反应的逆反应速率常数k= L3·mol-3·min-1。
2考法02 影响化学反应速率的因素
1.内因
反应物本身的性质是主要因素。如相同条件下Mg、Al与稀盐酸反应的速率大小关系为 v (Mg)> v (Al) 。
2.外因(其他条件不变,只改变一个条件)
【易错提醒】惰性气体对反应速率的影响
恒温恒容条件下 通入惰性气体,总压增大,反应物浓度不变,反应速率不变
恒温恒压条件下 通入惰性气体,总体积增大,反应物浓度减小,反应速率减小
3.有效碰撞理论解释外因对化学反应速率的影响
(1)有效碰撞
能够发生 的碰撞为有效碰撞。化学反应发生的先决条件是反应物分子间必须发生碰撞。有效碰
撞必须具备两个条件:一是发生碰撞的分子具有 ,二是碰撞时要有 。
(2)活化分子
有足够的能量,能够发生 的分子叫活化分子。
活化分子百分数=×100%。
(3)活化能:活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能。活化能越
小,反应速率 。
图中:E 为 , 为使用催化剂时正反应的活化能, 为逆反应的活化能。
1
(4)活化分子、有效碰撞与反应速率的关系
条件→活化分子→有效碰撞→反应速率变化
单位体积内 有效碰 化学反
条件改变
分子总数 活化分子数 活化分子百分数 撞次数 应速率
增大反应物浓度
增大压强
升高温度加催化剂
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)催化剂都不参加化学反应( )
(2)升高温度时,不论正反应是吸热还是放热,正、逆反应的速率都增大( )
(3)可逆反应中减小产物的浓度可增大正反应的速率( )
(4)增大反应体系的压强,反应速率不一定增大( )
(5)增大反应物的浓度,能够增大活化分子的百分数,所以反应速率增大( )
(6)对可逆反应FeCl +3KSCN Fe(SCN) +3KCl,增加氯化钾浓度,逆反应速率加快( )
3 3
(7)增大反应物的浓度,能够增大活化分子的百分含量,所以反应速率增大( )
(8)对可逆反应FeCl +3KSCN Fe(SCN) +3KCl,增加氯化钾浓度,逆反应速率加快( )
3 3
(9)FeCl 和MnO 均可加快HO 分解,同等条件下二者对HO 分解速率的改变相同( )
3 2 2 2 2 2
(10)用稀硫酸和锌粒制取H 时,加几滴CuSO 溶液以加快反应速率( )
2 4
考向01 考查影响化学反应速率的因素
【例1】(2024·吉林通化·一模)根据v-t图像分析外界条件的改变对可逆反应A(g)+3B(g)2C(g)
ΔH<0的影响。该反应的速率与时间的关系如图所示:
可见在t、t、t、t 时反应都达到平衡,如果t、t、t、t 时都只改变了一个反应条件,则下列对t、t、
1 3 5 7 2 4 6 8 2 4
t、t 时改变条件的判断正确的是( )
6 8
A.使用了催化剂、增大压强、减小反应物浓度、降低温度
B.升高温度、减小压强、减小反应物浓度、使用了催化剂
C.增大反应物浓度、使用了催化剂、减小压强、升高温度
D.升高温度、减小压强、增大反应物浓度、使用了催化剂
考向02 考查“变量控制”实验探究
【例2】(2024·江西景德镇·二模)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数
据如下表所示:
序号 纯锌粉/g 2.0 mol·L-1硫酸溶液/mL 温度/℃ 硫酸铜固体/g 加入蒸馏水/mL
Ⅰ 2.0 50.0 25 0 0
Ⅱ 2.0 40.0 25 0 10.0Ⅲ 2.0 50.0 25 0.2 0
Ⅳ 2.0 50.0 25 4.0 0
(1)本实验待测数据可以是_____________________________________________________,
实验Ⅰ和实验Ⅱ可以探究________对锌与稀硫酸反应速率的影响。
(2)实验Ⅲ和实验Ⅳ的目的是___________________________________________________,
写出有关反应的离子方程式___________________________________________________。
【思维建模】关于“变量控制法”题目的解题策略
【对点1】(2024·山东聊城·模拟)下列说法正确的是( )
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增多
B.有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增大活化分子的百分数,从而使反应
速率增大
C.升高温度能使化学反应速率增大的主要原因是减小了反应物分子中活化分子的百分数
D.催化剂能增大单位体积内活化分子的百分数,从而增大反应速率
【对点2】(2024·四川雅安·模拟)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实
验:
[实验原理] 2KMnO +5HC O+3HSO ===K SO +2MnSO +10CO↑+8HO
4 2 2 4 2 4 2 4 4 2 2
[实验内容及记录]
试管中所加试剂及其用量/mL 溶液褪至
实验 实验
0.6 mol/L 3 mol/L 0.05 mol/L 无色所需
编号 温度/℃ HO
HC O 溶液 2 稀HSO 溶液 KMnO 溶液 时间/min
2 2 4 2 4 4
① 25 3.0 V 2.0 3.0 1.5
1
② 25 2.0 3.0 2.0 3.0 2.7
③ 50 2.0 V 2.0 3.0 1.0
2
(1)请完成此实验设计,其中:V=________,V=________。
1 2
(2)实验①、②探究的是________对化学反应速率的影响,根据上表中的实验数据,可以得到的结论是
__________________________________________________________________________________。
(3)探究温度对化学反应速率的影响,应选择实验________(填实验编号)。(4)利用实验①中的数据,计算用KMnO 表示的化学反应速率为____________。
4
考法03 基元反应与反应机理
1.基元反应
(1)大多数化学反应都是分几步完成的,其中的 都称为基元反应。
(2)基元反应速率方程
对于基元反应aA+bB===gG+hH,其速率方程可写为v=k·ca(A)·cb(B)(其中k称为速率常数,恒温下,k不
因反应物浓度的改变而变化),这种关系可以表述为基元反应的 与 以其化学计量数为
的乘积成正比。
2.反应机理
基元反应构成的反应序列称为反应历程(又称反应机理),基元反应的总和称为总反应。由几个基元反应组
成的总反应也称复杂反应。
例如H(g)+I(g)===2HI(g),它的反应历程有如下两步基元反应:
2 2
①I ===I·+I·(快)
2
②H +2I·===2HI(慢)
2
其中慢反应为整个反应的决速步骤。
3.过渡态理论
(1)化学反应并不是通过反应物分子的简单碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能
的过渡态,处于过渡态的分子叫做 。活化络合物是一种高能量的不稳定的反应物原子组合体,
它能较快地分解为新的能量较低的较稳定的生成物。
(2)活化能(E)是处在过渡态的活化络合物分子平均能量与反应物分子平均能量的差值。
a
4.催化机理
从碰撞理论解释:催化剂通过参加反应, 反应历程, 反应的活化能,使活化分子百分数 ,
从而 反应速率,图示如下。
5.催化剂的特征
(1)催化剂只能改变反应途径(又称反应机理),不能改变反应的 和 。它同时加快了正、逆反应速
率,缩短了达到平衡的时间,并不能改变 。
(2)催化剂有选择性,不同的反应常用不同的催化剂,即每个反应有它特有的催化剂。生产上常利用催化剂
的选择性,使所希望的化学反应 ,同时抑制某些副反应的 。
(3)每种催化剂只有在特定条件下才能体现出它的 ,否则将失去活性或发生催化剂中毒。考向01 考查催化剂与反应机理
【例1】(2024·安徽阜阳·一模)已知反应:2NO(g)+Br (g) 2NOBr(g) ΔH=-a kJ·mol-1(a>0),其反
2
应机理如下:
①NO(g)+Br (g) NOBr (g) 快
2 2
②NO(g)+NOBr (g) 2NOBr(g) 慢
2
下列有关该反应的说法正确的是( )
A.该反应的速率主要取决于①的快慢
B.NOBr 是该反应的催化剂
2
C.正反应的活化能比逆反应的活化能小a kJ·mol-1
D.增大Br (g)浓度能增大活化分子百分数,加快反应速率
2
考向02 考查反应历程图像
【例2】(2024·湖北孝感·二模)汽车尾气处理时存在反应:NO (g)+CO(g) NO(g)+CO(g),该反应过
2 2
程及能量变化如图所示。
下列说法正确的是( )
A.使用催化剂活化分子百分数增多
B.使用催化剂,反应物分子的能量变高
C.使用催化剂可以有效减少反应放出的热量
D.无论是反应物还是生成物,转化为活化络合物都要吸收能量
【对点1】(2024·河南鹤壁·模拟)向HO 溶液中加入少量FeCl 溶液,混合溶液中有大量气泡逸出,查阅
2 2 3
资料知HO 的分解机理如下:
2 2
①2Fe3++HO 2Fe2++O↑+2H+ 慢
2 2 2
②HO+ 2Fe2++2H+ 2HO+2Fe3+ 快
2 2 2
下列有关说法正确的是( )
A.增大c(Fe3+)不影响产生气体的速率
B.第①步反应中Fe3+与HO 碰撞仅部分有效
2 2
C.Fe2+是该反应的催化剂D.第②步反应的活化能较大
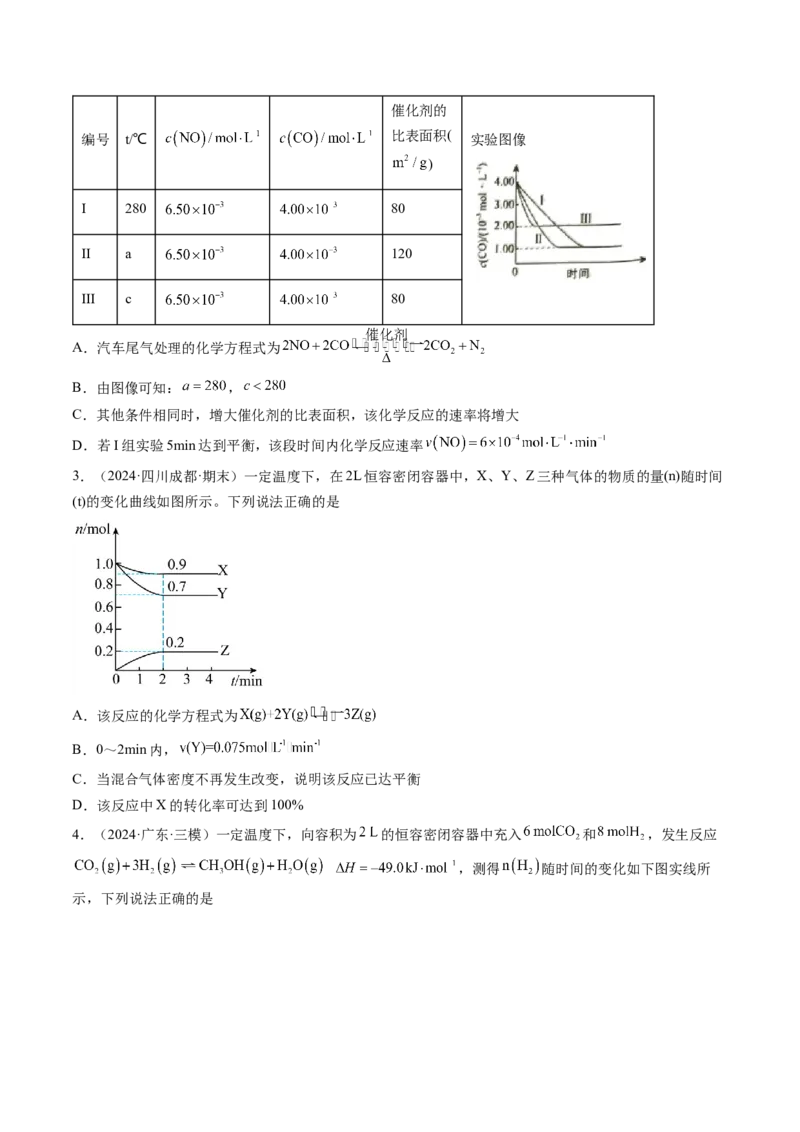
【对点2】(2024·辽宁本溪·模拟)二甲醚(CHOCH )被称为21世纪的“清洁能源”,科学家研究在酸性
3 3
条件下,用甲醇可合成二甲醚,反应历程中相对能量变化如图所示。
下列叙述错误的是( )
A.循环过程中,催化剂参与了中间反应
B.该历程中最小的能垒(基元反应活化能)为1.31 kJ·mol-1
C.制约总反应速率关键步骤的基元反应方程式为 ―→CHOCH +H+
3 3
D.总反应方程式为2CHOH=====CHOCH +HO
3 3 3 2
1.(2024·山东临沂·期中)已知CH(g)+2NO (g)=N(g)+CO (g)+2HO(g),在2L密闭容器中分别加入
4 2 2 2 2
0.5molCH 和1molNO ,保持温度不变,测得n(CH)随时间变化的有关实验数据如表所示。
4 2 4
时间/min 0 10 20 30 40 50
n(CH)/mol 0.5 0.35 0.25 0.17 0.10 0.10
4
下列说法错误的是
A.0~20min内,NO 的反应速率为 0.0125mol•L﹣1•min﹣1
2
B.随着反应的进行,反应物的浓度降低,反应速率减慢
C.单位时间内,若生成1molN 同时生成2molNO ,则反应达到平衡
2 2
D.达到平衡时,CH 的转化率与 NO 的转化率之比为1:2
4 2
2.(2024·黑龙江齐齐哈尔·期末)汽车尾气系统中安装催化转化器可减少CO和NO的污染。查阅资料可
知使用同种催化剂,质量相等时催化剂的比表面积对催化效率有影响。某实验小组的实验数据、图像分析
与结论如下。下列说法不正确的是催化剂的
编号 t/℃ 比表面积( 实验图像
)
I 280 80
II a 120
III c 80
A.汽车尾气处理的化学方程式为
B.由图像可知: ,
C.其他条件相同时,增大催化剂的比表面积,该化学反应的速率将增大
D.若I组实验5min达到平衡,该段时间内化学反应速率
3.(2024·四川成都·期末)一定温度下,在2L恒容密闭容器中,X、Y、Z三种气体的物质的量(n)随时间
(t)的变化曲线如图所示。下列说法正确的是
A.该反应的化学方程式为
B.0~2min内,
C.当混合气体密度不再发生改变,说明该反应已达平衡
D.该反应中X的转化率可达到100%
4.(2024·广东·三模)一定温度下,向容积为 的恒容密闭容器中充入 和 ,发生反应
,测得 随时间的变化如下图实线所
示,下列说法正确的是A.升高温度,可以提高上述反应的平衡产率
B.该反应在 内 的平均反应速率是
C.该反应在 后,容器内总压强不再改变
D.加入催化剂(其他条件相同), 随时间的变化会如上图虚线所示
5.(2024·河北保定·三模)铌被广泛应用于航空航天、电子、原子能、超导材料及新型功能材料等领域,
是一种十分重要的战略物资。 常用于萃取稀土金属铌:
。某温度下,萃取过程中溶液中
与时间的变化关系如图所示。下列叙述正确的是
A.其他条件不变, 时萃取反应已停止
B. 增大,萃取反应平衡向左移动,平衡常数减小
C. min、 min时萃取反应的正反应速率:
D. min内, 的平均反应速率
6.(2024·安徽安庆·模拟预测)我国科学家团队打通了温和条件下草酸二甲酯【 】催化加氢制
乙二醇的技术难关,反应为 。如图所示,
在恒容密闭容器中,反应温度为 时, 和 随时间t的变化分别为曲线I和Ⅱ,反应温度为 时, 随时间t的变化为曲线Ⅲ。下列判断错误的是
A.ΔH<0
B.a、b两时刻生成乙二醇的速率:
C.其他条件相同,在 温度下,起始时向该容器中充入一定量的氮气,则反应达到平衡的时间小于
D.在 温度下,反应在0~ 内的平均速率为
7.(2024·山东淄博·三模)某密闭容器中发生以下两个反应:① ;②
。反应①的正反应速率 ,反应②的正反应速率
,其中 、 为速率常数。某温度下,体系中生成物浓度随时间变化的关系如图所
示。下列说法正确的是
A.反应①的活化能大于反应②
B. 时,正反应速率
C. 内,X的平均反应速率
D.该温度时,
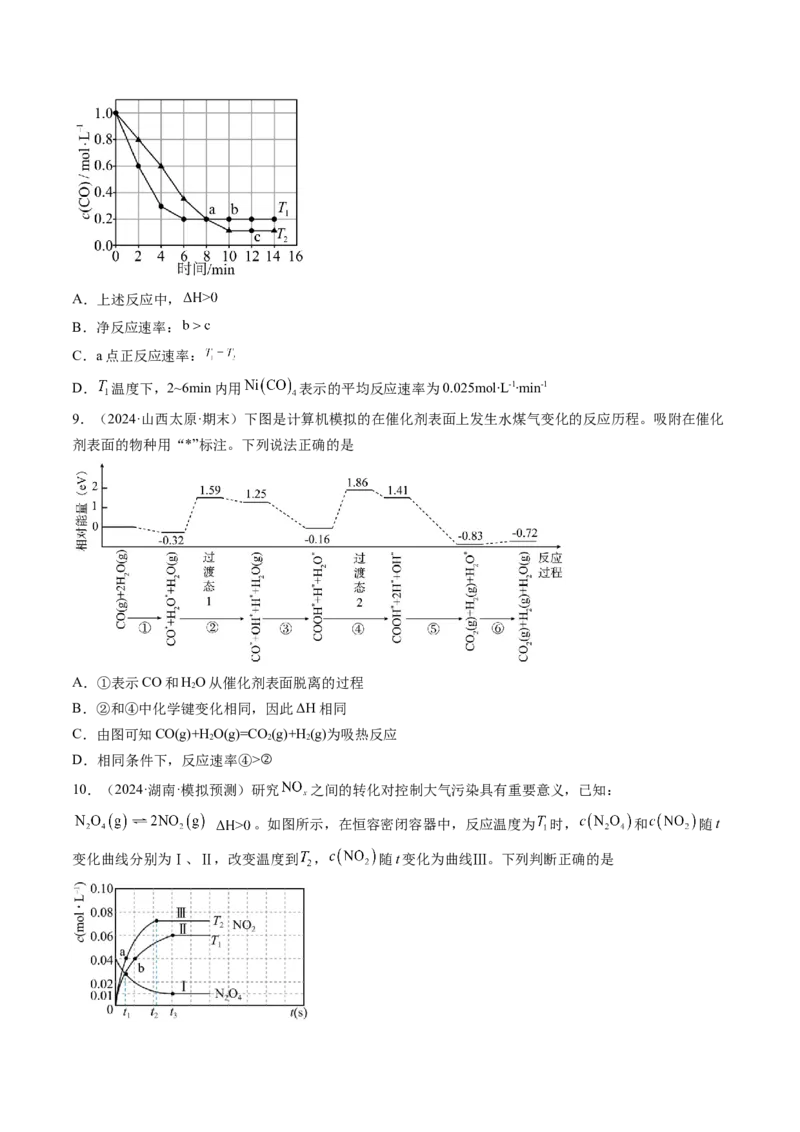
8.(2024·江西·期末)工业上常用羰基法提纯镍,其原理是 ,速率方
程式为 ( 为速率常数)。在恒容密闭容器中充入足量的含难熔
杂质的镍粉和4molCO发生上述反应,测得CO浓度与温度关系如图所示。下列叙述正确的是A.上述反应中,
B.净反应速率:
C.a点正反应速率:
D. 温度下,2~6min内用 表示的平均反应速率为0.025mol∙L-1∙min-1
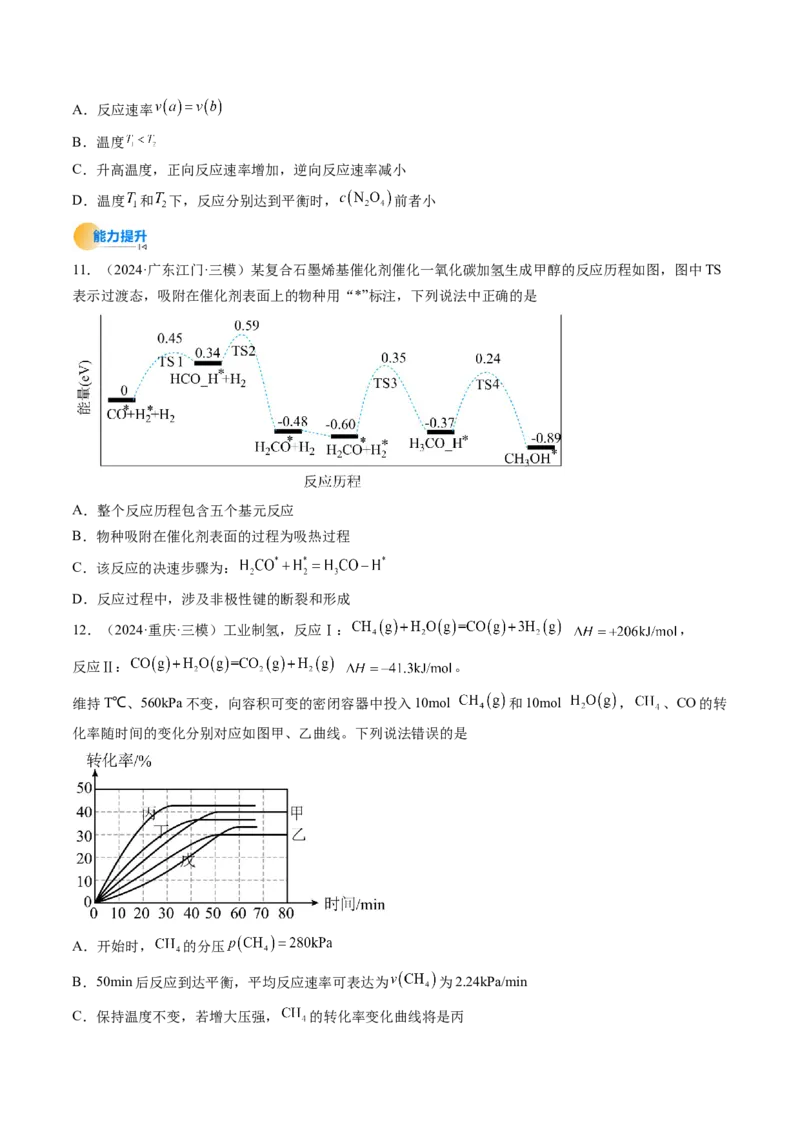
9.(2024·山西太原·期末)下图是计算机模拟的在催化剂表面上发生水煤气变化的反应历程。吸附在催化
剂表面的物种用“*”标注。下列说法正确的是
A.①表示CO和HO从催化剂表面脱离的过程
2
B.②和④中化学键变化相同,因此ΔH相同
C.由图可知CO(g)+HO(g)=CO(g)+H(g)为吸热反应
2 2 2
D.相同条件下,反应速率④>②
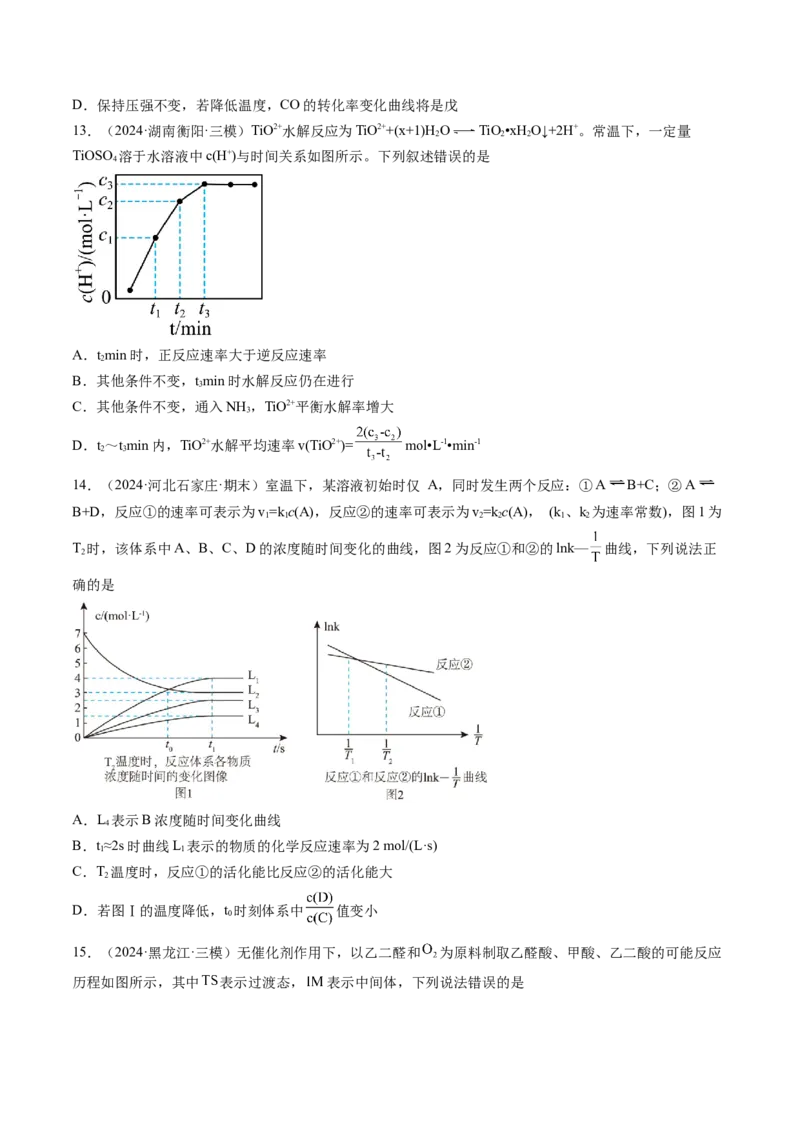
10.(2024·湖南·模拟预测)研究 之间的转化对控制大气污染具有重要意义,已知:
。如图所示,在恒容密闭容器中,反应温度为 时, 和 随t
变化曲线分别为Ⅰ、Ⅱ,改变温度到 , 随t变化为曲线Ⅲ。下列判断正确的是A.反应速率
B.温度
C.升高温度,正向反应速率增加,逆向反应速率减小
D.温度 和 下,反应分别达到平衡时, 前者小
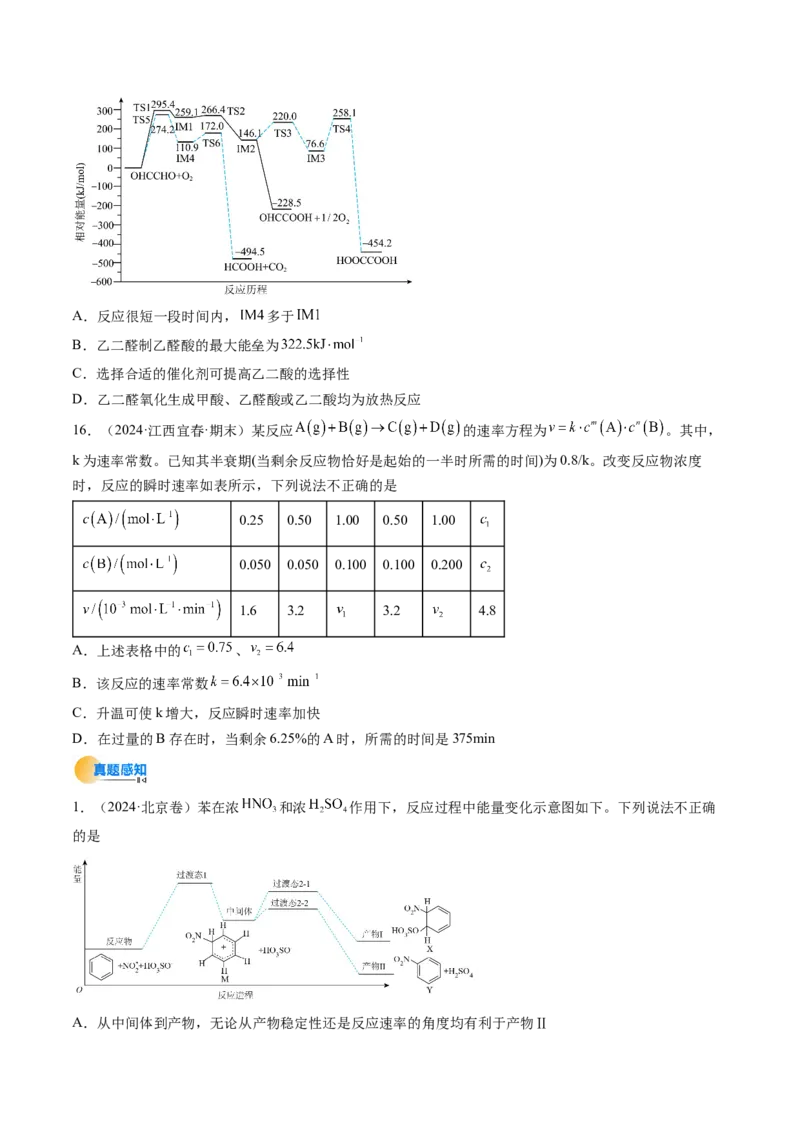
11.(2024·广东江门·三模)某复合石墨烯基催化剂催化一氧化碳加氢生成甲醇的反应历程如图,图中TS
表示过渡态,吸附在催化剂表面上的物种用“*”标注,下列说法中正确的是
A.整个反应历程包含五个基元反应
B.物种吸附在催化剂表面的过程为吸热过程
C.该反应的决速步骤为:
D.反应过程中,涉及非极性键的断裂和形成
12.(2024·重庆·三模)工业制氢,反应Ⅰ: ,
反应Ⅱ: 。
维持T℃、560kPa不变,向容积可变的密闭容器中投入10mol 和10mol , 、CO的转
化率随时间的变化分别对应如图甲、乙曲线。下列说法错误的是
A.开始时, 的分压
B.50min后反应到达平衡,平均反应速率可表达为 为2.24kPa/min
C.保持温度不变,若增大压强, 的转化率变化曲线将是丙D.保持压强不变,若降低温度,CO的转化率变化曲线将是戊
13.(2024·湖南衡阳·三模)TiO2+水解反应为TiO2++(x+1)H O TiO•xH O↓+2H+。常温下,一定量
2 2 2
TiOSO 溶于水溶液中c(H+)与时间关系如图所示。下列叙述错误的是
4
A.tmin时,正反应速率大于逆反应速率
2
B.其他条件不变,tmin时水解反应仍在进行
3
C.其他条件不变,通入NH ,TiO2+平衡水解率增大
3
D.t~tmin内,TiO2+水解平均速率v(TiO2+)= mol•L-1•min-1
2 3
14.(2024·河北石家庄·期末)室温下,某溶液初始时仅 A,同时发生两个反应:①A B+C;②A
B+D,反应①的速率可表示为v=kc(A),反应②的速率可表示为v=kc(A), (k、k 为速率常数),图1为
1 1 2 2 1 2
T 时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk— 曲线,下列说法正
2
确的是
A.L 表示B浓度随时间变化曲线
4
B.t≈2s时曲线L 表示的物质的化学反应速率为2 mol/(L·s)
1 1
C.T 温度时,反应①的活化能比反应②的活化能大
2
D.若图Ⅰ的温度降低,t 时刻体系中 值变小
0
15.(2024·黑龙江·三模)无催化剂作用下,以乙二醛和 为原料制取乙醛酸、甲酸、乙二酸的可能反应
历程如图所示,其中 表示过渡态, 表示中间体,下列说法错误的是A.反应很短一段时间内, 多于
B.乙二醛制乙醛酸的最大能垒为
C.选择合适的催化剂可提高乙二酸的选择性
D.乙二醛氧化生成甲酸、乙醛酸或乙二酸均为放热反应
16.(2024·江西宜春·期末)某反应 的速率方程为 。其中,
k为速率常数。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.8/k。改变反应物浓度
时,反应的瞬时速率如表所示,下列说法不正确的是
0.25 0.50 1.00 0.50 1.00
0.050 0.050 0.100 0.100 0.200
1.6 3.2 3.2 4.8
A.上述表格中的 、
B.该反应的速率常数
C.升温可使k增大,反应瞬时速率加快
D.在过量的B存在时,当剩余6.25%的A时,所需的时间是375min
1.(2024·北京卷)苯在浓 和浓 作用下,反应过程中能量变化示意图如下。下列说法不正确
的是
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物ⅡB.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大 键没有变化
D.对于生成Y的反应,浓 作催化剂
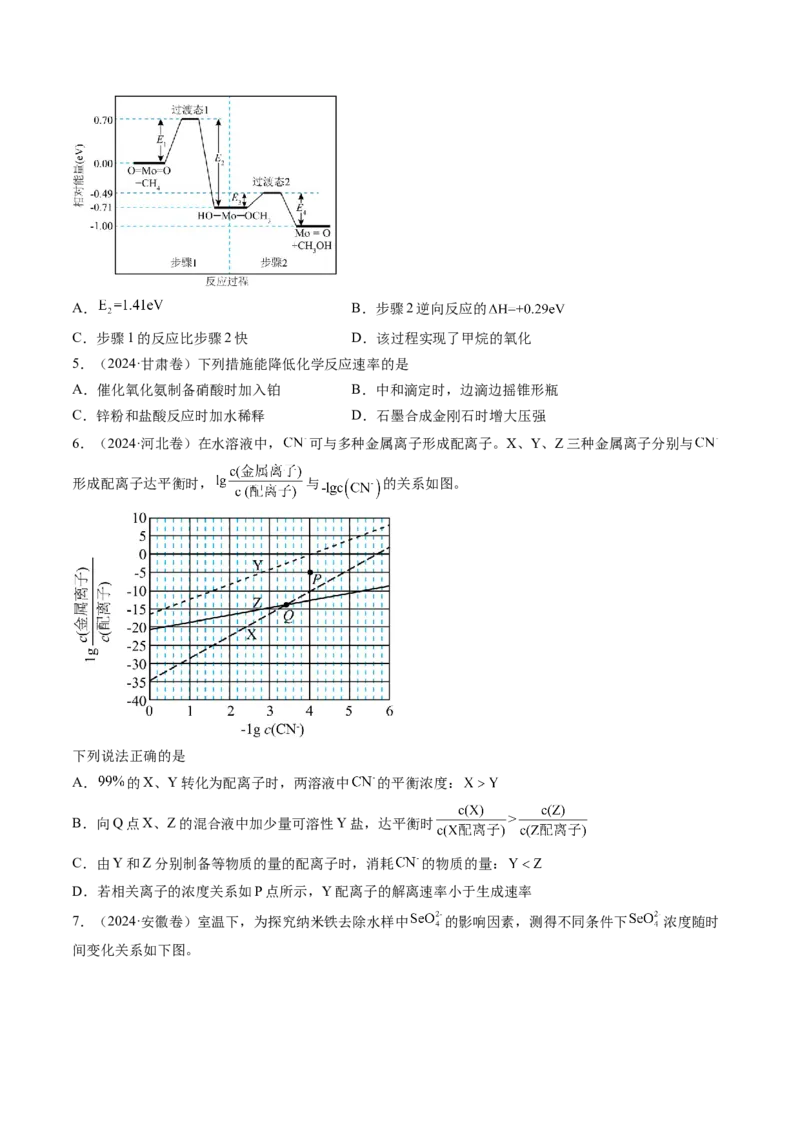
2.(2024·贵州卷)AgCN与 可发生取代反应,反应过程中 的C原子和N原子均可进攻
,分别生成腈 和异腈 两种产物。通过量子化学计算得到的反应历程
及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是
A.从 生成 和 的反应都是放热反应
B.过渡态TS1是由 的C原子进攻 的 而形成的
C.Ⅰ中“ ”之间的作用力比Ⅱ中“ ”之间的作用力弱
D.生成 放热更多,低温时 是主要产物
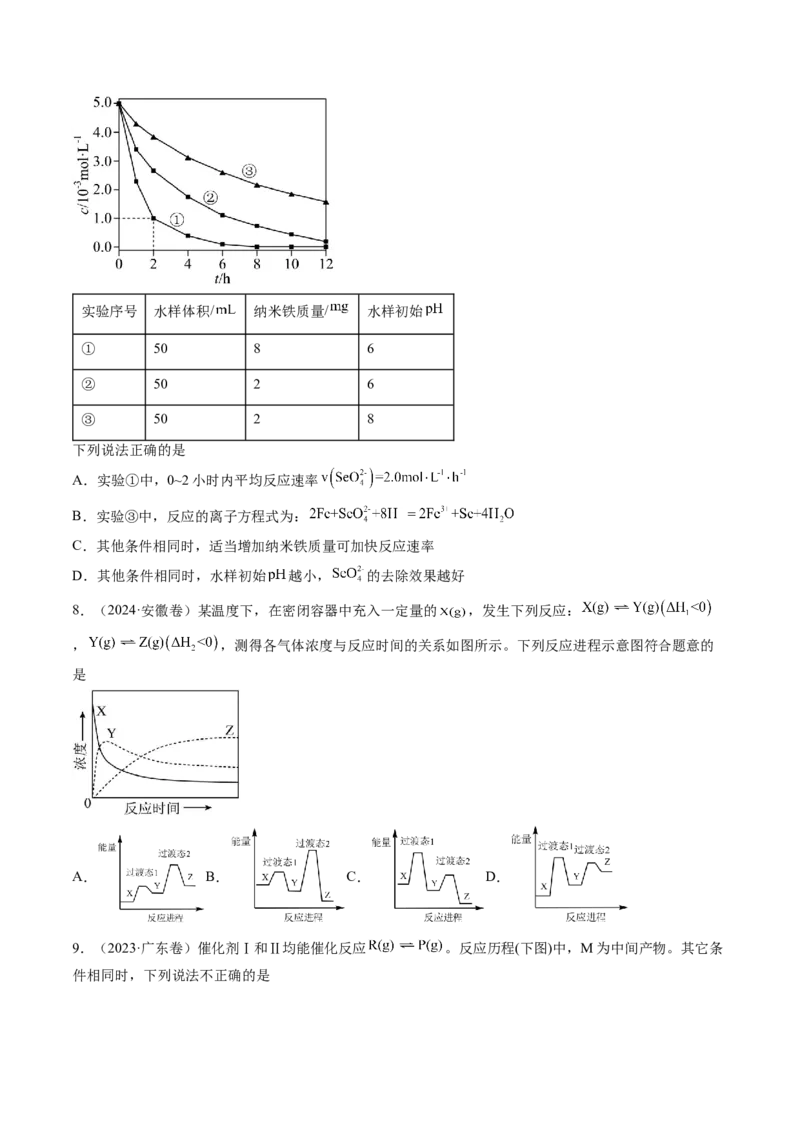
3.(2024·广东卷)对反应 (I为中间产物),相同条件下:①加入催化剂,反应达到平衡所需
时间大幅缩短;②提高反应温度, 增大, 减小
。基于以上事实,可能的反应历程示意图(——为无催化剂,------为有催化剂)为
A. B. C. D.
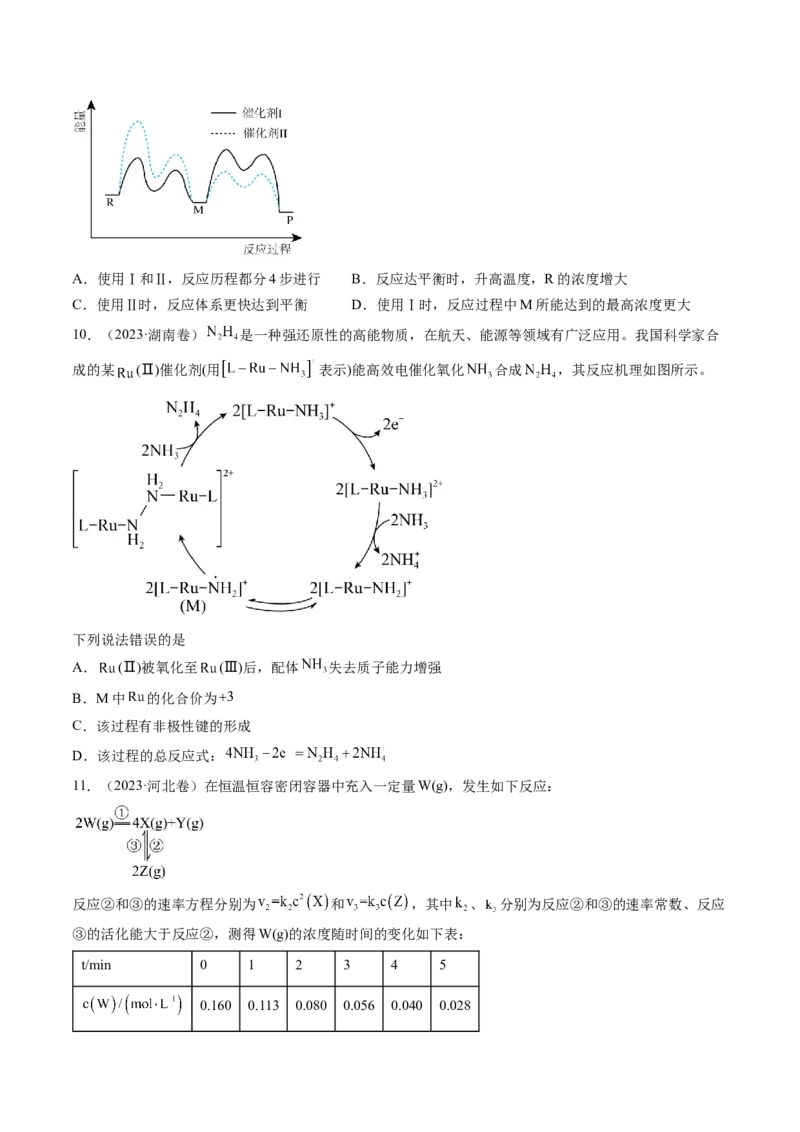
4.(2024·甘肃卷)甲烷在某含 催化剂作用下部分反应的能量变化如图所示,下列说法错误的是A. B.步骤2逆向反应的
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
5.(2024·甘肃卷)下列措施能降低化学反应速率的是
A.催化氧化氨制备硝酸时加入铂 B.中和滴定时,边滴边摇锥形瓶
C.锌粉和盐酸反应时加水稀释 D.石墨合成金刚石时增大压强
6.(2024·河北卷)在水溶液中, 可与多种金属离子形成配离子。X、Y、Z三种金属离子分别与
形成配离子达平衡时, 与 的关系如图。
下列说法正确的是
A. 的X、Y转化为配离子时,两溶液中 的平衡浓度:
B.向Q点X、Z的混合液中加少量可溶性Y盐,达平衡时
C.由Y和Z分别制备等物质的量的配离子时,消耗 的物质的量:
D.若相关离子的浓度关系如P点所示,Y配离子的解离速率小于生成速率
7.(2024·安徽卷)室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下 浓度随时
间变化关系如下图。实验序号 水样体积/ 纳米铁质量/ 水样初始
① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是
A.实验①中,0~2小时内平均反应速率
B.实验③中,反应的离子方程式为:
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始 越小, 的去除效果越好
8.(2024·安徽卷)某温度下,在密闭容器中充入一定量的 ,发生下列反应:
, ,测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的
是
A. B. C. D.
9.(2023·广东卷)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。其它条
件相同时,下列说法不正确的是A.使用Ⅰ和Ⅱ,反应历程都分4步进行 B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡 D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
10.(2023·湖南卷) 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合
成的某 (Ⅱ)催化剂(用 表示)能高效电催化氧化 合成 ,其反应机理如图所示。
下列说法错误的是
A. (Ⅱ)被氧化至 (Ⅲ)后,配体 失去质子能力增强
B.M中 的化合价为
C.该过程有非极性键的形成
D.该过程的总反应式:
11.(2023·河北卷)在恒温恒容密闭容器中充入一定量W(g),发生如下反应:
反应②和③的速率方程分别为 和 ,其中 、 分别为反应②和③的速率常数、反应
③的活化能大于反应②,测得W(g)的浓度随时间的变化如下表:
t/min 0 1 2 3 4 5
0.160 0.113 0.080 0.056 0.040 0.028下列说法正确的是
A. 内,W的平均反应速率为
B.若升高温度,平衡时 减小
C.若 ,平衡时
D.若增大容器容积,平衡时Y的产率增大
12.(2023·新课标卷)“肼合成酶”以其中的Fe2+配合物为催化中心,可将NH OH与NH 转化为肼
2 3
(NH NH ),其反应历程如下所示。
2 2
下列说法错误的是( )
A.NH OH、NH 和HO均为极性分子
2 3 2
B.反应涉及N—H、N—O键断裂和N—N键生成
C.催化中心的Fe2+被氧化为Fe3+,后又被还原为Fe2+
D.将NH OH替换为ND OD,反应可得ND ND
2 2 2 2
13.(2023·辽宁卷)一定条件下,酸性KMnO 溶液与HC O 发生反应,Mn (Ⅱ)起催化作用,过程中不同价
4 2 2 4
态含 粒子的浓度随时间变化如下图所示。下列说法正确的是( )
A.Mn (Ⅲ)不能氧化HC O
2 2 4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下, (Ⅱ)和 (Ⅶ)不能大量共存
D.总反应为:2MnO -+5C O2-+16H+=2Mn2++10CO ↑+8H O
4 2 4 2 2
14.(2022·浙江选择考,20)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:2NH (g)
3
N(g)+3H(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法不
2 2
正确的是( )
时间/minc
编号 (NH )/(10-3 mol·L- 0 20 40 60 80
3
1)表面积/cm2① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,0~20 min,v(N )=1.00×10-5mol·L-1·min-1
2
B.实验②,60 min时处于平衡状态,x≠0.40
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
15.(2022·广东选择考,15)在相同条件下研究催化剂Ⅰ、Ⅱ对反应X→2Y的影响,各物质浓度c随反应时
间t的部分变化曲线如图,则下列说法正确的是( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1
16. (2022·山东等级考,10)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错
误的是( )
A.含N分子参与的反应一定有电子转移
B.由NO生成HONO的反应历程有2种
C.增大NO的量,C H 的平衡转化率不变
3 8
D.当主要发生包含②的历程时,最终生成的水减少
17.(2022·湖南选择考,12)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如图所示:
下列有关四种不同反应进程的说法正确的是( )
A.进程Ⅰ是放热反应
B.平衡时P的产率:Ⅱ>ⅠC.生成P的速率:Ⅲ>Ⅱ
D.进程Ⅳ中,Z没有催化作用
18.(2022·北京卷)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完成之后,以
2 2
N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量
2 2 4
随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2
下列说法不正确的是( )
A.反应①为CaO+CO===CaCO ;反应②为CaCO +CH=====CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH=====C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
19.(2022·河北省选择性考试,11)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为
①X Y;②Y Z。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲
为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是( )
A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
120.(2022·湖北卷)某温度下,在1 L恒容密闭容器中2.0 mol X发生反应2X(s)Y(g)+2Z(g),有关数据如
下:
时间段/min 产物Z的平均生成速率/mol·L-1· min-1
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是( )
A.1 min时,Z的浓度大于0.20 mol·L-1
B.2 min时,加入0.20 mol Z,此时v (Z)