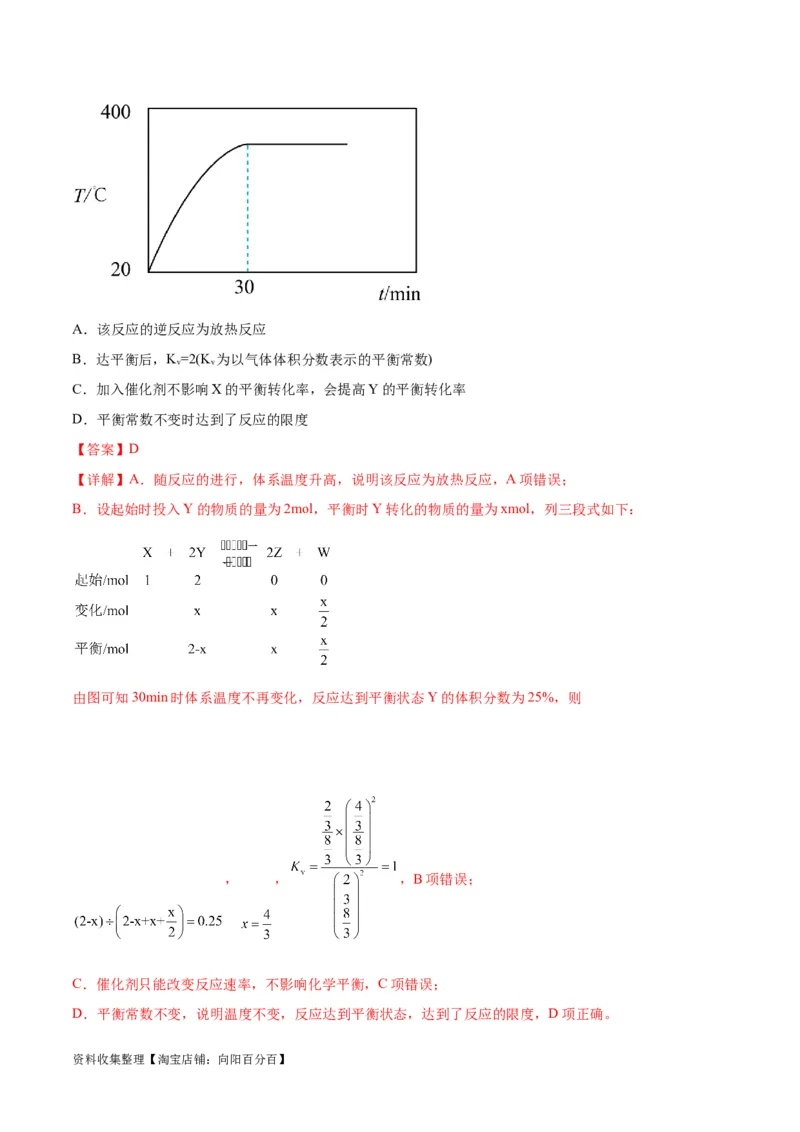
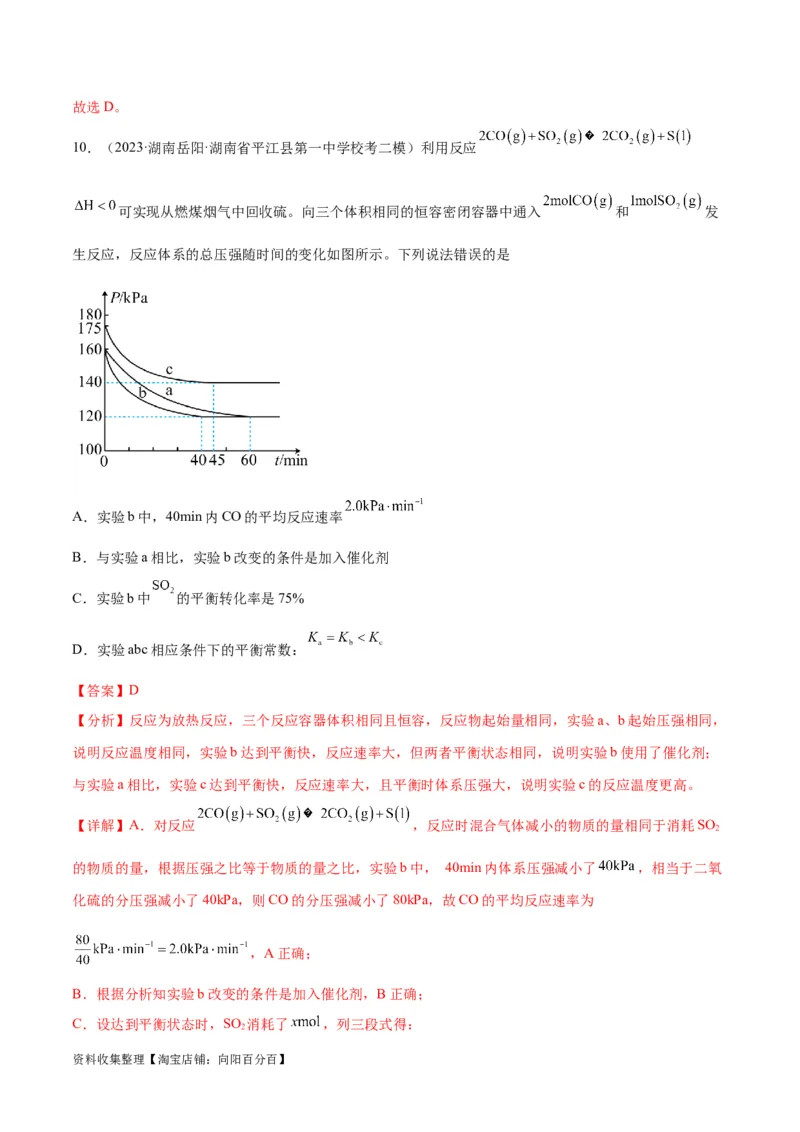
文档内容
考点巩固卷 08 化学反应速率与化学平衡
考点 题型
考点一 化学反应速率与化学平衡图像 选择题(15题)
考点二 化学平衡状态 平衡的移动 选择题(15题)
考点三 平衡常数 化学反应进行的方向 选择题(15题)
考点一 化学反应速率与化学平衡图像 分值:30分 建议用时:20分钟
一、选择题(每小题2分,共30分)
1.(2023·海南海口·统考模拟预测)天然气脱硝的反应原理为
。在1L恒容密闭容器中充入3mol (g)和2mol
(g)发生上述反应,平衡时 、 的物质的量分数与温度的关系如图所示,N点表示410K时
的物质的量分数。下列说法正确的是
A.上述反应的正反应是吸热反应 B.443K时, 和 的平衡转化率相等
C.N点的正反应速率大于逆反应速率 D.443K时该反应的平衡常数K为4
【答案】D
【详解】A.由图可知,升高温度, 的物质的量分数减小,说明平衡逆向移动,该反应是放热反应,故
A错误;
资料收集整理【淘宝店铺:向阳百分百】B.由方程式 可知,在1L恒容密闭容器中充入3mol
(g)和2mol (g)发生反应, 和 转化量之比为2:1, 和 的平衡转化率不相等,故B错误;
C.N点表示410K时 的物质的量分数,小于平衡时 的物质的量分数,说明此时反应逆向进行,N
点的正反应速率小于逆反应速率,故C错误;
D.443K时, 和 的物质的量分数相等,设 的转化量为xmol,则3-x=0.5x,x=2,该反应的平
衡常数K= =4,故D正确;
故选D。
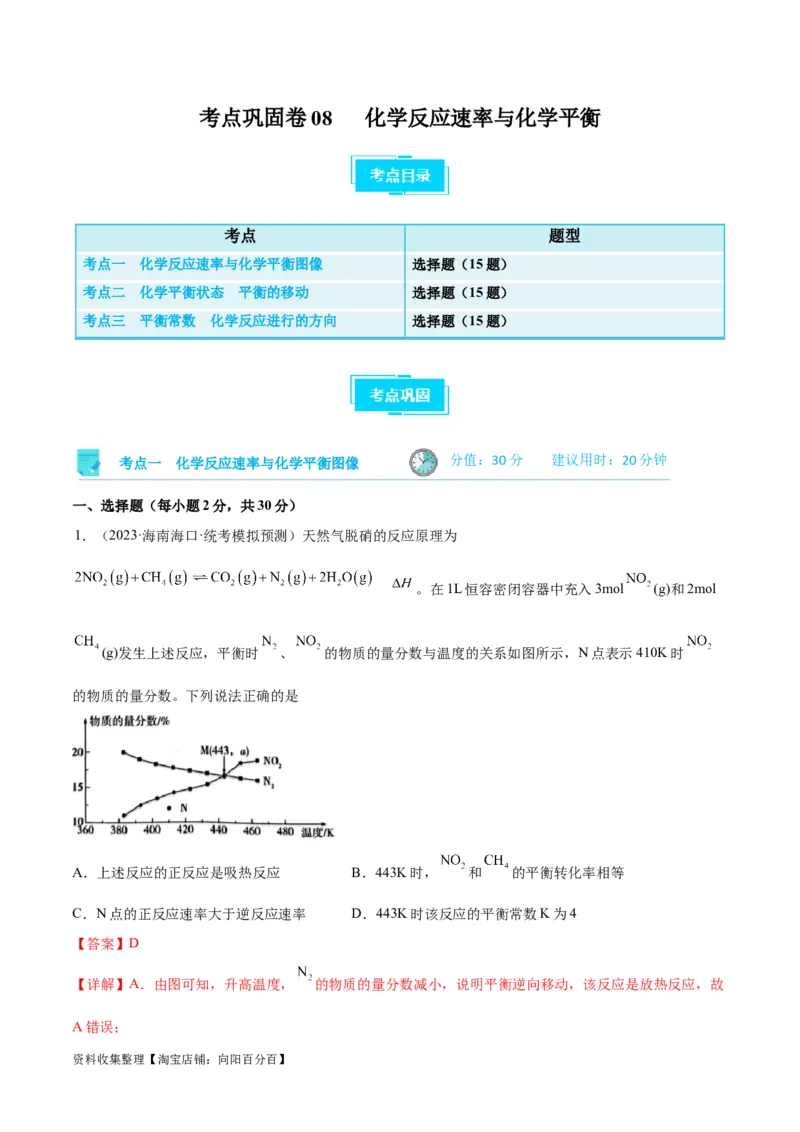
2.(2023·天津·校联考模拟预测)某温度下,发生反应 ,
的平衡转化率( )与体系总压强(p)的关系如图所示。下列说法正确的是
A.将1mol 和3mol 置于1L密闭容器中发生反应,放出的热量小于92.4kJ
B.平衡状态由A到B时,平衡常数
C.上述反应在达到平衡后,增大压强, 的产率减小
D.反应建立平衡后分离出部分 时,浓度商Q大于平衡常数K
【答案】A
【分析】图像中横坐标表示压强,纵坐标表示 的平衡转化率( ),随着压强的增大 的平衡转化率( )
资料收集整理【淘宝店铺:向阳百分百】增大,增大压强平衡向右移动,依此解题。
【详解】A.该反应为可逆反应,加入的1 mol N 和3 mol H 不可能完全反应生成2 mol NH ,所以反应放
2 2 3
出的热量小于92.4 kJ,A正确;
B.从状态A到状态B,改变的是压强,温度未发生变化,所以平衡常数不变, ,B错误;
C.该反应是反应前后气体分子数减小的反应,增大压强平衡向正反应方向移动, 的产率增大,C错
误;
D.反应建立平衡后分离出部分 时,生成物的浓度减小所以浓度商Q小于平衡常数K,D错误;
故选A。
3.(2023·江苏徐州·统考三模) 与 重整是 利用的研究热点之一,该重整反应体系主要涉及以
下反应,且1300K以上会产生积碳现象。
反应Ⅰ:
反应Ⅱ:
反应Ⅲ: (该反应只在高温下自发)
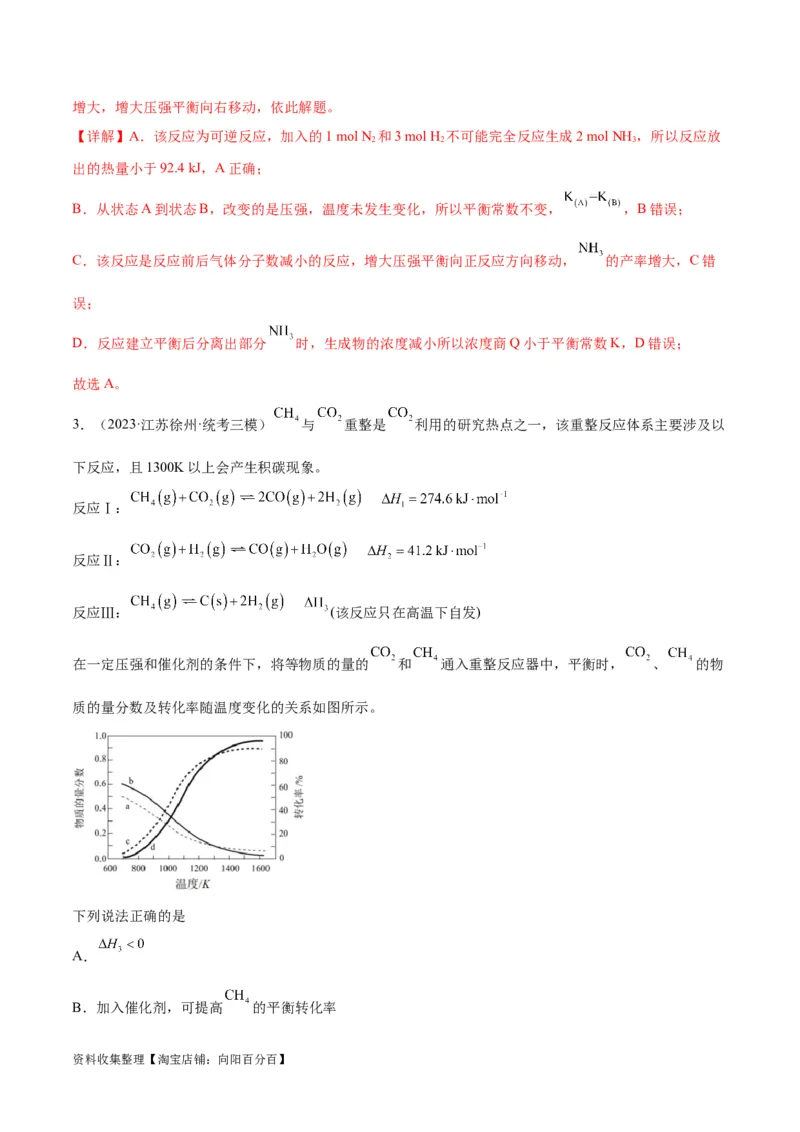
在一定压强和催化剂的条件下,将等物质的量的 和 通入重整反应器中,平衡时, 、 的物
质的量分数及转化率随温度变化的关系如图所示。
下列说法正确的是
A.
B.加入催化剂,可提高 的平衡转化率
资料收集整理【淘宝店铺:向阳百分百】C.平衡时 的物质的量分数随温度变化的曲线是b
D.温度高于1300K后,曲线d超过曲线c的可能原因是升高温度有利于反应Ⅲ进行,导致 的转化率
大于 的转化率
【答案】D
【详解】A.反应Ⅲ的气体分子数增大即∆S>0,该反应只在高温下自发,该反应为吸热反应,则 ,
故A错误;
B.加入催化剂只改变反应速率,不影响平衡移动,不能提高 的平衡转化率,故B错误;
C.物质的量分数均随温度升高减小,温度低温时反应Ⅲ不发生,只发生反应Ⅰ和Ⅱ,所以二氧化碳的物
质的量分数小于甲烷物质的量分数,平衡时CO 的物质的量分数随温度变化的曲线是a,故C错误;
2
D.曲线c、d分别代表CO 和CH 的转化率曲线,温度高于1300K后,升高温度有利于积碳反应的进行,
2 4
导致CH 的转化率大于CO,故D正确;
4 2
故选:D。
4.(2023·江苏·校联考模拟预测)工业上利用两种温室气体CH 和CO 催化重整制取H 和CO,主要反应
4 2 2
为
反应I:CH(g)+CO (g) 2CO(g)+2H(g) △H=+247.4kJ•mol-1 K
4 2 2 1
过程中还发生三个副反应:
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) △H=+41.2kJ•mol-1 K
2 2 2 2
反应Ⅲ:2CO(g) CO(g)+C(s) △H=-171.0kJ•mol-1 K
2 3
反应Ⅳ:CH(g) 2H(g)+C(s) △H K
4 2 4
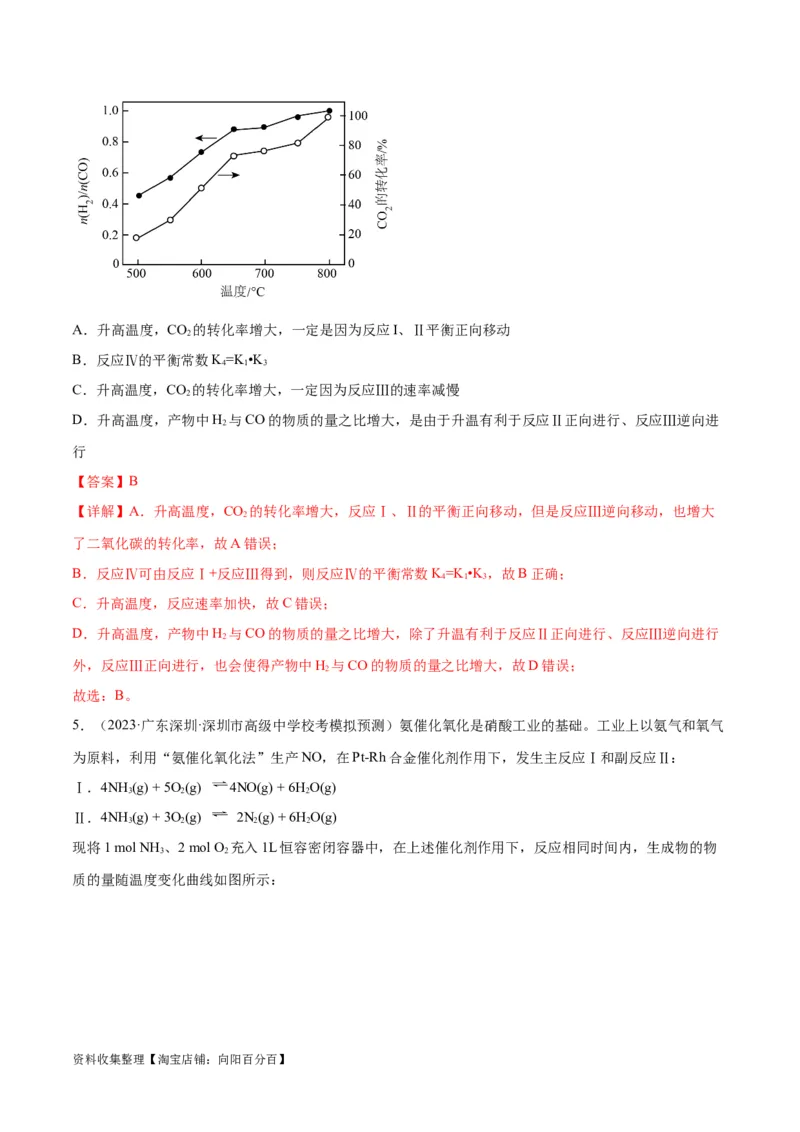
将CH 与CO(体积比为1:1)的混合气体以一定流速通过催化剂,产物中H 与CO的物质的量之比、CO
4 2 2 2
的转化率与温度的关系如图所示。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A.升高温度,CO 的转化率增大,一定是因为反应I、Ⅱ平衡正向移动
2
B.反应Ⅳ的平衡常数K=K •K
4 1 3
C.升高温度,CO 的转化率增大,一定因为反应Ⅲ的速率减慢
2
D.升高温度,产物中H 与CO的物质的量之比增大,是由于升温有利于反应Ⅱ正向进行、反应Ⅲ逆向进
2
行
【答案】B
【详解】A.升高温度,CO 的转化率增大,反应Ⅰ、Ⅱ的平衡正向移动,但是反应Ⅲ逆向移动,也增大
2
了二氧化碳的转化率,故A错误;
B.反应Ⅳ可由反应Ⅰ+反应Ⅲ得到,则反应Ⅳ的平衡常数K=K •K ,故B正确;
4 1 3
C.升高温度,反应速率加快,故C错误;
D.升高温度,产物中H 与CO的物质的量之比增大,除了升温有利于反应Ⅱ正向进行、反应Ⅲ逆向进行
2
外,反应Ⅲ正向进行,也会使得产物中H 与CO的物质的量之比增大,故D错误;
2
故选:B。
5.(2023·广东深圳·深圳市高级中学校考模拟预测)氨催化氧化是硝酸工业的基础。工业上以氨气和氧气
为原料,利用“氨催化氧化法”生产NO,在Pt-Rh合金催化剂作用下,发生主反应Ⅰ和副反应Ⅱ:
Ⅰ.4NH (g) + 5O(g) 4NO(g) + 6H O(g)
3 2 2
Ⅱ.4NH (g) + 3O(g) 2N(g) + 6HO(g)
3 2 2 2
现将1 mol NH 、2 mol O 充入1L恒容密闭容器中,在上述催化剂作用下,反应相同时间内,生成物的物
3 2
质的量随温度变化曲线如图所示:
资料收集整理【淘宝店铺:向阳百分百】已知:有效转化率= ×100%
下列说法不正确的是
A.该催化剂在低温时对反应Ⅱ的选择性更好
B.520℃时,NH 的有效转化率约为66.7%
3
C.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
D.高于400℃,n(N )随温度升高而下降可能是反应Ⅱ的平衡逆向移动导致
2
【答案】B
【详解】A.由图可知,低温时反应的主要产物为氮气,即主要发生反应Ⅱ,说明该催化剂在低温时对反
应Ⅱ的选择性更好,A正确;
B.由图可知,520℃时,NH 发生反应I生成NO 0.2mol,消耗氨气0.2mol,NH 发生反应Ⅱ生成N
3 3 2
0.2mol,消耗氨气0.4mol,则NH 的有效转化率为 ,B错误;
3
C.由图可知,840℃时,反应相同时间内,NO的物质的量最大,副产物N 的物质的量最小,说明该温度
2
下最有利于NO的生成,因此工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右,C正确;
D.400℃后n(N )随温度升高而下降,其原因可能是:该反应为放热反应,高于400℃时平衡逆向移动,使
2
得N 的物质的量减少,D正确;
2
故选B。
6.(2023·广东广州·华南师大附中校考三模)在盛有 载氧体的恒容密闭容器中充入空气,发生
反应: 。平衡时 的体积分数 随反应温度 变化的曲线如图所
示。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.
B.该反应的平衡常数表达式为
C.在 时加入催化剂,平衡时
D. 达到平衡状态后,充入纯氧,再次达到平衡后,
【答案】C
【详解】A.平衡时 的体积分数 随温度升高而增大,则升温平衡左移, ,A正确;
B. 该反应方程式为 ,则按定义,其平衡常数表达式为 ,B正
确;
C. 由图知,在 时平衡时 ,催化剂通常能加快反应但不影响平衡,则加入催化剂时
,C不正确;
D. 达到平衡状态后,充入纯氧不影响平衡常数, ,则再次达到平衡后, ,
D正确;
答案选C。
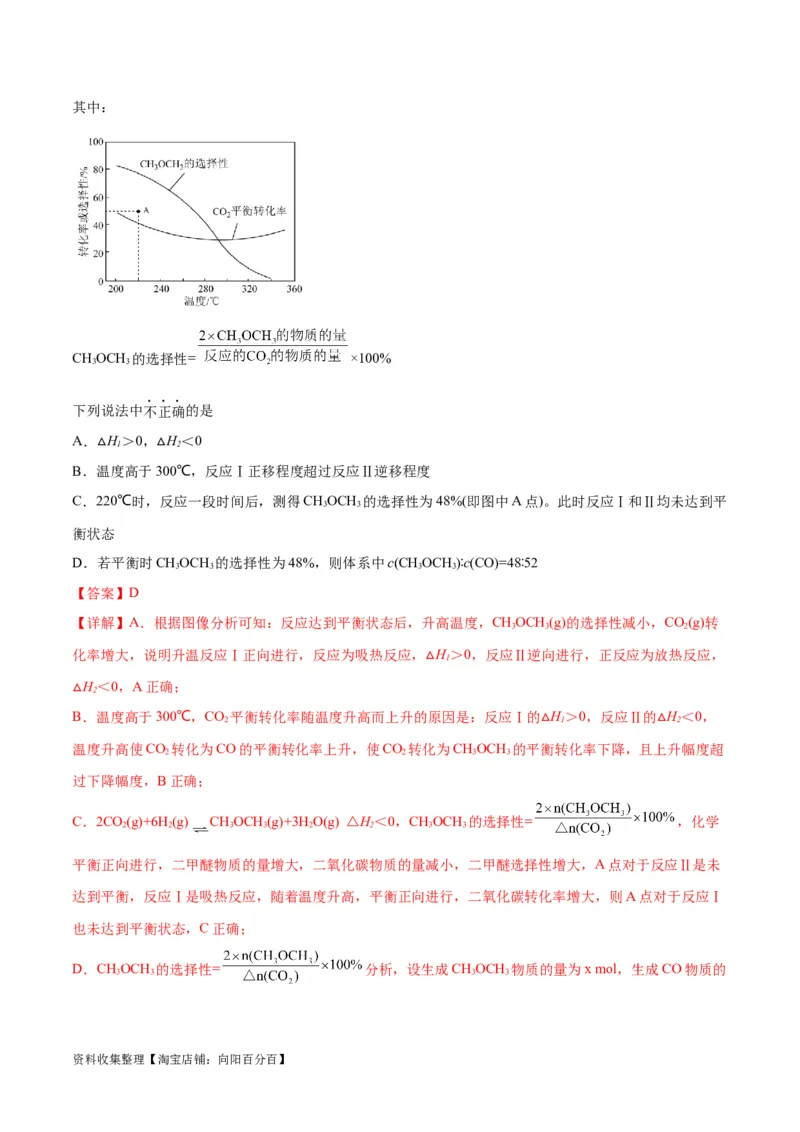
7.(2023·北京海淀·101中学校考三模)CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发
2 2
生下列反应:
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g) △H
2 2 2 1
反应Ⅱ:2CO(g)+6H(g) CHOCH (g)+3HO(g) △H
2 2 3 3 2 2
恒压,投入1 mol CO 和适当过量的H,CO 平衡转化率和平衡时CHOCH 的选择性随温度的变化如图。
2 2 2 3 3
资料收集整理【淘宝店铺:向阳百分百】其中:
CHOCH 的选择性= ×100%
3 3
下列说法中不正确的是
A. H>0, H<0
1 2
B.温△度高于3△00℃,反应Ⅰ正移程度超过反应Ⅱ逆移程度
C.220℃时,反应一段时间后,测得CHOCH 的选择性为48%(即图中A点)。此时反应Ⅰ和Ⅱ均未达到平
3 3
衡状态
D.若平衡时CHOCH 的选择性为48%,则体系中c(CHOCH )∶c(CO)=48∶52
3 3 3 3
【答案】D
【详解】A.根据图像分析可知:反应达到平衡状态后,升高温度,CHOCH (g)的选择性减小,CO(g)转
3 3 2
化率增大,说明升温反应Ⅰ正向进行,反应为吸热反应, H>0,反应Ⅱ逆向进行,正反应为放热反应,
1
H<0,A正确; △
2
△B.温度高于300℃,CO 平衡转化率随温度升高而上升的原因是:反应Ⅰ的 H>0,反应Ⅱ的 H<0,
2 1 2
温度升高使CO 转化为CO的平衡转化率上升,使CO 转化为CHOCH 的平衡△转化率下降,且上△升幅度超
2 2 3 3
过下降幅度,B正确;
C.2CO(g)+6H(g) CHOCH (g)+3HO(g) △H<0,CHOCH 的选择性= ,化学
2 2 3 3 2 2 3 3
平衡正向进行,二甲醚物质的量增大,二氧化碳物质的量减小,二甲醚选择性增大,A点对于反应Ⅱ是未
达到平衡,反应Ⅰ是吸热反应,随着温度升高,平衡正向进行,二氧化碳转化率增大,则A点对于反应Ⅰ
也未达到平衡状态,C正确;
D.CHOCH 的选择性= 分析,设生成CHOCH 物质的量为x mol,生成CO物质的
3 3 3 3
资料收集整理【淘宝店铺:向阳百分百】量为y mol,反应的二氧化碳为(2x+y) mol,得到 =48%, ,则体系中
c(CHOCH )∶c(CO)=6∶13,D错误;
3 3
故合理选项是D。
8.(2023·重庆·校联考三模) 时,存在如下平衡: 。该反应正、逆反应速率与
的浓度关系为: , ( 是速率常数),且 与
的关系如图所示,下列说法正确的是
A.图中表示 的是线Ⅱ
B. 时,往刚性容器中充入一定量 ,平衡后测得 为 ,则平衡时
C. 时,该反应的平衡常数
D. 时向 恒容密闭容器中充入 ,某时刻 ,则此时 的转化率
为
【答案】C
【分析】因 ,则 ; ,同理可得:
,由函数关系可知 的斜率大于 ,结合图像可知线Ⅰ应为 ,
资料收集整理【淘宝店铺:向阳百分百】线Ⅱ应为 ,据此分析解答。
【详解】A.由以上分析可知线Ⅰ应为 ,故A错误;
B.由以上分析可知线Ⅱ应为 ,又 ,结合图像可知当 =0
时, =a,则 ,平衡后测得 为 ,则平衡时 ,故B错误;
C.线Ⅰ应为 , ,当 =0时, =a+2,则
,反应达到平衡状态时: , = =100,故
C正确;
D.某时刻 ,此时 ,则此时 的转化率=
,故D错误;
故选:C。
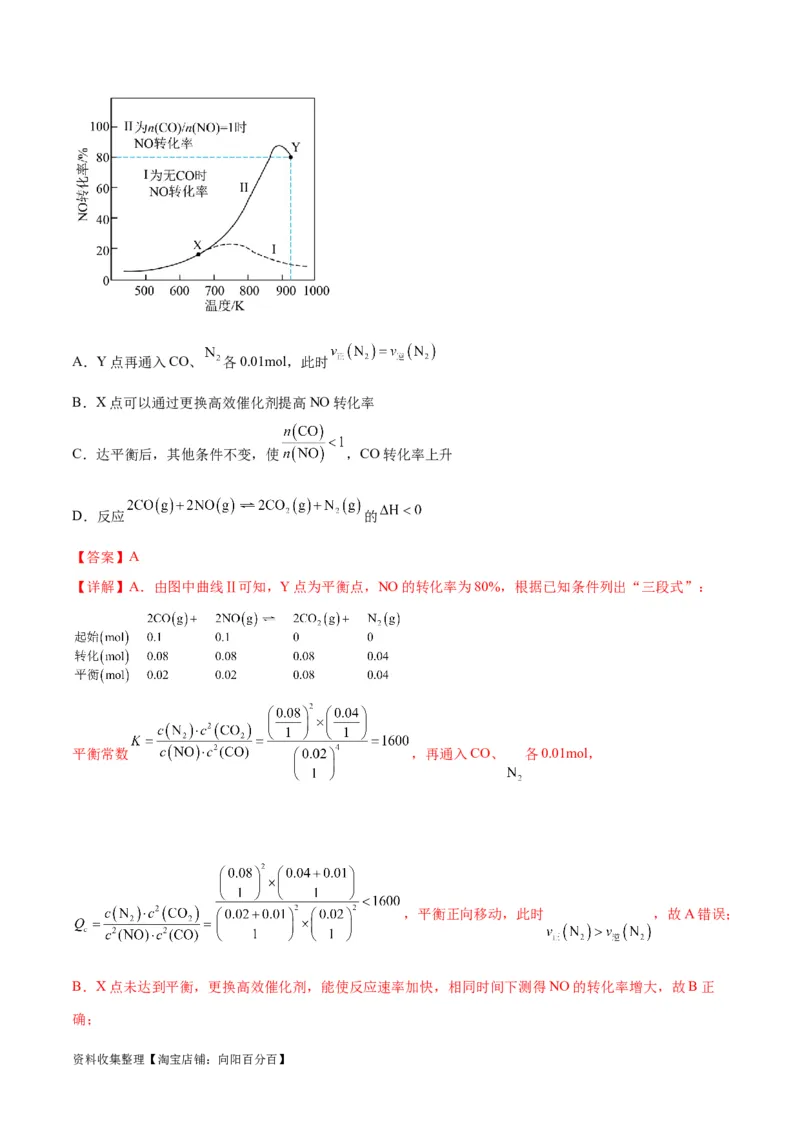
9.(2023·湖南长沙·长沙一中校考模拟预测)某研究小组以,Ag-ZSM为催化剂,在容积为1L的容器中,
相同时间下测得0.1molNO转化为 的转化率随温度变化如图所示[无CO时反应为
;有CO时反应为 ]。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.Y点再通入CO、 各0.01mol,此时
B.X点可以通过更换高效催化剂提高NO转化率
C.达平衡后,其他条件不变,使 ,CO转化率上升
D.反应 的
【答案】A
【详解】A.由图中曲线Ⅱ可知,Y点为平衡点,NO的转化率为80%,根据已知条件列出“三段式”:
平衡常数 ,再通入CO、 各0.01mol,
,平衡正向移动,此时 ,故A错误;
B.X点未达到平衡,更换高效催化剂,能使反应速率加快,相同时间下测得NO的转化率增大,故B正
确;
资料收集整理【淘宝店铺:向阳百分百】C.达平衡后,其他条件不变,使 ,相当于增大NO的浓度,平衡正向移动,CO的转化率上升,
故C正确;
D.由图中曲线Ⅱ可知,随着温度的升高,反应速率增大,相同时间内NO的转化率增大,当NO的转化率
最大时,说明反应达到平衡,继续升高温度,NO的转化率减小,说明平衡进向移动,该反应为放热反应,
反应 的 ,故D正确;
故选A。
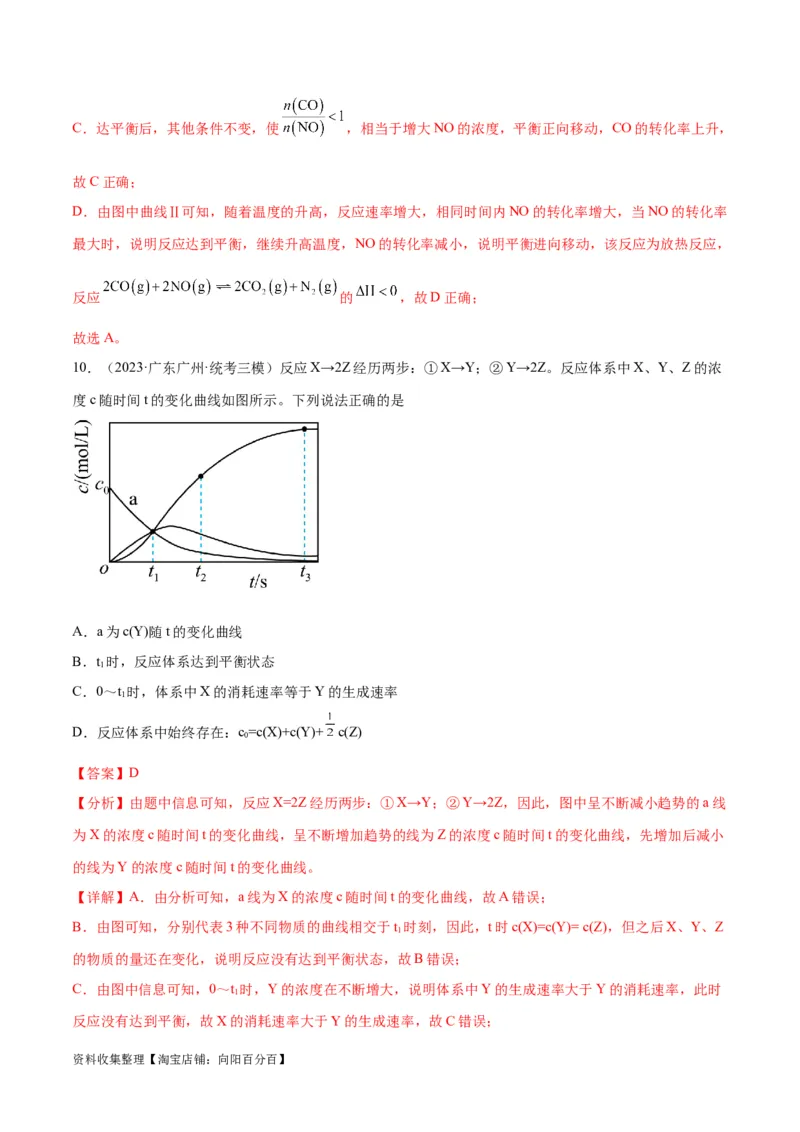
10.(2023·广东广州·统考三模)反应X→2Z经历两步:①X→Y;②Y→2Z。反应体系中X、Y、Z的浓
度c随时间t的变化曲线如图所示。下列说法正确的是
A.a为c(Y)随t的变化曲线
B.t 时,反应体系达到平衡状态
1
C.0~t 时,体系中X的消耗速率等于Y的生成速率
1
D.反应体系中始终存在:c=c(X)+c(Y)+ c(Z)
0
【答案】D
【分析】由题中信息可知,反应X=2Z经历两步:①X→Y;②Y→2Z,因此,图中呈不断减小趋势的a线
为X的浓度c随时间t的变化曲线,呈不断增加趋势的线为Z的浓度c随时间t的变化曲线,先增加后减小
的线为Y的浓度c随时间t的变化曲线。
【详解】A.由分析可知,a线为X的浓度c随时间t的变化曲线,故A错误;
B.由图可知,分别代表3种不同物质的曲线相交于t 时刻,因此,t时c(X)=c(Y)= c(Z),但之后X、Y、Z
1
的物质的量还在变化,说明反应没有达到平衡状态,故B错误;
C.由图中信息可知,0~t 时,Y的浓度在不断增大,说明体系中Y的生成速率大于Y的消耗速率,此时
1
反应没有达到平衡,故X的消耗速率大于Y的生成速率,故C错误;
资料收集整理【淘宝店铺:向阳百分百】D.反应X→2Z经历两步:①X→Y;②Y→2Z,反应刚开始时c(X)=c mol/L,c(Z)=c(Y)=0mol/L,由反应
0
的系数关系可知,X的消耗量等于Y的生产量,Y的消耗量等于Z生成量的一半,则反应体系中始终存在:
c=c(X)+c(Y)+ c(Z),故D正确;
0
故选D。
11.(2023·重庆渝中·重庆巴蜀中学校考模拟预测)1,2-二甲基环丙烷的顺反异构体可相互转化:
(顺式) (反式) ,该反应的速率方程为: (顺)和 (反),
和 分别为正、逆反应速率常数。 ℃时,加入顺式异构体发生反应,两种异构体的质量分数w随时间t
的变化如图所示。下列说法正确的是
A.反应速率: (正) (逆)
B.L点:转化率为50%,Q(浓度商)>K
C.升高温度, 、 增大倍数:
D. ℃时发生反应,测得 ,则
【答案】C
【详解】A.M和N点反应未达到平衡,则 (正) (逆), (正) (逆),反应过程中v(正)不断减小,
则 (正)> (正),则 (正) (逆),故A错误;
资料收集整理【淘宝店铺:向阳百分百】B.L点时,顺1,2-二甲基环丙烷和逆1,2-二甲基环丙烷的质量分数相等,由方程式 (顺式)
(反式)可知,此时顺1,2-二甲基环丙烷转化了一半,转化率为50%,此时反应未达到平
衡,平衡正向进行,Q(浓度商)M(c)。同一温度下,增大压强平衡正向,即压强越大平均摩尔
质量越大即M(b)>M(d),B项错误;
C. 建立三段式位 ,计算x(A)= 、x(B)=
、x(C)= 。最终计算Kp= ,C项正确;
D.d点平衡点2v (A)=2v (A)=v (B),D项错误;
正 逆 逆
故选C。
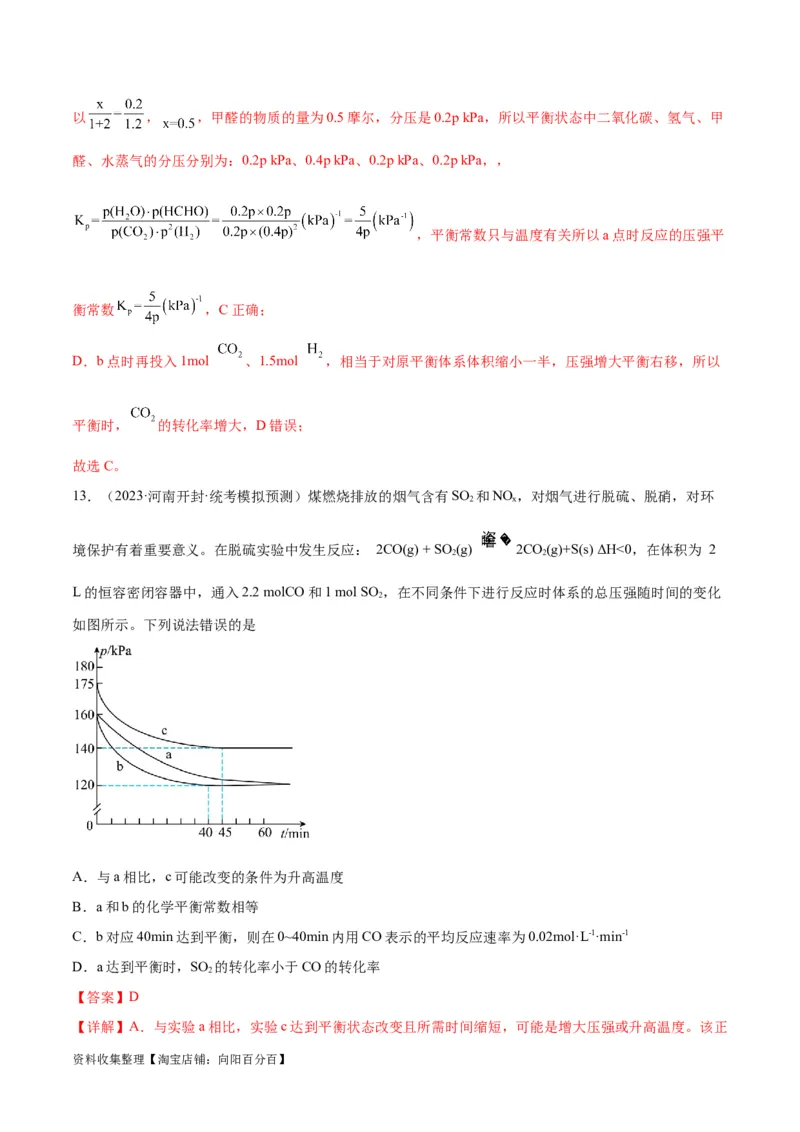
15.(2023·江苏南通·统考模拟预测)利用 和CO反应生成 的过程中主要涉及的反应如下:
反应Ⅰ kJ⋅mol-1
反应Ⅱ kJ⋅mol-1
[ 的产率 , 的选择性 ]。保持温度一定,在固定容积
的密闭容器中进行上述反应,平衡时 和 的产率及CO和 的转化率随 的变化情况如图所
示。下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.当容器内气体总压不变时,反应Ⅱ达到平衡状态75a
B.曲线c表示 的产率随 的变化
C. ,反应达平衡时, 的选择性为50%
D.随着 增大, 的选择性先增大后减小
【答案】B
【详解】A.反应I、Ⅱ可以合并为反应2CO(g)+2H(g)==CH (g)+CO (g),是气体总体积缩小的反应,当固
2 4 2
定密闭容器内总压不变时则反应I、Ⅱ都达到平衡状态,A正确;
B.通过总反应式2CO(g)+2H(g)=CH (g)+CO (g),随着n(H )的增加,超过1时,CH 的产率n(CO)受CO
2 4 2 2 4
浓度影响,故CH 的产率曲线会先增大后平缓,应该是a曲线,B错误;
4
C.通过总反应式2CO(g)+2H(g)=CH (g)+CO (g),当 =0.5时,生成物n(CH)=n(CO),故CH 的选
2 4 2 4 4
择性为50%,C正确;
D.随着 的不断增加,作为反应Ⅱ的生成物浓度不断增加会抑制CO 的生成,故CO 选择性先增大
2 2
后减小,D正确;
故选B。
考点二 化学平衡状态 平衡的移动 分值:30分 建议用时:20分钟
资料收集整理【淘宝店铺:向阳百分百】一、选择题(每小题2分,共30分)
1.(2023·江苏扬州·统考三模)含氮物质可发生如下反应:①
②
③
下列说法正确的是
A.常温下,NO与 混合能立即看到红棕色气体,说明该反应已达平衡
B.反应②的
C.反应③消耗 ,理论上会生成标准状况下约
D.利用反应①、②、③可以同时处理 含量较高的废气和含 的废水
【答案】C
【详解】A.常温下,NO与 混合能立即看到红棕色气体,说明该反应生成了二氧化氮气体,但是不确
定是否平衡,故A错误;
B.反应②为气体分子数减小的反应,为熵减反应,故B错误;
C.由方程式可知,反应③消耗 ,理论上会生成1mol氮气,在标准状况下约 ,故C正
确;
D.反应中涉及氢氧化钠和氯化铵两种物质,两者会反应生成氨气和氯化钠,故不能利用反应①、②、③
可以同时处理 含量较高的废气和含 的废水,故D错误。
故选C。
2.(2023·上海·模拟预测)一定温度下,向1L密闭容器中充入2molX和1molY,发生反应2X(g)
+Y(g)⇌3Z(?)。达到平衡时,容器的压强从原来的P
0
变为0.4P
0
。下列说法错误的是
A.Z不可能为气体
B.达到平衡时容器内有1.8molZ
C.压缩体积,再次达到平衡,X的浓度不变
D.Y的体积分数不变说明反应达到平衡状态
资料收集整理【淘宝店铺:向阳百分百】【答案】D
【详解】A.若Z为气体,则反应前后气体的压强不变,题目中压强从原来的P 变为0.4P 故Z不可能为气
0 0
体,故A正确;
B.根据向1L密闭容器中充入2molX和1molY,发生反应2X(g)+Y(g)⇌3Z(?)。达到平衡时,容器的压强
从原来的P 变为0.4P ,则
0 0
则 ,则x= 0.6,故达到平衡时容器内有1.8molZ,故B正确;
C.Z为非气体,故压缩体积,再次达到平衡,X的浓度不变,故C正确;
D.反应体系中只有X和Y,Y的体积分数一直为 ,故Y的体积分数不变不能说明反应达到平衡状态,
故D错误;
故选D。
3.(2023·全国·模拟预测)在恒温恒容的密闭容器中,在某催化剂表面上发生分解反应:
,测得不同起始浓度和不同催化剂表面积时Z的浓度随时间的变化如表所示。下列
说法错误的是
编
0 20 40 60 80
号
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,100 min时反应达到平衡状态
B.实验②,60 min时反应处于平衡状态
C.相同条件下,增大催化剂的表面积,Z的平衡转化率不变
D.相同条件下,增加Z的浓度,反应速率增大
资料收集整理【淘宝店铺:向阳百分百】【答案】D
【详解】A.由实验①中数据可知,该反应的速率保持不变,对比实验①、③可知,实验①达到平衡时Z
的浓度也为 ,而实验①中100 min时Z的浓度减小到 ,即100 min时反
应达到平衡状态,选项A正确;
B.由数据分析知,反应速率不变,若实验②中60 min时没有达到平衡状态,则Z的浓度为0,与可逆反
应的特点不符,所以60 min时反应已达平衡状态,选项B正确;
C.增大催化剂的表面积,能加快反应速率,但不影响化学平衡,即Z的平衡转化率不变,选项C正确;
D.实验①和②催化剂表面积相同,实验①中Z的起始浓度是实验②的2倍,实验①、②中0~20 min和
20~40 min内,∆c(Z)都是 ,则相同条件下增加Z的浓度,反应速率并未增大,选项D错
误;
答案选D。
4.(2023·重庆万州·重庆市万州第二高级中学校考模拟预测)在恒温恒容密闭容器中进行反应:
,下列能作为反应已达到平衡状态的依据是
A. 不再变化 B.反应速率:
C.容器内气体的压强不再变化 D.容器内气体的密度不再变化
【答案】A
【详解】A.反应 的平衡常数K= ,当
不再变化时,说明 =K,说明反应达到平衡,故A选;
B.反应速率: ,不能说明正逆反应速率相等,不能作为反应已达到平衡状态的依据,故
B不选;
C.反应 是气体体积不变的反应,反应过程中容器内气体的压强不变,
资料收集整理【淘宝店铺:向阳百分百】当容器内气体的压强不再变化时,不能说明反应达到平衡,故C不选;
D.反应过程中气体总质量和总体积不变,则反应过程中容器内气体的密度是定值,当容器内气体的密度
不再变化时,不能说明反应达到平衡,故D不选;
故选A。
5.(2023·江苏·模拟预测)对于可逆反应 ,下列说法错误的是
A.当 时,该反应达到平衡状态
B.该反应在一定条件下能自发进行,则
C.恒温恒容条件下,若混合气体的颜色保持不变,则该反应达到平衡状态
D.恒温恒容条件下,达平衡状态后,再充入一定量的 , 转化率将减小
【答案】D
【详解】A.反应达到平衡状态,正逆反应速率比等于系数比,所以当 时,该反应
达到平衡状态,故A正确;
B. ,该反应在一定条件下能自发进行,说明在一定条件下 ,则
,故B正确;
C.恒温恒容条件下,若混合气体的颜色保持不变,说明 浓度不变,则该反应达到平衡状态,故C正
确;
D. 正反应气体系数和减小,恒温恒容条件下,达平衡状态后,再充入一定量的 ,
相当于加压, 转化率将增大,故D错误;
选D。
6.(2023·辽宁·校联考一模)一种制备蓝氢的原理是 。向一体积为
1L的恒容密闭容器中充入1mol 和2mol ,在一定条件下发生上述反应,测得 的物质的量
与时间的关系如表所示。下列叙述错误的是
t/min 0 5 10 15 20 25
资料收集整理【淘宝店铺:向阳百分百】/mol 0 0.5 0.75 0.85 0.9 0.9
A.0~10min,
B.CO的体积分数不变时,反应达到平衡状态
C.上述反应中, 的转化率大于 的转化率
D.其他条件不变。若加入高效催化剂,则 的转化率达到45%时所用时间小于20min
【答案】A
【详解】A.0~10min, ,由方程式可知
,故A错误;
B.CO的体积分数不变时,说明CO的物质的量不变,说明反应达到平衡,故B正确;
C.达到平衡时, =0.9mol,由方程式的系数关系可知, 的转化率为 =45%,
的转化率为 =22.5%, 的转化率大于 的转化率,故C正确;
D.其他条件不变。若加入高效催化剂,反应速率增大,但不影响最终平衡时 的转化率,则 的转
化率达到45%时所用时间小于20min,故D正确;
故选A。
7.(2023·天津·校联考一模)一定温度下,在密闭容器中发生反应:
。下列说法正确的是
A.在恒容条件下,向平衡体系中充入惰性气体,平衡不移动
B.在恒压条件下,向平衡体系中加入 , 的转化率不变
C.混合气体的物质的量不再发生变化可说明反应达到平衡
D.该反应在任何温度下都能自发进行
【答案】A
资料收集整理【淘宝店铺:向阳百分百】【详解】A.在恒容条件下,向平衡体系中充入惰性气体,反应体系中各物质的浓度不变,平衡不移动,A
正确;
B.在恒压条件下,向平衡体系中加入 ,平衡正向移动, 的转化率变大,B错误;
C.该反应气体总物质的量不变,故混合气体的物质的量不变不能说明反应到平衡,C错误;
D.该反应为吸热的,不是在任何温度下都能自发进行,D错误;
故选A。
8.(2023·辽宁鞍山·统考一模)T 时,向容积为5L的恒容密闭容器中充入一定量的A(g)和B(g),发生反
0
应: 。测得反应过程中的部分数据如表所示,下列说法错误的是
t/min n(A)/mol n(B)/mol
0 4.0 2.0
5 2.0 1.0
10 2.0 1.0
A.其他条件不变,温度变为T 时,平衡时测得C的浓度为0.8mol/L,则T>T
1 1 0
B.8min时,该反应的v(正)=v(逆)
C.5min时,该反应达到平衡状态,且A、B的转化率相等
D.平衡时,C的体积分数约为42.9%
【答案】A
【详解】A.正反应放热,升高温度平衡逆向移动,根据图表数据,T 时达到平衡,消耗1molB,则生成
0
3molC,C的浓度为0.6 mol/L,其他条件不变,温度变为T 时,平衡时测得C的浓度为0.8mol/L,说明平
1
衡正向移动,则T0,下列说法正确的是
2 2 2
A.已知该反应在加热条件下能自发进行,则其 S>0
△
B.上述反应的平衡常数K=
C.上述反应中消耗1 mol H S,生成22.4 L水蒸气
2
D.实际应用中,通过增加HS的量来提高CO 转化率,能有效减少碳排放
2 2
【答案】A
【详解】A.已知该反应在加热条件下能自发进行所以 ,因为 H>0,所以 S>0,A正确;
△ △
B.由反应方程式,结合平衡常数含义可知,上述反应的平衡常数K= ,B错误;
C.没有指明具体条件,不能确定气体的体积,C错误;
D.增加HS毫无疑问可以增大CO 的转化率,减少二氧化碳的排放,但过量的HS对环境的危害更大,
2 2 2
实际中不能这样应用,D错误;
资料收集整理【淘宝店铺:向阳百分百】故选A。
15.(2023·江苏·模拟预测) 在催化剂条件下可被 还原为无害物质,反应为:
。下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中生成 ,转移电子的数目为
D.上述反应中,充入水蒸气增大压强可以提高 平衡转化率
【答案】B
【详解】A.由方程式可知,该反应是一个气体分子数减小的反应,即熵减的反应,反应 ,故A错
误;
B.由方程式可知,反应平衡常数 ,故B正确;
C.由方程式可知,生成 时,转移电子的数目为 ,故C错误;
D.充入水蒸气会增大水蒸气浓度,平衡逆向移动,NO转化率减小,故D错误;
故答案为:B。
资料收集整理【淘宝店铺:向阳百分百】