文档内容
解密 06 金属及其化合物
一、选择题
1.(2021·江苏期末)2020年11月10日8时12分,中国“奋斗者”号载人潜水器在马里亚纳海沟成功
坐底。“奋斗者”号研制及海试的成功,标志着我国具有了进入世界海洋最深处开展科学探索的能力,体
现了我国在海洋高技术领域的综合实力。其中,“奋斗者”号使用了钛合金材料。有关合金的说法中正确
的是( )
A.钛合金是一种新型金属单质
B.在合金中加入稀土金属,对改善合金的性能无太大影响
C.钛合金熔点比成分金属低,但硬度大
D.钛合金的化学性质与钛单质相同
2.(2021·辽宁省葫芦岛协作校高三第二次联考)我国古代的青铜器工艺精湛,有很高的艺术价值和历
史价值。下列说法不正确的是( )
A.我国使用青铜器的时间比使用铁器、铝器的时间均要早
B.将青铜器放在银质托盘上,青铜器容易生成铜绿
C.《本草纲日》中载有一药物,名“铜青”,铜青是铜器上的绿色物质,则铜青就是青铜
D.用蜂蜡做出铜器的蜡模,是古代青铜器的铸造方法之一,蜂蜡的主要成分是有机物
3.(2021·吉林省四平市双辽二中高三期末考试)明末科学家宋应星出版的《天工开物》中记载了有关
“五金”的内容:“∙∙∙∙∙∙黄金美者,其值去黑铁(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指
菜刀、镰刀、锄头等)、斧不呈效于日用之间∙∙∙∙∙∙ ∙∙∙∙∙∙贸迁有无,∙∙∙∙∙∙”,下列解释正确的是( )
A.明代使用的釜、鬵一类的炊具都属于青铜合金
B.添加了铬、镍的不锈钢菜刀和农具使用后即使不保养,也不会生锈
C.金属的另一个用途就是铸成钱币作为贸易交往中的流通手段
D.黑铁在空气中发生的腐蚀主要是化学腐蚀
4.下列关于元素及其化合物的说法不正确的是( )
A.Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应
B.Al、Cl 均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同
2
C.在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO 固体,铜粉会溶解
3
D.金属单质Na、Mg、Fe在一定条件下与水反应都生成H 和相应的碱
2
5.下列关于金属冶炼的说法正确的是( )
A.由于Al的活泼性强,故工业上采用电解熔融AlCl 的方法生产Al
3B.可以用钠加入氯化镁饱和溶液中制取镁
C.炼铁高炉中所发生的反应都是放热的,故无需加热
D.金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定
6.下列选项所表示的物质间转化关系均能一步转化的是( )
A.Na → Na O → Na CO → NaOH
2 2 2 3
B.NaCl → NaHCO → Na CO → Na O
3 2 3 2 2
C.Al → Al O → Al(OH) → NaAlO
2 3 3 2
D.Fe(s) Fe O(s) FeCl (aq)
2 3 3
7.(2021·河北衡水中学高三七调)硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制
备方法错误的是( )
A.制备碱式硫酸铁利用了过氧化氢氧化性
B.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D. 制备(NH )Fe(SO ) 利用了它的溶解度比FeSO 的溶解度大这一性质
4 2 4 2 4
8.(2021·安徽省皖江联盟高三联考).侯德榜是近代化学工业的奠基人之一,是世界制碱业的权威。某
同学在实验室模拟侯氏制碱法生产的纯碱中含有少量NaCl,下列说法正确的是( )
A.相同温度下,碳酸钙在纯碱溶液中的溶度积小于在水中的溶度积
B.用标准盐酸滴定一定质量的样品,可以测量出纯碱的纯度
C.用托盘天平称取10.60g样品配制溶液进行实验
D.只用硝酸银溶液,即可鉴别样品溶液中是否含有氯离子
9.(2021·湖南怀化市期末)下列实验方案不能准确测出NaCO、NaHCO 混合物中NaCO 质量分数的
2 3 3 2 3
是(不考虑实验误差)( )
A.取mg混合物充分加热,质量减少ng
B.取mg混合物与足量稀盐酸完全反应,将反应后溶液加热、蒸发、干燥,得到ng固体
C.取mg混合物与足量Ca(OH) 溶液完全反应将反应后浑浊液过滤、洗涤、干燥,得到ng固体
2
D.取mg混合物与足量稀硫酸完全反应,逸出气体直接用碱石灰吸收,质量增加ng
10.(2021·湖南怀化市期末)下列实验操作和现象、结论或目的均正确的是( )
选项 操作和现象 结论或目的
A 将饱和的FeCl 溶液滴加到浓NaOH溶液中 制备Fe(OH) 胶体
3 3
B 向钠与水反应形成的溶液中滴加几滴酚酞,溶液变红 钠与水反应生成了碱C 向CuSO 溶液中加入一小块钠,生成气体和沉淀 沉淀为Cu
4
D 向某溶液中通入HO,再加入KSCN溶液,溶液变红色 原溶液中一定含有Fe3+
2 2
11.混合物M中可能含有A1 O、Fe O、Al、Cu,为确定其组成,某同学设计如图所示分析方案。下
2 3 2 3
列分析正确的是( )
A.已知m>m,则混合物M中一定含有A1 O
1 2 2 3
B.生成蓝绿色溶液的离子方程式为Cu+Fe3+=Cu2+ +Fe2+
C.固体P既可能是纯净物,又可能是混合物
D.要确定混合物M中是否含有A1,可取M加入过量NaOH溶液
12.某兴趣小组将过量Cu与FeCl 溶液充分及应,静置后取上层清液于试管中,将KSCN溶液滴加到
3
清液中,观察到瞬间产生白色沉淀,局部出现红色;振荡试管,红色又迅速褪去。已知:
①CuCl +Cu=2CuCl↓(白色)——该反应速率很慢
2
②2CuCl +4KSCN=2CuSCN↓(白色)+(SCN) +4KCl——该反应速率很快
2 2
③(SCN) 是拟卤素,化学性质和氯气相似
2
下列说法正确的是( )
A.用KSCN溶液检验Fe3+时,Cu2+的存在不会对检验产生干扰
B.局部出现红色主要是因为溶液中的Fe2+被空气中的O 氧化成Fe3+,Fe3+与KSCN反应生成Fe(SCN)
2 3
C.白色沉淀是CuCl,是溶液中CuCl 与Cu反应生成的
2
D.红色迅速褪去的原因是振荡试管时Cu2+与SCN-发生反应,从而使Fe3++3SCN- Fe(SCN) 平衡逆移
3
13.向100mL Fe (SO ) 和CuSO 的混合溶液中逐渐加入铁粉,充分反应后溶液中⇌固体剩余物的质量与
2 4 3 4
加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法正确的是( )A.a点时溶液中阳离子仅为Cu2+和Fe2+
B.b点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+
C.c点时加入的铁粉与Cu2+反应
D.原溶液中Fe (SO ) 和CuSO 的物质的量浓度之比为1∶1
2 4 3 4
14.(2021·陕西汉中市高三月考)工业以软锰矿(主要成分是MnO ,含有SiO、Fe O 等少量杂质)为主
2 2 2 3
要原料制备高性能的磁性材料碳酸锰(MnCO ),其工业流程如图。下列说法错误的是( )
3
A.浸锰过程中Fe O 与SO 反应的离子方程式为: Fe O+SO +2H+=2Fe2++SO +HO
2 3 2 2 3 2 2
B.过滤I所得滤液中主要存在的金属阳离子为Mn2+、Fe3+和Fe2+
C.滤渣II的主要成分含有Fe(OH)
3
D.过滤II所得的滤液中加入NH HCO 溶液发生反应的主要离子方程式为: Mn2++2HCO =MnCO↓
4 3 3
+CO↑+HO
2 2
15.(2021·四川成都市期末)高铁酸钠(NaFeO)具有很强的氧化性,能有效地杀灭水中的细菌和病毒,
2 4
同时被还原成Fe(OH) 能高效地除去水中的悬浮物,是一种新型高效水处理剂。其制备方法如下:
3
2Fe(OH) +3NaClO+4NaOH=2NaFeO+3NaCl+5H O。下列说法错误的是( )
3 2 4 2
A.NaFeO 中 元素显+6价
2 4
B.碱性条件下 氧化性强于NaFeO
2 4
C.每生成1mol Na FeO 转移6mol电子
2 4
D.在水处理中,NaFeO 兼具消毒和净水两种功能
2 4
16.(2021·广东珠海市期末)用铁泥(主要成分为Fe O、FeO和Fe)制备纳米 (平均直径25nm)的
2 3
流程示意图如下:下列叙述错误的是( )
A.步骤①中,生成车间要禁止烟火
B.步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C.步骤④中HO 应该过量
2 2
D.步骤⑤中,为验证得到因体是纳米态Fe O 粒子,可将其形成分散系,做丁达尔效应实验
3 4
17.(2021·湖南省临澧县第一中学高三质检)某废催化剂含SiO、ZnS、CuS及少量的Fe O。某实验小
2 3 4
组以该废催化剂为原料,回收锌和铜,设计实验流程如下:
下列说法正确的是 ( )
A.检验滤液1中是否含有Fe2+,可以选用KFe(CN) 溶液
4 6
B.步骤②操作中,应先加6%H O,然后不断搅拌下缓慢加入1.0 mol·L-1HSO
2 2 2 4
C.滤渣1成分是SiO 和CuS,滤渣2成分只有SiO
2 2
D.步骤①操作中,生成的气体需用NaOH溶液或CuSO 溶液吸收
4
18.(2021·河北唐山市山一中高三质检)银铜合金广泛应用于航空工业。从银铜合金的切割废料中回收
银和制备CuAlO 的流程如下。
2
已知:Al(OH) 和Cu(OH) 开始分解的温度分别为450℃和80℃。下列说法错误的是( )
3 2
A.电解精炼时,粗银做阳极,纯银做阴极
B.为提高原料利用率,流程中应加过量的稀NaOH
C.滤渣B煅烧时发生的反应为4CuO+4Al(OH) 4CuA1O +O ↑+6H O
3 2 2 2
D.若用1.0kg 银铜合金(铜的质量分数为64%)最多可生成10mol CuAlO
219.(2021·沈阳市辽宁实验中学期末)常温下,c(H+)=0.1mol/L的某溶液中可能含有Na+、Fe3+、Fe2+、
I-、Cl-、CO2-中的某几种离子,现取100mL该溶液进行如图所示实验:
3
已知氧化性Fe3+>I 。根据实验结果,判断下列说法正确的是( )
2
A.Fe3+与Fe2+至少有一种
B.一定不存在CO2-,可能存在Na+和Cl-
3
C.一定存在Fe2+、I-、Cl-
D.该溶液中一定存在Fe2+、I-,可能含Cl-
20.(2021·浙江绍兴市期末)某混合物X由Fe O、Cu、SiO 三种物质组成,进行如图实验:
2 3 2
下列有关说法正确的是( )
A.由Ⅰ可知Cu能与过量的盐酸发生置换反应
B.蓝色溶液中一定含有Cu2+、Fe2+,可能含有Fe3+
C.原混合物X中含Fe O 的质量是4.48g,SiO 的质量为3.0g
2 3 2
D.将Ⅰ和Ⅱ的顺序互换,不影响实验最后残留固体的质量
二、非选择题
21.(2021·湖南怀化市期末)某工厂的工业废水中含有大量的FeSO 和较多的Cu2+。为了减少污染并变
4
废为宝,工厂计划从该废水中回收FeSO 和金属铜。请根据以下流程图,回答下列问题:
4
(1)⑥操作方法的名称是__________________;操作⑨包括:蒸发浓缩、____________、过滤、洗涤、
低温干燥。(2)加入试剂⑤发生反应的离子方程式为________________________。
(3)试剂⑦的化学式为____________。
(4)某兴趣小组同学欲鉴别④中的金属阳离子,设计如下实验:
甲同学取2.0mL④溶液,滴加氢氧化钠溶液,产生白色沉淀且很快变为灰绿色,最后变为红褐色沉淀,
其中涉及氧化还原反应的化学方程式为___________________。
乙同学取2.0mL④溶液,先加入几滴KSCN溶液,无明显现象,再加入几滴氯水,溶液变红,其中涉
及氧化还原反应的离子方程式为___________________。
(5)若按上述工艺处理1000L该工业废水,制得320g铜,则该工业废水中c(Cu2+)=______。
22.(2021·石家庄市藁城区第一中学高三月考)三草酸合铁酸钾晶体(K [Fe(C O)]·3H O)能溶于水,难
3 2 4 3 2
溶于乙醇,该物质对光敏感,光照下即发生分解,产物之一是黄色的草酸亚铁。实验室可用如图流程来制
备三草酸合铁酸钾晶体。根据题意完成下列各题:
(1)若用废铁屑和稀硫酸制备绿矾,需先将废铁屑碱煮水洗,其目的是___________;然后与硫酸反应
时___________(填物质名称)往往要过量。
(2)要从溶液中得到绿矾晶体,必须进行的实验操作是___________(按前后顺序填代号)。
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)称取制得的绿矾晶体7.00 g,加稀硫酸溶解。加入一定量的草酸后,加热煮沸,形成黄色沉淀,过
滤,洗涤。如何确定沉淀已经洗涤干净:___________。
(4)氧化过程中除不断搅拌外,还需维持温度在40 ℃左右,原因是___________;写出氧化生成三草酸
合铁酸钾的离子方程式___________。
(5)经过一系列操作后得到的最终产物晶体先用少量冰水洗涤,再用无水乙醇洗涤,低温干燥后称量,
得到9.82 g翠绿色晶体,用无水乙醇洗涤晶体的目的是___________。
(6)列式计算本实验中三草酸合铁酸钾晶体的产率___________(保留一位小数)。
(7)某同学制得的三草酸合铁酸钾晶体表面发黄,推测可能有部分晶体见光分解。为了验证此推测是否
正确,可用的试剂及现象是________________________。
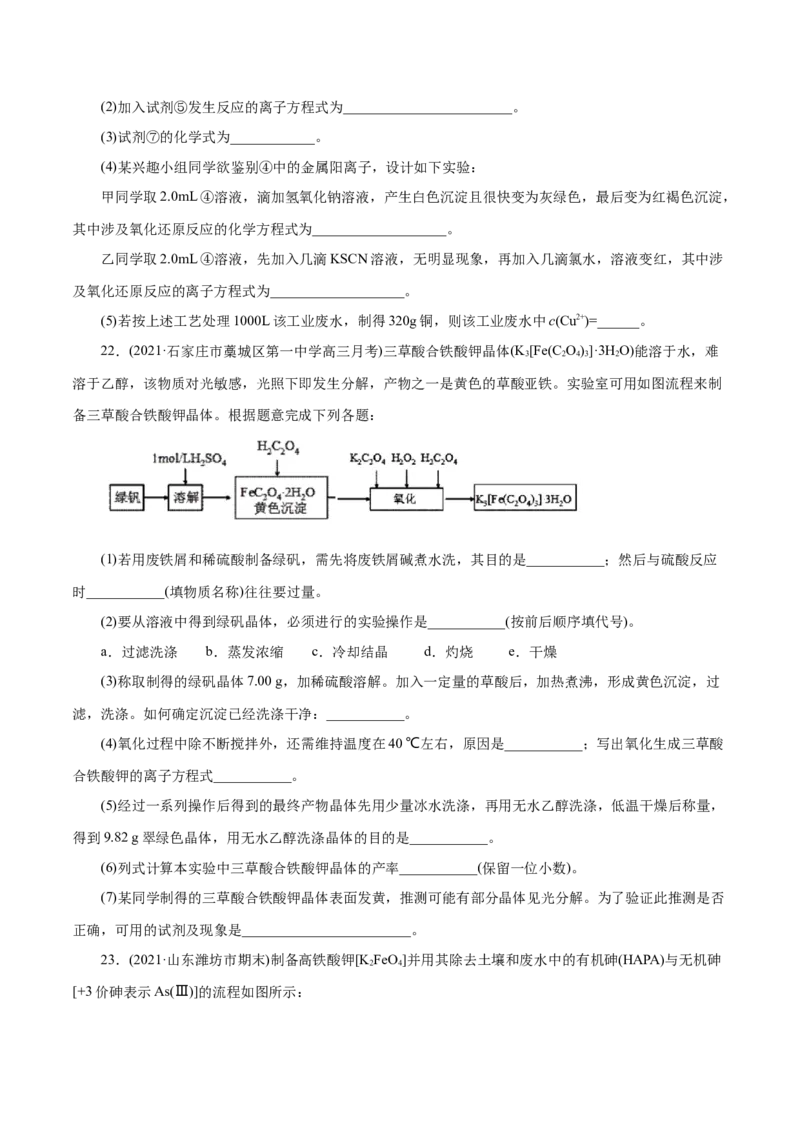
23.(2021·山东潍坊市期末)制备高铁酸钾[K FeO]并用其除去土壤和废水中的有机砷(HAPA)与无机砷
2 4
[+3价砷表示As(Ⅲ)]的流程如图所示:已知:酸性越强,KFeO 越容易发生反应生成O。
2 4 2
回答下列问题:
(1)生成KFeO 的化学方程式为________________。
2 4
(2)K FeO 去除砷污染时作_________(填“氧化剂”或“还原剂”)。若污染物中的砷全部以NaAsO 计,则
2 4 3 3
去除全部污染时NaAsO 与KFeO 的物质的量之比为_______________。
3 3 2 4
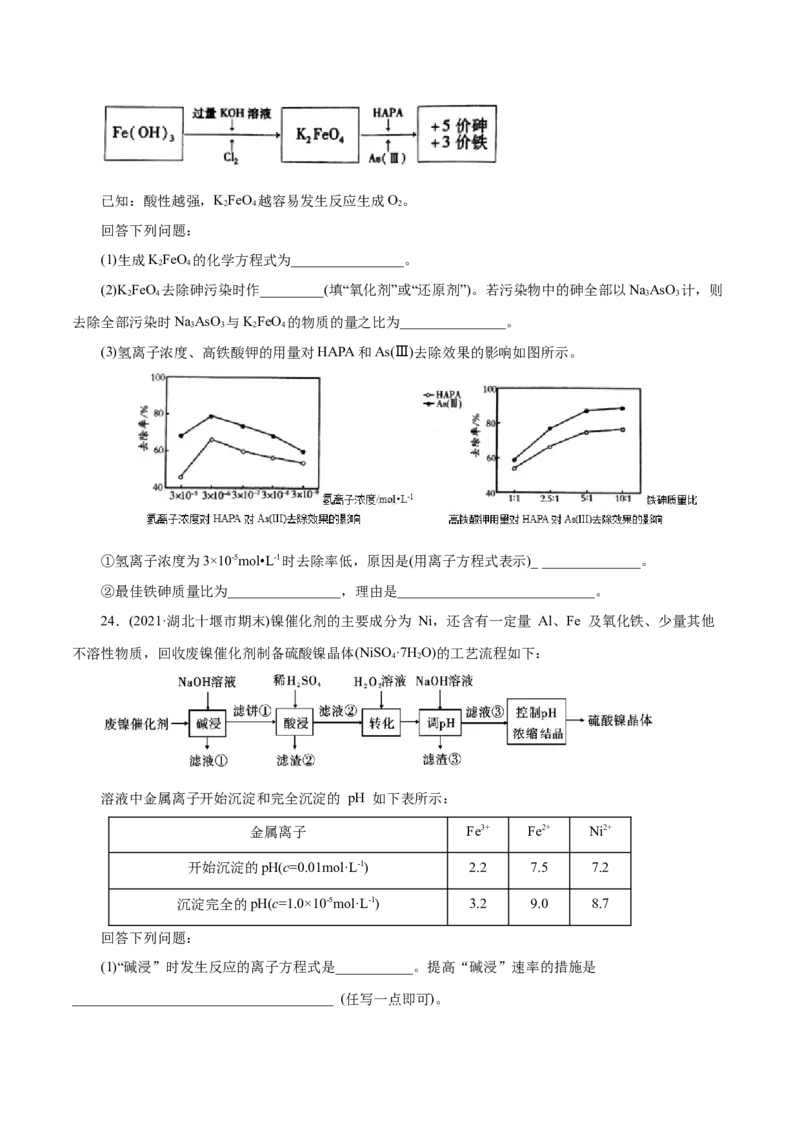
(3)氢离子浓度、高铁酸钾的用量对HAPA和As(Ⅲ)去除效果的影响如图所示。
①氢离子浓度为3×10-5mol•L-1时去除率低,原因是(用离子方程式表示)_ ______________。
②最佳铁砷质量比为________________,理由是____________________________。
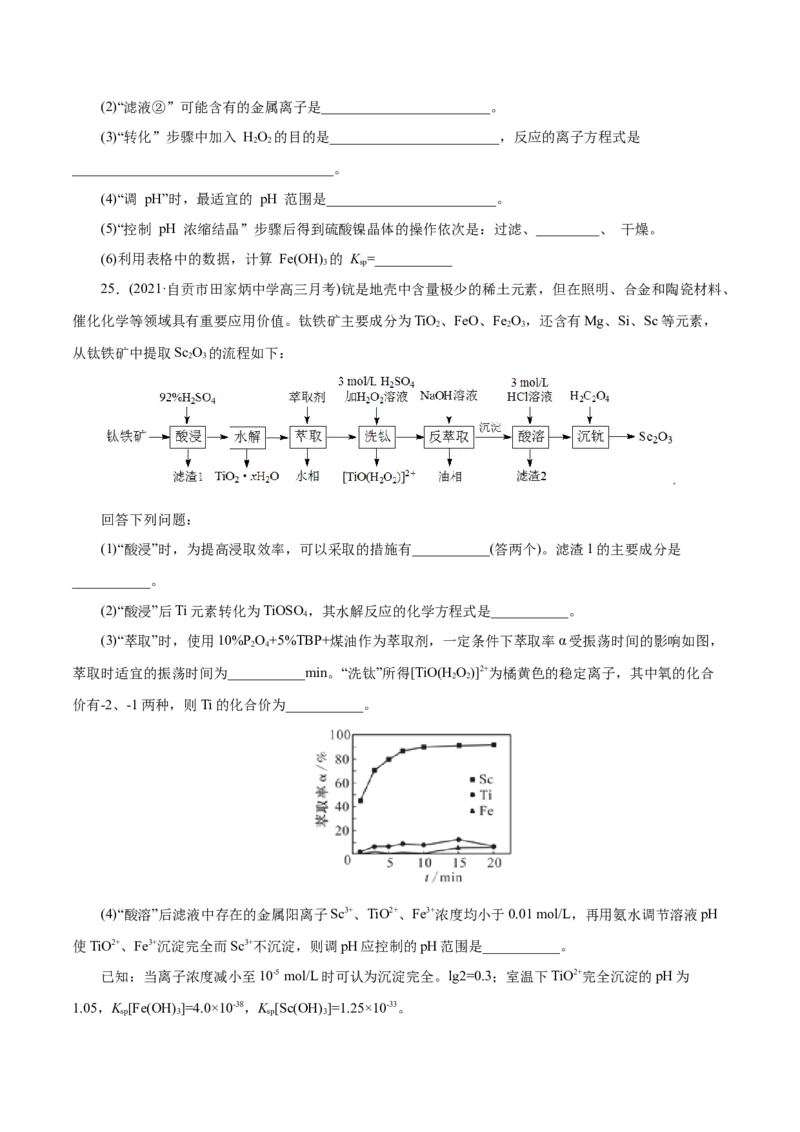
24.(2021·湖北十堰市期末)镍催化剂的主要成分为 Ni,还含有一定量 Al、Fe 及氧化铁、少量其他
不溶性物质,回收废镍催化剂制备硫酸镍晶体(NiSO ·7HO)的工艺流程如下:
4 2
溶液中金属离子开始沉淀和完全沉淀的 pH 如下表所示:
金属离子 Fe3+ Fe2+ Ni2+
开始沉淀的pH(c=0.01mol·L-1) 2.2 7.5 7.2
沉淀完全的pH(c=1.0×10-5mol·L-1) 3.2 9.0 8.7
回答下列问题:
(1)“碱浸”时发生反应的离子方程式是___________。提高“碱浸”速率的措施是
_____________________________________ (任写一点即可)。(2)“滤液②”可能含有的金属离子是________________________。
(3)“转化”步骤中加入 HO 的目的是________________________,反应的离子方程式是
2 2
_____________________________________。
(4)“调 pH”时,最适宜的 pH 范围是________________________。
(5)“控制 pH 浓缩结晶”步骤后得到硫酸镍晶体的操作依次是:过滤、_________、 干燥。
(6)利用表格中的数据,计算 Fe(OH) 的 K =___________
3 sp
25.(2021·自贡市田家炳中学高三月考)钪是地壳中含量极少的稀土元素,但在照明、合金和陶瓷材料、
催化化学等领域具有重要应用价值。钛铁矿主要成分为TiO、FeO、Fe O,还含有Mg、Si、Sc等元素,
2 2 3
从钛铁矿中提取Sc O 的流程如下:
2 3
回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有___________(答两个)。滤渣1的主要成分是
___________。
(2)“酸浸”后Ti元素转化为TiOSO ,其水解反应的化学方程式是___________。
4
(3)“萃取”时,使用10%P O+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,
2 4
萃取时适宜的振荡时间为___________min。“洗钛”所得[TiO(H O)]2+为橘黄色的稳定离子,其中氧的化合
2 2
价有-2、-1两种,则Ti的化合价为___________。
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH
使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是___________。
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为
1.05,K [Fe(OH) ]=4.0×10-38,K [Sc(OH) ]=1.25×10-33。
sp 3 sp 3(5)加草酸“沉钪”的离子方程式为___________。
(6)“沉钪”后获得Sc O 的方法是___________,该反应产生的气体必须回收利用,其意义是
2 3
_____________________________________。
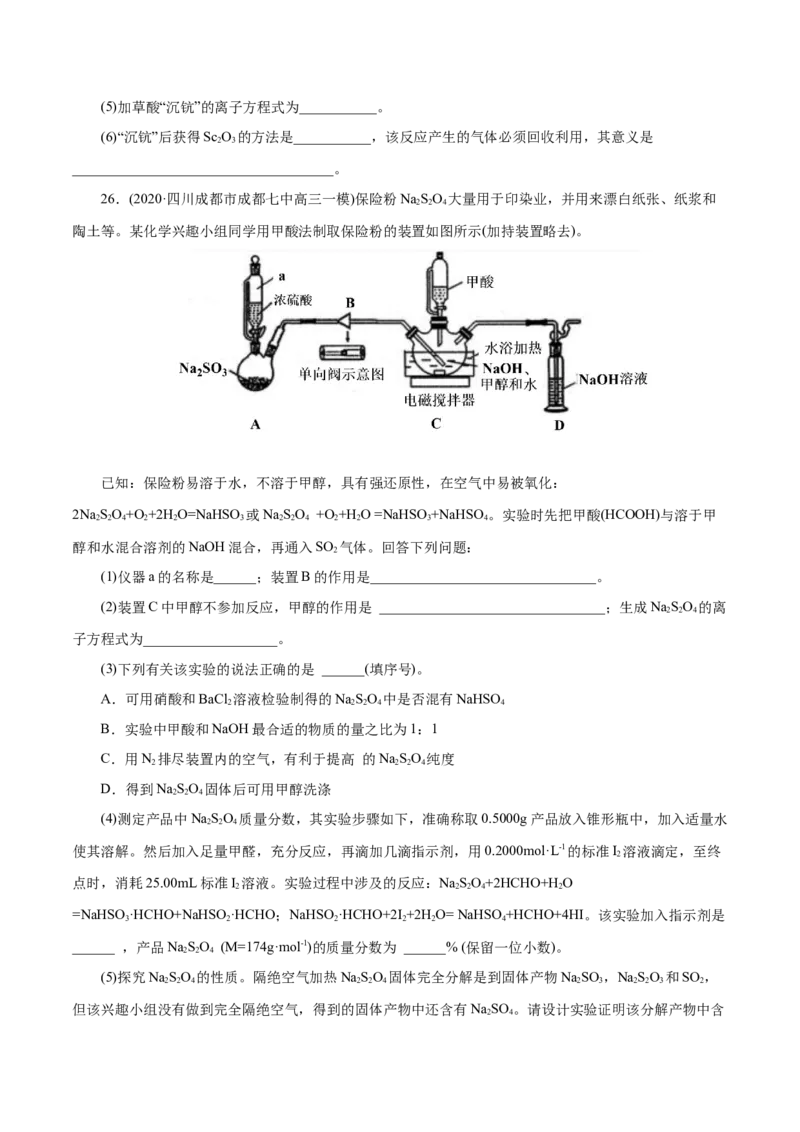
26.(2020·四川成都市成都七中高三一模)保险粉NaSO 大量用于印染业,并用来漂白纸张、纸浆和
2 2 4
陶土等。某化学兴趣小组同学用甲酸法制取保险粉的装置如图所示(加持装置略去)。
已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:
2NaSO+O +2H O=NaHSO 或NaSO +O +H O =NaHSO +NaHSO 。实验时先把甲酸(HCOOH)与溶于甲
2 2 4 2 2 3 2 2 4 2 2 3 4
醇和水混合溶剂的NaOH混合,再通入SO 气体。回答下列问题:
2
(1)仪器a的名称是______;装置B的作用是________________________________。
(2)装置C中甲醇不参加反应,甲醇的作用是 ________________________________;生成NaSO 的离
2 2 4
子方程式为___________________。
(3)下列有关该实验的说法正确的是 ______(填序号)。
A.可用硝酸和BaCl 溶液检验制得的NaSO 中是否混有NaHSO
2 2 2 4 4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N 排尽装置内的空气,有利于提高 的NaSO 纯度
2 2 2 4
D.得到NaSO 固体后可用甲醇洗涤
2 2 4
(4)测定产品中NaSO 质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水
2 2 4
使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I 溶液滴定,至终
2
点时,消耗25.00mL标准I 溶液。实验过程中涉及的反应:NaSO+2HCHO+H O
2 2 2 4 2
=NaHSO ·HCHO+NaHSO ·HCHO;NaHSO·HCHO+2I +2H O= NaHSO +HCHO+4HI。该实验加入指示剂是
3 2 2 2 2 4
______ ,产品NaSO (M=174g·mol-1)的质量分数为 ______% (保留一位小数)。
2 2 4
(5)探究NaSO 的性质。隔绝空气加热NaSO 固体完全分解是到固体产物NaSO ,NaSO 和SO ,
2 2 4 2 2 4 2 3 2 2 3 2
但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有NaSO 。请设计实验证明该分解产物中含
2 4有NaSO 。实验方案是__________________________。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl 溶液、
2 4 2
KMnO 溶液)
4