文档内容
解密 09 化学反应速率与平衡
一、选择题
1.(2021·湖南株洲市高三一模)下列有关说法中,正确的是( )
A.在 KMnO 酸性溶液做电解质的原电池中,MnO -一定向负极移动
4 4
B.常温常压下能发生自发反应的两种物质,在常温常压下一定不能大量共存
C.燃烧反应一定有电子的转移,并一定伴随着能量的放出
D.其他条件不变时,向平衡体系 mA(g)+nB(g)=pC(g)中加入一定量的A,A的转化率一定减小
2.(2021·雷州市第二中学质检)下列关于可逆反应A(?) 2B(s)+C(g) ∆H=+Q;(Q>0)的说法
正确的是 ( )
A.若反应中气体的摩尔质量保持不变,则反应一定达到平衡状态
B.平衡后,恒温下扩大容器体积,再次平衡后气体密度一定减小
C.平衡后,恒容下升高温度,再次平衡后气体C的体积分数可能减小
D.平衡后,恒温恒容下,通入气体C,C的浓度可能不变
3.(2021·广东中山市期末)某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下
反应:3A(g)+2B(g) 4C(s)+x D(g),反应2 min后达到平衡,测得生成2 mol C,且反应前后压强
之比为6∶5,则下列说法正确的是( )
A.根据题意计算可得
B.用A表示的反应速率是0.75 mol˙L-1˙min-1
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.若起始时A、B的物质的量之比为3∶2,则2 min末A、B的转化率相等
4(2021·福建高三零模)KCr O 溶液中存在平衡:Cr O2-+H O 2CrO2-+2H+。分别在26.3℃,
2 2 7 2 7 2 4
50.0℃恒温条件下,往100mL0.100 mol·L-1的KCr O 溶液中加入一定量KCr O 固体,持续搅拌下pH传感
2 2 7 2 2 7
器连续测量溶液的pH,得到如下实验图像,下列说法正确的是( )
A.曲线①是50.0℃的pH-t曲线
B.曲线②对应的平衡常数的数量级是10-14
C.t 后,c(CrO2-)+ c(CrO 2-)=c(K+)
1 2 7 4
D.26.3℃,与0.100mol·L-1的KCr O 溶液相比,达到新平衡时c2(CrO 2-)/c(CrO2-)增大
2 2 7 4 2 7
5.(2021·广东广州市期末)某课题组利用碳氨液[(NH )CO、NH ·H O)]从辉铜矿石(主要成分
4 2 3 3 2
Cu S)中直接浸取铜并制取铜盐,其过程如下图所示。
2其反应机理如下:
①CuS(s) 2Cu+(aq)+ S2-(aq)(快反应)
2
②4Cu++O +2H O=4Cu2++OH-(慢反应)
2 2
③Cu2++4NH·H O = Cu(NH )2++4H O (快反应)
3 2 3 4 2
下列说法正确的是
A.通入热的空气可以加快铜的浸出率,温度越高,浸出率越大
B.浸出装置发生的反应中,热空气的作用是氧化剂,Cu(NH )2+是还原产物
3 4
C.在浸出装置中加入适量的(NH )SO,使平衡①、②正向移动,铜的浸出率增大
4 2 2 8
D.提高铜的浸出率的关键因素是提高反应②的速率,原因是反应②的活化能比反应①、③的小
6.(2021·山西运城市期末)利用辉钼矿冶炼组的原理为M S(s)+4H(g)+2 Na CO(s) M (s)
O 2 2 2 3 O
+2CO(g)+4H O(g)+2NaS(s) ΔH。在压强为 的条件下,测得达到平衡时的有关气体体积分数的变
2 2
化如图中实线所示:
下列判断正确的是( )
A.通过图象曲线变化规律无法判断ΔH正负
B.a为CO变化曲线,b为水蒸气变化曲线
C.压强为0.5MPa时,虚线Ⅱ可能为H 的变化曲线
2
D.M点H 的转化率为75%
2
7.(2021·河北石家庄二中期末)80℃时,NO (g)+SO (g) SO (g)+NO(g)。该温度下,在甲、乙、
2 2 3
丙三个恒容密闭容器中,投入NO 和SO ,起始浓度如下表所示,其中甲经2min达平衡时,NO 的转化率
2 2 2
为50%,下列判断不正确的是( )
起始浓度 甲 乙 丙
c(NO )/mol ·L-1 0.10 0.20 0.20
2
c(SO )/mol ·L-1 0.10 0.10 0.20
2
A.平衡时,乙中SO 的转化率大于50%
2
B.当反应平衡时,丙中c(SO )是甲中的2倍
2
C.温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应D.其他条件不变,若起始时向容器乙中充入0.10mol ·L-1 NO 和0.20 mol ·L-1 SO ,达到平衡时
2 2
c(NO)与原平衡不同
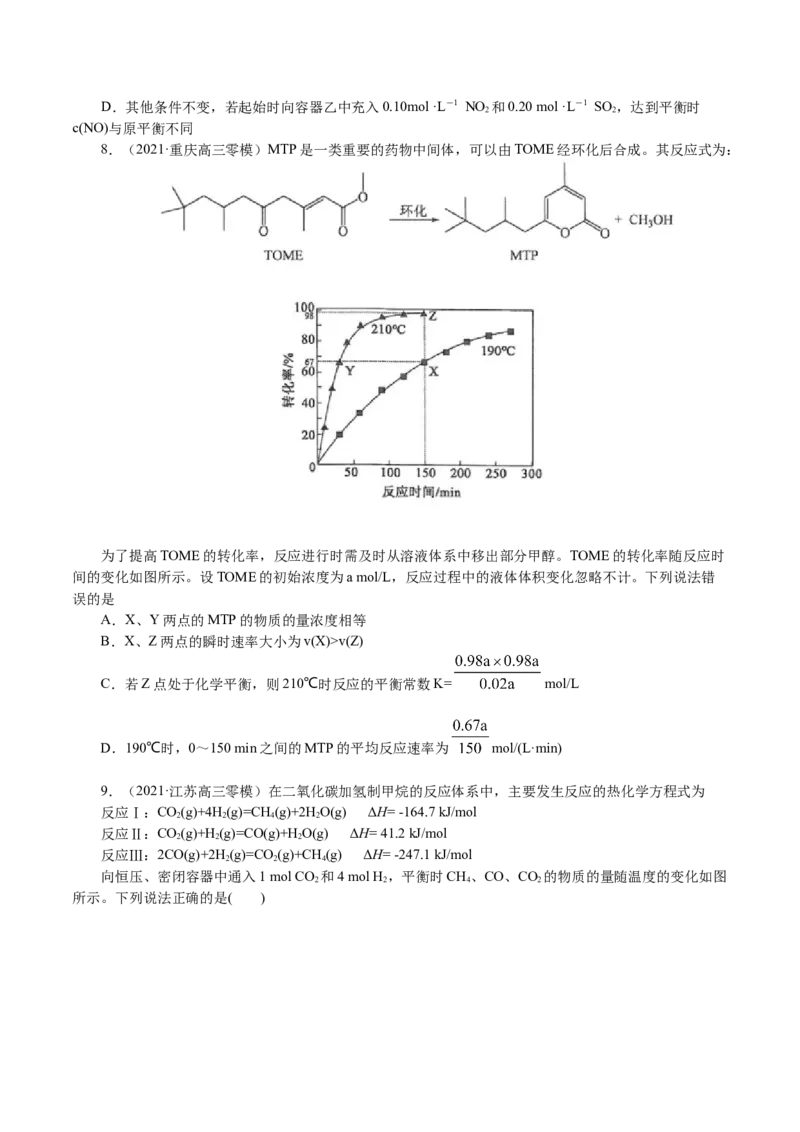
8.(2021·重庆高三零模)MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为:
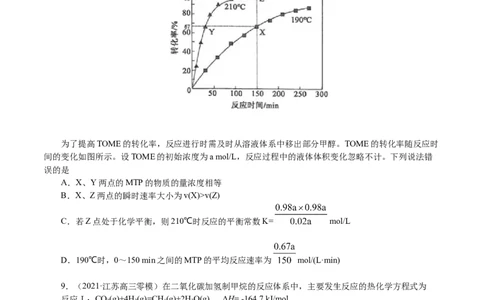
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时
间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计。下列说法错
误的是
A.X、Y两点的MTP的物质的量浓度相等
B.X、Z两点的瞬时速率大小为v(X)>v(Z)
C.若Z点处于化学平衡,则210℃时反应的平衡常数K= mol/L
D.190℃时,0~150 min之间的MTP的平均反应速率为 mol/(L·min)
9.(2021·江苏高三零模)在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:CO(g)+4H(g)=CH (g)+2HO(g) ΔH= -164.7 kJ/mol
2 2 4 2
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ΔH= 41.2 kJ/mol
2 2 2
反应Ⅲ:2CO(g)+2H(g)=CO (g)+CH (g) ΔH= -247.1 kJ/mol
2 2 4
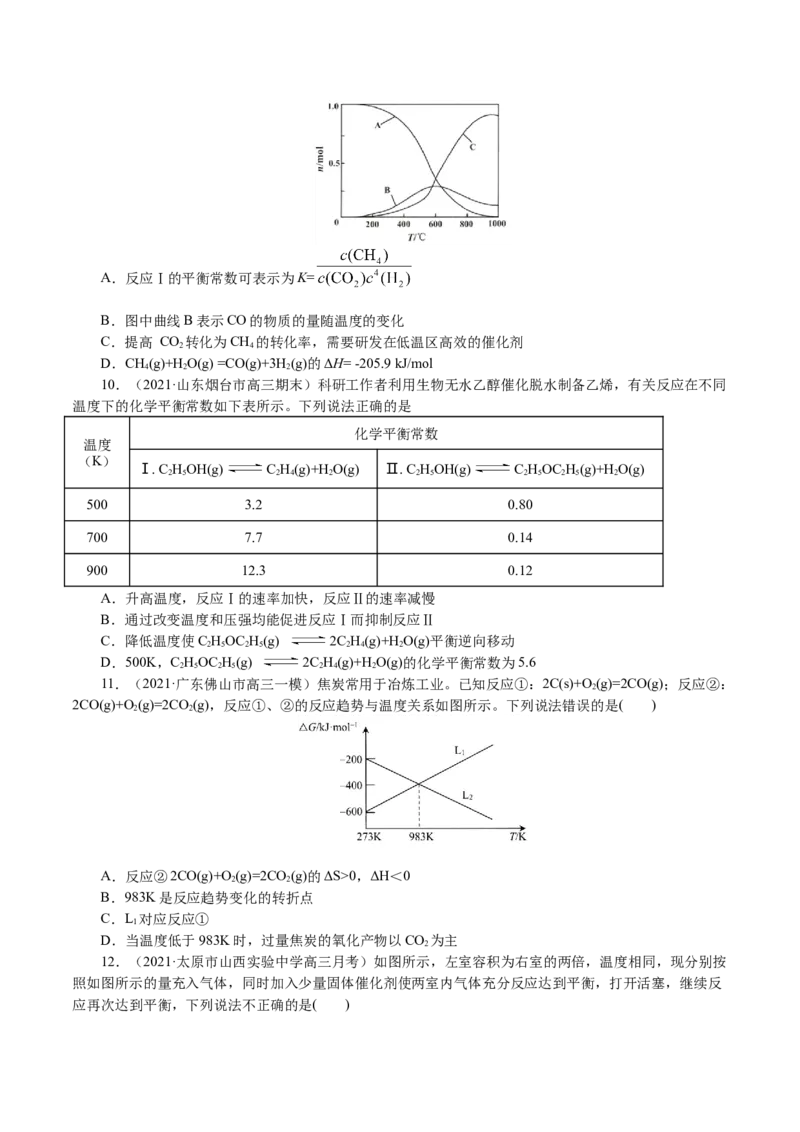
向恒压、密闭容器中通入1 mol CO 和4 mol H ,平衡时CH、CO、CO 的物质的量随温度的变化如图
2 2 4 2
所示。下列说法正确的是( )A.反应Ⅰ的平衡常数可表示为K=
B.图中曲线B表示CO的物质的量随温度的变化
C.提高 CO 转化为CH 的转化率,需要研发在低温区高效的催化剂
2 4
D.CH(g)+HO(g) =CO(g)+3H (g)的ΔH= -205.9 kJ/mol
4 2 2
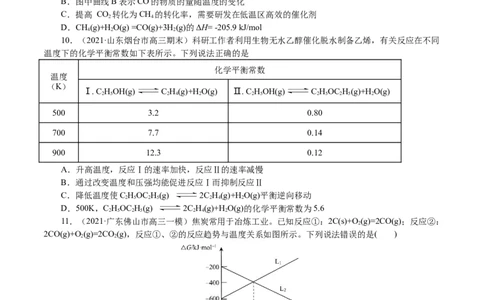
10.(2021·山东烟台市高三期末)科研工作者利用生物无水乙醇催化脱水制备乙烯,有关反应在不同
温度下的化学平衡常数如下表所示。下列说法正确的是
化学平衡常数
温度
(K)
Ⅰ. C HOH(g) C H(g)+HO(g) Ⅱ. C HOH(g) C HOC H(g)+HO(g)
2 5 2 4 2 2 5 2 5 2 5 2
500 3.2 0.80
700 7.7 0.14
900 12.3 0.12
A.升高温度,反应Ⅰ的速率加快,反应Ⅱ的速率减慢
B.通过改变温度和压强均能促进反应Ⅰ而抑制反应Ⅱ
C.降低温度使C HOC H(g) 2C H(g)+HO(g)平衡逆向移动
2 5 2 5 2 4 2
D.500K,C HOC H(g) 2C H(g)+HO(g)的化学平衡常数为5.6
2 5 2 5 2 4 2
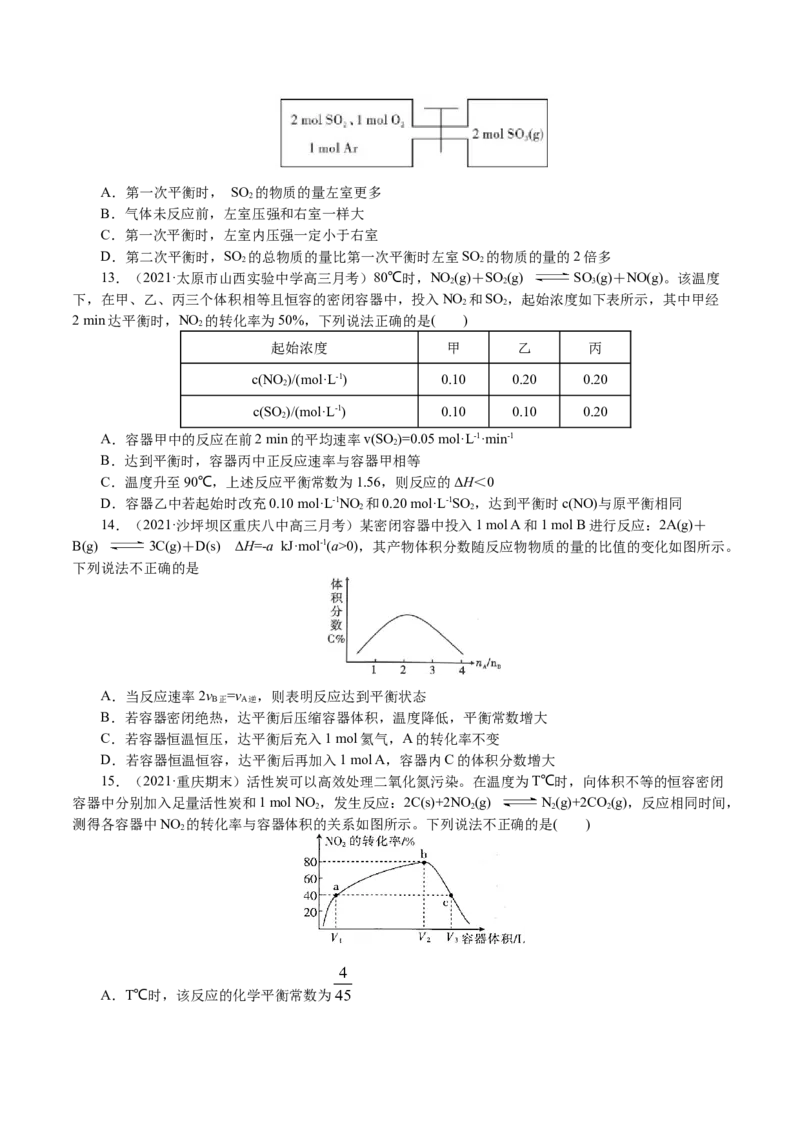
11.(2021·广东佛山市高三一模)焦炭常用于冶炼工业。已知反应①:2C(s)+O(g)=2CO(g);反应②:
2
2CO(g)+O(g)=2CO (g),反应①、②的反应趋势与温度关系如图所示。下列说法错误的是( )
2 2
A.反应②2CO(g)+O(g)=2CO (g)的ΔS>0,ΔH<0
2 2
B.983K是反应趋势变化的转折点
C.L 对应反应①
1
D.当温度低于983K时,过量焦炭的氧化产物以CO 为主
2
12.(2021·太原市山西实验中学高三月考)如图所示,左室容积为右室的两倍,温度相同,现分别按
照如图所示的量充入气体,同时加入少量固体催化剂使两室内气体充分反应达到平衡,打开活塞,继续反
应再次达到平衡,下列说法不正确的是( )A.第一次平衡时, SO 的物质的量左室更多
2
B.气体未反应前,左室压强和右室一样大
C.第一次平衡时,左室内压强一定小于右室
D.第二次平衡时,SO 的总物质的量比第一次平衡时左室SO 的物质的量的2倍多
2 2
13.(2021·太原市山西实验中学高三月考)80℃时,NO (g)+SO (g) SO (g)+NO(g)。该温度
2 2 3
下,在甲、乙、丙三个体积相等且恒容的密闭容器中,投入NO 和SO ,起始浓度如下表所示,其中甲经
2 2
2 min达平衡时,NO 的转化率为50%,下列说法正确的是( )
2
起始浓度 甲 乙 丙
c(NO )/(mol·L-1) 0.10 0.20 0.20
2
c(SO )/(mol·L-1) 0.10 0.10 0.20
2
A.容器甲中的反应在前2 min的平均速率v(SO )=0.05 mol·L-1·min-1
2
B.达到平衡时,容器丙中正反应速率与容器甲相等
C.温度升至90℃,上述反应平衡常数为1.56,则反应的ΔH<0
D.容器乙中若起始时改充0.10 mol·L-1NO 和0.20 mol·L-1SO ,达到平衡时c(NO)与原平衡相同
2 2
14.(2021·沙坪坝区重庆八中高三月考)某密闭容器中投入1 mol A和1 mol B进行反应:2A(g)+
B(g) 3C(g)+D(s) ΔH=-a kJ·mol-1(a>0),其产物体积分数随反应物物质的量的比值的变化如图所示。
下列说法不正确的是
A.当反应速率2v =v ,则表明反应达到平衡状态
B正 A逆
B.若容器密闭绝热,达平衡后压缩容器体积,温度降低,平衡常数增大
C.若容器恒温恒压,达平衡后充入1 mol氦气,A的转化率不变
D.若容器恒温恒容,达平衡后再加入1 mol A,容器内C的体积分数增大
15.(2021·重庆期末)活性炭可以高效处理二氧化氮污染。在温度为T℃时,向体积不等的恒容密闭
容器中分别加入足量活性炭和1 mol NO ,发生反应:2C(s)+2NO (g) N(g)+2CO (g),反应相同时间,
2 2 2 2
测得各容器中NO 的转化率与容器体积的关系如图所示。下列说法不正确的是( )
2
A.T℃时,该反应的化学平衡常数为B.图中c点所示条件下:v(正)>v(逆)
C.图中a、c点对应的CO 浓度:c(CO)>c(CO)
2 a 2 c 2
D.容器内的压强:p︰p>6︰7
a b
16.(2020·海伦市第一中学高三月考)在某温度下,向三个初始体积均为 的密闭容器中按下表所
示投料,发生反应:2SO (g)+O(g) 2SO (g) ΔH<0。下列说法不正确的是( )
2 2 3
起始物质的量/
容器编
容器类型 平衡时SO 的物质的量/
号 3
SO O SO
2 2 3
Ⅰ 恒温恒容 2 1 0 1.8
Ⅱ 绝热恒容 0 0 2 a
Ⅲ 恒温恒压 2 1 0 b
A.容器Ⅰ中SO 转化率小于容器Ⅲ中SO 的转化率
2 2
B.容器Ⅲ平衡体系中保持容器压强不变,充入0.10mol SO (g),新平衡后SO 浓度未变
3 3
C.平衡时SO 的物质的量:a>1.8、b<1.8
3
D.若容器Ⅰ中有0.10mol SO (g)、0.20molSO (g)和0.10mol SO (g),则此时
2 2 3
17.(2020·河南开封市质检)已知反应H(g)+I (g) 2HI(g) H<0。温度T时,在两个体积均
2 2
为1 L的恒容密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如
△
表:
容器编号 起始物质 t/min 0 20 40 60 80 100
Ⅰ 0.5 mol I 、0.5 mol H ω(HI)/% 0 50 68 76 80 80
2 2
Ⅱ x mol HI ω(HI)/% 100 91 84 81 80 80
上述反应中v =k·w(H )·w(I),v =k·w2(HI),其中k、k 为常数。下列说法正确的是( )
正 a 2 2 逆 b a b
A.温度为T时,该反应的 =64
B.容器Ⅰ中,前20 min的平均速率v(HI)=0.05 mol·L-1·min -1
C.若起始时,向容器Ⅰ中加入物质的量均为0.1 mol的H、I 和HI,反应逆向进行
2 2
D.x的值一定为1
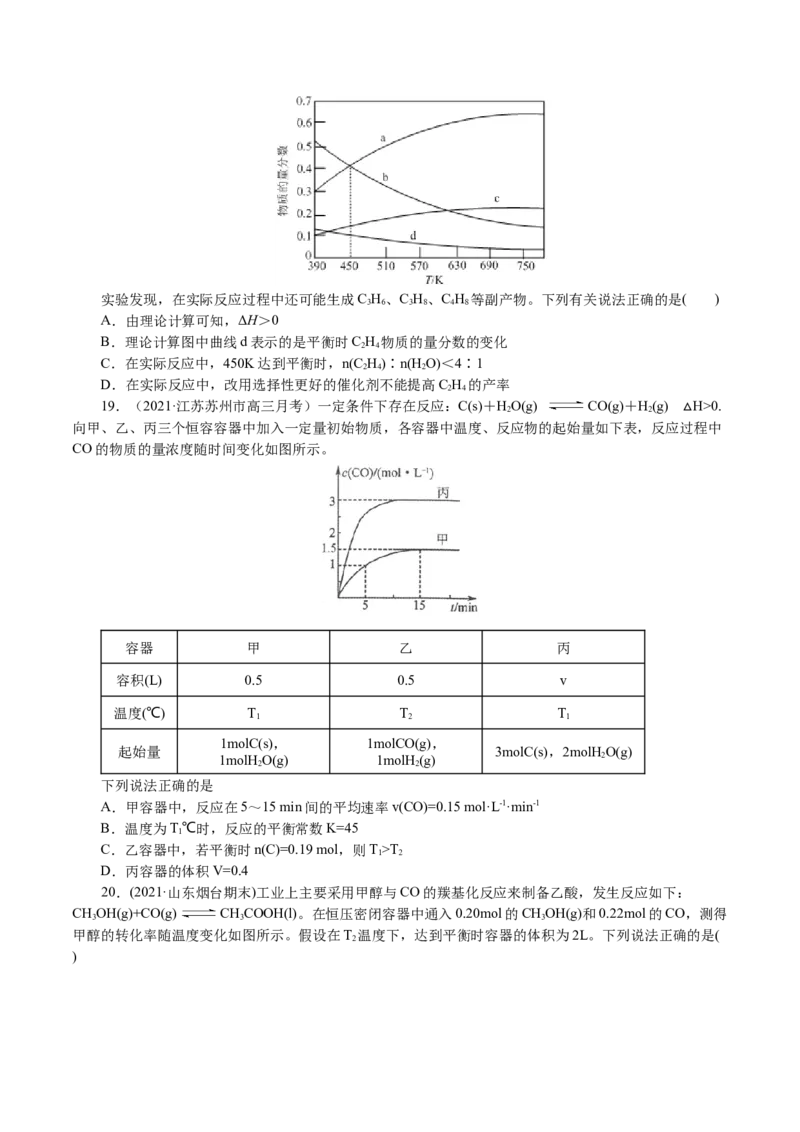
18.(2021·江苏扬州市高三期末)已知反应2CO(g)+6H(g) C H(g)+4HO(g)ΔH。根据理论计
2 2 2 4 2
算,在恒压、起始物质的量之比n(CO)∶n(H )=1∶3条件下,该反应达平衡时各组分的物质的量分数随温
2 2
度变化的曲线如图所示。实验发现,在实际反应过程中还可能生成C H、C H、C H 等副产物。下列有关说法正确的是( )
3 6 3 8 4 8
A.由理论计算可知,ΔH>0
B.理论计算图中曲线d表示的是平衡时C H 物质的量分数的变化
2 4
C.在实际反应中,450K达到平衡时,n(C H)∶n(H O)<4∶1
2 4 2
D.在实际反应中,改用选择性更好的催化剂不能提高C H 的产率
2 4
19.(2021·江苏苏州市高三月考)一定条件下存在反应:C(s)+HO(g) CO(g)+H(g) H>0.
2 2
向甲、乙、丙三个恒容容器中加入一定量初始物质,各容器中温度、反应物的起始量如下表,反应过程中
△
CO的物质的量浓度随时间变化如图所示。
容器 甲 乙 丙
容积(L) 0.5 0.5 v
温度(℃) T T T
1 2 1
1molC(s), 1molCO(g),
起始量 3molC(s),2molH O(g)
1molH O(g) 1molH (g) 2
2 2
下列说法正确的是
A.甲容器中,反应在5~15 min间的平均速率v(CO)=0.15 mol·L-1·min-1
B.温度为T℃时,反应的平衡常数K=45
1
C.乙容器中,若平衡时n(C)=0.19 mol,则T>T
1 2
D.丙容器的体积V=0.4
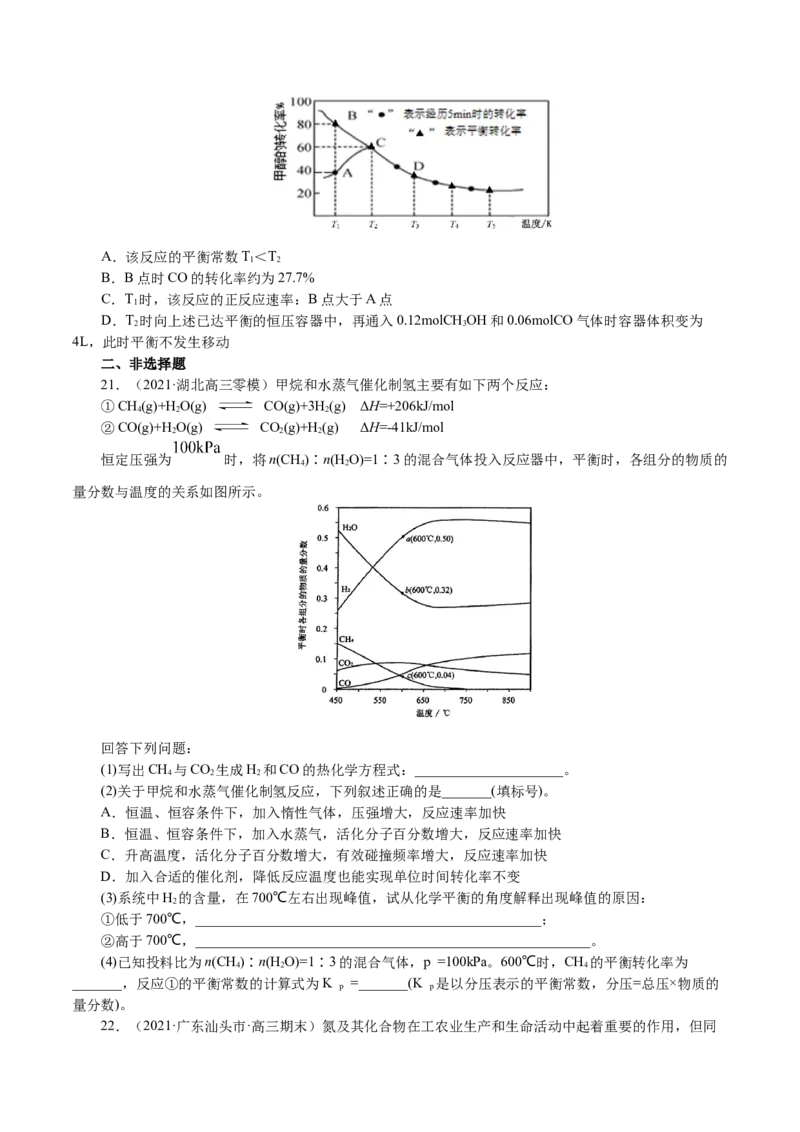
20.(2021·山东烟台期末)工业上主要采用甲醇与CO的羰基化反应来制备乙酸,发生反应如下:
CHOH(g)+CO(g) CHCOOH(l)。在恒压密闭容器中通入0.20mol的CHOH(g)和0.22mol的CO,测得
3 3 3
甲醇的转化率随温度变化如图所示。假设在T 温度下,达到平衡时容器的体积为2L。下列说法正确的是(
2
)A.该反应的平衡常数T<T
1 2
B.B点时CO的转化率约为27.7%
C.T 时,该反应的正反应速率:B点大于A点
1
D.T 时向上述已达平衡的恒压容器中,再通入0.12molCHOH和0.06molCO气体时容器体积变为
2 3
4L,此时平衡不发生移动
二、非选择题
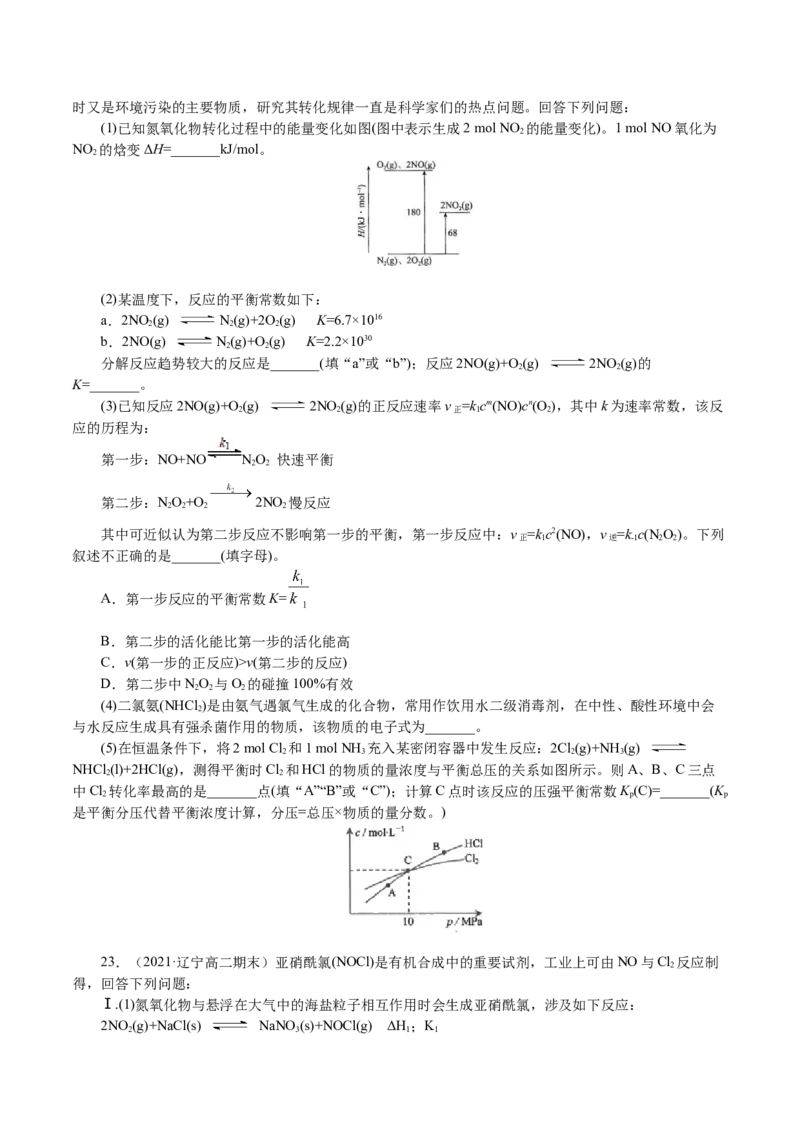
21.(2021·湖北高三零模)甲烷和水蒸气催化制氢主要有如下两个反应:
①CH(g)+HO(g) CO(g)+3H (g) ΔH=+206kJ/mol
4 2 2
②CO(g)+HO(g) CO(g)+H(g) ΔH=-41kJ/mol
2 2 2
恒定压强为 时,将n(CH)∶n(H O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的
4 2
量分数与温度的关系如图所示。
回答下列问题:
(1)写出CH 与CO 生成H 和CO的热化学方程式:_____________________。
4 2 2
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是_______(填标号)。
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,降低反应温度也能实现单位时间转化率不变
(3)系统中H 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
2
①低于700℃,_________________________________________________;
②高于700℃,________________________________________________________。
(4)已知投料比为n(CH)∶n(H O)=1∶3的混合气体,p =100kPa。600℃时,CH 的平衡转化率为
4 2 4
_______,反应①的平衡常数的计算式为K =_______(K 是以分压表示的平衡常数,分压=总压×物质的
p p
量分数)。
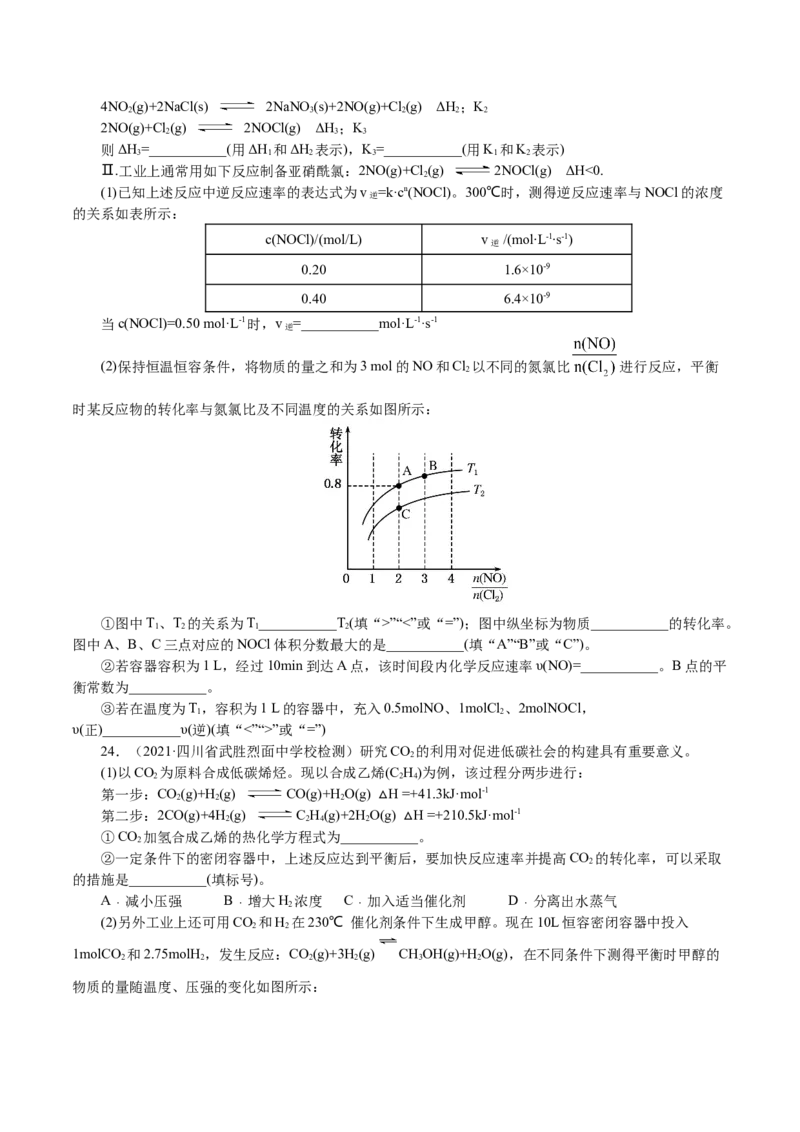
22.(2021·广东汕头市·高三期末)氮及其化合物在工农业生产和生命活动中起着重要的作用,但同时又是环境污染的主要物质,研究其转化规律一直是科学家们的热点问题。回答下列问题:
(1)已知氮氧化物转化过程中的能量变化如图(图中表示生成2 mol NO 的能量变化)。1 mol NO氧化为
2
NO 的焓变ΔH=_______kJ/mol。
2
(2)某温度下,反应的平衡常数如下:
a.2NO (g) N(g)+2O(g) K=6.7×1016
2 2 2
b.2NO(g) N(g)+O(g) K=2.2×1030
2 2
分解反应趋势较大的反应是_______(填“a”或“b”);反应2NO(g)+O (g) 2NO (g)的
2 2
K=_______。
(3)已知反应2NO(g)+O (g) 2NO (g)的正反应速率v =kcm(NO)cn(O ),其中k为速率常数,该反
2 2 正 1 2
应的历程为:
第一步:NO+NO NO 快速平衡
2 2
第二步:NO+O 2NO 慢反应
2 2 2 2
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v =kc2(NO),ν =k c(N O)。下列
正 1 逆 -1 2 2
叙述不正确的是_______(填字母)。
A.第一步反应的平衡常数K=
B.第二步的活化能比第一步的活化能高
C.v(第一步的正反应)>v(第二步的反应)
D.第二步中NO 与O 的碰撞100%有效
2 2 2
(4)二氯氨(NHCl )是由氨气遇氯气生成的化合物,常用作饮用水二级消毒剂,在中性、酸性环境中会
2
与水反应生成具有强杀菌作用的物质,该物质的电子式为_______。
(5)在恒温条件下,将2 mol Cl 和1 mol NH 充入某密闭容器中发生反应:2Cl(g)+NH (g)
2 3 2 3
NHCl (l)+2HCl(g),测得平衡时Cl 和HCl的物质的量浓度与平衡总压的关系如图所示。则A、B、C三点
2 2
中Cl 转化率最高的是_______点(填“A”“B”或“C”);计算C点时该反应的压强平衡常数K (C)=_______(K
2 p p
是平衡分压代替平衡浓度计算,分压=总压×物质的量分数。)
23.(2021·辽宁高二期末)亚硝酰氯(NOCl)是有机合成中的重要试剂,工业上可由NO与Cl 反应制
2
得,回答下列问题:
Ⅰ.(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
2NO (g)+NaCl(s) NaNO (s)+NOCl(g) ΔH;K
2 3 1 14NO (g)+2NaCl(s) 2NaNO (s)+2NO(g)+Cl (g) ΔH;K
2 3 2 2 2
2NO(g)+Cl (g) 2NOCl(g) ΔH;K
2 3 3
则ΔH=___________(用ΔH 和ΔH 表示),K=___________(用K 和K 表示)
3 1 2 3 1 2
Ⅱ.工业上通常用如下反应制备亚硝酰氯:2NO(g)+Cl (g) 2NOCl(g) ΔH<0.
2
(1)已知上述反应中逆反应速率的表达式为v =k·cn(NOCl)。300℃时,测得逆反应速率与NOCl的浓度
逆
的关系如表所示:
c(NOCl)/(mol/L) v /(mol∙L-1∙s-1)
逆
0.20 1.6×10-9
0.40 6.4×10-9
当c(NOCl)=0.50 mol·L-1时,v =___________mol·L-1·s-1
逆
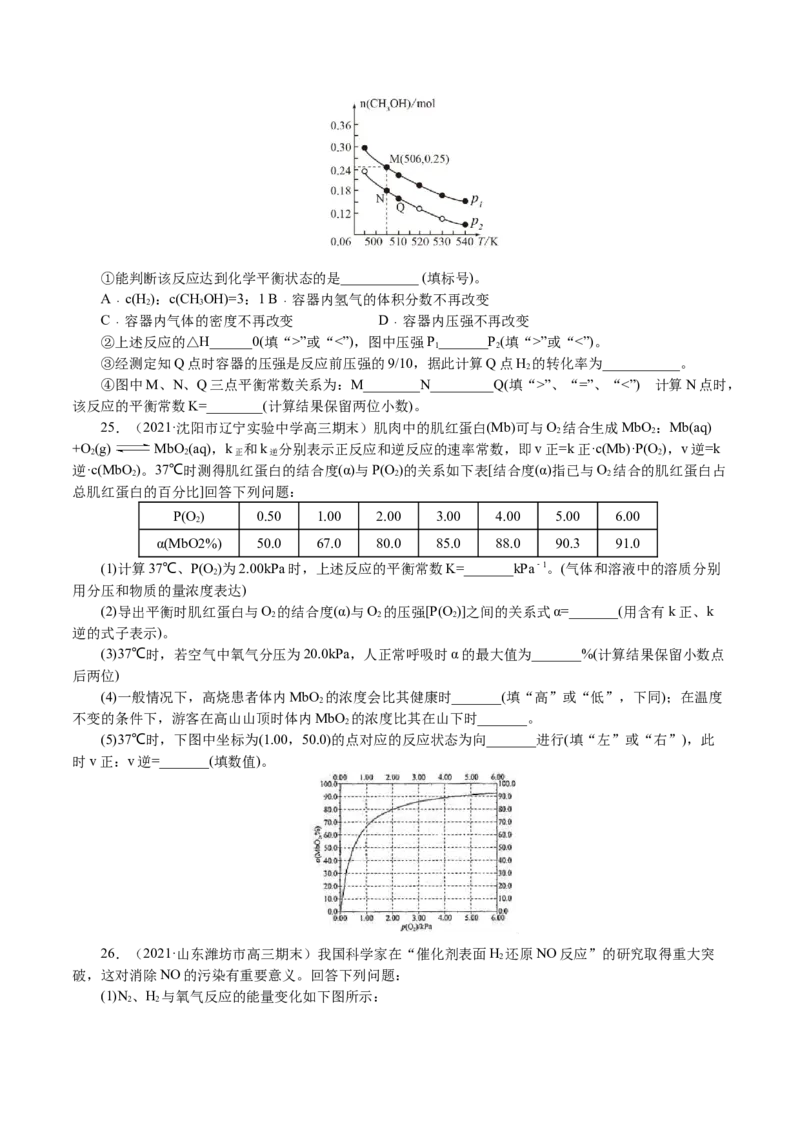
(2)保持恒温恒容条件,将物质的量之和为3 mol的NO和Cl 以不同的氮氯比 进行反应,平衡
2
时某反应物的转化率与氮氯比及不同温度的关系如图所示:
①图中T、T 的关系为T___________T(填“>”“<”或“=”);图中纵坐标为物质___________的转化率。
1 2 1 2
图中A、B、C三点对应的NOCl体积分数最大的是___________(填“A”“B”或“C”)。
②若容器容积为1 L,经过10min到达A点,该时间段内化学反应速率υ(NO)=___________。B点的平
衡常数为___________。
③若在温度为T,容积为1 L的容器中,充入0.5molNO、1molCl 、2molNOCl,
1 2
υ(正)___________υ(逆)(填“<”“>”或“=”)
24.(2021·四川省武胜烈面中学校检测)研究CO 的利用对促进低碳社会的构建具有重要意义。
2
(1)以CO 为原料合成低碳烯烃。现以合成乙烯(C H)为例,该过程分两步进行:
2 2 4
第一步:CO(g)+H(g) CO(g)+HO(g) H =+41.3kJ·mol-1
2 2 2
第二步:2CO(g)+4H(g) C H(g)+2HO(g) H =+210.5kJ·mol-1
2 2 4 2
△
①CO 加氢合成乙烯的热化学方程式为___________。
2
△
②一定条件下的密闭容器中,上述反应达到平衡后,要加快反应速率并提高CO 的转化率,可以采取
2
的措施是___________(填标号)。
A﹒减小压强 B﹒增大H 浓度 C﹒加入适当催化剂 D﹒分离出水蒸气
2
(2)另外工业上还可用CO 和H 在230℃ 催化剂条件下生成甲醇。现在10L恒容密闭容器中投入
2 2
1molCO 和2.75molH,发生反应:CO(g)+3H(g) CHOH(g)+H O(g),在不同条件下测得平衡时甲醇的
2 2 2 2 3 2
物质的量随温度、压强的变化如图所示:①能判断该反应达到化学平衡状态的是___________ (填标号)。
A﹒c(H ):c(CHOH)=3:1 B﹒容器内氢气的体积分数不再改变
2 3
C﹒容器内气体的密度不再改变 D﹒容器内压强不再改变
②上述反应的△H______0(填“>”或“<”),图中压强P_______P(填“>”或“<”)。
1 2
③经测定知Q点时容器的压强是反应前压强的9/10,据此计算Q点H 的转化率为___________。
2
④图中M、N、Q三点平衡常数关系为:M________N_________Q(填“>”、“=”、“<”) 计算N点时,
该反应的平衡常数K=________(计算结果保留两位小数)。
25.(2021·沈阳市辽宁实验中学高三期末)肌肉中的肌红蛋白(Mb)可与O 结合生成MbO :Mb(aq)
2 2
+O (g) MbO (aq),k 和k 分别表示正反应和逆反应的速率常数,即v正=k正·c(Mb)·P(O ),v逆=k
2 2 正 逆 2
逆·c(MbO )。37℃时测得肌红蛋白的结合度(α)与P(O )的关系如下表[结合度(α)指已与O 结合的肌红蛋白占
2 2 2
总肌红蛋白的百分比]回答下列问题:
P(O ) 0.50 1.00 2.00 3.00 4.00 5.00 6.00
2
α(MbO2%) 50.0 67.0 80.0 85.0 88.0 90.3 91.0
(1)计算37℃、P(O )为2.00kPa时,上述反应的平衡常数K=_______kPa﹣1。(气体和溶液中的溶质分别
2
用分压和物质的量浓度表达)
(2)导出平衡时肌红蛋白与O 的结合度(α)与O 的压强[P(O )]之间的关系式α=_______(用含有k正、k
2 2 2
逆的式子表示)。
(3)37℃时,若空气中氧气分压为20.0kPa,人正常呼吸时α的最大值为_______%(计算结果保留小数点
后两位)
(4)一般情况下,高烧患者体内MbO 的浓度会比其健康时_______(填“高”或“低”,下同);在温度
2
不变的条件下,游客在高山山顶时体内MbO 的浓度比其在山下时_______。
2
(5)37℃时,下图中坐标为(1.00,50.0)的点对应的反应状态为向_______进行(填“左”或“右”),此
时v正:v逆=_______(填数值)。
26.(2021·山东潍坊市高三期末)我国科学家在“催化剂表面H 还原NO反应”的研究取得重大突
2
破,这对消除NO的污染有重要意义。回答下列问题:
(1)N 、H 与氧气反应的能量变化如下图所示:
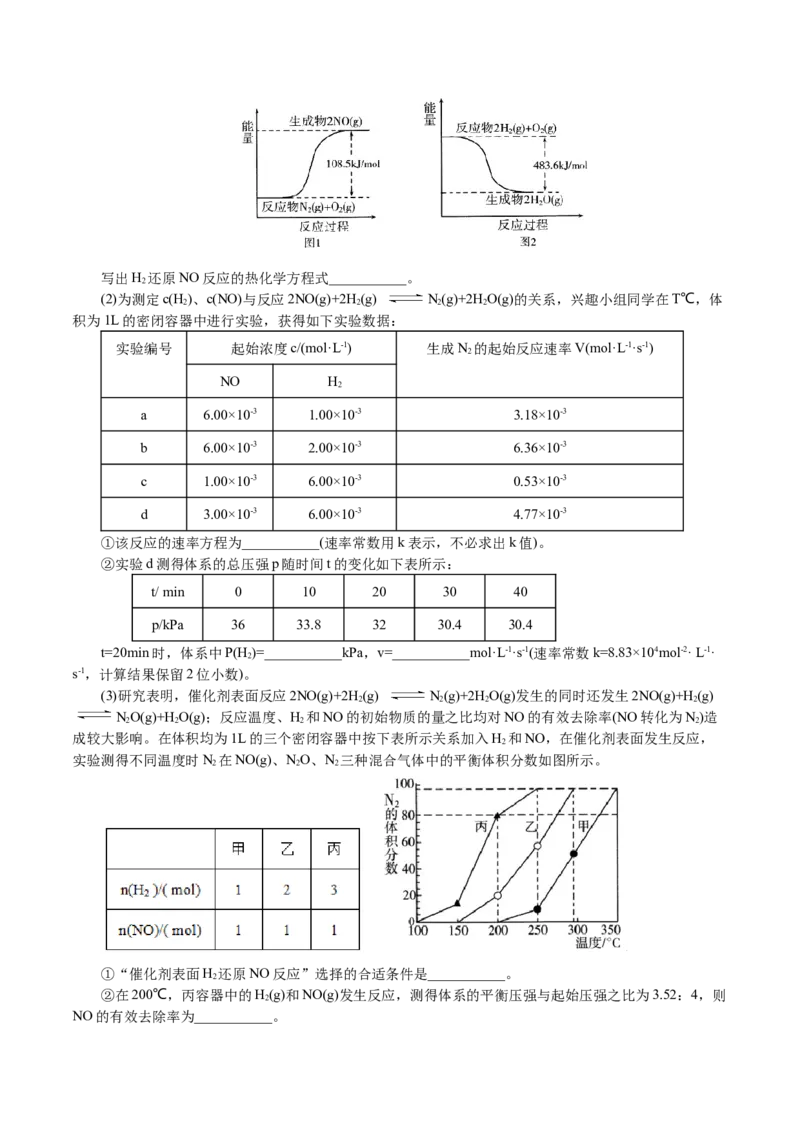
2 2写出H 还原NO反应的热化学方程式___________。
2
(2)为测定c(H)、c(NO)与反应2NO(g)+2H (g) N(g)+2HO(g)的关系,兴趣小组同学在T℃,体
2 2 2 2
积为1L的密闭容器中进行实验,获得如下实验数据:
实验编号 起始浓度c/(mol·L-1) 生成N 的起始反应速率V(mol·L-1·s-1)
2
NO H
2
a 6.00×10-3 1.00×10-3 3.18×10-3
b 6.00×10-3 2.00×10-3 6.36×10-3
c 1.00×10-3 6.00×10-3 0.53×10-3
d 3.00×10-3 6.00×10-3 4.77×10-3
①该反应的速率方程为___________(速率常数用k表示,不必求出k值)。
②实验d测得体系的总压强p随时间t的变化如下表所示:
t/ min 0 10 20 30 40
p/kPa 36 33.8 32 30.4 30.4
t=20min时,体系中P(H )=___________kPa,v=___________mol·L-1·s-1(速率常数k=8.83×104mol-2· L-1·
2
s-1,计算结果保留2位小数)。
(3)研究表明,催化剂表面反应2NO(g)+2H (g) N(g)+2HO(g)发生的同时还发生2NO(g)+H (g)
2 2 2 2
NO(g)+H O(g);反应温度、H 和NO的初始物质的量之比均对NO的有效去除率(NO转化为N)造
2 2 2 2
成较大影响。在体积均为1L的三个密闭容器中按下表所示关系加入H 和NO,在催化剂表面发生反应,
2
实验测得不同温度时N 在NO(g)、NO、N 三种混合气体中的平衡体积分数如图所示。
2 2 2
①“催化剂表面H 还原NO反应”选择的合适条件是___________。
2
②在200℃,丙容器中的H(g)和NO(g)发生反应,测得体系的平衡压强与起始压强之比为3.52:4,则
2
NO的有效去除率为___________。