文档内容
第 6 单元碳和碳的氧化物知识清单
考点1 金刚石、石墨和C
60
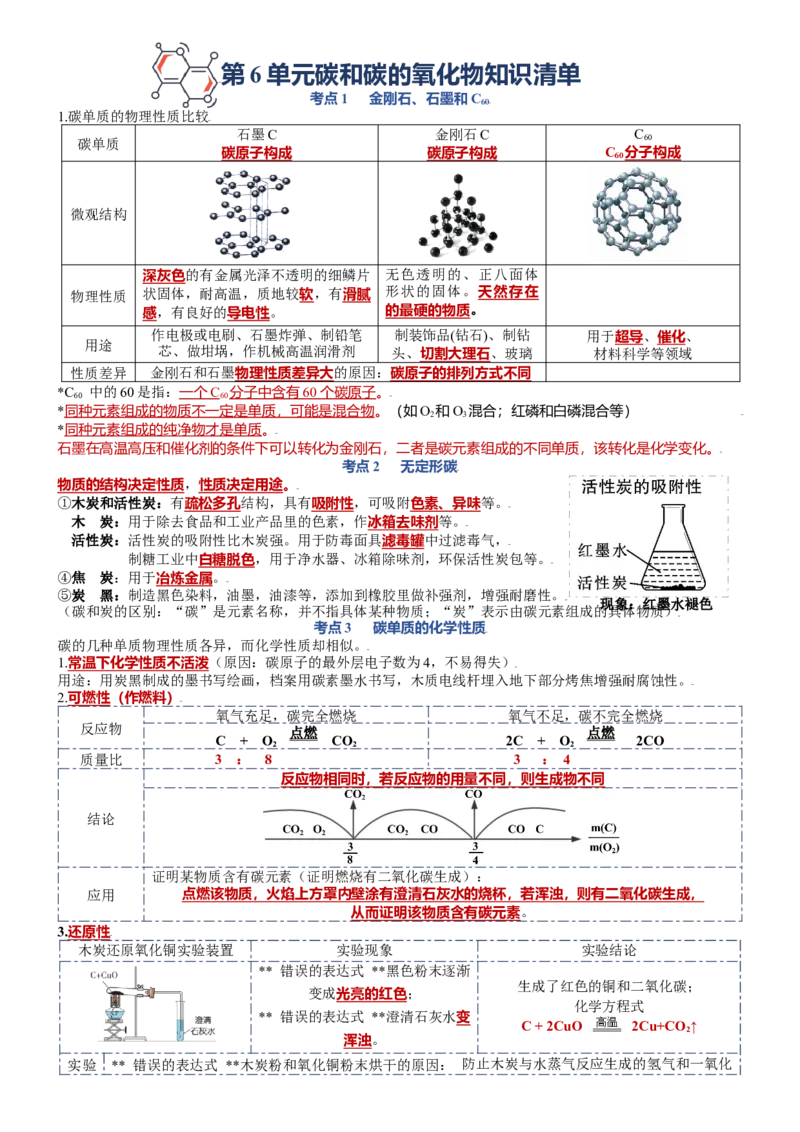
1.碳单质的物理性质比较
石墨C 金刚石C C
碳单质 60
碳原子构成 碳原子构成 C 分子构成
60
微观结构
深灰色的有金属光泽不透明的细鳞片 无色透明的、正八面体
物理性质 状固体,耐高温,质地较软,有滑腻 形状的固体。天然存在
感,有良好的导电性。 的最硬的物质。
作电极或电刷、石墨炸弹、制铅笔 制装饰品(钻石)、制钻 用于超导、催化、
用途
芯、做坩埚,作机械高温润滑剂 头、切割大理石、玻璃 材料科学等领域
性质差异 金刚石和石墨物理性质差异大的原因:碳原子的排列方式不同
*C 中的60是指: 一个 C 分子中含有 60 个碳原子 。
60 60
* 同种元素组成的物质不一定是单质,可能是混合 物 。(如O 和O 混合;红磷和白磷混合等)
2 3
*同种元素组成的纯净物才是单质。
石墨在高温高压和催化剂的条件下可以转化为金刚石,二者是碳元素组成的不同单质,该转化是化学变化。
考点2 无定形碳
物质的结构决定性质,性质决定用途。
①木炭和活性炭:有疏松多孔结构,具有吸附性,可吸附色素、异味等。
木 炭:用于除去食品和工业产品里的色素,作冰箱去味剂等。
活性炭:活性炭的吸附性比木炭强。用于防毒面具滤毒罐中过滤毒气,
制糖工业中白糖脱色,用于净水器、冰箱除味剂,环保活性炭包等。
④焦 炭:用于冶炼金属。
⑤炭 黑:制造黑色染料,油墨,油漆等,添加到橡胶里做补强剂,增强耐磨性。
现象:红墨水褪色
(碳和炭的区别:“碳”是元素名称,并不指具体某种物质;“炭”表示由碳元素组成的具体物质)
考点3 碳单质的化学性质
碳的几种单质物理性质各异,而化学性质却相似。
1. 常温下化学性质不活泼 (原因:碳原子的最外层电子数为4,不易得失)
用途:用炭黑制成的墨书写绘画,档案用碳素墨水书写,木质电线杆埋入地下部分烤焦增强耐腐蚀性。
2.可燃性(作燃料)
氧气充足,碳完全燃烧 氧气不足,碳不完全燃烧
反应物 点燃 点燃
C + O CO 2C + O 2CO
2 2 2
质量比 3 : 8 3 : 4
反应物相同时,若反应物的用量不同,则生成物不同
结论
证明某物质含有碳元素(证明燃烧有二氧化碳生成):
应用 点燃该物质,火焰上方罩内壁涂有澄清石灰水的烧杯,若浑浊,则有二氧化碳生成,
从而证明该物质含有碳元素。
3.还原性
木炭还原氧化铜实验装置 实验现象 实验结论
** 错误的表达式 **黑色粉末逐渐
生成了红色的铜和二氧化碳;
变成光亮的红色;
化学方程式
** 错误的表达式 **澄清石灰水变
C + 2CuO 2Cu+CO ↑
2
浑浊。
实验 ** 错误的表达式 **木炭粉和氧化铜粉末烘干的原因: 防止木炭与水蒸气反应生成的氢气和一氧化碳与氧化铜反应。
** 错误的表达式 **火焰加金属网罩的目的:集中火焰,提高温度。
** 错误的表达式 **实验结束后,先撤出导气管,再停止加热的目的:防止石灰水倒流炸裂热的试
分析
管。
** 错误的表达式 **待试管冷却后再把试管中的粉末倒出的原因:防止热的铜接触空气又被氧化。
⑤木炭配比比理论值稍微多一点,因为木炭会和试管中的氧气反应,
考点4 氧化还原反应
1.碳还原金属氧化物 (用于工业冶炼金属)
高温
碳 + 某些金属氧化物 金属单质 + CO ↑
2
2.氧化还反应分析
CuO 失去 氧 元素 ,有氧化性,是氧化剂,被还原,发生还原反应
C 夺取 氧 元素 ,有还原性,是还原剂,被氧化,发生氧化反应
氧化反应:物质结合氧元素的反应。 还原反应:含氧化合物里的氧被夺去的反应。
氧化剂:在反应中提供氧元素的物质,具有氧化性,如CuO;
还原剂:在反应中得到氧元素的物质,具有还原性,如C、CO、H 等;
2
3.碳与二氧化碳反应:C + CO 2CO(吸热反应)
2
4.补充:置换反应:一种单质与一种化合物反应生成另一种单质和另一种化合物的反应。
考点5 二氧化碳制取的研究
高温
1.工业制二氧化碳:煅烧石灰石:CaCO CaO+CO ↑
3 2
(石灰石、大理石主要成分为碳酸钙CaCO ;氧化钙CaO俗称生石灰;氢氧化钙Ca(OH) 俗称熟石灰)
3 2
2.实验室制二氧化碳:
(1)药品:块状石灰石(或大理石)和稀盐酸(均为混合物)
(2)反应原理:CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
①为什么不能用纯的CaCO 或NaCO 粉末?反应速率太快,不易控制。
3 2 3
②为什么不用浓盐酸?浓盐酸易挥发, 挥发出的氯化氢( HC l )气体使制得的二氧化碳不纯 。
③为什么不用稀硫酸? 生成微溶于水的 CaSO 覆盖在石灰石表面,阻碍反应的进一步进行。
4
(3)检验方法:将制得的气体通入澄清石灰水,若澄清石灰水变浑浊,则证明是二氧化碳。
(4)验满方法:用燃着的木条,放在集气瓶口,木条熄灭,证明二氧化碳气体已经收集满。
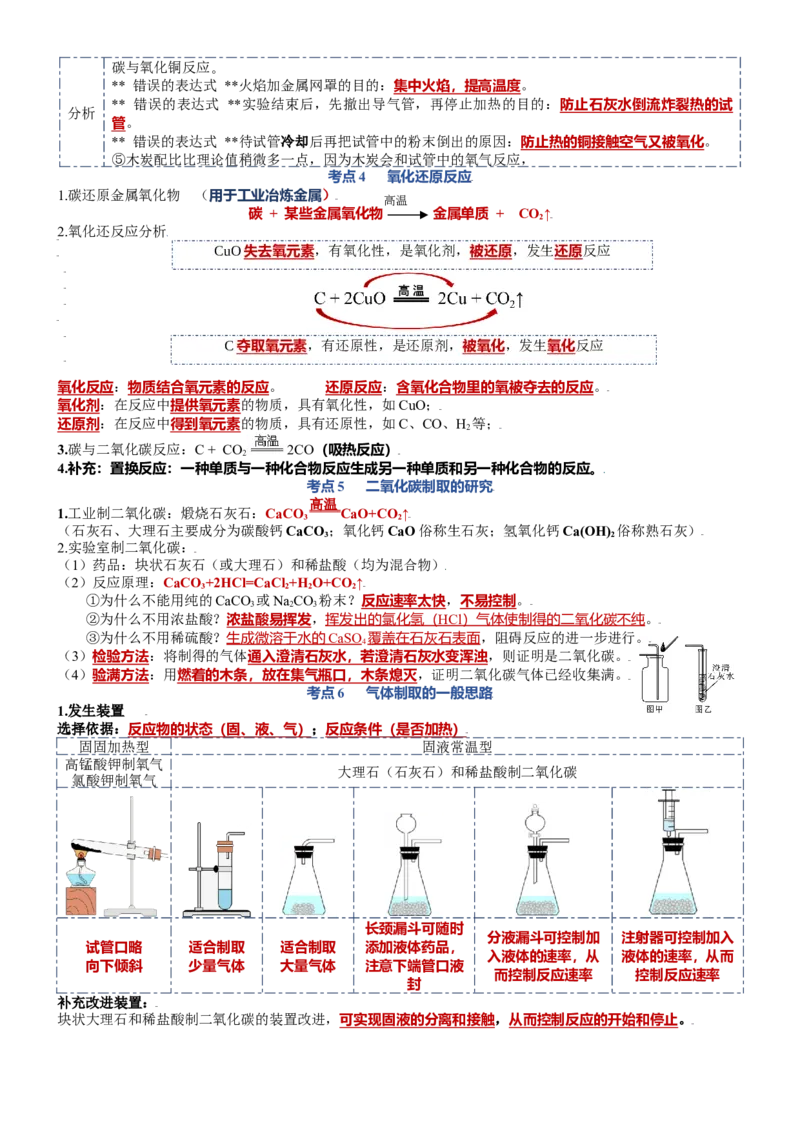
考点6 气体制取的一般思路
1.发生装置
选择依据:反应物的状态(固、液、气);反应条件(是否加热)
固固加热型 固液常温型
高锰酸钾制氧气
大理石(石灰石)和稀盐酸制二氧化碳
氯酸钾制氧气
长颈漏斗可随时
分液漏斗可控制加 注射器可控制加入
试管口略 适合制取 适合制取 添加液体药品,
入液体的速率,从 液体的速率,从而
向下倾斜 少量气体 大量气体 注意下端管口液
而控制反应速率 控制反应速率
封
补充改进装置:
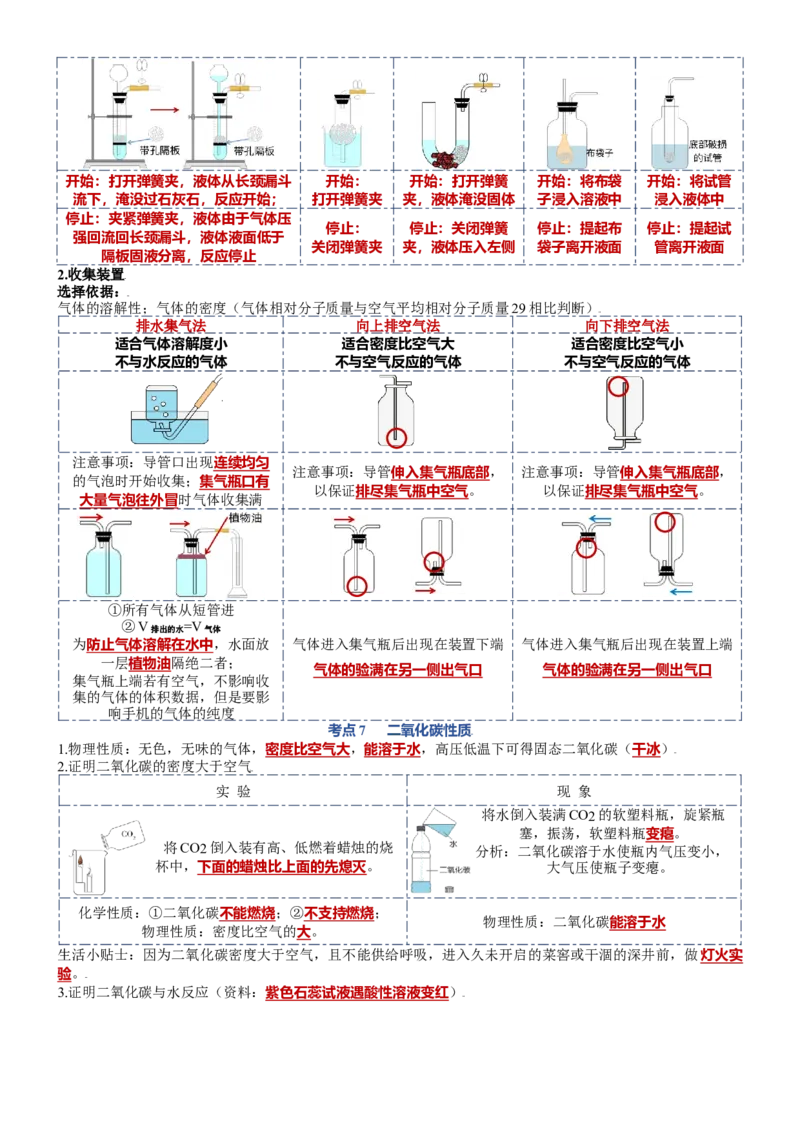
块状大理石和稀盐酸制二氧化碳的装置改进,可实现固液的分离和接触,从而控制反应的开始和停止。开始:打开弹簧夹,液体从长颈漏斗 开始: 开始:打开弹簧 开始:将布袋 开始:将试管
流下,淹没过石灰石,反应开始; 打开弹簧夹 夹,液体淹没固体 子浸入溶液中 浸入液体中
停止:夹紧弹簧夹,液体由于气体压
停止: 停止:关闭弹簧 停止:提起布 停止:提起试
强回流回长颈漏斗,液体液面低于
关闭弹簧夹 夹,液体压入左侧 袋子离开液面 管离开液面
隔板固液分离,反应停止
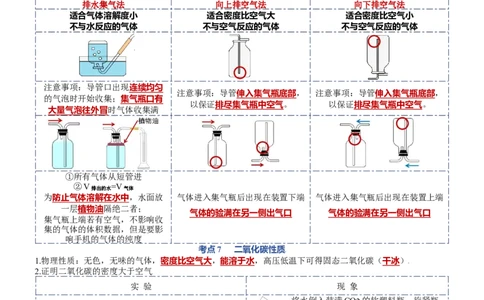
2.收集装置
选择依据:
气体的溶解性;气体的密度(气体相对分子质量与空气平均相对分子质量29相比判断)
排水集气法 向上排空气法 向下排空气法
适合气体溶解度小 适合密度比空气大 适合密度比空气小
不与水反应的气体 不与空气反应的气体 不与空气反应的气体
注意事项:导管口出现连续均匀
注意事项:导管伸入集气瓶底部, 注意事项:导管伸入集气瓶底部,
的气泡时开始收集;集气瓶口有
以保证排尽集气瓶中空气。 以保证排尽集气瓶中空气。
大量气泡往外冒时气体收集满
①所有气体从短管进
②V =V
排出的水 气体
为防止气体溶解在水中,水面放 气体进入集气瓶后出现在装置下端 气体进入集气瓶后出现在装置上端
一层植物油隔绝二者;
气体的验满在另一侧出气口 气体的验满在另一侧出气口
集气瓶上端若有空气,不影响收
集的气体的体积数据,但是要影
响手机的气体的纯度
考点7 二氧化碳性质
1.物理性质:无色,无味的气体,密度比空气大,能溶于水,高压低温下可得固态二氧化碳(干冰)
2.证明二氧化碳的密度大于空气
实 验 现 象
将水倒入装满CO2的软塑料瓶,旋紧瓶
塞,振荡,软塑料瓶变瘪。
将CO2倒入装有高、低燃着蜡烛的烧
分析:二氧化碳溶于水使瓶内气压变小,
杯中,下面的蜡烛比上面的先熄灭。 大气压使瓶子变瘪。
化学性质:①二氧化碳不能燃烧;②不支持燃烧;
物理性质:二氧化碳能溶于水
物理性质:密度比空气的大。
生活小贴士:因为二氧化碳密度大于空气,且不能供给呼吸,进入久未开启的菜窖或干涸的深井前,做灯火实
验。
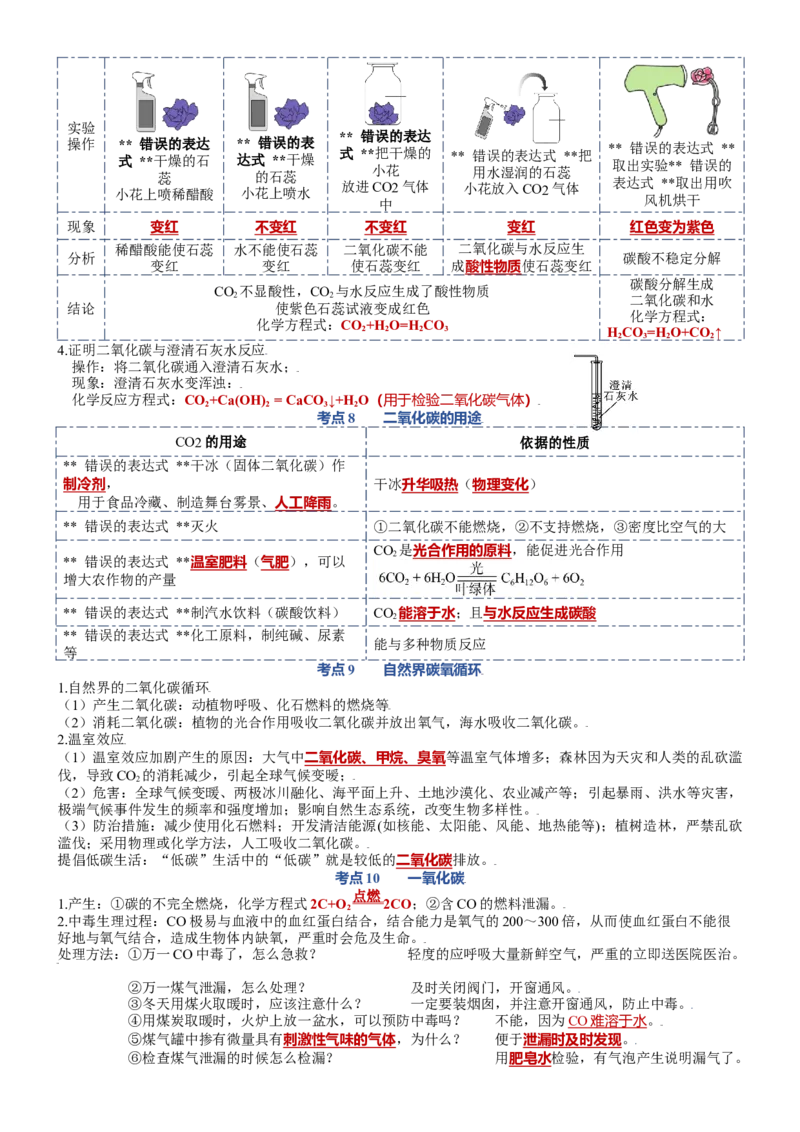
3.证明二氧化碳与水反应(资料:紫色石蕊试液遇酸性溶液变红)实验
** 错误的表达
操作 ** 错误的表达 ** 错误的表 ** 错误的表达式 **
式 **干燥的石 达式 **干燥 式 **把干燥的 ** 错误的表达式 **把
取出实验** 错误的
小花 用水湿润的石蕊
蕊 的石蕊
小花上喷稀醋酸 小花上喷水
放进CO2气体 小花放入CO2气体 表达式 **取出用吹
风机烘干
中
现象 变红 不变红 不变红 变红 红色变为紫色
稀醋酸能使石蕊 水不能使石蕊 二氧化碳不能 二氧化碳与水反应生
分析 碳酸不稳定分解
变红 变红 使石蕊变红 成酸性物质使石蕊变红
碳酸分解生成
CO 不显酸性,CO 与水反应生成了酸性物质
2 2 二氧化碳和水
结论 使紫色石蕊试液变成红色
化学方程式:
化学方程式:CO +H O=H CO
2 2 2 3 HCO =H O+CO ↑
2 3 2 2
4.证明二氧化碳与澄清石灰水反应
操作:将二氧化碳通入澄清石灰水;
现象:澄清石灰水变浑浊:
化学反应方程式:CO +Ca(OH) = CaCO ↓+H O(用于检验二氧化碳气体)
2 2 3 2
考点8 二氧化碳的用途
CO2的用途 依据的性质
** 错误的表达式 **干冰(固体二氧化碳)作
制冷剂, 干冰升华吸热(物理变化)
用于食品冷藏、制造舞台雾景、人工降雨。
** 错误的表达式 **灭火 ①二氧化碳不能燃烧,②不支持燃烧,③密度比空气的大
CO 是光合作用的原料,能促进光合作用
2
** 错误的表达式 **温室肥料(气肥),可以
增大农作物的产量
** 错误的表达式 **制汽水饮料(碳酸饮料) CO 能溶于水;且与水反应生成碳酸
2
** 错误的表达式 **化工原料,制纯碱、尿素
能与多种物质反应
等
考点9 自然界碳氧循环
1.自然界的二氧化碳循环
(1)产生二氧化碳:动植物呼吸、化石燃料的燃烧等
(2)消耗二氧化碳:植物的光合作用吸收二氧化碳并放出氧气,海水吸收二氧化碳。
2.温室效应
(1)温室效应加剧产生的原因:大气中二氧化碳、甲烷、臭氧等温室气体增多;森林因为天灾和人类的乱砍滥
伐,导致CO 的消耗减少,引起全球气候变暧;
2
(2)危害:全球气候变暖、两极冰川融化、海平面上升、土地沙漠化、农业减产等;引起暴雨、洪水等灾害,
极端气候事件发生的频率和强度增加;影响自然生态系统,改变生物多样性。
(3)防治措施:减少使用化石燃料;开发清洁能源(如核能、太阳能、风能、地热能等);植树造林,严禁乱砍
滥伐;采用物理或化学方法,人工吸收二氧化碳。
提倡低碳生活:“低碳”生活中的“低碳”就是较低的二氧化碳排放。
考点10 一氧化碳
点燃
1.产生:①碳的不完全燃烧,化学方程式2C+O 2CO;②含CO的燃料泄漏。
2
2.中毒生理过程:CO极易与血液中的血红蛋白结合,结合能力是氧气的200~300倍,从而使血红蛋白不能很
好地与氧气结合,造成生物体内缺氧,严重时会危及生命。
处理方法:①万一CO中毒了,怎么急救? 轻度的应呼吸大量新鲜空气,严重的立即送医院医治。
②万一煤气泄漏,怎么处理? 及时关闭阀门,开窗通风。
③冬天用煤火取暖时,应该注意什么? 一定要装烟囱,并注意开窗通风,防止中毒。
④用煤炭取暖时,火炉上放一盆水,可以预防中毒吗? 不能,因为 CO 难溶于水 。
⑤煤气罐中掺有微量具有刺激性气味的气体,为什么? 便于泄漏时及时发现。
⑥检查煤气泄漏的时候怎么检漏? 用肥皂水检验,有气泡产生说明漏气了。3.可燃性
①纯净的CO安静的燃烧,产生蓝色火焰,用内壁涂有澄清石灰水的烧杯罩在火焰上方,澄清石灰水变变浑浊。
点燃
②燃烧的化学方程式:2CO+O 2CO
2 2
澄清石灰水变浑浊的化学方程式:CO +Ca(OH) = CaCO ↓+H O
2 2 3 2
③用途:作燃料。注意点燃前先检验气体的纯度(验纯)。
点燃 高温 点燃
煤炉底部:C+O CO 煤炉中部:C+CO 2CO 煤炉上口:2CO+O 2CO
2 2 2 2 2
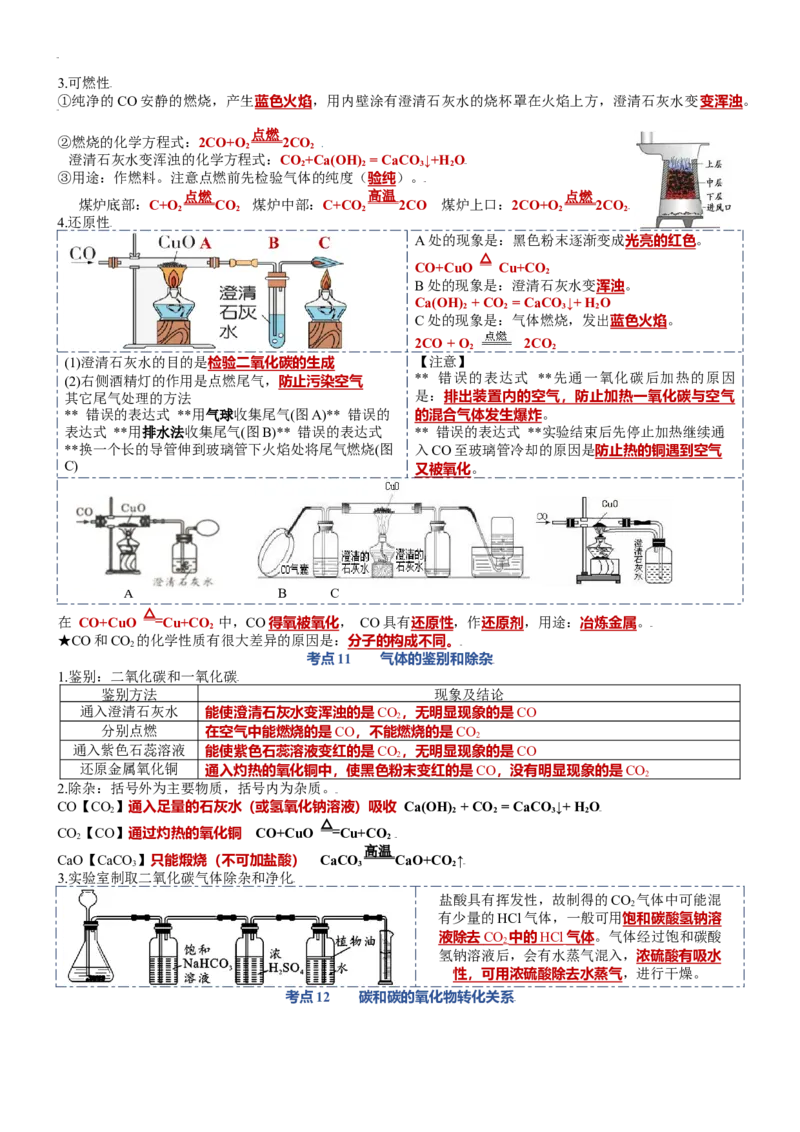
4.还原性
A处的现象是:黑色粉末逐渐变成光亮的红色。
CO+CuO Cu+CO
2
B处的现象
△
是:澄清石灰水变浑浊。
Ca(OH) + CO = CaCO ↓+ H O
2 2 3 2
C处的现象是:气体燃烧,发出蓝色火焰。
2CO + O 2CO
2 2
(1)澄清石灰水的目的是检验二氧化碳的生成 【注意】
(2)右侧酒精灯的作用是点燃尾气,防止污染空气 ** 错误的表达式 **先通一氧化碳后加热的原因
其它尾气处理的方法 是:排出装置内的空气,防止加热一氧化碳与空气
** 错误的表达式 **用气球收集尾气(图A)** 错误的 的混合气体发生爆炸。
表达式 **用排水法收集尾气(图B)** 错误的表达式 ** 错误的表达式 **实验结束后先停止加热继续通
**换一个长的导管伸到玻璃管下火焰处将尾气燃烧(图 入CO至玻璃管冷却的原因是防止热的铜遇到空气
C) 又被氧化。
A B C
在 CO+CuO Cu+CO 中,CO得氧被氧化, CO具有还原性,作还原剂,用途:冶炼金属。
2
★CO和CO
2
的
△
化学性质有很大差异的原因是:分子的构成不同。
考点11 气体的鉴别和除杂
1.鉴别:二氧化碳和一氧化碳
鉴别方法 现象及结论
通入澄清石灰水 能使澄清石灰水变浑浊的是CO,无明显现象的是CO
2
分别点燃 在空气中能燃烧的是CO,不能燃烧的是CO
2
通入紫色石蕊溶液 能使紫色石蕊溶液变红的是CO,无明显现象的是CO
2
还原金属氧化铜 通入灼热的氧化铜中,使黑色粉末变红的是CO,没有明显现象的是CO
2
2.除杂:括号外为主要物质,括号内为杂质。
CO【CO】通入足量的石灰水(或氢氧化钠溶液)吸收 Ca(OH) + CO = CaCO ↓+ H O
2 2 2 3 2
CO【CO】通过灼热的氧化铜 CO+CuO Cu+CO
2 2
高温
CaO【CaCO 】只能煅烧(不可加盐酸) C △ aCO CaO+CO ↑
3 3 2
3.实验室制取二氧化碳气体除杂和净化
盐酸具有挥发性,故制得的CO 气体中可能混
2
有少量的HCl气体,一般可用饱和碳酸氢钠溶
液除去 CO 中的 HC l 气体 。气体经过饱和碳酸
2
氢钠溶液后,会有水蒸气混入,浓硫酸有吸水
性,可用浓硫酸除去水蒸气,进行干燥。
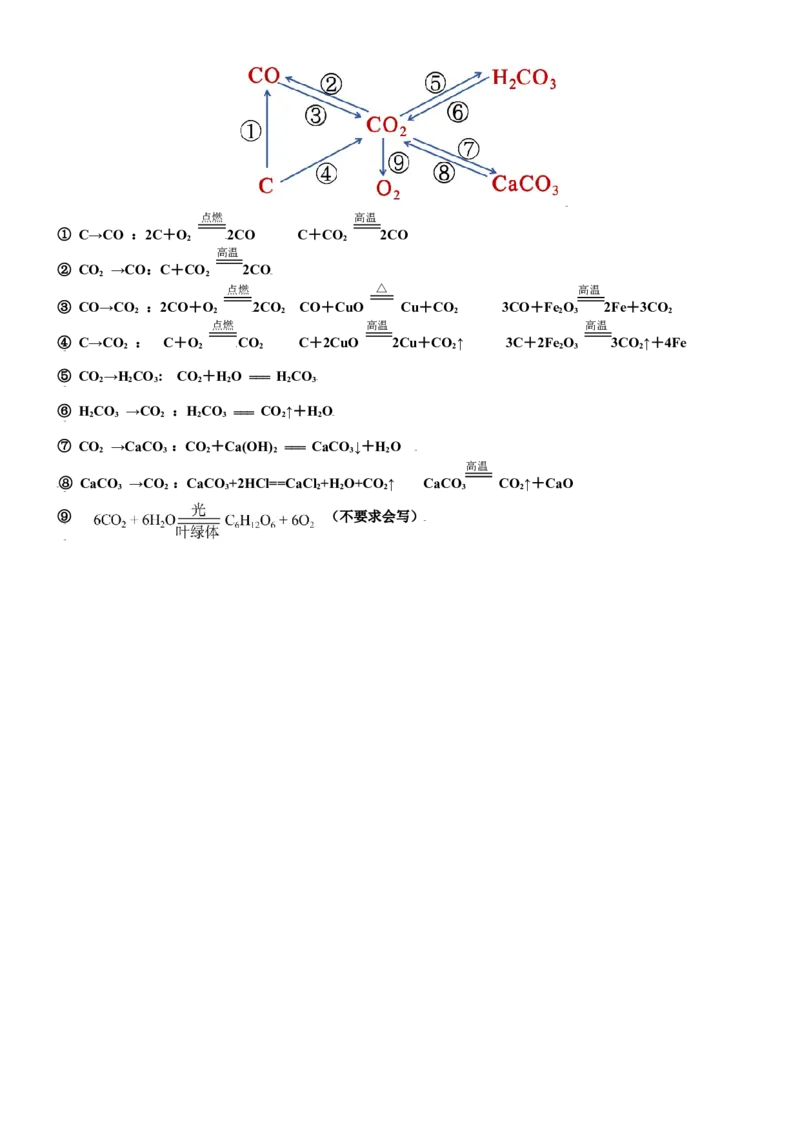
考点12 碳和碳的氧化物转化关系点燃 高温
① C→CO :2C+O
2
2CO C+CO
2
2CO
高温
② CO
2
→CO:C+CO
2
2CO
点燃 △ 高温
③ CO→CO
2
:2CO+O
2
2CO
2
CO+CuO Cu+CO
2
3CO+Fe
2
O
3
2Fe+3CO
2
点燃 高温 高温
④ C→CO
2
: C+O
2
CO
2
C+2CuO 2Cu+CO
2
↑ 3C+2Fe
2
O
3
3CO
2
↑+4Fe
⑤ CO
2
→H
2
CO
3
: CO
2
+H
2
O === H
2
CO
3
⑥ H
2
CO
3
→CO
2
:H
2
CO
3
=== CO
2
↑+H
2
O
⑦ CO →CaCO :CO +Ca(OH) === CaCO ↓+HO
2 3 2 2 3 2
高温
⑧ CaCO
3
→CO
2
:CaCO
3
+2HCl==CaCl
2
+H
2
O+CO
2
↑ CaCO
3
CO
2
↑+CaO
⑨ (不要求会写)