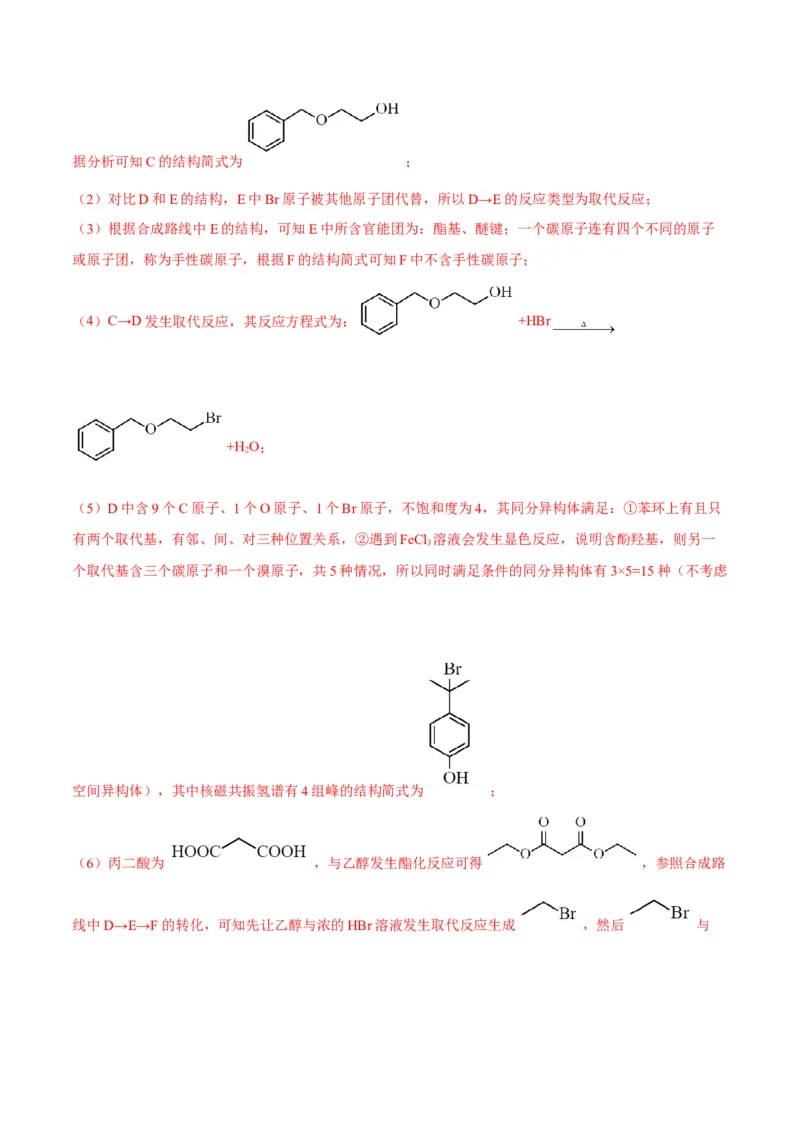
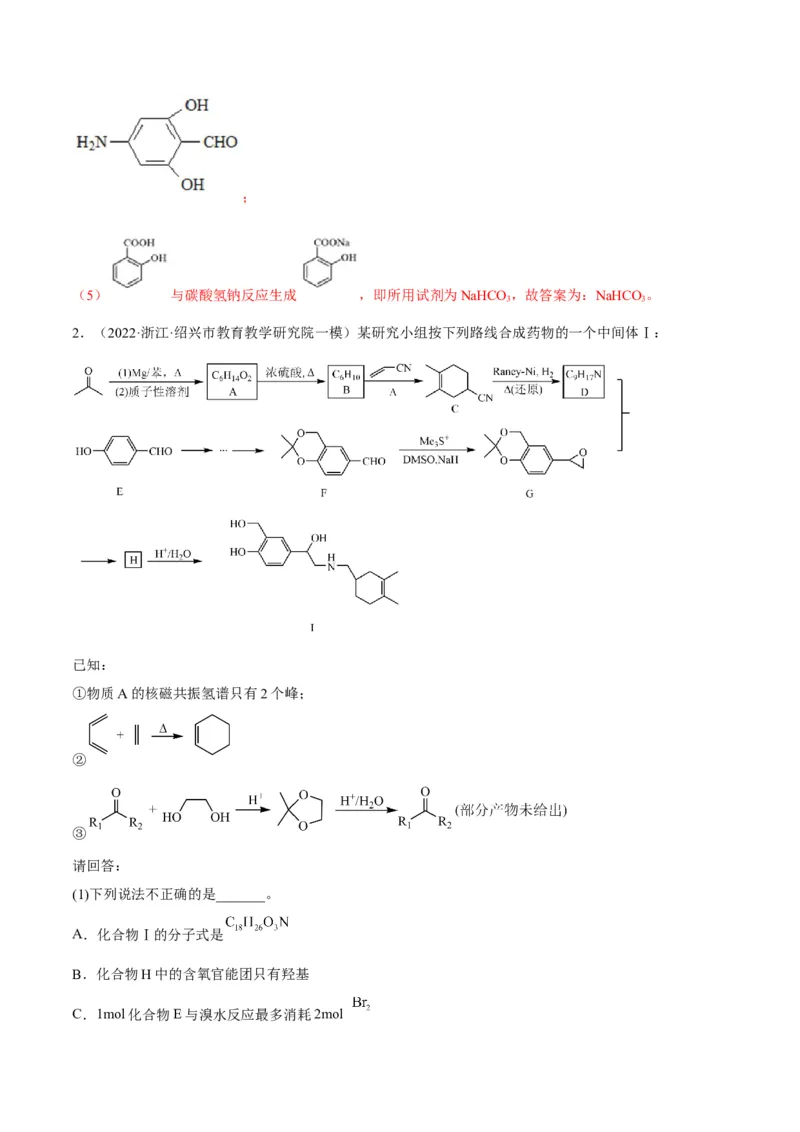
文档内容
解密 17 有机合成与推断
考点热度 ★★★★★
【考纲导向】
1.了解烃类及衍生物的重要应用以及烃的衍生物的合成方法。
2.根据信息能设计有机化合物的合成路线。
3.了解加成反应、取代反应、消去反应、加聚反应和缩聚反应的含义。
4.了解合成高分子化合物的组成与结构特点,能依据简单合成高分子的结构分析其链节和单体。
【命题分析】
依据有机物之间的转化流程进行有机结构推断是高考的重要题型,也是每年全国卷高考的必考内容,主要
考查有机物官能团的结构与性质、化学方程式书写、反应类型判断、同分异构体的书写与判断等内容。此
类题目综合性强、情景新、难度较大。有机合成也是近几年全国卷命题的热点和难点,《考试大纲》中有
机化学明确要求考生能够“组合多个化合物的化学反应,合成具有指定结构简式的产物”,有机合成的实
质是利用有机反应的基本规律,进行必要的官能团的转化,合成目标产物。预计2023年有机合成推断难度
会略有增加。
核心考点一 有机物的推断
1.有机推断中反应条件与反应类型的关系
(1)在NaOH的水溶液中发生水解反应,可能是酯的水解反应或卤代烃的水解反应。(2)在NaOH的乙醇溶液中加热,发生卤代烃的消去反应。
(3)在浓HSO 存在的条件下加热,可能发生醇的消去反应、酯化反应、成醚反应或硝化反应等。
2 4
(4)能与溴水或溴的CCl 溶液反应,可能为烯烃、炔烃的加成反应。
4
(5)在光照、X(表示卤素单质)条件下发生烷基上的取代反应;在Fe粉、X 条件下发生苯环上的取代反应。
2 2
2.根据反应条件推断反应物或生成物
(1)“光照”为烷烃的卤代反应。
(2)“NaOH水溶液、加热”为R—X的水解反应,或酯( )的水解反应。
(3)“NaOH醇溶液、加热”为R—X的消去反应。
(4)“HNO (H SO )”为苯环上的硝化反应。
3 2 4
(5)“浓HSO 、加热”为R—OH的消去或酯化反应。
2 4
(6)“浓HSO 、170 ℃”是乙醇消去反应的条件。
2 4
3.根据有机反应的特殊现象推断有机物的官能团
(1)使溴水褪色,则表示有机物分子中可能含有碳碳双键、碳碳三键或醛基。
(2)使酸性KMnO 溶液褪色,则该物质中可能含有碳碳双键、碳碳三键、醛基或苯的同系物(连接苯环的碳
4
上含有氢原子)。
(3)遇FeCl 溶液显紫色或加入浓溴水出现白色沉淀,表示该物质分子中含有酚羟基。
3
(4)加入新制Cu(OH) 悬浊液并加热,有砖红色沉淀生成(或加入银氨溶液并水浴加热有银镜出现),说明该
2
物质中含有—CHO。
(5)加入金属钠,有H 产生,表示该物质分子中可能有—OH或—COOH。
2
(6)加入NaHCO 溶液有气体放出,表示该物质分子中含有—COOH。
3
4.以特征产物为突破口来推断碳架结构和官能团的位置
(1)醇的氧化产物与结构的关系
(2)由消去反应的产物可确定“—OH”或“—X”的位置。
(3)由取代产物的种类或氢原子环境可确定碳架结构。有机物取代产物越少或相同环境的氢原子数越多,说
明此有机物结构的对称性越高,因此可由取代产物的种类或氢原子环境联想到此有机物碳架结构的对称性
而快速进行解题。
(4)由加氢后的碳架结构可确定碳碳双键或碳碳三键的位置。
(5)由有机物发生酯化反应能生成环酯或高聚酯,可确定该有机物是含羟基的羧酸;根据酯的结构,可确定
—OH与—COOH的相对位置。
5.根据关键数据推断官能团的数目(1)CHO
(5)RCHOH――→CHCOOCH R
2 3 2
(M) (M+42)
r r
考法 有机推断(题型预测:非选择题)
1.(2022·青海·海东市第一中学一模)化合物F是用于治疗疱疹药品的合成中间体,其合成路线如图所示。
回答下列问题:
(1)A—B反应所需的试剂和条件分别为_______、_______;C的结构简式为_______;
(2)D—E的反应类型为_______;
(3)E中所含官能团的名称是_______;F中_______(填“含”或“不含”)手性碳原子;
(4)C—D的反应方程式为_______;
(5)D有多种同分异构体,同时满足下列条件的同分异构体有_______种(不考虑立体异构);其中核磁共振氢
谱有4组峰的结构简式为_______;
①苯环上有且只有两个取代基;
②遇FeCl 溶液会发生显色反应;
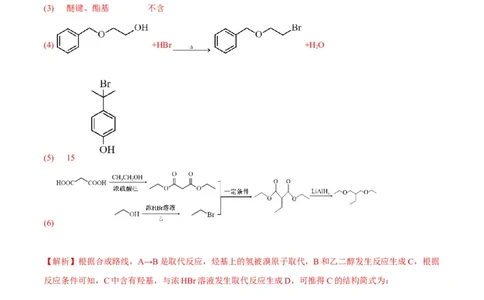
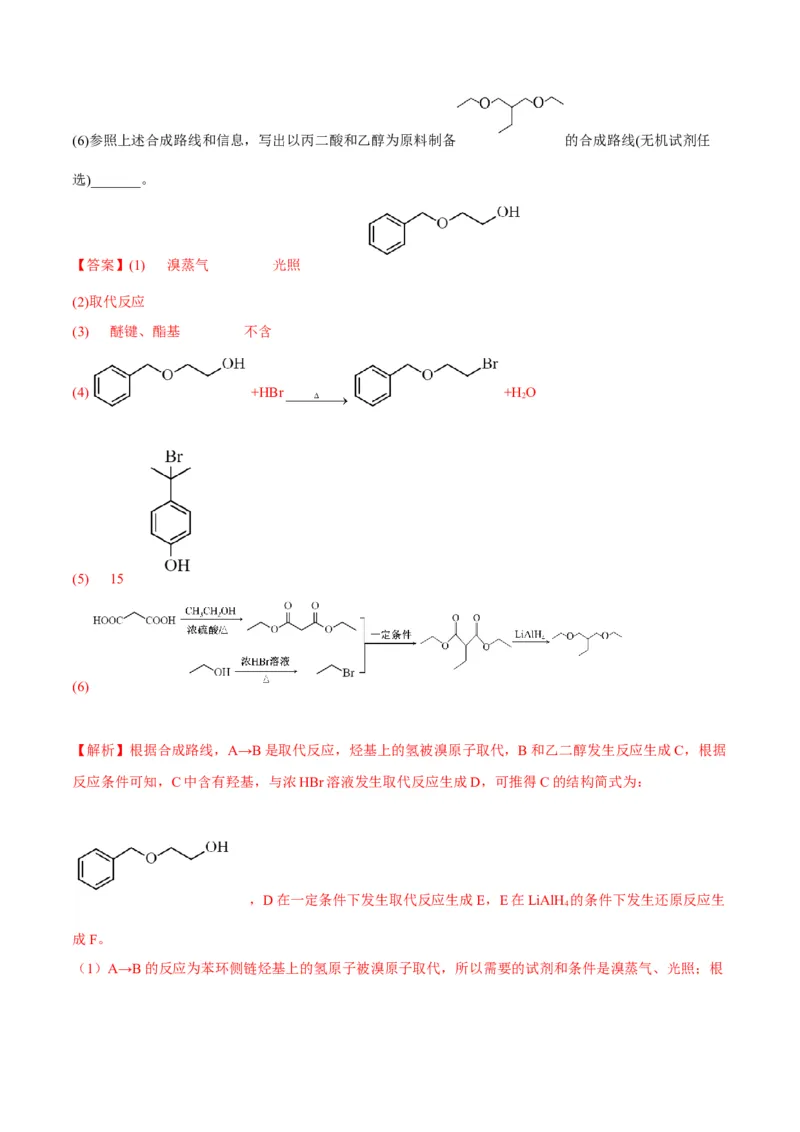
3(6)参照上述合成路线和信息,写出以丙二酸和乙醇为原料制备 的合成路线(无机试剂任
选)_______。
【答案】(1) 溴蒸气 光照
(2)取代反应
(3) 醚键、酯基 不含
(4) +HBr +H O
2
(5) 15
(6)
【解析】根据合成路线,A→B是取代反应,烃基上的氢被溴原子取代,B和乙二醇发生反应生成C,根据
反应条件可知,C中含有羟基,与浓HBr溶液发生取代反应生成D,可推得C的结构简式为:
,D在一定条件下发生取代反应生成E,E在LiAlH 的条件下发生还原反应生
4
成F。
(1)A→B的反应为苯环侧链烃基上的氢原子被溴原子取代,所以需要的试剂和条件是溴蒸气、光照;根据分析可知C的结构简式为 ;
(2)对比D和E的结构,E中Br原子被其他原子团代替,所以D→E的反应类型为取代反应;
(3)根据合成路线中E的结构,可知E中所含官能团为:酯基、醚键;一个碳原子连有四个不同的原子
或原子团,称为手性碳原子,根据F的结构简式可知F中不含手性碳原子;
(4)C→D发生取代反应,其反应方程式为: +HBr
+H O;
2
(5)D中含9个C原子、1个O原子、1个Br原子,不饱和度为4,其同分异构体满足:①苯环上有且只
有两个取代基,有邻、间、对三种位置关系,②遇到FeCl 溶液会发生显色反应,说明含酚羟基,则另一
3
个取代基含三个碳原子和一个溴原子,共5种情况,所以同时满足条件的同分异构体有3×5=15种(不考虑
空间异构体),其中核磁共振氢谱有4组峰的结构简式为 ;
(6)丙二酸为 ,与乙醇发生酯化反应可得 ,参照合成路
线中D→E→F的转化,可知先让乙醇与浓的HBr溶液发生取代反应生成 ,然后 与发生取代反应生成 ,最后在LiAlH 的条件下发生还原
4
反应生成目标产物,所以合成路线为:
。
高考常见的新信息反应总结
(1)丙烯αH被取代的反应:
CHCHCH +Cl――→ClCH CHCH +HCl。
3 2 2 2 2
(2)共轭二烯烃的1,4加成反应:
② 。
(3)烯烃被O 氧化:
3
(4) 苯 环 侧 链 的 烃 基 ( 与 苯 环 相 连 的 碳 上 含 有 氢 原 子 ) 被 酸 性 KMnO 溶 液 氧 化 :
4
。
(5)苯环上硝基被还原: 。
(6)醛、酮的加成反应(加长碳链,—CN水解得—COOH):
;(8)醛或酮与格氏试剂(R′MgX)发生加成反应,所得产物经水解可得醇:
(10)羧酸用LiAlH 还原时,可生成相应的醇:RCOOH――→RCHOH。
4 2
(11)酯交换反应(酯的醇解):R COOR +R OH―→R COOR +R OH。
1 2 3 1 3 2
变式一 分子式、反应条件有机推断
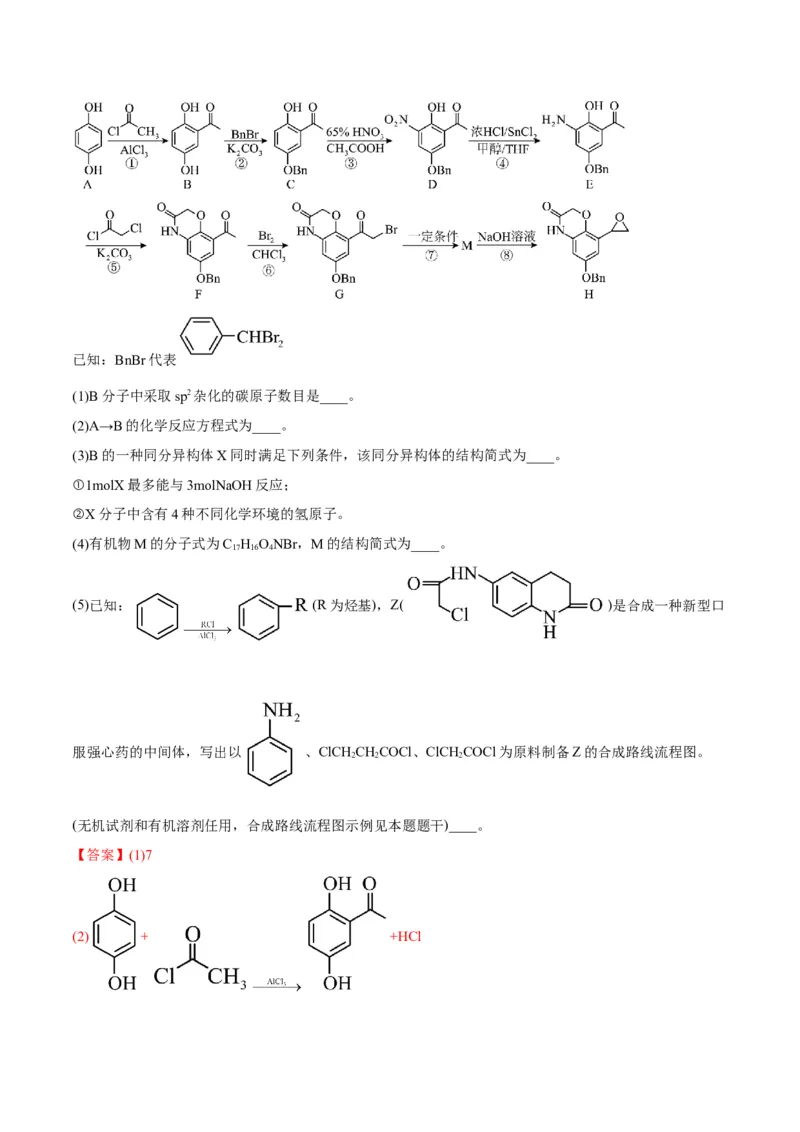
1.(2022·江苏·苏州中学高三期中)化合物H是用于治疗慢性阻塞性肺病奥达特罗的合成中间体,合成路
线如图:已知:BnBr代表
(1)B分子中采取sp2杂化的碳原子数目是____。
(2)A→B的化学反应方程式为____。
(3)B的一种同分异构体X同时满足下列条件,该同分异构体的结构简式为____。
①1molX最多能与3molNaOH反应;
②X分子中含有4种不同化学环境的氢原子。
(4)有机物M的分子式为C H ONBr,M的结构简式为____。
17 16 4
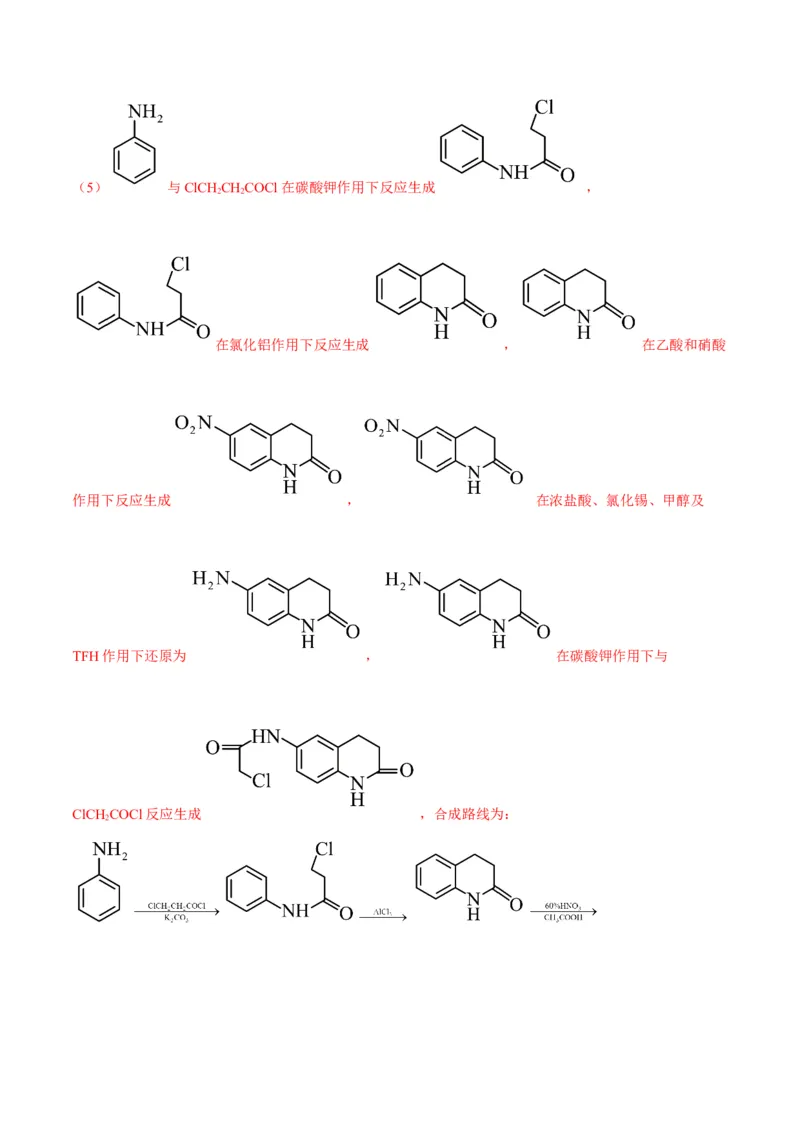
(5)已知: (R为烃基),Z( )是合成一种新型口
服强心药的中间体,写出以 、ClCH CHCOCl、ClCH COCl为原料制备Z的合成路线流程图。
2 2 2
(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)____。
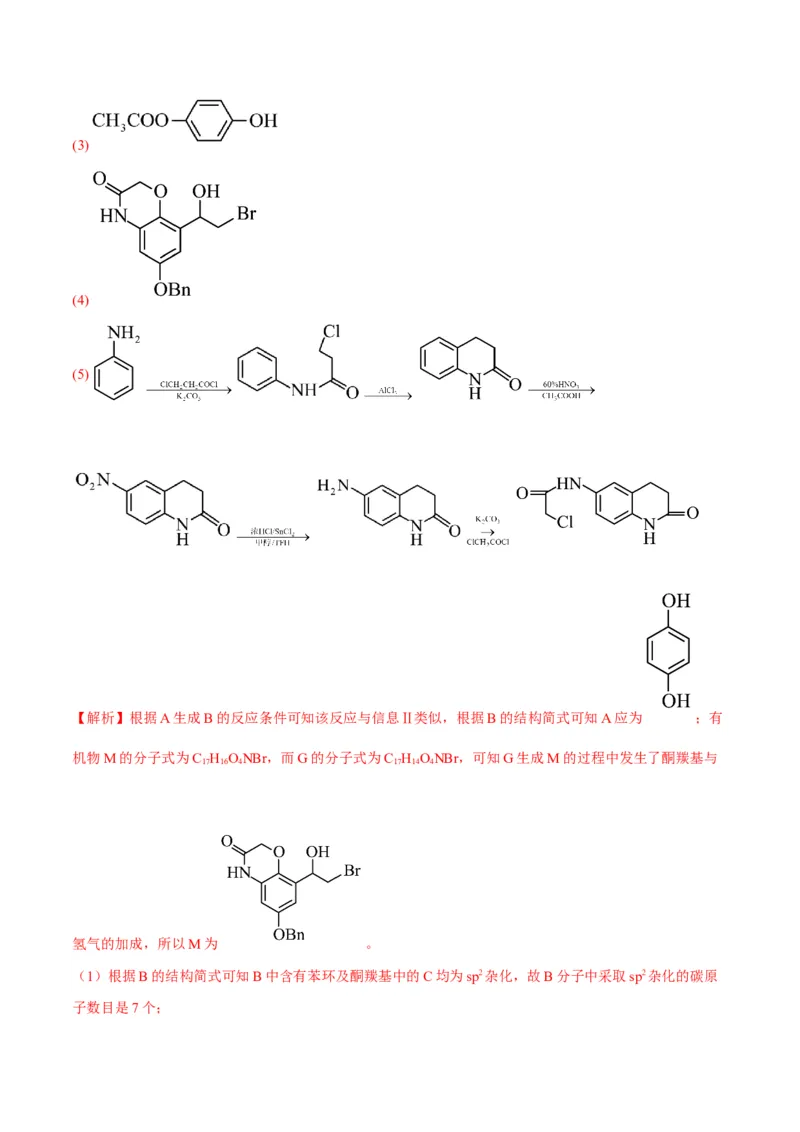
【答案】(1)7
(2) + +HCl(3)
(4)
(5)
【解析】根据A生成B的反应条件可知该反应与信息Ⅱ类似,根据B的结构简式可知A应为 ;有
机物M的分子式为C H ONBr,而G的分子式为C H ONBr,可知G生成M的过程中发生了酮羰基与
17 16 4 17 14 4
氢气的加成,所以M为 。
(1)根据B的结构简式可知B中含有苯环及酮羰基中的C均为sp2杂化,故B分子中采取sp2杂化的碳原
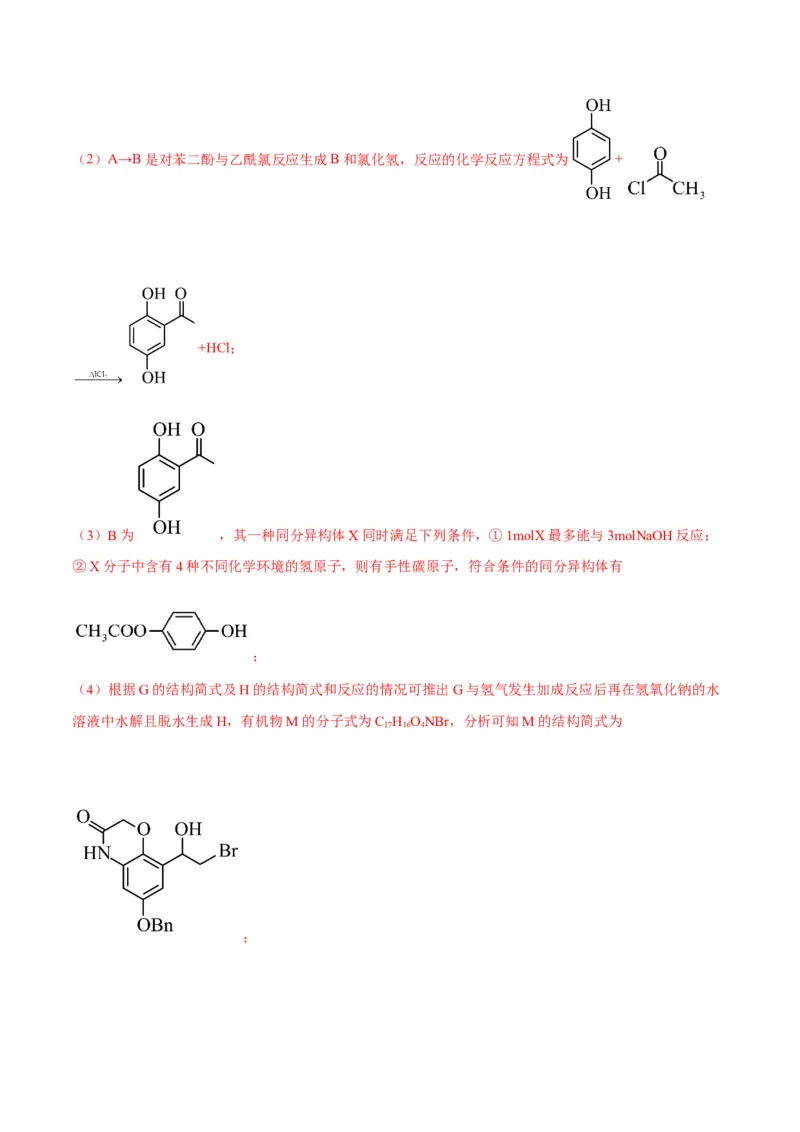
子数目是7个;(2)A→B是对苯二酚与乙酰氯反应生成B和氯化氢,反应的化学反应方程式为 +
+HCl;
(3)B为 ,其一种同分异构体X同时满足下列条件,①1molX最多能与3molNaOH反应;
②X分子中含有4种不同化学环境的氢原子,则有手性碳原子,符合条件的同分异构体有
;
(4)根据G的结构简式及H的结构简式和反应的情况可推出G与氢气发生加成反应后再在氢氧化钠的水
溶液中水解且脱水生成H,有机物M的分子式为C H ONBr,分析可知M的结构简式为
17 16 4
;(5) 与ClCH CHCOCl在碳酸钾作用下反应生成 ,
2 2
在氯化铝作用下反应生成 , 在乙酸和硝酸
作用下反应生成 , 在浓盐酸、氯化锡、甲醇及
TFH作用下还原为 , 在碳酸钾作用下与
ClCH COCl反应生成 ,合成路线为:
2。
变式二 物质性质和转化信息的有机推断
2.(2022·广东·高三阶段练习)吡唑类化合物G是一种重要的医用中间体,也可作为某些光敏材料、染料
的原材料。其合成路线如下:
已知:
Ⅰ.R -CHO+R CH-COOR
1 2 2 3
Ⅱ.R -CHO+R NH R -CH=N-R
1 2 2 1 2
(1)反应①所需试剂、条件分别是_______,C的名称是_______
(2)A→B的化学方程式为_______
(3)测定E所含化学键和官能团的仪器应选用_______
A.元素分析仪 B.质谱仪 C.红外光谱仪 D.分光光度计
(4)若D与液溴发生加成反应生成E,写出在碱醇条件下E生成F的化学方程式_______
(5)X为D的同分异构体,写出满足如下条件X的结构简式_______
①含有苯环;
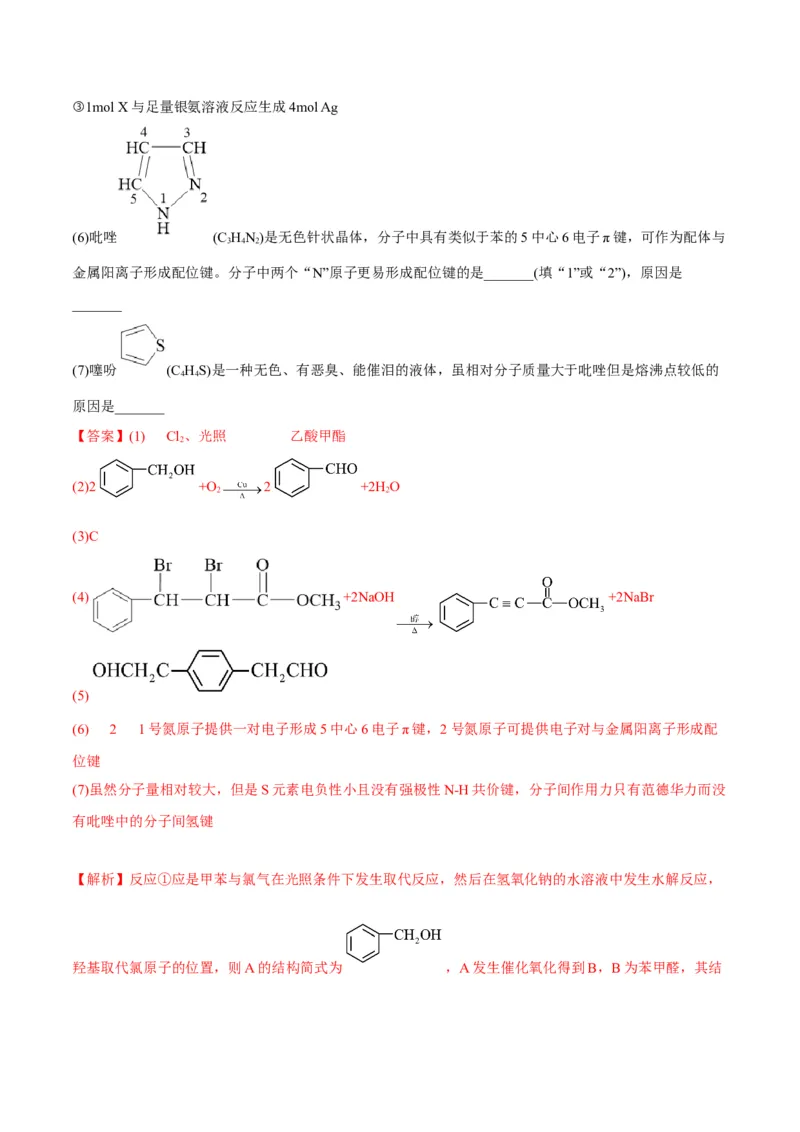
②核磁共振氢谱有三组峰,峰面积之比为2:2:1;③1mol X与足量银氨溶液反应生成4mol Ag
(6)吡唑 (C HN)是无色针状晶体,分子中具有类似于苯的5中心6电子π键,可作为配体与
3 4 2
金属阳离子形成配位键。分子中两个“N”原子更易形成配位键的是_______(填“1”或“2”),原因是
_______
(7)噻吩 (C HS)是一种无色、有恶臭、能催泪的液体,虽相对分子质量大于吡唑但是熔沸点较低的
4 4
原因是_______
【答案】(1) Cl 、光照 乙酸甲酯
2
(2)2 +O 2 +2H O
2 2
(3)C
(4) +2NaOH +2NaBr
(5)
(6) 2 1号氮原子提供一对电子形成5中心6电子π键,2号氮原子可提供电子对与金属阳离子形成配
位键
(7)虽然分子量相对较大,但是S元素电负性小且没有强极性N-H共价键,分子间作用力只有范德华力而没
有吡唑中的分子间氢键
【解析】反应①应是甲苯与氯气在光照条件下发生取代反应,然后在氢氧化钠的水溶液中发生水解反应,
羟基取代氯原子的位置,则A的结构简式为 ,A发生催化氧化得到B,B为苯甲醛,其结构简式为 ,根据信息I、C的分子式以及D的结构简式,推出C的结构简式为
CHCOOCH ,根据B、G、CH-NH-NH 的结构简式以及F的分子式C HO,推出F的结构简式为
3 3 3 2 10 8 2
,对比D和F的结构简式,D与Br 发生加成反应,E发生消去反应得到F。
2
(1)根据上述分析,反应①所需试剂和条件分别是Cl、光照;C的结构简式为CHCOOCH ,属于酯,
2 3 3
名称为乙酸甲酯;
(2)A生成B为羟基的催化氧化,化学方程式为2 +O 2 +2H O;
2 2
(3)测定所含化学键和官能团的仪器是红外光谱仪,故选C;
(4)D与Br 发生加成反应,所以E为 ,E发生消去反应得到
2
,化学方程式为 +2NaOH
+2NaBr;
(5)核磁共振氢谱有三组峰,说明含有三种不同化学环境的氢原子,即该结构为对称结构,三种氢原子
的个数比为2:2:1,1molX与足量银氨溶液反应生成4molAg,说明1个X分子中含有2个醛基,符合条
件的结构简式为 ;
(6)1号氮原子提供一对电子形成5中心6电子π键,2号氮原子可提供电子对与金属阳离子形成配位键,
所以2号氮原子更易形成配位键;
(7)虽然噻吩分子量相对较大,但是S元素电负性小且没有强极性N-H共价键,分子间作用力只有范德华力而没有吡唑中的分子间氢键,所以熔沸点较低。
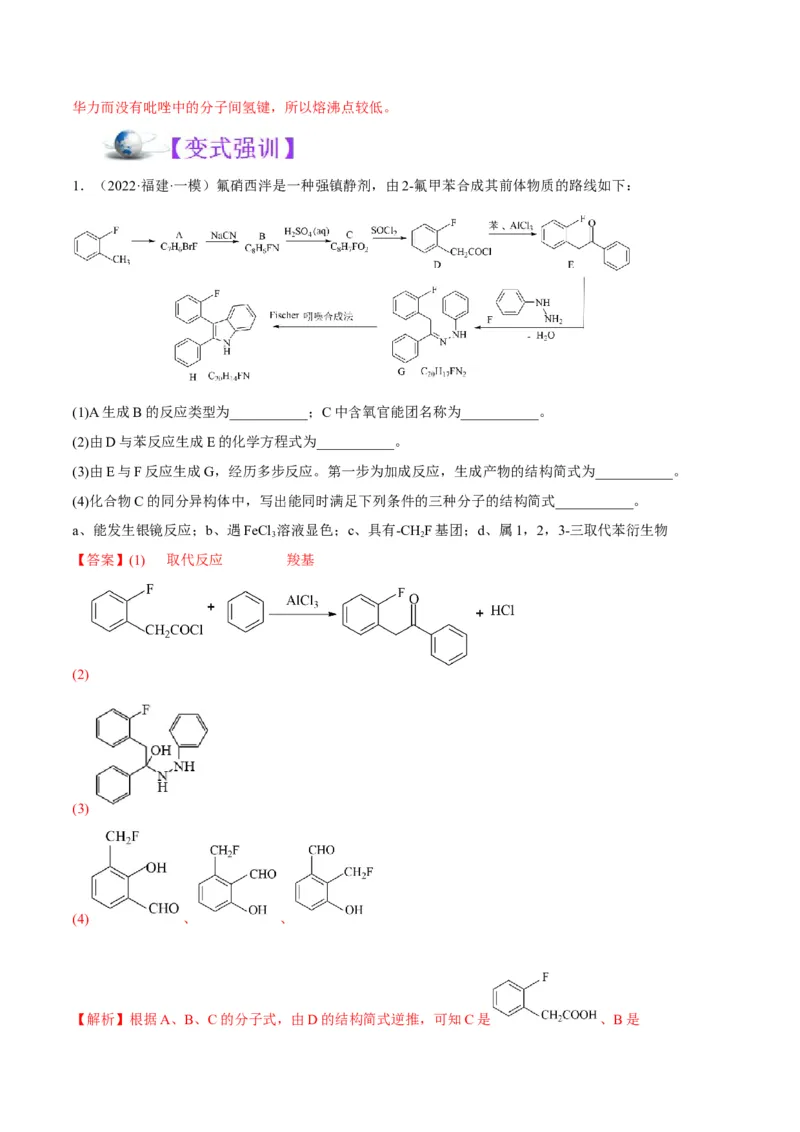
1.(2022·福建·一模)氟硝西泮是一种强镇静剂,由2-氟甲苯合成其前体物质的路线如下:
(1)A生成B的反应类型为___________;C中含氧官能团名称为___________。
(2)由D与苯反应生成E的化学方程式为___________。
(3)由E与F反应生成G,经历多步反应。第一步为加成反应,生成产物的结构简式为___________。
(4)化合物C的同分异构体中,写出能同时满足下列条件的三种分子的结构简式___________。
a、能发生银镜反应;b、遇FeCl 溶液显色;c、具有-CHF基团;d、属1,2,3-三取代苯衍生物
3 2
【答案】(1) 取代反应 羧基
(2)
(3)
(4) 、 、
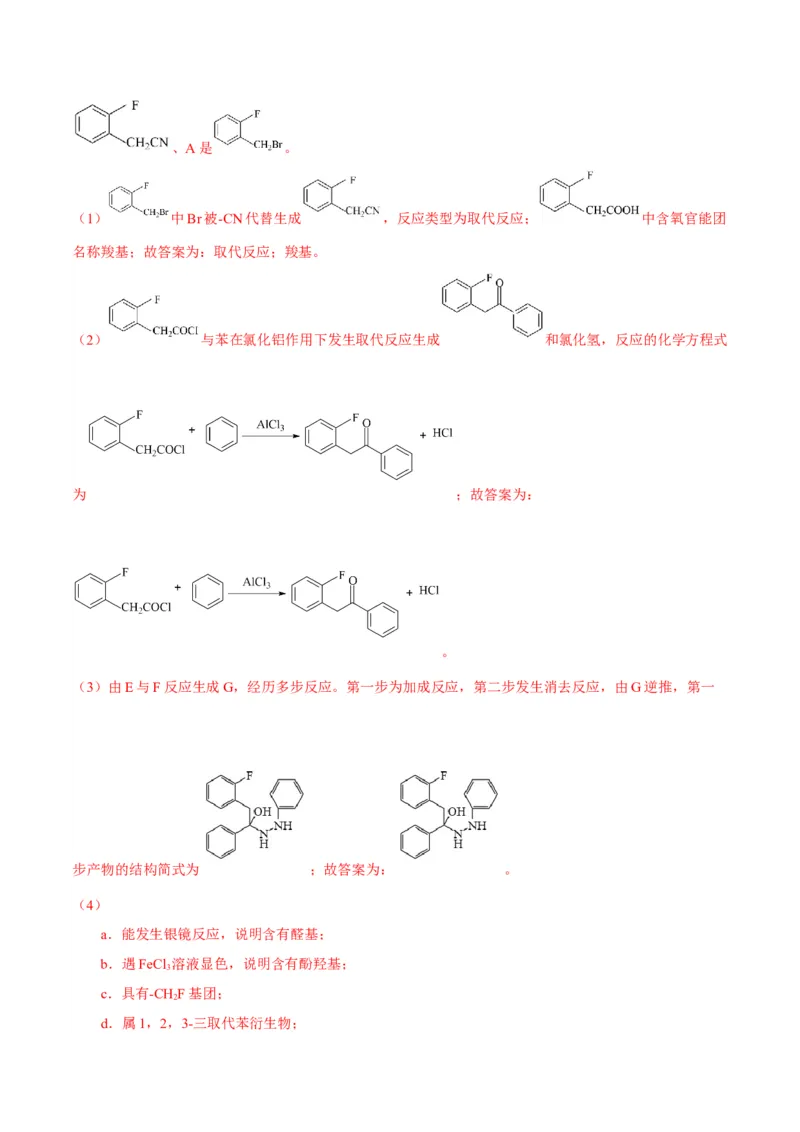
【解析】根据A、B、C的分子式,由D的结构简式逆推,可知C是 、B是、A是 。
(1) 中Br被-CN代替生成 ,反应类型为取代反应; 中含氧官能团
名称羧基;故答案为:取代反应;羧基。
(2) 与苯在氯化铝作用下发生取代反应生成 和氯化氢,反应的化学方程式
为 ;故答案为:
。
(3)由E与F反应生成G,经历多步反应。第一步为加成反应,第二步发生消去反应,由G逆推,第一
步产物的结构简式为 ;故答案为: 。
(4)
a.能发生银镜反应,说明含有醛基;
b.遇FeCl 溶液显色,说明含有酚羟基;
3
c.具有-CHF基团;
2
d.属1,2,3-三取代苯衍生物;符合条件的C的同分异构体有 、 、 。
2.(2023·广东·惠州一中模拟预测)化合物H是一种医药中间体,H的一种合成路线如图所示:
已知:① ②
回答下列问题:
(1)有机物D中所含官能团的名称为_____________。
(2)写出 的第二步反应方程式__________________________;反应类型为_____________。
(3)有机物C的同分异构体有多种,满足下列条件的有_____________种。
①分子除苯环外不再含其他环; ②与 溶液发生显色反应
其中核磁共振氢谱有5组峰且峰面积为1∶2∶2∶2∶2的有机物结构简式为_____________。
(4)苯环上已有的取代基叫做定位取代基,它们的存在会影响苯环上再引入其它基团时进入的位置,已知
是邻对位定位基, 是间位定位基。写出以硝基苯、 为原料制备 的合成路线(无
机试剂任选) ____________。
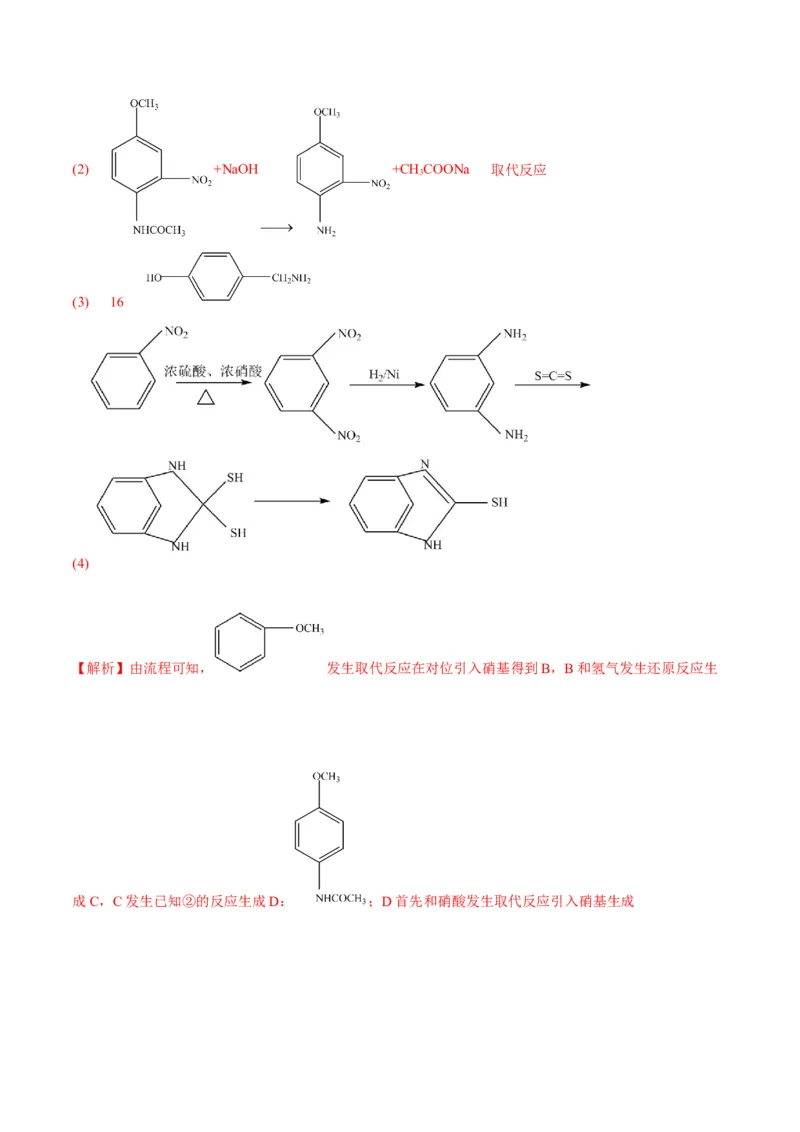
【答案】(1)醚键、酰胺基(2) +NaOH +CH COONa 取代反应
3
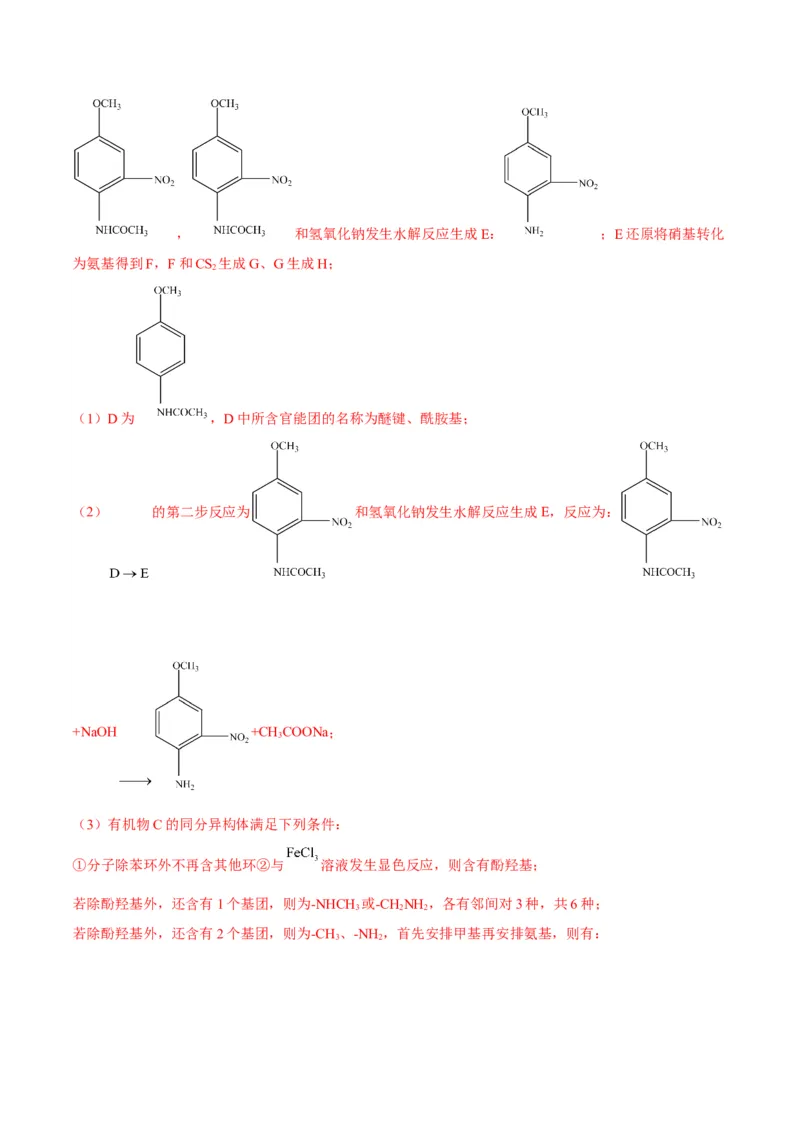
(3) 16
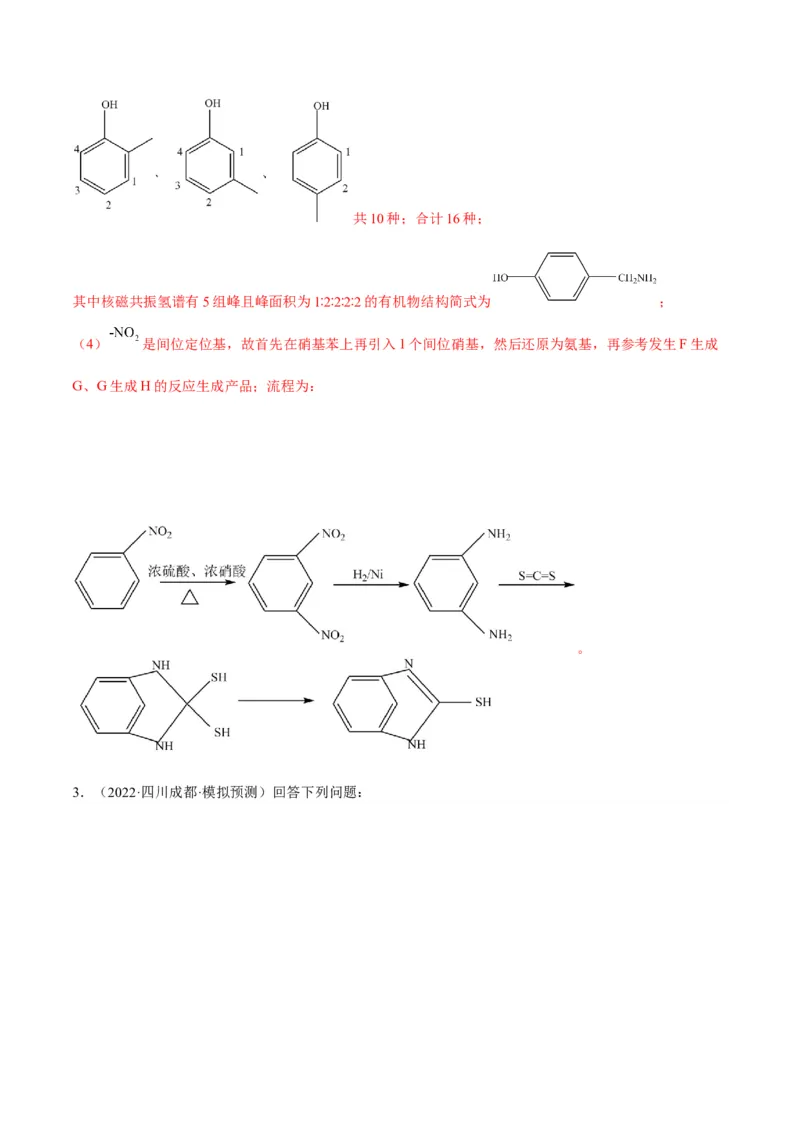
(4)
【解析】由流程可知, 发生取代反应在对位引入硝基得到B,B和氢气发生还原反应生
成C,C发生已知②的反应生成D: ;D首先和硝酸发生取代反应引入硝基生成, 和氢氧化钠发生水解反应生成E: ;E还原将硝基转化
为氨基得到F,F和CS 生成G、G生成H;
2
(1)D为 ,D中所含官能团的名称为醚键、酰胺基;
(2) 的第二步反应为 和氢氧化钠发生水解反应生成E,反应为:
+NaOH +CH COONa;
3
(3)有机物C的同分异构体满足下列条件:
①分子除苯环外不再含其他环②与 溶液发生显色反应,则含有酚羟基;
若除酚羟基外,还含有1个基团,则为-NHCH 或-CHNH ,各有邻间对3种,共6种;
3 2 2
若除酚羟基外,还含有2个基团,则为-CH、-NH ,首先安排甲基再安排氨基,则有:
3 2共10种;合计16种;
其中核磁共振氢谱有5组峰且峰面积为1∶2∶2∶2∶2的有机物结构简式为 ;
(4) 是间位定位基,故首先在硝基苯上再引入1个间位硝基,然后还原为氨基,再参考发生F生成
G、G生成H的反应生成产品;流程为:
。
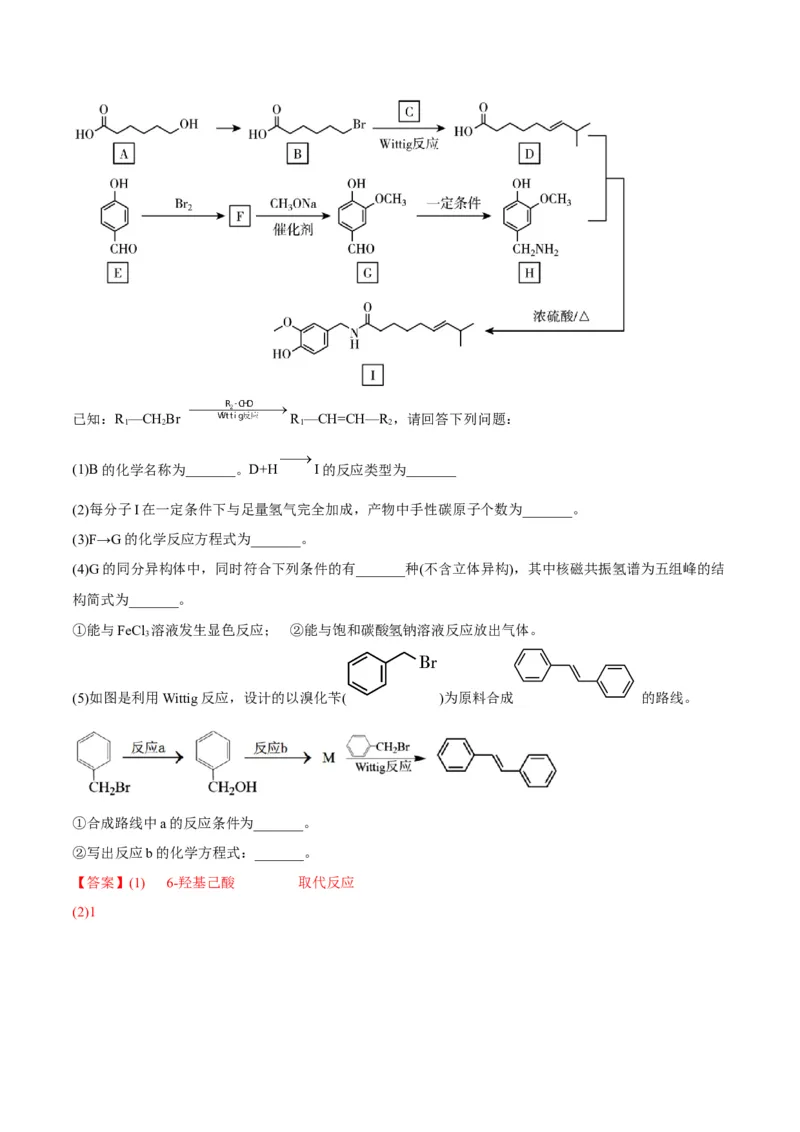
3.(2022·四川成都·模拟预测)回答下列问题:已知:R —CHBr R —CH=CH—R ,请回答下列问题:
1 2 1 2
(1)B的化学名称为_______。D+H I的反应类型为_______
(2)每分子I在一定条件下与足量氢气完全加成,产物中手性碳原子个数为_______。
(3)F→G的化学反应方程式为_______。
(4)G的同分异构体中,同时符合下列条件的有_______种(不含立体异构),其中核磁共振氢谱为五组峰的结
构简式为_______。
①能与FeCl 溶液发生显色反应; ②能与饱和碳酸氢钠溶液反应放出气体。
3
(5)如图是利用Wittig反应,设计的以溴化苄( )为原料合成 的路线。
①合成路线中a的反应条件为_______。
②写出反应b的化学方程式:_______。
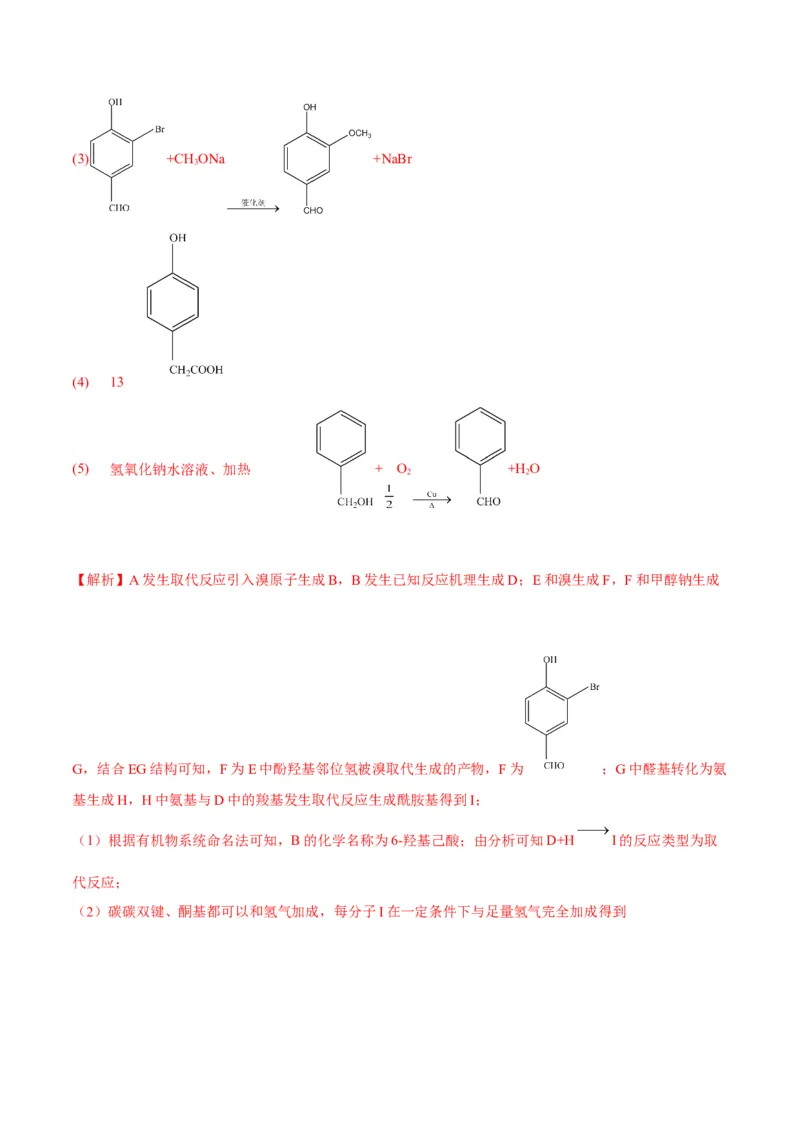
【答案】(1) 6-羟基己酸 取代反应
(2)1(3) +CH ONa +NaBr
3
(4) 13
(5) 氢氧化钠水溶液、加热 + O +H O
2 2
【解析】A发生取代反应引入溴原子生成B,B发生已知反应机理生成D;E和溴生成F,F和甲醇钠生成
G,结合EG结构可知,F为E中酚羟基邻位氢被溴取代生成的产物,F为 ;G中醛基转化为氨
基生成H,H中氨基与D中的羧基发生取代反应生成酰胺基得到I;
(1)根据有机物系统命名法可知,B的化学名称为6-羟基己酸;由分析可知D+H I的反应类型为取
代反应;
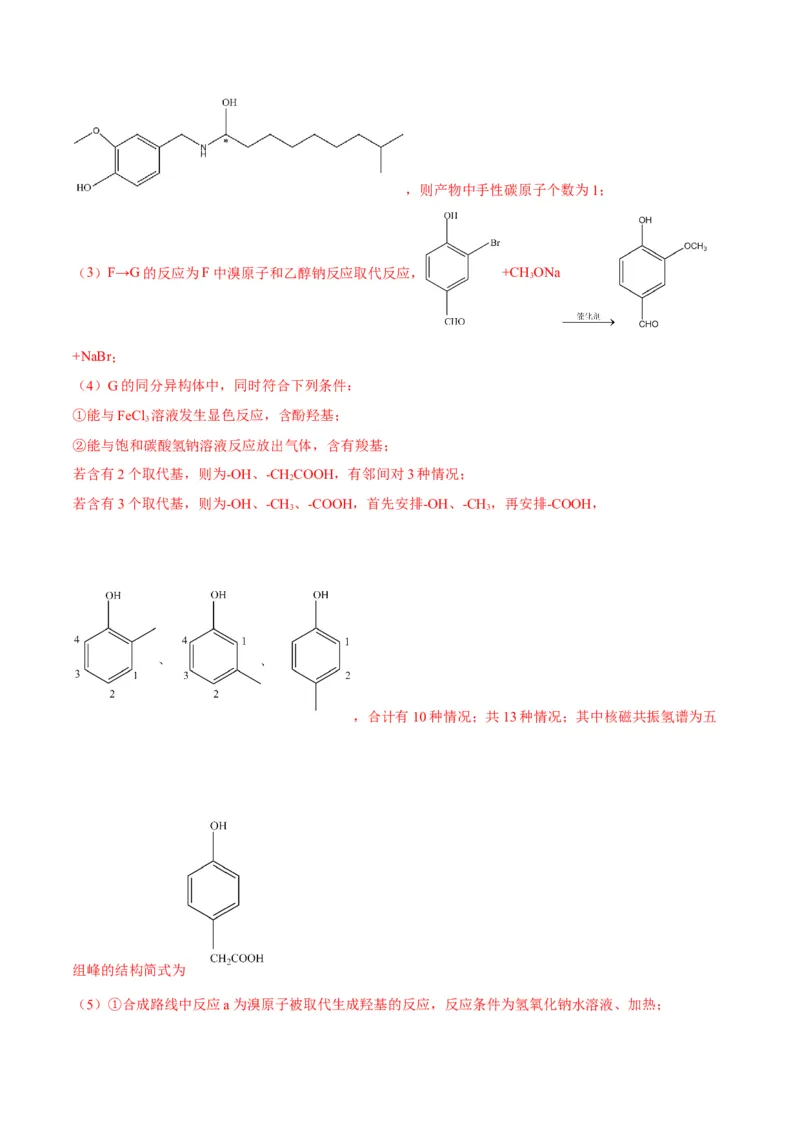
(2)碳碳双键、酮基都可以和氢气加成,每分子I在一定条件下与足量氢气完全加成得到,则产物中手性碳原子个数为1;
(3)F→G的反应为F中溴原子和乙醇钠反应取代反应, +CH ONa
3
+NaBr;
(4)G的同分异构体中,同时符合下列条件:
①能与FeCl 溶液发生显色反应,含酚羟基;
3
②能与饱和碳酸氢钠溶液反应放出气体,含有羧基;
若含有2个取代基,则为-OH、-CHCOOH,有邻间对3种情况;
2
若含有3个取代基,则为-OH、-CH、-COOH,首先安排-OH、-CH,再安排-COOH,
3 3
,合计有10种情况;共13种情况;其中核磁共振氢谱为五
组峰的结构简式为
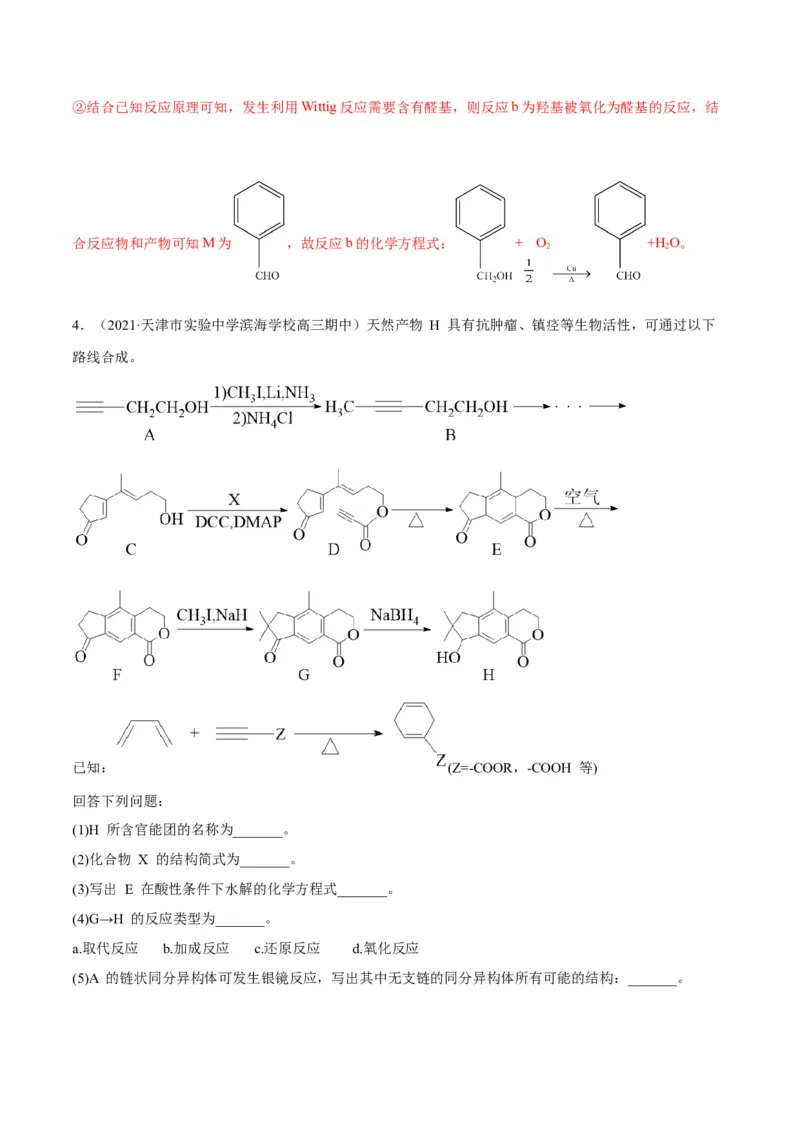
(5)①合成路线中反应a为溴原子被取代生成羟基的反应,反应条件为氢氧化钠水溶液、加热;②结合已知反应原理可知,发生利用Wittig反应需要含有醛基,则反应b为羟基被氧化为醛基的反应,结
合反应物和产物可知M为 ,故反应b的化学方程式: + O +H O。
2 2
4.(2021·天津市实验中学滨海学校高三期中)天然产物 H 具有抗肿瘤、镇痉等生物活性,可通过以下
路线合成。
已知: (Z=-COOR,-COOH 等)
回答下列问题:
(1)H 所含官能团的名称为_______。
(2)化合物 X 的结构简式为_______。
(3)写出 E 在酸性条件下水解的化学方程式_______。
(4)G→H 的反应类型为_______。
a.取代反应 b.加成反应 c.还原反应 d.氧化反应
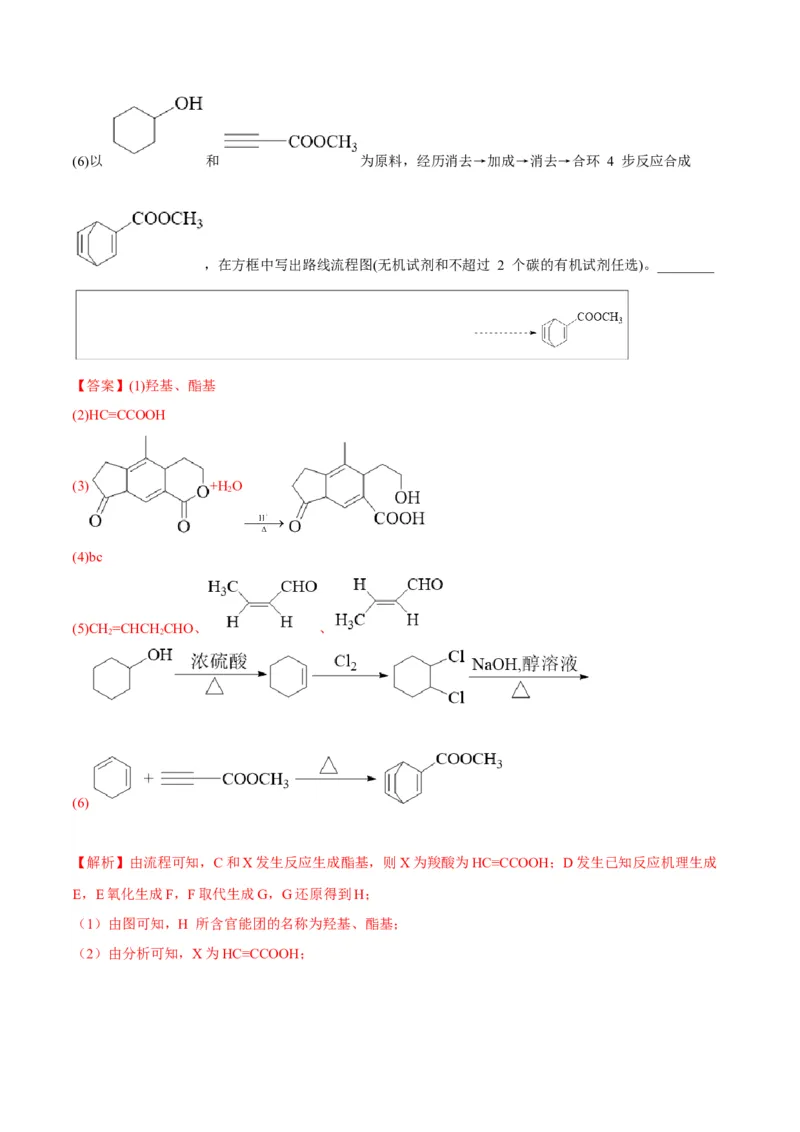
(5)A 的链状同分异构体可发生银镜反应,写出其中无支链的同分异构体所有可能的结构:_______。(6)以 和 为原料,经历消去→加成→消去→合环 4 步反应合成
,在方框中写出路线流程图(无机试剂和不超过 2 个碳的有机试剂任选)。________
【答案】(1)羟基、酯基
(2)HC≡CCOOH
(3) +H O
2
(4)bc
(5)CH =CHCHCHO、 、
2 2
(6)
【解析】由流程可知,C和X发生反应生成酯基,则X为羧酸为HC≡CCOOH;D发生已知反应机理生成
E,E氧化生成F,F取代生成G,G还原得到H;
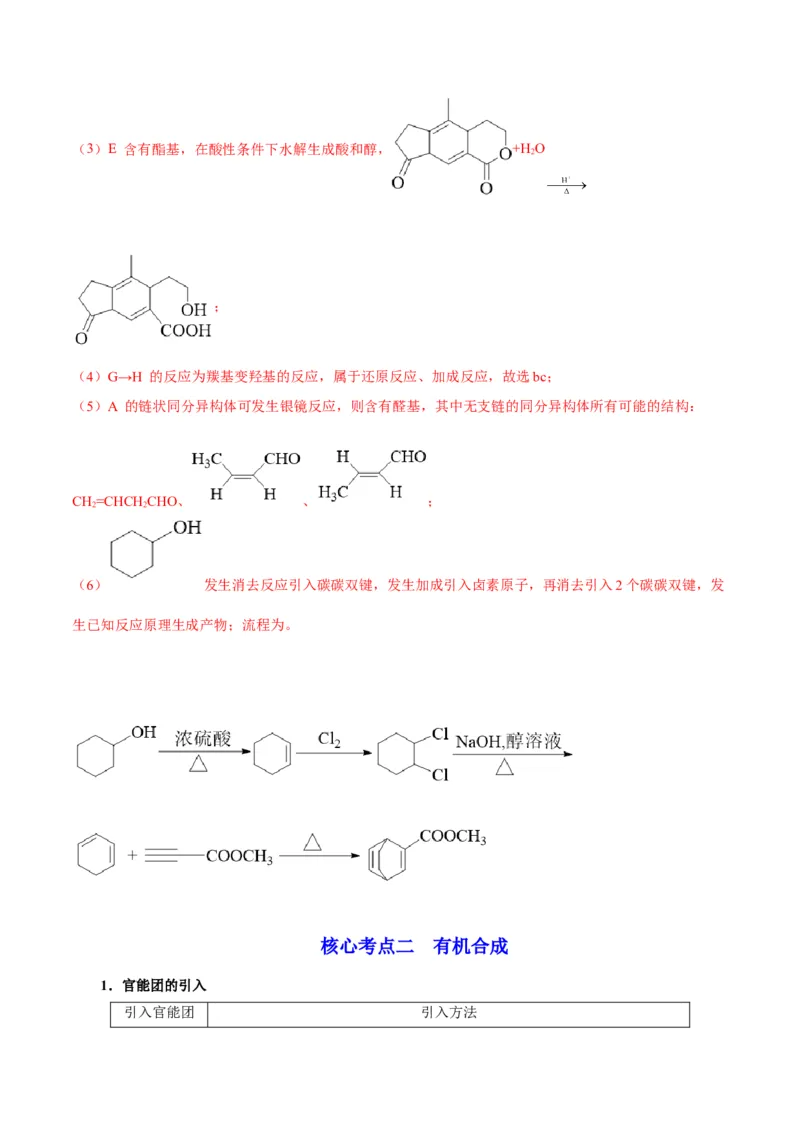
(1)由图可知,H 所含官能团的名称为羟基、酯基;
(2)由分析可知,X为HC≡CCOOH;(3)E 含有酯基,在酸性条件下水解生成酸和醇, +H O
2
;
(4)G→H 的反应为羰基变羟基的反应,属于还原反应、加成反应,故选bc;
(5)A 的链状同分异构体可发生银镜反应,则含有醛基,其中无支链的同分异构体所有可能的结构:
CH=CHCHCHO、 、 ;
2 2
(6) 发生消去反应引入碳碳双键,发生加成引入卤素原子,再消去引入2个碳碳双键,发
生已知反应原理生成产物;流程为。
核心考点二 有机合成
1.官能团的引入
引入官能团 引入方法卤素原子 ①烃、酚的取代;②不饱和烃与HX、X 的加成;③醇与氢卤酸(HX)取代
2
①烯烃与水加成;②醛、酮与氢气加成;
羟基
③卤代烃在碱性条件下水解;④酯的水解;⑤葡萄糖发酵产生乙醇
碳碳双键 ①某些醇或卤代烃的消去;②炔烃不完全加成;③烷烃裂化
①醇的催化氧化;②连在同一个碳上的两个卤素原子水解;③含碳碳三键的
碳氧双键
物质与水加成
羧基 ①醛基氧化;②酯、肽、蛋白质、羧酸盐的水解
其中苯环上引入基团的方法:
2.官能团的消除
(1)通过加成消除不饱和键。
如CH===CH +H――→CHCH。
2 2 2 3 3
(2)通过消去或氧化或酯化消除羟基(—OH)。
如CHCHOH――→CH===CH ↑+HO;
3 2 2 2 2
2CHCHOH+O――→2CHCHO+2HO。
3 2 2 3 2
(3)通过加成或氧化等消除醛基(—CHO)。
如2CHCHO+O――→2CHCOOH;
3 2 3
CHCHO+H――→CHCHOH。
3 2 3 2
(4)通过水解反应消除—COO—。
如CHCOOC H+HO―→CHCOOH+C HOH。
3 2 5 2 3 2 5
3.官能团的衍变
根据合成需要(有时题目信息中会明示某些衍变途径),可进行有机物的官能团衍变,以使中间产物向
产物递进。常见的有三种方式:
(1)利用官能团的衍变关系进行衍变。
如RCHOH→醛→羧酸。
2
(2)通过某种化学途径使一个官能团变为两个。
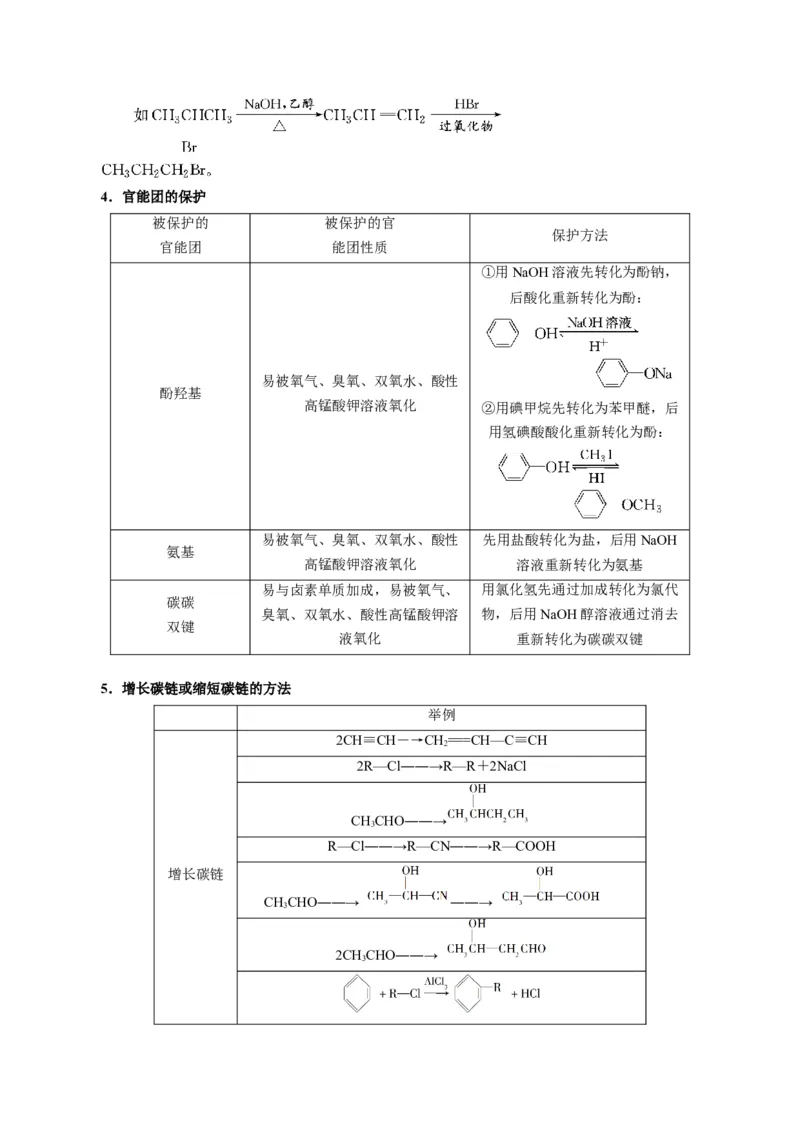
(3)通过某种手段,改变官能团的位置。4.官能团的保护
被保护的 被保护的官
保护方法
官能团 能团性质
①用NaOH溶液先转化为酚钠,
后酸化重新转化为酚:
易被氧气、臭氧、双氧水、酸性
酚羟基
高锰酸钾溶液氧化 ②用碘甲烷先转化为苯甲醚,后
用氢碘酸酸化重新转化为酚:
易被氧气、臭氧、双氧水、酸性 先用盐酸转化为盐,后用NaOH
氨基
高锰酸钾溶液氧化 溶液重新转化为氨基
易与卤素单质加成,易被氧气、 用氯化氢先通过加成转化为氯代
碳碳
臭氧、双氧水、酸性高锰酸钾溶 物,后用NaOH醇溶液通过消去
双键
液氧化 重新转化为碳碳双键
5.增长碳链或缩短碳链的方法
举例
2CH≡CH―→CH===CH—C≡CH
2
2R—Cl――→R—R+2NaCl
CHCHO――→
3
R—Cl――→R—CN――→R—COOH
增长碳链
CHCHO――→ ――→
3
2CHCHO――→
3nCH===CH ――→ ;
2 2
nCH==CH—CH==CH ――→
2 2
+(n-1)H O
2
缩短碳链 +NaOH――→RH+NaCO
2 3
R —CH==CH—R ――→R CHO+R CHO
1 2 1 2
6.常见有机物转化应用举例
(1)
(2)
(3)
(4)
7.有机合成路线设计的几种常见类型
根据目标分子与原料分子在碳骨架和官能团两方面变化的特点,我们将合成路线的设计分为
(1)以熟悉官能团的转化为主型
例如:请设计以 CH==CHCH 为主要原料(无机试剂任选)制备CHCH(OH)COOH的合成路线流程图
2 3 3(须注明反应条件)。
(2)以分子碳骨架变化为主型
例如:请以苯甲醛和乙醇为原料设计苯乙酸乙酯( )的合成路线流程图(须注明
反应条件)。
提示:R—Br+NaCN―→R—CN+NaBr
(3)陌生官能团兼有碳骨架显著变化型(多为考查的重点)
要注意模仿题干中的变化,找到相似点,完成陌生官能团及骨架的变化。例如:
8.有机合成路线的设计方法
(1)正推法
即从某种原料分子开始,对比目标分子与原料分子的结构(碳骨架及官能团),对该原料分子进行碳骨
架的构建和官能团的引入(或者官能团的转化),从而设计出合理的合成路线,其思维程序为
⇨……⇨⇨
如利用乙烯为原料合成乙酸乙酯,可采用正推法:
(2)逆推法
即从目标分子着手,分析目标分子的结构,然后由目标分子逆推出原料分子,并进行合成路线的设计,
其思维程序为⇨……⇨⇨
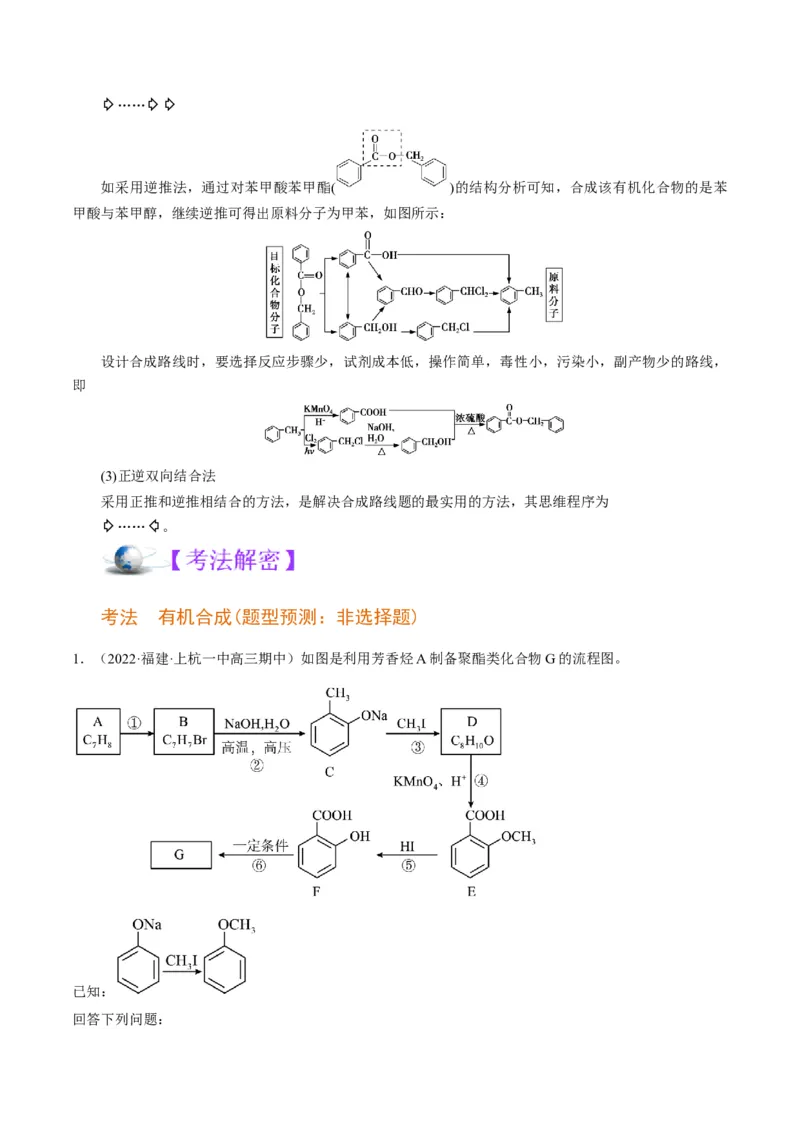
如采用逆推法,通过对苯甲酸苯甲酯( )的结构分析可知,合成该有机化合物的是苯
甲酸与苯甲醇,继续逆推可得出原料分子为甲苯,如图所示:
设计合成路线时,要选择反应步骤少,试剂成本低,操作简单,毒性小,污染小,副产物少的路线,
即
(3)正逆双向结合法
采用正推和逆推相结合的方法,是解决合成路线题的最实用的方法,其思维程序为
⇨……⇦。
考法 有机合成(题型预测:非选择题)
1.(2022·福建·上杭一中高三期中)如图是利用芳香烃A制备聚酯类化合物G的流程图。
已知:
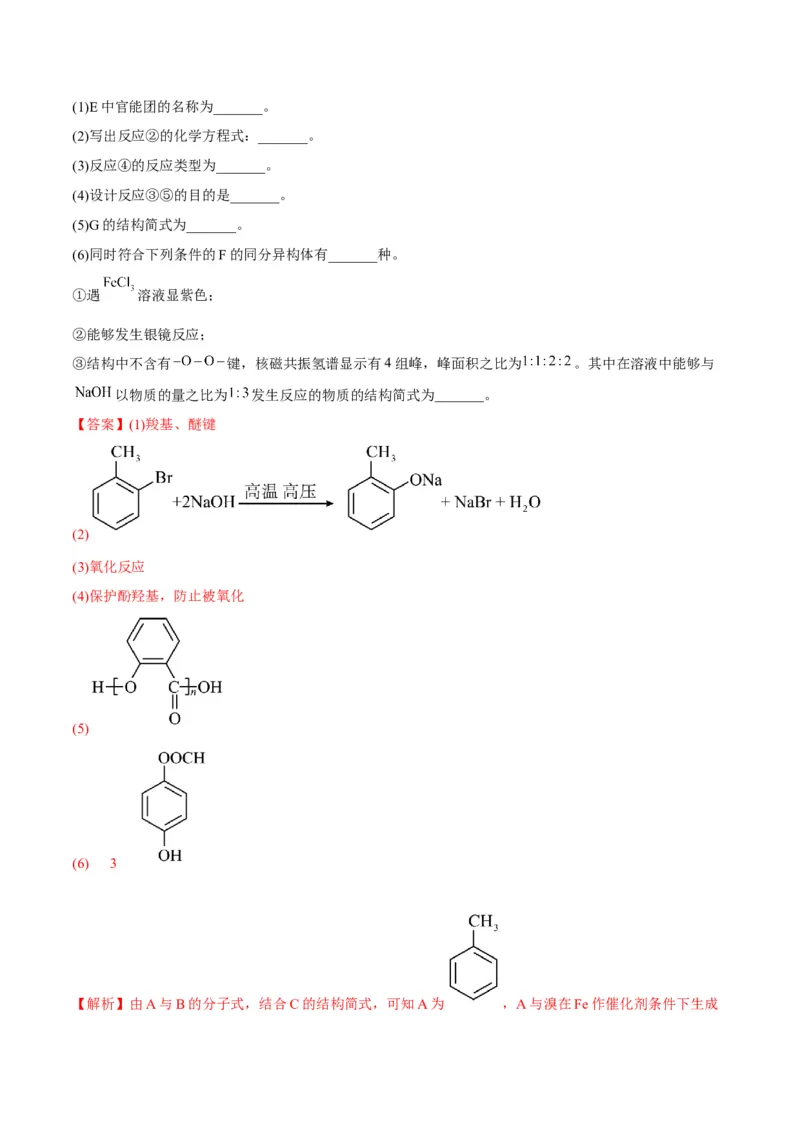
回答下列问题:(1)E中官能团的名称为_______。
(2)写出反应②的化学方程式:_______。
(3)反应④的反应类型为_______。
(4)设计反应③⑤的目的是_______。
(5)G的结构简式为_______。
(6)同时符合下列条件的F的同分异构体有_______种。
①遇 溶液显紫色;
②能够发生银镜反应;
③结构中不含有 键,核磁共振氢谱显示有4组峰,峰面积之比为 。其中在溶液中能够与
以物质的量之比为 发生反应的物质的结构简式为_______。
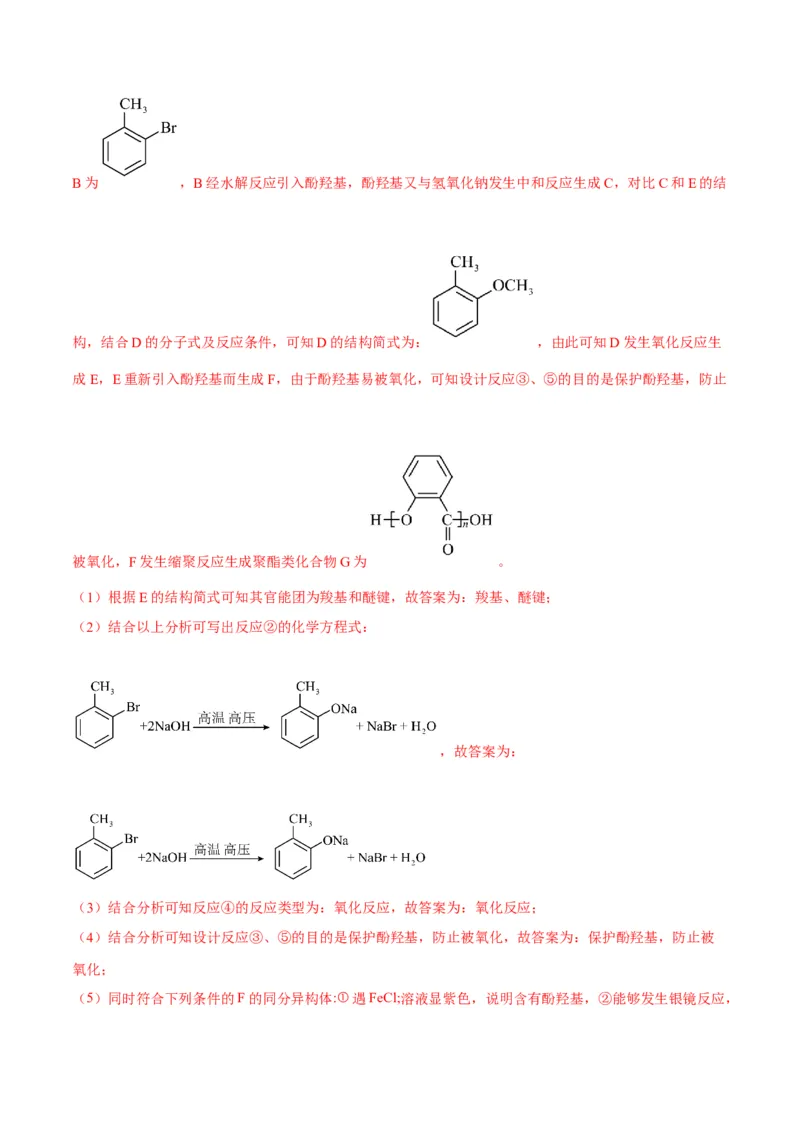
【答案】(1)羧基、醚键
(2)
(3)氧化反应
(4)保护酚羟基,防止被氧化
(5)
(6) 3
【解析】由A与B的分子式,结合C的结构简式,可知A为 ,A与溴在Fe作催化剂条件下生成B为 ,B经水解反应引入酚羟基,酚羟基又与氢氧化钠发生中和反应生成C,对比C和E的结
构,结合D的分子式及反应条件,可知D的结构简式为: ,由此可知D发生氧化反应生
成E,E重新引入酚羟基而生成F,由于酚羟基易被氧化,可知设计反应③、⑤的目的是保护酚羟基,防止
被氧化,F发生缩聚反应生成聚酯类化合物G为 。
(1)根据E的结构简式可知其官能团为羧基和醚键,故答案为:羧基、醚键;
(2)结合以上分析可写出反应②的化学方程式:
,故答案为:
(3)结合分析可知反应④的反应类型为:氧化反应,故答案为:氧化反应;
(4)结合分析可知设计反应③、⑤的目的是保护酚羟基,防止被氧化,故答案为:保护酚羟基,防止被
氧化;
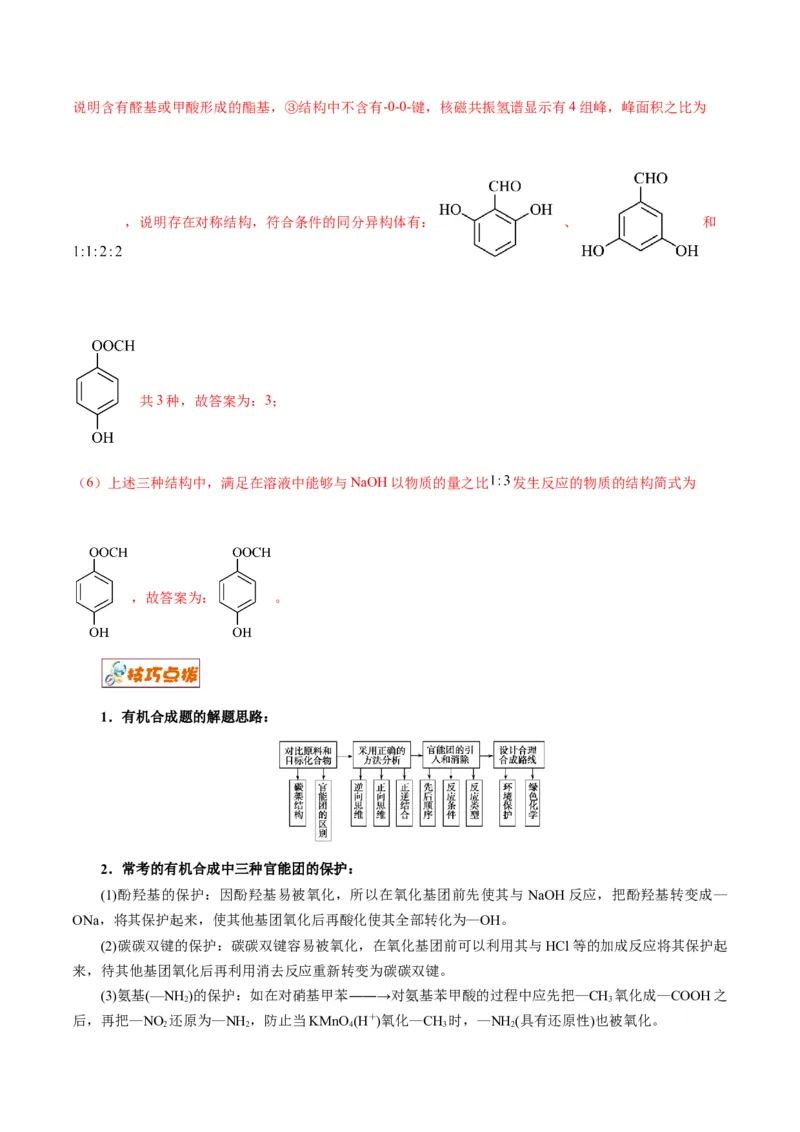
(5)同时符合下列条件的F的同分异构体:①遇FeCl;溶液显紫色,说明含有酚羟基,②能够发生银镜反应,说明含有醛基或甲酸形成的酯基,③结构中不含有-0-0-键,核磁共振氢谱显示有4组峰,峰面积之比为
,说明存在对称结构,符合条件的同分异构体有: 、 和
共3种,故答案为:3;
(6)上述三种结构中,满足在溶液中能够与NaOH以物质的量之比 发生反应的物质的结构简式为
,故答案为: 。
1.有机合成题的解题思路:
2.常考的有机合成中三种官能团的保护:
(1)酚羟基的保护:因酚羟基易被氧化,所以在氧化基团前先使其与 NaOH反应,把酚羟基转变成—
ONa,将其保护起来,使其他基团氧化后再酸化使其全部转化为—OH。
(2)碳碳双键的保护:碳碳双键容易被氧化,在氧化基团前可以利用其与HCl等的加成反应将其保护起
来,待其他基团氧化后再利用消去反应重新转变为碳碳双键。
(3)氨基(—NH )的保护:如在对硝基甲苯――→对氨基苯甲酸的过程中应先把—CH 氧化成—COOH之
2 3
后,再把—NO 还原为—NH ,防止当KMnO (H+)氧化—CH 时,—NH (具有还原性)也被氧化。
2 2 4 3 2变式一 羟醛缩合
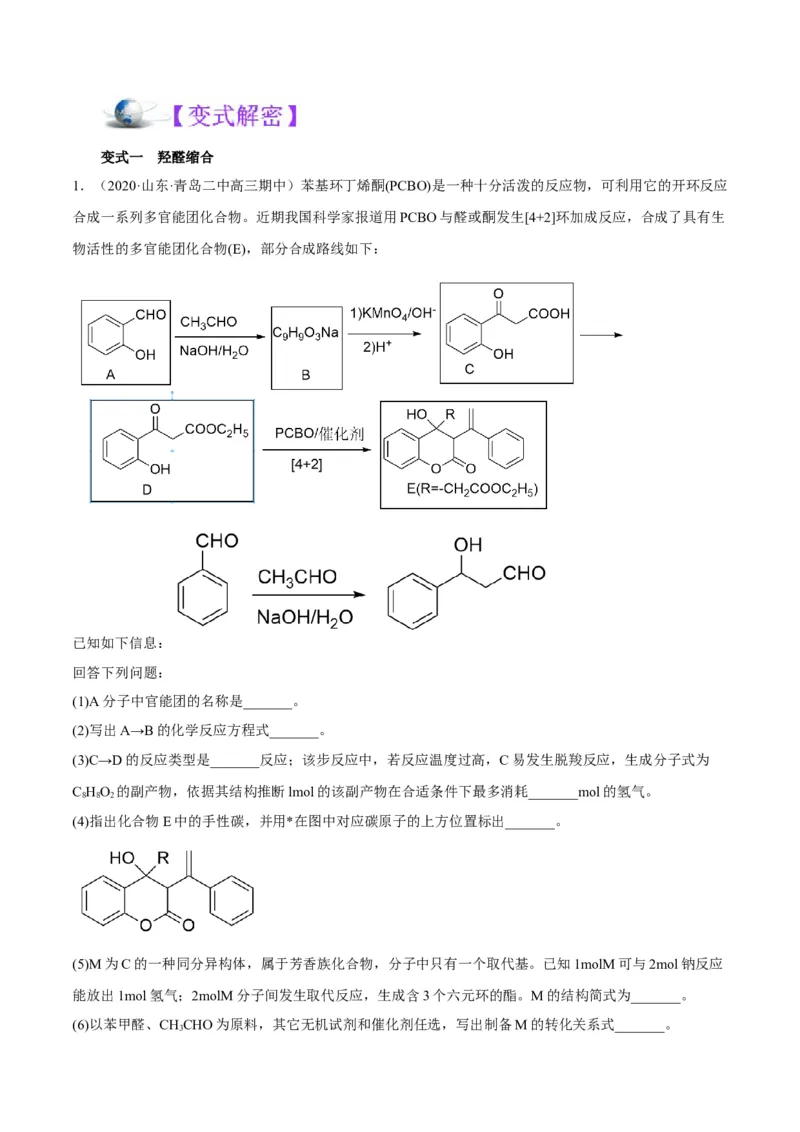
1.(2020·山东·青岛二中高三期中)苯基环丁烯酮(PCBO)是一种十分活泼的反应物,可利用它的开环反应
合成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生
物活性的多官能团化合物(E),部分合成路线如下:
已知如下信息:
回答下列问题:
(1)A分子中官能团的名称是_______。
(2)写出A→B的化学反应方程式_______。
(3)C→D的反应类型是_______反应;该步反应中,若反应温度过高,C易发生脱羧反应,生成分子式为
C HO 的副产物,依据其结构推断lmol的该副产物在合适条件下最多消耗_______mol的氢气。
8 8 2
(4)指出化合物E中的手性碳,并用*在图中对应碳原子的上方位置标出_______。
(5)M为C的一种同分异构体,属于芳香族化合物,分子中只有一个取代基。已知1molM可与2mol钠反应
能放出1mol氢气;2molM分子间发生取代反应,生成含3个六元环的酯。M的结构简式为_______。
(6)以苯甲醛、CHCHO为原料,其它无机试剂和催化剂任选,写出制备M的转化关系式_______。
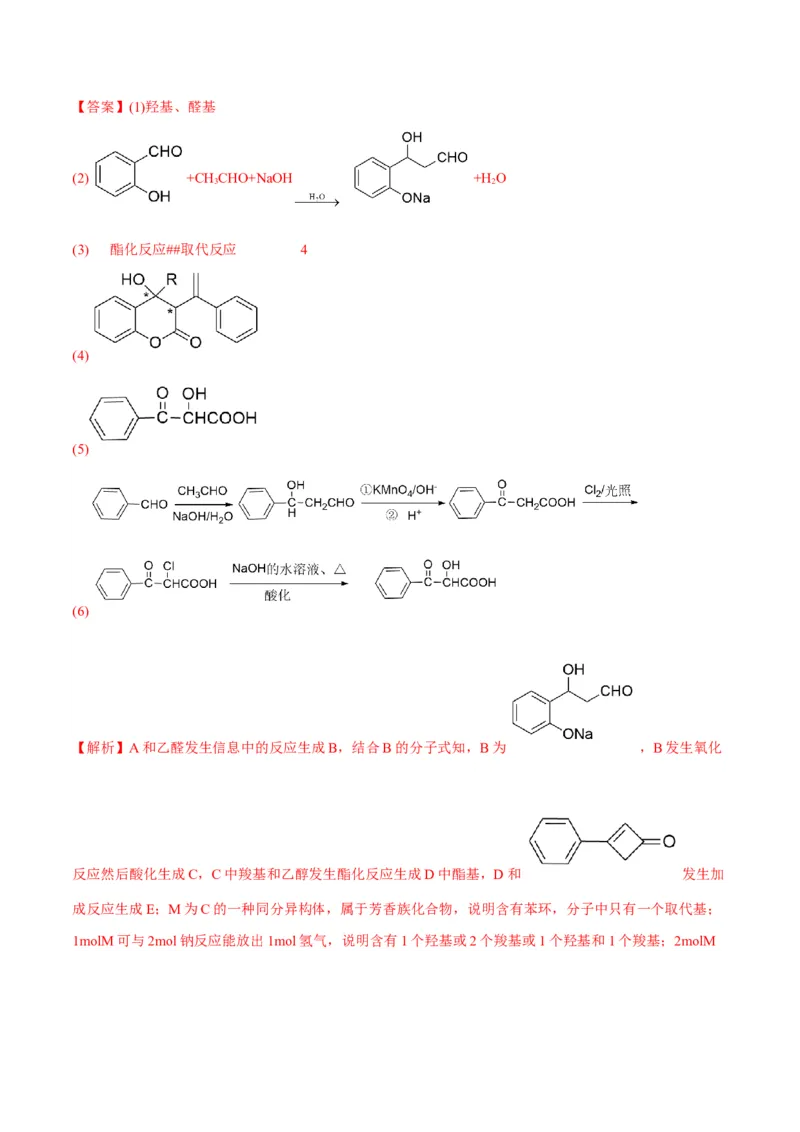
3【答案】(1)羟基、醛基
(2) +CH CHO+NaOH +H O
3 2
(3) 酯化反应##取代反应 4
(4)
(5)
(6)
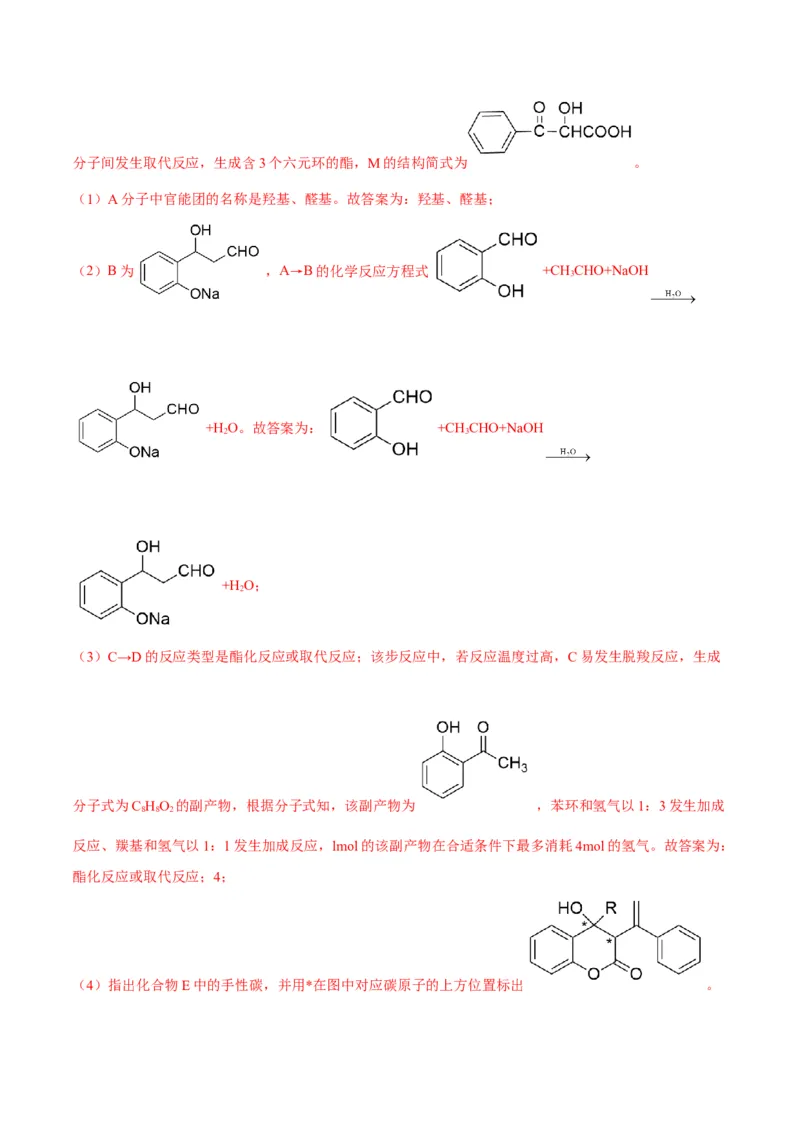
【解析】A和乙醛发生信息中的反应生成B,结合B的分子式知,B为 ,B发生氧化
反应然后酸化生成C,C中羧基和乙醇发生酯化反应生成D中酯基,D和 发生加
成反应生成E;M为C的一种同分异构体,属于芳香族化合物,说明含有苯环,分子中只有一个取代基;
1molM可与2mol钠反应能放出1mol氢气,说明含有1个羟基或2个羧基或1个羟基和1个羧基;2molM分子间发生取代反应,生成含3个六元环的酯,M的结构简式为 。
(1)A分子中官能团的名称是羟基、醛基。故答案为:羟基、醛基;
(2)B为 ,A→B的化学反应方程式 +CH CHO+NaOH
3
+H O。故答案为: +CH CHO+NaOH
2 3
+H O;
2
(3)C→D的反应类型是酯化反应或取代反应;该步反应中,若反应温度过高,C易发生脱羧反应,生成
分子式为C HO 的副产物,根据分子式知,该副产物为 ,苯环和氢气以1:3发生加成
8 8 2
反应、羰基和氢气以1:1发生加成反应,lmol的该副产物在合适条件下最多消耗4mol的氢气。故答案为:
酯化反应或取代反应;4;
(4)指出化合物E中的手性碳,并用*在图中对应碳原子的上方位置标出 。故答案为: ;
(5)M为C的一种同分异构体,属于芳香族化合物,分子中只有一个取代基。已知1molM可与2mol钠
反应能放出1mol氢气;2molM分子间发生取代反应,生成含3个六元环的酯。M的结构简式为
。故答案为: ;
(6)以苯甲醛、CHCHO为原料制备 ,苯甲醛和乙醛发生信息中的反应生成
3
, 发生发生氧化反应生成 ,
和氯气发生取代反应生成 ,
发生水解反应生成 ,合成路线为,故答案为:
。
变式二 成环合成
2.(2022·辽宁大连·高三期中)A(C H)是基本有机化工原料。由A制备聚合物C和
3 6
的合成路线(部分反应条件略去)如图所示。
已知: ; 。
请回答下列问题:
(1)A的名称是_______。
(2)B的分子式是_______;B中含有的官能团的名称是_______(写名称)。
(3)C的结构简式为_______,A→D的反应类型为_______。
(4)E→F的化学方程式为_______。(5) 中最多有_______个原子共平面。
(6)B的同分异构体中,与B具有相同的官能团且能发生银镜反应的共有_______种;其中核磁共振氢谱为3
组峰,且峰面积之比为6∶1∶1的是_______(写结构简式)。
【答案】(1)丙烯
(2) 碳碳双键、酯基
(3) 取代反应(或水解反应)
(4)
(5)10
(6) 8
【解析】 为 的加聚产物,则B为 ,其分子式
,其官能团为碳碳双键、酯基。 水解(取代反应)后酸化生成聚合物C,故C为
。根据已知信息及 ,逆推可得G为
,由G逆推可知F为 ,由已知反应及E→F的反应,可推
知E为 ,则D为 。结合A分别生成B、D的反应条件可推知,A为。
(1)根据分析可知,A是 ,名称是丙烯,故答案为:丙烯。
(2)根据分析可知,B是 ,B的分子式是 ,含有的官能团的名称是碳碳双键、
酯基,故答案为: ;碳碳双键、酯基。
(3)根据分析可知,C的结构简式为: ,A→D的反应类型为:取代反应(或水解反应),
故答案为: ;取代反应(或水解反应)。
(4)根据分析可知,E→F的化学方程式为:
,故答案为:
。
(5) 该分子中含有10个原子,根据乙烯结构特点,结合碳碳单键可以旋转,可知该分子中10个
原子可能共平面。故答案为:10。
(6)B的结构简式为 ,B的同分异构体中,与B具有相同的官能团且能发生银镜反
应,说明其为含有碳碳双键的甲酸酯,符合条件的同分异构体有
、 、 、 、
、 、 、 ,
所以符合条件的共有8种;其中核磁共振氢谱为3组峰,且峰面积之比为6∶1∶1的是。故答案为:8; 。
变式三碳链增长合成
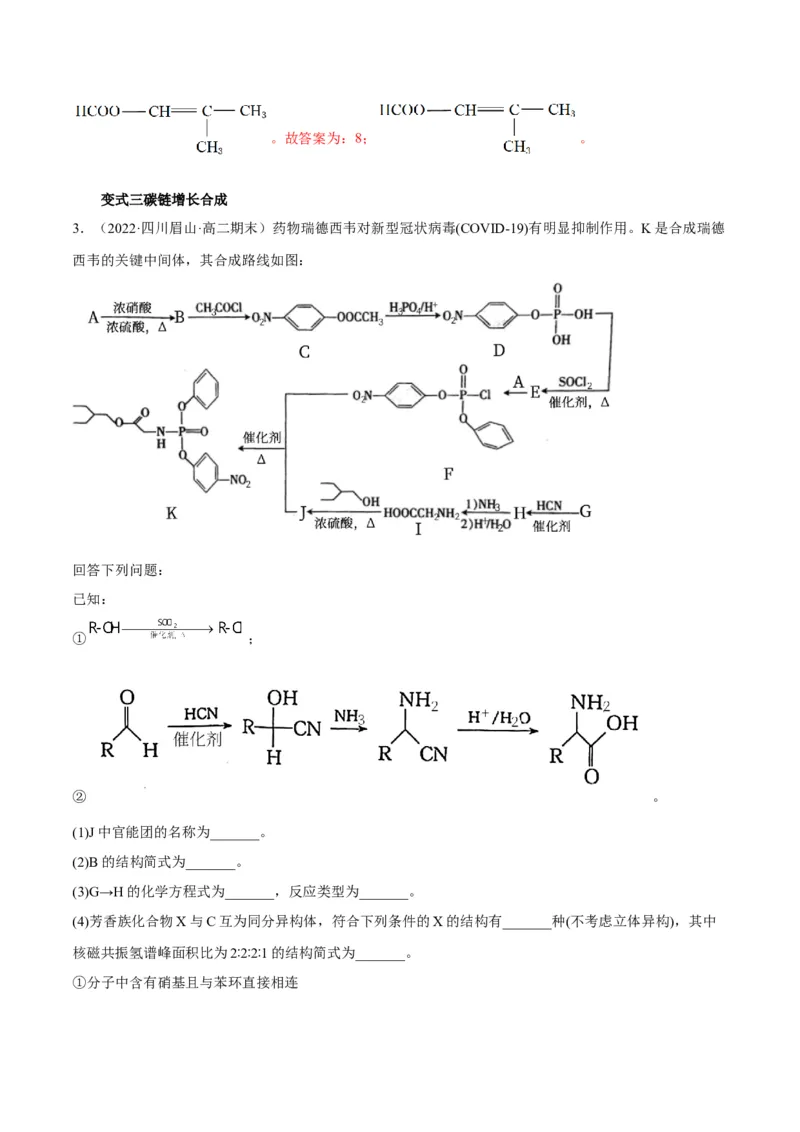
3.(2022·四川眉山·高二期末)药物瑞德西韦对新型冠状病毒(COVID-19)有明显抑制作用。K是合成瑞德
西韦的关键中间体,其合成路线如图:
回答下列问题:
已知:
① ;
② 。
(1)J中官能团的名称为_______。
(2)B的结构简式为_______。
(3)G→H的化学方程式为_______,反应类型为_______。
(4)芳香族化合物X与C互为同分异构体,符合下列条件的X的结构有_______种(不考虑立体异构),其中
核磁共振氢谱峰面积比为2∶2∶2∶1的结构简式为_______。
①分子中含有硝基且与苯环直接相连②能与 溶液发生反应
(5)写出以苯甲醇为原料制备 的合成路线(无机试剂任选)_______。
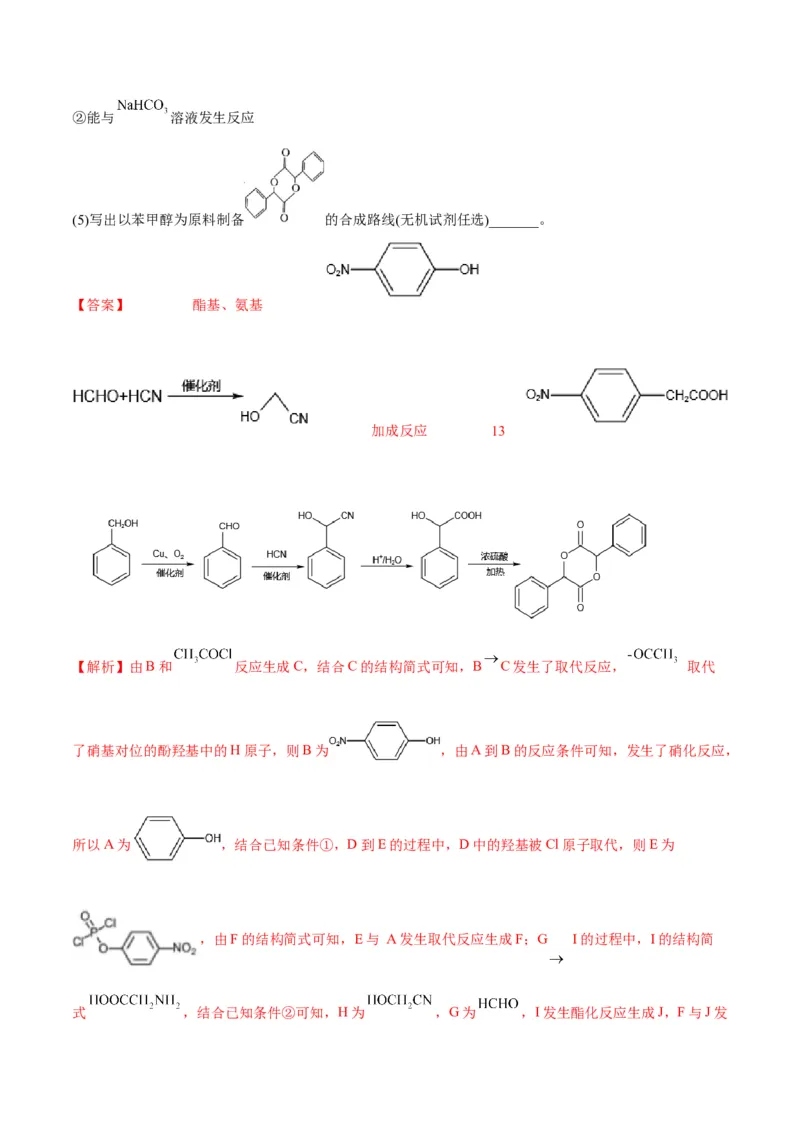
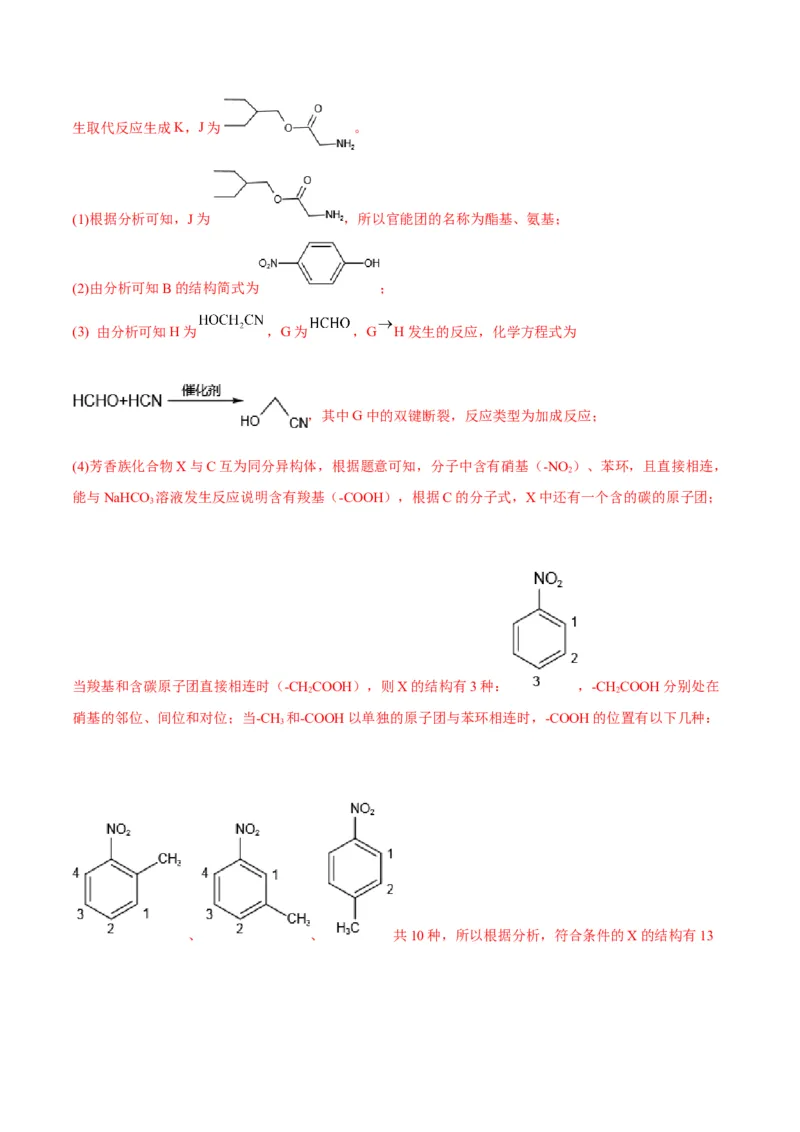
【答案】 酯基、氨基
加成反应 13
【解析】由B和 反应生成C,结合C的结构简式可知,B C发生了取代反应, 取代
了硝基对位的酚羟基中的H原子,则B为 ,由A到B的反应条件可知,发生了硝化反应,
所以A为 ,结合已知条件①,D到E的过程中,D中的羟基被Cl原子取代,则E为
,由F的结构简式可知,E与 A发生取代反应生成F;G I的过程中,I的结构简
式 ,结合已知条件②可知,H为 ,G为 ,I发生酯化反应生成J,F与J发生取代反应生成K,J为 。
(1)根据分析可知,J为 ,所以官能团的名称为酯基、氨基;
(2)由分析可知B的结构简式为 ;
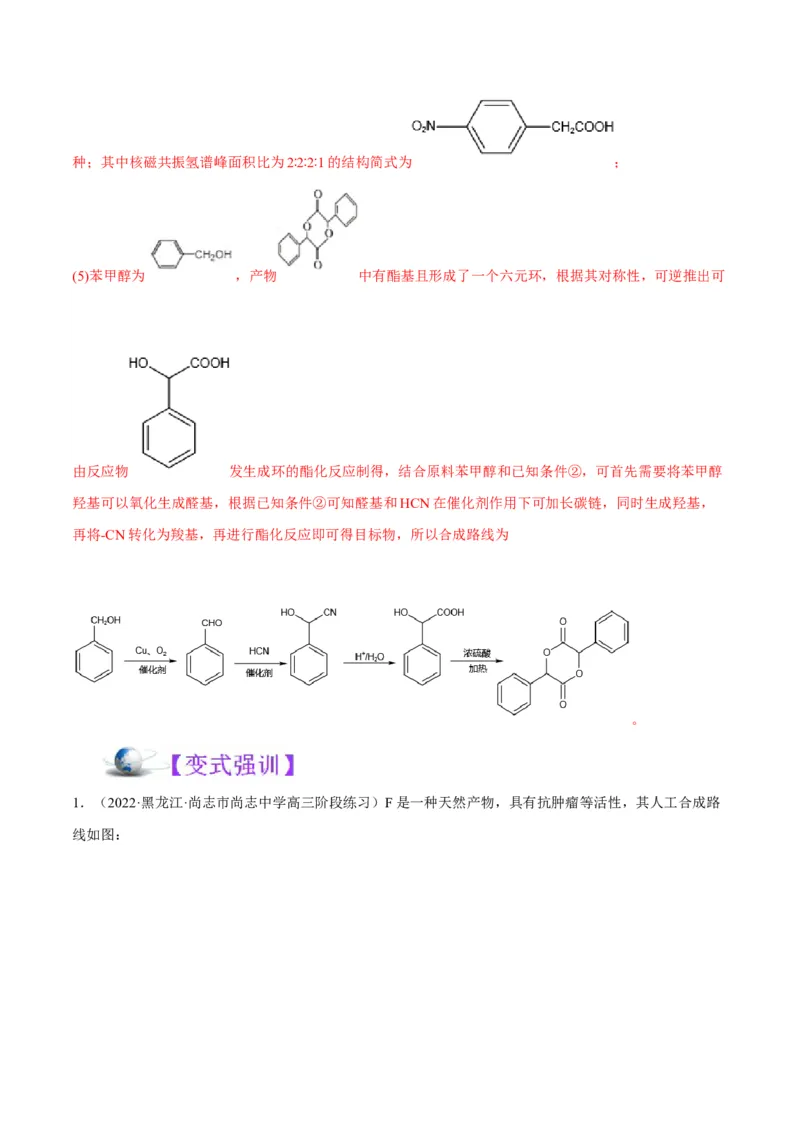
(3) 由分析可知H为 ,G为 ,G H发生的反应,化学方程式为
,其中G中的双键断裂,反应类型为加成反应;
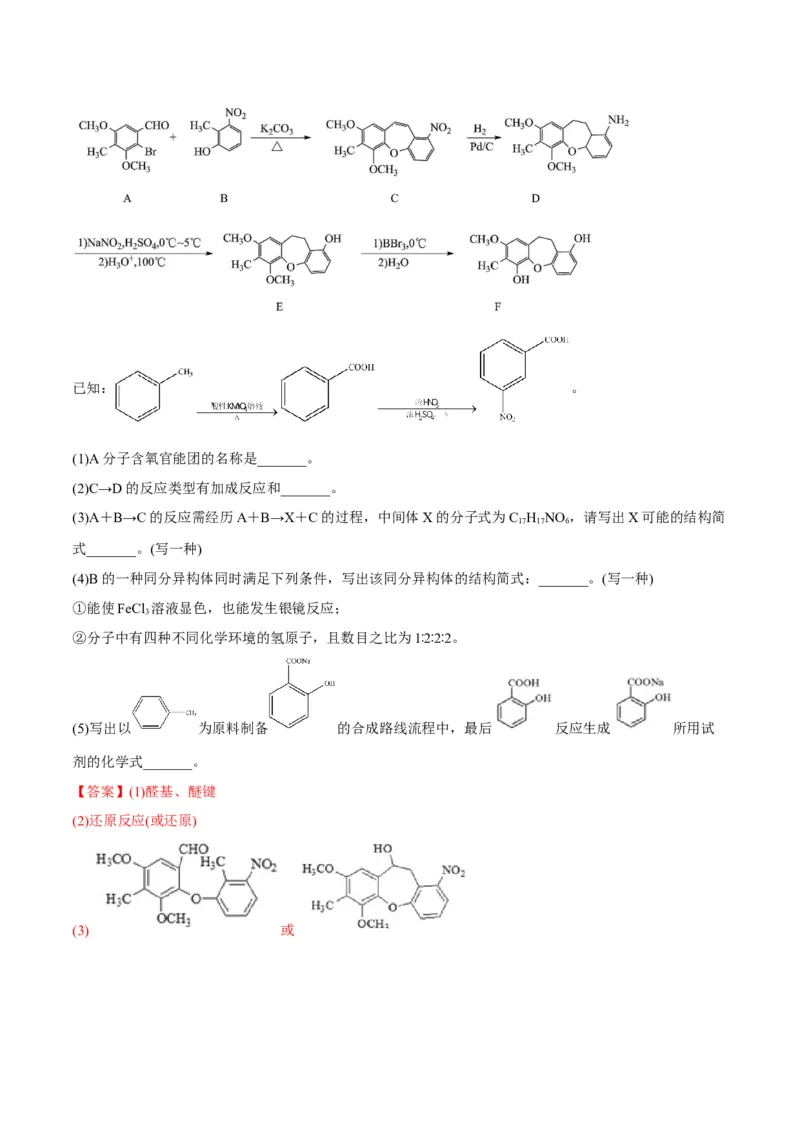
(4)芳香族化合物X与C互为同分异构体,根据题意可知,分子中含有硝基(-NO )、苯环,且直接相连,
2
能与NaHCO 溶液发生反应说明含有羧基(-COOH),根据C的分子式,X中还有一个含的碳的原子团;
3
当羧基和含碳原子团直接相连时(-CHCOOH),则X的结构有3种: ,-CHCOOH分别处在
2 2
硝基的邻位、间位和对位;当-CH 和-COOH以单独的原子团与苯环相连时,-COOH的位置有以下几种:
3
、 、 共10种,所以根据分析,符合条件的X的结构有13种;其中核磁共振氢谱峰面积比为2∶2∶2∶1的结构简式为 ;
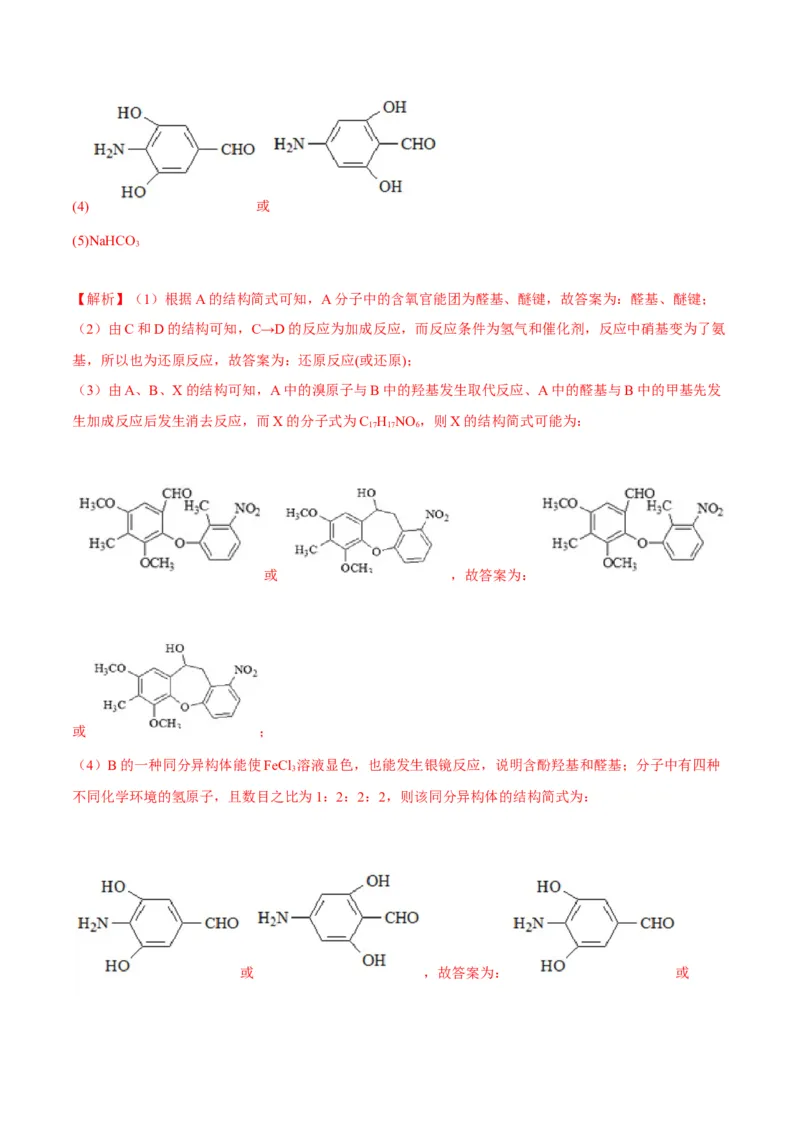
(5)苯甲醇为 ,产物 中有酯基且形成了一个六元环,根据其对称性,可逆推出可
由反应物 发生成环的酯化反应制得,结合原料苯甲醇和已知条件②,可首先需要将苯甲醇
羟基可以氧化生成醛基,根据已知条件②可知醛基和HCN在催化剂作用下可加长碳链,同时生成羟基,
再将-CN转化为羧基,再进行酯化反应即可得目标物,所以合成路线为
。
1.(2022·黑龙江·尚志市尚志中学高三阶段练习)F是一种天然产物,具有抗肿瘤等活性,其人工合成路
线如图:已知: 。
(1)A分子含氧官能团的名称是_______。
(2)C→D的反应类型有加成反应和_______。
(3)A+B→C的反应需经历A+B→X+C的过程,中间体X的分子式为C H NO ,请写出X可能的结构简
17 17 6
式_______。(写一种)
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______。(写一种)
①能使FeCl 溶液显色,也能发生银镜反应;
3
②分子中有四种不同化学环境的氢原子,且数目之比为1∶2∶2∶2。
(5)写出以 为原料制备 的合成路线流程中,最后 反应生成 所用试
剂的化学式_______。
【答案】(1)醛基、醚键
(2)还原反应(或还原)
(3) 或(4) 或
(5)NaHCO
3
【解析】(1)根据A的结构简式可知,A分子中的含氧官能团为醛基、醚键,故答案为:醛基、醚键;
(2)由C和D的结构可知,C→D的反应为加成反应,而反应条件为氢气和催化剂,反应中硝基变为了氨
基,所以也为还原反应,故答案为:还原反应(或还原);
(3)由A、B、X的结构可知,A中的溴原子与B中的羟基发生取代反应、A中的醛基与B中的甲基先发
生加成反应后发生消去反应,而X的分子式为C H NO ,则X的结构简式可能为:
17 17 6
或 ,故答案为:
或 ;
(4)B的一种同分异构体能使FeCl 溶液显色,也能发生银镜反应,说明含酚羟基和醛基;分子中有四种
3
不同化学环境的氢原子,且数目之比为1:2:2:2,则该同分异构体的结构简式为:
或 ,故答案为: 或;
(5) 与碳酸氢钠反应生成 ,即所用试剂为NaHCO ,故答案为:NaHCO 。
3 3
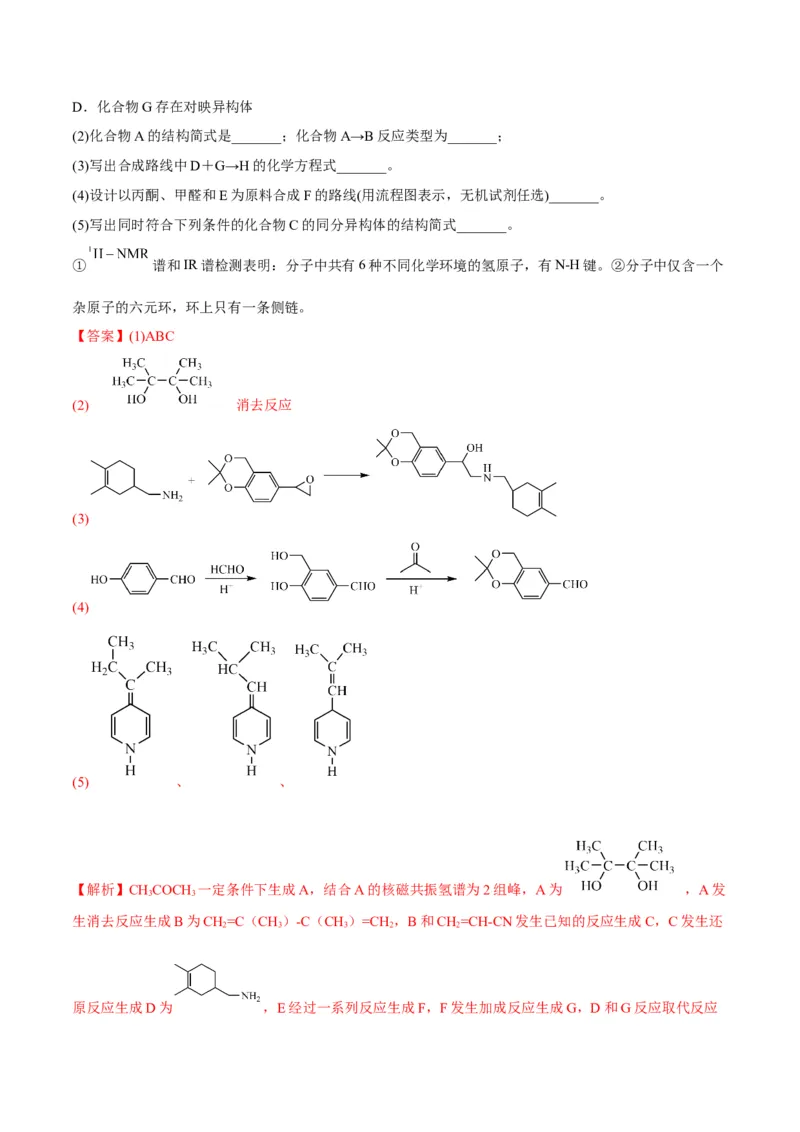
2.(2022·浙江·绍兴市教育教学研究院一模)某研究小组按下列路线合成药物的一个中间体Ⅰ:
已知:
①物质A的核磁共振氢谱只有2个峰;
②
③
请回答:
(1)下列说法不正确的是_______。
A.化合物Ⅰ的分子式是
B.化合物H中的含氧官能团只有羟基
C.1mol化合物E与溴水反应最多消耗2molD.化合物G存在对映异构体
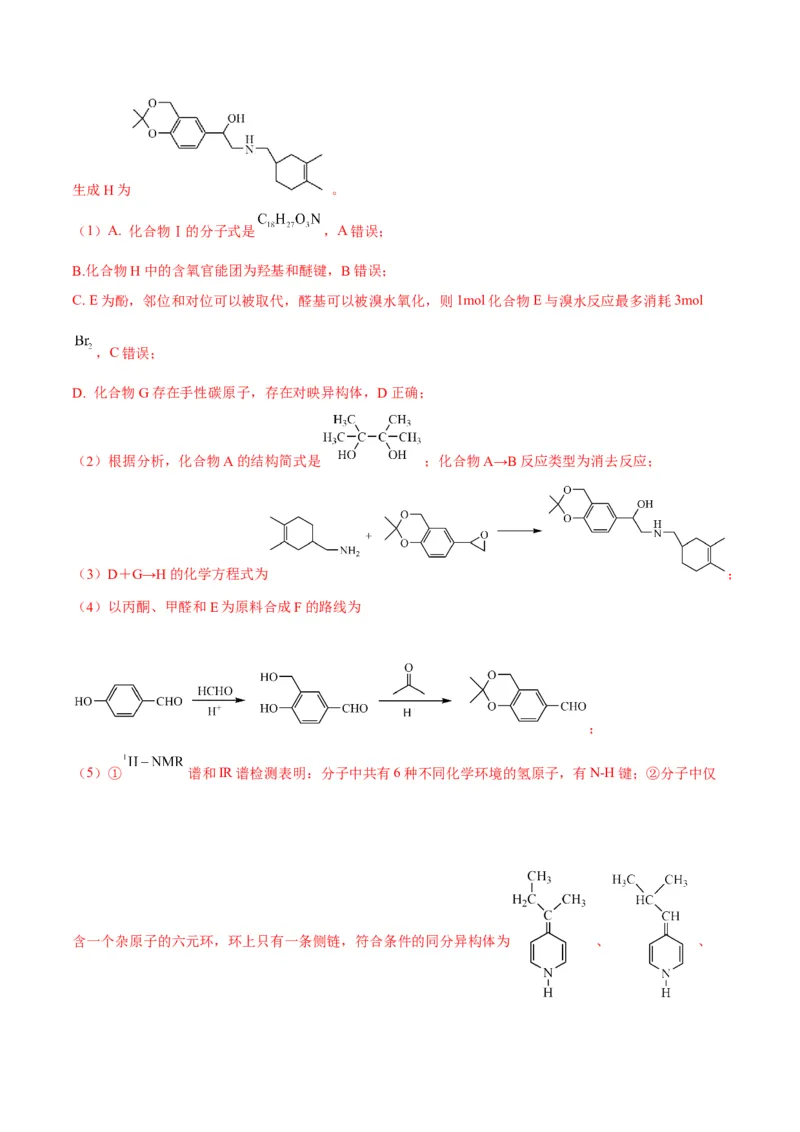
(2)化合物A的结构简式是_______;化合物A→B反应类型为_______;
(3)写出合成路线中D+G→H的化学方程式_______。
(4)设计以丙酮、甲醛和E为原料合成F的路线(用流程图表示,无机试剂任选)_______。
(5)写出同时符合下列条件的化合物C的同分异构体的结构简式_______。
① 谱和IR谱检测表明:分子中共有6种不同化学环境的氢原子,有N-H键。②分子中仅含一个
杂原子的六元环,环上只有一条侧链。
【答案】(1)ABC
(2) 消去反应
(3)
(4)
(5) 、 、
【解析】CHCOCH 一定条件下生成A,结合A的核磁共振氢谱为2组峰,A为 ,A发
3 3
生消去反应生成B为CH=C(CH)-C(CH)=CH ,B和CH=CH-CN发生已知的反应生成C,C发生还
2 3 3 2 2
原反应生成D为 ,E经过一系列反应生成F,F发生加成反应生成G,D和G反应取代反应生成H为 。
(1)A. 化合物Ⅰ的分子式是 ,A错误;
B.化合物H中的含氧官能团为羟基和醚键,B错误;
C. E为酚,邻位和对位可以被取代,醛基可以被溴水氧化,则1mol化合物E与溴水反应最多消耗3mol
,C错误;
D. 化合物G存在手性碳原子,存在对映异构体,D正确;
(2)根据分析,化合物A的结构简式是 ;化合物A→B反应类型为消去反应;
(3)D+G→H的化学方程式为 ;
(4)以丙酮、甲醛和E为原料合成F的路线为
;
(5)① 谱和IR谱检测表明:分子中共有6种不同化学环境的氢原子,有N-H键;②分子中仅
含一个杂原子的六元环,环上只有一条侧链,符合条件的同分异构体为 、 、。
3.(2022·江苏南京·高三阶段练习)二甲双酮是一种抗惊厥药,以丙烯为起始原料的合成路线如图:
(1)化合物C分子中碳原子的杂化轨道类型为____。
(2)B→C的反应类型为____。
(3)上述合成路线中E制备二甲双酮时生成了副产物X,X的分子式C H ON,则X结构简式为____。
5 10 3 2
(4)E的一种同分异构体同时满足以下条件,写出该同分异构体的结构简式:____。
a.能发生银镜反应,碱性条件下能发生水解反应;
b.分子中只有3种不同化学环境的氢原子。
c.分子中不含-O-O-
(5)已知:①R-Br R-CN② 。设计以化合物B为原
料合成乌头酸( )的路线(无机试剂任选)____。
【答案】(1)sp、sp3
(2)加成反应
(3)(CH )C(OH)CO(NH)CONH
3 2 2
(4)HCOOCH OC(CH )
2 3 3(5)
【解析】根据流程图,A发生催化氧化生成B,结合B的分子式和C的结构可知,B为丙酮( );
结合二甲双酮的结构可知,D与乙醇在酸性条件下发生酯化反应生成E,E为 ,
结合官能团的性质和转化关系分析解答。
(1)成四个共价单键的碳原子是sp3杂化,成共价三键的碳原子是sp杂化;
(2)根据流程图, 为丙酮和HCN的加成反应;
(3)根据X的分子式C H ON,相比二甲双酮多了2个H、1个O,推测合成路线中E制备二甲双酮时
5 10 3 2
生成了没有成环的副产物(CH)C(OH)CO(NH)CONH ;
3 2 2
(4)E为 ,要求同分异构体能发生银镜反应,碱性条件下能发生水解反应,
说明具有HCOO-基团,结合分子中只有三种氢原子,且不含-O-O-,可推知符合条件的同分异构体
结构简式为:HCOOCH OC(CH );
2 3 3
(5)以 为原料合成乌头酸( ),需要增长碳链和引
入羧基,根据题干流程图中BCD的转化关系,结合已知信息①②,需要将 氧化为丙酮后利
用②引入溴原子,在利用①和题干流程图中BCD的转化关系,即可引入三个羧基,具体合成路线为:。
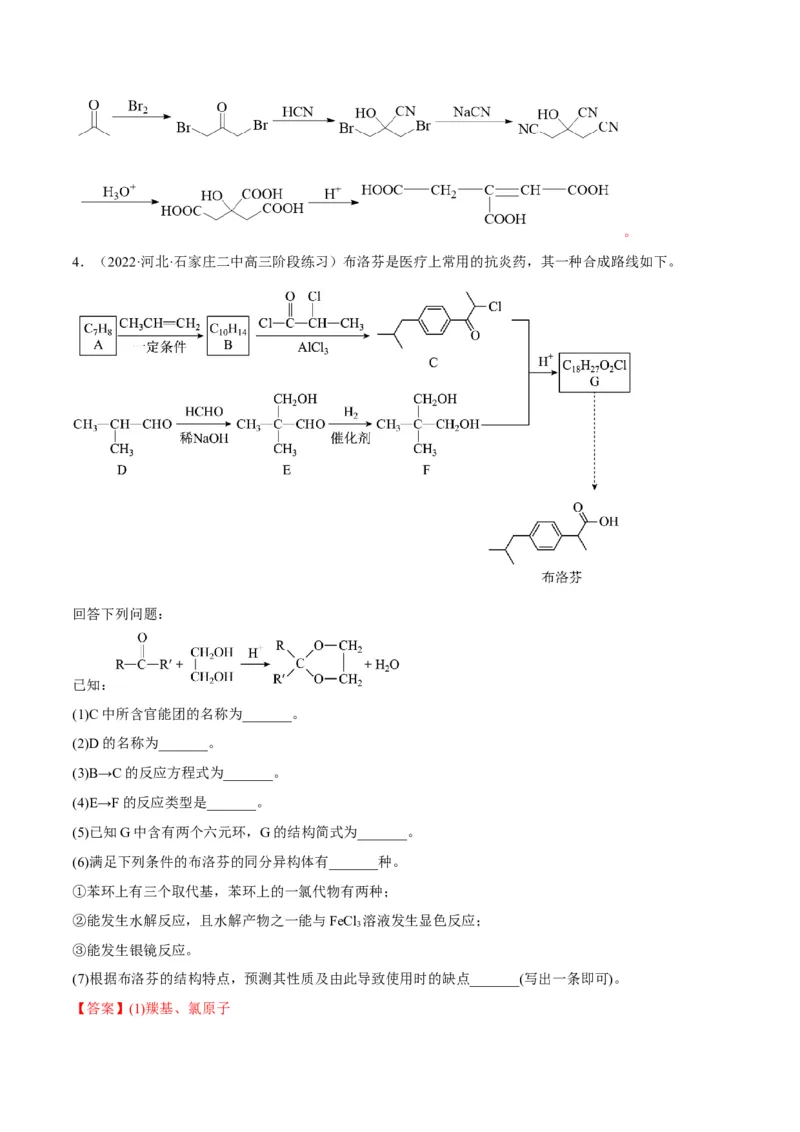
4.(2022·河北·石家庄二中高三阶段练习)布洛芬是医疗上常用的抗炎药,其一种合成路线如下。
回答下列问题:
已知:
(1)C中所含官能团的名称为_______。
(2)D的名称为_______。
(3)B→C的反应方程式为_______。
(4)E→F的反应类型是_______。
(5)已知G中含有两个六元环,G的结构简式为_______。
(6)满足下列条件的布洛芬的同分异构体有_______种。
①苯环上有三个取代基,苯环上的一氯代物有两种;
②能发生水解反应,且水解产物之一能与FeCl 溶液发生显色反应;
3
③能发生银镜反应。
(7)根据布洛芬的结构特点,预测其性质及由此导致使用时的缺点_______(写出一条即可)。
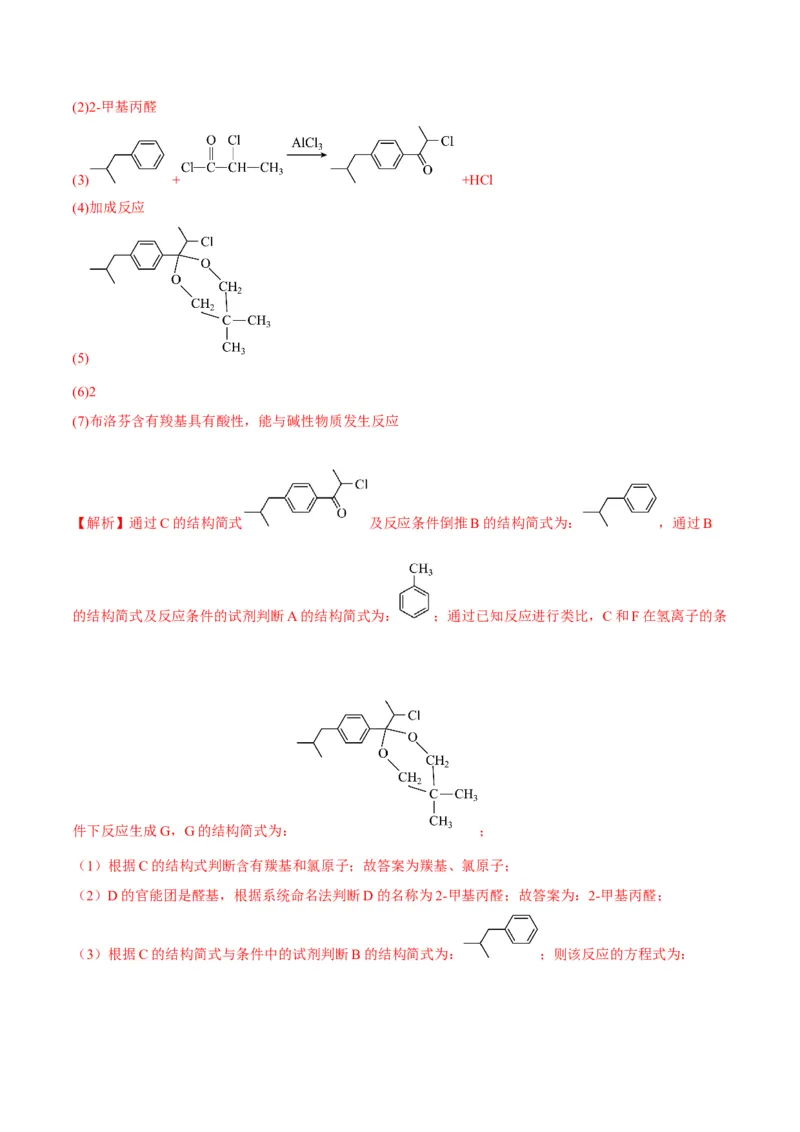
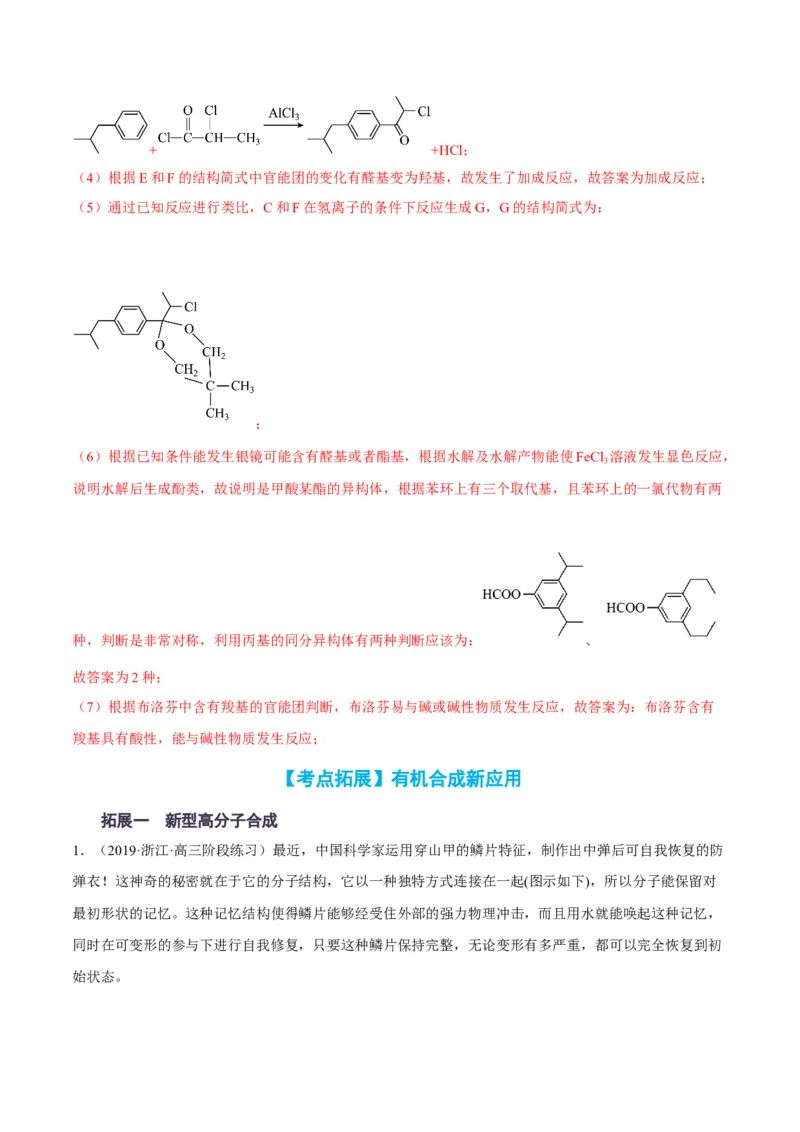
【答案】(1)羰基、氯原子(2)2-甲基丙醛
(3) + +HCl
(4)加成反应
(5)
(6)2
(7)布洛芬含有羧基具有酸性,能与碱性物质发生反应
【解析】通过C的结构简式 及反应条件倒推B的结构简式为: ,通过B
的结构简式及反应条件的试剂判断A的结构简式为: ;通过已知反应进行类比,C和F在氢离子的条
件下反应生成G,G的结构简式为: ;
(1)根据C的结构式判断含有羰基和氯原子;故答案为羰基、氯原子;
(2)D的官能团是醛基,根据系统命名法判断D的名称为2-甲基丙醛;故答案为:2-甲基丙醛;
(3)根据C的结构简式与条件中的试剂判断B的结构简式为: ;则该反应的方程式为:+ +HCl;
(4)根据E和F的结构简式中官能团的变化有醛基变为羟基,故发生了加成反应,故答案为加成反应;
(5)通过已知反应进行类比,C和F在氢离子的条件下反应生成G,G的结构简式为:
;
(6)根据已知条件能发生银镜可能含有醛基或者酯基,根据水解及水解产物能使FeCl 溶液发生显色反应,
3
说明水解后生成酚类,故说明是甲酸某酯的异构体,根据苯环上有三个取代基,且苯环上的一氯代物有两
种,判断是非常对称,利用丙基的同分异构体有两种判断应该为: 、
故答案为2种;
(7)根据布洛芬中含有羧基的官能团判断,布洛芬易与碱或碱性物质发生反应,故答案为:布洛芬含有
羧基具有酸性,能与碱性物质发生反应;
【考点拓展】有机合成新应用
拓展一 新型高分子合成
1.(2019·浙江·高三阶段练习)最近,中国科学家运用穿山甲的鳞片特征,制作出中弹后可自我恢复的防
弹衣!这神奇的秘密就在于它的分子结构,它以一种独特方式连接在一起(图示如下),所以分子能保留对
最初形状的记忆。这种记忆结构使得鳞片能够经受住外部的强力物理冲击,而且用水就能唤起这种记忆,
同时在可变形的参与下进行自我修复,只要这种鳞片保持完整,无论变形有多严重,都可以完全恢复到初
始状态。试分析并回答:
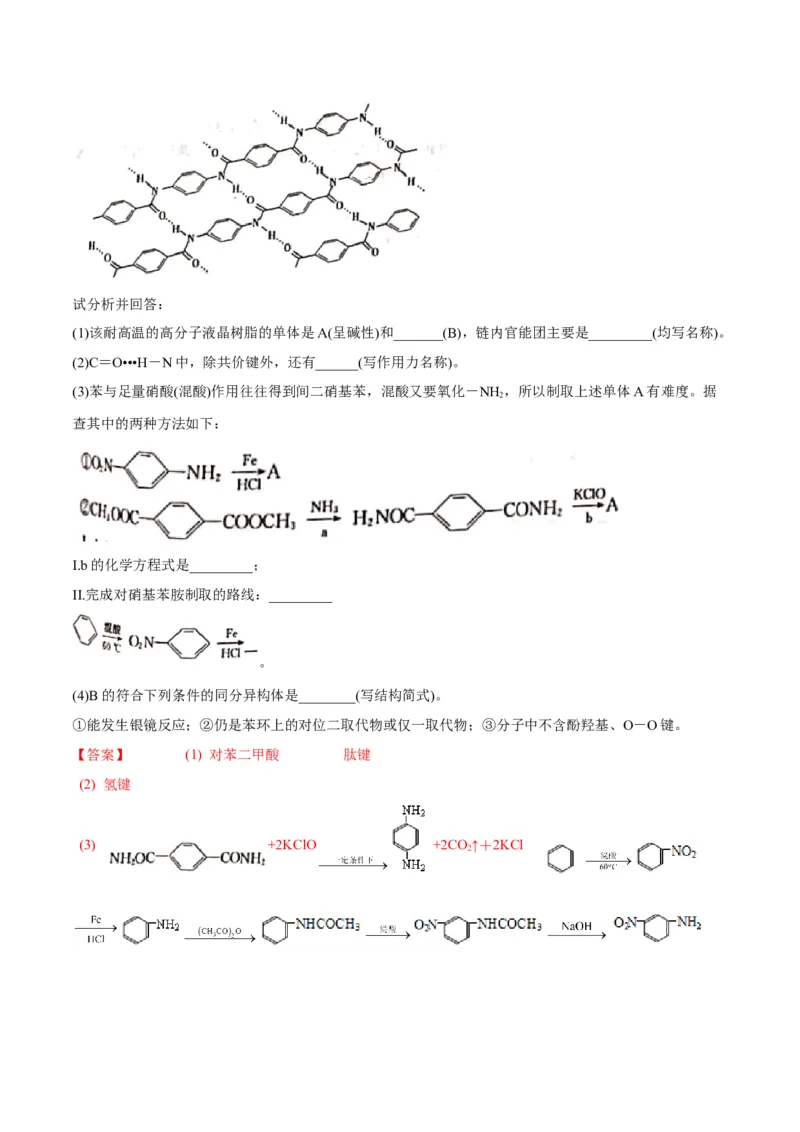
(1)该耐高温的高分子液晶树脂的单体是A(呈碱性)和_______(B),链内官能团主要是_________(均写名称)。
(2)C=O•••H-N中,除共价键外,还有______(写作用力名称)。
(3)苯与足量硝酸(混酸)作用往往得到间二硝基苯,混酸又要氧化-NH ,所以制取上述单体A有难度。据
2
查其中的两种方法如下:
I.b的化学方程式是_________;
II.完成对硝基苯胺制取的路线:_________
。
(4)B的符合下列条件的同分异构体是________(写结构简式)。
①能发生银镜反应;②仍是苯环上的对位二取代物或仅一取代物;③分子中不含酚羟基、O-O键。
【答案】 (1) 对苯二甲酸 肽键
(2) 氢键
(3) +2KClO +2CO ↑+2KCl
2(4) 、 、 、
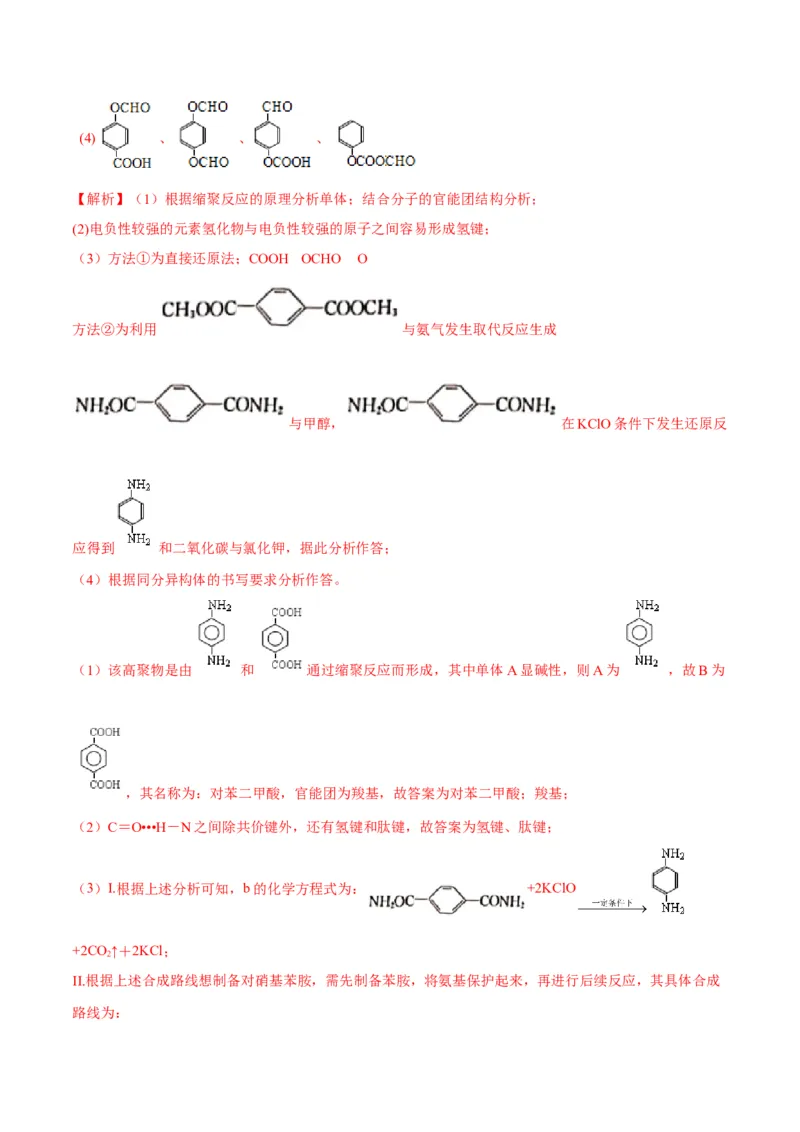
【解析】(1)根据缩聚反应的原理分析单体;结合分子的官能团结构分析;
(2)电负性较强的元素氢化物与电负性较强的原子之间容易形成氢键;
(3)方法①为直接还原法;COOH OCHO O
方法②为利用 与氨气发生取代反应生成
与甲醇, 在KClO条件下发生还原反
应得到 和二氧化碳与氯化钾,据此分析作答;
(4)根据同分异构体的书写要求分析作答。
(1)该高聚物是由 和 通过缩聚反应而形成,其中单体A显碱性,则A为 ,故B为
,其名称为:对苯二甲酸,官能团为羧基,故答案为对苯二甲酸;羧基;
(2)C=O•••H-N之间除共价键外,还有氢键和肽键,故答案为氢键、肽键;
(3)I.根据上述分析可知,b的化学方程式为: +2KClO
+2CO ↑+2KCl;
2
II.根据上述合成路线想制备对硝基苯胺,需先制备苯胺,将氨基保护起来,再进行后续反应,其具体合成
路线为:;
(4)B为 ,分子式为C HO 其不饱和度为6,同分异构体若满足①能发生银镜反应,则说明分子
8 6 4
含醛基;又是苯环上的对位二取代物或仅一取代物且分子中不含酚羟基、O-O键,则该同分异构体可以
为: 、 、 、 。
拓展二 特效药物的合成
2.(2022·湖南长沙·模拟预测)氧氮杂环是新药研制过程中发现的一类重要活性物质,有抗肿瘤功效。下
面是某研究小组提出的一种氧氮杂环类化合物F的合成路线:
已知:RCH=CHCOOR′+
回答下列问题:
(1)A的名称是_______,B中含氧官能团的名称是_______。
(2)B生成C的化学方程式为_______。
(3)C与M一定条件下反应生成D,M的结构简式为_______,D生成E的反应类型是_______。
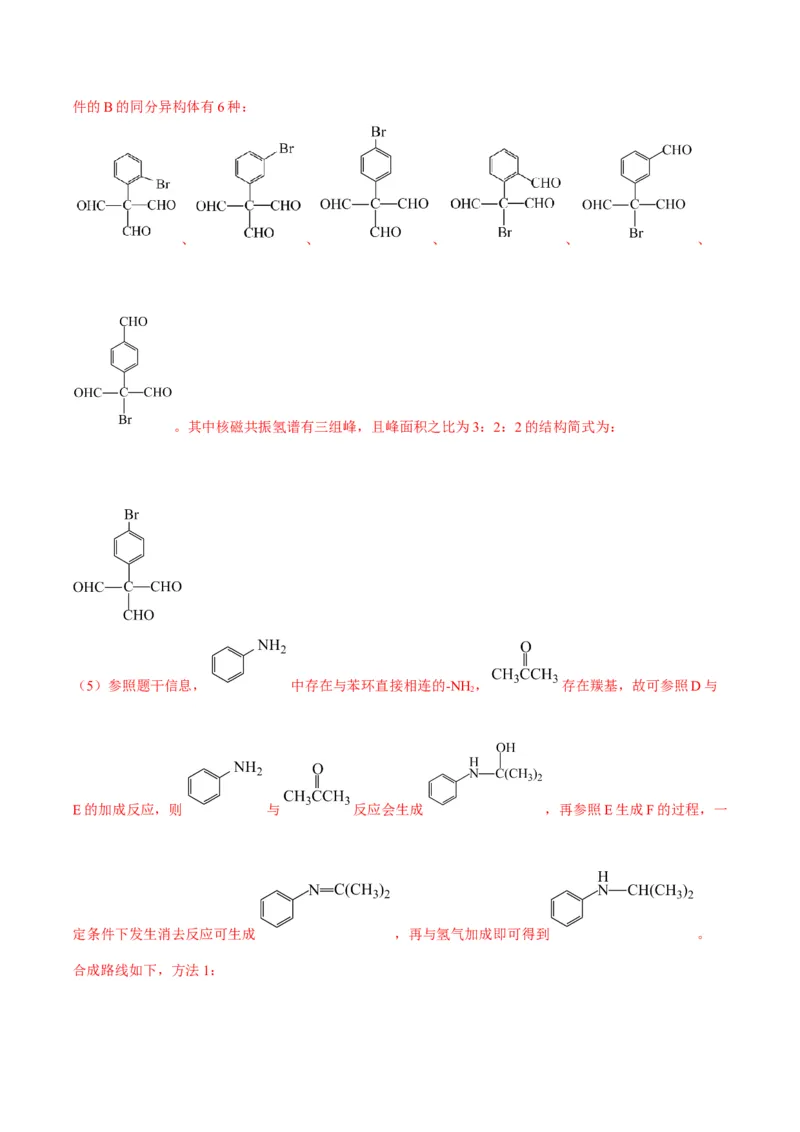
(4)B的同分异构体中,满足以下条件有_______种。①不含-CH ②含2种官能团 ③含苯环,无其他环,且苯环上仅有2个取代基
3
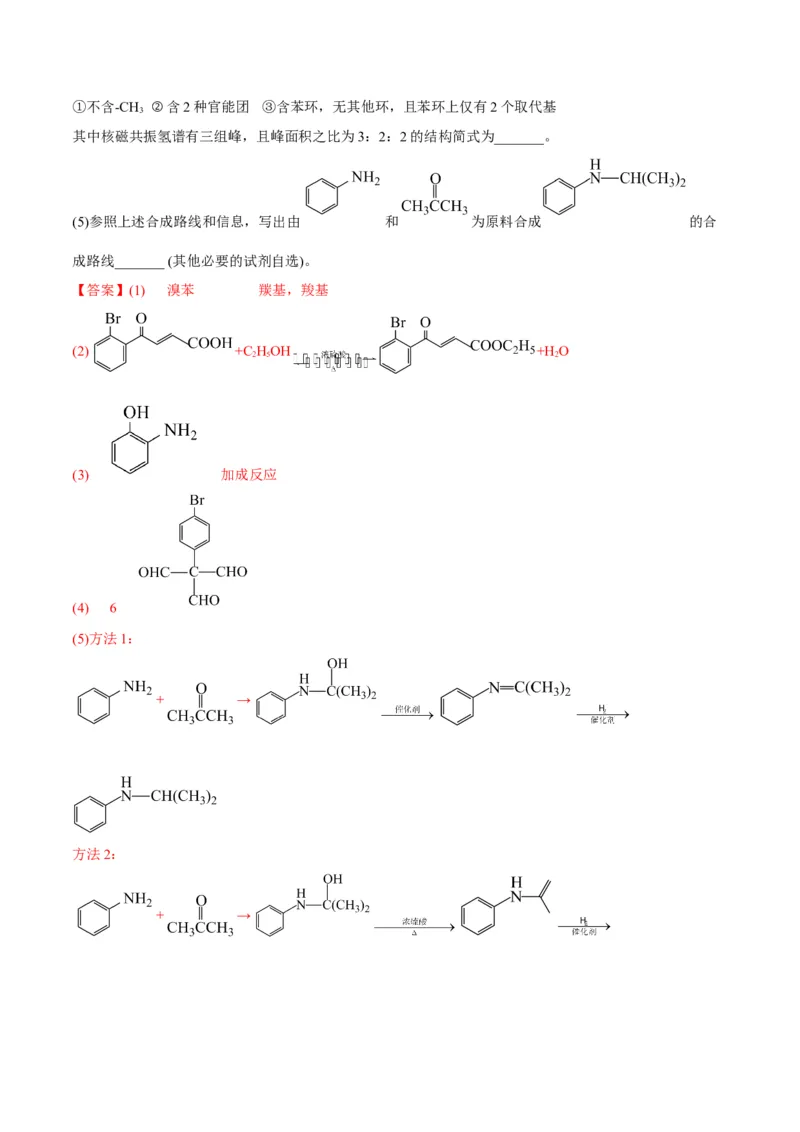
其中核磁共振氢谱有三组峰,且峰面积之比为3:2:2的结构简式为_______。
(5)参照上述合成路线和信息,写出由 和 为原料合成 的合
成路线_______ (其他必要的试剂自选)。
【答案】(1) 溴苯 羰基,羧基
(2) +C HOH +H O
2 5 2
(3) 加成反应
(4) 6
(5)方法1:
+ →
方法2:
+ →【解析】根据题中已知条件可知酚羟基可以与RCH=CHCOOR′结构中的碳碳双键发生加成反应。根据本题
合成路线,A结构为: ;B与乙醇发生酯化反应生成C,C中存在结构-CH=CHCOOC H,C转化成
2 5
D过程中碳碳双键变为单键,可知M中存在酚羟基,M与C发生加成反应生成D,M结构应为:
;D中存在碳氧双键,E中变为碳氧单键同时形成羟基,-NH 转化为-NH-连接到了之前存在
2
羰基的碳原子上,由此可知-NH 少的H应该转移成为羟基氢,故D转化成E的反应为加成反应;E转化为
2
F的过程中N与C之间形成双键,-H与-OH消失,可知此步发生消去反应。
(1)A名称为溴苯;B中含氧官能团为: 、-COOH,名称是羰基、羧基。
(2)B生成C为酯化反应,故反应方程式为: +C HOH
2 5
+H O
2
(3)M的结构简式为: ;D生成E的反应类型是加成反应。
(4)观察B结构,B中存在一个溴和三个氧,故B的同分异构体中应有三个相同的含氧官能团,想要满
足条件①②,此官能团只能是-CHO,则B的同分异构体中的两种官能团分别是-Br和-CHO。满足全部条件的B的同分异构体有6种:
、 、 、 、 、
。其中核磁共振氢谱有三组峰,且峰面积之比为3:2:2的结构简式为:
(5)参照题干信息, 中存在与苯环直接相连的-NH , 存在羰基,故可参照D与
2
E的加成反应,则 与 反应会生成 ,再参照E生成F的过程,一
定条件下发生消去反应可生成 ,再与氢气加成即可得到 。
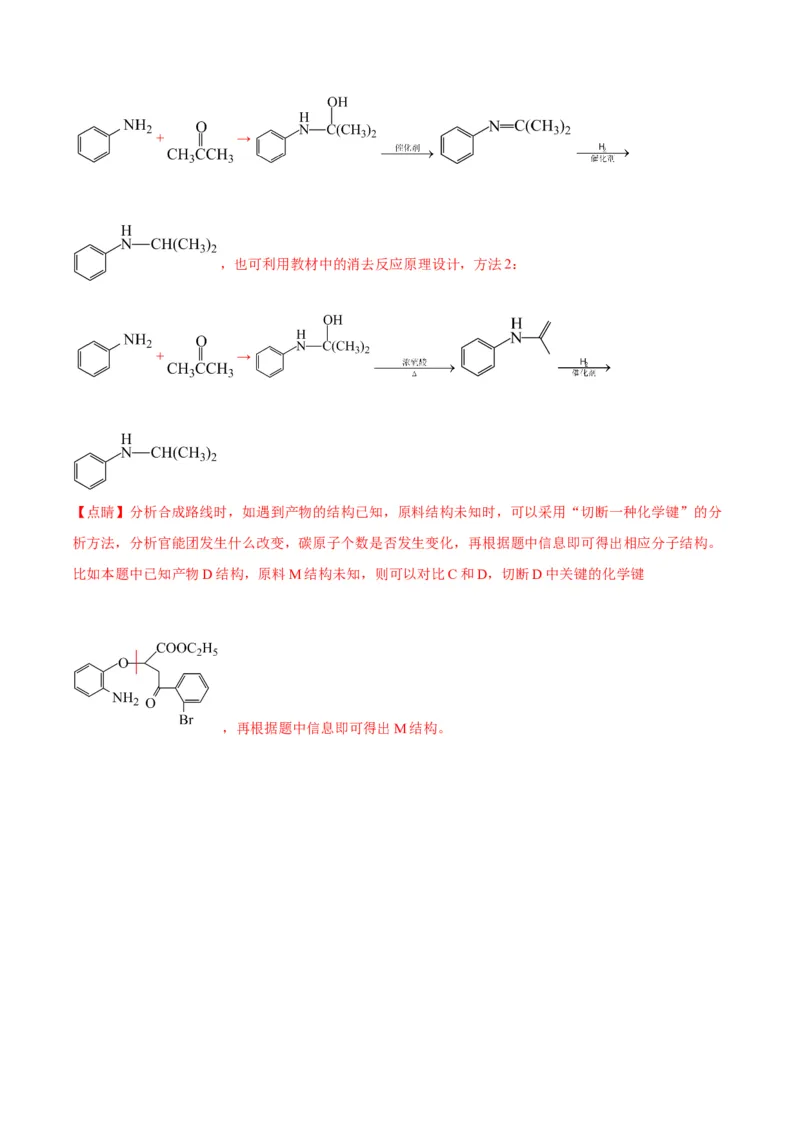
合成路线如下,方法1:+ →
,也可利用教材中的消去反应原理设计,方法2:
+ →
【点睛】分析合成路线时,如遇到产物的结构已知,原料结构未知时,可以采用“切断一种化学键”的分
析方法,分析官能团发生什么改变,碳原子个数是否发生变化,再根据题中信息即可得出相应分子结构。
比如本题中已知产物D结构,原料M结构未知,则可以对比C和D,切断D中关键的化学键
,再根据题中信息即可得出M结构。