文档内容
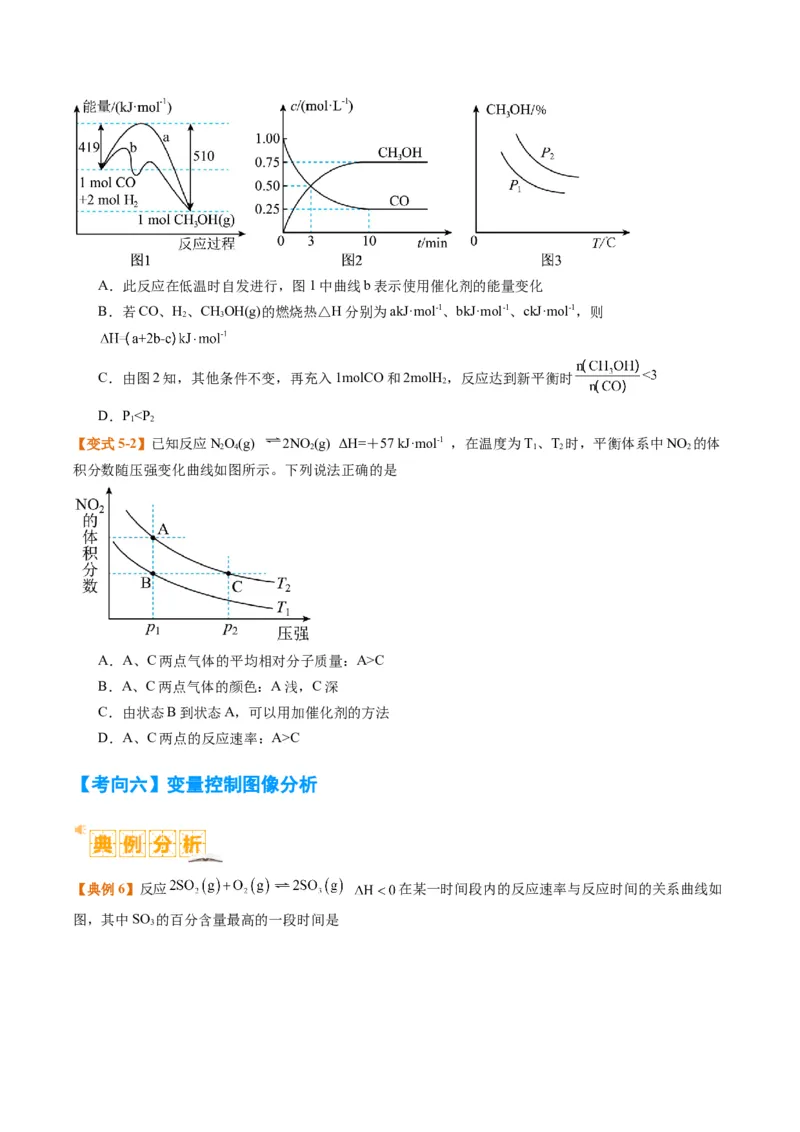
C
B.A、C两点气体的颜色:A浅,C深
C.由状态B到状态A,可以用加催化剂的方法
D.A、C两点的反应速率:A>C
【考向六】变量控制图像分析
【典例6】反应 在某一时间段内的反应速率与反应时间的关系曲线如
图,其中SO 的百分含量最高的一段时间是
3A. B. C. D.
1.解化学图像题的“三步骤”
2.解化学平衡图像题的“五项注意”
(1)注意曲线上的特殊点,如与坐标轴的交点、多条曲线的交点、拐点、极值点等。
(2)注意曲线坡度的“平”与“陡”,并弄清其意义。
(3)注意弄清高温、高压时反应速率快,有利于先达到平衡,即“先拐先平”。也就是说其他条件不变
时,较高温度或较大压强时达到平衡所用的时间短。
(4)注意运用图像中浓度(或物质的量)的变化来确定反应中化学计量数的关系,即化学计量数之比等于同
一时间内各反应物、生成物的浓度(或物质的量)变化量之比。
(5)对时间—速率图像,注意分清曲线的连续性、跳跃性,是“渐变”还是“突变”,是“大变”还是
“小变”,是“变大”还是“变小”,变化后是否仍然相等等情况,才可确定对应改变的条件是什么及如
何改变。
如:某密闭容器中发生如下反应: 。如图表示该反应的速率( )随时间(t)
变化的关系,t、t、t 时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
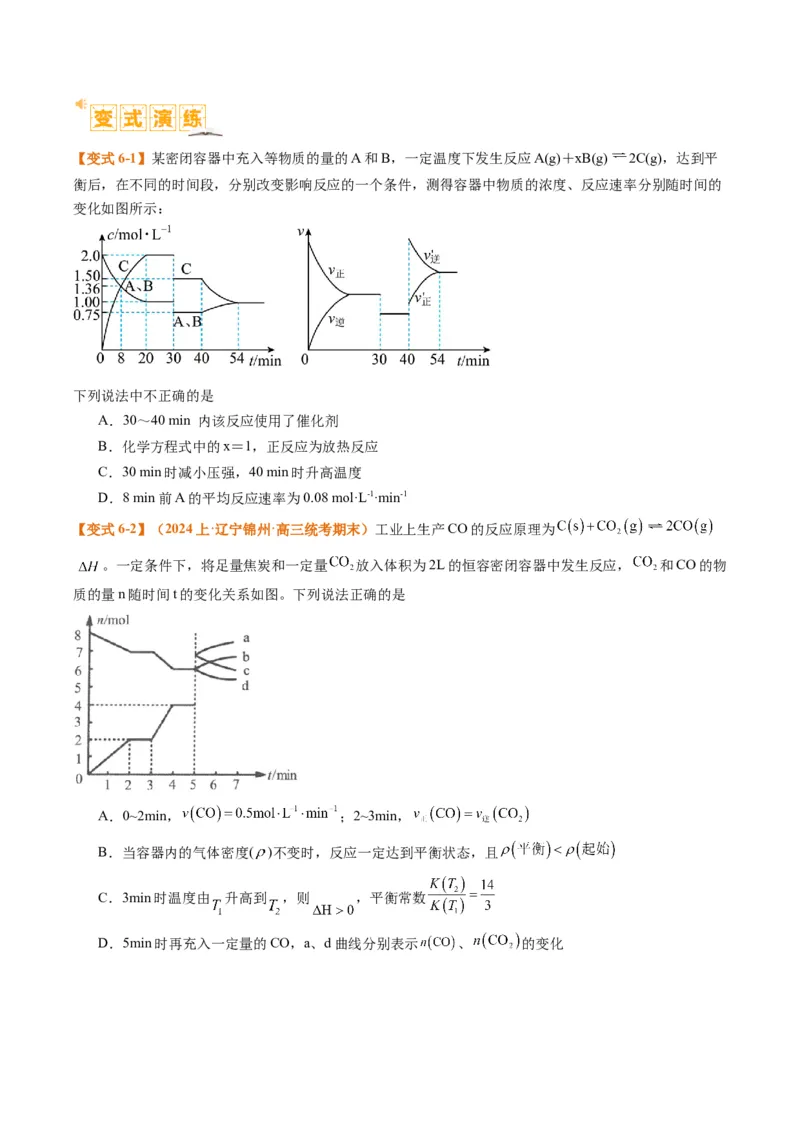
2 3 5【变式6-1】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平
衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的浓度、反应速率分别随时间的
变化如图所示:
下列说法中不正确的是
A.30~40 min 内该反应使用了催化剂
B.化学方程式中的x=1,正反应为放热反应
C.30 min时减小压强,40 min时升高温度
D.8 min前A的平均反应速率为0.08 mol·L-1·min-1
【变式6-2】(2024上·辽宁锦州·高三统考期末)工业上生产CO的反应原理为
。一定条件下,将足量焦炭和一定量 放入体积为2L的恒容密闭容器中发生反应, 和CO的物
质的量n随时间t的变化关系如图。下列说法正确的是
A.0~2min, ;2~3min,
B.当容器内的气体密度( )不变时,反应一定达到平衡状态,且
C.3min时温度由 升高到 ,则 ,平衡常数
D.5min时再充入一定量的CO,a、d曲线分别表示 、 的变化【考向七】转化率—投料比—温度图像分析
【典例7】(2023上·江苏泰州·高三姜堰中学校考期中) 重整反应能够有效去除大气中的 ,
是实现“碳中和”的重要途径之一,发生的反应如下:
重整反应:
积炭反应I:
积炭反应Ⅱ:
在恒压、起始投料比 条件下,体系中含碳组分平衡时的物质的量随温度变化关系曲线
如图所示。下列说法正确的是
A.曲线B表示平衡时 物质的量随温度的变化
B.减小起始投料比 ,有利于去除
C.积炭会导致催化剂失活,降低 的平衡转化率
D.高于600℃时,升高温度有利于减少积炭的量并去除 气体
1.转化率—投料比—温度图像
新型图像往往根据实际工业生产,结合图像,分析投料比、转化率、产率的变化。此类题目信息量较大,
能充分考查学生读图、提取信息、解决问题的能力,在新课标高考中受到命题者的青睐。
2.投料比对转化率和百分含量的影响
(1)反应物转化率相等的唯一条件:投料比=化学计量数比
(2)生成物含量最大的条件:投料比=化学计量数比
(3)催化剂的组成不变:投料比=化学计量数比
3.图像分析:
(1)如:一定条件下,CH 与HO(g)发生反应:CH(g)+HO(g) CO(g)+3H(g)。设起始=Z,在
4 2 4 2 2恒压下,平衡时CH 的体积分数φ(CH)与Z和T(温度)的关系如图所示 。
4 4
(2)如:以mA(g)+nB(g) pC(g)+qD(g)为例
n(A)
起始
n(B)
① 随着 起始增大,若保持B的量不变,增加A的量,平衡正向移动,C的量增多。
A.开始阶段,C量的增加值比总量的增加值大,所以C的含量增加。
n(A)
起始 m
B.b点
n(B)
起始=n ,C的含量最大
C.后来阶段,C量的增加值比总量的增加值小,所以C的含量降低。
②反应物转化率间的关系
A.a、b、c三点A的转化率:a>b>c
B.a、b、c三点B的转化率:c>b>a
【变式7-1】(2023上·江苏南通·高三江苏省如皋中学校考)二氧化碳加氢制甲烷过程中的主要反应为
CO(g)+4H(g)=CH (g)+2HO(g) ΔH=-164.7kJ·mol-1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2kJ·mol-1
2 2 2
在密闭容器中,1.01×105Pa,n (CO):n (H )=1:4时,CO 平衡转化率、在催化剂作用下反应相同时
起始 2 起始 2 2
间所测得的CO 实际转化率随温度的变化如图所示。
2CH 的选择性可表示为 ×100%。
4
下列说法正确的是
A.反应2CO(g)+2H(g)=CO (g)+CH (g)的焓变ΔH=-205.9kJ·mol-1
2 2 4
B.CH 的平衡选择性随着温度的升高而减少
4
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450℃时,提高 的值或增大压强,均能使CO₂平衡转化率达到X点的值
【变式7-2】(2023上·贵州贵阳·高三统考)已知气相直接水合法可以制取乙醇:
。在 的条件下投料,乙烯的平衡转化率
与温度(T)及压强(p)的关系如图所示。
下列有关说法错误的是
A.
B.
C.在 、280℃条件下,C点的
D.A点对应条件下反应的平衡常数 (用平衡分压代替浓度,分压=总压×物质的量分数)
【考向八】新型陌生图像分析
【典例8】(2024上·江苏南通·高三校联考)二氧化碳的资源化利用对实现“双碳”有着重要意义。二氧
化碳加氢制甲烷过程中的主要反应为在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同
时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列
说法正确的是
A.反应
B. 的选择性一定随着温度的升高而增加
C.用该催化剂催化二氧化碳反应的最佳温度约为 的原因是此温度下 的平衡转化率接近
100%
D. 时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
1.图像表格信息试题分析
图像表格类试题是以图像、图形和表格为试题的信息来源,以化学中的基本概念、基本理论、元素化合物和
化学实验等知识为载体,精心设计问题的一种信息处理和分析题。主要考查学生实验设计能力,数据读取、
分析与处理能力,图像的识别与分析能力。通过对图像、表格类试题信息的规范审读,进一步提高学生获取
信息的能力。
2.图表信息试题的解题策略
(1)应用分析归纳的方法,得出表格数据中蕴含的具有本质性的规律。
(2)应用观察方法,准确理解图示中纵横轴代表的含义,并能结合化学知识分析判断曲线的走向趋势及起点、
拐点、水平线的含义。
(3)注意信息的情境化,理解所给信息的作用。注意信息与基础知识间的联系。
3.选择竞争型图像分析
现代化工生产过程中,因为存在着多个副反应,所以要提高目标产品的产率,就要选择适当的催化剂提高
目标产品的选择性,使反应物尽可能多地转化成目标产品。所以,在多重平衡的反应中,要降低副产品的
选择性。
(竞争、连续)反应图像的解题思维流程
第一步:审反应方程式:①找准竞争(或连续)反应在反应特点方面的异同
②分清主、副反应
第二步:提取研究状态(平衡、非平衡):
①非平衡状态量,其变化与反应速率有关
②平衡状态量,则与平衡移动有关
第三步:析图:依据图中横坐标、纵坐标的内容找出图中曲线中的“点”“线”的含义和变化趋势并用平
衡移动原理解答具体问题
如:CH 与 CO 重整生成 H 和 CO 的过程中主要发生下列反应:CH(g)+CO (g) 2H(g)+2CO(g)
4 2 2 4 2 2
ΔH=247.1 kJ·mol-1 H(g)+CO (g) HO(g)+CO(g) ΔH=41.2 kJ·mol-1。在恒压、反应物起始物质的量比
2 2 2
n(CH)∶n(CO)=1∶1条件下,CH 和CO 的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是(
4 2 4 2
)
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线A表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH)∶n(CO)=1∶1条件下,反应至CH 转化率达到X点的值,改变除温度外的特定条件
4 2 4
继续反应,CH 转化率能达到Y点的值
4
4.表格信息试题分析
(1)明确表格数据的单位
(2)总结表格数据的变化规律,判断相应的平衡状态。
(3)结合化学平衡常数、化学反应速率、平衡转化率进行相关计算。
(4)不同状态下的数据处理要注意利用对比法综合分析。
如:将一定量的SO (g)和O(g)分别通入体积为2 L的恒容密闭容器中,在不同温度下进行反应,得到如下表
2 2
中的两组数据:
实 平 起 始 量 /平 衡 量 /
达到平衡
验 温度衡 mol mol
所需时间
编 ℃ 常
min
SO O SO O
号 数 2 2 2 2
1 T K 4 2 x 0.8 6
1 1
2 T K 4 2 0.4 y t
2 2下列说法中不正确的是( )
A.x=2.4
B.T、T 的关系:T>T
1 2 1 2
C.K 、K 的关系:K >K
1 2 2 1
D.实验1在前6 min的反应速率v(SO )=0.2 mol·L-1·min-1
2
【变式8-1】(2023上·江西南昌·高三校联考期中)CO 催化加氢制CH 的反应为:
2 4
。催化剂上反应过程示意如图1所示。其他条件不变时,
10min时CO 的转化率和CH 的选择性(CO 转化为甲烷的量/CO 转化的总量)随温度变化如图2所示。下列
2 4 2 2
说法不正确的是
A.催化剂改变了 中O—C—O键的键角
B.150℃到350℃时,基本没有发生副反应
C. 催化加氢制 是一个吸热反应
D.使用催化剂不能改变 反应的△H
【变式8-2】(2023上·江苏徐州·高三统考期中)乙二醇在生产、生活中有着广泛的用途,某工艺制取乙二
醇所涉及的反应如下:
反应Ⅰ
反应Ⅱ
在压强一定的条件下,将 、 按1:3进料比通入装有催化剂的反应器中,测得
的转化率与 、 的选择性[ ]。下列说法正确的是
A.曲线a表示 转化率
B.195℃时,反应Ⅰ的平衡常数约为2904
C.190~198℃范围内,温度升高, 的值减小
D.其它条件相同时,增大压强和升高温度均可以提高平衡时 的产量
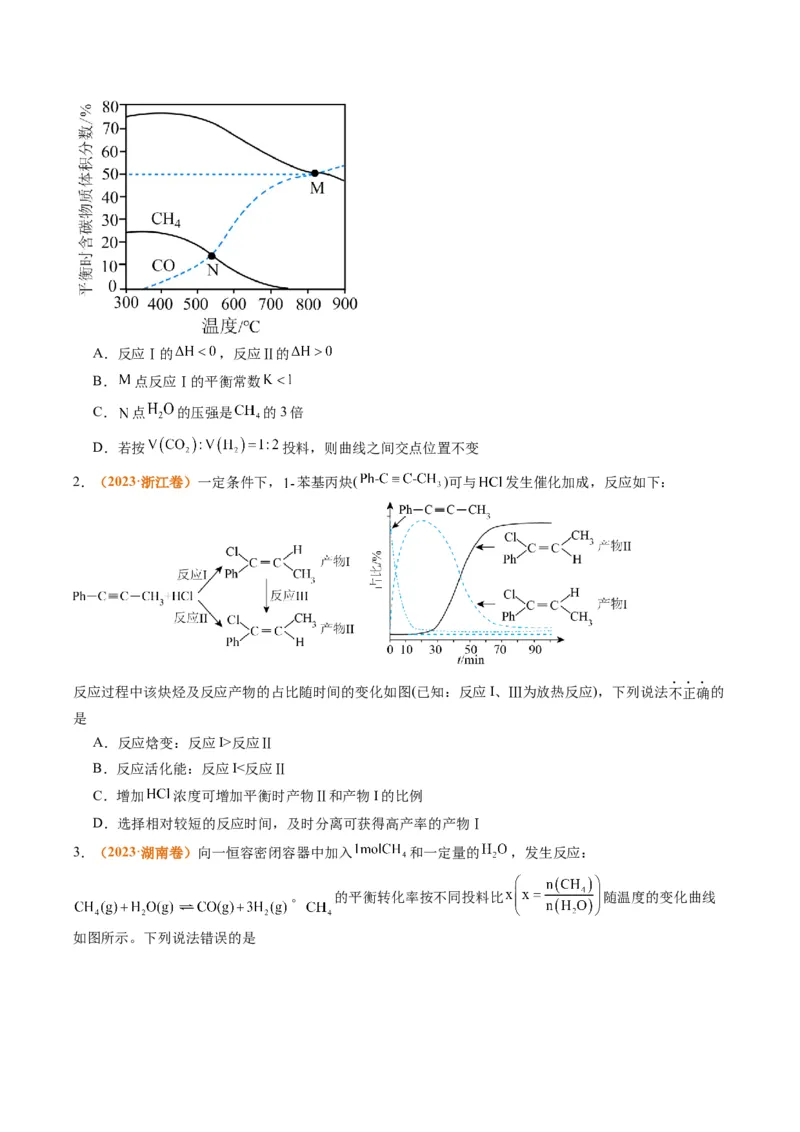
1.(2023·重庆卷)逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:
反应Ⅱ:
在恒容条件下,按 投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所
示。下列说法正确的是A.反应Ⅰ的 ,反应Ⅱ的
B. 点反应Ⅰ的平衡常数
C. 点 的压强是 的3倍
D.若按 投料,则曲线之间交点位置不变
2.(2023·浙江卷)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
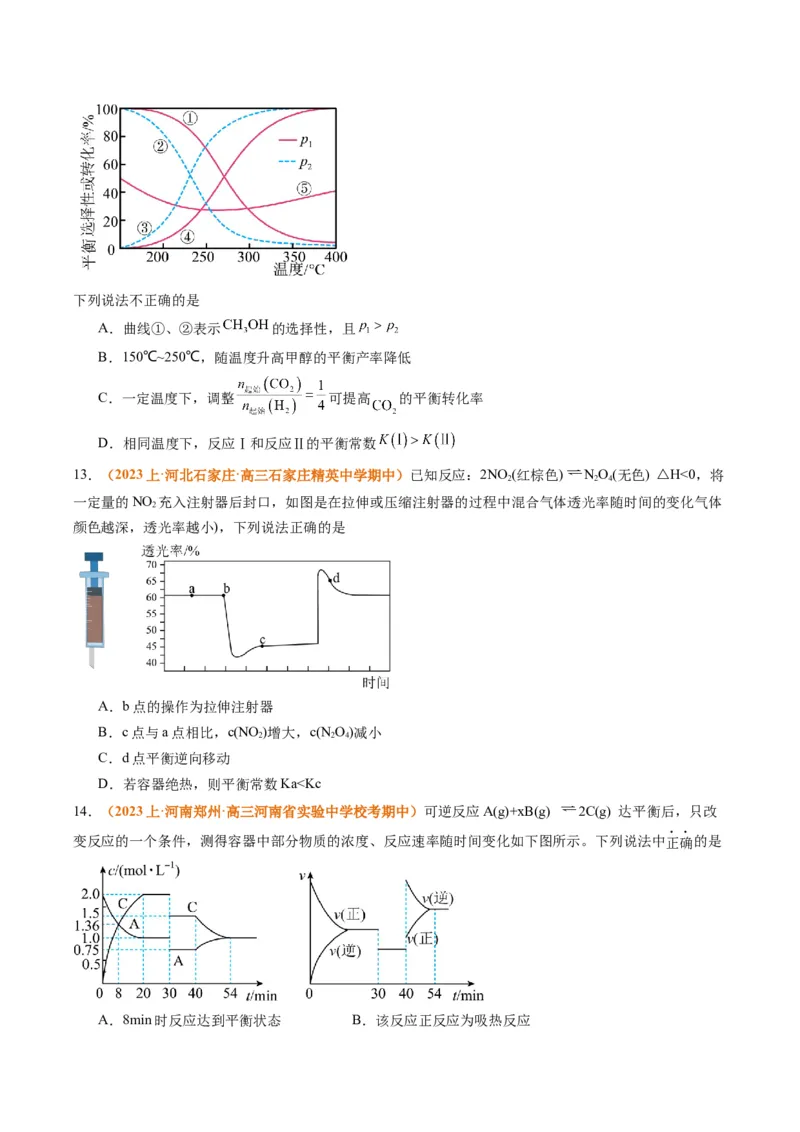
3.(2023·湖南卷)向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 随温度的变化曲线
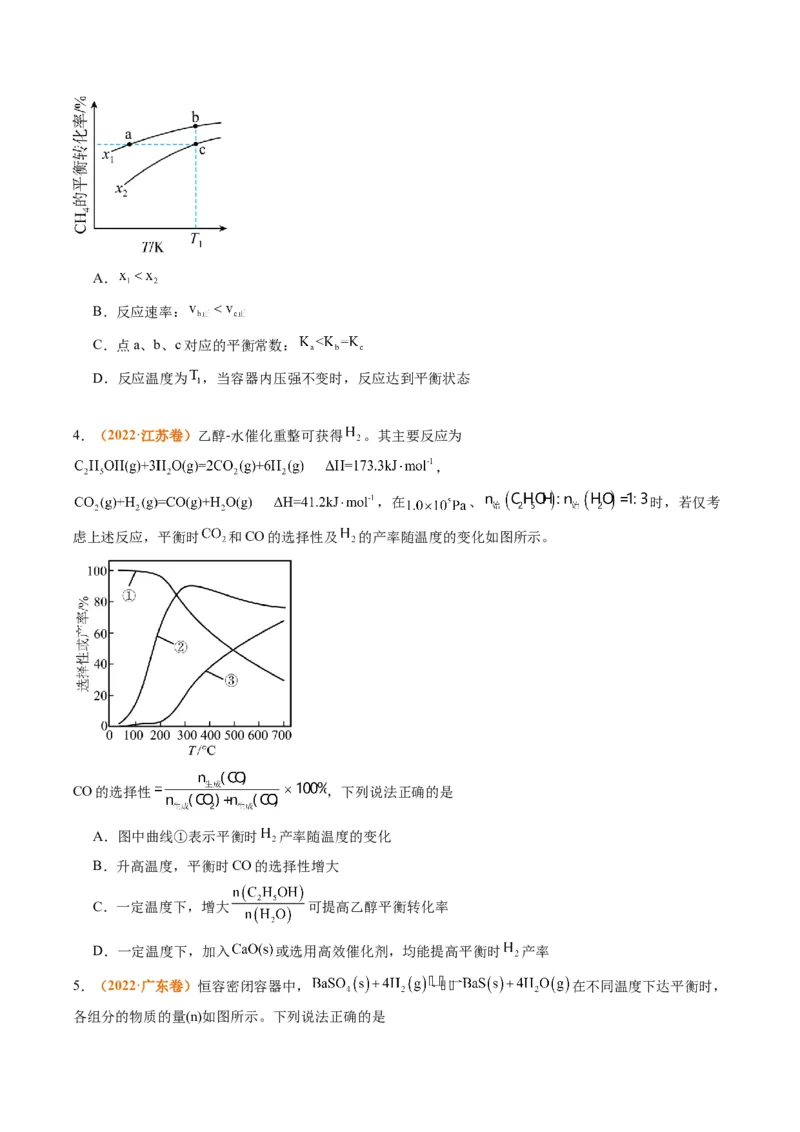
如图所示。下列说法错误的是A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
4.(2022·江苏卷)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若仅考
虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
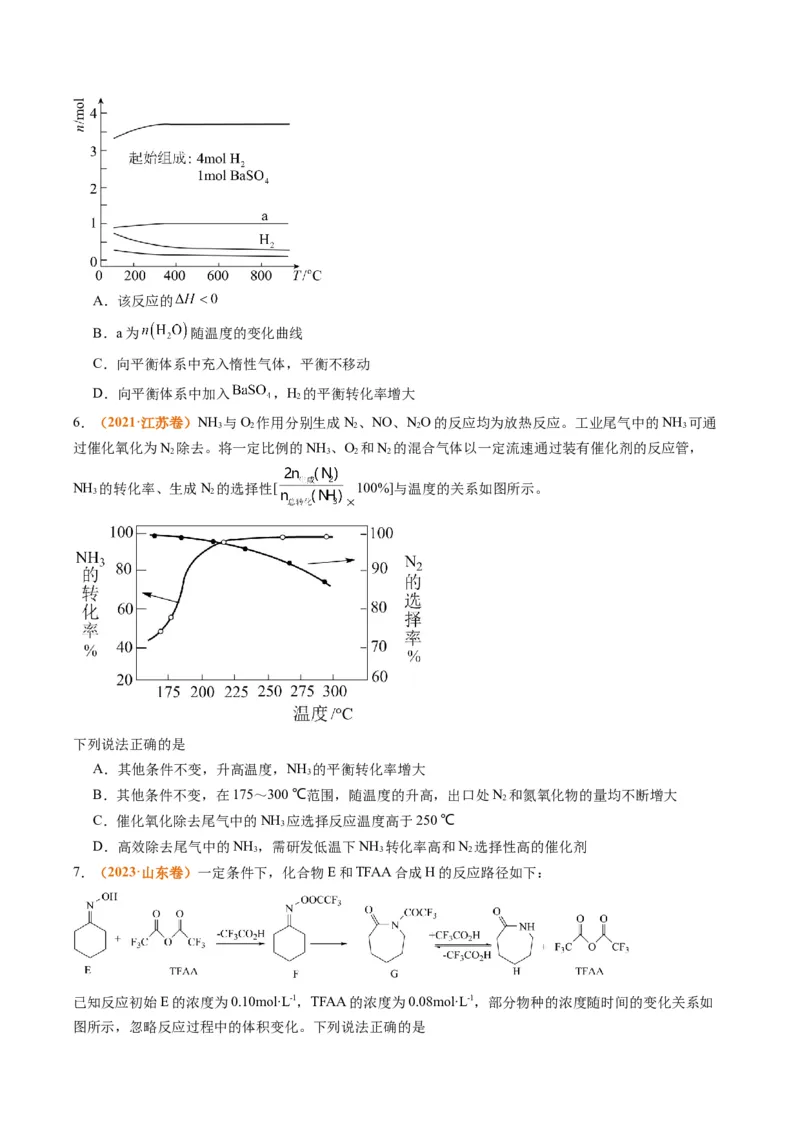
5.(2022·广东卷)恒容密闭容器中, 在不同温度下达平衡时,
各组分的物质的量(n)如图所示。下列说法正确的是A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
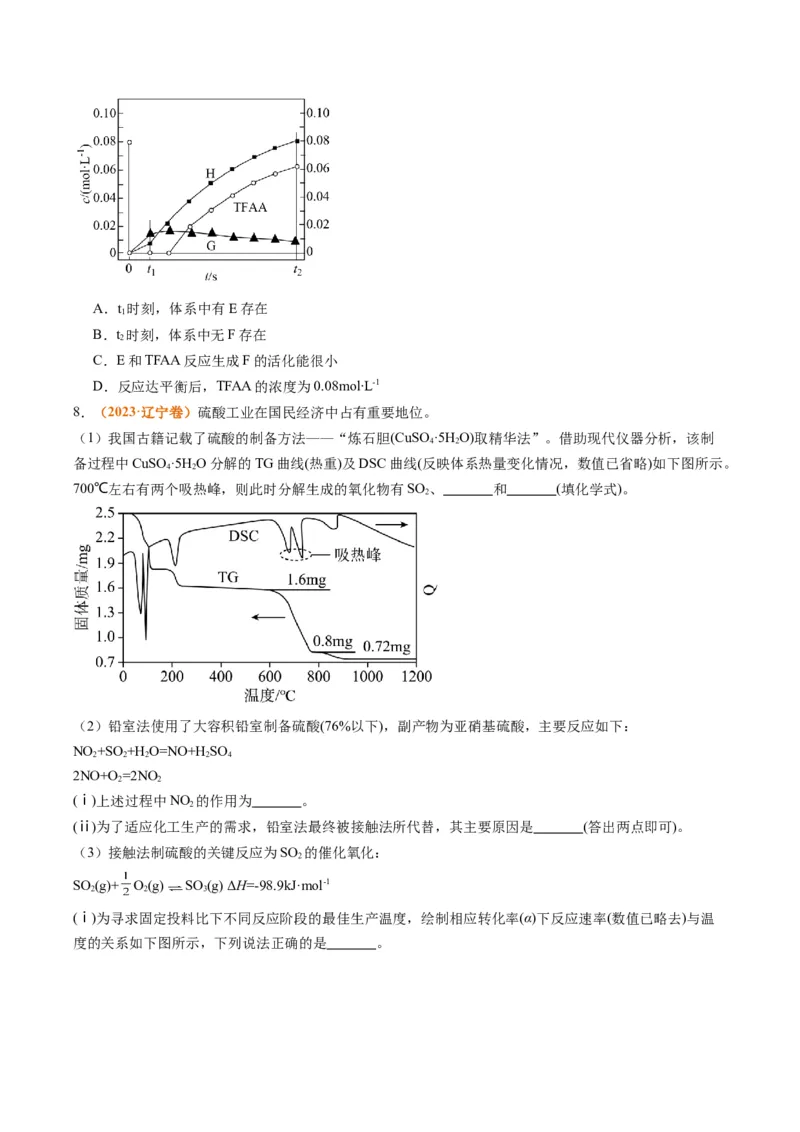
6.(2021·江苏卷)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可通
3 2 2 2 3
过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,
2 3 2 2
NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2
下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
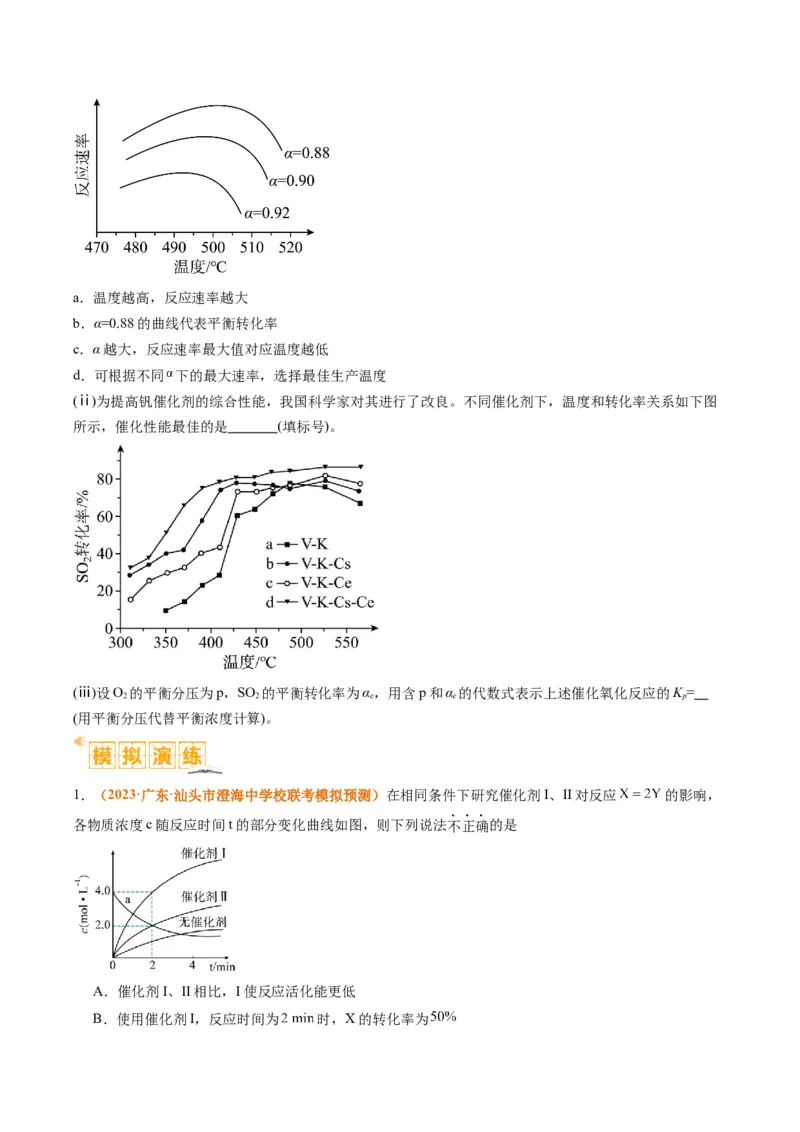
7.(2023·山东卷)一定条件下,化合物E和TFAA合成H的反应路径如下:
已知反应初始E的浓度为0.10mol∙L-1,TFAA的浓度为0.08mol∙L-1,部分物种的浓度随时间的变化关系如
图所示,忽略反应过程中的体积变化。下列说法正确的是A.t 时刻,体系中有E存在
1
B.t 时刻,体系中无F存在
2
C.E和TFAA反应生成F的活化能很小
D.反应达平衡后,TFAA的浓度为0.08mol∙L-1
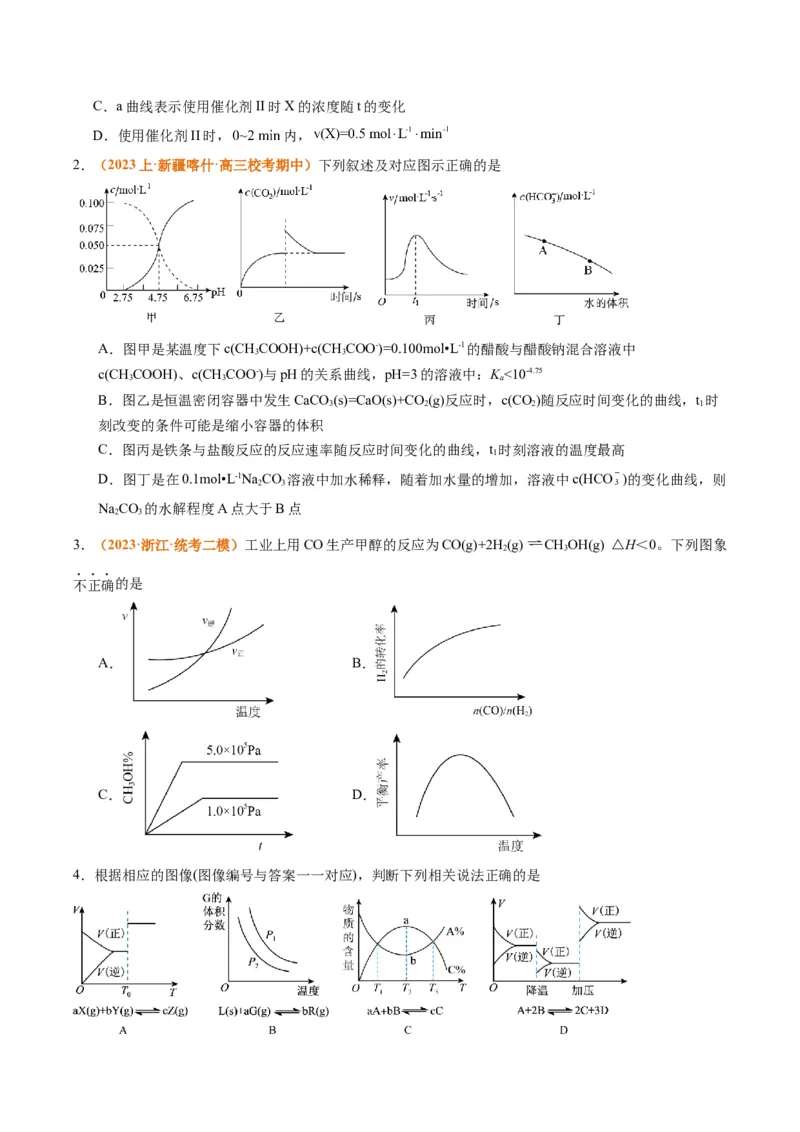
8.(2023·辽宁卷)硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO ·5H O)取精华法”。借助现代仪器分析,该制
4 2
备过程中CuSO ·5H O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。
4 2
700℃左右有两个吸热峰,则此时分解生成的氧化物有SO 、 和 (填化学式)。
2
(2)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:
NO +SO+H O=NO+H SO
2 2 2 2 4
2NO+O =2NO
2 2
(ⅰ)上述过程中NO 的作用为 。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是 (答出两点即可)。
(3)接触法制硫酸的关键反应为SO 的催化氧化:
2
SO (g)+ O(g) SO (g) ΔH=-98.9kJ·mol-1
2 2 3
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温
度的关系如下图所示,下列说法正确的是 。a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同 下的最大速率,选择最佳生产温度
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图
所示,催化性能最佳的是 (填标号)。
(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α,用含p和α 的代数式表示上述催化氧化反应的K =
2 2 e e p
(用平衡分压代替平衡浓度计算)。
1.(2023·广东·汕头市澄海中学校联考模拟预测)在相同条件下研究催化剂I、II对反应 的影响,
各物质浓度c随反应时间t的部分变化曲线如图,则下列说法不正确的是
A.催化剂I、II相比,I使反应活化能更低
B.使用催化剂I,反应时间为 时,X的转化率为C.a曲线表示使用催化剂II时X的浓度随t的变化
D.使用催化剂II时, 内,
2.(2023上·新疆喀什·高三校考期中)下列叙述及对应图示正确的是
A.图甲是某温度下c(CHCOOH)+c(CH COO-)=0.100mol•L-1的醋酸与醋酸钠混合溶液中
3 3
c(CHCOOH)、c(CHCOO-)与pH的关系曲线,pH=3的溶液中:K <10-4.75
3 3 a
B.图乙是恒温密闭容器中发生CaCO (s)=CaO(s)+CO (g)反应时,c(CO)随反应时间变化的曲线,t 时
3 2 2 1
刻改变的条件可能是缩小容器的体积
C.图丙是铁条与盐酸反应的反应速率随反应时间变化的曲线,t 时刻溶液的温度最高
1
D.图丁是在0.1mol•L-1NaCO 溶液中加水稀释,随着加水量的增加,溶液中c(HCO )的变化曲线,则
2 3
NaCO 的水解程度A点大于B点
2 3
3.(2023·浙江·统考二模)工业上用CO生产甲醇的反应为CO(g)+2H(g) CHOH(g) △H<0。下列图象
2 3
不正确的是
A. B.
C. D.
4.根据相应的图像(图像编号与答案一一对应),判断下列相关说法正确的是A.密闭容器中反应达到平衡,T 时改变某一条件有如图变化所示,则改变的条件一定是加入催化剂
0
B.反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应,且a>b
C.物质的百分含量和温度关系如图所示,则该反应的正反应为放热反应
D.反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C、D均是气体
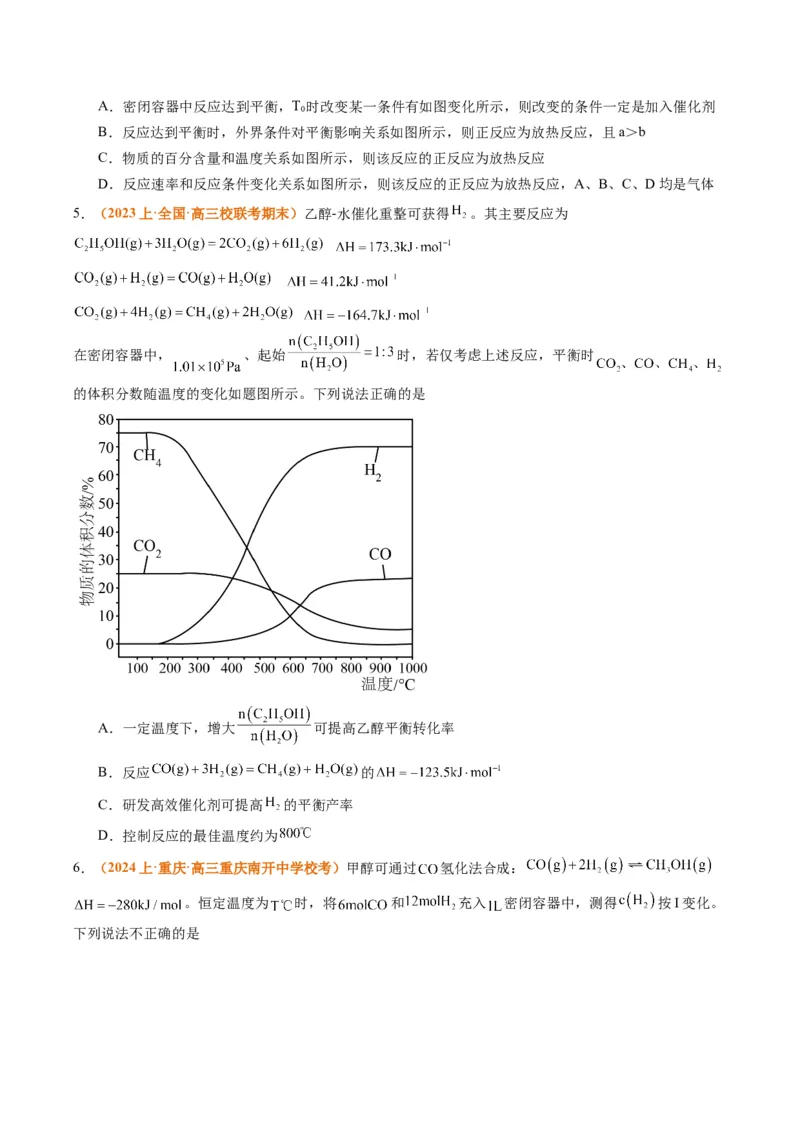
5.(2023上·全国·高三校联考期末)乙醇-水催化重整可获得 。其主要反应为
在密闭容器中, 、起始 时,若仅考虑上述反应,平衡时
的体积分数随温度的变化如题图所示。下列说法正确的是
A.一定温度下,增大 可提高乙醇平衡转化率
B.反应 的
C.研发高效催化剂可提高 的平衡产率
D.控制反应的最佳温度约为
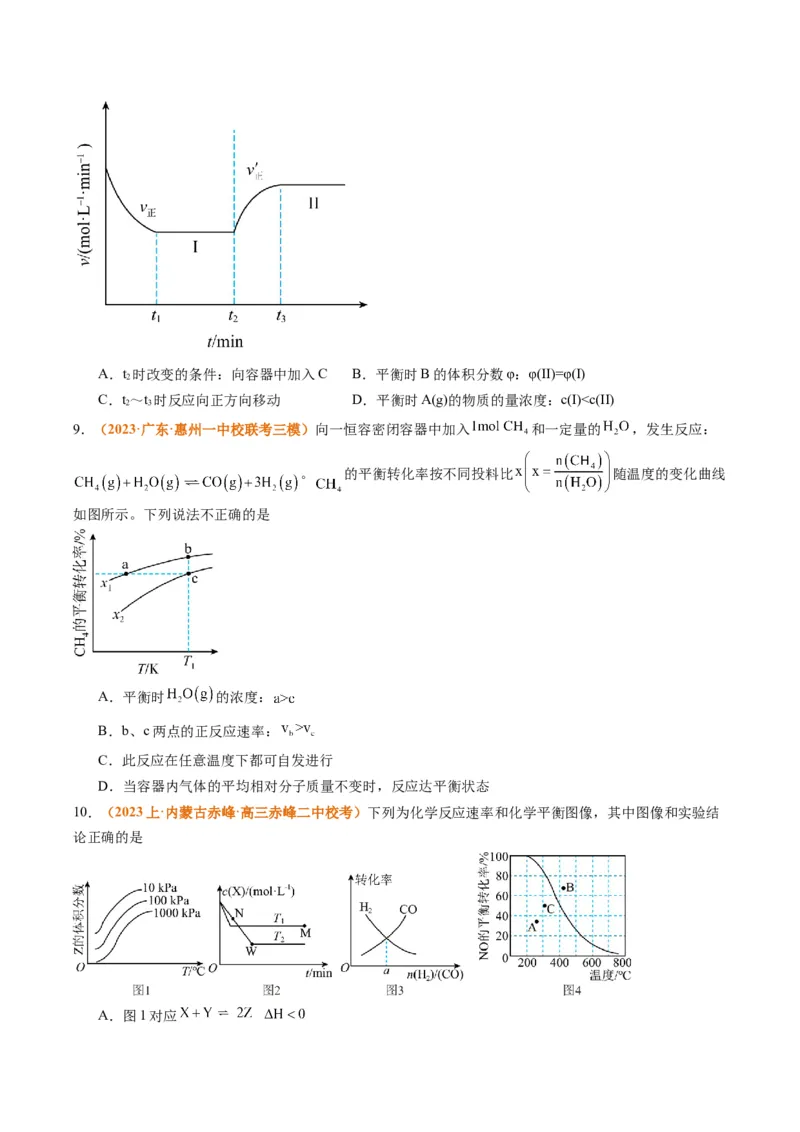
6.(2024上·重庆·高三重庆南开中学校考)甲醇可通过 氢化法合成:
。恒定温度为 时,将 和 充入 密闭容器中,测得 按I变化。
下列说法不正确的是A. 时,I中反应进行到B点时释放的热量为
B. 时,该反应平衡常数为
C.若其他条件不变,增大起始 ,所得 可能按Ⅱ变化
D.若其他条件不变,缩小容器体积,所得 可能按Ⅱ无变化
7.(2023上·内蒙古赤峰·高三赤峰二中校考)常温下,取一定量的PbI 固体配成饱和溶液,t时刻改变某
2
一条件,离子浓度变化如图所示。下列有关说法正确的是
A.常温下,PbI 的K 为2×10-6
2 sp
B.温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,平衡向生产沉淀的方向移动,Pb2+的浓度减
2
小
C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI 的K 增大
2 sp
D.常温下,K (PbS)=8×10-28,向PbI 的悬浊液中加入NaS溶液,反应PbI (s)+S2-(aq) PbS(s)+2I-
sp 2 2 2
(aq)的平衡常数为5×1018
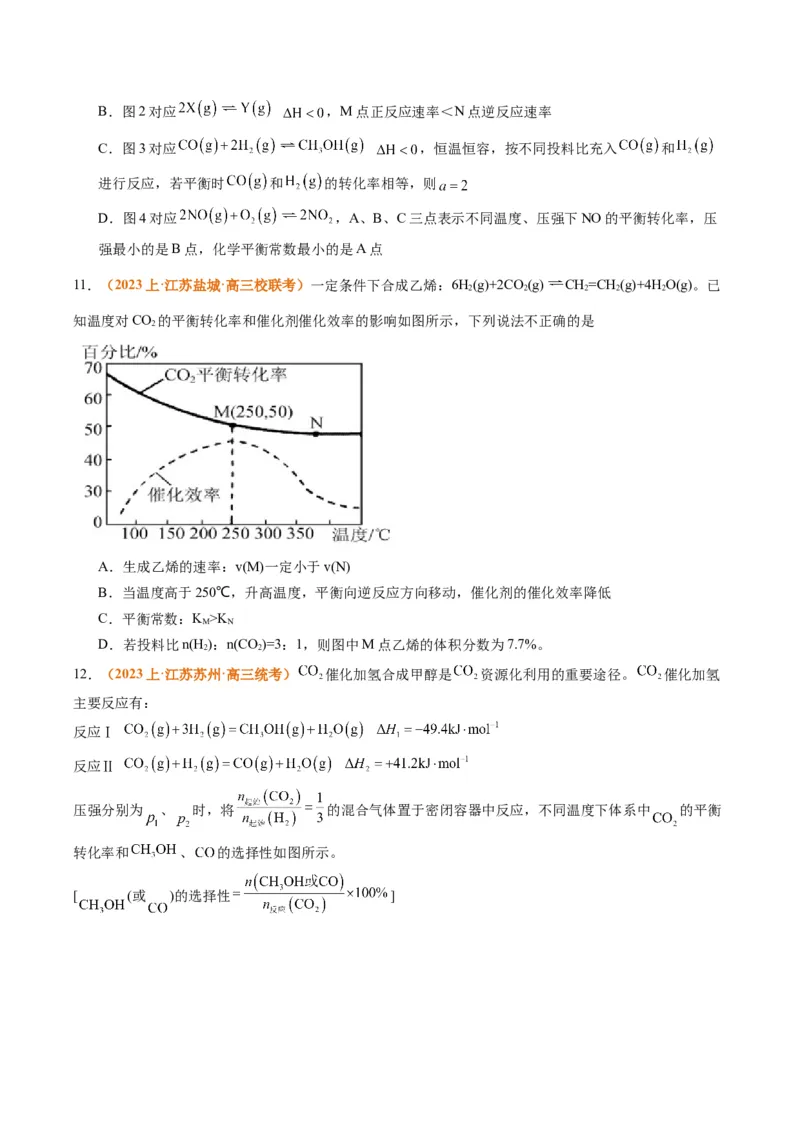
8.已知:A(g)+2B(g) 3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1 mol A和2 mol B发生反应,t
1
时达到平衡状态I,在t 时改变某一条件,t 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
2 3
下列说法不正确的是A.t 时改变的条件:向容器中加入C B.平衡时B的体积分数φ:φ(II)=φ(I)
2
C.t~t 时反应向正方向移动 D.平衡时A(g)的物质的量浓度:c(I)