文档内容
高频考点 22 反应热的计算
1.(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
能量/ kJmol-1 249 218 39 10 0 0 136 242
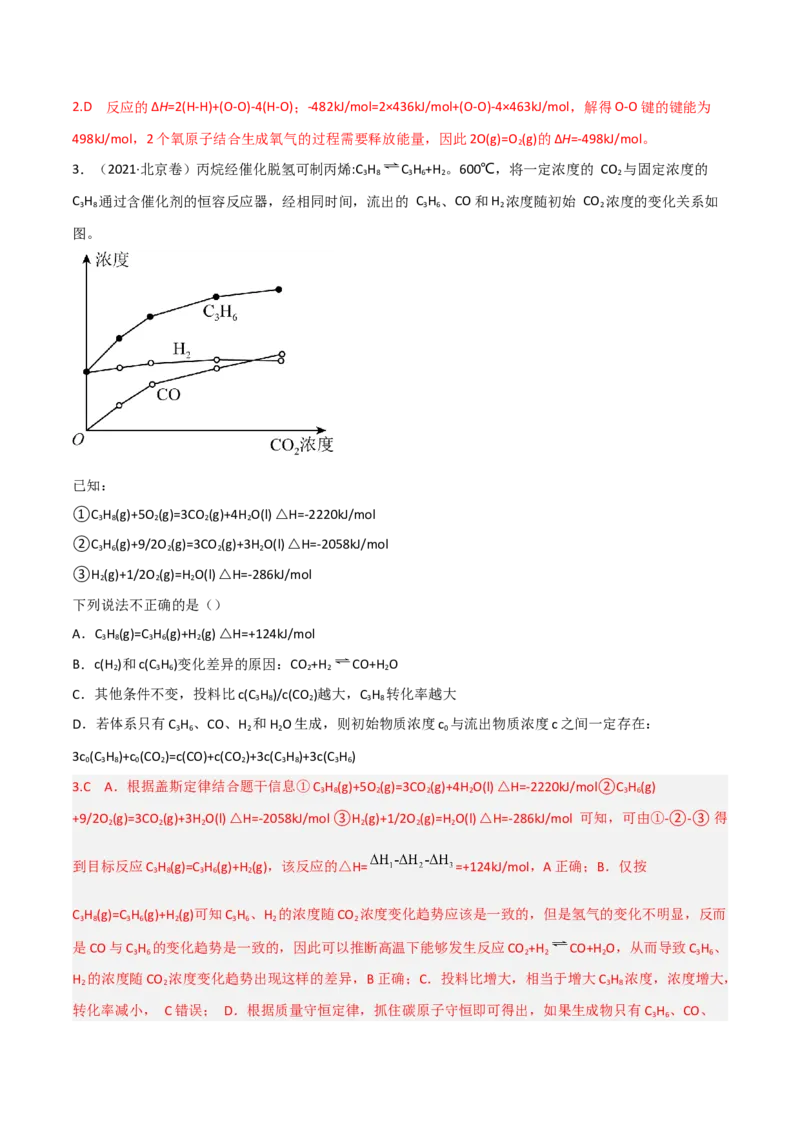
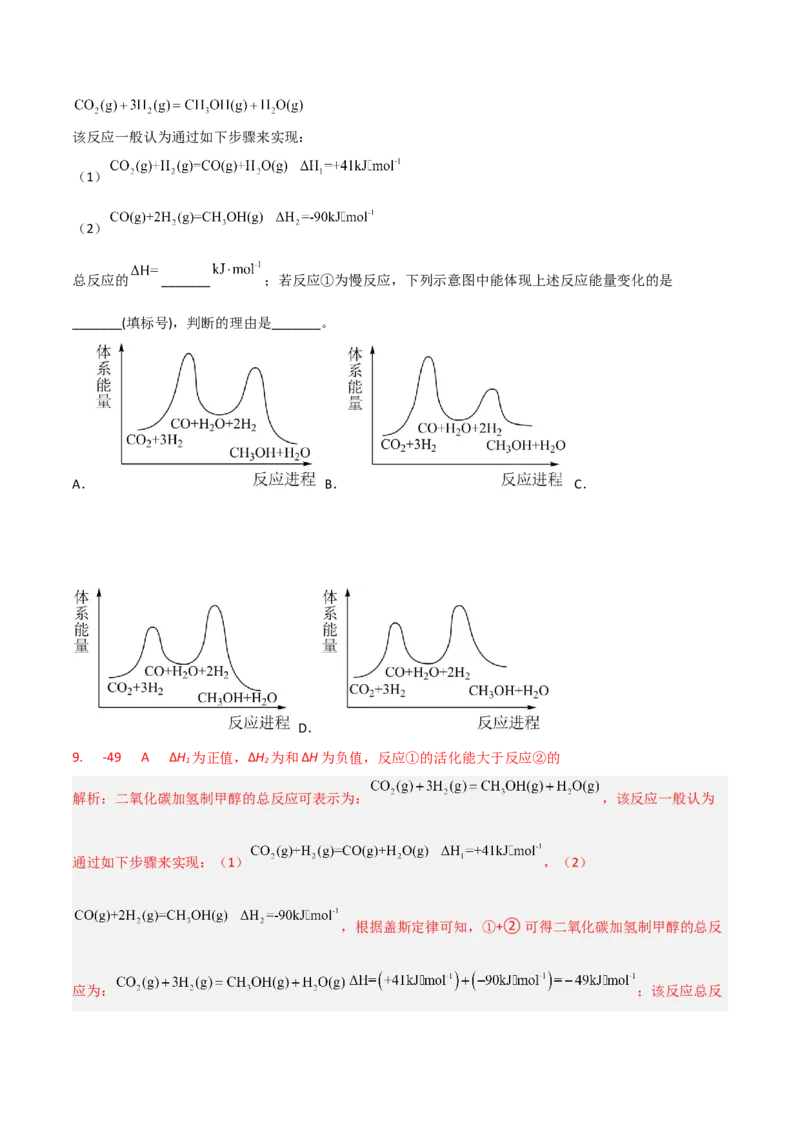
HO(g)+HO(g)=H O (g) H O 214kJmol-1
可根据 2 2 计算出 2 2中氧氧单键的键能为 。下列说法不正确的是( )
H 436kJmol-1
2
A. 的键能为
O H O
B. 2的键能大于 2 2中氧氧单键的键能的两倍
HOOn。
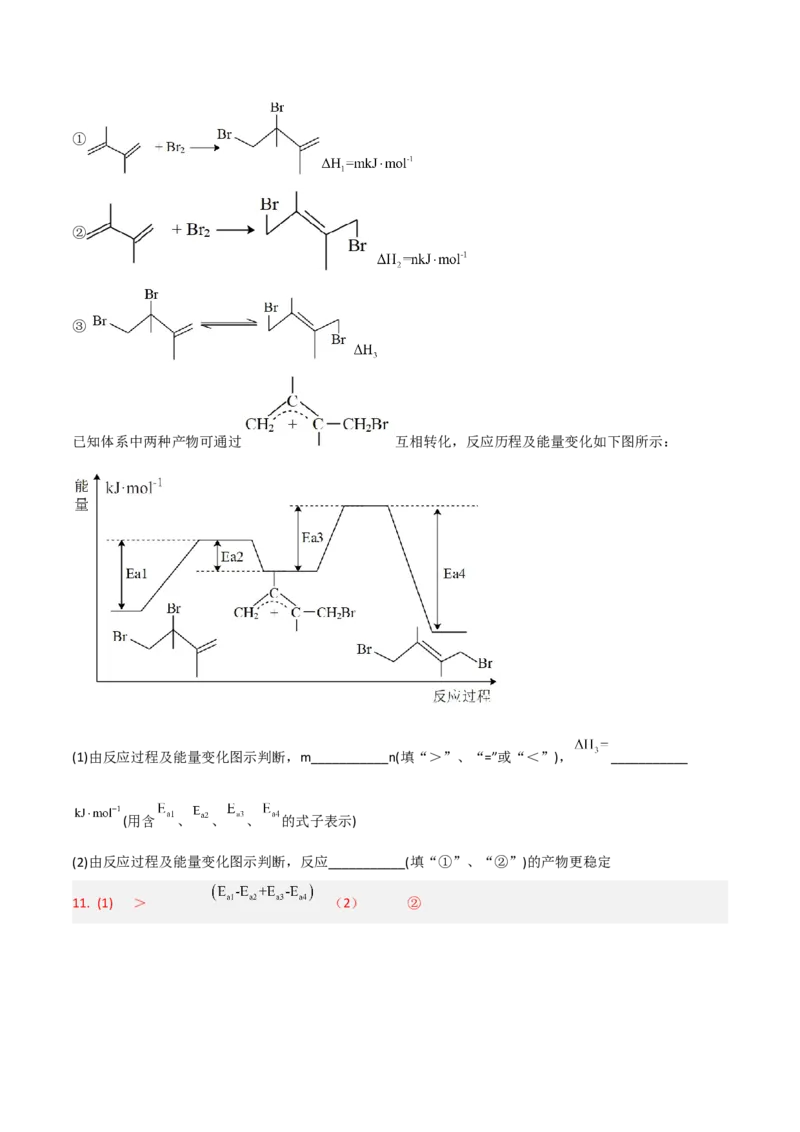
生成 , =E -E , 生成
a1 a2
, =E -E ,整个过程的反应热= E -E + E -E ,即 = E -E + E -E 。
a3 a4 a1 a2 a3 a4 a1 a2 a3 a4
(2) 物质的能量越大,该物质越稳定,故反应过程中反应②的产物更稳定。
12.回答下列问题
(1)水煤气变换[CO(g)+H O(g)=CO (g)+H (g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等
2 2 2
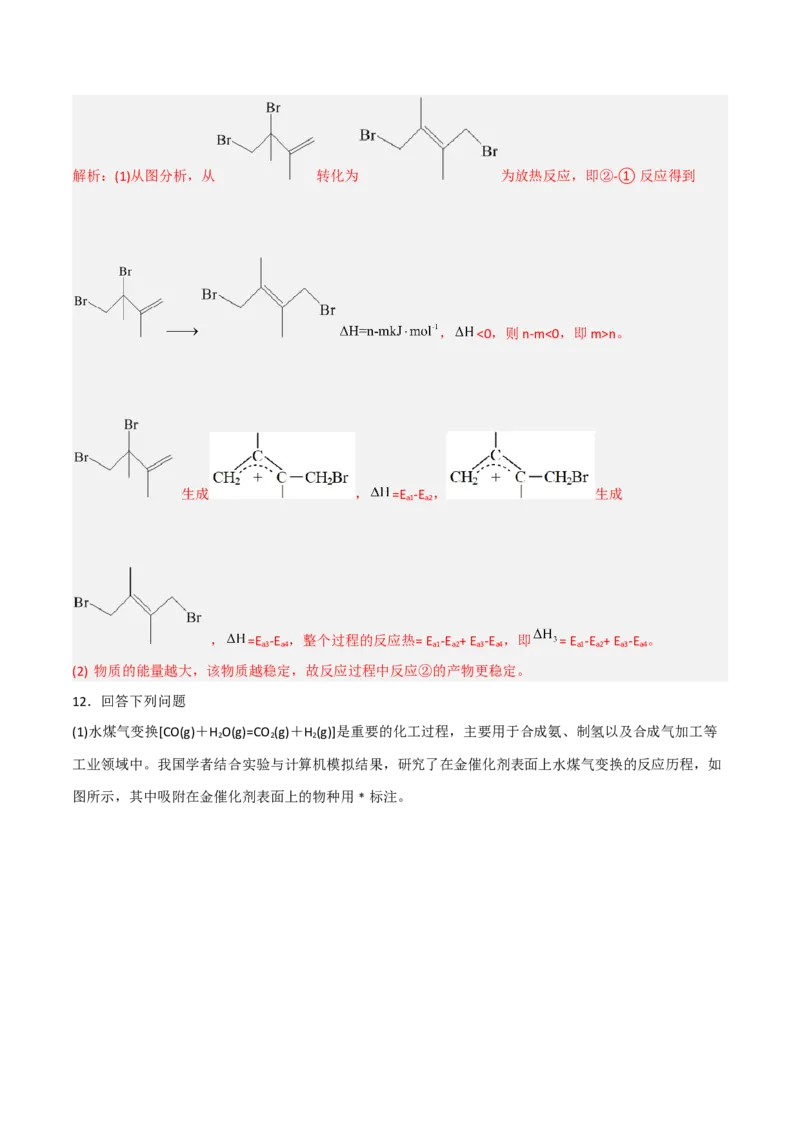
工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如
图所示,其中吸附在金催化剂表面上的物种用﹡标注。可知水煤气变换的ΔH___________0(填“大于”“等于”或“小于”)。该历程中最大能垒(活化能)E
正
=___________eV。
(2)已知:
P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;
P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;
由此推知,其中最稳定的磷单质是___________。
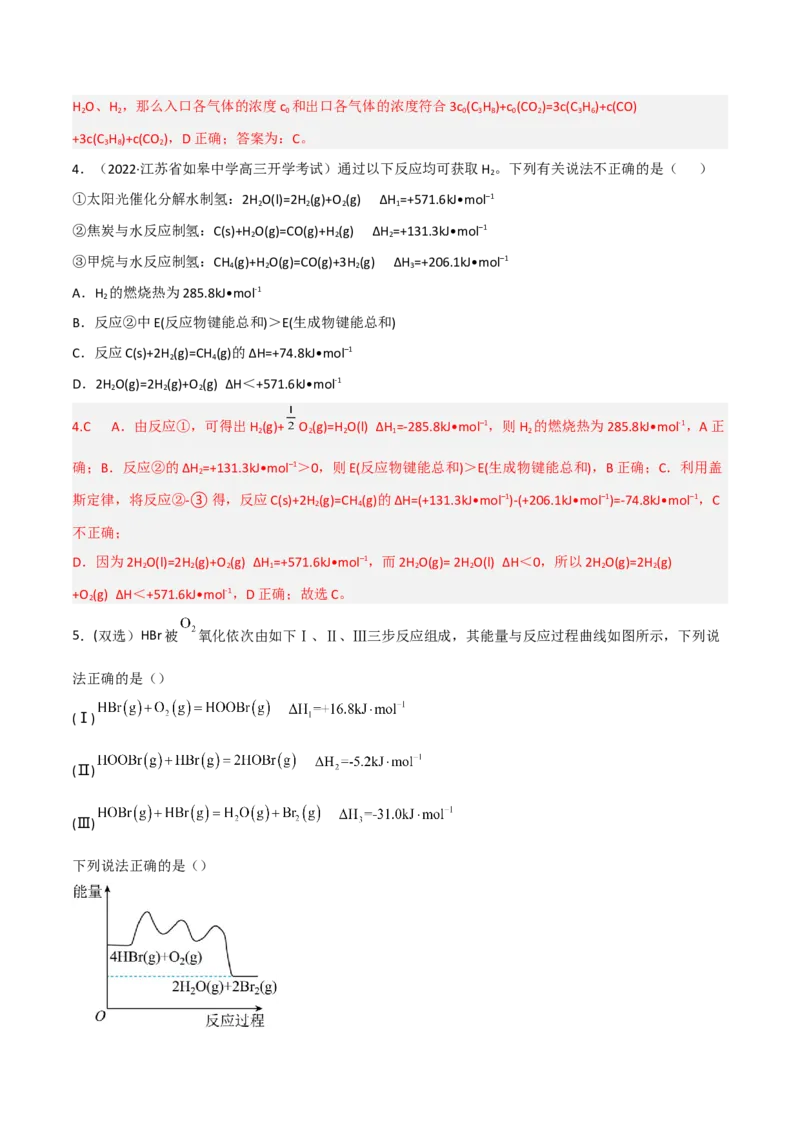
(3)已知反应器中还存在如下反应:
ⅰ.CH (g)+H O(g)=CO(g)+3H (g) ΔH
4 2 2 1
ⅱ.CO(g)+H O(g)=CO (g)+H (g) ΔH
2 2 2 2
ⅲ.CH (g)=C(s)+2H (g) ΔH
4 2 3
……
ⅲ为积炭反应,利用ΔH 和ΔH 计算ΔH 时,还需要利用___________反应的ΔH。
1 2 3
12.(1) 小于 2.02
(2)黑磷
(3)C(s)+2H O(g)=CO (g)+2H (g)或C(s)+CO (g)=2CO(g)
2 2 2 2
解析:(1)根据图像,初始时反应物的总能量为0,反应后生成物的总能量为-0.72 eV,则ΔH=-0.72 eV,
即ΔH小于0;由图像可看出,反应的最大能垒在过渡态2,此能垒E =1.86 eV-(-0.16 eV)=2.02 eV;
正
(2)由盖斯定律得P(s,黑磷)=P(s,红磷) ΔH=+21.7 kJ·mol-1,能量越低越稳定,P的三种同素异形体的
稳定性顺序为P(s,黑磷)>P(s,红磷)>P(s,白磷),因此黑磷最稳定;
(3)根据盖斯定律,ⅰ式+ⅱ式可得:CH (g)+2H O(g)=CO (g)+4H (g) ΔH +ΔH ,则(ⅰ式+ⅱ式)-ⅲ式
4 2 2 2 1 2可得:C(s)+2H O(g)=CO (g)+2H (g) ΔH;ⅰ式-ⅱ式可得:CH (g)+CO (g)=2CO(g)+2H (g) ΔH -ΔH ,则(ⅰ
2 2 2 4 2 2 1 2
式-ⅱ式)-ⅲ式可得:C(s)+CO (g)=2CO(g) ΔH,因此,要求反应ⅲ式的ΔH ,还必须利用反应C(s)+
2 3
2H O(g)=CO (g)+2H (g)或C(s)+CO (g)=2CO(g)的ΔH。
2 2 2 2