文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷01
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、二硫化钼的工业化制取(本题共20分)
1.二硫化钼(MoS ,难溶于水)具有良好的光、电性能,可由钼精矿(主要含MoS ,还含
2 2
NiS、CaMoO 等)为原料经过如下过程制得。(20分)
4
(1)“浸取”。向钼精矿中加入NaOH溶液,再加入NaClO溶液,充分反应后的溶液中含有
NaMoO 、NaSO 、NiSO 、NaCl。
2 4 2 4 4
①写出浸取时MoS 发生反应的离子方程式: 。
2
②浸取后的滤渣中含CaMoO。若浸取时向溶液中加入______________,可提高浸出液中
4
Mo元素的含量,原因是 。
a. NaCO b.稀硫酸 c.H O d.KNO
2 3 2 2 3
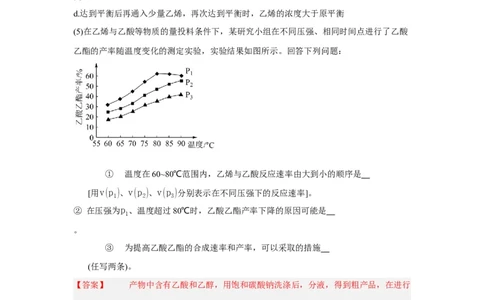
③浸取时,Mo元素的浸出率与时间的变化如图1所示。已知生成物对反应无影响,则反应
3~4min时,Mo元素的浸出率迅速上升的原因是
。
(2)“制硫代钼酸铵[(NH )MoS ,摩尔质量260g•mol-1]”。向浸出液中加入NH NO 和
4 2 4 4 3
HNO,析出(NH )MoO ,将(NH )MoO 溶于水,向其中加入(NH )S溶液,可得
3 4 2 4 13 4 2 4 13 4 2
(NH )MoS ,写出生成(NH )MoS 反应的化学方程式:
4 2 4 4 2 4
。
(3)“制MoS ”。(NH )MoS 可通过如下两种方法制取MoS :
2 4 2 4 2方法一:将(NH )MoS 在一定条件下加热,可分解得到MoS 、NH 、HS和硫单质。其中
4 2 4 2 3 2
NH 、HS和硫单质的物质的量之比为8:4:1。
3 2
方法二:将(NH )MoS 在空气中加热可得MoS ,加热时所得剩余固体的质量与原始固体质
4 2 4 2
量的比值与温度的关系如图2所示。
① 方法一中,所得硫单质的分子式为
。
② 方法二中,500℃可得到Mo的一种氧化物,该氧化物的化学式为
。
【答案】(1) MoS
2
+6OH-+9ClO-=MoO
❑
2−+2SO
❑
2−+9Cl-+3H
2
O CaMoO
4
(s)❑Ca2+
4 4 ⇌
(aq)+MoO (aq), a 加入NaCO 溶液,CO 结合Ca2+生成CaCO 沉淀,促进沉淀溶
❑ 2− 2 3 ❑ 2− 3
4 3
解平衡向离子化方向进行,使浸出液MoO 浓度增大,从而提高Mo元素浸出率 该
2−
❑
4
反应为放热反应,随着反应进行,溶液温度升高,反应速率加快
(2)(NH )MoO +16(NH)S+13HO=4(NH )MoS +26NH•H O或
4 2 4 13 4 2 2 4 2 4 3 2
(NH )MoO +16(NH)S=4(NH )MoS +13H O+26NH ↑
4 2 4 13 4 2 4 2 4 2 3
(3) S MoO
4 3
【解析】(1)①“浸取”,向钼精矿中加入NaOH溶液,再加入NaClO溶液,充分反应
后的溶液中含有NaMoO 、NaSO 、NiSO 、NaCl,即ClO-将Mo元素被氧化为MoO
2 4 2 4 4 ❑ 2−
4
、硫元素被氧化为反应为SO 而自身被还原为Cl-,反应为MoS +6OH-+9ClO-=MoO
❑ 2− 2 ❑ 2−
4 4+2SO +9Cl-+3H O。
2− 2
❑
4
②溶液中存在平衡CaMoO(s) Ca2+(aq)+ (aq),加入NaCO 消耗Ca2+使平衡正向,
4 MoO2- 2 3
4
⇌
浓度增大。
MoO2-
4
③加快反应速率可以从反应物的浓度增大、温度升高、反应中产生催化剂等方面考虑。该
反应中生成物对反应没有影响,所以该反应为放热反应导致体系温度升高加快反应速率。
(2)(NH )MoO 溶于水,向其中加入(NH )S溶液,可得(NH )MoS 和氨水,反应为
4 2 4 13 4 2 4 2 4
(NH )MoO +16(NH)S+13HO=4(NH )MoS +26NH•H O或
4 2 4 13 4 2 2 4 2 4 3 2
(NH )MoO +16(NH)S=4(NH )MoS +13H O+26NH ↑。
4 2 4 13 4 2 4 2 4 2 3
(3)①将(NH )MoS 在一定条件下加热,可分解得到MoS 、NH 、HS和硫单质。其中
4 2 4 2 3 2
NH 、HS和硫单质(S)的物质的量之比为8:4:1,根据已知信息写出方程式并按照N
3 2 x
原子和Mo原子守恒配平方程式为4(NH ) MoS 高温4MoS +8NH ↑+4H S↑+S ,即
4 2 4 2 3 2 x
4×4=2×4+4×1+x计算得x=4。该硫单质的化学式为S。
4
②由图可知起始(NH )MoS 的质量可视为260g即1mol,根据加热分解过程总Mo元素守恒
4 2 4
可知,最终氧化物中Mo的质量为96g,氧化物中氧元素的质量为144g-96g=48g,Mo原子
核O原子的个数比为1:3,氧化物的化学式为MoO 。
3
二、乙酸乙酯的制备工艺(本题共23分)
2.乙酸乙酯是一种用途广泛的精细化工产品,一般通过乙酸和乙醇酯化合生成。(23
分)
(1)在实验室利用上述方法制得乙酸乙酯含有杂质(不计副反应),简述如何提纯产品
。
(2)若用❑ 18O标记乙醇,该反应的化学方程式 。
(3)一定温度下该反应的平衡常数K=4.0。若按化学方程式中乙酸和乙醇的化学计量数比例
投料,则乙酸乙酯的平衡产率y= (计算时不计副
反应);若乙酸和乙醇的物质的量之比为n:1,相应平衡体系中乙酸乙酯的物质的量分数为
x,请绘制x随n变化的示意图 。
(4)近年来,用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,具有明显的经济优势,其合成的基本反应为 杂多酸 (Q>0)。在
CH =CH (g)+CH COOH(l)
⇌
CH COOC H (l)+Q
2 2 3 3 2 5
恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是
。
a.当乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol,反应已达到化学平衡
b.当乙烯的百分含量保持不变时,反应已达到化学平衡
c.在反应过程中任意时刻移除部分产品,都可以使平衡正向移动,但该反应的平衡常数不
变
d.达到平衡后再通入少量乙烯,再次达到平衡时,乙烯的浓度大于原平衡
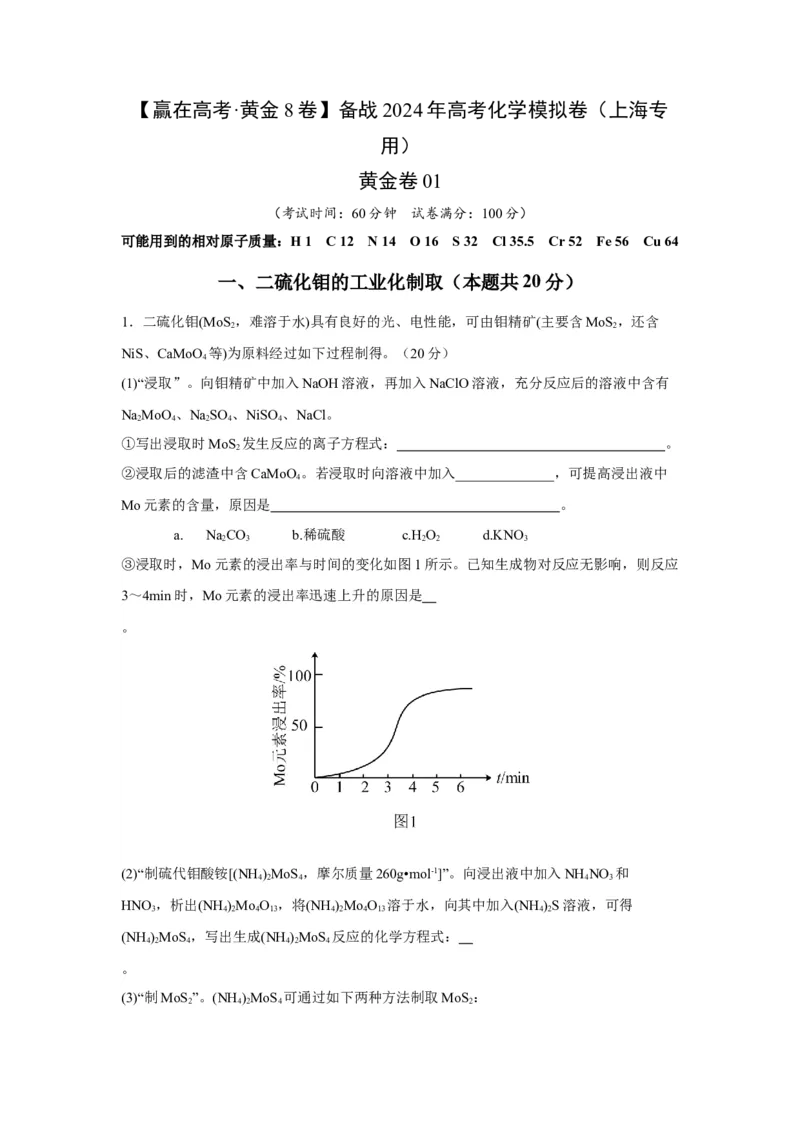
(5)在乙烯与乙酸等物质的量投料条件下,某研究小组在不同压强、相同时间点进行了乙酸
乙酯的产率随温度变化的测定实验,实验结果如图所示。回答下列问题:
① 温度在60~80℃范围内,乙烯与乙酸反应速率由大到小的顺序是
[用v(p )、v(p )、v(p )分别表示在不同压强下的反应速率]。
1 2 3
② 在压强为p 、温度超过80℃时,乙酸乙酯产率下降的原因可能是
1
。
③ 为提高乙酸乙酯的合成速率和产率,可以采取的措施
(任写两条)。
【答案】 产物中含有乙酸和乙醇,用饱和碳酸钠洗涤后,分液,得到粗产品,在进行
浓硫酸
蒸馏 CH 3 COOH+CH 3 CH 2 18OH ⇌ CH 3 CO18OCH 2 CH 3 +H 2 O 66.7%
△bc v(P )>v(P )>v(P ) 由图象可知,PMPa、
1 2 3 1
80℃时反应已达平衡且正反应放热,故压强不变升高温度平衡逆向移动产率下降 通入
乙烯气体或增大压强
【解析】(1)实验室用乙醇和乙酸在浓硫酸的作用下制备乙酸乙酯,乙酸乙酯中含有乙酸和
乙醇的杂质,利用饱和碳酸钠溶液可以中和乙酸、溶解乙醇,而且乙酸乙酯不溶于饱和碳
酸钠溶液,分液得到乙酸乙酯,再蒸馏除去残留的杂质;答案为产物中含有乙酸和乙醇,
用饱和碳酸钠洗涤后,分液,得到粗产品,在进行蒸馏;
(2)根据酯化反应的原理,酸脱羟基醇脱氢,因此乙醇中的18O会在酯中,化学方程式为
浓硫酸
CH 3 COOH+CH 3 CH 2 18OH ⇌ CH 3 CO18OCH 2 CH 3 +H 2 O;
△
(3)利用三等式进行计算;有
+
¿
❑
⇌
❑
CH COOH ¿
¿开始的物质的量 3 CH CH OH +
1 3 2
转化的物质的量 1 CH COOCH CH ¿
x ¿ 3 2 3 H O
平衡的物质的量 x 0 2
1−x 1−x ¿ x ¿ ¿
¿
x ¿
¿
¿
¿
2
x2 2
平衡常数K= =4,得x= ,转化率为3 ;
(1−x) 2 3 ×100%≈66.7%
1
乙酸和乙醇的物质的量之比,随乙酸的物质的量增加,乙酸乙酯的产量也会增加,当n:11
=1:1时,乙酸乙酯的物质的量分数达到最大 ,乙酸的物质的量继续增大,乙酸乙酯物
3
质的量分数反而逐渐减小图象如图所示: ;
(4)a.当乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol,表示的都是正反应速率,无法
判断正逆反应速率是否相等,a错误;
b.当体系中乙烯的百分含量保持不变,说明正逆反应速率相等,该反应已达到化学平衡,
b正确;
1
c.产品减少,平衡正向移动,但是由于该反应的平衡常数表达式K= ,温度
c(CH =CH )
2 2
不变则平衡常数不变,所以平衡时乙烯的浓度与原平衡相等,c正确;
d.乙酸和乙酸乙酯为液态,在平衡常数表达式中不能标出,该反应的平衡常数表达式为:
1
K= ,达到平衡后再通入少量乙烯,再次达到平衡时,乙烯的浓度不变,d
c(CH =CH )
2 2
错误;
故答案为:bc;
(5)①温度一定压强增大平衡正向进行,反应速率增大,图象分析可知P>P>P,则温度
1 2 3
在60~80℃范围内,乙烯与乙酸酯化合成反应速率由大到小的顺序是v(P)>v(P)>v
1 2
(P);
3
②由图象可知,PMPa、80℃时反应已达平衡且正反应放热,故压强不变升高温度平衡逆
1
向移动产率下降;
③为提高乙酸乙酯的合成速率和产率,改变的条件加快反应速率且平衡正向进行,可以增
大反应物浓度或增大压强等,通入乙烯气体或增大压强。
三、化学键与分子间作用力理论(本题共18分)
3.关于化学键和分子间作用力的理论是关于物质结构的基本理论,回答下列问题:(18
分)(1) M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其
中有2个未成对电子。下列说法不正确的是_________
A.氢化物沸点:XZ
(2)用“>”或“<”填空:
第一电离能 离子半径 熔点 酸性
O2- Na
Si S NaCl Si HSO HClO
+ 2 4 4
(3)MgCl 在工业上应用广泛,可由 MgO 制备。MgO 的熔点比 BaO 的熔点
2
(填“高” 或“低”)。
(4)HCHO 分子的立体构型为 形,它与 H 加成后,加成产物的熔、沸点比
2
CH 的熔、沸点高,其主要原因是 (须指明加成产物是何物质) 。
4
(5)已知 HO 分子的结构如图所示:HO 分子不是直线形的,两个氢原子犹如在半展开的
2 2 2 2
书的两面上,两个氧原子在书脊位置上,书页夹角为 93o52′,而两个O—H 键与O—O 键
的夹角均为96o52′。
①HO 分子是含有 键和 键的 (填“极性”或“非极性”)分子。
2 2
② HO 难溶于 CS,简要说明理由: 。
2 2 2
【答案】(1) A
(2) < > < <
(3)高
(4) 平面三角 加成产物 CHOH 分子之间能形成氢键
3
(5) 极性 非极性 极性 HO 为极性分子,而 CS 为非极性溶剂,根据
2 2 2
“相似相溶”规律,HO 难溶于 CS
2 2 2
【解析】(1)M、W、X、Y、Z原子序数依次增大,基态Z原子的电子填充了3个能级,
则分别为1s、2s、2p,有两个未成对电子,Z能形成2条单键,则Z电子排布式为1s22s22p4,Z为O,X形成4条单键,X为C,M形成1条单键,M为H,则Y为N,W为
B。
A.C的氢化物有多种,如碳原子数较多的烃沸点较高,因此无法确定氢化物的沸点
CO2-,D正确;
故答案选A。
(2)第一电离能Si Na+。NaCl为离子晶体,Si为共价晶体,所以熔点NaCl;<;
2 4 4
<;
(3)MgO 、 BaO 均为离子晶体,Mg2+半径小于Ba2+,MgO离子键强,熔点高。答案:
高;
(4)HCHO中心碳原子形成3个σ键,中心碳原子无孤电子对,所以HCHO 分子的立体
构型为平面三角形。HCHO它与 H 加成生成乙醇。乙醇的熔、沸点比 CH 的熔、沸点高,
2 4
其主要原因是加成产物 CHOH 分子之间能形成氢键,答案:平面三角;加成产物
3
CHOH 分子之间能形成氢键;
3
(5)①HO 分子含有的H-O键为极性键, O-O键为非极性键,正负电荷中心不重合,为
2 2
极性分子。答案:极性;非极性;极性;
②分子的溶解性可根据“相似相溶”规律解释,HO 为极性分子,而 CS 为非极性溶剂,
2 2 2
根据“相似相溶”规律,HO 难溶于 CS。
2 2 2
四、抗肿瘤药物阿法替尼的合成(本题共24分)
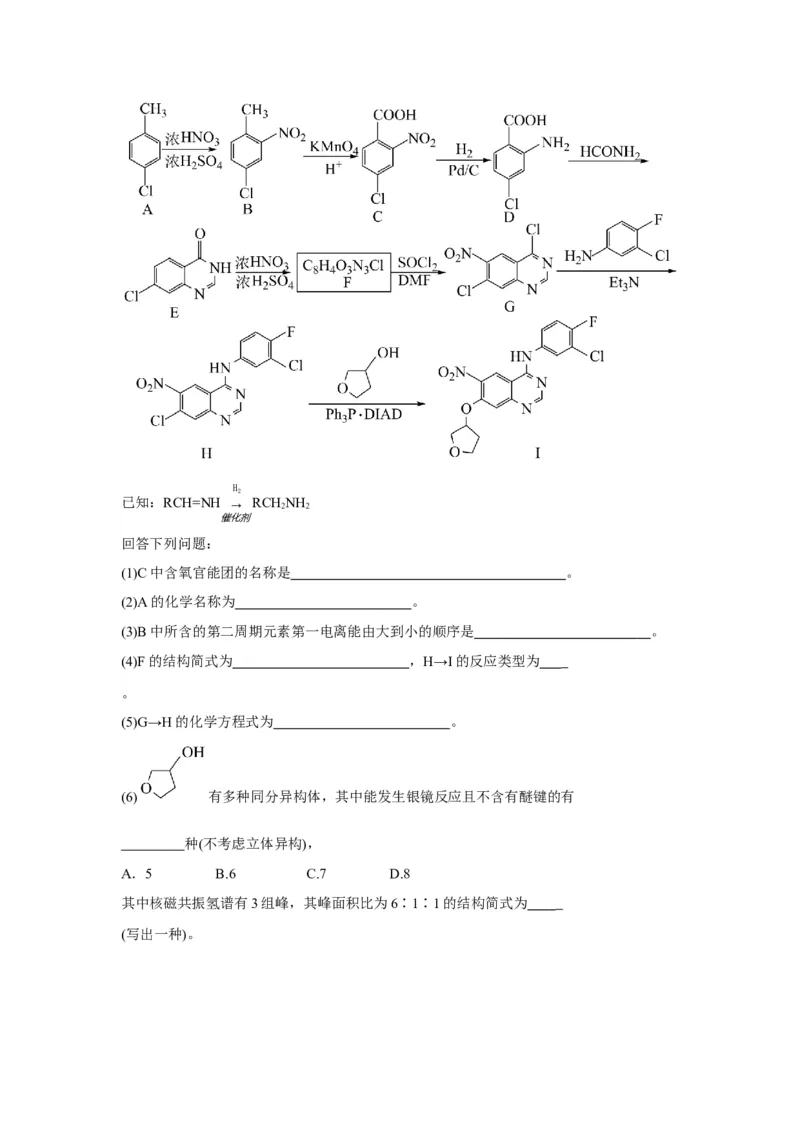
4.化合物I是制备抗肿瘤药物阿法替尼的重要中间体,化合物I的一种合成路线如图。
(24分)H
2
已知:RCH=NH → RCHNH
2 2
催化剂
回答下列问题:
(1)C中含氧官能团的名称是 。
(2)A的化学名称为 。
(3)B中所含的第二周期元素第一电离能由大到小的顺序是 。
(4)F的结构简式为 ,H→I的反应类型为
。
(5)G→H的化学方程式为 。
(6) 有多种同分异构体,其中能发生银镜反应且不含有醚键的有
种(不考虑立体异构),
A.5 B.6 C.7 D.8
其中核磁共振氢谱有3组峰,其峰面积比为6∶1∶1的结构简式为
(写出一种)。(7)参考上述合成路线,以HOOCCH NH 、HCONH 为原料合成 ,合成过程中无
2 2 2
机试剂任选 。
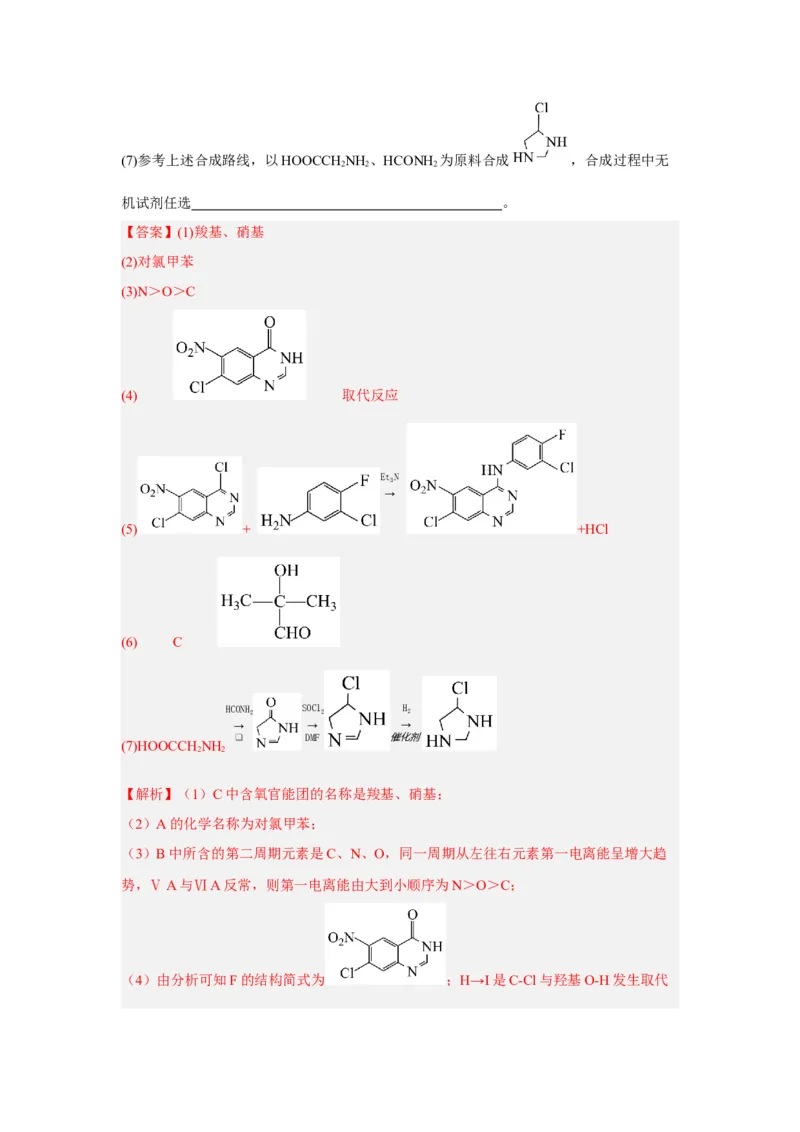
【答案】(1)羧基、硝基
(2)对氯甲苯
(3)N>O>C
(4) 取代反应
Et N
3
→
(5) + +HCl
(6) C
HCONH SOCl H
2 2 2
→ → →
❑ DMF 催化剂
(7)HOOCCH NH
2 2
【解析】(1)C中含氧官能团的名称是羧基、硝基;
(2)A的化学名称为对氯甲苯;
(3)B中所含的第二周期元素是C、N、O,同一周期从左往右元素第一电离能呈增大趋
势,ⅤA与ⅥA反常,则第一电离能由大到小顺序为N>O>C;
(4)由分析可知F的结构简式为 ;H→I是C-Cl与羟基O-H发生取代反应,反应类型为取代反应;
(5)G→H是氨基与C-Cl发生取代反应,化学方程式为 +
Et N
3
→
+HCl;
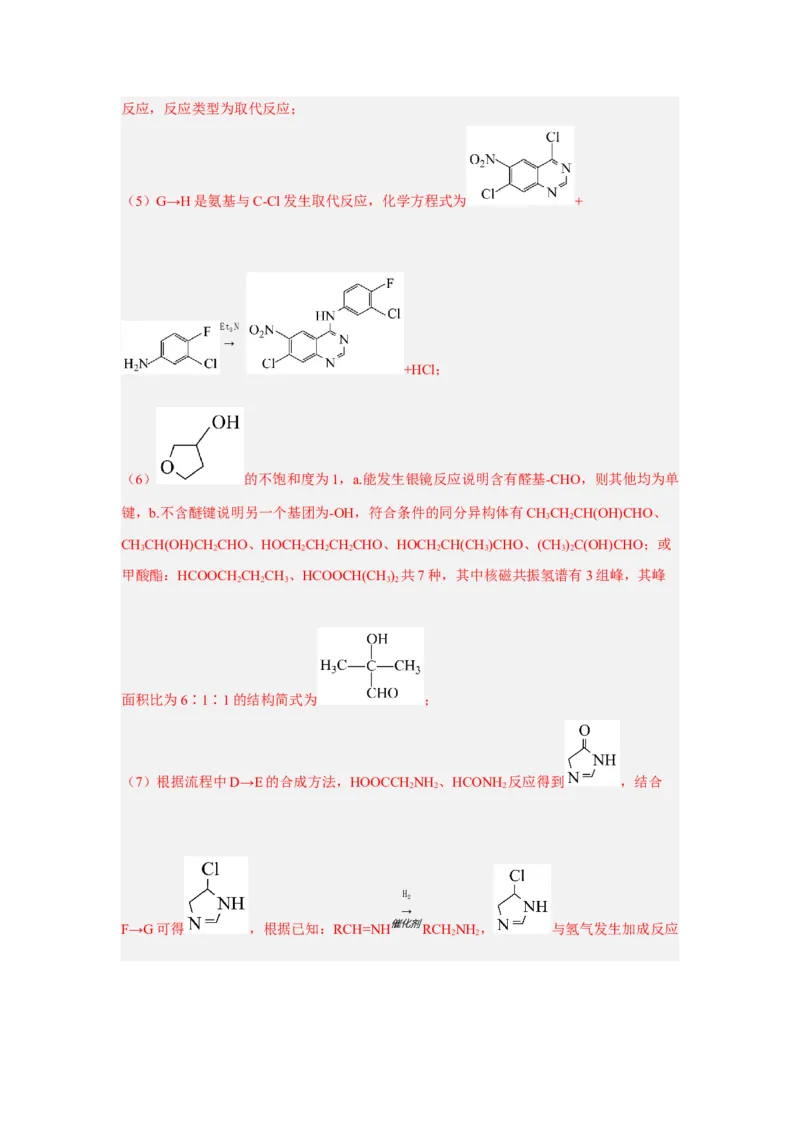
(6) 的不饱和度为1,a.能发生银镜反应说明含有醛基-CHO,则其他均为单
键,b.不含醚键说明另一个基团为-OH,符合条件的同分异构体有CHCHCH(OH)CHO、
3 2
CHCH(OH)CH CHO、HOCH CHCHCHO、HOCH CH(CH )CHO、(CH)C(OH)CHO;或
3 2 2 2 2 2 3 3 2
甲酸酯:HCOOCH CHCH、HCOOCH(CH ) 共7种,其中核磁共振氢谱有3组峰,其峰
2 2 3 3 2
面积比为6∶1∶1的结构简式为 ;
(7)根据流程中D→E的合成方法,HOOCCH NH 、HCONH 反应得到 ,结合
2 2 2
H
2
→
F→G可得 ,根据已知:RCH=NH催化剂RCHNH , 与氢气发生加成反应
2 2HCONH SOCl H
2 2 2
→ → →
可得 ,合成路线为:HOOCCH 2 NH 2 ❑ DMF 催化剂 。
五、载人航天中二氧化碳的清除方法(本题共15分)
5.吸入氧气、排出二氧化碳,这看似再简单不过的新陈代谢,在遥远的太空中却并不容易,
因为在航天服、航天器、空间站等密闭系统中,CO 浓度会高得多,而超过一定浓度会导
2
致呼吸急促、头晕头痛、昏迷甚至死亡,因此必须通过一定方法将CO 清除。(15分)
2
I.非再生式氢氧化锂(LiOH)除碳技术
(1)我国“飞天”舱外航天服采用非再生式氢氧化锂(LiOH)吸附CO 生成碳酸锂,该技术设
2
备操作简单,功能可靠,适用于短期出舱任务。吸附时发生反应的化学方程式为
。采用LiOH而不用NaOH的原因是 。
Ⅱ.再生式快速循环胺技术
(2)以固态胺作为吸附剂,吸附CO 与水蒸气。当固态胺吸附饱和后,将其暴露于真空中,
2
破坏碳酸氢盐的化学键,释放出CO,从而完成吸附剂的再生。该技术大大提升了舱外航
2
天服的续航时间。固态胺的吸附是 变化。
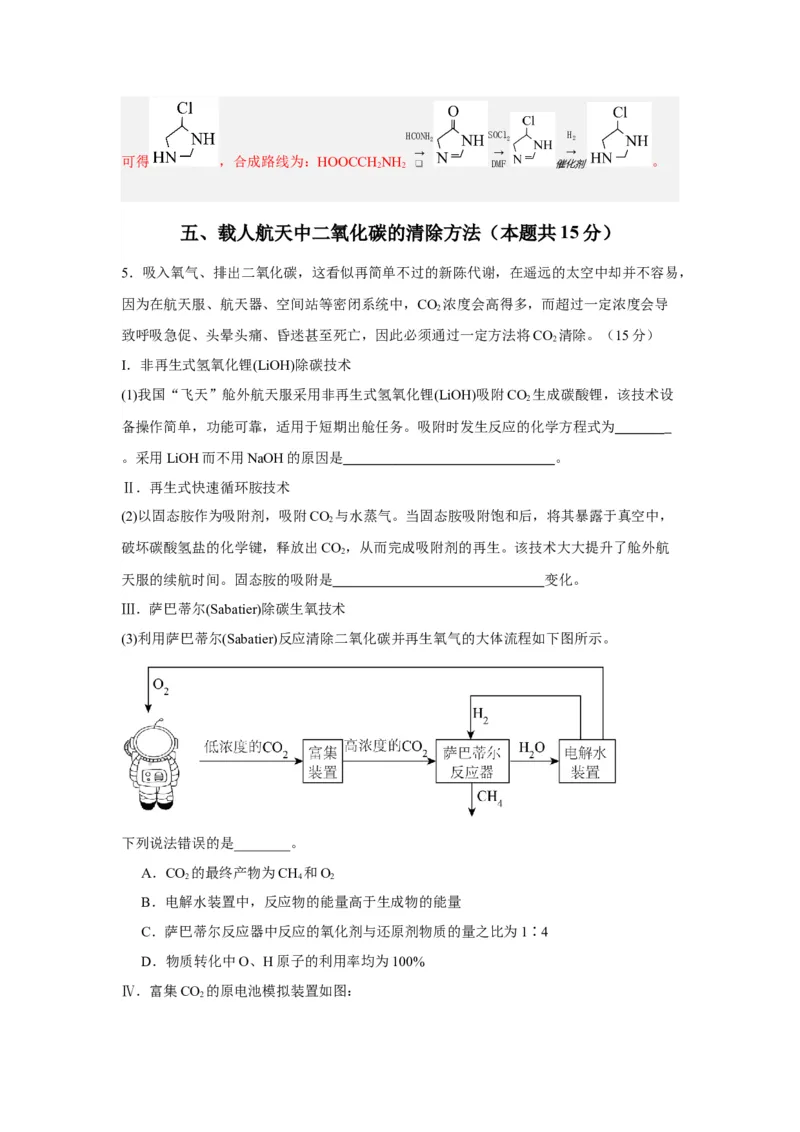
Ⅲ.萨巴蒂尔(Sabatier)除碳生氧技术
(3)利用萨巴蒂尔(Sabatier)反应清除二氧化碳并再生氧气的大体流程如下图所示。
下列说法错误的是________。
A.CO 的最终产物为CH 和O
2 4 2
B.电解水装置中,反应物的能量高于生成物的能量
C.萨巴蒂尔反应器中反应的氧化剂与还原剂物质的量之比为1∶4
D.物质转化中O、H原子的利用率均为100%
Ⅳ.富集CO 的原电池模拟装置如图:
2(4)b极为 极,a电极上发生的电极反应为
。
(5)上述电极材料采用多孔碳载镍,“多孔”的优点是 。
(6)该装置若消耗2 mol H ,则理论上在b极除去CO 的体积约为
2 2
L(标准状况下)。
【答案】(1) 2LiOH+CO =Li CO+H O 单位质量时,LiOH吸收的二氧化碳的量更
2 2 3 2
多
(2)化学
(3)BD
(4) 正 H+CO -2e-=H O+CO
2 2− 2 2
❑
3
(5)提高气体在电极表面的吸附量,使其与溶液充分接触,提高反应速率
(6)44.8
(7)AD
【解析】(1)氢氧化锂(LiOH)吸附CO 生成碳酸锂,化学方程式为:
2
2LiOH+CO =Li CO+H O。LiOH的摩尔质量小于NaOH,单位质量时,LiOH吸收的二氧
2 2 3 2
化碳的量更多。
(2)固态胺的吸附过程中破坏了化学键,是化学变化。
(3)A.由图可知,CO 的最终产物为CH 和O,故A正确;
2 4 2
B.电解水装置中,电能转化为化学能,反应物的能量低于生成物的能量,故B错误;
C.由图可知,萨巴蒂尔反应器中发生反应:CO+4H =CH +2H O,氧化剂与还原剂物质的
2 2 4 2
量之比为1∶4,故C正确;
D.由图可知,该反应的总方程式为:CO+2H =CH +O ,O原子的利用率小于100%,故
2 2 4 2
D错误;故选BD。
(4)b极通入空气为正极,a极通入H 为负极,H 在负极失去电子生成HO,用CO
2 2 2 ❑ 2−
3
来配平电荷,根据得失电子守恒和电荷守恒配平电极方程式为:H+CO -2e-
2 2−
❑
3
=H O+CO。
2 2
(5)上述电极材料采用多孔碳载镍,“多孔”的优点是提高气体在电极表面的吸附量,使
其与溶液充分接触,提高反应速率。
(6)O 在正极得到电子生成CO ,根据得失电子守恒和电荷守恒配平电极方程式为:
2 ❑ 2−
3
O+2CO +4e-=2CO ,该装置若消耗2 mol H ,转移4mol电子,则b极吸收2mol CO,
2 2 2− 2 2
❑
3
标准状况下的体积为44.8L。