文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(福建专用)
黄金卷05
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32
第Ⅰ卷
一、单项选择题:共10题,每题4分,共40分。每题只有一个选项最符合题意。
1.央视栏目《国家宝藏》介绍了历史文化知识,彰显了民族自信、文化自信,其中也蕴含着许多化学知
识。下列说法错误的是
A.传统鎏金士艺是将金溶于汞中制成“金汞漆”,涂在器物表面,然后加火除汞,鎏金工艺利用了汞
的挥发性
B.《吕氏春秋•别类编》中有关于青铜的记载“金(铜)柔锡柔,合两柔则为刚”。“合两柔则为刚”体
现了合金的硬度通常大于各组分金属的特点
C.宋•王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是碱式碳酸铜
D.明代《本草纲目》中记载:“……,惟以糯米,或粳米,……,和曲酿瓮中七日,以甑蒸取”。酒
化酶将葡萄糖转化为乙醇时,温度越高反应速率一定越快
【答案】D
【详解】A.Hg常温下为液体,易挥发,加热除去汞利用了汞的挥发性,A正确;
B.铜和锡的合金硬度较大,合两柔则为刚体现了合金硬度的特点,即合金的硬度通常大于各组分金属的
硬度,B正确;
C.铜绿的主要成分是碱式碳酸铜Cu (OH) CO,C正确;
2 2 3
D.温度过高会使酶失去活性,使反应速率变慢,D错误;
故选D。
2.解热镇痛药双氯芬酸钠栓主要成分的结构如图所示。下列有关该物质的说法错误的是
A.化学式为 B.1mol该物质最多能消耗C.1mol该物质最多能消耗 D.能发生取代反应、氧化反应
【答案】A
【详解】A.化学式应该为C H ClONNa,A选项错误;
14 10 2 2
B.分子中苯环上的氯原子发生水解生成HCl和酚羟基,故最多消耗4molNaOH,B选项正确;
C.分子中亚氨基-NH-和-COONa分别消耗1molHCl,C选项正确;
D.该有机物分子中苯环上可以发生取代反应,亚氨基可以发生氧化反应,D选项正确;
答案选A。
3. 为阿伏加德罗常数的值。HgS溶于“王水”的反应如下:
(未配平)。下列叙述正确的是
A. 盐酸中含HCl分子数为
B.标准状况下,生成2.24LNO时转移电子数为
C.该反应中氧化剂与还原剂物质的量之比为
D.生成9.6gS时,同时生成氢氧键的数目为
【答案】B
【分析】 中N元素化合价由+5降低为+2,氧化剂是 ;HgS中S元素化合价由-2升高为0,还
原剂是HgS;盐酸没有参与氧化还原反应,根据得失电子守恒,反应方程式为
;
【详解】A.盐酸中HCl完全电离为 和 ,溶液中不存在HCl分子,故A错误;
B.反应过程中N元素化合价由+5降低为+2,生成1molNO时转移3mol电子,故生成0.1molNO时转移
0.3mol电子,故B正确;
C. 中N元素化合价由+5降低为+2,氧化剂是 ;HgS中S元素化合价由-2升高为0,还原剂是
HgS;盐酸没有参与氧化还原反应,根据得失电子守恒,两者物质的量之比为 ,故C错误;
试卷第2页,共3页D.根据 ,生成3molS时,生成4molH O,所以同
2
时生成8molH-O键,故D错误;
选B。
4.W、X、Y、Z为原子序数依次增大的短周期主族元素,其中W的核电荷数等于Y的最外层电子数,Z
的电子总数是X的2倍,四种元素可形成离子化合物 。下列说法错误的是
A. 和 中阴阳离子个数比相同
B.水溶液中 与 之间能发生反应
C. 与 可以发生氧化还原反应生成
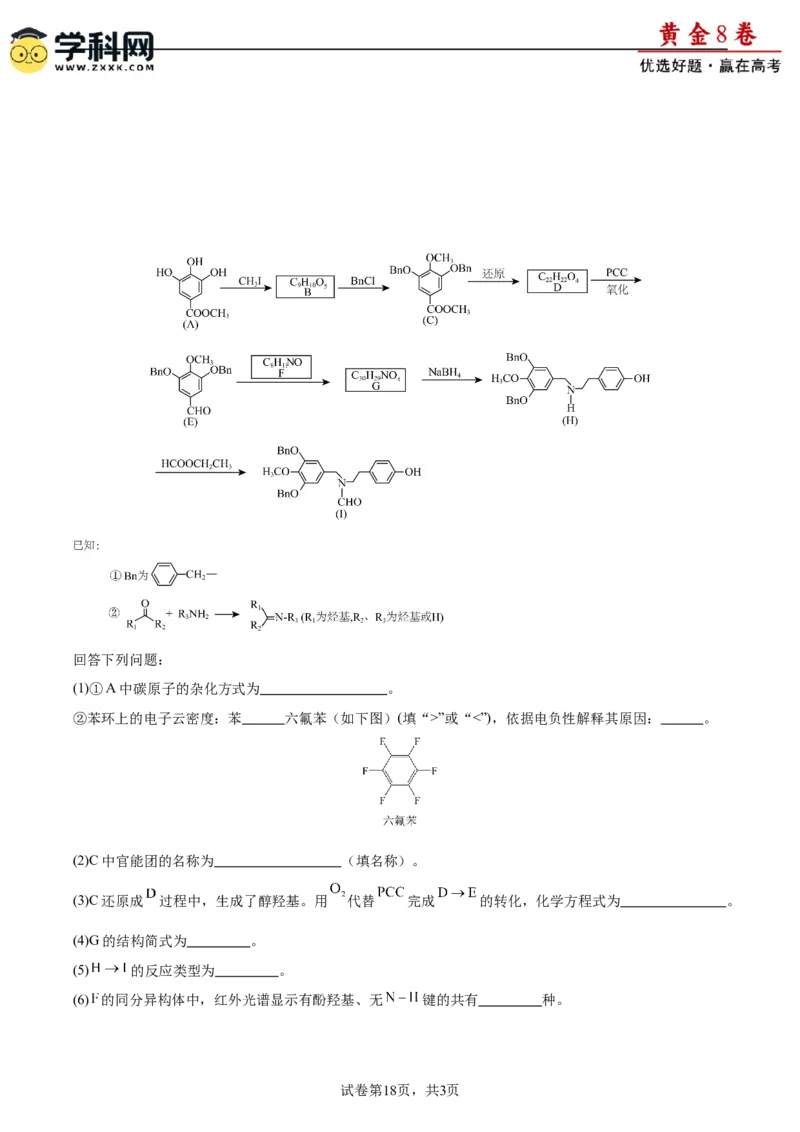
D.X和Z的最简单氢化物的稳定性X”或“<”),依据电负性解释其原因: 。
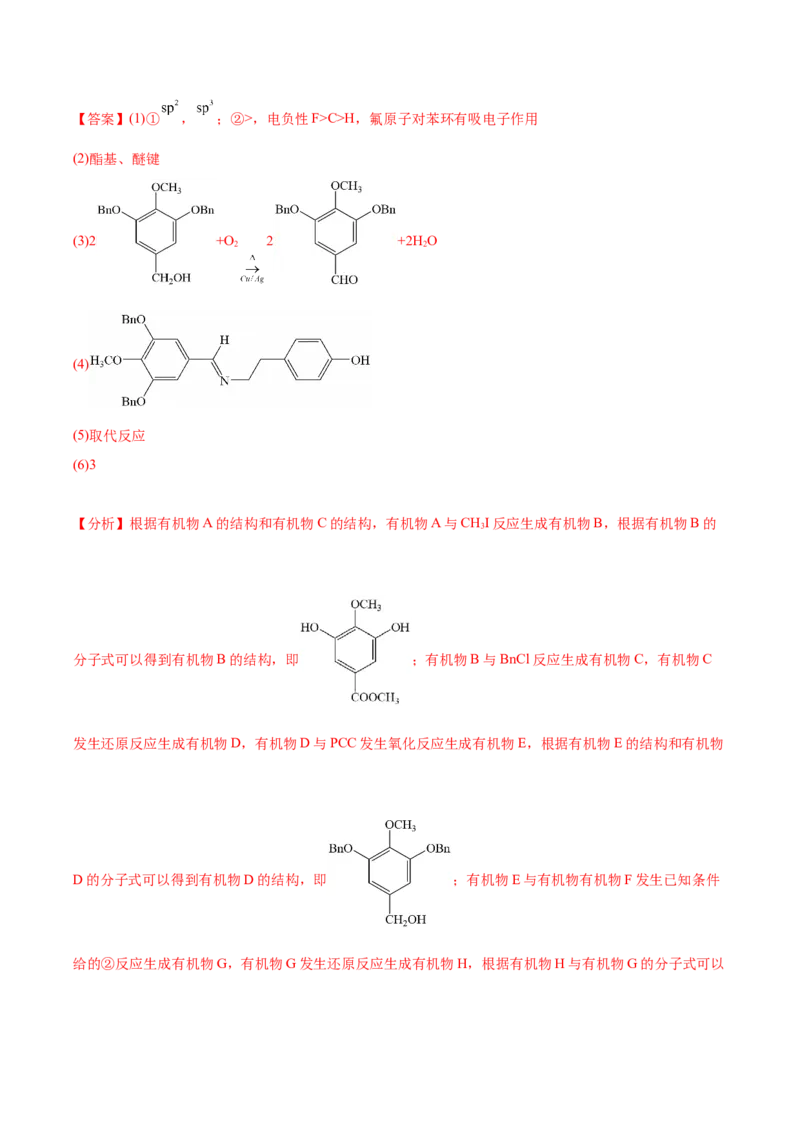
(2)C中官能团的名称为 (填名称)。
(3)C还原成 过程中,生成了醇羟基。用 代替 完成 的转化,化学方程式为 。
(4)G的结构简式为 。
(5) 的反应类型为 。
(6) 的同分异构体中,红外光谱显示有酚羟基、无 键的共有 种。
试卷第18页,共3页【答案】(1)① , ;②>,电负性F>C>H,氟原子对苯环有吸电子作用
(2)酯基、醚键
(3)2 +O 2 +2H O
2 2
(4)
(5)取代反应
(6)3
【分析】根据有机物A的结构和有机物C的结构,有机物A与CHI反应生成有机物B,根据有机物B的
3
分子式可以得到有机物B的结构,即 ;有机物B与BnCl反应生成有机物C,有机物C
发生还原反应生成有机物D,有机物D与PCC发生氧化反应生成有机物E,根据有机物E的结构和有机物
D的分子式可以得到有机物D的结构,即 ;有机物E与有机物有机物F发生已知条件
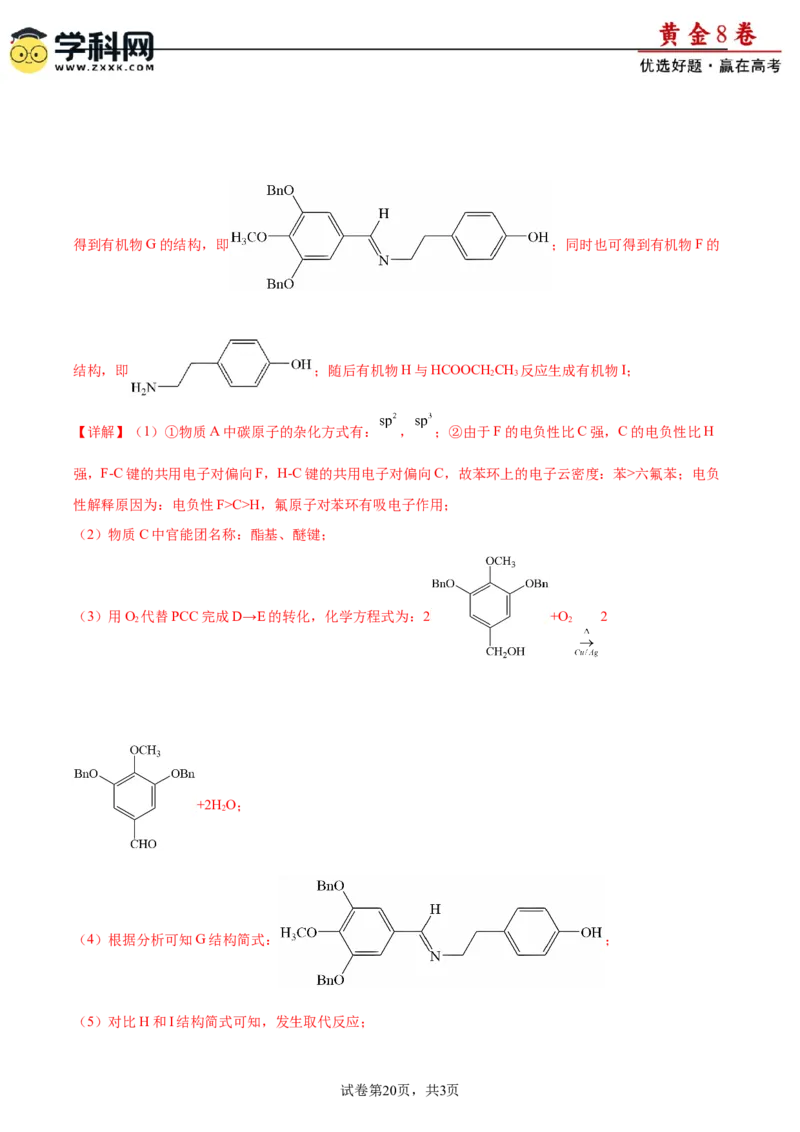
给的②反应生成有机物G,有机物G发生还原反应生成有机物H,根据有机物H与有机物G的分子式可以得到有机物G的结构,即 ;同时也可得到有机物F的
结构,即 ;随后有机物H与HCOOCH CH 反应生成有机物I;
2 3
【详解】(1)①物质A中碳原子的杂化方式有: , ;②由于F的电负性比C强,C的电负性比H
强,F-C键的共用电子对偏向F,H-C键的共用电子对偏向C,故苯环上的电子云密度:苯>六氟苯;电负
性解释原因为:电负性F>C>H,氟原子对苯环有吸电子作用;
(2)物质C中官能团名称:酯基、醚键;
(3)用O 代替PCC完成D→E的转化,化学方程式为:2 +O 2
2 2
+2H O;
2
(4)根据分析可知G结构简式: ;
(5)对比H和I结构简式可知,发生取代反应;
试卷第20页,共3页(6)F的同分异构体中不含有N-H键,说明结构中含有 ,结构,又因红外中含有酚羟基,说
明结构中含有苯环和羟基,固定羟基的位置 有邻、间、对三种情况,故有3种同分异构体。