文档内容
解密共价键
重难点 题型 分值
1. 熟知共价键的概念与形成,知道共价键的特
征——具有饱和性和方向性。
2. 能够从不同的角度对共价键分类,会分析σ
重点
键和π键的形成及特点。
选择题、填空
3. 知道键能、键长、键角等键参数的概念,能 4-6分
题
用键参数说明简单分子的某些性质
1. 能够从不同的角度对共价键分类,会分析σ
难点 键和π键的形成及特点。
2. 利用键参数说明简单分子的某些性质
第1页【课前回顾】
1. 化学键:
(1)定义:是指相邻的原子之间强烈的相互作用。
(2)分类:化学键包括:共价键、离子键、金属键。共价键包括:极性键和非极性键
2. 化学反应的本质:旧化学键的断裂和新化学键形成的过程。断裂化学键需要吸收能量,
形成化学键需要放出能量,导致化学反应过程中能量变化(吸热或放热)。
3. 由离子键构成的化合物叫做离子化合物,离子化合物中一定含有离子键,可能含有共
价键。以共用电子对形成的化合物叫做共价化合物。共价化合物中只含有共价键,但只含
共价键的物质不一定是共价化合物,如O、N 等单质中只含有共价键。
2 2
【注意】并不是所有的物质都含有化学键,例如:稀有气体。
一、共价键的定义、特征与形成条件
1. 共价键的定义
原子间通过共用电子对所形成的相互作用称为共价键。
【注意】1 使离子相结合或原子相结合的化学作用力叫做化学键,共价键是化学键的
一种,化学键包括共价键、离子键和金属键。
共价键的本质:原子间通过共用电子对(即电子云重叠)产生的强烈作用。
2. 共价键的特征
共价键具有饱和性和方向性。
(1)共价键的饱和性
共价键的饱和性与形成共价键的原子的未成对电子数目有关。
①按照价键理论,一个原子有几个未成对电子,便可和几个自旋状态相反的电子配对
成键,这就是共价键的饱和性。
② 共价键的饱和性决定了各种原子相互结合形成分子时的数量关系。
举例:用电子排布图表示HF分子中共用电子对的形成如下:
由以上分析可知,F原子与H原子间只能形成1 个共价键,所形成的简单化合物为
HF。同理,O原子与2 个H原子形成2 个共用电子对,2个N原子间形成3 个共用电子对。
第2页再比如:H原子、Cl原子都只有一个未成对电子,因而只能形成H、HCl、C1 分子,
2 2
不能形成H、HCl、Cl 分子。
3 2 3
【思考】1 NH 分子中N原子为1个,氢原子只能为3个的原因?
3
N和H原子的电子式分别为 和H·,N原子最外层有3个未成对电子,H原子有1
个未成对电子,形成共价键时每个N原子只需与3个H原子分别形成3对共用电子即可达
到稳定状态,共价键达到饱和,从而决定了分子中H原子个数。
(2)方向性
在形成共价键时,两个参与成键的原子轨道总是尽可能沿着电子出现概率最大的方向
重叠成键,原子轨道重叠越多,电子在两核间出现的概率越大,体系的能量下降得越多,
形成的共价键也就越牢固。因此,共价键具有方向性。
【划重点】共价键的饱和性与方向性
(1)所有的共价键都具有饱和性,但并不是所有的共价键都具有方向性,如两个 s轨
道形成的共价键就没有方向性(原因是s轨道是球形的)。
(2)共价键的饱和性决定了分子的组成,而共价键的方向性决定了分子的空间结构。
3. 形成条件:通常电负性相同或差值小(电负性之差小于1. 7)的非金属元素原子之间
或者个别金属元素与非金属元素原子之间形成共价键。
【注意】2 ①AlC1 的组成元素均为较活泼的元素,但Al与Cl 原子间以共价键结合,
3
AlCl 为共价化合物。类似的还有BeCl 等。②共价键分为极性键和非极性键。同种元素的
3 2
原子之间形成的共价键是非极性键,不同元素的原子之间形成的共价键是极性键。
【即时练】下列说法正确的是( )
A. 若把HS分子写成HS分子,违背了共价键的饱和性
2 3
B. HO+的存在说明共价键不具有饱和性
3
C. 所有共价键都有方向性
D. 两个原子轨道发生重叠后,电子仅存在于两核之间
【答案】A
【解析】S原子有两个未成对电子,根据共价键的饱和性,形成的氢化物为 HS,A项
2
对;HO能结合1个H+形成HO+,不能说明共价键不具有饱和性,B项错;H 分子中,H
2 3 2
原子的s轨道成键时,因为s轨道为球形,所以H 分子中的H—H键没有方向性,C项错;
2
两个原子轨道发生重叠后,电子只是在两核之间出现的概率大,D项错。
【考点】共价键的形成与特征
【题点】共价键的特征
第3页二、共价键的类型
1. σ键
(1)概念:未成对电子的原子轨道采取“头碰头”的方式重叠形成的共价键叫σ键。
(2)种类及形成过程(以H 分子、Cl 分子和HCl分子为例说明)
2 2
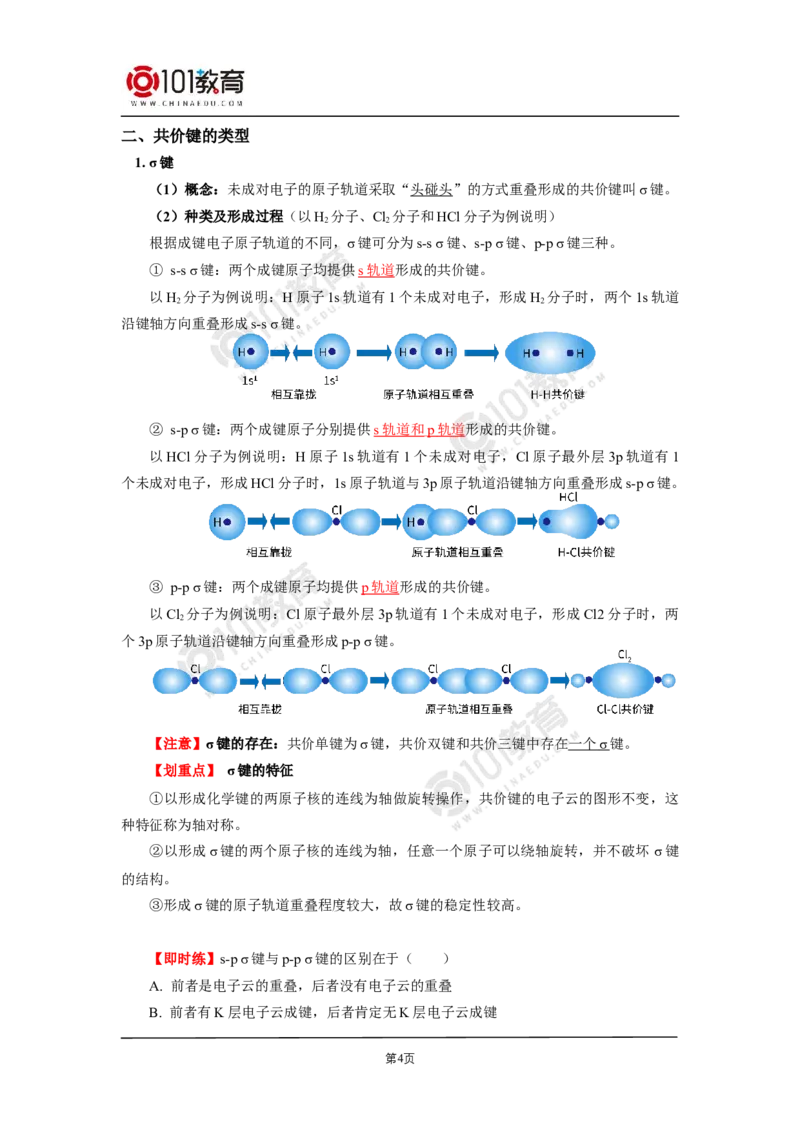
根据成键电子原子轨道的不同,σ键可分为s-s σ键、s-p σ键、p-p σ键三种。
① s-s σ键:两个成键原子均提供 s 轨道 形成的共价键。
以H 分子为例说明:H原子1s轨道有1个未成对电子,形成H 分子时,两个1s轨道
2 2
沿键轴方向重叠形成s-s σ键。
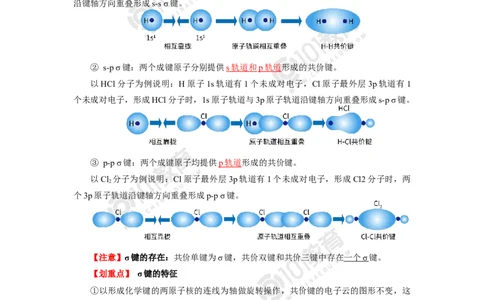
② s-p σ键:两个成键原子分别提供 s 轨道和 p 轨道 形成的共价键。
以HCl分子为例说明:H原子1s轨道有1个未成对电子,Cl原子最外层3p轨道有1
个未成对电子,形成HCl分子时,1s原子轨道与3p原子轨道沿键轴方向重叠形成s-p σ键。
③ p-p σ键:两个成键原子均提供 p 轨道 形成的共价键。
以Cl 分子为例说明:Cl原子最外层3p轨道有1个未成对电子,形成Cl2分子时,两
2
个3p原子轨道沿键轴方向重叠形成p-p σ键。
【注意】σ键的存在:共价单键为σ键,共价双键和共价三键中存在 一个 σ 键。
【划重点】 σ键的特征
①以形成化学键的两原子核的连线为轴做旋转操作,共价键的电子云的图形不变,这
种特征称为轴对称。
②以形成σ键的两个原子核的连线为轴,任意一个原子可以绕轴旋转,并不破坏 σ键
的结构。
③形成σ键的原子轨道重叠程度较大,故σ键的稳定性较高。
【即时练】s-p σ键与p-p σ键的区别在于( )
A. 前者是电子云的重叠,后者没有电子云的重叠
B. 前者有K层电子云成键,后者肯定无K层电子云成键
第4页C. 前者是电子云“头碰头”重叠,后者是电子云“肩并肩”重叠
D. 前者是电子云“肩并肩”重叠,后者是电子云“头碰头”重叠
【答案】B
【解析】凡是σ键,都是电子云“头碰头”的重叠。s-p σ键是由s能级的电子云
(“球形”)与p能级的电子云(“哑铃形”)以“头碰头”重叠而成键的。由于 K层不
存在p能级,故p-p σ键不可能有K层电子云成键。
【考点】共价键的类型
【题点】σ键与π键的比较
2. π键
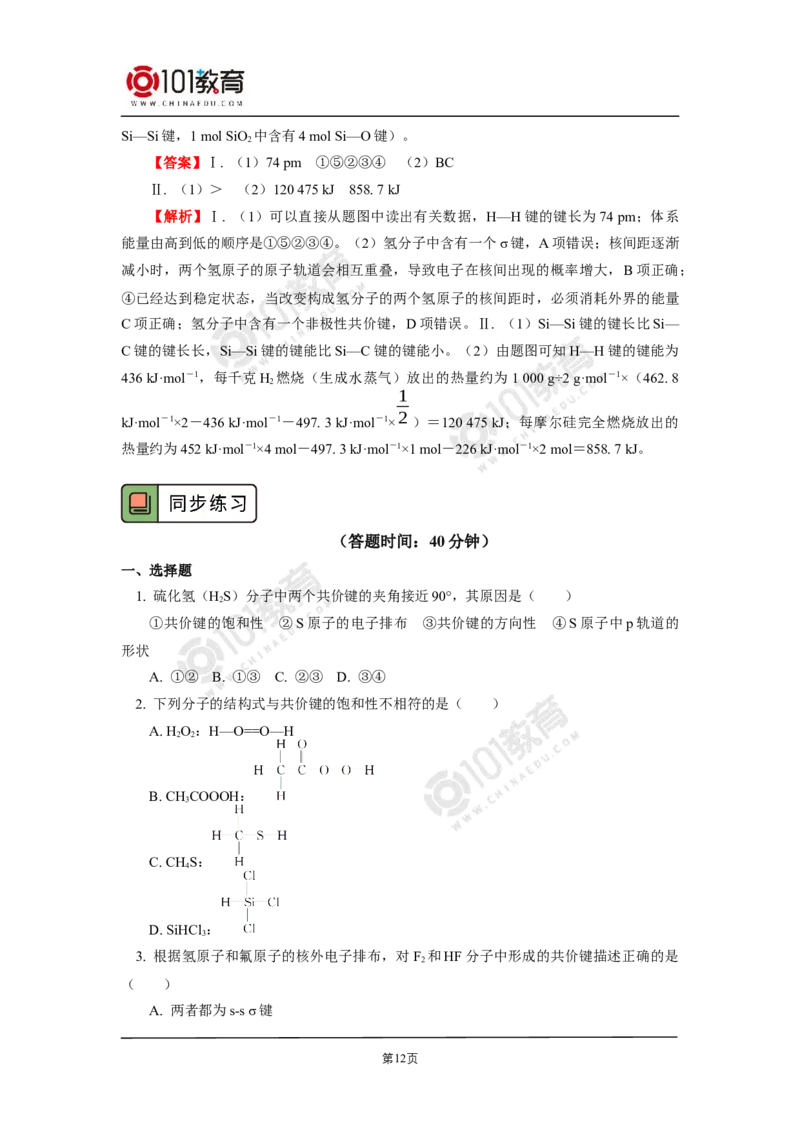
(1)概念及形成过程: 未成对电子的原子轨道采取“肩并肩”的方式重叠形成的共
价键叫π键。π键形成过程如图所示。
(2)存在:通常存在于共价双键或共价三键中。
【划重点】π键的特征
①镜面对称:每个π键的电子云由两块组成,分别位于由两原子核构成平面的两侧,
如果以它们之间包含原子核的平面为镜面,它们互为镜像,这种特征称为镜面对称。
②强度小:形成π键时原子轨道重叠程度比形成σ键时小,π键没有σ键牢固。
③不能旋转:以形成π键的两个原子核连线为轴,任意一个原子并不能单独旋转,若
单独旋转则会破坏π键的结构。
【思考】2 N 分子中的共价键类型
2
① N 原子的价层电子排布式:2s22p3
② N 原子的价电子轨道表示式:
③ N 的形成过程:
2
当氮原子结合成分子时,2p轨道上有3个未成对电子,若两个氮原子的2p 轨道以
x
“头碰头”的方式相互重叠,则2p 和2p 轨道只能分别采取相互平行的“肩并肩”的方式
x y
重叠,这样便形成了氮氮三键,如图所示。
第5页④ 共价键类型
1个 σ 键和 2个 π 键。
【总结提升】
(1)共价键的分类
(2)σ键和π键的区别于联系
σ键 π键
轨道组成 s—s轨道、s—p轨道、p—p轨道 p—p轨道
成键方式 以“头碰头”方式重叠 以“肩并肩”方式重叠
以包含原子核的平面为镜面,电
沿键轴呈轴对称,电子密集出现
重叠部分 子云呈镜面对称,电子密集出现
在键轴上
在键轴的上面或下面。
存在形式 一般是由一对电子组成的单键 仅存在于双键或三键中
轨道重叠程度大,键能大,稳定 轨道重叠程度小,键能小,稳定
键的性质
性高 性低
示意图
联系 只有在形成σ键后,余下的p轨道才能形成π键
一般规律:共价化合物分子中,共价单键全是 σ键;共价双键中有一个σ键,另一个
是π键;共价三键由一个σ键和两个π键构成。
三、键参数——键能、键长与键角
1. 键能
第6页(1)键能的概念:气态分子中1 mol化学键解离成气态原子所吸收的能量称为键能。
键能的单位是 kJ·mol - 1 。键能越大,化学键越稳定。
如:形成 1 mol H—H 键释放的最低能量为 436. 0 kJ,即 H—H 键的键能为 436. 0
kJ·mol-1。
(2)键能的应用
① 判断共价键的稳定性。原子间形成共价键时,原子轨道重叠程度越大,体系能量降
低越多,释放能量越多,形成共价键的键能越大,共价建越牢固。
② 判断分子的稳定性。一般来说,结构相似的分子,共价键的键能越大,分子越稳定。
如分子的稳定性:HF>HC1>HBr>HI。
③ 利用键能计算反应热。△H=反应物的键能总和 - 生成物的键能总和。
【举例】
共价键 H—F H—Cl H—Br H—I
键能/kJ·mol-1 568 431. 8 366 298. 7
①若使2 mol H—Cl键断裂为气态原子,则发生的能量变化是 吸收 863. 6 k J 的能量。
②表中共价键最难断裂的是H—F,最易断裂的是H—I。
③由表中键能大小数据说明键能与分子稳定性的关系:HF、HCl、HBr、HI的键能依
次减小,说明四种分子的稳定性依次减弱,即最稳定的是HF,最不稳定的是HI。
【即时练】N—H键键能的含义是( )
A. 由N和H形成1 mol NH 所放出的能量
3
B. 把1 mol NH 中的共价键全部拆开所吸收的热量
3
C. 拆开约6. 02×1023个N—H键所吸收的热量
D. 形成1个N—H键所放出的热量
【答案】C
【解析】N—H键的键能是指形成1 mol N—H键放出的能量或拆开1 mol N—H键所吸
收的能量,不是指形成1个N—H 键释放的能量。1 mol NH 中含有3 mol N—H键,拆开1
3
mol NH 或形成1 mol NH 吸收或放出的能量应是1 mol N—H键键能的3倍。
3 3
【考点】共价键的键参数
【题点】键能、键长和键角的概念
2. 键长
(1)概念
两个成键原子的原子核间的距离叫做该化学键的键长。
【拓展】共价半径
第7页相同原子形成的共价键键长的一半称为共价半径。
(2)键长与键的稳定性的关系
键长是衡量共价键稳定性的另一个重要参数。键长越短,往往键能越大,表明共价键
越稳定。
【思考】3 为什么 F-F 键键长比Cl-Cl 键键长短,但键能却比Cl-Cl键键能小?
氟原子的半径很小,因而F-F键键长比Cl-Cl键键长短,但也是由于F-F键键长短,两
个氟原子在形成共价键时,原子核之间的距离就小,排斥力大,因此键能比 Cl-Cl键键能
小。因为F-F键的键能小,所以F 的稳定性差,很容易和其他物质反应。
2
(3)键长与分子空间结构的关系
键长是影响分子空间结构的因素之一。如 CH 分子的空间结构是正四面体形,而
4
CHCl只是四面体形而不是正四面体形,原因是C-H键和C-Cl键的键长不相等。
3
(4)定性判断键长的方法
① 根据原子半径进行判断。
在其他条件相同时,成键原子的半径越小,键长越短。如键长:H-I键>H-Br键>H-Cl
键。
② 根据共用电子对数判断。
就相同的两原子形成的共价键而言,当两个原子形成双键或者三健时,由于原子轨道
的重叠程度增大,原子之间的核间距减小,键长变短:故单键键长>双键键长>三键键长。
3. 键角
(1)概念:在多原子分子中,两个相邻共价键之间的夹角称为键角。
(2)应用:在多原子分子中键角是一定的,这表明共价键具有方向性,因此键角决定
着共价分子的立体构型。
(3)常见分子的键角
如三原子分子CO 的结构式为O=C=O,键角为180°,为直线形分子;三原子分子HO
2 2
中的键角为105°,是V形(或称角形)分子;四原子分子NH 中的键角是107°,分子呈三
3
角锥形。
分子立体构型 键角 实例
正四面体形 109°28′ CH、CCl
4 4
平面形 120° 苯、乙烯、BF 等
3
第8页三角锥形 107° NH
3
V形(角形) 105° HO
2
直线形 180° CO、CS、CH≡CH
2 2
【划重点】键参数对分子性质的影响
相同类型思维共价化合物分子,成键原子半径越小,键长越短,键能越大,分子越稳
定。
【即时练】能说明 BF 分子中四个原子在同一平面的理由是( )
3
A. 任意两个键的夹角为120°
B. B—F键是非极性共价键
C. 三个B—F键的键能相同
D. 三个B—F键的键长相等
【答案】A
【解析】本题考查共价键键参数的运用。当键角为120°时,BF 的空间构型为平面三
3
角形,故分子中四个原子共面。
四、典型有机物的化学键类型
1. 乙烷的化学键
乙烷的结构简式是CHCH ,在乙烷分子中,每个碳原子与3个氢原子形成3个σ键,
3 3
2个碳原子之间形成1个σ键,所以1个乙烷分子中共有7个σ键。
2. 乙烯的化学键
乙烯的结构简式是CH=CH ,在乙烯分子中,每个碳原子与2个氢原子形成2个σ键,
2 2
2个碳原子之间形成1个σ键和1个π键,所以1个乙烯分子中共有5个σ键和1个π键。
3. 乙炔的化学键
乙炔的结构简式是CH≡CH,在乙炔分子中,每个碳原子与1个氢原子形成1个σ键,
2个碳原子之间形成1个σ键和2个π键,所以1个乙炔分子中共有3个σ键和2个π键。
第9页乙烷、乙烯和乙炔的球棍模型
4. 苯的化学键
苯的分子式是C H ,结构简式为 。苯分子中的6个碳原子都以σ键与氢原子结合,
6 6
每个碳原子以2个σ键与其他碳原子形成环状结构,同时,每个碳原子各有一个垂直于分
子平面的p轨道,形成了一个以6个碳原子为中心的π键(称为大π键)。苯的这种结构,
使任意两个相邻碳原子间形成的共价键的键能和键长完全相同。
例题1 下列有关化学键知识的比较肯定错误的是( )
A. 键能:C—N<C===N<C≡N
B. 键长:I—I>Br—Br>Cl—Cl
C. 分子中的键角:HO>CO
2 2
D. 相同元素原子间形成的共价键键能:σ键>π键
【答案】C
【解析】C、N原子间形成的化学键,三键键能最大,单键键能最小,A正确;原子半
径:I>Br>Cl,则键长:I—I>Br—Br>Cl—Cl,B正确;HO分子中键角是105°,CO 分
2 2
子中键角是180°,C错误;相同元素原子之间形成的σ键的键能比π键的大,D正确。
例题2 回答下列问题
某有机物的结构式如下图所示:
第10页则分子中有________个σ键,________个π键。
【答案】7 3
【解析】除共价单键全部为σ键外,双键中有一个为σ键,另一个为π键;三键中有
一个为σ键,另两个为π键,故该有机物分子中σ键总数为7,π键总数为3。
【考点】共价键的综合
【题点】共价键的综合
例题3 Ⅰ. 已知氢分子的形成过程示意图如图所示,请据图回答问题。
(1)H—H键的键长为________,①~⑤中,体系能量由高到低的顺序是________。
(2)下列说法中正确的是________(填字母)。
A. 氢分子中含有一个π键
B. 由①到④,电子在核间出现的概率增大
C. 由④到⑤,必须消耗外界的能量
D. 氢分子中含有一个极性共价键
Ⅱ. 几种常见化学键的键能如下表所示。
化学键 Si—O H—O O==O Si—Si Si—C
键能/(kJ·mol-1) 452 462. 8 497. 3 226 X
请回答下列问题:
(1)试比较Si—Si键与Si—C键的键能大小:X___________(填“>”“<”或
“=”)226 kJ·mol-1。
(2)H 被认为是21世纪人类最理想的燃料,而又有科学家提出硅是“21世纪的能
2
源”“未来的石油”等观点。试计算每千克 H 燃烧(生成水蒸气)放出的热量约为
2
___________;每摩尔硅完全燃烧放出的热量约为___________(已知1 mol Si中含有2 mol
第11页Si—Si键,1 mol SiO 中含有4 mol Si—O键)。
2
【答案】Ⅰ. (1)74 pm ①⑤②③④ (2)BC
Ⅱ. (1)> (2)120 475 kJ 858. 7 kJ
【解析】Ⅰ. (1)可以直接从题图中读出有关数据,H—H键的键长为74 pm;体系
能量由高到低的顺序是①⑤②③④。(2)氢分子中含有一个σ键,A项错误;核间距逐渐
减小时,两个氢原子的原子轨道会相互重叠,导致电子在核间出现的概率增大,B项正确;
④已经达到稳定状态,当改变构成氢分子的两个氢原子的核间距时,必须消耗外界的能量
C项正确;氢分子中含有一个非极性共价键,D项错误。Ⅱ. (1)Si—Si键的键长比Si—
C键的键长长,Si—Si键的键能比Si—C键的键能小。(2)由题图可知H—H键的键能为
436 kJ·mol-1,每千克H 燃烧(生成水蒸气)放出的热量约为1 000 g÷2 g·mol-1×(462. 8
2
1
2
kJ·mol-1×2-436 kJ·mol-1-497. 3 kJ·mol-1× )=120 475 kJ;每摩尔硅完全燃烧放出的
热量约为452 kJ·mol-1×4 mol-497. 3 kJ·mol-1×1 mol-226 kJ·mol-1×2 mol=858. 7 kJ。
(答题时间:40分钟)
一、选择题
1. 硫化氢(HS)分子中两个共价键的夹角接近90°,其原因是( )
2
①共价键的饱和性 ②S原子的电子排布 ③共价键的方向性 ④S原子中p轨道的
形状
A. ①② B. ①③ C. ②③ D. ③④
2. 下列分子的结构式与共价键的饱和性不相符的是( )
A. H O:H—O==O—H
2 2
B. CHCOOOH:
3
C. CHS:
4
D. SiHCl :
3
3. 根据氢原子和氟原子的核外电子排布,对F 和HF分子中形成的共价键描述正确的是
2
( )
A. 两者都为s-s σ键
第12页B. 两者都为p-p σ键
C. 前者为p-p σ键,后者为s-p σ键
D. 前者为s-s σ键,后者为s-p σ键
4. 下列有关化学键类型的判断不正确的是( )
A. s-s σ键与s-p σ键的对称性不同
B. 分子中含有共价键,则至少含有一个σ键
C. 已知乙炔的结构式为H—C≡C—H,则乙炔分子中存在2个σ键(C—H)和3个π
键(C≡C)
D. 乙烷分子中只存在σ键,即6个C—H键和1个C—C键都为σ键,不存在π键
5. 下列分子中含有两个π键的组合是( )
①HO ②CO ③H—C≡N ④NH ⑤N ⑥CH
2 2 3 2 4
A. ①③⑥ B. ②③⑤
C. ①②③⑥ D. ③④⑤⑥
6. 下列说法正确的是( )
A. Cl 是双原子分子,HS是三原子分子,这是由共价键的方向性决定的
2 2
B. HO与HS的立体结构一样是由共价键的饱和性决定的
2 2
C. 并非所有的共价键都有方向性
D. 两原子轨道发生重叠后,电子出现在两核间的概率减小
7. 由短周期前10号元素组成的物质T和X,有如图所示的转化。X不稳定,易分解。下
列有关说法正确的是( )
A. 为使该转化成功进行,Y可以是酸性KMnO 溶液
4
B. 等物质的量的T、X分子中含有π键的数目均为N
A
C. X分子中含有的σ键个数是T分子中含有的σ键个数的2倍
D. T分子中只含有极性键,X分子中既含有极性键又含有非极性键
8. 下列说法不正确的是( )
A. 键能越小,表示化学键越牢固,越难以断裂
B. 成键的两原子核越近,键长越短,化学键越牢固,性质越稳定
C. 破坏化学键时消耗能量,而形成化学键时释放能量
D. 键能、键长只能定性地分析化学键的强弱
9. 下列叙述中的距离属于键长的是( )
A. 氨分子中两个氢原子间的距离
第13页B. 氯分子中两个氯原子间的距离
C. 金刚石中任意两个相邻的碳原子核间的距离
D. 氯化钠中相邻的氯离子和钠离子核间的距离
10. 下列分子中的键角最大的是( )
A. CO B. NH C. HO D. CH ==CH
2 3 2 2 2
11. 从实验测得不同物质中氧氧之间的键长和键能的数据如下:
O—O键 2− − +
O2 O2 O O2
2
数据
键长/10-12 m 149 128 121 112
键能/kJ·mol-1 x y z=494 w=628
其中x、y的键能数据尚未测定,但可根据规律性推导键能的大小顺序为 w>z>y>x;该
规律性是( )
A. 成键的电子数越多,键能越大
B. 键长越长,键能越小
C. 成键所用的电子数越少,键能越大
D. 成键时电子对越偏移,键能越大
12. 已知N+O===2NO为吸热反应,ΔH=+180 kJ·mol-1,其中N≡N、O==O键的键能
2 2
分别为946 kJ·mol-1、498 kJ·mol-1,则N—O键的键能为( )
A. 1 264 kJ·mol-1 B. 632 kJ·mol-1
C. 316 kJ·mol-1 D. 1 624 kJ·mol-1
13. 化学反应可视为旧键的断裂和新键的形成过程。化学键的键能是形成化学键时释放
的能量。已知白磷和PO 的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P
4 6
—P:198 P—O:360 O==O:498,则反应P (白磷)+3O===P O 的反应热ΔH为(
4 2 4 6
)
A. -1 638 kJ·mol-1 B. +1 638 kJ·mol-1
C. -126 kJ·mol-1 D. +126 kJ·mol-1
14. 六氟化硫分子呈正八面体结构(如图所示),在高电压下仍有良好的绝缘性,性质
稳定,在电器工业方面有着广泛的用途,但逸散到空气中会引起强温室效应,下列有关六
氟化硫的推测正确的是( )
第14页A. 六氟化硫中各原子均为8电子稳定结构
B. 六氟化硫易燃烧生成二氧化硫
C. 六氟化硫分子中含极性键、非极性键
D. S—F键是σ键,且键长、键能都相等
二、非选择题
15. 已知某些共价键的键能、键长数据如表所示:
共价键 键能/(kJ·mol-1) 键长/pm
Cl—Cl 242. 7 198
Br—Br 193. 7 228
I—I 152. 7 267
H—F 568
H—Cl 431. 8
H—Br 366
H—I 298. 7
H—O 462. 8 96
C—C 347. 7 154
C===C 615 133
C≡C 812 120
C—H 413. 4 109
N—H 390. 8 101
N===O 607
O—O 142
O===O 497. 3
(1)下列推断正确的是________(填字母,下同)。
A. 稳定性:HF>HCl>HBr>HI
B. 氧化性:I>Br >Cl
2 2 2
C. 沸点:HO>NH
2 3
D. 还原性:HI>HBr>HCl>HF
第15页(2)下列有关推断正确的是________。
A. 同种元素原子形成的共价键的稳定性:三键>双键>单键
B. 同种元素原子形成的双键的键能一定小于单键的2倍
C. 键长越短,键能一定越大
(3)在 HX(X=F、Cl、Br、I)分子中,键长最短的是________,最长的是
________;O—O键的键长________(填“大于”“小于”或“等于”)O===O键的键长。
16. 回答下列问题:
(1)1个CO(NH ) 分子中含有σ键的个数为________。1 mol乙醛分子中含有 σ
2 2
键的数目为________个。
(2)已知CO和CN-与N 结构相似,CO分子内σ键与π键个数之比为__________。
2
HCN分子内σ键与π键数目之比为______________。
(3)C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为
________________。
第16页1.【答案】D
【解析】S原子的价电子排布式是3s23p4,有2个未成对电子,并且分布在相互垂直的
两个p轨道中,当与两个H原子配对成键时,形成的两个共价键间夹角接近90°,这体现
了共价键的方向性,是由p轨道的伸展方向决定的。
2.【答案】A
【解析】由共价键的饱和性可知:C、Si均形成4个共价键,H形成1个共价键,O、
S均形成2个共价键。A项中O原子之间不可能形成双键;B项是过氧乙酸,含有过氧键
“O—O”;C项相当于S取代了CHOH中的氧原子;D项中Si原子形成4个共价键。
3
3.【答案】C
【解析】氢原子的核外电子排布式为1s1,氟原子的核外电子排布式为1s22s22p5,p轨
道上有1个未成对的p电子。F 是由两个氟原子未成对的p电子轨道重叠形成的p-p σ键,
2
HF是由氢原子中的s轨道与氟原子中的1个p轨道形成的s-p σ键。
4.【答案】C
【解析】s-s σ键无方向性,s-p σ键轴对称,A项对;在含有共价键的分子中一定有σ
键,可能有π键,如HCl、N 等,B项对;单键都为σ键,乙烷分子结构式为 ,
2
其6个C—H键和1个C—C键都为σ键,D项正确;共价三键中有一个为σ键,另外两个
为π键,故乙炔(H—C≡C—H)分子中有2个C—H σ键,C≡C键中有1个σ键、2个π键,
C项错。
5.【答案】B
【解析】HO分子中含有2个H—O键,不含π键,①错误;CO 的分子中只有两个
2 2
C==O键,含有两个π键,②正确;H—C≡N的分子中有1个C≡N键,含有两个π键,③
正确;NH 分子中含有3个H—N键,不含π键,④错误;N 的分子中有1个N≡N键,含
3 2
有两个π键,⑤正确;CH 的分子中有4个H—C键,不含π键,⑥错误。故分子中含有
4
两个π键的是②③⑤。
6.【答案】C
【解析】
第17页7.【答案】A
【解析】由球棍模型可知,T为HCHO,X不稳定,易分解,则X为HCO ,则Y为
2 3
氧化剂,可以选择氧化性较强的酸性KMnO 溶液,A项正确;等物质的量并不一定是1
4
mol,B项错误;X分子中含有的σ键个数为5,T分子中含有的σ键个数为3,C项错误;
T、X分子中均只含有极性键,无非极性键,D项错误。
8.【答案】A
【解析】键能越大,断开该键所需的能量越多,化学键越牢固,性质越稳定,故 A错
误;B、C、D均正确。
9.【答案】C
【解析】键长是指形成共价键的两个原子核间的距离,仅仅说成是原子间的距离是错
误的。A项,NH 分子中的两个H原子间不存在化学键,错误;B项,未指出是核间距离,
3
错误;C项,金刚石中只要两个碳原子相邻,它们之间就有共价键,正确;D项,NaCl中
的阴、阳离子之间形成离子键,没有键长。
10.【答案】A
【解析】CO 为直线形分子,键角为180°;NH 为三角锥形结构,键角为107°;HO分
2 3 2
子立体构型为V形,键角为105°;CH==CH 为平面结构,键角为120°,故键角最大的是
2 2
CO,A正确。
2
11.【答案】B
【解析】共用一对共用电子对形成一个共价键,所以成键电子数越多,共价键数越多,
但键能不一定大,A错误;键长越长,说明轨道的重合程度越小,越容易断裂,键能越小,
B正确;成键电子数越多,键能越大,C错误;电子对越偏移说明极性越大,和键能没有
必然关系,D错误。
12.【答案】B
【解析】180 kJ·mol-1=946 kJ·mol-1+498 kJ·mol-1-2E(N—O),所以E(N—O)
=632 kJ·mol-1。
13.【答案】A
【解析】反应中的键能包括:断裂1 mol P 和3 mol O 分子中共价键吸收的能量和形
4 2
成1 mol P O 分子中共价键放出的能量。由各物质的分子结构知1 mol P 含6 mol P—P键,
4 6 4
3 mol O 含3 mol O==O键,化学反应的反应热ΔH=反应物的总键能-生成物的总键能。
2
故ΔH=(198 kJ·mol-1×6+498 kJ·mol-1×3)-360 kJ·mol-1×12=-1 638 kJ·mol-1。
14.【答案】D
【解析】根据题图知,每个F原子和1个S原子形成1对共用电子对,每个S原子和6
个F原子形成6对共用电子对,所以F原子都达到8电子稳定结构,但S原子最外层达到
12电子,A错误;六氟化硫中F为-1价,S为+6价,S元素不能再失去电子,所以不能
第18页被氧化,故六氟化硫不易燃烧生成二氧化硫,B错误;同种原子间形成非极性键,不同种
原子间形成极性键,六氟化硫分子中的S—F键均为极性键,不含非极性键,C错误;六氟
化硫分子中的S—F键都是σ键,为正八面体结构,所以键长、键能都相等,D正确。
15.【答案】(1)ACD (2)A (3)HF HI 大于
【解析】(1)根据表中数据知,同主族元素从上至下气态氢化物的键能逐渐减小,稳
定性逐渐减弱,A项正确;从键能看,氯气、溴单质、碘单质的稳定性逐渐减弱,由原子
结构知,氧化性也逐渐减弱,B项错误;HO在常温下为液态,NH 在常温下为气态,则
2 3
HO的沸点比NH 的高,C项正确;还原性与得失电子能力有关,还原性:HI>HBr>HCl
2 3
>HF,D项正确。(2)键能越大,化学键越稳定,越不容易断裂,由表中碳碳键的数据
知A项正确;由O—O键、O===O键的键能知,B项错误;C—H键的键长大于N—H键的
键长,但是N—H键的键能反而较小,C项错误。
16.【答案】(1)7 6N (或3. 612×1024) (2)1∶2 1∶1 (3)5∶1
A
【解析】(1)乙醛和CO(NH ) 的结构简式分别为 、 ,
2 2
1个CO(NH ) 分子中含有7个σ键。1 mol乙醛中含有σ键6N 个。
2 2 A
(2)N 的结构式为N≡N,推知:CO结构式为C≡O,1个CO分子含有1个σ键、2
2
个π键;CN-结构式为[C≡N]-,HCN的结构式为H—C≡N,1个HCN分子中σ键与π键均
为2个。
(3)设分子式为C H ,则6m+n=16,解之得m=2,n=4,即C H ,结构式为
m n 2 4
。单键为σ键,双键有1个σ键和1个π键,所以1个C H 分子中共含有5个
2 4
σ键和1个π键。
第19页