文档内容
第 18 课时:配制一定物质的量浓度的溶液
【学习目标】
学会溶液配制的一般方法。
了解实验中错误操作会导致结果的变化。
【重点难点】
1.重点:熟悉溶液配制的一般步骤;
2.难点:溶液配制中基本的误差分析。
【高频考点】
溶液配制中操作错误对于溶液浓度的影响。
【教学内容】
一、玻璃仪器
容量瓶,玻璃棒,烧杯,胶头滴管
其中容量瓶需要注意规格。
例:实验室需 480mL 的 1mol/L 的 NaOH 溶液,应选用 500mL 规格
的容量瓶进行配制。
二、容量瓶注意事项
1.只用于配制溶液,不可长期储存溶液;
不能用作反应容器,不能直接溶解物质或稀释较浓溶液,温度较高或
较低的液体转移至容量瓶前,需先冷却至室温。
第 1 页2.向容量瓶中注入液体时,应沿玻璃棒注入,
以防液体溅落到瓶外。
3.使用前首先要检查容量瓶是否漏液。
三、基本步骤
以配制 500mL0.1mol•L-1Na CO 溶液为例:
2 3
1.计算:
500mL0.1mol•L-1Na CO 溶液所含 Na CO 溶质的质量是 5.3g
2 3 2 3
0.5L×0.1mol•L-1×106g/mol=5.3g
2.称量:
用托盘天平准确称取 Na CO 固体 5.3g;
2 3
3.溶解:
将 Na CO 用适量蒸馏水溶解在烧杯中,恢复到室温;
2 3
4.转移:
将烧杯中的溶液用玻璃棒小心地引流到容量瓶中
5.洗涤:
用蒸馏水洗涤烧杯内壁和玻璃棒 2~3 次,洗涤液同样要转移至容量瓶
中;
6.定容:
将蒸馏水沿玻璃棒注入容量瓶中至液面距刻度线 1~2cm 处,改用胶
头滴管逐滴加入,至液面正好与刻度线相切;
思考:
若定容时加水超过刻度线,应该怎么办?
第 2 页7.摇匀:
将容量瓶瓶塞盖好,反复上下颠倒、摇匀。
8.装瓶、贴标签。
【经典例题】
1.某同学用物质的量浓度为18.4mol/L 的浓硫酸配制250mL1.84mol/L
的稀硫酸,下列操作正确的是 ( )
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌,然后
迅速注入容量瓶中
B.将浓硫酸转移至烧杯后须用蒸馏水洗涤量筒,并将洗涤液一并转移
至烧杯
C.定容时不小心加水超过了刻度线,应重新配制
D.先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
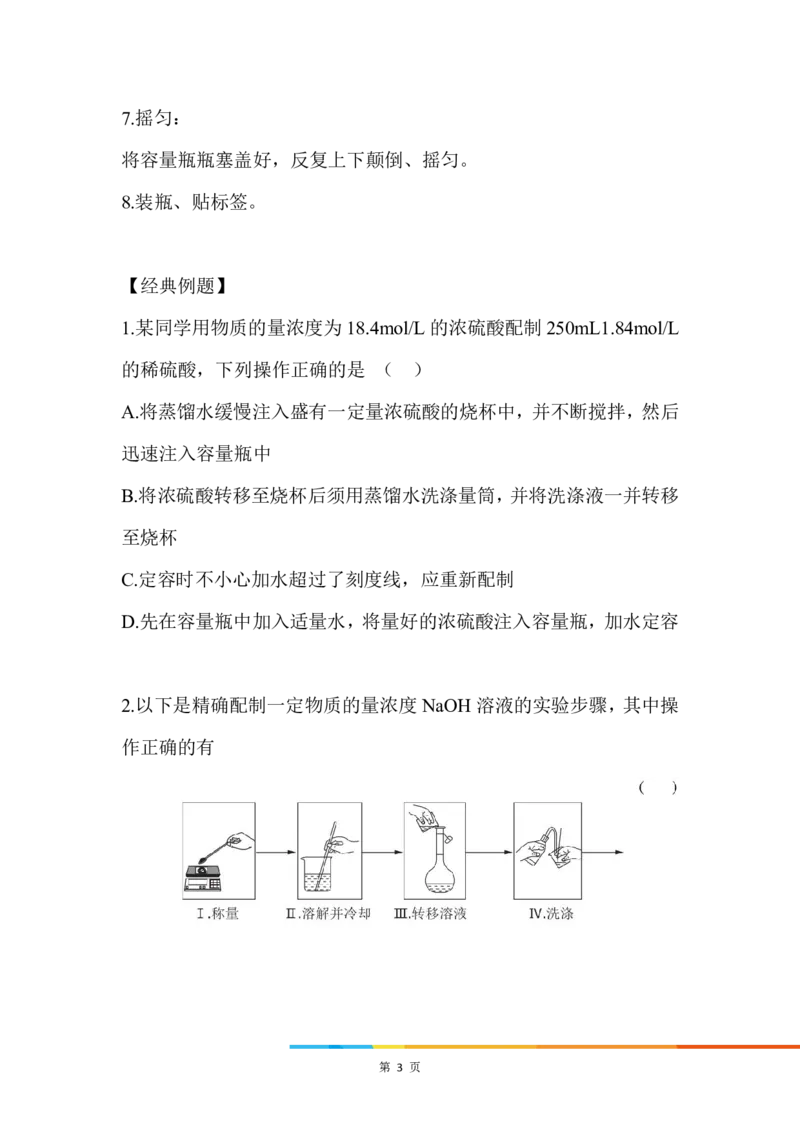
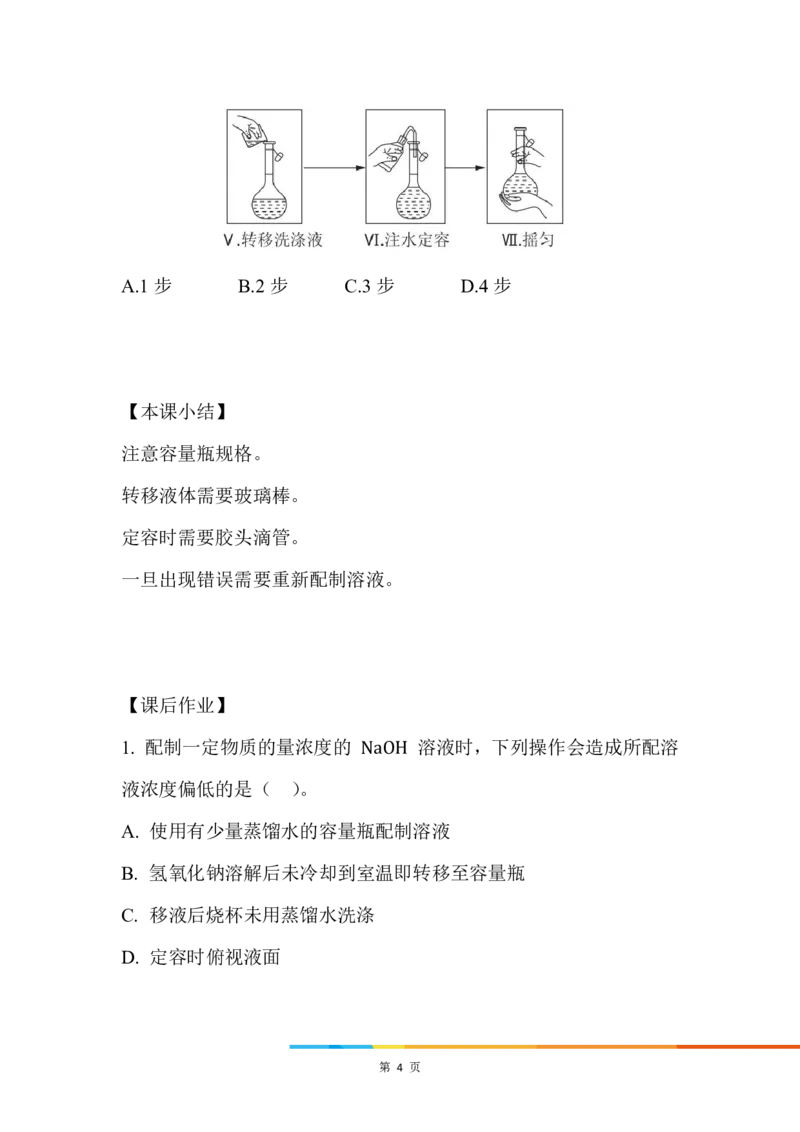
2.以下是精确配制一定物质的量浓度 NaOH 溶液的实验步骤,其中操
作正确的有
第 3 页A.1 步 B.2 步 C.3 步 D.4 步
【本课小结】
注意容量瓶规格。
转移液体需要玻璃棒。
定容时需要胶头滴管。
一旦出现错误需要重新配制溶液。
【课后作业】
1. 配制一定物质的量浓度的 溶液时,下列操作会造成所配溶
液浓度偏低的是( )。 NaOH
A. 使用有少量蒸馏水的容量瓶配制溶液
B. 氢氧化钠溶解后未冷却到室温即转移至容量瓶
C. 移液后烧杯未用蒸馏水洗涤
D. 定容时俯视液面
第 4 页2. 实验室需配制 溶液,下列叙述正确的是
( )。 �th mL � mol�L NaOH
A. 用托盘天平称量 固体
B. 移液时,为防止液�体th�洒g出Na,O用H玻璃棒插在刻度线以上引流
C. 定容时,液面接近刻度线 时,用胶体滴管滴加蒸馏水,
至液面与刻度线相切 � � � cm
D. 定容时若俯视刻度线观察液面,会使所配制的 溶液的浓度
偏低 NaOH
3. 配制 溶液,下列操作正确的是( )。
A. 称取 �hh mL无�hh水m碳ol酸�L钠N,a � C加O入� 容量瓶中,加水溶解、
定容 �hh�g �hh mL
B. 称取 无水碳酸钠,加入 蒸馏水,搅拌、溶解
C. 转移 �hh�g 溶液时,未用玻璃�棒hh引m流L,直接倒入容量瓶中
D. 定容后N,a �塞CO好� 瓶塞,反复倒转、摇匀
4. 欲配制 溶液,下列方法正确的方法是
( )。 �hh mL �hhmol�L Na � SO �
A. 将 溶于 水中
B. 将 ��h�g Na � SO � �hh溶m于L少量水中,再用水稀释至
C. 将 ��h�g Na � SO � � �hH � O 溶液加 蒸馏水稀释 �hh mL
D. 将 �h mL �hhmol�溶L N于a � SO � 蒸馏水�h中mL
� �
��h�g Na SO ��h�g
第 5 页5. 利用碳酸钠晶体( ,相对分子质量 286)来配制
的碳酸钠溶液Na � CO � � �hH,�假O 如其他操作均准确无误,下列
h情h�况m会ol引�L起配制溶液的浓度t�偏h高mL的是( )。
A. 称取碳酸钠晶体 28.6 克
B. 溶解时进行加热,并将热溶液转移到容量瓶中至刻度线
C. 转移时,对用于溶解碳酸钠晶体的烧杯没有进行洗涤
D. 定容后,将容量瓶振荡摇匀,静置发现液面低于刻度线,又加入
少量水至刻度线
6. 某课外兴趣小组需要用 的浓硫酸配制
稀硫酸的实验步骤如下:�①�计m算ol�所L用浓硫酸的体积�;h②m量L �取hh一m定ol体�
L积的浓硫酸;③稀释;④检漏、转移、洗涤;⑤定容、摇匀;回答下
列问题。
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规
格是 (用下列编号填空)。 mL
A. B. C. D.
(2�)h第mL⑤步实验��的m操L 作是继�续hm向L容量瓶�中hh注m入L蒸馏水至离刻度
线 ,改用 向容量瓶中滴加蒸馏水至 为止。塞紧瓶塞,
倒转摇匀并装试剂瓶。
(3)下列情况对所配制的稀硫酸浓度有何影响(填“偏大”“偏小”或
“无影响”):
第 6 页①定容时仰视刻度线 ;
②容量瓶用蒸馏水洗涤后残留有少量的水 ;
③在转入容量瓶前烧杯中溶液未冷却至室温 ;
④取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯 ;
⑤定容摇匀后发现液面低于刻度线,又向容量瓶加水 。
【答案与解析】
1. C
C 项,烧杯没有洗涤,则会有部分溶质损耗,导致溶质的物质的量偏
小,根据 可知,溶液浓度偏低,故选 C 项;
�
A 项,容量�瓶t中�含有少量蒸馏水,对溶质的物质的量和溶液体积都不
会产生影响,根据
�
B 项,根据热胀冷缩�原t理�可知,冷却后液面下降,溶液体积偏小,根
据 可知,溶液浓度偏高,故不选 B 项;
�
D 项�,t定� 容时俯视液面,导致溶液体积偏小,根据 可知,溶
�
液浓度偏高,故不选 D 项。 � t �
2. C
C 项,定容时,液面接近刻度线 时,就要用胶体滴管滴加
蒸馏水,直至液面与容量瓶刻度线�相�切� c,m故 C 项正确;
A 项,由于实验室没有 的容量瓶,所以只能选用 的
容量瓶,所以需要的氢氧�t化h m钠L的质量为 �hhmL
��
,故 A 项错误; �hh � �h L � � mol�L �
�h t �hhhg
第 7 页B 项,移液时,为防止液体洒出,应该把玻璃棒插在容量瓶口内部刻
度线以下引流,故 B 项错误;
D 项,定容时若俯视刻度线观察液面,当液面还没有到达刻度线时就
会以为已经到达刻度线,使得溶剂的体积偏小,导致配得的溶液的物
质的量浓度偏高,故 D 项错误。
3. D
D 项,在定容后,应该塞好瓶塞,并将液体摇匀,故 D 项正确;
A 项,溶质的溶解过程不在容量瓶中进行,而是在烧杯中进行,故 A
项错误;
B 项,配制 溶液,称取了 无水碳
酸钠,由于在�后hh续m的L �洗hh涤m、ol定�L容N等a �过CO程� 中还需要加入蒸�馏hh水�g,所以在
溶解的过程中加入的的蒸馏水应该少于 ,故 B 项错误;
C 项,转移溶液时,为了防止溶液洒出瓶�外hh,m必L须使用玻璃棒引流,
故 C 项错误。
4. B
B 项,配制 溶液需要 的
质量为 �hh mL �hhmol�L Na � SO � ,故NaB � S项O �正� �确h;H � O
A 项,由h于h�配L �制�溶m液ol的�L体�积��为� g�mol t �,�h所�g以需要水的体积不是
,故 A 项错误; �hh mL
�Ch项h m,将L 溶液加 蒸馏水稀释,由于
溶液的密度�h与m水L不�hh同m,o所l�以L N不a能� SO直�接加 �h m水L稀释,故 C 项错误;
D 项,将 溶于 蒸�馏h m水L中,由于溶液的密度与
� �
��h�gNa SO ��h�g
第 8 页水不同,所以溶液质量为 ,但溶液的体积不是 ,故
D 项错误。 �hh g �hh mL
5. B
B 项,溶解时进行加热,并将热溶液转移到容量瓶中至刻度线,溶液
的体积受热膨胀,遇冷收缩,因此溶液恢复至室温时,体积小于 ,
根据 可知,体积偏小,则浓度偏高,故选 B 项; � L
�
A 项,�配t制� 溶液,应要选择 容量瓶,因此需要溶
质的物质的量t�为h mL �hhh mL ,根据
��Na � CO � � t hh�可m知ol�,L � � L t hh�mol
��Na � CO � � �hH � O� t ��Na � CO,� �因此不会产��生Na误� C差O,� �故�h不H选� O�At项;
hCh�项m,o转l �移�时��,没g�有m洗ol涤t烧��杯h�,g会导致溶质的物质的量偏少,根据
�
可知,物质的量偏小,则浓度偏低,故不选 C 项; � t �
D 项,定容后,将容量瓶振荡摇匀、静置,由于部分溶液粘在容量瓶
颈,导致液面低于刻度线,若再加入少量水至刻度线,则体积偏大,
根据 可知,体积偏大,浓度偏低,故不选 D 项。
�
6. (1�)t16�.7(2 分);B(2 分)
(2) ;胶头滴管;凹液面与刻度线相切
(3)①�偏�小�②cm无影响③偏大④偏大⑤偏小
(1)配制 稀硫酸需要用 的浓硫酸的体
积为: �h mL �hhmol�L �,� m应o该l�选L 择 的
�hhmol�L�hh�L
量筒。 ��mol�L � hhh��香L t ��h香mL �� mL
(2)定容操作为:继续向容量瓶注入蒸馏水至离刻度线 处,
�� � cm
第 9 页改用胶头滴管向容量瓶滴加至凹液面与刻度线相切。
(3)①定容时仰视溶液的凹液面,会导致加入的蒸馏水体积偏大,
根据 可得,配制的溶液浓度偏小;
�
②容量�瓶t用� 蒸馏水洗涤后残留有少量的水,由于定容时还需要加入蒸
馏水,所以不影响配制结果;
③在转入容量瓶前烧杯中溶液未冷却至室温,液体受热膨胀,所以
溶液体积偏小浓度偏大;
④取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯,则溶质的物质的
量偏大;
⑤定容摇匀后发现液面低于刻度线,又向容量瓶加水,相当于将溶
液稀释,所以溶液的浓度偏小。
第 10 页