文档内容
无机工业流程综合分析同步练习
(答题时间:40分钟)
1. 工业上制备下列物质的生产流程合理的是( )
A. 由铝土矿冶炼铝:铝土矿⃗提纯 Al O⃗HClAlCl ⃗电解 Al
2 3 3
B. 从海水中提取镁:海水⃗石灰乳Mg(OH)⃗加热 MgO⃗电解 Mg
2
C. 由NaCl制漂白粉:饱和食盐水⃗电解 Cl⃗NaOH溶液漂白粉
2
D. 由黄铁矿制硫酸:黄铁矿⃗煅烧 SO⃗催化氧化SO⃗98%浓硫酸吸收HSO
2 3 2 4
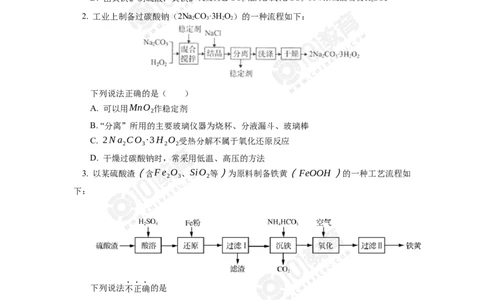
2. 工业上制备过碳酸钠(2NaCO·3H O)的一种流程如下:
2 3 2 2
下列说法正确的是( )
A. 可以用MnO 作稳定剂
2
B. “分离”所用的主要玻璃仪器为烧杯、分液漏斗、玻璃棒
C. 2Na CO ·3H O 受热分解不属于氧化还原反应
2 3 2 2
D. 干燥过碳酸钠时,常采用低温、高压的方法
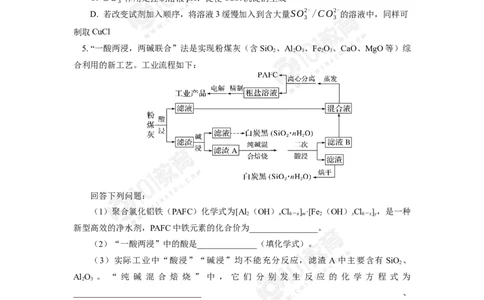
3. 以某硫酸渣(含Fe O 、SiO 等)为原料制备铁黄(FeOOH)的一种工艺流程如
2 3 2
下:
下列说法不正确的是
A. “酸溶”中加热或搅拌或适当增大硫酸浓度均可加快溶解速度
B. 滤渣的主要成分是SiO 和Fe
2
C. “沉铁”过程中生成Fe(OH)的化学方程式为:
2
FeSO +2N H HCO =Fe(OH)↓+ (N H )SO + 2CO ↑。
4 4 3 2 4 2 4 2
D. “氧化”Fe(OH)浆液时,可用氯气代替空气
2
4. CuCl是难溶于水的白色固体,是一种重要的催化剂。工业上,由孔雀石[主要成分
Cu(OH)·CuCO ,含FeS、FeO和SiO 杂质]制备CuCl的某流程如下:
2 3 2
第1页下列说法不正确的是( )
A. H O 将溶液1中Fe2+氧化为Fe3+,再通过控制pH转化为Fe(OH)除去
2 2 3
B. SO2- 将溶液3中的Cu2+还原,反应得到CuCl
3
C.
CO2-
作用是控制溶液pH,促使CuCl沉淀的生成
3
D.
若改变试剂加入顺序,将溶液3缓慢加入到含大量SO2-/CO2-
的溶液中,同样可
3 3
制取CuCl
5. “一酸两浸,两碱联合”法是实现粉煤灰(含SiO 、Al O 、Fe O 、CaO、MgO等)综
2 2 3 2 3
合利用的新工艺。工业流程如下:
回答下列问题:
(1)聚合氯化铝铁(PAFC)化学式为[Al (OH) Cl ] ·[Fe (OH)Cl ],是一种
2 n 6-n m 2 x 6-x y
新型高效的净水剂,PAFC中铁元素的化合价为________________。
(2)“一酸两浸”中的酸是______________(填化学式)。
(3)实际工业中“酸浸”“碱浸”均不能充分反应,滤渣 A中主要含有 SiO 、
2
Al O 。 “ 纯 碱 混 合 焙 烧 ” 中 , 它 们 分 别 发 生 反 应 的 化 学 方 程 式 为
2 3
______________________________ 、
________________________________________________________________________。
(4)“滤液B”的主要溶质有______________(填化学式)。滤液混合后“蒸发”的
作用是____________________。
6. NaAlH (四氢铝钠)是有机合成的重要还原剂。某小组以铝合金厂的废边脚料为原料
4
(主要成分为Al,含有少量Al O、Fe O、MgO和SiO 等杂质)制备四氢铝钠的工艺流程
2 3 2 3 2
如下:
第2页资料显示:NaH、NaAlH 遇水蒸气发生剧烈反应。
4
请回答下列问题:
(1)NaAlH 中氢元素的化合价为________________。
4
(2)试剂A中溶质的阴、阳离子所含电子数相等,其电子式为________________。
在空气中灼烧滤渣2,得到的固体的主要成分为____________________(填化学式)。
(3)滤液 3 可以循环利用,写出滤液 2 与滤液 3 反应的离子方程式:
________________
_________________________________________________________________________。
( 4 ) 实 验 前 要 保 证 NaH 与 AlCl 反 应 的 装 置 干 燥 , 其 目 的 是
3
_______________________。
第3页无机工业流程综合分析同步练习参考答案
1.【答案】D
【解析】A. 工业上通过电解熔融氧化铝制备金属铝,氯化铝是共价化合物,熔融状态
下不电离,故A错误;B. 工业上通过电解熔融的氯化镁制备金属镁,氯化镁熔点低于氧化
镁,能耗低,故B错误;C. 工业上用氯气和石灰乳反应制备漂白粉,漂白粉的有效成分是
次氯酸钙,不是次氯酸钠,故C错误;D. 黄铁矿煅烧得到二氧化硫,再转变为三氧化硫,
最后得到硫酸,故D正确。
2.【答案】D
【解析】A. 由于MnO 可以使H O 分解,所以不能用作稳定剂,故A错误;B. “分
2 2 2
离”是过滤,所以所用的主要玻璃仪器为烧杯、漏斗、玻璃棒,故B错误;C.
2Na CO ·3H O 受热分解时,由于元素的化合价发生变化,所以属于氧化还原反应,
2 3 2 2
故C错误。D. 干燥过碳酸钠时,为防止过碳酸钠分解,常采用低温、高压的方法,故D
正确。
故选D。
3.【答案】D
【解析】硫酸渣(含Fe O 、SiO 等)加硫酸溶解,金属氧化物转化为金属阳离子,
2 3 2
二氧化硅不溶,再加Fe把铁离子还原为Fe2+,过滤,滤渣含有二氧化硅,滤液中含有
Fe2+,加入碳酸氢铵,发生
FeSO +2N H HCO =Fe(OH)↓+(N H )SO +2CO ↑,通入空气氧化,
4 4 3 2 4 2 4 2
同时调节pH生成FeOOH沉淀,过滤、洗涤、烘干,得到纯净的FeOOH,
A. 加热可增大活化分子百分数,搅拌可增大接触面积,且适当增大硫酸浓度等,都可
加快酸溶的速率,故A正确;B. 二氧化硅不溶于酸,且铁粉过量,则滤渣的主要成分是
SiO 和Fe,故B正确;C. 硫酸亚铁与碳酸氢铵发生互促水解反应,方程式为
2
FeSO +2N H HCO =Fe(OH)↓+(N H )SO +2CO ↑,故C正确;D. 氯
4 4 3 2 4 2 4 2
气污染空气,不能用氯气代替,故D错误。
4. 【答案】D
【解析】孔雀石(主要成分Cu(OH)⋅CuCO ,含FeS、FeO和SiO 杂质)用
2 3 2
硫酸浸取,得到的气体主要含有硫化氢、二氧化碳,滤渣1为二氧化硅,溶液1中含有
Fe2+、Fe3+、Cu2+,加双氧水将亚铁离子氧化成铁离子,加氢氧化钠溶液调节pH,使铁
离子沉淀,得到滤渣2为氢氧化铁,溶液2主要含有硫酸铜,溶液2中加入氯化钠再加入
亚硫酸钠将铜离子还原成亚铜离子,加入碳酸钠调节pH,使CuCl沉淀,由于
SO2-/CO2- 的溶液呈碱性,所以如果将溶液3缓慢加入到含大量SO2-/CO2-
的溶液中,
3 3 3 3
有可能生成氢氧化亚铜沉淀,得到的氯化亚铜不纯。
第4页A. 根据上面的分析可知,H O 将溶液1中Fe2+氧化为Fe3+,再通过控制pH转化为
2 2
Fe(OH)除去,故A正确;B. 根据上面的分析可知,SO2- 将溶液3中的Cu2+还原,
3 3
反应得到CuCl,故B正确;C.
根据上面的分析可知,CO2-
作用是控制溶液pH,促使
3
CuCl沉淀的生成,故C正确;D. 根据上面的分析可知,将溶液3缓慢加入到含大量
SO2-/CO2-
的溶液中,制得的CuCl可能不纯,故D错误。
3 3
5. 【答案】(1)+3
(2)HCl
(3)NaCO+SiO NaSiO+CO↑
2 3 2 2 3 2
NaCO+Al2O3 2NaAlO +CO↑
2 3 2 2
(4)AlCl 、NaCl 促进Al3+、Fe3+水解生成聚合氯化铝铁(PAFC)
3
【解析】(1)由Fe (OH)Cl-x中元素化合价代数和等于零求得铁元素的化合价为
2 x 6
+3。(2)由最后产品含有氯元素分析可知,此酸是盐酸。(4)生成的NaSiO、NaAlO
2 3 2
经盐酸酸浸后生成硅酸沉淀、氯化铝溶液、氯化钠溶液;加热可促进铝离子、铁离子水解
生成聚合氯化铝铁。
6. 【答案】(1)-1价
(2) Fe O、MgO
2 3
(3)AlO—+HCO —+H2O === Al(OH)↓+CO2—
2 3 3 3
(4)防止NaH、NaAlH 与水蒸气反应
4
【解析】(1)四氢铝钠中氢元素显-1价。(2)试剂A为强碱,将铝元素转化成偏
铝酸盐,由于试剂A中溶质的阴离子和阳离子所含电子数相等,则试剂A为氢氧化钠。滤
渣1的主要成分是二氧化硅,滤渣2的 主要成分是氢氧化铁和氢氧化镁,在空气中灼烧生
成氧化铁、氧化镁。(3)偏铝酸钠和碳酸氢钠反应类似于较强酸制备较弱酸。(4)
NaH、NaAlH 均能够与水蒸气反应。
4
第5页