文档内容
热化学方程式
重难点 题型 分值
1. 掌握热化学方程式的概念及意义
重点 2. 掌握热化学方程式的书写步骤及其注意事项
3. 热化学方程式的正误判断方法
选择与填空 4-6分
1. 热化学方程式的书写以及书写中的注意事项
难点
2. 热化学方程式的正误判断方法
一、热化学方程式的概念及意义
1. 定义:表明反应所释放或吸收的热量的化学方程式叫做热化学方程式。
2. 表示意义:热化学方程式既能表示化学反应的物质变化又可表示化学反应中的能量变
化。
如:H(g)+1/2O (g)=H O(l) ΔH = -285.8kJ·mol-1,表示1mol氢气与1/2mol
2 2
氧气反应生成1mol液态水放出了285.8kJ的热量。由此可见热化学方程式表示意义更加丰
第1页富,对化学反应特征的表达更加饱满。
【求甚解】化学方程式与热化学方程式的比较
化学方程式 热化学方程式
是整数,既表示微粒个数,又 既可以是整数也可以是分数,只表
化学计量数
表示物质的物质的量 示物质的量
物质状态 不要求注明 必须在化学式后注明
H 无 有,且必须注明正负号及单位
△ 不仅表示化学反应中的物质变化,
意义 表示化学反应中的物质变化
还表示化学反应中的能量变化
二、热化学方程式的书写
1. “四步”书写热化学方程式
一写方程式——写出配平的化学方程式
二标状态——注明反应物的和生成物的聚集状态,(用 s、1、g、aq标明物质的聚集
状态)
三标条件——标明反应时的温度和压强(25℃、101kPa时无需注明)
四标ΔH——在方程式后写出ΔH(注意单位和“+”“-”)
2. 书写热化学方程式应注意的问题
热化学方程式与普通化学方程式相比,除了要遵守书写化学方程式的要求外还应注意
以下问题:
①注意△H 的符号和单位
ΔH只能写在标有反应物和生成物状态的化学方程式的右边。若为放热反应,ΔH为
“-”;若为吸热反应,ΔH为“+”。△H的单位一般为kJ/mol或kJ·mol-1。
②注意反应条件
反应热△H与测定条件(温度、压强等)有关。因此书写热化学方程式时应注明△H
的测定条件。绝大多数ΔH是在25℃、101kPa下测定的,此条件下进行的反应可不注明温
度和压强。
③注意物质的聚集状态
反应物和生成物的聚集状态不同,反应热△H不同。因此,必须注明物质的聚集状态
才能完整的体现出热化学方程式的意义。气体用“g”,液体用“l”,固体用“s”,溶液用
“aq”。注意溶液和纯液体的区别,如FeCl 溶液标注“aq”,纯水标注“l”。另外化学式相
3
同的同素异形体还应注明名称,如金刚石表示为“C(金刚石,s)”
④注意热化学方程式中的化学计量数
第2页a. 热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,并不表
示物质的分子数或原子数。因此化学计量数可以是整数,也可以是分数。
b. 热化学方程式中的反应热表示已完成时的热量变化。由于△H与反应完成的量有关,
所以方程式中的化学式前面的化学计量数必须与△H相对应,如果化学计量数加倍,则
△H也要加倍。当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
例如:已知H (g)+1/2O =H O(l) ΔH=-285.8kJ▪mol-1,则2H (g)+O =2H O
2 2 2 2 2 2
(l) ΔH=-571.6kJ▪mol-1,HO(l)= H (g)+1/2O ΔH=+285.8kJ▪mol-1
2 2 2
【求甚解】可逆反应的△H和实际吸收或放出热量的区别
不论化学反应是否可逆,热化学方程式中的△H都表示反应按照化学计量数所表示的
物质的量完全进行所放出或吸收的热量。
如2SO (g)+O (g) SO (g ΔH =-197kJ·mol-1是指2mol SO (g)和1mol
2 2 3 2
O (g)完全转化为2mol SO (g)时放出的热量为197kJ。若在相同的温度和压强下,向
2 3
某容器中加入2mol SO (g)和1molO (g),反应达到平衡时放出的热量为Q,因反应不
2 2
能进行彻底,故Q<197kJ。
三、热化学方程式的正误判断技巧
五个角度判断热化学方程式的正误:
一审“+”“-” →放热反应的△H一定为“-”,吸热反应的△H一定为“+”
二审单位→单位一般为“kJ·mol-1”,易错写成“kJ”或漏写
三审状态→物质的状态必须正确
四审数值→反应热的数值必须与方程式中的化学计量数相对应,即△H与化学计量数
成正比。当反应向逆向进行时,其反应热与正反应的反应热数值相等,符号相反
五审是否符合概念→如表示燃烧热、中和热的热化学方程式
例题1 根据热化学方程式:S(s)+O (g)=SO (g) ΔH=a kJ·mol-1(a=-
2 2
297.2)。分析下列说法,其中不正确的是( )
A. S(s)在O(g)中燃烧的反应是放热反应
2
B. S(g)+O(g)=SO(g) ΔH=b kJ·mol-1,则a>b
2 2
C. 1 mol SO (g)所具有的能量低于1 mol S(s)与1 mol O (g)所具有的能量之和
2 2
D. 16 g固体硫在空气中充分燃烧,可吸收148.6 kJ的热量
第3页【答案】D
【解析】由题中条件可知:反应的热效应ΔH=a kJ·mol-1=-297.2 kJ·mol-1,可知该
反应的正向反应为放热反应,故D错误;气态硫比固态硫放出热量多,由于 ΔH为负值,
所以a>b,故B正确。
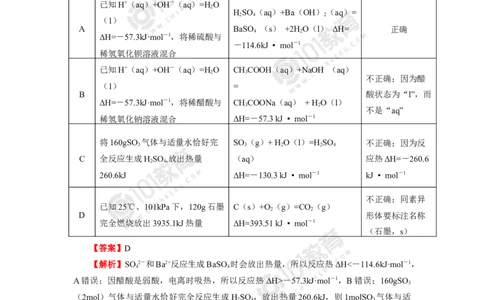
例题2 下列有关热化学方程的评价合理的是( )
实验事实 热化学方程式 评价
已知H+(aq)+OH-(aq)=H O
2
HSO (aq)+Ba(OH)(aq)=
2 4 2
(1)
A BaSO (s) +2H O(l) ΔH= 正确
4 2
ΔH=-57.3kJ·mol-1,将稀硫酸与
-114.6kJ ▪ mol-1
稀氢氧化钡溶液混合
已知H+(aq)+OH-(aq)=H O CHCOOH(aq)+NaOH (aq)
2 3
不正确;因为醋
(1) =
B 酸状态为“l”,而
ΔH=-57.3kJ·mol-1,将稀醋酸与 CHCOONa(aq) + H O(l)
3 2
不是“aq”
稀氢氧化钠溶液混合 ΔH=-57.3 kJ ▪ mol-1
将160gSO 气体与适量水恰好完 SO (g)+ H O(l)=H SO 不正确;因为反
3 3 2 2 4
C 全反应生成HSO ,放出热量 (aq) 应热ΔH=-260.6
2 4
260.6kJ ΔH=-130.3 kJ ▪ mol-1 kJ ▪ mol-1
不正确;同素异
已知25℃、101kPa下,120g石墨 C(s)+O (g)=CO (g)
2 2
D 形体要标注名称
完全燃烧放出3935.1kJ热量 ΔH=393.51 kJ ▪ mol-1
(石墨,s)
【答案】D
【解析】SO 2-和Ba2+反应生成BaSO 时会放出热量,所以反应热ΔH<-114.6kJ·mol-1,
4 4
A错误;因醋酸是弱酸,电离时吸热,所以反应热ΔH>-57.3kJ·mol-1,B错误;160gSO
3
(2mol)气体与适量水恰好完全反应生成HSO ,放出热量260.6kJ,则1molSO 气体与适
2 4 3
量水恰好完全反应生成HSO ,放出热量130.3kJ,评价错误,C错误;因C有多种同素异
2 4
形体,而同素异形体的能量是不同的,故在热化学方程式中要标明物质名称,D正确。
例题 书写下列热化学方程式:
(1)使氯气和水蒸气通过灼热的炭层,生成氯化氢气体和二氧化碳气体,该反应是放
热反应,当 1mol 氯气参与反应时释放 145kJ 的热量,写出该反应的热化学方程式:
第4页__________________________________。
(2)已知断开1mol H—H键、1mol N—H键、1mol N N键分别需要吸收的能量是
436kJ、391 kJ、946kJ,则 N (g)与 H (g)反应生成 NH (g)的热化学方程式为
2 2 3
_______________。
(3)硅粉与HC1在300℃时反应生成H 和标准状况下22.4L的SiHCl 气体,放出
2 3
225kJ热量,写出该反应的热化学方程式:__________________________。
【答案】(1)2C1 (g)+2H O(g)+C(s)=4HCl(g)+CO (g)ΔH =-290kJ·mol
2 2 2
-1
(2)N(g)+3H (g 2NH (g)ΔH =-92J·mol-1
2 2 3
(3)Si(s)+3HCl(g) SiHCl(g)+H (g)ΔH =-225kJ·mol-1
2
【解析】(1)使氯气和水蒸气通过灼热的炭层,生成氯化氢气体和二氧化碳气体,该
反应是放热反应,当1mol氯气参与反应时释放145kJ的热量,则该反应的热化学方程式为
2C1 (g)+2H O(g)+C(s)=4HCl(g)+CO (g)ΔH=-290kJ·mol-1。
2 2 2
(2)反应热=反应物总键能之和-生成物总键能之和,已知断开 1mol H—H键、
1molN—H键、1mol N N键分别需要吸收的能量是436kJ、391kJ、946kJ,所以N (g)与
2
H (g)反应生成 NH (g)的热化学方程式为 N (g)+3H (g) 2NH (g)ΔH
2 3 2 2 3
=946kJ·mol-1+3×436kJ·mol-1-6×391kJ·mol-1=-92kJ·mol-1。
(3)硅粉与 HC1 在 300℃时反应生成 H 和标准状况下 22.4L 的 SiHC1 气体(即
2
1mol),放出225kJ热量,则反应的热化学方程式为 Si(s)+3HCl(g) SiHCl
(g)+H (g)ΔH =-225 kJ·mol-1。
2
【点拨】在书写热化学方程式时,应先根据已知的反应物和生成物确定反应的化学方
程式,再标出各物质的聚集状态,并计算出反应热,注意ΔH的值与各物质化学计量数的
对应关系。
(答题时间:40分钟)
一、选择题
1. 胶状液氢(主要成分是H 和CH)有望用于未来的运载火箭和空间运输系统。实验测
2 4
得101kPa时,1 molH 完全燃烧生成液态水,放出285.8kJ的热量;1 mol CH 完全燃烧生
2 4
成液态水和CO,放出890.3kJ的热量。下列热化学方程式书写正确的是( )
2
A. 2H (g)+O (g)═2HO(l) ΔH=-285.8 kJ•mol-1
2 2 2
B. CH(g)+2O (g)═CO(g)+2H O(l) ΔH=-890.3 kJ•mol-1
4 2 2 2
C. CH(g)+2O (g)═CO(g)+2H O(g) ΔH=-890.3 kJ•mol-1
4 2 2 2
第5页D. CH (g)+2O (g)═CO(g)+2H O(l) ΔH=+890.3 kJ•mol-1
4 2 2 2
2. 乙醇燃料是一种清洁的能源燃料。燃烧a g乙醇(液态)生成CO 气体和液态HO,
2 2
放出热量为Q kJ,经测定a g乙醇与足量Na反应能生成H 5.6 L(标准状况),则乙醇燃
2
烧的热化学方程式表示正确的是( )
A. C HOH(l)+3O(g)=2CO(g)+3HO(l) ΔH(298 K)=-Q kJ·mol-1
2 5 2 2 2
1
2
B. C HOH(l)+3O(g)=2CO(g)+3HO(l) ΔH(298 K)=- Q kJ·mol-1
2 5 2 2 2
1 3 3
2 2 2
C. C HOH(l)+ O(g)=CO(g)+ HO(l) ΔH(298 K)=-Q kJ·mol
2 5 2 2 2
-1
3
2
D. C HOH(l)+3O(g)=2CO(g)+3HO(l) ΔH(298 K)=- Q kJ·mol-1
2 5 2 2 2
3. 已知:①2H(g)+O(g)=2HO(g) ΔH=-483.6 kJ·mol-1
2 2 2
②H(g)+S(g)=HS(g) ΔH=-20.1 kJ·mol-1
2 2
下列判断正确的是( )
A. 1 mol氢气完全燃烧生成液态水吸收热量241.8 kJ
B. 1 mol H O(g)和1 mol H S(g)的能量相差221.7 kJ
2 2
C. 由①②知,水的热稳定性小于硫化氢
D. 若反应②中改用固态硫,则1 mol S(s)完全反应放出的热量小于20.1 kJ
4. 下列依据热化学方程式得出的结论正确的是( )
A. 若S(单斜,s)=S(斜方,s)ΔH=-0.33 kJ·mol-1,则单斜硫比斜方硫稳定
B. 若2C H(g)+5O(g)=4CO(g)+2HO(l) ΔH=-2 687.2 kJ·mol-1,则
2 2 2 2 2
C H(g)的燃烧热ΔH=-1 343.6 kJ·mol-1
2 2
C. 已知H+(aq)+OH-(aq)=HO(l) ΔH=-57.3 kJ·mol-1,则NaOH(s)与
2
稀盐酸完全中和生成1 mol H O(l)时,放出57.3 kJ的热量
2
D. 已知2HS(g)+O(g)=2S(g)+2HO(l) ΔH;2HS(g)+3O(g)=
2 2 2 1 2 2
2SO (g)+2HO(l) ΔH,则ΔH<ΔH
2 2 2 1 2
二、填空题
5. 依据叙述,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO 和液态水时放热22.68 kJ。则表示
2
甲醇燃烧的热化学方程式为 __________________________________________。
(2)若适量的N 和O 完全反应,每生成23 g NO 需要吸收16.95 kJ热量。其热化学
2 2 2
方程式为 __________________________________________。
(3)用N 表示阿伏加德罗常数,在C H(气态)完全燃烧生成CO 和液态水的反应
A 2 2 2
第6页中,每有5N 个电子转移时,放出650 kJ的热量。其热化学方程
A
___________________________。
(4)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436
kJ、391 kJ、946 kJ,则N 与H 反应生成NH 的热化学方程式为_____________________ 。
2 2 3
6. 城市现使用的燃料大多用煤气、液化石油气。煤气的主要成分是一氧化碳和氢气的混
合气,它由煤炭与水(蒸气)反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式:______________________。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为:
C H(g)+5O(g)=3CO(g)+4HO(l)ΔH=-2219.9 kJ·mol-1
3 8 2 2 2
已知CO气体燃烧的热化学方程式为:
1
2
CO(g)+ O(g)=CO(g)ΔH=-283.0 kJ·mol-1
2 2
试比较同物质的量的C H 和CO燃烧,产生的热量比值约为________。
3 8
(3)已知氢气燃烧的热化学方程式为2H(g)+O(g)=2HO(l) ΔH=-
2 2 2
571.6 kJ·mol-1
试比较同质量的氢气和丙烷燃烧,产生的热量比值约为________。
(4)氢气是未来最理想的能源,除产生的热量大之外,还具有的优点是______。
7. 氨气具有还原性,例如,氨气能与卤素单质发生置换反应。已知几种化学键的键能数
据如表所示:
化学键 N—H N≡N Br—Br H—Br
键能/kJ·mol-1 391 946 194 366
请写出氨气与溴蒸气反应的热化学方程式:___________________________________。
第7页1.【答案】B
【解析】1molH 完全燃烧生成液态水,放出285.8kJ的热量,则热化学方程式为:H
2 2
(g)+1/2 O (g)═HO(l)△H=-285.8 kJ•mol-1;1 molCH 完全燃烧生成液态水和
2 2 4
CO ,放出890.3kJ的热量,则热化学方程式为:CH (g)+2O (g)═CO (g)+2H O
2 4 2 2 2
(l)△H=-890.3 kJ•mol-1;故答案为B。
2.【答案】C
【解析】据化学方程式:
2C HOH+2Na→2C HONa+H↑
2 5 2 5 2
2 mol 22.4 L
n(C HOH) 5.6 L
2 5
n(C HOH)=0.5 mol,即0.5 mol C HOH完全燃烧生成CO(g)和HO(l)的反
2 5 2 5 2 2
应热为ΔH=-Q kJ·mol-1,C项正确。
3.【答案】D
【解析】A项,1 mol氢气完全燃烧生成气态水放出热量241.8 kJ;B项,1 mol H O
2
(g)和1 mol H S(g)的能量无法比较;C项,水的热稳定性大于硫化氢;由固态硫到气
2
态硫需吸收热量,故1 mol S (s)完全反应放出的热量小于20.1 kJ。
4.【答案】B
【解析】单斜硫转化为斜方硫的反应为放热反应,说明等质量的斜方硫能量比单斜硫
的低,能量越低的物质越稳定,A项错误;燃烧热为1 mol可燃物完全燃烧生成稳定氧化
物时放出的热量,B项正确;NaOH固体溶于水放热,C项错误;物质完全燃烧时放热更多,
而比较ΔH 和ΔH 时要带上正负号比较,D项错误。
1 2
3
2
5.【答案】(1)CHOH(l)+ O(g)=CO(g)+2HO(l) ΔH=-725.76 kJ·mol
3 2 2 2
-1
(2)N(g)+2O(g)=2NO (g) ΔH=+67.8 kJ·mol-1
2 2 2
5
2
(3)C H(g)+ O(g)=2CO(g)+HO(l) ΔH=-1 300 kJ·mol-1
2 2 2 2 2
(4)N(g)+3H(g)=2NH (g) ΔH=-92 kJ·mol-1
2 2 3
【解析】根据反应热的定义计算出相关的热量,同时注意物质的状态,再书写相应的
热化学方程式即可。(4)ΔH=946+3×436-6×391=-92 kJ/mol。
6.【答案】(1)C+HO(g) CO+H (2)7.8 (3)2.8
2 2
(4)来源丰富,产物无污染等
【解析】(1)由题意“它由煤炭与水(蒸气)反应制得,故又称水煤气”知,反应方
第8页程式为C+HO(g) CO+H。
2 2
2219.9
283.0
(2)同物质的量的C H 和CO燃烧,产生的热量比值为 ≈7.8。
3 8
m 571.6
×
2 2
m
×2219.9
44
(3)同质量的氢气和丙烷燃烧,产生的热量比值为 ≈2.8。
7.【答案】2NH (g)+3Br (g)=N(g)+6HBr(g) ΔH=-214 kJ·mol-1
3 2 2
【解析】NH 与溴蒸气发生置换反应,化学方程式为 2NH (g)+3Br (g)=N
3 3 2 2
(g)+6HBr(g),ΔH=∑(反应物的键能)-∑(生成物的键能)=(6×391 kJ·mol-1
+3×194 kJ·mol-1)-(946 kJ·mol-1+6×366 kJ·mol-1)=-214 kJ·mol-1。
第9页燃烧热
重难点 题型 分值
1. 掌握燃烧热的概念并能进行简单的计算
重点
2. 掌握燃烧热与中和热的异同
选择与填空 4-6分
1. 燃烧热定义的理解
难点
2. 重点掌握燃烧热与中和热的异同
一、燃烧热
1. 定义
在25℃、101 kPa时,1mol纯物质完全燃烧生成指定产物时放出的热量,叫做该物质
的燃烧热,单位是kJ·mol-1或kJ/mol。
【求甚解】1燃烧热与反应热的关系
反应热范围广,包括中和热、燃烧热等所有化学反应中的热量变化,而燃烧热只是反
应热的一种形式。
【求甚解】2燃烧热定义中的几个限定词
第10页①温度、压强——“25℃、101kPa”是指燃烧前后的温度和压强,并非燃烧过程的温度
和压强;燃烧热一般是由实验测得。
②量——可燃烧物的物质的量为1mol;
③纯物质——“纯物质”是指纯净物,可以是单质也可以是化合物。
④指定产物——“指定产物”应满足化学性质稳定和状态稳定。如可燃物中的 C转化
为CO(g),S转化为SO (g),H转化为HO(l)。
2 2 2
指定产物没有特殊说明,一般是在氧气或空气中进行,因此并非所有的燃烧放热都叫
燃烧热,如H 在Cl 中的燃烧放热不是燃烧热。
2 2
【易错】对于中和热、燃烧热,用文字描述时不带负号,但其焓变(ΔH)还是负值。
【理解】研究燃烧热的意义
在工业生产中,所需要的热量大多数是通过可燃物燃烧产生的。研究燃烧热可实现充
分合理利用能源,节约资源,减少环境污染的目标。
2. 意义
燃烧热是以1 mol纯物质完全燃烧所放出的热量来定义的,因此在书写表示燃烧热的
热化学方程式时,可燃物必须是1 mol且生成稳定的氧化物,然后以此为标准来配平其余
物质的化学计量数,故在其热化学方程式中常出现分数;燃烧反应热化学方程式以实际燃
烧物质的量和生成物状态表示,可燃物不一定是1 mol。
【即时练】(1)以乙醇为例,25℃时乙醇的燃烧热ΔH=-1366.8kJ·mol-1,表示在25
℃、101 kPa时,1mol的CHCHOH(l)完全燃烧生成指定产物(CO 气体和液态水)时
3 2 2
放出1366.88kJ的热量。表示乙醇燃烧热的热化学方程式为 CHCHOH(l)+3O (g)=
3 2 2
2CO(g)+3H O(l) ΔH=-1366.8kJ·mol-1
2 2
(2)25 ℃、101 kPa时,甲烷的燃烧热 ΔH为-890.31 kJ·mol-1,热化学方程式为
CH g)+2O (g)=CO (g)+2HO(l) ΔH=-890.31 kJ·mol-1。表示1mol甲烷完
4( 2 2 2
全燃烧生成CO(g)和HO(l)时放出890.31 kJ的热量。
2 2
书写或判断表示燃烧热的热化学方程式要做到“四看”
一看可燃物的化学计量数是否为1。
二看碳元素是否完全燃烧生成CO(g)。
2
三看氢元素是否完全燃烧生成HO(l)。
2
四看ΔH数值是否为负及单位是否正确。
3. 燃烧反应释放的热量的计算方法
燃烧热是以1mol物质完全燃烧所放出的热量来定义的,因此计算燃烧反应释放的热量
时先应计算出可燃物的物质的量[(n(可燃物)],然后根据该可燃物的燃烧热ΔH计算燃
烧反应所释放的热量。其计算公式为:Q = n(可燃物)×ΔH(燃烧热)
放
【即时练】已知丙烷的燃烧热ΔH=-2215 kJ·mol-1。若一定量的丙烷完全燃烧后生成
第11页1.8g水,放出的热量约为________。
【答案】55.4 kJ
【解析】若生成1.8 g水,则放出的热量为2215×0.1/4 kJ≈55.4 kJ 。
二、燃烧热和中和热的比较
燃烧热 中和热
反应类型 放热反应
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 可燃物为1mol 不一定为1mol
生成物的量 不限量 生成水1mol
101 kPa 时,1mol 纯物质完
在稀溶液中,酸与碱反应生
反应热的含义 全燃烧生成指定产物时放出
成1mol水时所放出的热量。
不同点 的热量。
燃烧热为a kJ·mol-1 中和热为 57.3 kJ·mol-1或
表示法
或ΔH=-a kJ·mol-1 ΔH=-57.3 kJ·mol-1
热量大小与反应物的性质有 与酸、碱的强弱有关,与量
影响因素
关,与量无关 无关
例题1 下列热化学方程式中,ΔH能正确表示物质的燃烧热的是( )
1
2
A. CO(g)+ O(g)=CO (g) ΔH=-283.0 kJ·mol-1
2 2
1
2
B. C(s)+ O(g)=CO(g) ΔH=-110.5 kJ·mol-1
2
1
2
C. H(g)+ O(g)=H O(g) ΔH=-241.8 kJ·mol-1
2 2 2
D. 2C H (l)+25O(g)=16CO(g)+18HO(l) ΔH=-11036 kJ·mol-1
8 18 2 2 2
【答案】A
【解析】燃烧热表示1 mol纯物质完全燃烧生成稳定氧化物所放出的热量。A项,CO
的化学计量数为1,产物为稳定氧化物,ΔH代表燃烧热,正确;B、C项产物不是稳定氧
化物,ΔH不代表燃烧热,错误;D项,C H 的化学计量数为2,ΔH不代表燃烧热,错误。
8 18
例题2 已知:2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ·mol-1
2 2 2
第12页2CHOH(l)+3O(g)=2CO(g)+4HO(l) ΔH=-1452 kJ·mol-1
3 2 2 2
H+(aq)+OH-(aq)=HO(l) ΔH=-57.3 kJ·mol-1
2
下列说法正确的是( )
A. H (g)的燃烧热为571.6 kJ·mol-1
2
B. 同质量的H(g)和CHOH(l)完全燃烧,H(g)放出的热量多
2 3 2
1 1 1
2 2 2
C. HSO (aq)+ Ba(OH) (aq)= BaSO (s)+HO(l) ΔH=-57.3
2 4 2 4 2
kJ·mol-1
D. HCl(aq)+NaOH(s)=NaCl(aq)+HO(l) ΔH=-57.3 kJ·mol-1
2
【答案】B
【解析】A项,571.6 kJ热量是2 mol氢气完全燃烧时放出的,所以571.6 kJ·mol-1不
是氢气的燃烧热,错误;B项,1 g氢气完全燃烧放出的热量是571.6 kJ/4=142.9 kJ,1 g甲
醇完全燃烧放出的热量是1452 kJ/64≈22.7 kJ<142.9 kJ,正确;C项,生成物BaSO 难溶于
4
水,该反应不符合离子反应H++OH-=H O,故硫酸与氢氧化钡溶液反应生成硫酸钡和 1
2
mol水时,放出的热量不是57.3 kJ,错误;D项,氢氧化钠固体溶于水放出热量,因此氢
氧化钠固体与盐酸反应生成1 mol H O(l)放出的热量不是57.3 kJ,错误。
2
例题 一些烷烃的燃烧热如下表:
化合物 燃烧热(kJ·mol-1) 化合物 燃烧热(kJ·mol-1)
甲烷 890.3 正丁烷 2878.0
乙烷 1560.8 异丁烷 2869.6
丙烷 2221.5 2-甲基丁烷 3531.3
下列说法正确的是 ( )
A. 正戊烷的燃烧热大约是3 540 kJ·mol-1
B. 热稳定性:正丁烷>异丁烷
C. 乙烷燃烧的热化学方程式为2C H(g)+7O (g)= 4CO(g)+ 6 H O(g) ΔH=
2 6 2 2 2
-1 560.8 kJ·mol-1
D. 相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
【答案】A
【解析】根据正丁烷和异丁烷的燃烧热数据,可知正戊烷比2-甲基丁烷的燃烧热略
小些,A正确;1mol正丁烷、异丁烷完全燃烧放出的热量,前者比后者大,生成物和消耗
氧气的能量相同,说明异丁烷比正丁烷比能量低,能量越低越稳定,B错误;C中燃料加
倍,ΔH也应加倍,ΔH=-3121.6 kJ·mol-1,且HO应为液态,C错误;1gCH 燃烧放热约
2 4
第13页为55.69kJ,1gC H 燃烧放热约为52.03kJ,而C H 碳的质量分数比CH 的大,D错误。
2 6 2 6 4
(答题时间:40分钟)
一、选择题
1. 在25 ℃、101 kPa下,1 g甲醇燃烧生成CO 和液态水时放热22.68 kJ,下列表示甲醇
2
燃烧热的热化学方程式正确的是( )
A. CH OH(l)+ 3/2O (g)=CO(g)+2HO(l)
3 2 2 2
ΔH=+725.76 kJ mol-1
B. 2CHOH(l)+3O(g)=2CO(g)+4HO(g)
3 2 2 2
ΔH=-1 452.52 kJ mol-1
C. CHOH(l)+3/2O (g)=CO(g)+2HO(l)
3 2 2 2
ΔH=-725.76 kJ mol-1
D. 2CH OH(l)+3O(g)=2CO(g)+4HO(l)
3 2 2 2
ΔH=+1 452.52 kJ mol-1
1
2
2. 已知:CHOH(g)+ O(g)→CO(g)+2H(g) ΔH=+190 kJ·mol-1。下列
3 2 2 2
说法正确的是( )
A. CH OH的燃烧热为190 kJ·mol-1
3
B. 该反应说明CHOH比H 稳定
3 2
C. 反应中的能量变化与反应体系的温度和压强无关
1
2
D. CO (g)+2H(g)→CHOH(g)+ O(g) ΔH=-190 kJ·mol-1
2 2 3 2
3. 在一定条件下,S(s)和O(g)发生反应依次转化为SO (g)和SO (g)(已知:
8 2 2 3
2SO +O 2SO ),反应过程中的能量关系如图所示(图中的ΔH表示生成1mol产物
2 2 3
的数据)。下列说法正确的是( )
A. S (s)的燃烧热ΔH=-akJ·mol-1
8
第14页B. 1molSO 和过量O 反应可释放出bkJ的热量
2 2
C. 2SO (g) 2SO (g)+O(g) ΔH=+2bkJ·mol-1
3 2 2
D. 若使用VO 作催化剂,当SO (g)转化生成1molSO (g)时,释放的热量小于
2 5 2 3
bkJ
4. 有关氢气(H)、一氧化碳(CO)、辛烷(C H )、甲烷(CH)的热化学方程式
2 8 18 4
分别为:
2H(g)+O(g)=2HO(l) ΔH=-571.6kJ·mol-1
2 2 2
2CO(g)+O(g)=2CO(g) ΔH=-566kJ·mol-1
2 2
2C H (l)+25O(g)=16CO(g)+18HO(l) ΔH=-11036kJ·mol-1
8 18 2 2 2
CH(g)+2O(g)=CO(g)+2HO(l) ΔH=-890.3kJ·mol-1
4 2 2 2
下列说法正确的是( )
A. 1molC H (g)完全燃烧释放出的热量等于5518kJ
8 18
B. 相同质量的H、CO、CH 完全燃烧时,放出热量最少的是CH
2 4 4
C. 一氧化碳的燃烧热为566kJ·mol-1
D. 甲烷燃烧释放出445.15kJ热量时,转移4mol电子
二、填空题
5. 1 mol O 与足量氢气反应产生水蒸气放热483.6 kJ,写出该反应的热化学方程式:
2
________________________。
若1 g水蒸气转化成液态水放热2.444 kJ,请写出表示氢气燃烧热的热化学方程式:
________________________________。
6. 化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热
量的形式表现出来,叫做反应热。由于反应热的情况不同,反应热可以分为许多种,如燃
烧热和中和热等。
(1)下列ΔH表示物质燃烧热的是_________;表示物质中和热的是_________。(填
“ΔH”“ΔH ”或“ΔH”等)
1 2 3
A. 2H (g)+O(g)=2HO(l) ΔH
2 2 2 1
B. C(s)+1/2O (g)=CO(g) ΔH
2 2
C. CH(g)+2O(g)=CO(g)+2HO(g) ΔH
4 2 2 2 3
D. C(s)+O(g)=CO(g) ΔH
2 2 4
E. C H O(s)+6O(g)=6CO(g)+6HO(l) ΔH
6 12 6 2 2 2 5
F. NaOH(aq)+HCl(aq)=NaCl(aq)+HO(l) ΔH
2 6
G. 2NaOH(aq)+HSO (aq)=NaSO (aq)+2HO(l) ΔH
2 4 2 4 2 7
(2)根据2.00 g C H 气体完全燃烧生成液态水和CO 气体,放出99.6 kJ的热量,写
2 2 2
第15页出该反应的热化学方程式: ____________________________________。
第16页1.【答案】C
【解析】A. 在热化学反应方程式中ΔH>0,表示吸热,而甲醇燃烧生成CO 和液态水
2
的反应是放热反应,故A错误;B. 燃烧热是1 mol可燃物,该热化学方程式是2 mol甲醇
燃烧放出的热量,且HO为气态,故B错误;C. 1 mol甲醇完全燃烧生成二氧化碳和液态
2
水放热725.76 kJ,燃烧热的热化学方程式为CHOH(l)+3/2O (g)=CO(g)+2HO
3 2 2 2
(l) ΔH=-725.76 kJ/mol,故C正确;D. 反应吸热时焓变值为正值,放热时焓变值为
负值,甲醇完全燃烧生成二氧化碳和液态水放热,ΔH<0,故D错误。
2.【答案】D
【解析】燃烧热的定义中必须生成稳定的氧化物,而该反应没有生成液态水,A选项
错误;该反应为吸热反应,反应物的总能量小于生成物的总能量,反应物总体的稳定性大
于生成物总体的稳定性,不能单一反应物与单一生成物进行比较,B选项错误;反应中的
能量变化与压强和温度也有关系,C选项错误;该反应的逆过程为放热反应,且各物质的
物质的量无变化所以热量数值不变,D选项正确。
3.【答案】C
1
8
【解析】根据题图可知,1molO (g)和 molS (s)反应生成1mol二氧化硫气体时
2 8
放热akJ,依据燃烧热的概念,可写出热化学方程式:S(s)+8O(g)=8SO (g)
8 2 2
ΔH=-8akJ·mol-1,则S(s)的燃烧热ΔH=-8akJ·mol-1,A项错误;由题图可知,
8
1molSO 和0.5molO 完全反应生成1molSO (g)时释放出bkJ的热量,但SO 和O 的反应
2 2 3 2 2
是可逆反应,1molSO 不能完全转化为1molSO ,故1molSO 和过量氧气反应释放出的热量
2 3 2
小于bkJ,B项错误;催化剂不会改变反应热,故当使用VO 作催化剂时,SO (g)转化
2 5 2
生成1molSO (g),反应的ΔH=-bkJ·mol-1,D项错误。
3
4.【答案】D
【解析】C H (l)→C H (g)吸收热量,所以1 mol C H (g)完全燃烧释放出的
8 18 8 18 8 18
热量大于5 518 kJ,A项错误;根据题给的热化学方程式,可知每克物质完全燃烧时放出的
热量为H 142.9 kJ,CO 10.1 kJ,CH 55.6 kJ,则相同质量的H 、CO、CH 完全燃烧时,
2 4 2 4
放出热量最少的是CO,B项错误;根据燃烧热的定义可知,C项错误;CH 燃烧释放出
4
445.15 kJ热量时,消耗0.5 mol CH ,转移4 mol电子,D项正确。
4
5.【答案】2H(g)+O(g)=2HO(g) ΔH=-483.6 kJ·mol-1
2 2 2
1
2
H(g)+ O(g)=HO(l) ΔH=-285.8 kJ·mol-1
2 2 2
【解析】据题意知1 mol O 与足量H 反应的热化学方程式为:
2 2
O(g)+2H(g)=2HO(g) ΔH=-483.6 kJ·mol-1。
2 2 2
第17页上述反应中共生成36 g气态水,1 g H O(g)―→HO(l)放出的热量为2.444 kJ,所
2 2
以36 g H O(g)―→HO(l)放出的热量为2.444 kJ·g-1×36 g≈88.0 kJ,所以1 mol O 与2
2 2 2
mol H 反应生成液态水时的热化学方程式为:
2
O(g)+2H(g)=2HO(l)
2 2 2
ΔH=-571.6 kJ·mol-1。
故H的燃烧热为285.8 kJ·mol-1,表示H 燃烧热的热化学方程式为:
2
1
2
H(g)+ O(g)=HO(l)
2 2 2
ΔH=-285.8 kJ·mol-1。
6.【答案】(1)ΔH、ΔH ΔH
4 5 6
5
2
(2)C H(g)+ O(g)=2CO(g)+HO(l) ΔH=-1 294.8 kJ·mol-1
2 2 2 2 2
【解析】(1)根据燃烧热的含义可知 ΔH 、ΔH 为燃烧热。根据中和热的含义可知
4 5
ΔH 为中和热。(2)由2.00 g C H 完全燃烧放出热量为99.6 kJ可得1 mol C H 气体完全燃
6 2 2 2 2
烧放出热量为99.6 kJ÷(2.00 g/26 g)=1 294.8 kJ。故C H 气体燃烧的热化学方程式为
2 2
5
2
C H(g)+ O(g)=2CO(g)+HO(l) ΔH=-1 294.8 kJ·mol-1。
2 2 2 2 2
第18页