文档内容
1.2.1 盖斯定律(学案)
1.巩固化学反应热效应与反应的焓变之间的关系
2.能用盖斯定律进行有关反应热的简单计算。
1.用盖斯定律进行有关反应热的简单计算。
已知1g氢气燃烧生成液态水和气态水时分别放出142.9 kJ和120.9 kJ的热量,分别写出氢气燃烧
生成液态水和气态水的热化学方程式。
__________________________________________________________________________________
_____________________________________________________________________________
一、盖斯定律
1.1840年,盖斯(G.H.Hess,俄国化学家)从大量的实验事实中总结出一条规律:化学
反应不管是一步完成还是分几步完成,其_____是相同的。也就是说,化学反应的____只与反应的
___和_____有关,而与具体反应进行的_____无关。如果一个反应可以分几步进行,则各分步反应
的反应热之和与该反应一步完成时的反应热是_______的,这就是盖斯定律。
2.盖斯定律在生产和科学研究中的意义
【练习】下列与化学反应能量变化相关的叙述正确的是( )
A.生成物总能量一定低于反应物总能量
B.加入催化剂,能加快化学反应速率,同时提高了反应物的平衡转化率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.需要加热才能发生的反应一定是吸热反应
【练习】如图所示转化关系(X代表卤素),下列说法错误的是( )A.△H
2
>0 B.△H
3
=△H
1
﹣△H
2
C.按Cl、Br、I的顺序,△H 依次增大 D.△H 越大,HX越稳定
3 1
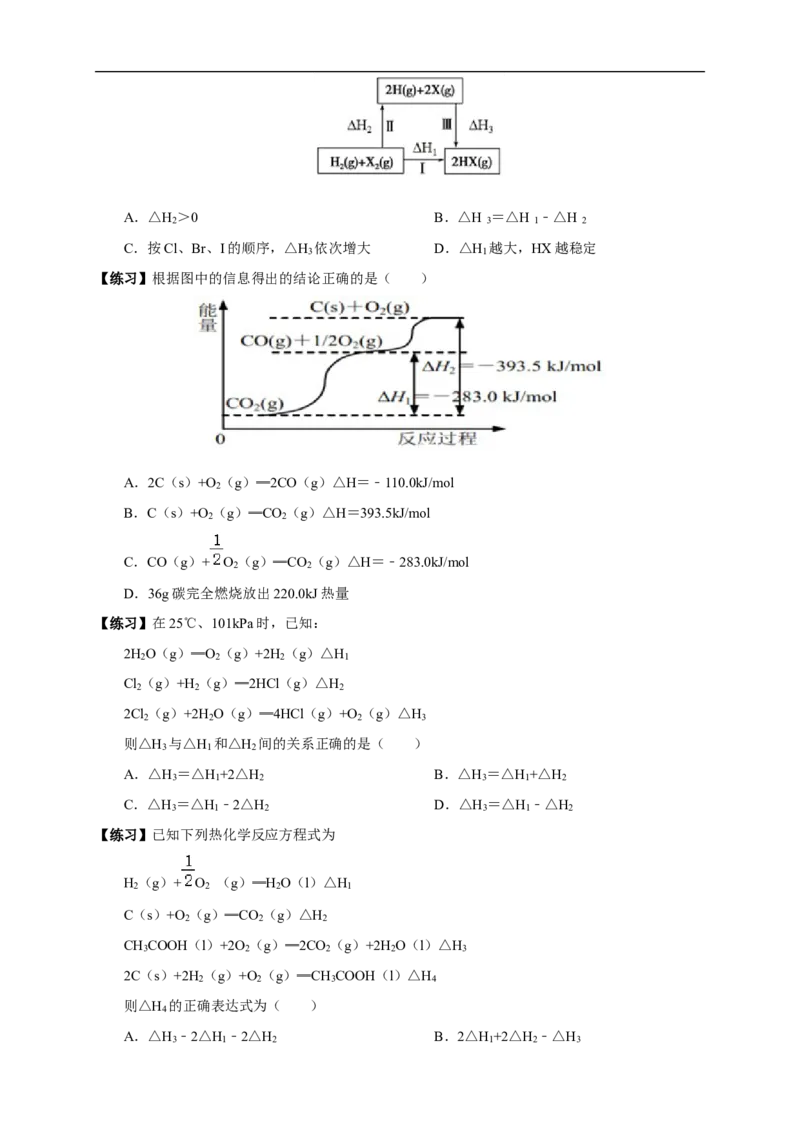
【练习】根据图中的信息得出的结论正确的是( )
A.2C(s)+O (g)═2CO(g)△H=﹣110.0kJ/mol
2
B.C(s)+O (g)═CO (g)△H=393.5kJ/mol
2 2
C.CO(g)+ O (g)═CO (g)△H=﹣283.0kJ/mol
2 2
D.36g碳完全燃烧放出220.0kJ热量
【练习】在25℃、101kPa时,已知:
2H O(g)═O (g)+2H (g)△H
2 2 2 1
Cl (g)+H (g)═2HCl(g)△H
2 2 2
2Cl (g)+2H O(g)═4HCl(g)+O (g)△H
2 2 2 3
则△H 与△H 和△H 间的关系正确的是( )
3 1 2
A.△H =△H +2△H B.△H =△H +△H
3 1 2 3 1 2
C.△H =△H ﹣2△H D.△H =△H ﹣△H
3 1 2 3 1 2
【练习】已知下列热化学反应方程式为
H (g)+ O (g)═H O(l)△H
2 2 2 1
C(s)+O (g)═CO (g)△H
2 2 2
CH COOH(l)+2O (g)═2CO (g)+2H O(l)△H
3 2 2 2 3
2C(s)+2H (g)+O (g)═CH COOH(l)△H
2 2 3 4
则△H 的正确表达式为( )
4
A.△H ﹣2△H ﹣2△H B.2△H +2△H ﹣△H
3 1 2 1 2 3C.2△H ﹣2△H +△H D.2△H ﹣2△H ﹣△H
1 2 3 1 2 3
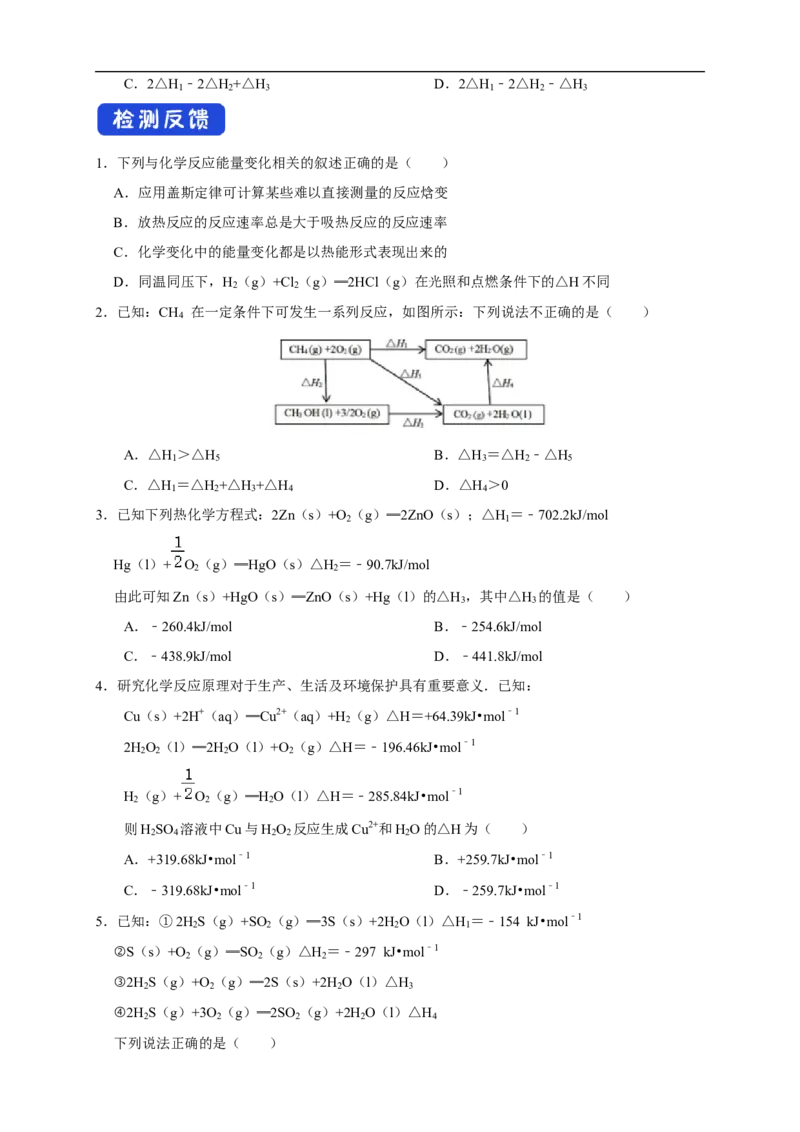
1.下列与化学反应能量变化相关的叙述正确的是( )
A.应用盖斯定律可计算某些难以直接测量的反应焓变
B.放热反应的反应速率总是大于吸热反应的反应速率
C.化学变化中的能量变化都是以热能形式表现出来的
D.同温同压下,H (g)+Cl (g)═2HCl(g)在光照和点燃条件下的△H不同
2 2
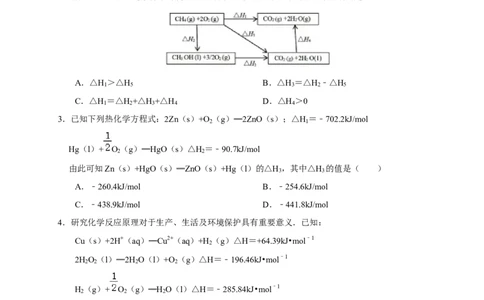
2.已知:CH 在一定条件下可发生一系列反应,如图所示:下列说法不正确的是( )
4
A.△H >△H B.△H =△H ﹣△H
1 5 3 2 5
C.△H =△H +△H +△H D.△H >0
1 2 3 4 4
3.已知下列热化学方程式:2Zn(s)+O (g)═2ZnO(s);△H =﹣702.2kJ/mol
2 1
Hg(l)+ O (g)═HgO(s)△H =﹣90.7kJ/mol
2 2
由此可知Zn(s)+HgO(s)═ZnO(s)+Hg(l)的△H ,其中△H 的值是( )
3 3
A.﹣260.4kJ/mol B.﹣254.6kJ/mol
C.﹣438.9kJ/mol D.﹣441.8kJ/mol
4.研究化学反应原理对于生产、生活及环境保护具有重要意义.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H (g)△H=+64.39kJ•mol﹣1
2
2H O (l)═2H O(l)+O (g)△H=﹣196.46kJ•mol﹣1
2 2 2 2
H (g)+ O (g)═H O(l)△H=﹣285.84kJ•mol﹣1
2 2 2
则H SO 溶液中Cu与H O 反应生成Cu2+和H O的△H为( )
2 4 2 2 2
A.+319.68kJ•mol﹣1 B.+259.7kJ•mol﹣1
C.﹣319.68kJ•mol﹣1 D.﹣259.7kJ•mol﹣1
5.已知:①2H S(g)+SO (g)═3S(s)+2H O(l)△H =﹣154 kJ•mol﹣1
2 2 2 1
②S(s)+O
2
(g)═SO
2
(g)△H
2
=﹣297 kJ•mol﹣1
③2H
2
S(g)+O
2
(g)═2S(s)+2H
2
O(l)△H
3
④2H
2
S(g)+3O
2
(g)═2SO
2
(g)+2H
2
O(l)△H
4
下列说法正确的是( )A.△H >△H B.△H =+143kJ•mol﹣1
3 4 3
C.无法计算△H 的值 D.H S 燃烧热为1045kJ•mol﹣1
4 2
6.在1200℃时,天然气脱硫工艺中会发生下列反应
①H
2
S(g)+ O
2
(g)═SO
2
(g)+H
2
O(g)△H
1
②2H
2
S(g)+SO
2
(g)═ S
2
(g)+2H
2
O(g)△H
2
③H
2
S(g)+ O
2
(g)═S(g)+H
2
O(g)△H
3
2S(g)═S (g)△H 则△H 的正确表达式为( )
2 4 4
A.△H = (△H +△H ﹣3△H ) B.△H = (3△H ﹣△H ﹣△H )
4 1 2 3 4 3 1 2
C.△H = (△H +△H ﹣2△H ) D.△H = (△H ﹣△H ﹣3△H )
4 1 2 3 4 1 2 3
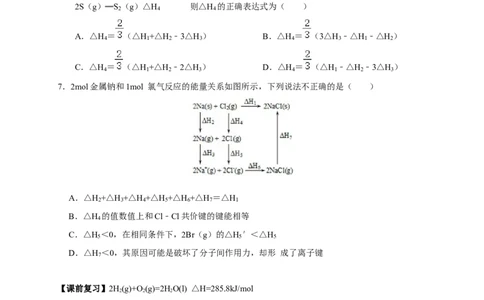
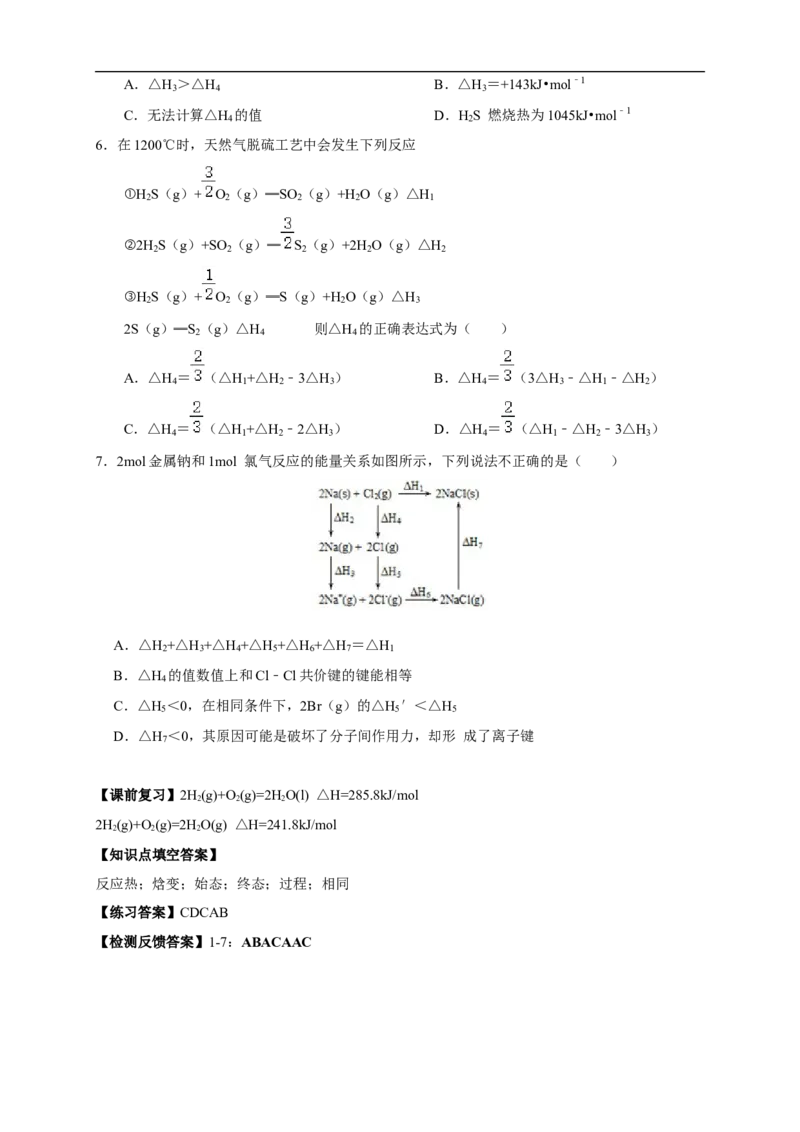
7.2mol金属钠和1mol 氯气反应的能量关系如图所示,下列说法不正确的是( )
A.△H +△H +△H +△H +△H +△H =△H
2 3 4 5 6 7 1
B.△H 的值数值上和Cl﹣Cl共价键的键能相等
4
C.△H <0,在相同条件下,2Br(g)的△H ′<△H
5 5 5
D.△H <0,其原因可能是破坏了分子间作用力,却形 成了离子键
7
【课前复习】2H(g)+O(g)=2HO(l) △H=285.8kJ/mol
2 2 2
2H(g)+O(g)=2HO(g) △H=241.8kJ/mol
2 2 2
【知识点填空答案】
反应热;焓变;始态;终态;过程;相同
【练习答案】CDCAB
【检测反馈答案】1-7:ABACAAC