文档内容
第一章《物质及其变化》教学设计
第二节《离子反应》
第二课时:离子反应和离子方程式
课题: 1.2.2 离子反应 课时 1 授课年级 高一
课标 通过实验事实认识离子反应及其发生的条件;能结合实例书写离子反应方程式及判断其正
要求 误;理解离子方程式的意义。
本节内容属于人教版(2019版)必修第一册第一章第二节内容。《离子反应》是重要的化
学用语,在中学阶段的基本概念基础理论知识中,占有极其重要的地位,是中学化学教学的重
点和难点之一,并贯穿于中学化学教材的始终。中学化学中要学习许多重要元素及其化合物的
知识,都可能涉及离子反应及其方程式的书写。学生要能通过实验认识离子反应及其离子反应
发生的条件,了解常见离子的检验方法,能初步认识到离子共存问题,为将来的离子平衡问题
打下伏笔。学好这一节内容,能很好揭示溶液中化学反应的本质,为今后元素化合物知识、电
解质溶液以及电离平衡的学习奠定一定的化学基础,并且正确而又熟练地书写离子方程式,是
高中学生必须掌握的基础知识,也是历年高考的必考内容。本节教学分三个课时,第一课时学
习电解质的电离,第二课时学习离子反应,第三课时学习“离子反应的应用”。
本课时第二课时“离子反应”是整个高中阶段化学学习的重要基础之一,本课时的内容主
要是使学生正确地理解离子反应的概念,并能够准确地书写离子方程式,为必修课程后续章节
以及选修中有关“溶液中的离子平衡”的学习打好根基。
本部分教材内容是在学习了电离合电离方程式的基础上,通过实验1-3的现象和分析,得
出硫酸钠溶液与氯化钡溶液反应的微观实质,从而引出离子反应和离子反应方程式。然后,教
教材 材以“思考与讨论”的形式,得出中和反应的实质,引导学生深入认识离子反应。最后,教材
说明酸、碱、盐在水溶液中发生复分解反应的微观实质,并总结出这类离子反应发生的条件。
分析
新版教材与旧版教材在此内容上有较大的不同,旧版中的实验直接放在了新版中的“思考与讨
论”,知识的呈现方式不同,新版的设置更符合学生现有的知识和能力,更符合学生的认知过
程。
新版教材对复分解反应的实质讲解更为详细,使学生对复分解反应理解更为透彻,形成从
宏观到微观的辨识能力。同时,电解质的电离、离子方程式及离子方程式的书写属于核心旧版
概念和基本理论,内容比较抽象,易于理解但难于掌握,应用更加复杂,这部分内容的学习为
选择性必修内容的学习奠定了一定的基础。
本课时教学可充分利用探究实验,采用实验、观察、思考和交流等方式,通过对实验现象
的分析,启发、引导学生得出结论,使学生在课堂学习中掌握好学习内容。既可以激发学生的
学习兴趣,调动学生的主体作用,又能通过实验使学生经历由感性认识到理性认识的过程,从
而使学生的认识有了一个质的飞跃,同时还可以提高学生的实验意识。总之,新知识的获得,
必须由浅入深,由远及近,由已知到未知,循序渐进。因上一课时已经学习了电解质的电离和
电离方程式的书写,因此教学时可将这部分知识应用于探究式教学,由实验探究旧知识,引出
新概念,由表及里地揭示反应的实质,使学生深刻地掌握离子反应、离子方程式的概念,教师
再通过对关键词的点拨,巩固定义的外延和内涵,培养学生分析、对比、归纳和总结的能力。
1.通过分析酸、碱、盐之间的反应事实及硫酸钠溶液与氯化钡溶液反应实质探究,认识
离子反应,理解离子反应的定义及实质。
教学
2.通过阅读思考,实例分析,知道离子方程式的定义、意义及书写步骤,理解离子反应
目标 发生的条件,掌握常见离子方程式的书写及正误判断的基本方法。
3.通过实验探究、讨论交流、分析归纳等一系列科学研究过程,体验科学研究的基本方
法,初步掌握溶液中离子反应的基本类型。教学 重点:离子反应的概念、发生条件、书写及正误判断
重、 难点:离子方程式的书写及正误的判断
难点
宏观辨识与微观探析:从宏观上理解离子反应及离子方程式表示的意义,并能够从微观上明确
复分解反应的本质就是溶液中离子之间的反应。通过实验探究与理论思考建立离子观,能从微
观的角度来解释宏观化学现象,进一步发展宏观现象与微观变化之间的联系。
核心
证据推理与模型认知:建立溶液中离子反应的基本模型,能够利用该模型理解电解质在溶液中
素养 发生复分解反应的条件。
科学探究与创新意识:通过实验探究、总结归纳、分析推理等一系列科学研究过程,了解科学
研究的基本方法,体会在离子反应的研究中体现的科学方法。
学生在第一课时的学习中,已经了解了电解质的基本概念、复分解反应发生的条件,能够
判断典型的电解质(酸、碱、盐),能够正确书写强酸、强碱和可溶盐的电离方程式,也能够
学情 理解电解质在溶液中的电离,明确电解质在溶液中以离子状态存在等。在此基础上又知道了硫
分析
酸钠与氯化钡溶液反应的实质是Ba2+与+SO
4
2-的反应,便能很自然地过渡到
离子
反 应及离子反
应方程式的书写的学习,再由不同的化学反应归纳出离子方程式所代表的应用,符合由宏观到
微观,由共性到一般的思维特点。
教学过程
教学 设计意
教学活动
环节 图
【回顾1】在酸的溶液里,酸根离子所带负电荷的总数等于酸电离时生成的H+的总
数;在碱的溶液里,跟金属离子结合的OH-的总数等于这种金属离子所带的正电荷
的总数;在盐的溶液中,金属(或铵根)离子所带的正电荷的总数等于酸根离子所带 回顾联
系旧
的负电荷的总数。
知,预
【回顾2】电解质电离方程式的书写的基本规律。 习新
知,为
【学生1】强酸、强碱、盐完全电离,用“===”表示。如HSO 、NaOH、(NH )SO
2 4 4 2 4 新知学
的电离方程式分别为HSO ===2H++SO、NaOH===Na++OH-、(NH )SO ===2NH 习作铺
2 4 4 2 4
垫。
+SO。
【学生 2】弱酸、弱碱部分电离,用“ ”表示。如 CHCOOH CHCOO-
3 3
环 +H+、NH 3 .H 2 O NH 4 ++OH-。
节
【学生3】多元弱酸分步电离分步写,且电离程度逐步减弱,以第一步电离为主。
一
、 如HS电离方程式为HS H++HS-;HS -H++S2-。多元弱碱分步电离一步
2 2
问
情 题 写。如Cu(OH) Cu2++2OH-。
2
景 情
导 境
【预习1】酸、碱、盐在水溶液中发生的复分解反应,实质是两种电解质在溶液中
利用化
入 相互交换离子,该类离子反应发生的条件是生成沉淀、放出气体或生成水。 学史创
设问题
【预习2】离子方程式定义:用实际参加反应的离子符号表示反应的式子 ; 情境,
激发学
【预习3】离子方程式的特点:①只表示实际发生反应的离子和其他物质 ;②不仅
习兴趣
可以表示一定物质间的某个反应,还可以表示所有同一类型的离子反应 ;
和探究
【预习4】离子方程式的书写:除了应遵守质量守恒定律外,还应遵守电荷守恒。 欲望。
培养安
【导入】传说三国时,诸葛亮为了擒拿南王孟获(历史上有名的七擒七纵),率军
全意
南征至云南西洱河,遇四口毒泉,其中一口为哑泉。时逢天气好生炎热,人马饮用
识。
了哑泉水后,全都中毒,将士们都说不出话来。后来幸得一智者指教,复饮安乐泉
水,“随即吐出恶涎,便能言语”。你知道其中的化学原理吗?通过本节课的学习,我们就能解开这个谜团!(见PPT图片)
【投影】
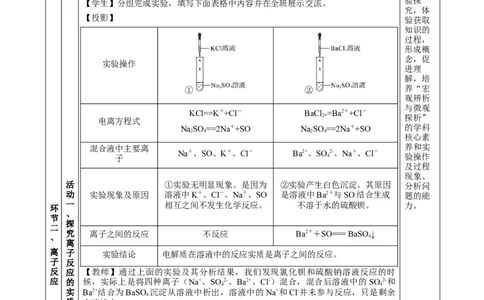
【问题1】实验探究:结合教材P17实验1-3,完成实验,并将实验现象及结论填在
下列表格中。 通过实
验探
【学生】分组完成实验,填写下面表格中内容并在全班展示交流。
究,体
【投影】 验获取
知识的
过程,
形成概
念,促
实验操作
进理
解,培
① ② 养“宏
观辨析
与微观
KCl==K++Cl- BaCl =Ba2++Cl-
2= 探析”
电离方程式
NaSO ==2Na++SO NaSO ==2Na++SO 的学科
2 4 2 4
核心素
混合液中主要离 养和实
Na+、SO、K+、Cl- Ba2+、SO 2-、Na+、Cl-
子 4 验操作
及过程
现象、
活 ①实验无明显现象。是因为 ②实验产生白色沉淀。其原因 分析问
动 实验现象及原因 溶液中K+、Cl-、Na+、SO 是溶液中Ba2+与SO结合生成 题的能
一 相互之间不发生化学反应。 不溶于水的硫酸钡。 力。
环
、
节
探
二
究 离子之间的反应 不反应 Ba2++SO=== BaSO↓
、 4
离
离 子 实验结论 电解质在溶液中的反应实质是离子之间的反应。
子 反
反 应 【教师】通过上面的实验及其分析结果,我们发现氯化钡和硫酸钠溶液反应的时
应 的 候,实际上是将四种离子(Na+、SO 2-、Ba2+、Cl-)混合,混合后溶液中的SO 2-和
4 4
实 Ba2+结合为BaSO 沉淀从溶液中析出,溶液中的Na+和Cl-并未参与反应,只是剩余
4
质 在溶液中。
【设疑】上述实验的化学反应方程式是什么?
【学生】板书:NaSO + BaCl = BaSO↓ + 2NaCl
2 4 2 4
【教师】同理,我们可以分析出在氯化钾溶液中存在的是钾离子和氯离子,在硝酸
钠溶液中存在的是钠离子和硝酸根离子,混合溶液中就必定存在上述四种离子。将
充分挖
溶液蒸干时,阴阳离子结合为固体从溶液中析出,显然我们无法控制哪个阴离子与
掘教材
哪个阳离子结合,所以一定会得到四种盐的混合物。这说明,在溶液中电解质常常
资源,
以离子形式存在,我们不能停留在物质层面上理解溶液中电解质之间的反应,应该
促进概
深入到微观领域,从离子的角度出发,重新审视溶液中电解质之间的反应。
念的理
【问题2】阅读教材P18页第二自然段,请写出BaCl 溶液与NaSO 溶液反应的化学 解与掌
2 2 4
握。
方程式,并从微观粒子的角度分析BaCl 溶液与NaSO 溶液反应的实质?回答什么
2 2 4是离子反应?。
【学生1】①化学方程式:BaCl 2 +Na 2 SO 4 ===BaSO 4 ↓+2NaCl; 利用所
学知识
【学生2】②该反应的本质:Ba2++SO 2-==BaSO ↓;
4 4
解决实
【学生3】③离子反应:离子之间的反应,即有离子参加或有离子生成的化学反 际问
题,充
应。中学阶段所学的离子反应一般是指在溶液中进行的反应。
分体现
【问题3】应用探究:已知,铜为重金属,可溶性的 Cu2+会使蛋白质变性,因此, 理论对
如果人和动物喝了含Cu2+的水就会中毒。哑泉水是一种含铜盐的泉水,主要成分为 实践的
硫酸铜,称为胆水。这种胆水饮用后会使人恶心、呕吐、腹泻,言语不清,直至虚 指导作
脱、痉挛而死。而安乐泉水中含有大量的石灰水,请你用所学知识解释用安乐泉水 用。
给哑泉水解毒的原理。
【学生1】①原理:CuSO ==Cu2++SO2-、Ca(OH) ==2OH-+Ca2+;
4 4 2
其中:Cu2++2OH-==Cu(OH) ↓,即:CuSO +Ca(OH) == Cu(OH) ↓+CaSO
2 4 2 2 4
【学生2】②误饮哑泉中含有较多的可溶性CuSO 的水后,再大量饮安乐泉中含有
4
大量碱的泉水,碱先中和了胃酸中的盐酸,然后多余的碱又会在胃肠中与CuSO 发
4
生反应Cu2++2OH-==Cu(OH) ↓。使原来会使人体吸收的可溶性铜盐变成不溶性的
2
分析学
Cu(OH) 沉淀而不再会被吸收,因此,具有解毒作用。
2 情,及
【对应训练1】NaHCO 和NaHSO 的溶液混合后,实际参加反应的离子是 时评
3 4
价,调
A.H+和CO B.HCO和HSO
控课
C.Na+、HCO和H+ D.HCO和H+ 堂,巩
固所
【答案】D
学。
【解析】NaHCO 和 NaHSO 的电离方程式分别如下:NaHCO ===Na++HCO;
3 4 3
NaHSO===Na++H++SO,故D项正确。
4
【对应训练2】下列各组物质相互混合后,不会发生离子反应的是
A.NaSO 溶液和MgCl 溶液 B.NaCO 溶液和稀硫酸
2 4 2 2 3
C.NaOH溶液和Fe (SO ) 溶液 D.Ca(OH) 和盐酸
2 4 3 2
【答案】A
【解析】题中的各种物质在溶液中如果能够发生反应,则都是复分解反应。NaSO
2 4
溶液和MgCl 溶液如果反应,则生成MgSO 和NaCl,由于MgSO 和NaCl都是可溶
2 4 4
性物质,不具备复分解反应发生的条件,所以不会发生离子反应。
【过渡】通过上面的学习,我们知道了电解质在溶液中进行的反应,本质上就是离
子之间的反应,我们还知道将KCl和NaSO 两种电解质的溶液混合后,离子之间却
2 4
并不能反应反应,那么,电解质需要哪些条件才能在溶液中发生离子反应呢?
【问题1】电解质溶液之间发生反应时有哪些不同情况?结合下表内容举例说明。
【学生】讨论交流,完成表格内容。 采用宏
微结合
【投影】
的方
式,开
向氢氧化钠溶液 展实验
向硫酸铜溶液中滴
举例 (含酚酞)中滴 向碳酸钠溶液中滴加稀盐酸 探究,
加氢氧化钠溶液
加酚酞 体验获
取知识
的过
程。现象 有蓝色沉淀生成 红色褪去 有无色无味气体产生
离子方程 Cu2+ + 2OH- =
H+ +2OH- = H O 2H++CO 2-=H O+CO
活 式 Cu(OH) ↓ 2 3 2 2 从个别
2
动 (溶液
二 中复分
、 解反应
生成沉淀使铜离子 生成水,使氢离
探 生成气体,使氢离子和碳酸 的三种
分析 和氢氧根离子浓度 子和氢氧根离子
究 根离子浓度减小 不同情
减小 浓度减小
离 况)到
子 一般
反 (复分
【问题2】归纳总结:结合上面分析,阅读教材P19页第二自然段,你认为酸、
应 解的离
碱、盐在水溶液中发生的复分解反应的条件及结果分别是什么?
发 子反应
生 【学生1】①由上表可知,酸、碱、盐在水溶液中发生复分解反应,本质上就是两 的条
的 种电解质在溶液中相互交换离子(即阴、阳离子重新组合)的过程。 件),
条
【学生 2】②这类离子反应发生的条件是:生成难溶于水的物质(又称沉淀反 形成对
件
应)、放出气体(又称产气反应)或生成水。只要具备上述条件之一,反应就能发 知识规
生。 律性的
认识。
【学生3】③离子反应发生后的结果(实质)是导致溶液中某些(或某种)离子浓
度明显减小。也是电解质在溶液中反应的实质。
【学生4】♦④氧化还原型离子反应(下节内容学习),必须通过自发反应以降低
参加反应的相关离子浓度。
分析学
【对应训练1】下列不能发生离子反应的是( )
情,及
①NaCl溶液与AgNO 溶液 ②KNO 溶液与NaOH溶液 ③稀硫酸与BaCl 溶液 ④ 时评
3 3 2
价,调
盐酸与NaCO 溶液 ⑤NaCO 溶液与Ca(OH) 溶液 ⑥NaOH溶液与稀HNO 溶液
2 3 2 3 2 3
控课
⑦锌与CuSO 溶液 ⑧稀HSO 和NaCl溶液 ⑨NaSO 溶液和CuCl 溶液
4 2 4 2 4 2 堂,巩
【答案】②⑧⑨ 固所
学。
【解析】复分解型离子反应的条件是a.生成难溶或微溶物质;b.生成难电离物质(弱
酸、弱碱、HO);c.生成挥发性物质(或气体)。三者满足其一即可发生离子反应,其
2
中①③⑤分别生成 AgCl 沉淀、BaSO 沉淀、CaCO 沉淀,⑥生成 HO,④生成
4 3 2
CO ,⑦Zn与Cu2+发生置换反应,故①③④⑤⑥⑦都能发生离子反应,②⑧⑨不符
2
合离子反应的条件,不能发生离子反应。
【对应训练2】下列叙述中正确的是( )
A.凡是盐在离子方程式中都要以离子形式表示
B.离子互换反应总是向着溶液中反应物离子浓度减小的方向进行
C.酸碱中和反应的实质是H+与OH-结合生成水,故所有的酸碱中和反应的离子方
程式都可写成H++OH-===H O的形式
2
D.复分解反应必须同时具备离子反应发生的三个条件才能进行
【答案】B
【解析】只有可溶性盐在离子方程式中才可以写成离子形式;离子反应的实质是离
子的浓度或数目减小;H++OH-===H O表示的是可溶性强酸与可溶性强碱反应生
2
成水和可溶性盐的一类反应;复分解反应只要满足三个条件之一即可发生。
【过渡】离子方程式是高中化学的重要概念,从这节课开始,同学们需要从离子的
角度来理解溶液中电解质的反应,将初中学习的反应用离子方程式并从离子的角度理解反应的本质。那么如何书写离子方程式呢?
【问题1】思考交流:阅读教材P18页内容,结合离子反应的实质回答离子方程式
通过问
题,引
的定义及意义是什么?
发思
【学生1】①定义:用实际参加反应的离子符合表示离子反应的式子叫做离子方程 考,根
据学生
式。
的最近
【交流2】②意义:离子方程式不仅可以表示某个具体的化学反应,还可以表示某 发展区
实现知
一类型的离子反应。如离子反应H++OH-===HO就可表示强酸与强碱生成可溶性盐
2 识的层
的反应。而并不是只表示某个具体的酸和碱的中和反应。 层递
进。
【问题2】讨论交流:阅读教材P18页第三自然段,思考书写离子方程式有哪些步
骤?并举例说明。
【学生1】离子方程式的书写步骤:
活
环
【板书1】第一步:写—写出反应的化学方程式
动
节
三
三 【板书2】第二步:拆—把易溶于水且易电离的物质(如强酸、强碱和大部分可溶性
、
、
探 盐)写成离子形式,难溶的物质、气体和水等仍用化学式表示。
离 究
【板书3】第三步:删—删去方程式两边不参加反应的离子,并将方程式化为最
子 离
方 子 简。
程 方
式 程
【板书4】第四步:查—检查离子方程式两边各元素的原子个数和电荷总数是否相
式 等。
书
【教师】书写离子方程式四步中“写”是基础→“拆”是关键→“删”是途径
写
→“查”是保证”。在“拆”关键一步中,要把易溶于水、易电离的物质拆成离子
的形式。
【教师】离子方程式书写要求按“写—拆—删—查”四步进行, 但一般不需要用上
通过对
述步骤书写,而是要抓住离子反应的实质,根据实验现象,直接书写出离子反应方
预设问
程式。如:CuSO 溶液与Ba(OH) 溶液反应的离子方程式书写步骤: 题的拓
4 2
展探
【副板书】第一步:首先分析溶液中的离子有:Cu2+、SO
4
2-、Ba2+、OH-;
究,
【副板书】第二步:然后分析哪些离子相互结合,Cu2+与OH-反应生成难溶的 突出教
学的重
Cu(OH) ,SO 2-与Ba2+反应生成难溶的BaSO;
2 4 4 点,突
【副板书】第三步:根据离子的个数比配平方程式:Cu2++SO 2-+Ba2++2OH- 破难
4
点。培
===Cu(OH) ↓+BaSO↓
2 4 养高阶
【问题3】拓展探究:在书写离子方程式时,有哪些特殊的物质需“拆”或“不 思维,
提升解
拆”?
决问题
【学生1】①常见要“拆”的酸有盐酸、硝酸、稀硫酸(三大强酸)、氢碘酸、氢 的能
力。
溴酸、高氯酸强酸(将要学习的强酸)等 ;
【学生2】②常见的碱有 NaOH、KOH、Ba(OH)2、Ca(OH)2(澄清)等强碱;
【学生3】③常见的盐有钾盐、钠盐、铵盐、硝酸盐等可溶性盐。
【学生4】④微溶物作为反应物,若是澄清溶液写离子符号,若是悬浊液写化学
式。微溶物作为生成物,一般写化学式(标“↓”),如石灰水和石灰乳:石灰水写成离子形式,而石灰乳则写化学式。
【学生5】⑤氨水作反应物可写作NH 3 ·H 2 O;作生成物,若有加热条件或浓度很大 分析学
情,及
时,可写作NH (标“↑”)。
3
时评
【学生6】⑥多元弱酸的酸式酸根离子,在离子方程式中不能拆开写,如NaHCO 与 价,调
3
控课
盐酸反应的离子方程式为HCO -+H+===CO ↑+HO。
3 2 2 堂,巩
【学生7】⑦单质、气体、氧化物、难溶物、难电离物(弱酸、弱碱、水等)不能 固所
学。
拆。同时,既不是水溶液中反应也不是熔融状态下反应,不能写离子方程式。
【对应训练1】下列指定溶液之间的反应不能用离子方程式SO 2-+Ba2+=BaSO ↓表示
4 4
的是( )
A.NaSO 与Ba(OH) B.MgSO 与BaCl
2 4 2 4 2
C.HSO 与Ba(OH) D.HSO 与Ba(NO )
2 4 2 2 4 3 2
【答案】C
【解析】NaSO 与 Ba(OH) 反应生成硫酸钡和氢氧化钠溶液,可用 SO 2-
2 4 2 4
+Ba2+=BaSO ↓表示,A不符合;MgSO 与BaCl 反应生成硫酸钡和氯化镁,可用
4 4 2
SO 2-+Ba2+=BaSO4↓表示,B不符合;HSO 与Ba(OH) 反应生成硫酸钡和水,不可
4 2 4 2
用SO 2-+Ba2+=BaSO ↓表示,C符合; HSO 与Ba(NO ) 反应生成硫酸钡和硝酸,可
4 4 2 4 3 2
用SO 2-+Ba2+=BaSO ↓表示,D不符合;答案选C。
4 4
【对应训练2】下列反应的离子方程式书写正确的是( )
A.氧化铜与稀硫酸反应:CuO+4H++SO2-=Cu2++SO↑+2H O
4 2 2
B.二氧化碳通入足量澄清石灰水中:Ca2++2OH-+CO2=CaCO ↓+H O
3 2
C.铁和盐酸反应:2Fe+6H+=2Fe3++3H ↑
2
D.氢氧化钡溶液与硫酸反应:OH-+H+=H O
2
【答案】B
【解析】氧化铜与稀硫酸反应生成硫酸铜和水,不会生成SO ,正确的离子方程式
2
为: CuO+2H+=Cu2+ +H O,A错误;二氧化碳通入足量澄清石灰水中,澄清石灰水
2
过量,生成白色沉淀,故离子方程式为:Ca2++2OH-+CO =CaCO ↓+H O,B正确;
2 3 2
铁和盐酸反应生成氯化亚铁而不是氯化铁,正确的离子方程式为: Fe+2H+=Fe2+
+H2↑,C错误;氢氧化钡溶液与硫酸反应生成硫酸钡是沉淀不能拆,正确的离子方
程式为:2OH-+2H++Ba2++ SO 2-=2H O+BaSO↓,D错误;故答案为:B。
4 2 4
【过渡】离子方程式满足原子个数守恒(质量守恒)和电荷守恒。初中我们已学习
过原子个数守恒,而电荷守恒判断的方法应该是将方程式左右两边的离子所带的电
荷分别相加(注意正负和系数),左右两边的总电荷应该分别相等。那么,离子方
程式除了必须满足两个守恒外,还有哪些要求呢?
【问题1】结合教材P19页“思考与讨论”,根据离子方程式的书写步骤,请同学
们交流讨论,并填写下表。
【学生】完成下表内容,并在全班交流。
【投影】
反应物 化学方程式 离子方程式 两种方程式的不同 利用具
体物质
** 错误的表 AgNO + NaCl = AgCl↓ + Ag+ + Cl- = AgCl↓ ⑥⑦⑧⑨四个反
3 之间的
达式 **AgNO NaNO 3 应的化学方程式 反应,
3 +NaCl 是不同的,但离 引发认
子方程式是完全
知冲
活 ** 错误的表 AgNO 3 + HCl = AgCl↓ + Ag+ + Cl- = AgCl↓ 相同的:四个反 突,发
达式 **AgNO HNO 3 应是不同的强酸 现问
+HCl 强碱之间的中和
3 题,总
反应,其对应的
结规
** 错误的表 Ba(OH) 2 + H 2 SO 4 = Ba2+ + 2OH- + 2H+ 离子方程式都是
律、探
达式 **Ba(O BaSO 4 ↓ + 2H 2 O + SO 4 2- = BaSO 4 ↓ + H+ + OH- =
寻方
H) 2 +H 2 SO 4 2H 2 O H 2 O。所以这说 法。
明化学方程式表
示是一个具体的
反应,而离子方
** 错误的表 CaCO + 2HCl = CaCl + CaCO + 2H+ =
3 2 3
程式还可以表示
达式 **CaCO 3 H 2 O + CO 2 ↑ Ca2+ + H 2 O + 一类反应。
+ HCl CO 2 ↑
⑤NaHCO +H 2NaHCO +H SO = NaSO HCO - + H+ = HO
3 2 3 2 4 2 4 3 2
SO + 2H O + 2CO ↑ + CO↑
动 4 2 2 2
活
** 错误的表 HCl + NaOH = NaCl + H O H+ + OH- = H O
2 2
动
达式 **HCl +
二 NaOH
、 ⑦HCl + KOH HCl + KOH = KCl + H O H+ + OH- = H O
2 2
探
⑧HSO + HSO + 2NaOH = Na SO H+ + OH- = H O
2 4 2 4 2 4 2
究 NaOH + 2H O
2
离
子 ⑨H SO + HSO + 2KOH = K SO + H+ + OH- = H O
2 4 2 4 2 4 2
KOH 2HO 通过归
方 2
纳和提
程 炼,形
【追问】通过上述的改写过程,在书写离子方程式的过程中注意哪些问题? 成对所
式
学知识
【学生1】①有的离子方程式可能出现某一侧所有物质均不能拆分的情况,例如**
正 规律性
错误的表达式 **中所有生成物均不能拆分。
认识。
误
【学生2】②一定要将方程式的系数化到最简,例如⑤⑧⑨。
的
【问题2】讨论交流:结合离子方程式的书写方法,思考如何判断离子方程式的正
通过讨
判
误? 论交
断 流,形
【学生1】①一看是否符合客观事实。如铁与稀硫酸反应生成Fe2+而不生成Fe3+。
成科学
【学生2】②二看物质的拆写是否正确。 方法。
有效突
【学生 3】③三看电荷是否守恒。如 FeCl 2 溶液与 Cl 2 反应,不能写成 Fe2++ 破教学
Cl===Fe3++2Cl-,而应写成2Fe2++Cl===2Fe3++2Cl-。 难点。
2 2
【学生4】④四看是否漏写离子反应。如Ba(OH) 溶液与CuSO 溶液反应,既要写
2 4
Ba2+与SO反应生成 BaSO 沉淀的离子反应,又不能漏写 Cu2+与OH-反应生成
4
Cu(OH) 沉淀的离子反应。
2
【学生5】⑤五看反应物或产物的配比是否正确。如稀硫酸与Ba(OH) 溶液反应不能
2写成H++OH-+SO+Ba2+===BaSO ↓+HO,而应写成2H++2OH-+SO+Ba2+
4 2
===BaSO ↓+2HO。
4 2
【学生6】♦⑥当多元弱酸与碱反应,若酸过量,生成酸式盐,反之,生成正盐。
如石灰水通入过量 CO ,生成可溶性 Ca(HCO ) ,离子方程式应为 OH-+
2 3 2
CO===HCO。
2
【对应训练1】判断下列离子方程式是否正确并说明理由:
分析学
(1)铁与稀盐酸反应:2Fe + 6H+ = 2Fe3++ 3H ↑(错误,违背客观事实,铁与稀盐
2 情,及
酸反应只能生成Fe2+。)
时评
(2)铝与稀盐酸反应:Al + 3H+ = Al3+ + H ↑(错误,原子个数不守恒) 价,调
2
控课
(3)澄清石灰水与盐酸反应:Ca(OH) 2 +2H+===2H 2 O+Ca2+ (错误,物质拆分不 堂,巩
正确,澄清石灰水属于强碱溶液要拆) 固所
学。
(4)硫酸和Ba(OH) 溶液反应:Ba2+ + OH-+ H+ + SO 2-= BaSO↓ + H O(错误,物
2 4 4 2
质比例不符合客观事实)
(5)碳酸钡和稀硝酸反应:CO2-+2H+ = H O+CO↑(错误,物质拆分不正确,碳酸
3 2 2
钡难溶不能拆)
【对应训练2】下列离子方程式正确的是( )
A.石灰石与盐酸反应:CO+2H+===CO ↑+HO
2 2
B.铜和硝酸银溶液反应:Cu+Ag+===Cu2++Ag
C.向Ba(OH) 溶液中逐滴滴加NaHSO 溶液至SO恰好沉淀完全:Ba2++2OH-+
2 4
2H++SO===BaSO ↓+2HO
4 2
D.NH HCO 溶液与过量稀盐酸混合:HCO+H+===CO ↑+HO
4 3 2 2
【答案】D
【解析】石灰石难溶于水,不能拆成离子形式,A不正确;该离子方程式没有配
平,电荷不守恒,B不正确;根据题意可知NaHSO 是少量的,则沉淀1个SO只要
4
1个Ba2+,同时中和1个H+只要1个OH-,故向Ba(OH) 溶液中滴加NaHSO 溶液
2 4
至SO恰好沉淀完全的离子方程式为 Ba2++OH-+H++SO===BaSO ↓+HO,C不
4 2
正确;NH HCO 溶液与过量稀盐酸反应的离子方程式为HCO+H+===CO ↑+HO,
4 3 2 2
D正确。
【作业】1.(中)教材作业:P20-21页练习3、6、7、8
2.(易)下列物质混合后,不会发生离子反应的是( )
A.NaOH溶液和FeCl 溶液 B.NaCO 溶液和稀硫酸
3 2 3
C.NaSO 溶液和MgCl 溶液 D.澄清的石灰水和盐酸
2 4 2
【答案】C
【解析】根据离子反应发生的条件,可判断C中没有发生反应。
环
3.(易)下列反应属于离子反应的是( )
节
四 A.HO和CO 气体的反应 B.NH 溶于水的反应
2 2 3
、
作 C.硝酸与Ca(OH) 溶液的反应 D.H 在O 中燃烧
课 2 2 2
业
后 【答案】C
设巩 计 【解析】离子反应是有离子参加的反应。A.HO+CO=H CO 不属于离子反
2 2 2 3
固 应,A不符合题意B.NH +H O=NH ·H O不属于离子反应,B不符合题意;C.
3 2 3 2
Ca(OH) +2HNO =Ca(NO)+2H O,参与反应的是氢离子和氢氧根离子:H++OH-
2 3 3 2 2
=H O,属于离子反应,C符合题意;D.2H+O 2HO不属于离子反应,D不
2 2 2 2
符合题意;所以答案选C。
4.(中)下列符合离子方程式Ba2++SO===BaSO ↓的化学反应是(均指溶液间)
4
( )
A. HSO 和Ba(OH) 混合 B.HSO 与BaCl 混合
2 4 2 2 4 2
及时巩
C.Ba(OH) 与NaSO 混合 D.Ba(OH) 与NaHSO 混合
2 2 4 2 4
固、消
【答案】BC 化所
学,促
【解析】A应写成:2H++SO+Ba2++2OH-===BaSO ↓+2HO。D项,若
4 2 进掌握
NaHSO 不足, 可以写成:Ba2++OH-+H++SO===BaSO ↓+HO;若NaHSO 过 必备知
4 4 2 4
识,评
量,可以写成:Ba2++2OH-+2H++SO===BaSO ↓+2HO。
4 2 价教学
5.(中)下列反应的离子方程式书写正确的是( ) 效果,
为后期
A.稀硫酸滴在铜片上:Cu+2H+===Cu2++H 2 ↑ 优化教
学方案
B.稀硫酸与氢氧化钡溶液混合:SO+Ba2+===BaSO ↓
4 提供依
C.稀硝酸滴在大理石上:CaCO +2H+===Ca2++HCO 据,培
3 2 3
养分析
D.氧化铁与稀盐酸混合:Fe O+6H+===2Fe3++3HO
2 3 2 问题和
【答案】D 解决问
题等关
【解析】选项A中铜与稀硫酸不反应;选项B中H+与OH-参加反应生成水;选
键能
力。
项C中反应生成的碳酸不稳定,可分解成二氧化碳和水。
6.(中)下列反应的离子方程式中,正确的是( )
A.氢氧化钡溶液和稀硫酸Ba2++OH-+H++SO2-==BaSO↓+2H O
4 4 2
B.氯化铁溶液中加铁粉 Fe3+ + Fe == 2Fe2+
C.少量CO 通入NaOH溶液中 CO + 2OH-== CO2- + H O
2 2 3 2
D.澄清石灰水与稀盐酸反应Ca(OH) +2H+== Ca2++2H O
2 2
【答案】C
7.(难)下列反应的离子方程式书写正确的是( )
A.向NaHSO 溶液中滴入Ba(OH) :H++OH-=H O
4 2 2
B.碳酸钙溶于醋酸:CaCO +2H+=Ca2++H O+CO↑
3 2 2
C.NaOH溶液与少量CO 反应的离子方程式:OH-+CO =H O+CO2-
2 2 2 3
D.碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀:
HCO -+Ca2++OH-=CaCO ↓+H O
3 3 2
【答案】C
【解析】A.向NaHSO 溶液中滴入Ba(OH) ,还生成硫酸钡沉淀,则Ba(OH)
4 2 2
少量时离子方程式为:2H++SO2-+Ba2++2OH-=BaSO ↓+2H O,过量时的离子方程式
4 4 2
为:H++SO2-+Ba2++OH-=BaSO ↓+H O,故A错误;B.碳酸钙溶于醋酸,离子方程
4 4 2
式为:CaCO +2CH COOH=Ca2++H O+CO↑+2CH COO-,故B错误;C.NaOH过量
3 3 2 2 3
时生成NaCO,离子方程式为:2OH-+CO =H O+CO2-;NaOH少量时生成
2 3 2 2 3NaHCO ,离子方程式为:OH-+CO =HCO -,故C错误;D.碳酸氢钠溶液与少量澄
3 2 3
清石灰水混合出现白色沉淀,离子方程式为:2HCO +Ca2++2OH-═CO2-
3
+CaCO ↓+H O,故D错误;故选C。
3 2
8.(难)♦向Ba(OH) 溶液中逐滴加入稀硫酸,请完成下列问题:
2
(1) 写 出 反 应 的 离 子 方 程 式 :
____________________________________________。
(2)下列三种情况下,离子方程式与(1)相同的是______(填字母)。
A.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至溶液显中性
4 2
B.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至SO恰好完全沉淀
4 2
C.向NaHSO 溶液中,逐滴加入Ba(OH) 溶液至过量
4 2
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I
表示)可近似用上图中的________曲线表示(填字母)。
(4)若向装有Ba(OH) 溶液的烧杯里缓缓滴入KAl(SO ) 溶液至Ba2+恰好完全反
2 4 2
应。则反应的离子方程式是__________________________________________。
【答案】(1)Ba2++2OH-+SO+2H+===BaSO ↓+2HO (2)A
4 2
(3)C (4)2Ba2++4OH-+Al3++2SO===2BaSO ↓+AlO+2HO
4 2
【解析】(1)Ba(OH) 溶液中逐滴加入稀硫酸生成水和硫酸钡沉淀,离子反应为
2
Ba2++2OH-+2H++SO===BaSO ↓+2HO。
4 2
(2)A的离子反应是Ba2++2OH-+2H++SO===BaSO ↓+2HO,B、C的离子反
4 2
应是Ba2++OH-+H++SO===BaSO ↓+HO,选A。
4 2
(3)随着HSO 的加入至二者刚好反应时,溶液的导电能力逐渐减弱至不导电,
2 4
随后硫酸过量,溶液的导电能力逐渐增强,选C。
(4)若向装有Ba(OH) 溶液的烧杯里缓缓滴入KAl(SO ) 溶液至Ba2+恰好完全反
2 4 2
应,此时二者物质的量比为2∶1,则OH-与Al3+的物质的量比为4∶1,Al3+全部变为
AlO,即:2Ba2++4OH-+Al3++2SO===2BaSO ↓+AlO+2HO。
4 2
第二节 离子反应
第二课时 离子反应及离子方程式
一、离子反应
1、离子反应的实质:离子之间的反应,即有离子参加或有离子生成的化学反应。
2、离子反应发生的条件:生成难溶于水的物质、放出气体或生成水(复分解反应)。
板书
二、离子方程式书写及正误判断
设计
1、离子方程式书写步骤:“写”是基础→“拆”是关键→“删”是途径→“查”是保
证”
2、离子方程式正误的判断:
“五看”、“一特殊“
本节课通过历史故事引入新课,更易激发学生思考和探究欲望,利用简单实验的现象观
察、原理分析自然形成理论,得出离子反应的概念后,立即利用所学理论去解决实际问题,从
而进一步理解概念,遵循由感性到实践的认知规律,同时也有利用帮助学生明确理论对实践的指导作用。在探究了离子反应的本质的基础上,再通过不同电解质溶液反应可以生成沉淀、气
体、难电离物的三种情况,学生就可以自主归纳出酸、碱、盐等电解质在溶液中发生复分解反
应的离子反应条件就是复分解反应的条件的结论。在此基础上提出“如何简单表示离子反应”
的问题引出离子反应方程式的概念及书写方法。最后,为了分散本节内容的难点,本节课还安
排了离子方程式正误的判断,这也是高考的考点之一,但要注意由于知识的局限性,切不可面
面俱到,重点强调遵循两个“守恒”和复分解反应的离子反应即可。整体来看,本节可的设计
学生主动参与、探究发现的学习方式在课堂上得到了充分体现,充分发挥了教师的主导作用和
教学 学生的主体作用,学生的认知过程和学习过程实现了有机统一,满足了学生的需要和接受水
平,有效强化了重点、突破了难点,较高效地达成了教学目标。
反思