文档内容
1.3.2 氧化还原反应规律及配平
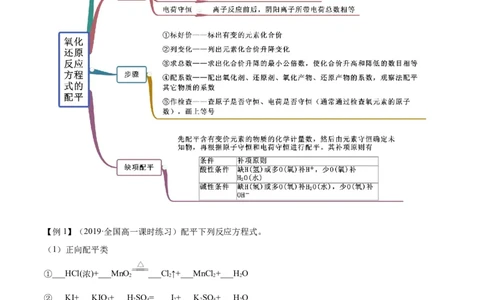
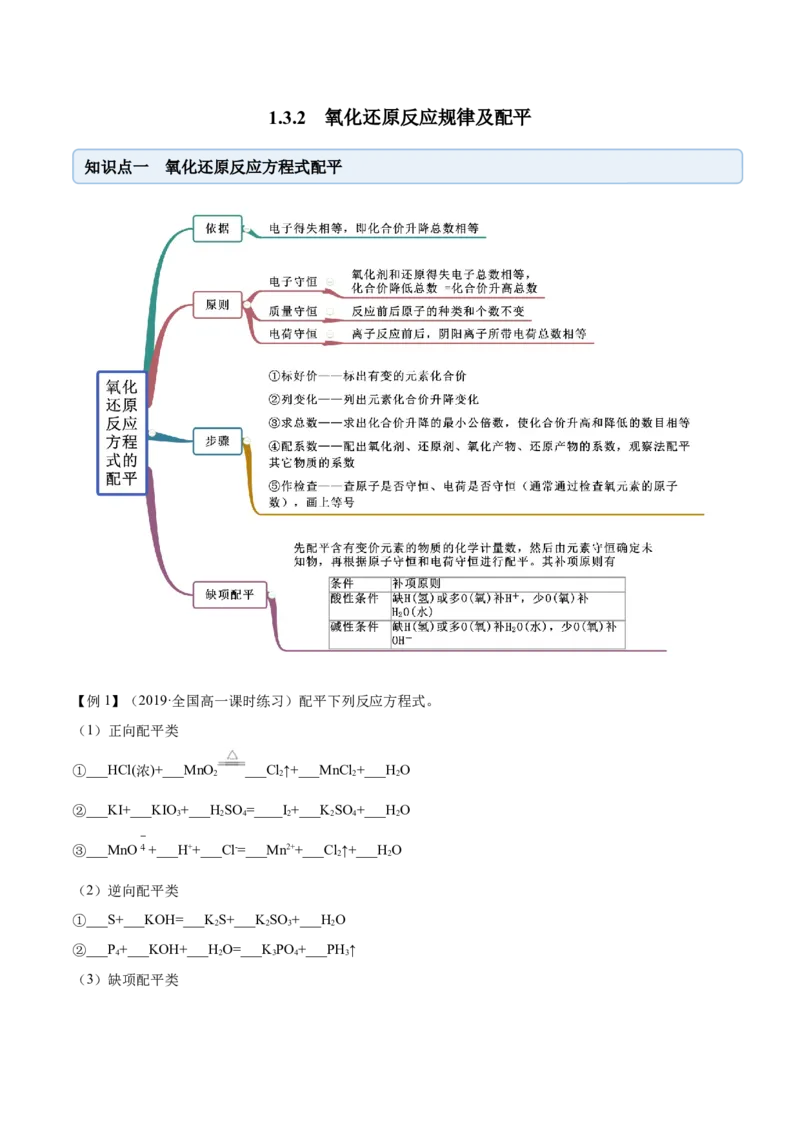
知识点一 氧化还原反应方程式配平
【例1】(2019·全国高一课时练习)配平下列反应方程式。
(1)正向配平类
①___HCl(浓)+___MnO ___Cl↑+___MnCl +___H O
2 2 2 2
②___KI+___KIO +___H SO =____I +___K SO +___H O
3 2 4 2 2 4 2
③___MnO +___H++___Cl-=___Mn2++___Cl↑+___H O
2 2
(2)逆向配平类
①___S+___KOH=___K S+___KSO +___H O
2 2 3 2
②___P+___KOH+___H O=___KPO +___PH↑
4 2 3 4 3
(3)缺项配平类①___ClO-+___Fe(OH) +___=___Cl-+___FeO +___H O
3 2
②___MnO +___H O+___=___Mn2++___O ↑+___H O
2 2 2 2
③某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al O、C、N、AlN、CO。请将反应
2 3 2
物与生成物分别填入以下空格内,并配平。___
+ + → +
【答案】(1)①4 1 1 1 2 ②5 1 3 3 3 3
③2 16 10 2 5 8
(2)①3 6 2 1 3 ②2 9 3 3 5
(3)①3 2 4OH- 3 2 5
②2 5 6H+ 2 5 8 A
③lO+3C+N =2AlN+3CO
2 3 2
【解析】(1)①浓盐酸中Cl元素的化合价从-1价失电子升高到0价,MnO 中Mn元素的化合价从+4价得
2
电子降低到+2价,由电子守恒和原子守恒可知方程式为4HCl(浓)+MnO Cl↑+ MnCl +2H O;答案为4,
2 2 2 2
1,1,1,2。
②KI中I元素的化合价从-1价失电子升高到0价,KIO 中I元素的化合价从+5价得电子降低到0价,由电
3
子守恒和原子守恒可知方程式为5KI+KIO +3H SO =3I +3K SO +3H O;答案为5,1,3,3,3,3。
3 2 4 2 2 4 2
③MnO -中Mn元素的化合价从+7价得电子降低到+2价,Cl-中Cl元素的化合价从-1价失电子升高到0价,
4
由电子守恒和原子守恒可知方程式为2MnO -+16H++10Cl-=2Mn2++5Cl↑+8H O;答案为2,16,10,2,5,
4 2 2
8。
(2)①S中部分S元素的化合价从0价失电子升高到+4价,S中部分S元素的化合价从0价得电子降低
到-2价,由电子守恒和原子守恒可知方程式为3S+6KOH=2K S+KSO +3H O;答案为3,6,2,1,3.
2 2 3 2
②P 中部分P元素的化合价从0价失电子升高到+5价,P 中部分P元素的化合价从0价得电子降低到-3价,
4 4
由电子守恒和原子守恒可知方程式为2P+9KOH+3H O=3KPO +5PH↑;答案为2,9,3,3,5.
4 2 3 4 3
(3)①ClO-中Cl元素的化合价从+1价得电子降低到-1价,Fe(OH) 中Fe元素的化合价从+3价失电子升高
3
到+6价,由电子守恒和原子守恒可知方程式为 3ClO-+2Fe(OH) + 4OH-=3Cl-+2FeO 2-+5H O;答案为3,2,
3 4 2
4OH-,3,2,5.
②MnO -中Mn元素的化合价从+7价得电子降低到+2价,HO 中O元素的化合价从-1价失电子升高到0价,
4 2 2
由电子守恒和原子守恒可知方程式为2MnO -+5H O+6H+=2Mn2++5O ↑+8H O;答案为2,5,6H+,2,5,8.
4 2 2 2 2③A1 O 是反应物,反应中A1 O→AlN,Al元素化合价不变化,根据氮元素守恒N 是反应物,反应中
2 3 2 3 2
N→AlN,N元素的化合价降低,根据电子转移守恒可知C是反应物,CO是生成物,反应中N→AlN,N
2 2
元素的化合价由0价降低为-3价,共降低6价,C→CO,C元素化合价由0价升高为+2价,共升高2价,
化合价升降最小公倍数为6,故N 系数为1,C系数为3,根据N元素守恒可知AlN系数为2,根据Al元
2
素守恒可知Al O 系数为1,根据C元素守恒可知CO系数为3,所以其化学反应方程式为
2 3
Al O+3C+N =2AlN+3CO;答案为Al O+3C+N =2AlN+3CO。
2 3 2 2 3 2
【一隅三反】
1.(2019·全国高一课时练习)配平下列反应的化学方程式。
(1)________ ________ ________ ________ ________
(2)________ ________ ________ ________ ________
(3)________ ________ ________ ________
【答案】(1)3 8 3 2 4 (2)1 4 1 2 2 (3)2 2 2 1
【解析】(1)该反应中元素的化合价变化如下:Cu→Cu(NO ),Cu元素的化合价由0价→+2价,一个Cu
3 2
失去2个电子; HNO→NO,N元素的化合价由+5价→+2价,一个HNO 得到3个电子,所以得失电子的
3 3
最小公倍数为6,所以Cu的计量数为3,Cu(NO ) 的计量数为3,NO的计量数为2,由于硝酸部分被还原,
3 2
根据原子守恒,HNO 的计量数为8,HO计量数为4,故答案为:3;8;3;2;4;
3 2
(2)该反应中元素的化合价变化如下:Cu→Cu(NO ),Cu元素的化合价由0价→+2价,一个Cu失去2
3 2
个电子; HNO→NO ,N元素的化合价由+5价→+4价,一个HNO 得到1个电子,所以得失电子的最小
3 2 3
公倍数为2,所以Cu的计量数为1,Cu(NO ) 的计量数为1,NO 的计量数为2,由于硝酸部分被还原,根
3 2 2
据原子守恒,HNO 的计量数为4,HO计量数为2,故答案为:1;4;1;2;2;
3 2
(3)该反应中元素的化合价变化如下:HO→H ,H元素的化合价由+1价→0价,生成一个H 得到2个电
2 2 2
子;
Na→NaOH,Na元素的化合价由0价→+1价,一个Na失去1个电子;
所以得失电子的最小公倍数为2,所以Na的计量数为2,NaOH的计量数为2,HO计量数为2,H 的计量
2 2
数为1;故答案为:2;2;2;1。
2.(2019·广东中山纪念中学高一月考)(1)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的
含量,配平以下离子方程式,并填上合适的微粒:___H++___MnO +___H C O =___CO ↑+___Mn2+
2 2 4 2
+______(2)请将5种物质NO、FeSO 、Fe(NO )、HNO 和Fe (SO ) 分别填入下面对应的横线上,组成一个未配平
2 4 3 3 3 2 4 3
的化学方程式。①________+________→________+________+__________+HO
2
【答案】(1)6 2 5 10 2 8
(2)FeSO HNO Fe(NO ) Fe (SO ) N O
4 3 3 3 2 4 3 2
【解析】(1)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,高锰酸根降低变为锰离子,
化合价降低5个,草酸化合价升高,1个草酸升高2个价态,根据化合价升降相等,得到高锰酸根配2,草
酸配5,根据元素守恒得到锰离子配2,二氧化碳配10,根据元素守恒,氢和氧结合变为水,再根据氧守
恒,水配8,氢守恒氢离子配6,最终得到离子方程式:6H++2MnO +5H C O =10CO ↑+2Mn2++8 H O;故
2 2 4 2 2
答案为:6;2;5;10;2;8HO。
2
(2)①HO是生成物,根据氢守恒,反应物为HNO,硝酸是氧化剂,则还原剂为FeSO ,氧化产物为
2 3 4
Fe(NO )、Fe (SO ),还原产物为NO,因此组成一个未配平的化学方程式为
3 3 2 4 3 2
FeSO +HNO→Fe(NO )+Fe (SO )+NO+HO;故答案为:FeSO ;HNO;Fe(NO );Fe (SO );NO。
4 3 3 3 2 4 3 2 2 4 3 3 3 2 4 3 2
3.(2020·全国课时练习)某同学做实验时不小心沾了一些 使皮肤上形成黑斑,这些黑斑很久才
能消失,如果用草酸的稀溶液洗涤马上可以消失,涉及的反应的离子方程式为
__________(未配平)。下列关于此反应的叙述正确的是( )
A.该反应的氧化产物是 B.1个 在反应中失去5个电子
C.横线上应是 D.配平该离子方程式后, 的化学计量数是6
【答案】D
【解析】A.该反应中, 得电子作氧化剂,则 为还原产物,A 不正确;
B.Mn元素由+7价降为+2价,则1个 在反应中得到5个电子,B不正确;
C.离子方程式左边有 ,则右边不能出现OH-,横线上应是 ,C不正确;
D.由分析知,配平该离子方程式后, 的化学计量数是6,D正确;故选D。知识点二 氧化还原反应的实际运用
【例2】(2020·长葛市第一高级中学月考)厨房中的化学知识很多,下面是有关厨房中的常见操作或者常
见现象,其中不属于氧化还原反应的是( )
A.烧菜用过的铁锅,经放置常出现红棕色斑迹
B.用煤气灶燃烧沼气(主要成分为甲烷:CH)为炒菜提供热量
4
C.牛奶久置变质腐败
D.用醋酸除去水垢[主要成分是CaCO 、Mg (OH) ]
3 2
【答案】D
【解析】A.Fe被氧化生成铁锈,发生氧化还原反应,故A不选;
B.CH 燃烧生成二氧化碳和水,C、O元素的化合价发生变化,属于氧化还原反应,故B不选;
4
C.牛奶久置变质腐败,被空气中的氧气氧化,元素的化合价发生变化,属于氧化还原反应,故C不选;
D.用醋酸除去水垢,属于复分解反应,不属于氧化还原反应,故D选;
答案选D。
【一隅三反】
1.(2020·湖北黄冈)下列文献记载内容不涉及氧化还原反应的是
A.明代宋应星所著的《天工开物》中记载的火法炼锌工艺
B.西汉刘安组织编撰的《淮南万毕术》中记载的“曾青得铁则铁化为铜”
C.葛洪《肘后备急方》记载的“青蒿一握,以水二升渍,绞取汁”
D.《己亥杂诗》中记载“落红不是无情物,化作春泥更护花”
【答案】C
【解析】A.火法炼锌是使锌的化合物变为单质,有元素化合价的变化,属于氧化还原反应,A不符合题
意;
B.曾青得铁则铁化为铜表示的是CuSO 与Fe发生置换反应产生Cu和FeSO ,反应过程中有元素化合价的
4 4
变化,属于氧化还原反应,B不符合题意;
C.青蒿一握,以水二升渍,绞取汁表示的是物质的粉碎、溶解、过滤过程,没有新物质产生,发生的是
物理变化,C符合题意;
D.落红不是无情物,化作春泥更护花表示了物质的腐烂、分解等过程,有新物质生成,有元素化合价的
变化,属于氧化还原反应,D不符合题意;
故答案为C。
2(2020·长葛市第一高级中学月考)厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,
其中不属于氧化还原反应的是( )A.烧菜用过的铁锅,经放置常出现红棕色斑迹
B.用煤气灶燃烧沼气(主要成分为甲烷:CH)为炒菜提供热量
4
C.牛奶久置变质腐败
D.用醋酸除去水垢[主要成分是CaCO 、Mg (OH) ]
3 2
【答案】D
【解析】A.Fe被氧化生成铁锈,发生氧化还原反应,故A不选;
B.CH 燃烧生成二氧化碳和水,C、O元素的化合价发生变化,属于氧化还原反应,故B不选;
4
C.牛奶久置变质腐败,被空气中的氧气氧化,元素的化合价发生变化,属于氧化还原反应,故C不选;
D.用醋酸除去水垢,属于复分解反应,不属于氧化还原反应,故D选;
答案选D。
3.(2020·全国高一单元测试)金属加工后的废切削液中含有2%~5%的NaNO ,它是一种环境污染物。
2
人们用NH Cl溶液来处理此废切削液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
4
第一步:NaNO +NHCl=NaCl+NH NO
2 4 4 2
第二步:NH NO N↑+2H O
4 2 2 2
下列对第二步反应的叙述中正确的是
①NH NO 仅是氧化剂
4 2
②NH NO 仅是还原剂
4 2
③NH NO 发生了分解反应
4 2
④只有氮元素的化合价发生了变化
⑤NH NO 既是氧化剂又是还原剂
4 2
A.①③ B.①④
C.②③④ D.③④⑤
【答案】D
【解析】第二步反应中NH NO 发生了自身的氧化还原反应,其中氮元素发生了归中反应,NH NO 中的两
4 2 4 2
个N原子的化合价分别由-3价变为0价、由+3价变为0价,该反应中只有N元素的化合价发生变化,所以
NH NO 既是氧化剂又是还原剂,从四大基本反应类型看,NH NO 发生的是分解反应,所以③④⑤是正确
4 2 4 2
的。故选D。