文档内容
2.1.2 活化能(学案)
1.了解碰撞理论。
2.了解活化能的概念和应用,理解化学反应速率与活化分子的关系。
1.活化能的应用,化学反应速率与活化分子的关系。
催化剂影响化学反应的机理是____________________________。
一、有效碰撞理论
1.有效碰撞
2.活化分子与活化能
活化分子:能够发生________________的分子。
活化能:_______比_______高出的能量。
3.化学反应速率与活化分子、有效碰撞的关系
活化分子的百分数越大,单位体积内_____________越多,单位时间内_____________越多,化学反
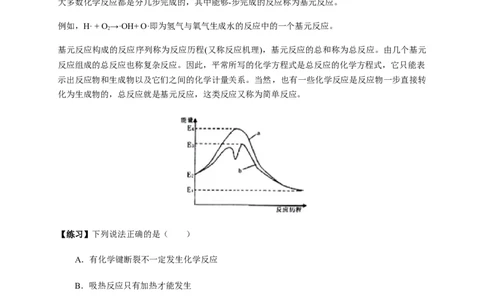
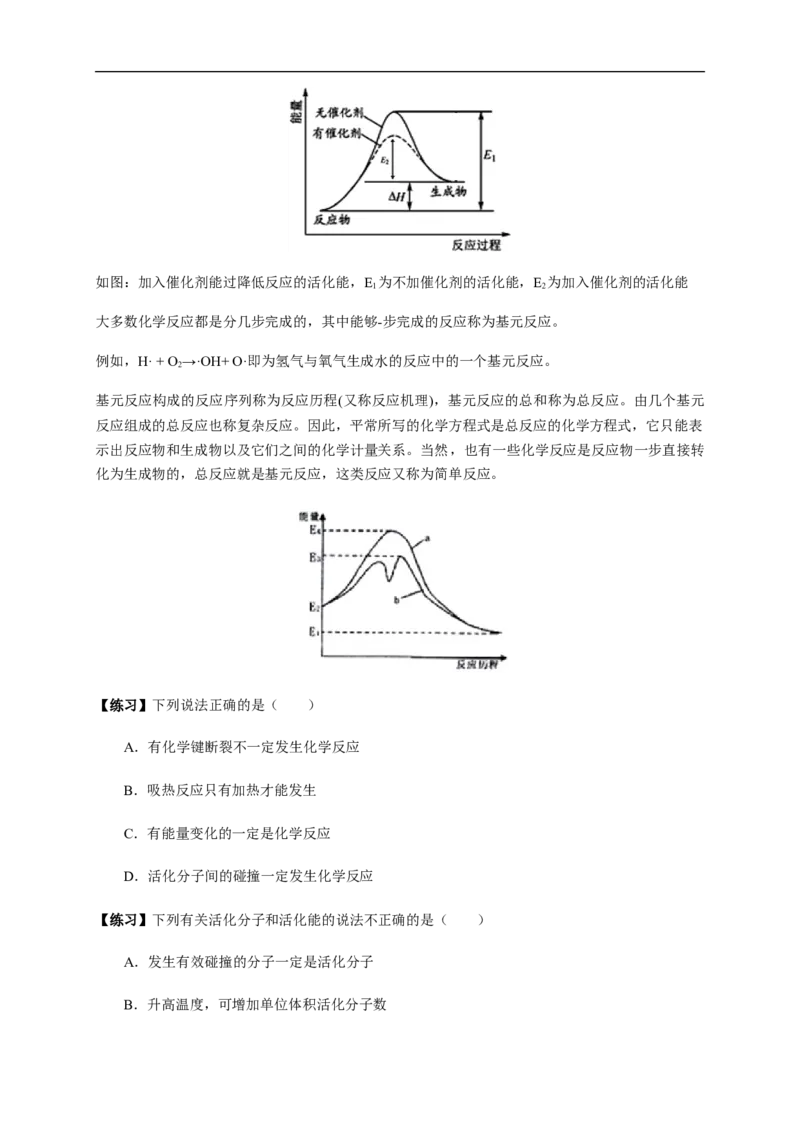
应速率_____________。如图:加入催化剂能过降低反应的活化能,E 为不加催化剂的活化能,E 为加入催化剂的活化能
1 2
大多数化学反应都是分几步完成的,其中能够-步完成的反应称为基元反应。
例如,H· + O →·OH+ O·即为氢气与氧气生成水的反应中的一个基元反应。
2
基元反应构成的反应序列称为反应历程(又称反应机理),基元反应的总和称为总反应。由几个基元
反应组成的总反应也称复杂反应。因此,平常所写的化学方程式是总反应的化学方程式,它只能表
示出反应物和生成物以及它们之间的化学计量关系。当然,也有一些化学反应是反应物一步直接转
化为生成物的,总反应就是基元反应,这类反应又称为简单反应。
【练习】下列说法正确的是( )
A.有化学键断裂不一定发生化学反应
B.吸热反应只有加热才能发生
C.有能量变化的一定是化学反应
D.活化分子间的碰撞一定发生化学反应
【练习】下列有关活化分子和活化能的说法不正确的是( )
A.发生有效碰撞的分子一定是活化分子
B.升高温度,可增加单位体积活化分子数C.增加气体反应物的浓度,可以提高单位体积活化分子百分数
D.使用催化剂可降低活化能,提高单位体积活化分子百分数
【练习】一定能增加反应物分子中活化分子的百分数的是( )
A.降低温度 B.增大压强 C.使用催化剂 D.增加浓度
【练习】A (g)+B (g)═2AB(g),△H<0,下列因素能使活化分子百分数增加的是
2 2
( )
A.降温 B.使用催化剂
C.增大反应物浓度 D.增大气体的压强
【练习】下列说法中正确的是( )
化学反应的实质是活化分子有合适取向时的有效碰撞
①
普通分子间的碰撞有时也能发生化学反应
②
活化分子比普通分子具有较高的能量
③
化学反应的实质是原子的重新组合
④
化学反应的实质是旧化学键的断裂和新化学键的形成过程
⑤
活化分子间的碰撞一定能发生化学反应.
⑥
A. B. C. D.
①③④⑤ ②③⑥ ③④⑤⑥ ②④⑤
1.下列有关有效碰撞模型说法不正确的是( )
A.能发生有效碰撞的分子一定是活化分子
B.有效碰撞是发生化学反应的充要条件
C.化学反应的活化能不可能为零
D.活化分子间的碰撞不一定是有效碰撞2.下列有关有效碰撞模型说法不正确的是( )
A.能发生有效碰撞的分子一定是活化分子
B.有效碰撞是发生化学反应的充要条件
C.不存在活化能为零的反应
D.活化分子间的碰撞不一定是有效碰撞
3.下列反应中活化能最低的是( )
A.氢气在氧气中燃烧
B.碳酸钙受热分解
C.盐酸与硝酸银溶液混合
D.草酸使酸性高锰酸钾溶液褪色
4.A (g)+B (g) 2AB(g),△H>0.下列因素能使活化分子百分数增加的是( )
2 2
⇌
A.降温 B.使用催化剂
C.增大反应物浓度 D.增大气体的压强
5.下列说法正确的是( )
A.催化剂能增大单位体积内活化分子的百分数,从而成千上万倍地增大反应速率
B.有气体参加的化学反应,缩小反应容器的容积以增大压强,可增大活化分子的百分数,从
而使反应速率增大
C.升高温度能使化学反应速率增大的主要原因是减小了反应物分子中活化分子的百分数
D.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增多
6.下列叙述正确的是( )
A.反应的活化能越小,单位时间内有效碰撞越多
B.反应的活化能越大,单位时间内有效碰撞越多C.反应的活化能越小,单位时间内有效碰撞越少
D.反应的活化能太小,单位时间内几乎无有效碰撞
【知识点填空答案】
降低活化能。
化学反应;活化分子;普通分子;活化分子数;有效碰撞的次数;越快。
【练习答案】ACCBA
【检测反馈答案】CCCBAA