文档内容
第二章 分子结构与性质
第一节 共价键
2.1.2 键参数—键能、键长与键角
1.理解键能、键长、键角等键参数的概念。
2.能应用键参数一键能、键长、键角说明简单分子的结构和性质。
教学重点:通过键参数解释物质的结构与性质
教学难点:通过键参数解释物质的结构与性质
一、键能
1.含义: 中 化学键解离成 所吸收的能量。键能的单位是
。
2.条件:键能通常是 条件下的标准值。
3.应用
①判断共价键的稳定性
从键能的定义可知,破坏 1mol 化学键所需能量越多,即共价键的键能越大,则共价键越
。
②判断分子的稳定性
一般来说,结构相似的分子中,共价键的键能越大,分子越 。如分子的稳定性:HF HCl
HBr HI。
③估算化学反应的反应热
同一化学键解离成气态原子所吸收的能量与气态原子结合形成化学键所释放的能量在数值上是相等
的 , 故 根 据 化 学 键 的 键 能 数 据 可 计 算 化 学 反 应 的 反 应 热 , 即 ΔH=
。
【学生活动】
依据表2—1,回答下列问题:
1、N、O、F 与氢气的反应能力依次增强,从键能的角度如何理解这一事实?
2 2 2
2、1mol H 分别与1mol Cl 、1mol Br (蒸气)反应,分别形成2mol HCl 和2mol HBr,哪一个反应释
2 2 2放的能量更多?如何用计算的结构说明氯化氢分子和溴化氢分子哪个更容易发生热分解生成相
应的单质?
二、键长
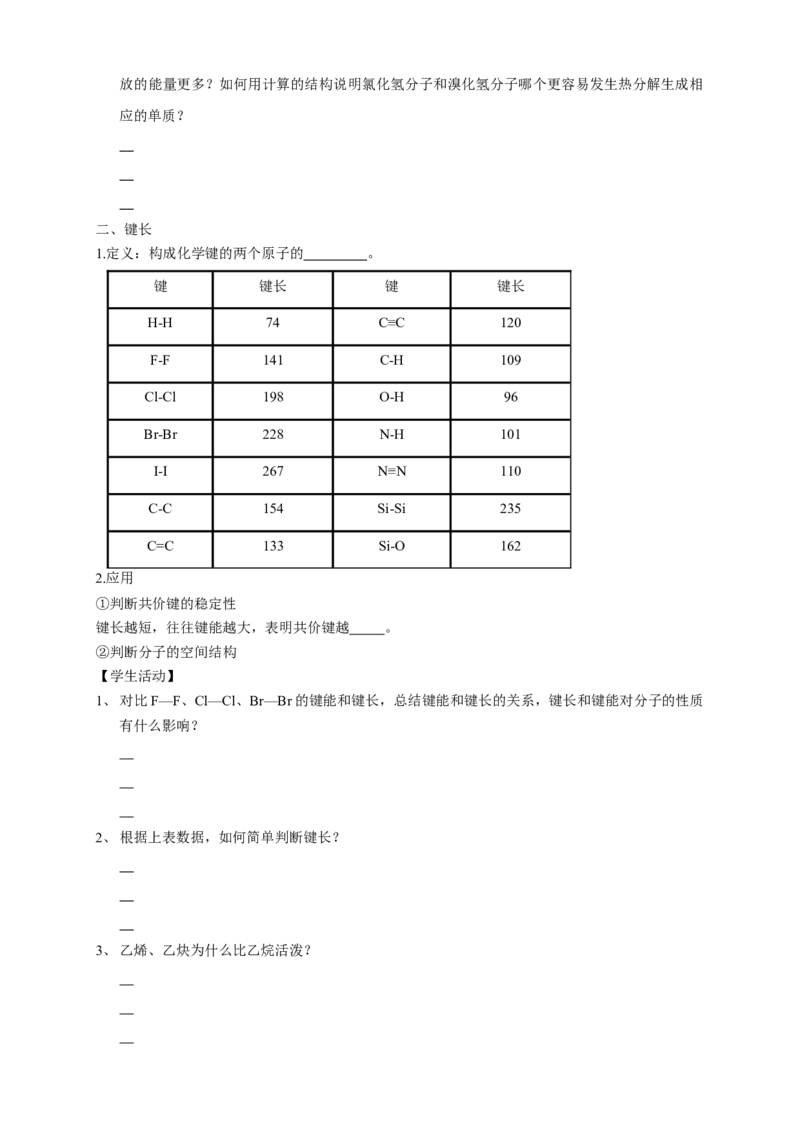
1.定义:构成化学键的两个原子的 。
键 键长 键 键长
H-H 74 C≡C 120
F-F 141 C-H 109
Cl-Cl 198 O-H 96
Br-Br 228 N-H 101
I-I 267 N≡N 110
C-C 154 Si-Si 235
C=C 133 Si-O 162
2.应用
①判断共价键的稳定性
键长越短,往往键能越大,表明共价键越 。
②判断分子的空间结构
【学生活动】
1、对比F—F、Cl—Cl、Br—Br的键能和键长,总结键能和键长的关系,键长和键能对分子的性质
有什么影响?
2、根据上表数据,如何简单判断键长?
3、乙烯、乙炔为什么比乙烷活泼?4、解释CH 分子的空间结构为正四面体形,而CHCl分子的空间结构是四面体形而不是正四面体
4 3
形。
三、键角
1、定义:在多原子分子中,两个 之间的夹角称为键角。
2、常见分子的键角:
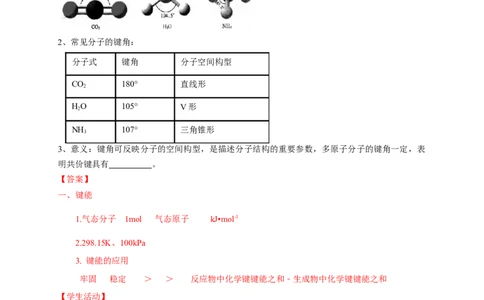
分子式 键角 分子空间构型
CO 180° 直线形
2
HO 105° V形
2
NH 107° 三角锥形
3
3、意义:键角可反映分子的空间构型,是描述分子结构的重要参数,多原子分子的键角一定,表
明共价键具有 。
【答案】
一、键能
1.气态分子 1mol 气态原子 kJ•mol-1
2.298.15K、100kPa
3. 键能的应用
牢固 稳定 > > 反应物中化学键键能之和﹣生成物中化学键键能之和
【学生活动】
1、N—H、O—H、H—F的键能依次为390.8 kJ•mol-1、462.8 kJ•mol-1、568 kJ•mol-1,键能依次增加,
分子的稳定性增强,故N、O、F 与氢气的反应能力依次增强。
2 2 2
2、通过计算,1mol H 分别与1mol Cl 、1mol Br (蒸气)反应,分别形成2mol HCl 和2mol HBr,放
2 2 2
出能量依次为184.9 kJ、102.3 kJ,1mol H 与1mol Cl 反应形成2mol HCl放出的能量多,氯化氢
2 2
分子更稳定,溴化氢分子更容易发生热分解生成相应的单质。
二、键长
1.核间距2.稳定
【学生活动】
1、利用键长可以判断共价键的稳定性,键长越短,键能越大,表明共价键越稳定,分子越稳定。
比如键长:F-F<Cl-Cl<Br-Br,则分子的稳定性F>Cl>Br 。
2 2 2
2、键长判断方法
①根据原子半径判断:其他条件相同时,成键原子的半径越小,键长越短。
②根据共用电子对数目判断
对于相同的两原子形成的共价键而言,当两个原子间形成双键、键时,由于原子轨道的重叠程
度增大,原子之间的核间距减小,键长变短,故单键键长>双键键长>三键键长。如键长:C-C
> C=C > C≡C。
3、虽然键长C≡C<C=C<C-C,键能C≡C>C=C>C-C,但乙烯、乙炔在发生加成反应时,只
有π键断裂(π键的键能一般小于σ键的键能),即共价键部分断裂。
4、由于C-H和C-Cl 的键长不相等,CH 分子的空间结构为正四面体形,而CHCl分子的空间结构
4 3
是四面体形而不是正四面体形。可见键长可以判断分子的空间结构
三、键角
相邻共价键 方向性
1.关于键长、键能和键角,下列说法中错误的是( )
A. 键角是描述分子立体结构的重要参数
B. 键长的大小与成键原子的半径和成键数目有关
C. C===C键等于C—C键键能的2倍
D. 因为O—H键的键能小于H—F键的键能,所以O、F 与H 反应的能力逐渐增强
2 2 2
【答案】C
【解析】键角是描述分子立体结构的重要参数,如HO中两个H—O键的键角为105°,故HO为V
2 2
形分子,A项正确;键长的大小与成键原子的半径有关,如Cl的原子半径小于I的原子半径,Cl—
Cl键的键长小于I—I键的键长,此外,键长还和成键数目有关,如乙烯分子中C===C键的键长比
乙炔分子中C≡C键的键长要大,B项正确;C===C键的键能为615 kJ·mol-1,C—C键的键能为
347.7 kJ·mol-1,二者不是2倍的关系,C项错误;O—H键的键能为462.8 kJ·mol-1,H—F键的
键能为568 kJ·mol-1,O—H键与H—F键的键能依次增大,意味着形成这些键时放出的能量依次
增大,化学键越来越稳定,O、F 跟H 反应的能力依次增强,D项正确。
2 2 2
2.下列有关性质的比较中,正确的是( )
A. 微粒半径:O2-<F-<Na+<Li+
B. 第一电离能:He<Ne<Ar
C. 分子中的键角:CH>HO>CO
4 2 2
D. 共价键的键能:C—C<C===C<C≡C【答案】D
【解析】Li+的电子层数最少,所以离子半径最小,其余三种离子的电子层结构相同,核电荷数越
大,离子半径越小,所以O2->F->Na+>Li+,A错误;稀有气体元素的第一电离能随电子层数的
增多而减小,所以He>Ne>Ar,B错误;甲烷分子为正四面体形,键角是109°28′,水为V形分子,
键角是105°,二氧化碳为直线形分子,键角为180°,所以二氧化碳分子中的键角最大,C错误;键
长:C—C>C===C>C≡C,所以键能:C—C<C===C<C≡C,D正确。
3.某些化学键的键能如表所示:
下列有关说法中正确的是( )
A. 1 mol H (g)分别与Cl(g)、Br (g)、I(g)反应,则与碘完全反应放出的热量最多
2 2 2 2
B. H—F键的键能大于431 kJ·mol-1
C. H 与Cl 反应的热化学方程式为H(g)+Cl(g)===2HCl(g) ΔH=-248 kJ·mol-1
2 2 2 2
D. 稳定性最强的化学键是H—Cl键
【答案】B
【解析】反应中的热量变化等于反应物的总键能减去生成物的总键能,通过计算易判断A、C错;
由表中三种卤化氢键能数据知,同一主族元素对应氢化物键能从上到下逐渐减小,故 B对;键能越
大,键越稳定,D错。
4.下表所列数据是在相同条件下,不同物质中氧氧键的键长和键能的实测数据,下列有关说法中正
确的是( )
A.a