文档内容
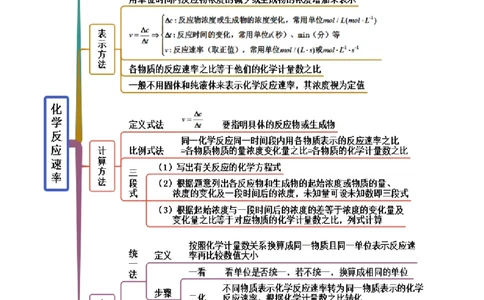
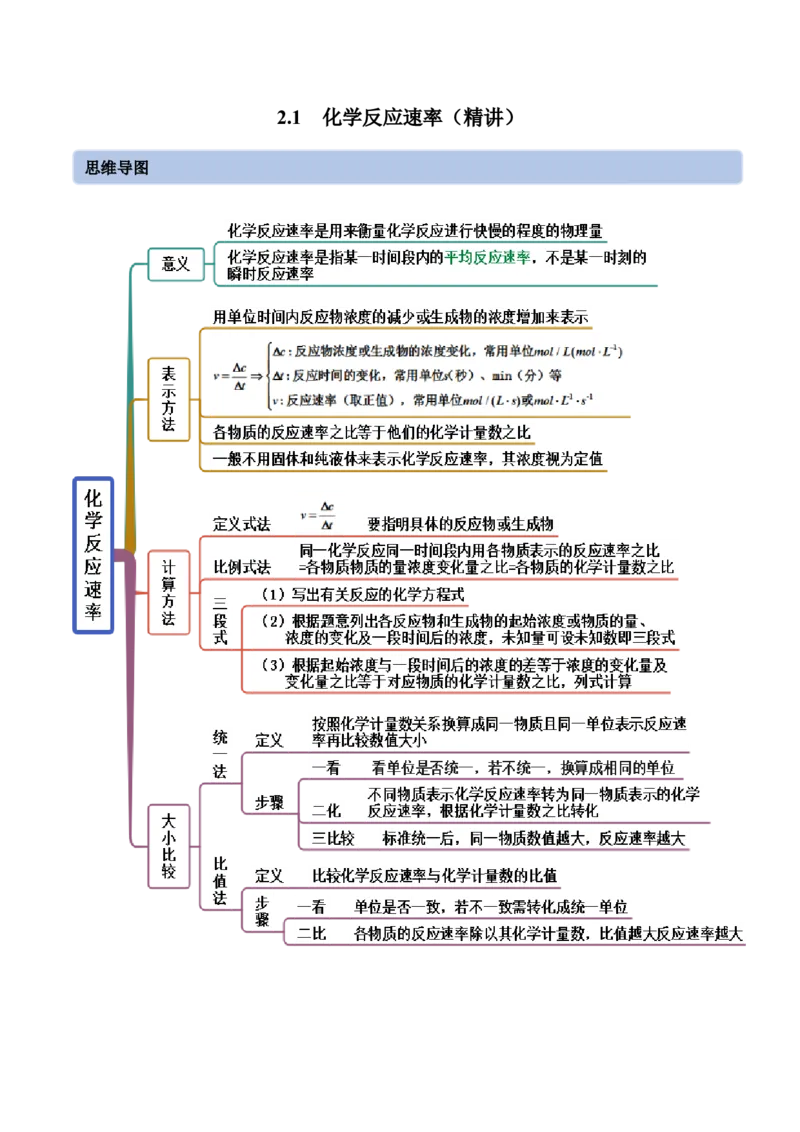
2.1 化学反应速率(精讲)
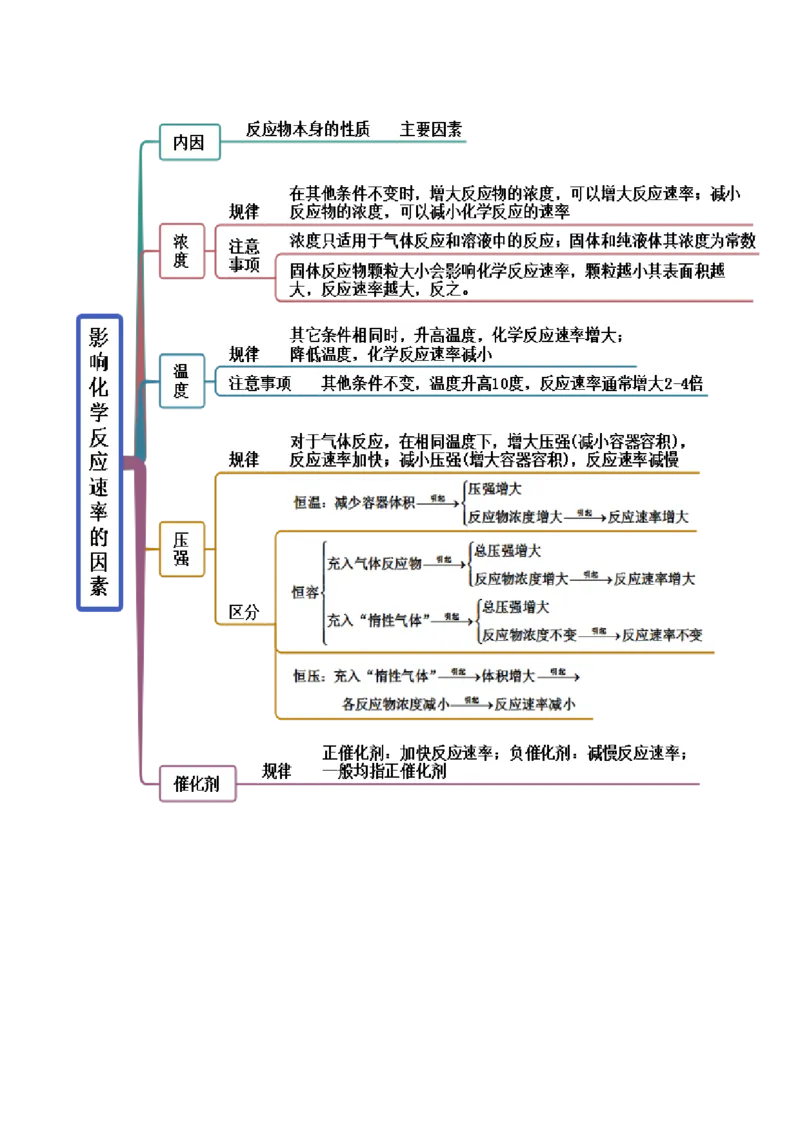
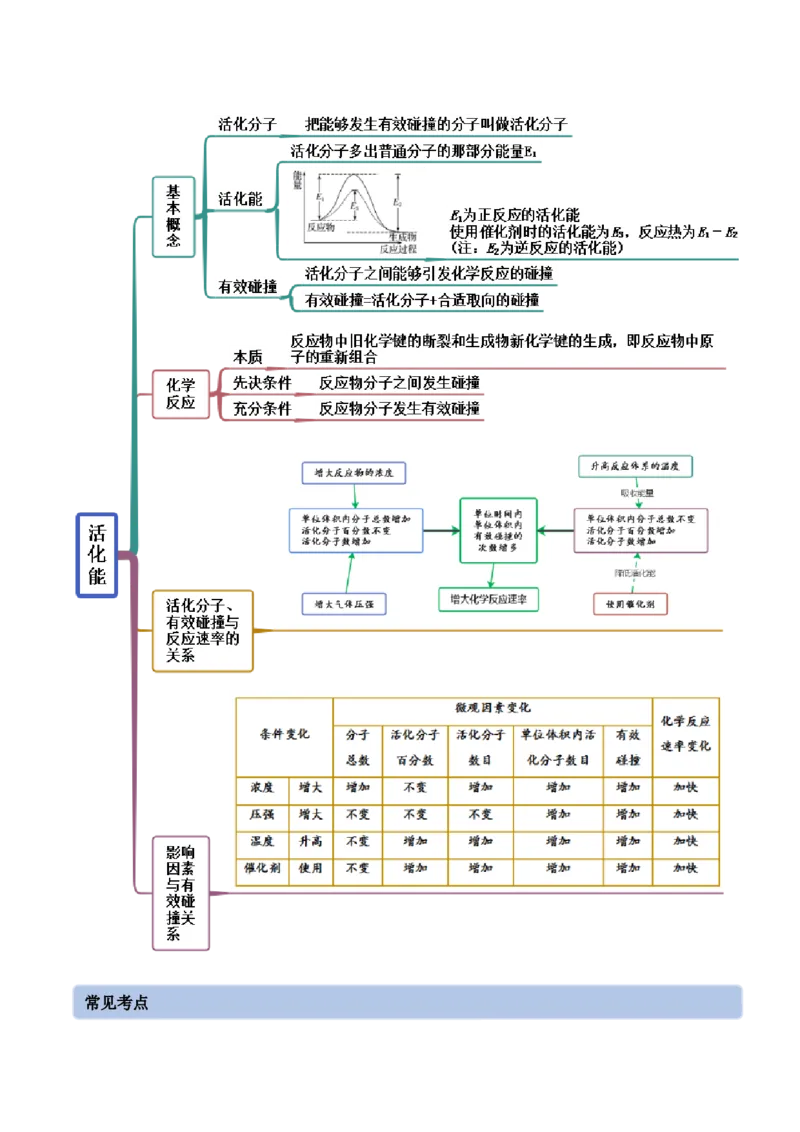
思维导图常见考点考点一 化学反应速率的计算
【例1-1】(2022·广西桂林·高二期末)一定条件下,向一4L密闭容器中充入2mol 和8mol 发生反
应: ,5min后测得 的物质的量为4mol,下列说法正确的是
A. B.
C. D.
【答案】A
【解析】列出三段式:
,由此解析。
A. ,故A正确;
B. ,故B错误;
C. ,故C错误;
D. ,故D错误;
故选A。
【例1-2】(2022·全国·高二课时练习)在密闭容器里,A与B反应生成C,其反应速率分别用v 、v 、v
A B C
表示,已知2v =3v 、3v =2v ,则此反应可表示为
B A C BA.A+3B=2C B.2A+3B=2C C.3A+B=2C D.A+B=C
【答案】B
【解析】在密闭容器里,A与B反应生成C,则A与B是反应物,C是生成物。在同一反应中用不同物质
表示反应速率时,速率比等于方程式中相应物质的化学计量数的比。由于2v =3v 、3v =2v ,则n(A):
B A C B
n(B):n(C)=v :v :v =2:3:2,故化学方程式为2A+3B=2C;答案选B。
A B C
【例1-3】(2022·全国·高二课时练习)在2L密闭容器中,3molA和1molB发生反应:3A(g)+B(g) 2C(g)
+2D(g),10s末时,生成0.6mol/LC,下列说法正确的是 ⇌
A.10s内,v(D)=0.12mol/(L·s) B.10s末时,物质A的转化率为40%
C.10s末时,B的物质的量为0.4mol D.10s末时,C的物质的量分数为15%
【答案】C
【解析】A. 10s末时,生成0.6mol/LC,由反应可知,生成1.2molC的同时也生成1.2molD,则v(D)=
,故A错误;
B.由变化量之比等于化学计量数之比可得,生成1.2molC时,消耗的A的物质的量为1.8mol,则A的转
化率= ,故B错误;
C.由变化量之比等于化学计量数之比可得,生成1.2molC时,消耗的B的物质的量为0.6mol,则剩余的
B的物质的量为1mol-0.6mol=0.4mol,故C正确;
D.由以上分析可知,平衡时A的物质的量为3mol -1.8mol=1.2mol,B的物质的量为0.4mol,C和D的物
质的量均为1.2mol,则C 的物质的量分数为= ,故D错误;故
选:C。
【一隅三反】
1.(2022·全国·高二课时练习)在 的反应中,2s后, 的物质的量浓度增加了
,用 来表示反应速率为
A. B. C. D.
【答案】C【解析】在 的反应中,2s后, 的物质的量浓度增加了 ,用 表示的化
学反应速率为v= = ,根据化学反应速率之比等于计量数之比,故用 来表示反应速
率为 = ;答案选C。
2.(2021·吉林·汪清县汪清第四中学高二阶段练习)在容积不变的密闭容器中,A和B反应生成C和D,
其化学反应速率分别用v(A)、v(B)、v(C)、v (D)表示。已知2 v (A)= v (C)、 3v (B)=4 v (D)、3 v (A)=2
v (D),则此反应可表示为
A.3A+4B=2C+3D B.3A+4B=4C+2D
C.2A+4B=4C+3D D.A+4B=3C+3D
【答案】C
【解析】由3v (B)=4 v (D)、3 v (A)=2 v (D)可知,v (B)=2v (A),由反应速率之比等于化学计量数之比
可得:A、B、C、D的化学计量数之比为v (A):2 v (A):2v (A): =2:4:4:3,反应的化学方
程式为2A+4B=4C+3D,故选C。
3.将6 mol A和5 mol B混合于4 L恒容密闭容器中,发生如下反应:
,5 s后反应达到平衡状态,生成2 mol D,经测定以C表示的平均反应速率为0.1 。则下列结论
中正确的是
A.5 s内以A表示的平均反应速率为0.075
B.平衡时,B的浓度为4
C.n值等于1
D.当反应速率符合2v (A)=3v (D)达到平衡
正 逆
【答案】A
【解析】A.平衡时生成2mol的D,所以参加反应的A为1.5mol,故 ,
故A正确;
B.平衡时生成2mol的D,所以参加反应的B为0.5mol,故平衡时B的物质的量为5mol-0.5mol=4.5mol,平衡时B的浓度为 ,故B错误;
C.速率之比等于化学计量数之比,故3:n=0.075mol•(L•s)-1:0.1mol••(L•s)-1,解得n=4,故C错误;
D.平衡时正逆反应速率相等,即4v (A)=3v (D) 达到平衡,故D错误;
正 逆
故选:A。
4.已知 ,反应速率分别用 、 、 、 表示,正确的是
A. B.
C. D.
【答案】A
【解析】A.由于v(O ):v(NO)=5:4,所以 ,A正确;
2
B.由于v(O ):v(H O)=5:6,所以 ,B错误;
2 2
C.由于v(NH ):v(H O)=4:6=2:3,所以 ,C错误;
3 2
D.由于v(NH ):v(O )=4:5,所以 ,D错误;
3 2
故合理选项是A。
考点二 比较化学反应速率
【例2-1】(2022·贵州遵义·高二期末)对于可逆反应 在不同条
件下的化学反应速率如下,其中表示反应速率最快的是
A. B.
C. D.
【答案】A
【解析】A. 即为v(NH )= ×v(H O)=60s/min×
3 2
×0.05molL−1s−1=2molL−1min−1;
⋅ ⋅ ⋅ ⋅
B.v(O )=1molL−1min−1即为v(NH )= ×v(O )= ×1molL−1s−1=0.8molL−1s−1;
2 3 2
⋅ ⋅ ⋅ ⋅ ⋅ ⋅C.v(NO)=1.6molL−1min−1即为v(NH )=v(NO)=1.6mol L−1min−1;
3
⋅ ⋅ ⋅ ⋅
D.
综上所述,反应最快的是 ,故答案为A。
【例2-2】反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)= 24mol·L-1·min-1,
②v(B)=1.5 mol·L-1·s-1,③v(C)=0.4 mol·L-1·s-1,④v(D)=0.5 mol·L-1·s-1,该反应进行的快慢顺序为
A.①<③<②<④ B.④<③<①<② C.②>①>④>③ D.④>③>②>①
【答案】C
【解析】同一反应中,不同物质的反应速率与反应方程式中的化学计量数的比值越大,反应速率越快,由
题给数据可得: = =0.4、 = =0.5、 =
=0.2、 = =0.25,则反应进行的快慢顺序为②>①>④>③,故选C。
【一隅三反】
1.(2022·四川达州·高二期末)反应 在不同条件下用不同物质表示的化学反
应速率如下,其中反应最快的是
A. B.
C. D.
【答案】C
【解析】由经验公式可知,同一化学反应中物质的反应速率与化学计量数的比值越大,反应速率越大,
= = 、 = = 、 = = 、 = = ,则反应速率最大的为C,故选
C。
2.反应4A(g)+3B(g)=2C(g)+5D(g)在四种不同条件下的反应速率分别为( )
①v(A)=0.02mol·L-1·s-1;②v(B)=0.6mol·L-1·min-1;③v(C)=0.3mol·L-1·min-1;④v(D)=1.2mol·L-1·min-1其中表示该反应速率最慢的是( )
A.① B.② C.③ D.④
【答案】C
【解析】v(A)=0.02mol·L-1·s-1=1.2mol·L-1·min-1,反应速率与化学计量数的比值越大,反应速率越快,则
① =0.3;② =0.2;③ =0.15;④ =0.24,显然表示该反应速率最慢的是③,故选C。
3.反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45 mol·L-1·s-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1
④v(D)=0.45 mol·L-1·s-1。下列有关反应速率的比较中正确的是
A.④>③=②>① B.①>④>②=③
C.①>②>③>④ D.④>③>②>①
【答案】B
【解析】同一化学反应中,不同物质表示的速率比等于系数比,都转化为用A表示的反应速率。①v(A)=
0.45 mol·L-1·s-1;②v(A)= v(B)= 0.6 mol·L-1·s-1=0.2 mol·L-1·s-1; ③v(A)= v(C)= 0.4
mol·L-1·s-1=0.2 mol·L-1·s-1;④v(A)= v(D)= 0.45 mol·L-1·s-1=0.225 mol·L-1·s-1,所以①>④>②=③,故B
正确;选B。
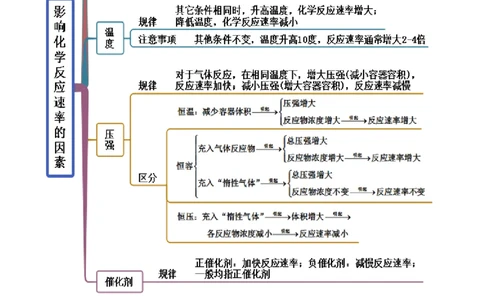
考点三 影响化学反应速率的因素
【例3-1】(2022·四川省蒲江县蒲江中学高二阶段练习)密闭容器中发生反应
。下列措施能增大反应速率的是
A.增加C的物质的量 B.降低反应温度
C.将容器的体积缩小一半 D.保持压强不变,充入
【答案】C
【解析】A.固体不影响反应速率,A错误;
B.温度降低,活化分子百分数降低,反应速率降低,B错误;
C.将容器的体积缩小一半,相当于加压,浓度增大,化学反应速率增大,C正确;
D.保持压强不变,充入 N 相当于减压,体积增大,浓度减小,反应速率降低,D错误;
2
故选C。
【例3-2】(2022·宁夏·银川二中高二阶段练习)回答下列问题:(1)我校化学社团做了如下探究实验:利用HC O 溶液和酸性KMnO 溶液之间的反应来探究外界条件改变
2 2 4 4
对化学反应速率的影响。实验数据如表所示:
实 KMnO 溶液(含硫酸) HC O 溶液 HO
4 2 2 4 2
验
实验温度/K 溶液颜色褪至无色时所需时间/s
序
号
A 293 2 0.02 5 0.1 3
B 293 2 0.02 3 0.1 8
C 313 2 0.02 0.1 5
①写出该反应的离子方程式:__ _____。
②通过实验A、B可探究_______(填外部因素)的改变对反应速率的影响,其中V=_______;通过实验
1
_______(填实验序号)可探究温度变化对化学反应速率的影响。
③利用实验B中数据计算,用KMnO 溶液的浓度变化表示的反应速率v(KMnO)=_______。
4 4
④实验中发现:反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的某种粒子对
KMnO 与HC O 之间的反应有某种特殊的作用,则该作用是_______,相应的粒子最有可能是_______。
4 2 2 4
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO 2CO+N 。已知增大催化剂的比表面积可提高该
2 2
反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表
所示。
实验
t/℃ NO初始浓度/mol·L-1 CO初始浓度/mol·L-1 催化剂的比表面积/m2/g
编号
I 280 82
II 280 b 124
Ⅲ 350 a 82
①表中a=_______,b=_______。
②能验证温度对化学反应速率影响规律的是实验_______(填实验编号)。
③实验I和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验II的是曲线
_______(填“甲”或“乙”)。【答案】(1) HC O 溶液浓度的改变对反应速率的影
2 2 4
响 5 BC 催化作用 Mn2+
(2) I、Ⅲ 乙
【解析】(1)①酸性KMnO 具有强氧化性,和HC O 溶液反应生成二氧化碳和锰离子,反应为
4 2 2 4
;
②实验A、B中控制的变量为HC O 溶液浓度,可探究HC O 溶液浓度的改变对反应速率的影响,实验中
2 2 4 2 2 4
溶液总体积要相同,故其中V=5;
1
实验BC中控制的变量为HC O 溶液浓度,通过实验BC可探究温度变化对化学反应速率的影响。
2 2 4
③实验B中n(KMnO)=2×10-3L×0.02mol/L=4×10-5mol,n(H C O)=3×10-3L×0.1mol/L=3×10-4mol,反应中
4 2 2 4
HC O 过量,KMnO 全部反应;KMnO 起始浓度为 ,用KMnO 溶液的浓
2 2 4 4 4 4
度变化表示的反应速率v(KMnO)= 。
4
④反应一段时间后该反应速率会突然加快,造成此种变化的原因是反应体系中的生成的锰离子对KMnO 与
4
HC O 之间的反应有催化作用,故填:催化作用,Mn2+;
2 2 4
(2)①验证温度、催化剂的比表面积对化学反应速率的影响规律,设计了三组实验,实验I、II中变量为催
化剂的比表面积,则b= ;实验I、Ⅲ中变量为温度,则a= ;
②实验I、Ⅲ中变量为温度,能验证温度对化学反应速率影响规律的是实验I、Ⅲ;
③已知增大催化剂的比表面积可提高该反应速率,实验Ⅱ中催化剂的比表面积更大,反应速率更快,故表
示实验II的是曲线乙。
【一隅三反】1.在一密闭容器中发生反应:3Fe(s)+4H O(g) Fe O(s)+4H(g),下列判断正确的是( )
2 3 4 2
A.升高反应温度对反应限度无影响
B.改变H 的浓度对正反应速率无影响
2
C.保持体积不变,充入N 反应速率增大
2
D.保持压强不变,充入N 反应速率减小
2
【答案】D
【解析】A.升高反应温度加快化学反应速率,平衡向着吸热方向移动,所以改变温度,对反应限度有影响,
故A错误;
B.增大反应物的浓度加快化学反应速率,平衡正向移动,减小反应物的浓度减慢化学反应速率,平衡逆向
移动。因为H 属于反应物,所以改变H 的浓度对正反应速率有影响,故B错误;
2 2
C.保持体积不变,充入N 气使体系压强增大,但反应物和生成物的浓度不变,所以反应速率不变,故C错
2
误;
D.压强不变,充入N 使容器的体积增大,反应气体的浓度减小,反应速率减小,故D正确;
2
故选D。
2.I.为探究H+对MnO 与HO 反应速率的影响。现取等量MnO 和表中有关物质,在相同温度下进行4组
2 2 2 2
实验,分别记录收集20.0mLO 所需时间。
2
实验编号 1 2 3 4
10%H O 的体积/mL 5.0 5.0 V V
2 2 1 2
20%硫酸的体积/mL 0 0.5 1.0 V
3
水的体积/mL 15.0 14.5 V 13.5
4
所需时间t/s t t t t
1 2 3 4
已知酸性条件下时:MnO +H O+2H+=Mn2++O ↑+2H O
2 2 2 2 2
(1)表中V=____mL,V=_____mL。
2 4
(2)实验测得t>t>t,则可得出的实验结论是____。
2 3 4
II.已知反应2NO(g)+2H (g)=N(g)+2HO(g)生成N 的初始速率与NO、H 的初始浓度的关系为
2 2 2 2 2
v=kcx(NO)cy(H ),k为速率常数。在800℃时测得的相关数据如表所示。
2
初始浓度
实验数据 生成N 的初始速率/mol·L-1·s-1
2
c(NO)/mol·L-1 c(H)/mol·L-1
2
1 2.00×10-3 6.00×10-3 1.92×10-32 1.00×10-3 6.00×10-3 4.80×10-4
3 2.00×10-3 3.00×10-3 9.60×10-4
(3)由表中的数据可算出x、k的值:x=_____,k=____。
(4)若800℃时,初始浓度c(NO)=c(H )=4.00×10-3mol·L-1,则生成N 的初始速率为_____mol·L-1·s-1。
2 2
【答案】(1) 5.0 14.0
(2)其他条件相同的情况下,H+的浓度越大,反应速率越快
(3) 2 8×104
(4)5.12×10-3
【解析】(1)为了探究H+浓度对MnO 与HO 反应速率的影响,只改变H+浓度,其他量都必须相同,所以
2 2 2
V=5.0mL;水和硫酸的体积之和为15.0mL,所以表中V=14.0mL。
1 4
(2)实验测得t>t>t,则实验2、3、4的反应速率依次加快,则可得出的实验结论是:其他条件相同的情况下,
2 3 4
H+的浓度越大,反应速率越快。
(3)将3组实验数据代入v=k cx(NO)•cy(H ),中有:
2
,
,
,解得:x=2,y=1,k=8×104。
(4)若800℃时,初始浓度c(NO)=c(H )=4.00×10-3mol·L-1,则生成N 的初始速率v=8×104×c2(NO)·c( H )
2 2 2
=8×104×(4.00×10-3)2×(4.00×10-3)=5.12×10-3mol·L-1·s-1。
3.(2022·江西吉安·高二期末)I.实验室利用下列方案探究影响化学反应速率的因素。请回答相关问题:
溶液 酸性 溶液
编
温度/℃
号
浓度/ 体积/ 浓度/ 体积/
① 25 0.10 2.0 0.010 4.0
② 25 0.20 2.0 0.010 4.0
③ 50 0.20 2.0 0.010 4.0
(1)实验时,分别量取 溶液和酸性 溶液,迅速混合并开始计时,通过测定_______来判断反
应的快慢。(2)实验①、②、③所加 溶液均要过量,理由是_______。
(3)实验①和实验②是探究_______对化学反应速率的影响,实验②和③是探究_______对化学反应速率的影
响。
(4)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是_______。
II.在恒容密闭容器中,用H 还原SO ,生成S的反应分两步完成(如图1所示),该过程中相关物质的物质
2 2
的量浓度随时间的变化关系如图2所示,请分析并回答如下问题:
(5)分析可知X为_______(填化学式)。
(6) 时间段的温度为_______。
(7) 时间段用SO 表示的化学反应速率为_______。
2
【答案】(1) 溶液褪色时间
(2)根据反应方程式: ,实验通过测定溶液
的褪色时间判断反应的快慢,则三个实验中所加 溶液均要过量
(3) 浓度 温度
(4)反应生成了具有催化作用的物质,其中可能起催化作用为
(5)H S
2
(6)300℃
(7)
【解析】(1) 溶液和酸性 溶液反应的化学方程式为:,通过测量 溶液褪色时间来判断
反应的快慢;
(2)根据反应方程式: ,实验通过测定溶液
的褪色时间判断反应的快慢,则三个实验中所加 溶液均要过量;
(3)①实验①和实验② 溶液的浓度不同,其他实验条件均相同,则实验①和实验②探究 溶液
的浓度对化学反应速率的影响;
②实验②和实验③中温度不同,其他实验条件均相同,则验②和实验③探究温度对化学反应速率的影响;
(4)实验①和②起初反应均很慢,过了一会儿速率突然增大,说明可能反应生成了具有催化作用的物质,其
中可能起催化作用为 ;
(5)根据图1可知,在300℃时,H 和SO 在催化剂条件下生成HS,在100℃到200℃时,HS与SO 在催
2 2 2 2 2
化剂生成S和HO,则物质X为HS;
2 2
(6)由图2可知, 时间段H 完全转化为HS, H 和SO 的浓度降低且HS的浓度增大,则 时间段
2 2 2 2 2
的温度为300℃;
(7) 时间段用SO 浓度的变化量为 ,SO 的化学反应速率为
2 2
。
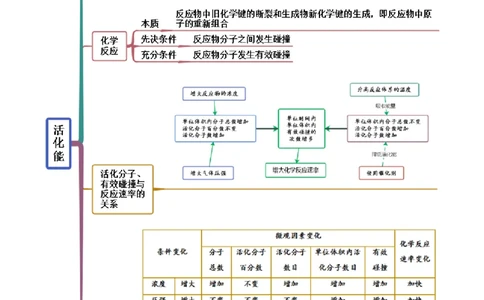
考点四 活化能
【例4】(2021·江西·高二阶段练习)下列说法正确的是
A.增大压强,活化分子百分数增大,化学反应速率一定增大
B.升高反应体系温度,活化分子百分数增大,化学反应速率一定增大
C.一般使用催化剂可降低反应的活化能,活化分子百分数不变,化学反应速率增大
D.增大反应物的浓度,使活化分子百分数增大,化学反应速率增大
【答案】B
【解析】A.增大压强,单位体积内活化分子的数目增大,活化分子的百分数不变,故A错误;
B.升高温度,活化分子的百分数增大,反应速率增大,故B正确;C.催化剂可以降低反应的活化能,增大活化分子百分数,故C错误;
D.加入反应物,反应物的浓度增大,单位体积内活化分子的数目增大,活化分子的百分数不变,故D错
误;故选:B。
【一隅三反】
1.(2022·云南·昆明市第三中学高二期中)下列对化学反应速率增大原因的分析错误的是
A.升高温度,使反应物分子中活化分子百分数增大
B.向反应体系中加入相同浓度的反应物,使活化分子百分数增大
C.对有气体参加的化学反应,增大压强使容器容积减小,单位体积内活化分子数增多
D.加入适宜的催化剂,使反应物分子中活化分子百分数增大
【答案】B
【解析】A.升温,反应物分子的能量升高,则活化分子百分数增大,A正确;
B.向反应体系中加入相同浓度的反应物,活化分子百分数不改变,B错误;
C.对有气体参加的反应,增大压强使容器减小,则浓度增大,单位体积的活化分子数增多,C正确;
D.加入适宜的催化剂,降低反应的活化能,使反应物中活化分子百分数增大,D正确;
故选B。
2.(2022·广东·肇庆市实验中学高二期末)下列说法不一定正确的是
A.增大反应物浓度能增大单位体积内活化分子总数,化学反应速率增大
B.增大压强能增大活化分子百分数,化学反应速率增大
C.升高温度能增大活化分子百分数,化学反应速率增大
D.加入合适催化剂能增大活化分子百分数,化学反应速率增大
【答案】B
【解析】A.增大浓度,单位体积活化分子数目增多,则使有效碰撞次数增大,反应速率加快,故A正确;
B.增大压强是能增大单位体积活化分子总数,使化学反应速率增大,活化分子百分数未发生变化,故B
错误;
C.升高温度,活化分子的百分数,反应速率增大,故C正确;
D.催化剂,降低反应所需的活化能,增大单位体积内活化分子的百分数,故D正确;
故选:B。
3.能增加反应物分子中活化分子的百分数的是:
①升高温度 ②增加浓度③增大压强 ④使用催化剂
A.① ③ B.①④ C.②③ D.①③④
【答案】B
【解析】①升高温度可以增大反应物分子中活化分子的百分数;②增加浓度可使活化分子的浓度增大,即可增加单位体积内活化分子数,但百分数不变;
③增大压强可使活化分子的浓度增大,即可增加单位体积内活化分子数,但百分数不变;
④使用催化剂可增大反应物中的活化分子百分数;
因此符合条件的是①④,答案选B。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育