文档内容
第 2 课时 炔烃
发 展 目 标 体 系 构 建
1.结合代表物,认识炔烃
的组成和结构,理解炔烃
的化学性质及应用,培养
“宏观辨识与微观探
析”的核心素养。
2.了解乙炔的实验室制
法,培养“科学探究”的
核心素养。
一、炔烃
1.结构
官能团为 碳碳三键 (—C≡C— ),含一个碳碳三键的炔烃通式为CH 。
n 2n-2
2.炔烃的物理性质递变性
随分子中碳原子数的递增沸点逐渐升高,密度逐渐增大。
二、乙炔
1.物理性质
颜色:无色;状态:气体;气味:无臭;密度:比空气略小;溶解性:水中微溶,有机溶剂中易
溶。
2.组成与结构
乙炔的分子式为 CH ,是最简单的炔烃,结构式是 ,结构简式是
2 2
,空间结构为直线形结构,分子中碳原子均采取sp 杂化,共价键类型有σ 键和π
键。
3.实验室制取
(1)试剂: 电石 (Ca C)和饱和氯化钠溶液。
2
(2)反应原理: 。
(3)杂质气体及除杂试剂为HS,CuSO 溶液。
2 4
(4)收集方法:排水法。
微点拨:①为了减小电石与水的反应速率,实验时常用饱和氯化钠溶液代替水作反应试剂。
②点燃乙炔、乙烯、甲烷前要检验纯度,防止爆炸。
4.乙炔化学性质
(1)氧化反应
①乙炔容易燃烧,燃烧时火焰明亮并伴有浓烈的黑烟。
1有关化学方程式:2CH + 5 O ――→ 4C O + 2 HO。
2 2 2 2 2
微点拨:①乙炔燃烧时产生浓烈黑烟的原因是因为乙炔的含碳量很高,没有完全燃烧。
②乙炔在氧气中燃烧时火焰温度可达3 000 ℃以上,故常用它来焊接或切割金属。
②乙炔能使酸性KMnO 溶液褪色,说明乙炔能被酸性KMnO 溶液氧化。
4 4
(2)加成反应
乙炔能与溴的四氯化碳溶液、卤素单质、氢气、氢氰酸、氢卤酸、水等在一定条件下发生加
成反应。如:
HCCH+Br―→ CHB r = = = CHBr(1, 2 二溴乙烯 );
2
CHBr===CHBr+Br―→CHBr—CHBr (1,1,2, 2 四溴乙烷 )。
2 2 2
CH≡CH+H――→CH===CH。
2 2 2
HCCH+HCl――→CH = = = CHCl ( 氯乙烯 )。
2
CH≡CH+HO――→CHCHO。
2 3
(3)加聚反应——制聚乙炔(制备导电高分子材料)
反应方程式为 。
丙炔有哪些化学性质?
[提示] 能发生氧化反应、加成反应、加聚反应。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)烯烃与炔烃均为不饱和烃,均能使酸性KMnO 溶液褪色。
4
( )
(2)乙炔分子中的σ键与π键个数比为1∶2。 ( )
(3)乙烷、乙烯、乙炔中的碳原子杂化类型分别为sp3、sp2、sp。
( )
(4)乙烯中混有的乙炔可用溴水除去。 ( )
(5)乙炔可以用电石与饱和氯化钠溶液制取。 ( )
[答案] (1)√ (2)× (3)√ (4)× (5)√
2.鉴别乙烷、乙烯、乙炔三种气体可采用的方法是( )
A.通入溴水中,观察溴水是否褪色
B.通入酸化的高锰酸钾溶液中,观察颜色是否变化
C.点燃,检验燃烧产物
D.点燃,观察火焰明亮程度及产生黑烟量的多少
[答案] D
3.写出下列反应的化学方程式
(1)乙炔与足量溴水反应:
______________________________________________________。
(2)乙炔与HO的加成反应:
2
______________________________________________________。
2[答案] (1)CH≡CH+2Br―→CHBrCHBr
2 2 2
(2)CH≡CH+HO――→CHCHO
2 3
实验室制取乙炔的实验探究
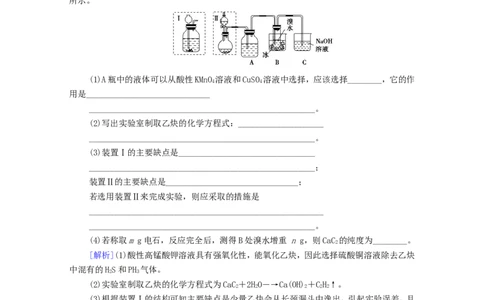
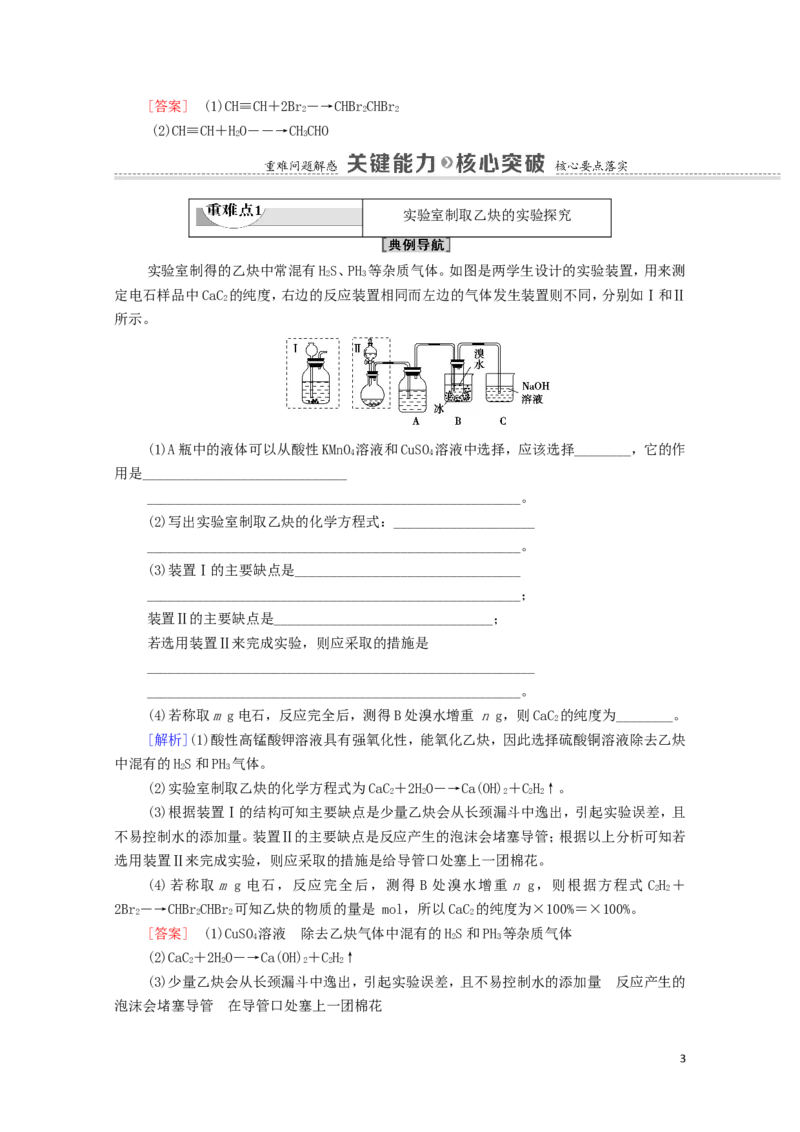
实验室制得的乙炔中常混有HS、PH 等杂质气体。如图是两学生设计的实验装置,用来测
2 3
定电石样品中CaC 的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ
2
所示。
(1)A瓶中的液体可以从酸性KMnO 溶液和CuSO 溶液中选择,应该选择________,它的作
4 4
用是_____________________________
_____________________________________________________。
(2)写出实验室制取乙炔的化学方程式:____________________
_____________________________________________________。
(3)装置Ⅰ的主要缺点是________________________________
_____________________________________________________;
装置Ⅱ的主要缺点是_______________________________;
若选用装置Ⅱ来完成实验,则应采取的措施是
_______________________________________________________
_____________________________________________________。
(4)若称取m g电石,反应完全后,测得B处溴水增重 n g,则CaC 的纯度为________。
2
[解析](1)酸性高锰酸钾溶液具有强氧化性,能氧化乙炔,因此选择硫酸铜溶液除去乙炔
中混有的HS和PH 气体。
2 3
(2)实验室制取乙炔的化学方程式为CaC+2HO―→Ca(OH)+CH↑。
2 2 2 2 2
(3)根据装置Ⅰ的结构可知主要缺点是少量乙炔会从长颈漏斗中逸出,引起实验误差,且
不易控制水的添加量。装置Ⅱ的主要缺点是反应产生的泡沫会堵塞导管;根据以上分析可知若
选用装置Ⅱ来完成实验,则应采取的措施是给导管口处塞上一团棉花。
(4)若称取m g 电石,反应完全后,测得 B 处溴水增重n g,则根据方程式 CH +
2 2
2Br―→CHBrCHBr 可知乙炔的物质的量是 mol,所以CaC 的纯度为×100%=×100%。
2 2 2 2
[答案] (1)CuSO 溶液 除去乙炔气体中混有的HS和PH 等杂质气体
4 2 3
(2)CaC+2HO―→Ca(OH)+CH↑
2 2 2 2 2
(3)少量乙炔会从长颈漏斗中逸出,引起实验误差,且不易控制水的添加量 反应产生的
泡沫会堵塞导管 在导管口处塞上一团棉花
3(4)×100%
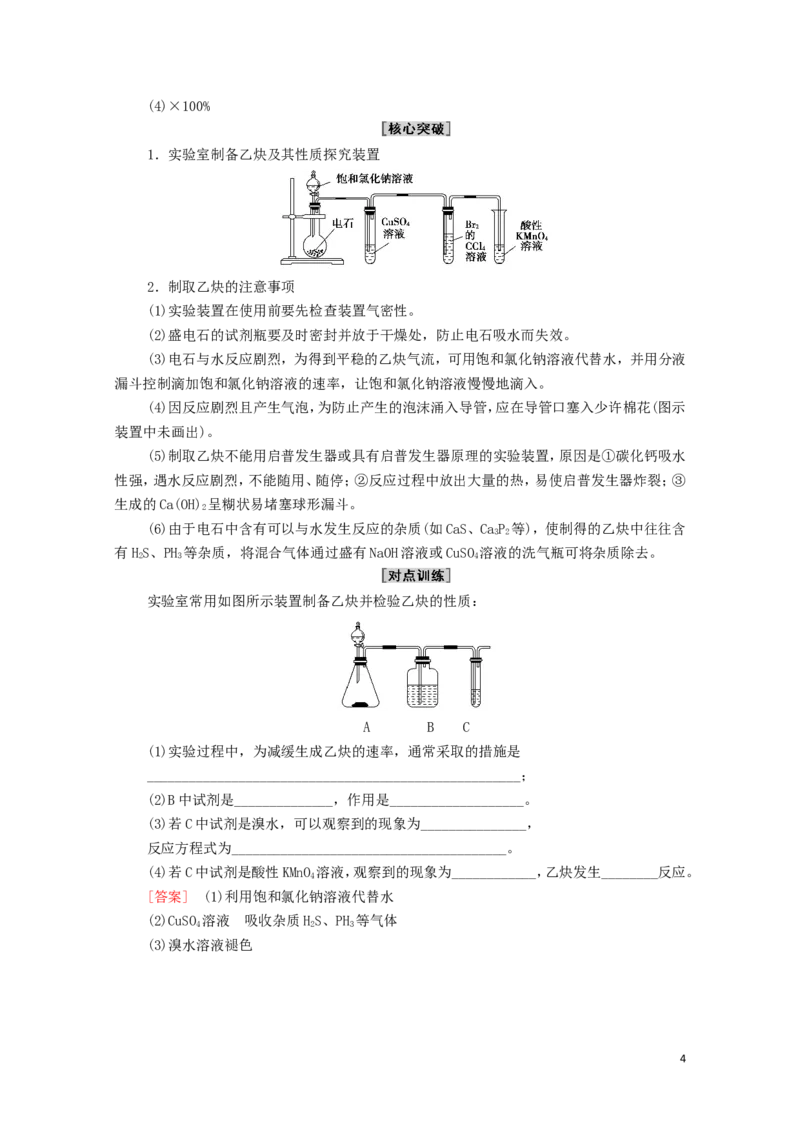
1.实验室制备乙炔及其性质探究装置
2.制取乙炔的注意事项
(1)实验装置在使用前要先检查装置气密性。
(2)盛电石的试剂瓶要及时密封并放于干燥处,防止电石吸水而失效。
(3)电石与水反应剧烈,为得到平稳的乙炔气流,可用饱和氯化钠溶液代替水,并用分液
漏斗控制滴加饱和氯化钠溶液的速率,让饱和氯化钠溶液慢慢地滴入。
(4)因反应剧烈且产生气泡,为防止产生的泡沫涌入导管,应在导管口塞入少许棉花(图示
装置中未画出)。
(5)制取乙炔不能用启普发生器或具有启普发生器原理的实验装置,原因是①碳化钙吸水
性强,遇水反应剧烈,不能随用、随停;②反应过程中放出大量的热,易使启普发生器炸裂;③
生成的Ca(OH) 呈糊状易堵塞球形漏斗。
2
(6)由于电石中含有可以与水发生反应的杂质(如CaS、CaP 等),使制得的乙炔中往往含
3 2
有HS、PH 等杂质,将混合气体通过盛有NaOH溶液或CuSO 溶液的洗气瓶可将杂质除去。
2 3 4
实验室常用如图所示装置制备乙炔并检验乙炔的性质:
A B C
(1)实验过程中,为减缓生成乙炔的速率,通常采取的措施是
_____________________________________________________;
(2)B中试剂是______________,作用是___________________。
(3)若C中试剂是溴水,可以观察到的现象为_______________,
反应方程式为_______________________________________。
(4)若C中试剂是酸性KMnO 溶液,观察到的现象为____________,乙炔发生________反应。
4
[答案] (1)利用饱和氯化钠溶液代替水
(2)CuSO 溶液 吸收杂质HS、PH 等气体
4 2 3
(3)溴水溶液褪色
4炔烃的结构与化学性质
1.分析指出丙炔中碳原子的杂化类型和共价键类型
[提示] ,4个C—H σ键,2个C—C σ键,2个π键。
2.请写出1丁炔与足量氢气完全反应的化学方程式,并分析该反应中化学键和官能团的
变化。
[提示] CH≡CCHCH+2H――→
2 3 2
CHCHCHCH,反应中碳原子之间形成的π键断裂,形成4个C—H σ键。
3 2 2 3
3.(1)请写出戊炔所有属于炔烃的同分异构体的结构简式,并用系统命名法命名。
(2)某炔烃通过催化加氢反应得到2甲基戊烷,请由此推断该炔烃可能的结构简式,并命
名。
[提示](1)CH≡C(CH)CH 1戊炔
2 2 3
51.炔烃的结构与性质
(1)结构:分子中的碳原子一定存在sp杂化,共价键一定存在σ键和π键,以“—C≡C
—”为中心的4原子共线结构。
(2)炔烃化学性质
②加成反应:与X、HX、HO、H 等发生加成反应
2 2 2
2.炔烃的命名方法
(1)选主链:将含碳碳三键的最长碳链作为主链,并按主链中所含碳原子数称为“某炔”。
(2)编序号:从距离三键最近的一端给主链上的碳原子依次编号,使三键碳原子的编号最
小。
(3)写名称:先用大写数字“二、三……”在炔烃的名称前表示三键的个数;然后在“某
炔”前面用阿拉伯数字表示出三键的位置(用三键碳原子的最小编号表示),最后在前面写出
支链的名称、个数和位置。
1.下列说法正确的是 ( )
A.丙炔分子中三个碳原子不可能在同一直线上
B.乙炔分子中碳碳间的三个共价键性质完全相同
C.分子组成符合CH 的链烃一定是炔烃
n 2n-2
D.在所有符合通式CH 的炔烃中,乙炔所含氢元素的质量分数最小
n 2n-2
D [丙炔分子中存在类似乙炔分子的碳碳三键直线形结构,丙炔分子中的三个碳原子在
同一直线上,故A错误;乙炔分子中的碳碳三键是由1个σ键和2个π键构成的,其中σ键
稳定、π键不稳定,分子中碳碳间的三个共价键性质不完全相同,故B错误;分子组成符合CH
n 2n
的链烃,可能含有2个碳碳双键,为二烯烃,也可能含有1个碳碳三键,为炔烃,故C错误;符
-2
合通式CH 的炔烃中,1个碳原子结合的氢原子的平均数目为2-,n越大,2-的值越大,氢
n 2n-2
元素的质量分数越大,则乙炔所含氢元素的质量分数最小,故D正确。]
2.下列各选项能说明分子式为CH 的某烃是HC≡C—CH—CH ,而不是CH===CH—
4 6 2 3 2
CH===CH 的是( )
2
A.燃烧有浓烟
B.能使酸性KMnO 溶液褪色
4
C.能与溴发生1,2加成反应
D.与足量溴反应,生成物中只有2个碳原子上有溴原子
D [无论HC≡C—CH—CH 还是CH===CH—CH===CH,A、B、C项所述事实均能发生,而与足
2 3 2 2
6量 溴 加 成 后 , 前 者 产 物 为 , 后 者 产 物 为
,故D正确。]
3.下列有机物的系统命名法正确的一组是( )
C [A项,应该是4甲基2戊炔,错误;B项,该有机物的名称为3甲基1戊烯,错误;C项,根
据有机物的命名原则,该有机物为2甲基2,4己二烯,正确;D项,该有机物的名称为2,2,4三甲
基戊烷,错误。]
已知使用活性较低的林德拉催化剂[Pd/(PbO、CaCO)],可使炔烃的氢化停留在生成烯烃
3
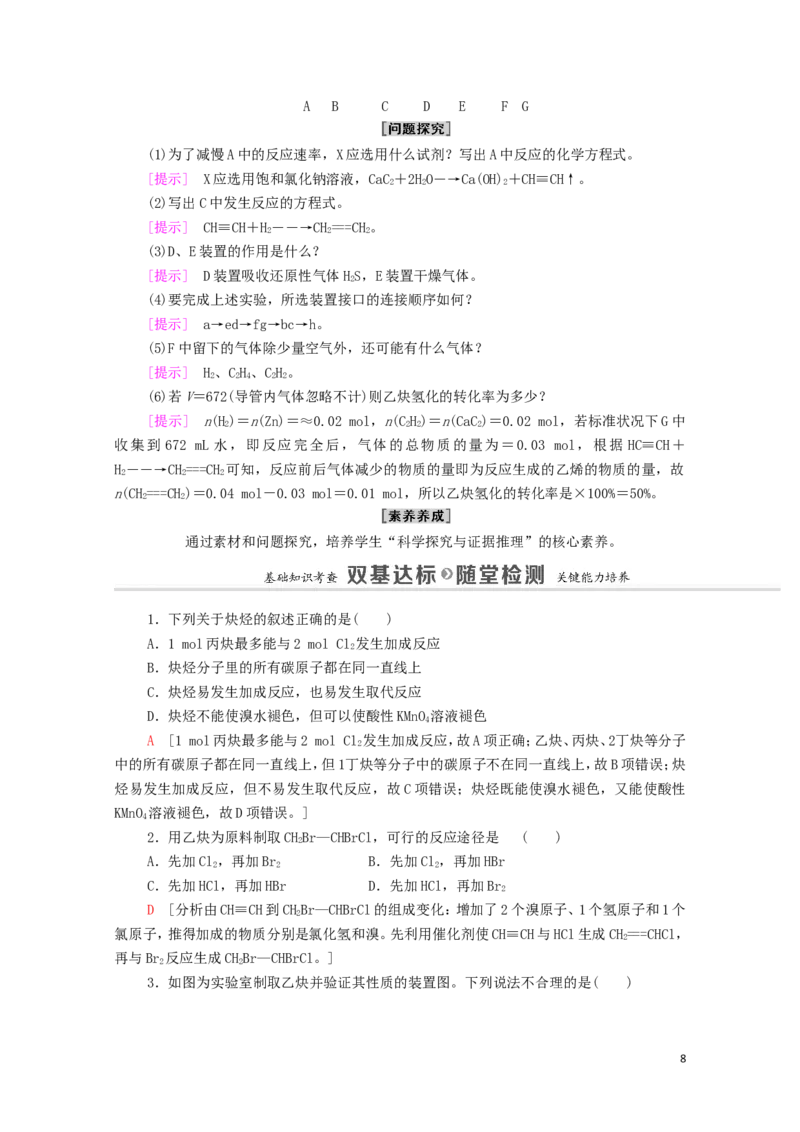
的阶段,而不再进一步氢化成烷烃。现有一课外活动兴趣小组利用上述原理设计了一套由如图
所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率
用含0.02 mol CaC 的电石和1.60 g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X
2
和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到V mL水。已知电石与HO反
2
应可能生成杂质气体HS。
2
7A B C D E F G
(1)为了减慢A中的反应速率,X应选用什么试剂?写出A中反应的化学方程式。
[提示] X应选用饱和氯化钠溶液,CaC+2HO―→Ca(OH)+CH≡CH↑。
2 2 2
(2)写出C中发生反应的方程式。
[提示] CH≡CH+H――→CH===CH。
2 2 2
(3)D、E装置的作用是什么?
[提示] D装置吸收还原性气体HS,E装置干燥气体。
2
(4)要完成上述实验,所选装置接口的连接顺序如何?
[提示] a→ed→fg→bc→h。
(5)F中留下的气体除少量空气外,还可能有什么气体?
[提示] H、CH、CH。
2 2 4 2 2
(6)若V=672(导管内气体忽略不计)则乙炔氢化的转化率为多少?
[提示] n(H)=n(Zn)=≈0.02 mol,n(CH)=n(CaC)=0.02 mol,若标准状况下G中
2 2 2 2
收集到 672 mL 水,即反应完全后,气体的总物质的量为=0.03 mol,根据 HC≡CH+
H――→CH===CH 可知,反应前后气体减少的物质的量即为反应生成的乙烯的物质的量,故
2 2 2
n(CH===CH)=0.04 mol-0.03 mol=0.01 mol,所以乙炔氢化的转化率是×100%=50%。
2 2
通过素材和问题探究,培养学生“科学探究与证据推理”的核心素养。
1.下列关于炔烃的叙述正确的是( )
A.1 mol丙炔最多能与2 mol Cl 发生加成反应
2
B.炔烃分子里的所有碳原子都在同一直线上
C.炔烃易发生加成反应,也易发生取代反应
D.炔烃不能使溴水褪色,但可以使酸性KMnO 溶液褪色
4
A [1 mol丙炔最多能与2 mol Cl 发生加成反应,故A项正确;乙炔、丙炔、2丁炔等分子
2
中的所有碳原子都在同一直线上,但1丁炔等分子中的碳原子不在同一直线上,故B项错误;炔
烃易发生加成反应,但不易发生取代反应,故C项错误;炔烃既能使溴水褪色,又能使酸性
KMnO 溶液褪色,故D项错误。]
4
2.用乙炔为原料制取CHBr—CHBrCl,可行的反应途径是 ( )
2
A.先加Cl,再加Br B.先加Cl,再加HBr
2 2 2
C.先加HCl,再加HBr D.先加HCl,再加Br
2
D [分析由CH≡CH到CHBr—CHBrCl的组成变化:增加了2个溴原子、1个氢原子和1个
2
氯原子,推得加成的物质分别是氯化氢和溴。先利用催化剂使CH≡CH与HCl生成CH===CHCl,
2
再与Br 反应生成CHBr—CHBrCl。]
2 2
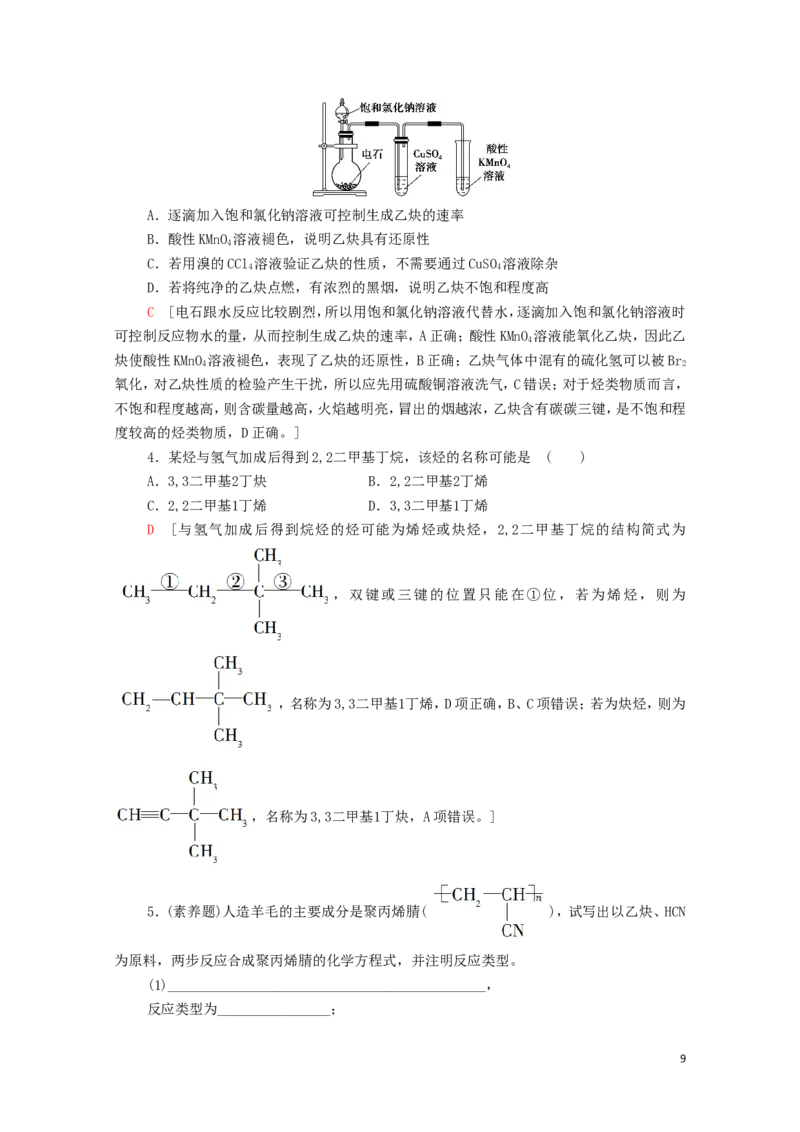
3.如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是( )
8A.逐滴加入饱和氯化钠溶液可控制生成乙炔的速率
B.酸性KMnO 溶液褪色,说明乙炔具有还原性
4
C.若用溴的CCl 溶液验证乙炔的性质,不需要通过CuSO 溶液除杂
4 4
D.若将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高
C [电石跟水反应比较剧烈,所以用饱和氯化钠溶液代替水,逐滴加入饱和氯化钠溶液时
可控制反应物水的量,从而控制生成乙炔的速率,A正确;酸性KMnO 溶液能氧化乙炔,因此乙
4
炔使酸性KMnO 溶液褪色,表现了乙炔的还原性,B正确;乙炔气体中混有的硫化氢可以被Br
4 2
氧化,对乙炔性质的检验产生干扰,所以应先用硫酸铜溶液洗气,C错误;对于烃类物质而言,
不饱和程度越高,则含碳量越高,火焰越明亮,冒出的烟越浓,乙炔含有碳碳三键,是不饱和程
度较高的烃类物质,D正确。]
4.某烃与氢气加成后得到2,2二甲基丁烷,该烃的名称可能是 ( )
A.3,3二甲基2丁炔 B.2,2二甲基2丁烯
C.2,2二甲基1丁烯 D.3,3二甲基1丁烯
D [与氢气加成后得到烷烃的烃可能为烯烃或炔烃,2,2二甲基丁烷的结构简式为
,双键或三键的位置只能在①位,若为烯烃,则为
,名称为3,3二甲基1丁烯,D项正确,B、C项错误;若为炔烃,则为
,名称为3,3二甲基1丁炔,A项错误。]
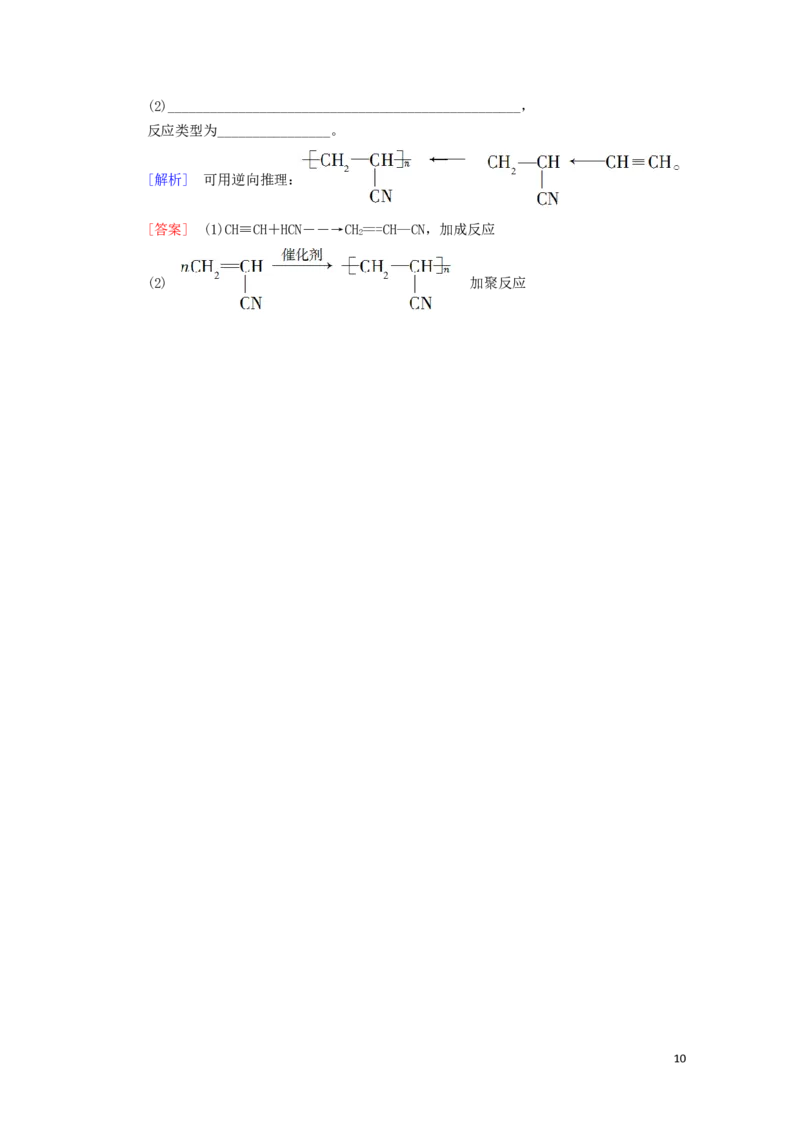
5.(素养题)人造羊毛的主要成分是聚丙烯腈( ),试写出以乙炔、HCN
为原料,两步反应合成聚丙烯腈的化学方程式,并注明反应类型。
(1)_____________________________________________,
反应类型为________________;
9(2)__________________________________________________,
反应类型为________________。
[解析] 可用逆向推理:
[答案] (1)CH≡CH+HCN――→CH===CH—CN,加成反应
2
(2) 加聚反应
10