文档内容
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
一.选择题
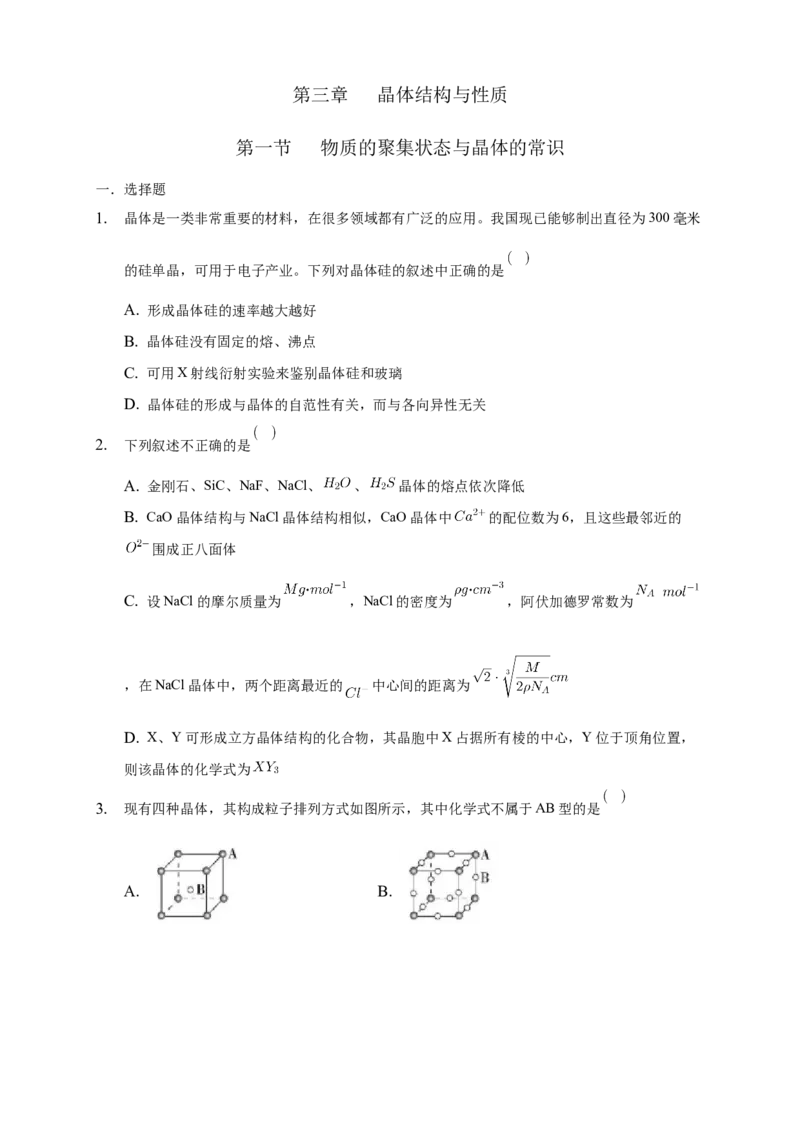
1. 晶体是一类非常重要的材料,在很多领域都有广泛的应用。我国现已能够制出直径为300毫米
的硅单晶,可用于电子产业。下列对晶体硅的叙述中正确的是
A. 形成晶体硅的速率越大越好
B. 晶体硅没有固定的熔、沸点
C. 可用X射线衍射实验来鉴别晶体硅和玻璃
D. 晶体硅的形成与晶体的自范性有关,而与各向异性无关
2. 下列叙述不正确的是
A. 金刚石、SiC、NaF、NaCl、 、 晶体的熔点依次降低
B. CaO 晶体结构与NaCl晶体结构相似,CaO 晶体中 的配位数为6,且这些最邻近的
围成正八面体
C. 设NaCl 的摩尔质量为 ,NaCl的密度为 ,阿伏加德罗常数为
,在NaCl 晶体中,两个距离最近的 中心间的距离为
D. X、Y 可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y 位于顶角位置,
则该晶体的化学式为
3. 现有四种晶体,其构成粒子排列方式如图所示,其中化学式不属于AB型的是
A. B.C. D.
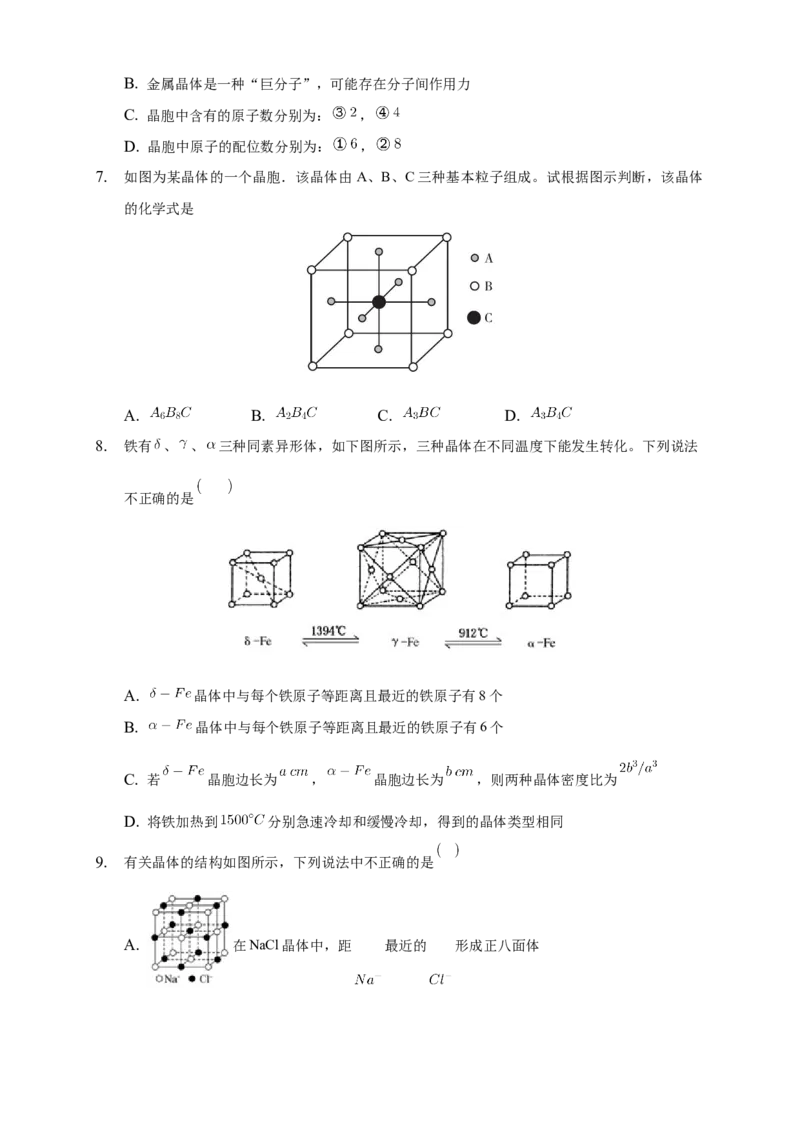
4. 如图是氯化铯晶体的晶胞结构示意图 晶胞是指晶体中最小的重复单元 ,其
中黑球表示氯离子、白球表示铯离子。已知晶体中2个最近的铯离子的核间距
离为 ,氯化铯的摩尔质量为 ,设 为阿伏加德罗常数的值,则氯化铯晶体的
密度为
A. B. C. D.
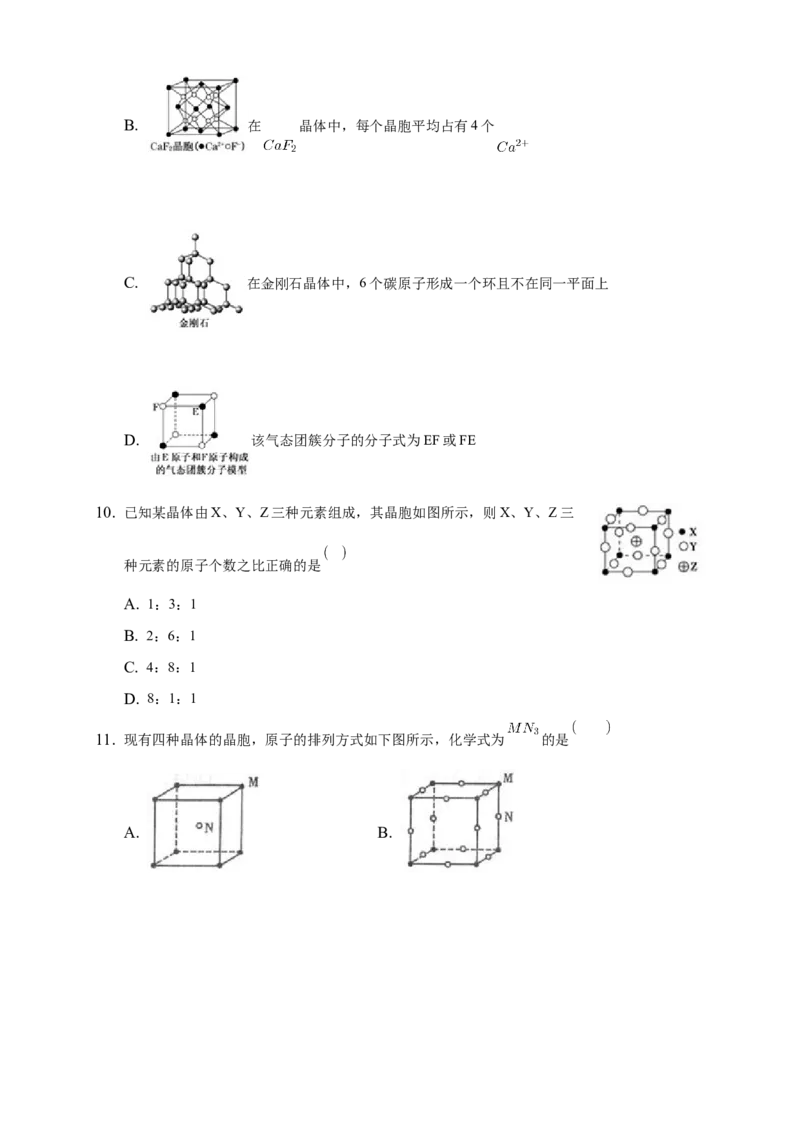
5. 下图所示是晶体结构中具有代表性的最小重复单元 晶胞 的排列方式,其对应的化学式正确
的是 图中: , , 。C选项中Y原子在面上
A. B.
C. D. XYZ
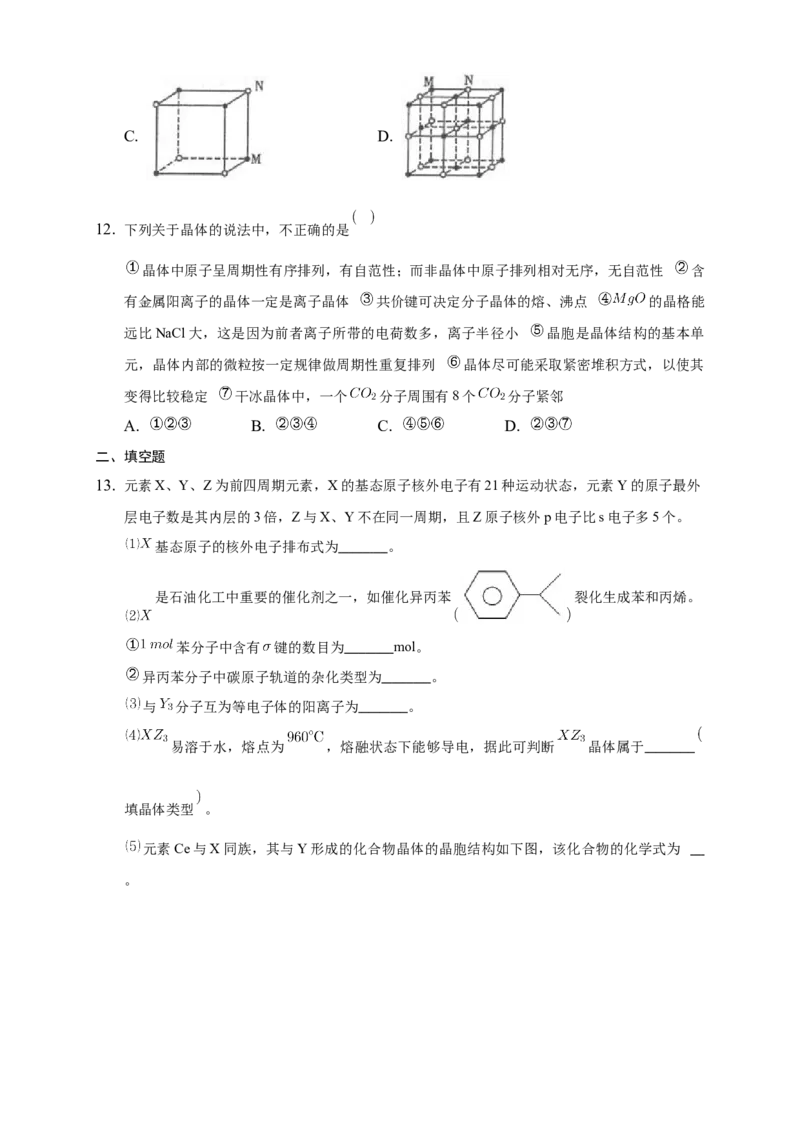
6. 有四种不同堆积方式的金属晶体的晶胞如图所示 原子半径为 ,下列叙述错误的是
A. 晶胞 的空间利用率:B. 金属晶体是一种“巨分子”,可能存在分子间作用力
C. 晶胞中含有的原子数分别为: ,
D. 晶胞中原子的配位数分别为: ,
7. 如图为某晶体的一个晶胞.该晶体由 A、B、C三种基本粒子组成。试根据图示判断,该晶体
的化学式是
A. B. C. D.
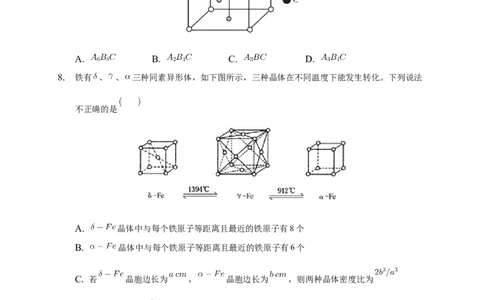
8. 铁有 、 、 三种同素异形体,如下图所示,三种晶体在不同温度下能发生转化。下列说法
不正确的是
A. 晶体中与每个铁原子等距离且最近的铁原子有8个
B. 晶体中与每个铁原子等距离且最近的铁原子有6个
C. 若 晶胞边长为 , 晶胞边长为 ,则两种晶体密度比为
D. 将铁加热到 分别急速冷却和缓慢冷却,得到的晶体类型相同
9. 有关晶体的结构如图所示,下列说法中不正确的是
A. 在NaCl晶体中,距 最近的 形成正八面体B. 在 晶体中,每个晶胞平均占有4个
C. 在金刚石晶体中,6个碳原子形成一个环且不在同一平面上
D. 该气态团簇分子的分子式为EF或FE
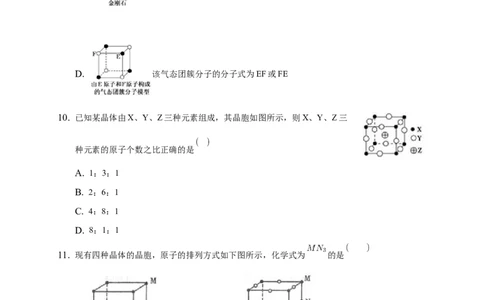
10. 已知某晶体由X、Y、Z三种元素组成,其晶胞如图所示,则X、Y、Z三
种元素的原子个数之比正确的是
A. 1:3:1
B. 2:6:1
C. 4:8:1
D. 8:1:1
11. 现有四种晶体的晶胞,原子的排列方式如下图所示,化学式为 的是
A. B.C. D.
12. 下列关于晶体的说法中,不正确的是
晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性 含
有金属阳离子的晶体一定是离子晶体 共价键可决定分子晶体的熔、沸点 的晶格能
远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小 晶胞是晶体结构的基本单
元,晶体内部的微粒按一定规律做周期性重复排列 晶体尽可能采取紧密堆积方式,以使其
变得比较稳定 干冰晶体中,一个 分子周围有8个 分子紧邻
A. B. C. D.
二、填空题
13. 元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外
层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
基态原子的核外电子排布式为 。
是石油化工中重要的催化剂之一,如催化异丙苯 裂化生成苯和丙烯。
苯分子中含有 键的数目为 mol。
异丙苯分子中碳原子轨道的杂化类型为 。
与 分子互为等电子体的阳离子为 。
易溶于水,熔点为 ,熔融状态下能够导电,据此可判断 晶体属于
填晶体类型 。
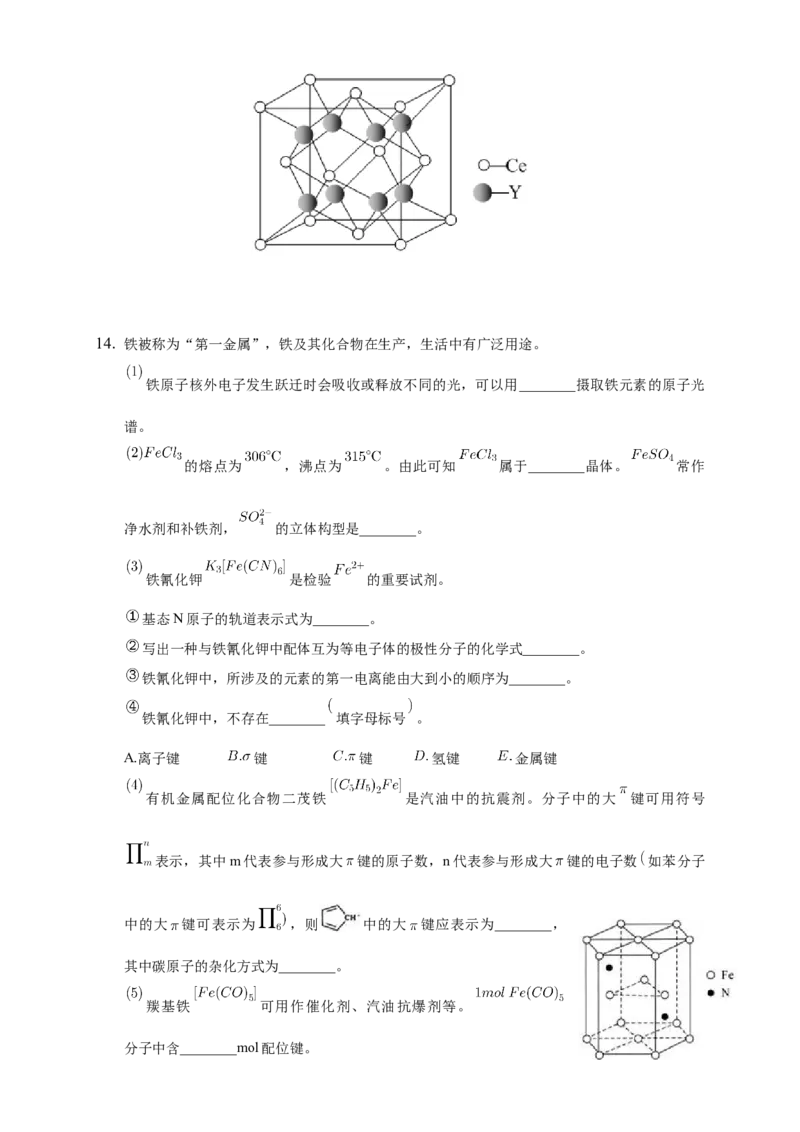
元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为
。14. 铁被称为“第一金属”,铁及其化合物在生产,生活中有广泛用途。
铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用________摄取铁元素的原子光
谱。
的熔点为 ,沸点为 。由此可知 属于________晶体。 常作
净水剂和补铁剂, 的立体构型是________。
铁氰化钾 是检验 的重要试剂。
基态N原子的轨道表示式为________。
写出一种与铁氰化钾中配体互为等电子体的极性分子的化学式________。
铁氰化钾中,所涉及的元素的第一电离能由大到小的顺序为________。
铁氰化钾中,不存在________ 填字母标号 。
A.离子键 键 键 氢键 金属键
有机金属配位化合物二茂铁 是汽油中的抗震剂。分子中的大 键可用符号
表示,其中m代表参与形成大 键的原子数,n代表参与形成大 键的电子数 如苯分子
中的大 键可表示为 ,则 中的大 键应表示为________,
其中碳原子的杂化方式为________。
羰基铁 可用作催化剂、汽油抗爆剂等。
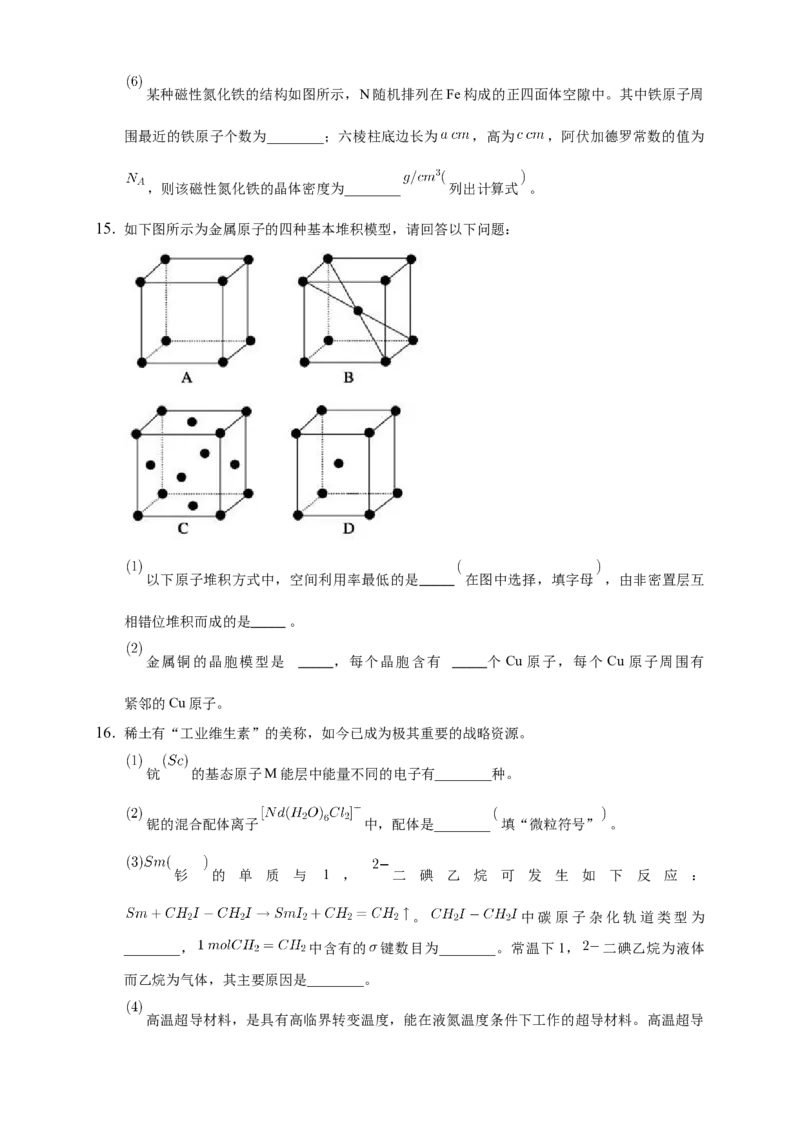
分子中含________mol配位键。某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四面体空隙中。其中铁原子周
围最近的铁原子个数为________;六棱柱底边长为 ,高为 ,阿伏加德罗常数的值为
,则该磁性氮化铁的晶体密度为________ 列出计算式 。
15. 如下图所示为金属原子的四种基本堆积模型,请回答以下问题:
以下原子堆积方式中,空间利用率最低的是 在图中选择,填字母 ,由非密置层互
相错位堆积而成的是 。
金属铜的晶胞模型是 ,每个晶胞含有 个 Cu 原子,每个 Cu 原子周围有
紧邻的Cu原子。
16. 稀土有“工业维生素”的美称,如今已成为极其重要的战略资源。
钪 的基态原子M能层中能量不同的电子有________种。
铌的混合配体离子 中,配体是________ 填“微粒符号” 。
钐 的 单 质 与 1 , 二 碘 乙 烷 可 发 生 如 下 反 应 :
。 中碳原子杂化轨道类型为
________, 中含有的 键数目为________。常温下1, 二碘乙烷为液体
而乙烷为气体,其主要原因是________。
高温超导材料,是具有高临界转变温度,能在液氮温度条件下工作的超导材料。高温超导材料镧钡铜氧化物中含有 。基态时 的电子排布式为________。化合物中,稀土元素
最常见的化合价是 ,但也有少数的稀土元素可以显 价。下面四种稀土元素的电离能 单
位: 数据如下表,判断最有可能显 价的稀土元素是________ 填元素符号 。
元素
钪 633 1235 2389 7019
铱 616 1181 1980 5963
镧 538 1067 1850 4819
铈 527 1047 1949 3547
二氧化镨 的晶体结构与 相似,则 二氧化镨 的晶胞中Pr原子的配位数
为________。O原子与Pr原子配位数不同,影响这一结果的是离子晶体的________ 填“几
何”“电荷”或“键性” 因素。
掺杂稀土的硼化镁在 时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分
层排布的,一层镁一层硼相间排列。图1是该晶体微观结构中取出的部分原子沿z轴方向的投
影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为________。
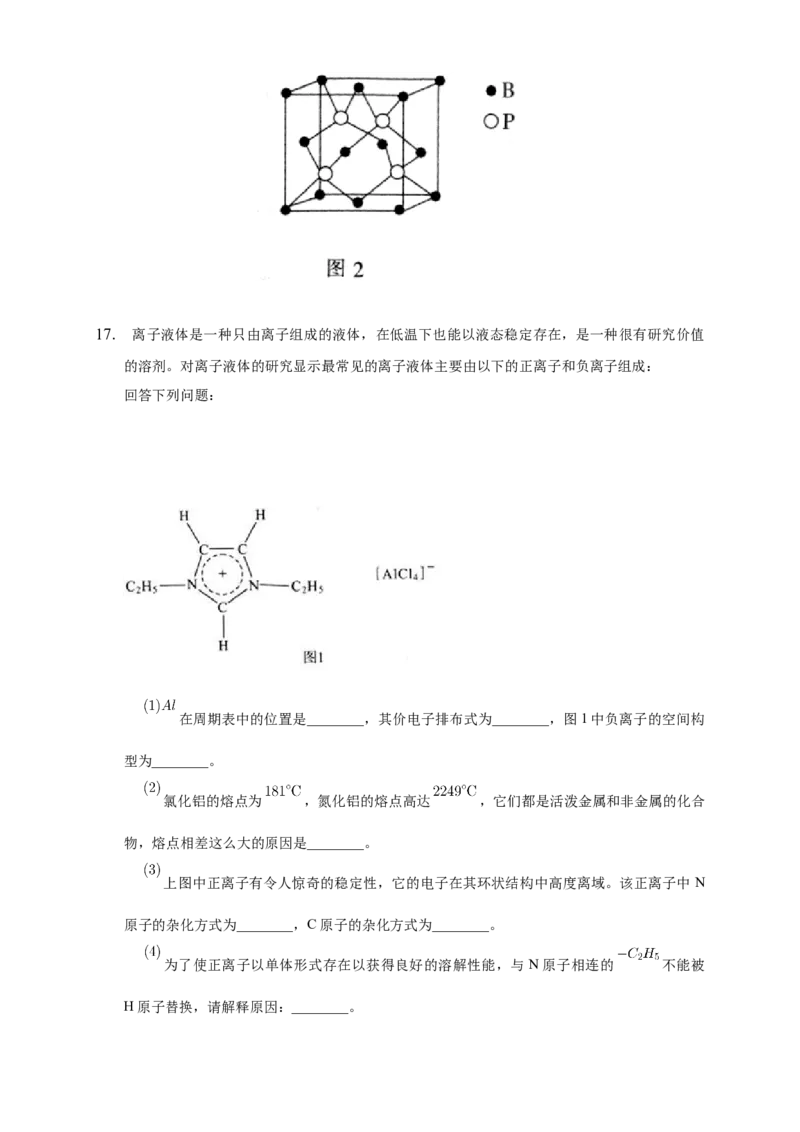
磷化硼 是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄
膜。磷化硼晶胞如图2所示,在BP晶胞中B的堆积方式为________,当晶胞晶格参数为
时,磷化硼中硼原子和磷原子之间的最近距离为________cm。17. 离子液体是一种只由离子组成的液体,在低温下也能以液态稳定存在,是一种很有研究价值
的溶剂。对离子液体的研究显示最常见的离子液体主要由以下的正离子和负离子组成:
回答下列问题:
在周期表中的位置是________,其价电子排布式为________,图1中负离子的空间构
型为________。
氯化铝的熔点为 ,氮化铝的熔点高达 ,它们都是活泼金属和非金属的化合
物,熔点相差这么大的原因是________。
上图中正离子有令人惊奇的稳定性,它的电子在其环状结构中高度离域。该正离子中 N
原子的杂化方式为________,C原子的杂化方式为________。
为了使正离子以单体形式存在以获得良好的溶解性能,与 N原子相连的 不能被
H原子替换,请解释原因:________。、Mg、Al三种元素的第一电离能由大到小的顺序是________。
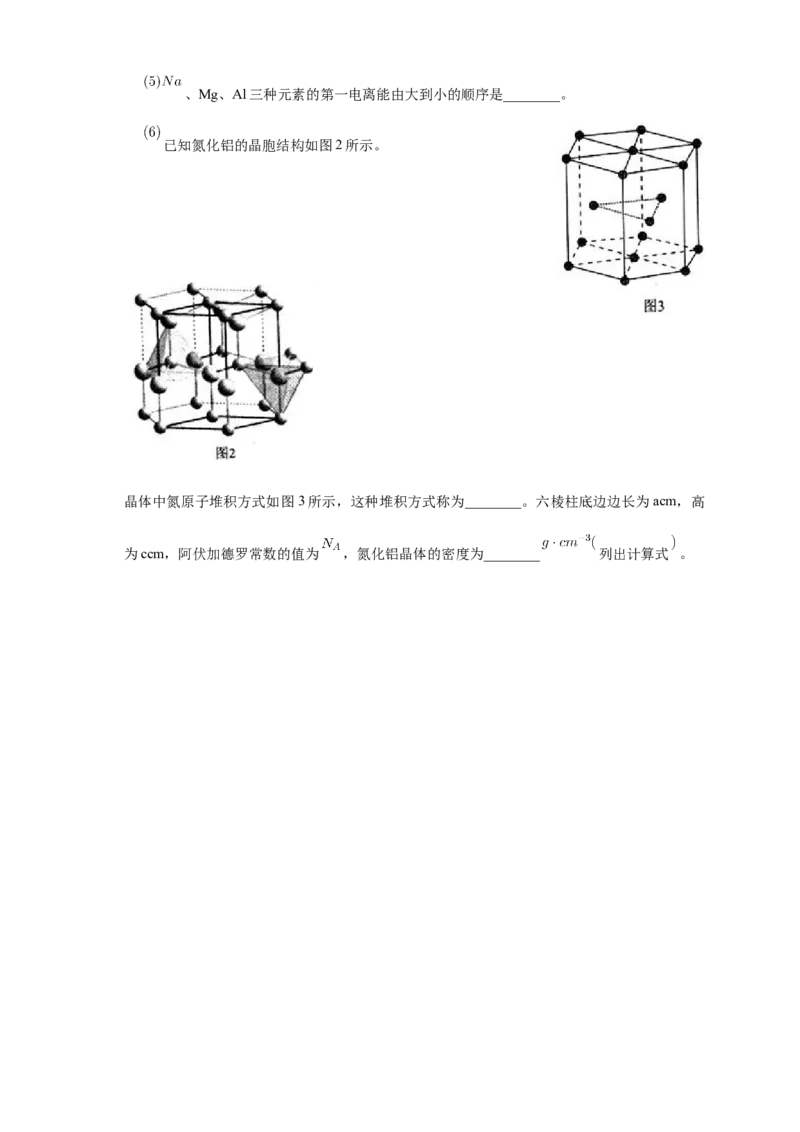
已知氮化铝的晶胞结构如图2所示。
晶体中氮原子堆积方式如图3所示,这种堆积方式称为________。六棱柱底边边长为acm,高
为ccm,阿伏加德罗常数的值为 ,氮化铝晶体的密度为________ 列出计算式 。