文档内容
3.2.1 分子晶体(分层作业)
1.下列各组晶体都属于化合物组成的分子晶体是
A.HO、O、CCl B.CCl 、NH Cl、HO
2 3 4 4 4 2 2
C.SO 、SiO、CS D.PO、CO、HPO
2 2 2 2 5 2 3 4
【答案】D
【解析】A.O 是单质不是化合物,A错误;
3
B.NH Cl晶体是离子晶体不是分子晶体,B错误;
4
C.SiO 晶体是共价晶体不是分子晶体,C错误;
2
D. PO、CO、HPO 均为化合物,且都是共价分子,它们的晶体均是分子晶体,D正确;
2 5 2 3 4
答案选D。
2.下列物质中属于分子晶体,而且既含δ键又含π键的是
A.NaCN B.CS C.HO D.Ca(OH)
2 2 2 2
【答案】B
【解析】A.NaCN是由阴阳离子组成的离子晶体,不符合题意,A错误;
B.CS 是分子晶体,结构与二氧化碳相似,碳原子与硫原子间形成碳硫双键,故既含δ键又含π键,符合题意,
2
B正确;
C.HO 是分子晶体,但原子间均由单键相连,只含δ键而不含π键,不符合题意,C错误;
2 2
D.Ca(OH) 是由阴阳离子组成的离子晶体,不符合题意,D错误;
2
故选B。
3.下列有关分子晶体结构特点的说法中正确的是
A.分子晶体在常温下都是气态
B.分子晶体中都存在化学键
C.分子晶体中分子间的作用力主要是范德华力
D.分子间一定存在氢键
【答案】C
【解析】A.分子晶体常温下不全为气态,如磷常温下是晶体,故A错误;
B.稀有气体元素组成的晶体中,不存在由多个原子组成的分子,而是原子间通过范德华力结合成晶体,所以
不存在任何化学键,故B错误;
C.分子晶体中分子间的作用力包括范德华力和氢键,但主要是范德华力,故C正确;
D.分子间作用力包括范德华力和氢键,而氢键只存在于含有与电负性较强的N、O、F原子结合的氢原子的分
子之间或者分子内,故D错误,
答案选C。4.下列关于物质性质的说法,不正确的是
A.I 晶体升华时破坏了分子内共价键
2
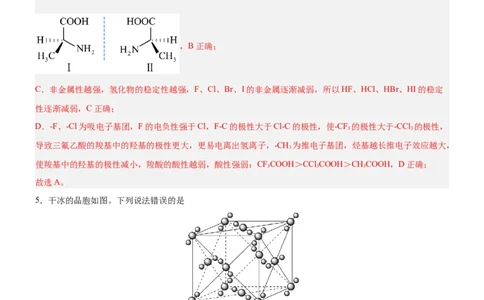
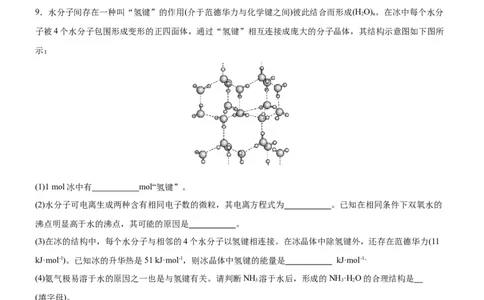
B.丙氨酸(CHCH(NH)COOH)分子是手性分子
3 2
C.HF、HCl、HBr、HI的稳定性依次减弱
D.酸性:CFCOOH>CCl COOH>CH COOH
3 3 3
【答案】A
【解析】A.碘是分子晶体,升华时只会破坏分子间作用力,不会破坏共价键,A错误;
B.丙氨酸[CHCH(NH)COOH]分子为手性分子,它存在对映异构,如图所示:
3 2
,B正确;
C.非金属性越强,氢化物的稳定性越强,F、Cl、Br、I的非金属逐渐减弱,所以HF、HCl、HBr、HI的稳定
性逐渐减弱,C正确;
D.-F、-Cl为吸电子基团,F的电负性强于Cl,F-C的极性大于Cl-C的极性,使-CF 的极性大于-CCl 的极性,
3 3
导致三氟乙酸的羧基中的羟基的极性更大,更易电离出氢离子,-CH 为推电子基团,烃基越长推电子效应越大,
3
使羧基中的羟基的极性减小,羧酸的酸性越弱,酸性强弱:CFCOOH>CCl COOH>CHCOOH,D正确;
3 3 3
故选A。
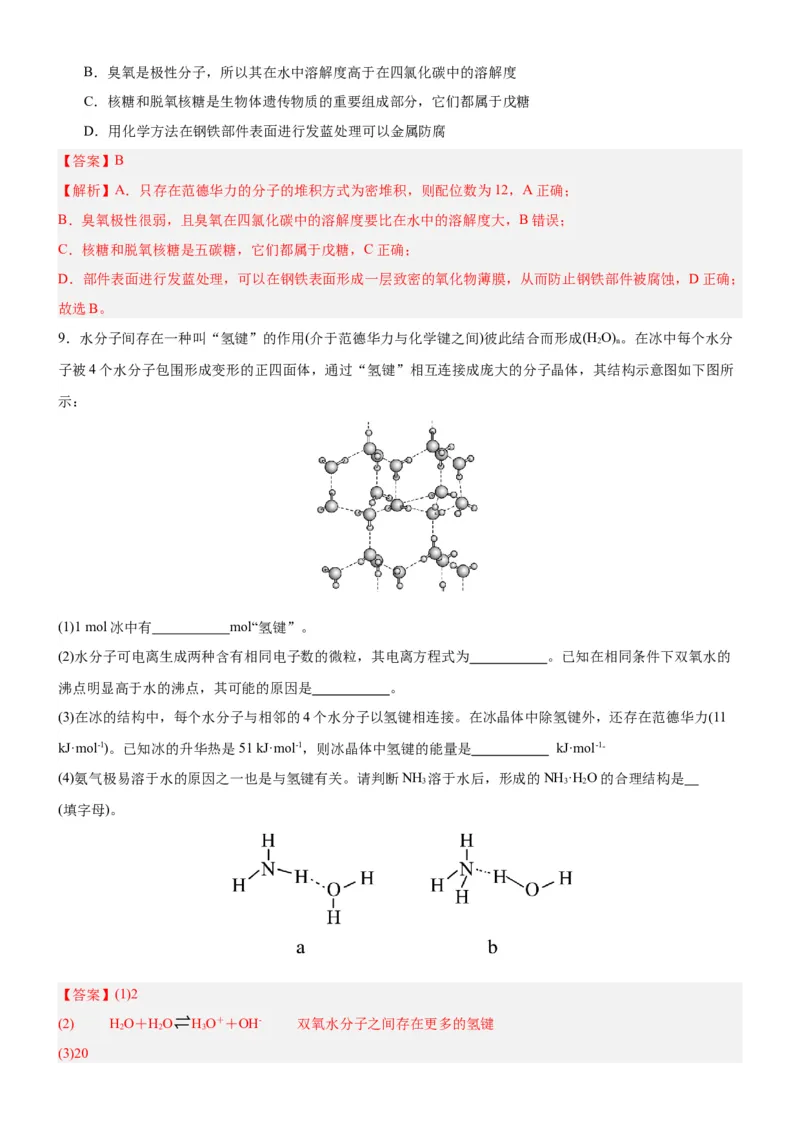
5.干冰的晶胞如图。下列说法错误的是
A.C元素和O元素均位于元素周期表P区
B.每个晶胞中CO 分子数目为4
2
C.该晶体属于分子晶体
D.每个CO 分子周围紧邻等距的CO 分子数为4
2 2
【答案】D
【解析】A.C元素和O元素均位于元素周期表P区,A项正确;
1 1
B.每个晶胞中CO 分子数目为8× +6× =4,B项正确;
2 8 2C.干冰属于分子晶体,C项正确;
D.由晶胞结构可知,每个CO 分子周围紧邻等距的CO 分子数为12,D项错误;
2 2
故选D。
6.某晶体的晶胞结构如图所示,黑球、白球均为C 分子。下列说法正确的是
60
A.C 的配位数为6 B.该晶体属于共价晶体
60
C.其硬度决定于共价键 D.1个晶胞中含有240个碳原子
【答案】D
【解析】A.以晶胞顶点的C 分子为例,这个晶胞中周围距离最近的C 分子有位于面心的3个C 分子,通过
60 60 60
此顶点C 分子的晶胞有8个,而每个面心的C 分子被重复了2次,所以每个C 分子周围距离最近且相等的
60 60 60
3×8
C 有 =12个,C 的配位数为12,A错误;
60 2 60
B.该晶体由C 分子组成,属于分子晶体,B错误;
60
C.该晶体属于分子晶体,其硬度决定于分子间作用力,C错误;
1 1
D.1个晶胞中含有8× +6× =4个C 分子,则含240个碳原子,D正确;
8 2 60
故选D。
7.邻苯二胺的结构简式为 ,下刻说法错误的是
A.邻苯二胺属于分子晶体 B.邻苯二胺中C、N的杂化方式均为
C.邻苯二胺组成元素中电负性最大的是N D.邻苯二胺比对苯二胺的熔点低
【答案】B
【解析】A.邻苯二胺是共价化合物,其晶体由分子通过分子间作用力形成的晶体,故属于分子晶体,A正确;
B.邻苯二胺中C周围的价层电子对数为3,其杂化方式为sp2、而N周围的价层电子对数为4,则其杂化方式
为sp3,B错误;
C.电负性:N>C>H,电负性最大的是N,C正确;
D.邻苯二胺易形成分子内氢键,对苯二胺易形成分子间氢键,故邻苯二胺比对苯二胺的熔点低,D正确;
故答案为:B。
8.下列说法不正确的是
A.只存在范德华力的分子,以一个分子为中心,其周围最多可以有12个紧邻的分子B.臭氧是极性分子,所以其在水中溶解度高于在四氯化碳中的溶解度
C.核糖和脱氧核糖是生物体遗传物质的重要组成部分,它们都属于戊糖
D.用化学方法在钢铁部件表面进行发蓝处理可以金属防腐
【答案】B
【解析】A.只存在范德华力的分子的堆积方式为密堆积,则配位数为12,A正确;
B.臭氧极性很弱,且臭氧在四氯化碳中的溶解度要比在水中的溶解度大,B错误;
C.核糖和脱氧核糖是五碳糖,它们都属于戊糖,C正确;
D.部件表面进行发蓝处理,可以在钢铁表面形成一层致密的氧化物薄膜,从而防止钢铁部件被腐蚀,D正确;
故选B。
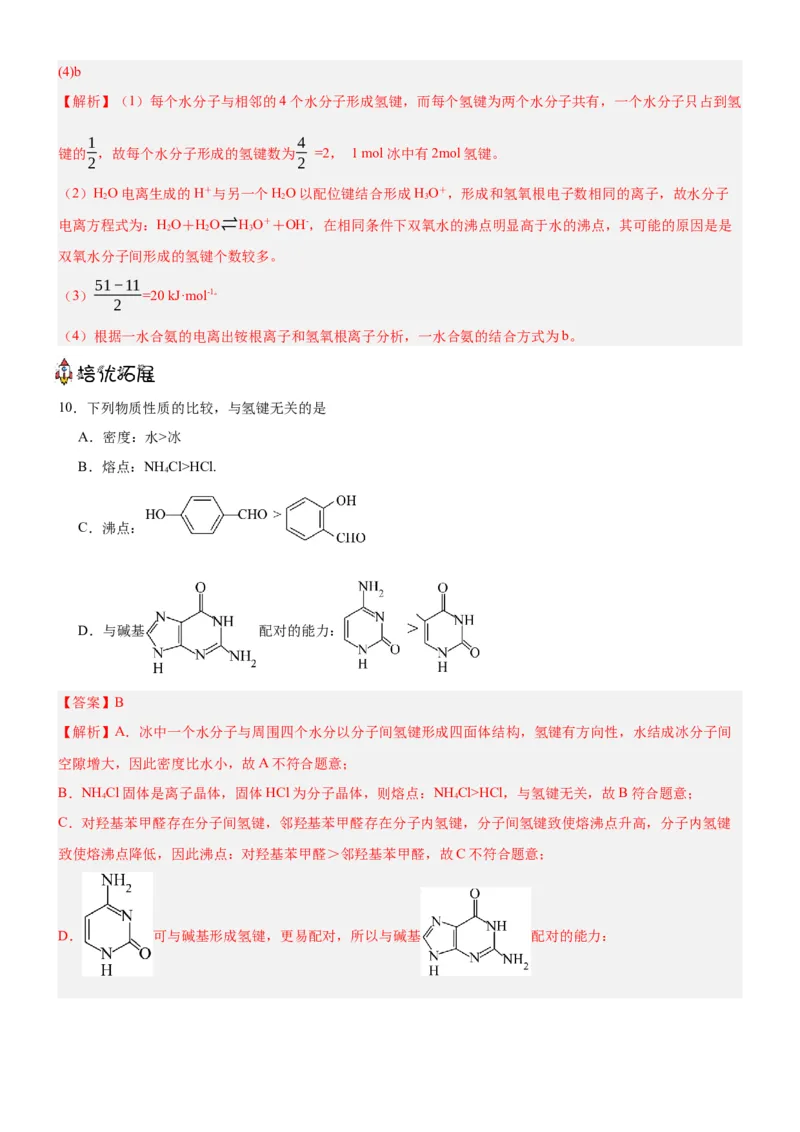
9.水分子间存在一种叫“氢键”的作用(介于范德华力与化学键之间)彼此结合而形成(H O) 。在冰中每个水分
2 n
子被4个水分子包围形成变形的正四面体,通过“氢键”相互连接成庞大的分子晶体,其结构示意图如下图所
示:
(1)1 mol冰中有 mol“氢键”。
(2)水分子可电离生成两种含有相同电子数的微粒,其电离方程式为 。已知在相同条件下双氧水的
沸点明显高于水的沸点,其可能的原因是 。
(3)在冰的结构中,每个水分子与相邻的4个水分子以氢键相连接。在冰晶体中除氢键外,还存在范德华力(11
kJ·mol-1)。已知冰的升华热是51 kJ·mol-1,则冰晶体中氢键的能量是 kJ·mol-1。
(4)氨气极易溶于水的原因之一也是与氢键有关。请判断NH 溶于水后,形成的NH ·H O的合理结构是
3 3 2
(填字母)。
【答案】(1)2
(2) H O+HO⇌HO++OH- 双氧水分子之间存在更多的氢键
2 2 3
(3)20(4)b
【解析】(1)每个水分子与相邻的4个水分子形成氢键,而每个氢键为两个水分子共有,一个水分子只占到氢
1 4
键的 ,故每个水分子形成的氢键数为 =2, 1 mol冰中有2mol氢键。
2 2
(2)HO电离生成的H+与另一个HO以配位键结合形成HO+,形成和氢氧根电子数相同的离子,故水分子
2 2 3
电离方程式为:HO+HO⇌HO++OH-,在相同条件下双氧水的沸点明显高于水的沸点,其可能的原因是是
2 2 3
双氧水分子间形成的氢键个数较多。
51−11
(3) =20 kJ·mol-1。
2
(4)根据一水合氨的电离出铵根离子和氢氧根离子分析,一水合氨的结合方式为b。
10.下列物质性质的比较,与氢键无关的是
A.密度:水>冰
B.熔点:NH Cl>HCl.
4
C.沸点:
D.与碱基 配对的能力:
【答案】B
【解析】A.冰中一个水分子与周围四个水分以分子间氢键形成四面体结构,氢键有方向性,水结成冰分子间
空隙增大,因此密度比水小,故A不符合题意;
B.NH Cl固体是离子晶体,固体HCl为分子晶体,则熔点:NH Cl>HCl,与氢键无关,故B符合题意;
4 4
C.对羟基苯甲醛存在分子间氢键,邻羟基苯甲醛存在分子内氢键,分子间氢键致使熔沸点升高,分子内氢键
致使熔沸点降低,因此沸点:对羟基苯甲醛>邻羟基苯甲醛,故C不符合题意;
D. 可与碱基形成氢键,更易配对,所以与碱基 配对的能力:,故D不符合题意;
故选B。
11.下列对物质性质解释合理的是
选项 性质 解释
A 酸性:F-CH -COOH>Cl-CH -COOH 电负性:F>Cl
2 2
B 熔点:晶体硅<碳化硅 碳化硅中分子间作用力较大
C 热稳定性:HF(g)>HCl(g) HF中存在氢键
D 熔点:Br H O>NH B.热稳定性:
3 2 3
C.沸点:HF>H O>NH D.第一电离能:P>S>Si
2 3
【答案】D
【解析】A.BF 中B价层电子对数为3,无孤电子对,为平面三角形,HO中O的价层电子对数4,有2个孤
3 2
电子对,NH 中N的价层电子对数为4,有1个孤电子对,孤电子对数越多,斥力越大,键角越小,键角大小
3
顺序是BF>NH >HO,故A错误;
3 3 2
B.非金属性越强,其简单氢化物稳定性越强,非金属性:O>N>C,则热稳定:HO>NH >CH,故B错误;
2 3 4
C.常温下水为液体,其余为气体,三种物质,水的沸点最大,故C错误;
D.同周期从左向右第一电离能逐渐增大,但ⅤA>ⅥA,因此第一电离能大小顺序是P>S>Si,故D正确;
答案为D。
15.下列说法正确的是A.如图碘晶胞中 分子的排列有4种不同取向
B.沸点:对二甲苯>间二甲苯>邻二甲苯
C.缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的晶体
D.能层、能级和轨道可以描述一个电子的运动状态
【答案】C
【解析】A.碘晶胞中,I 分子在顶点和面心的取向不同,I 分子有2种不同取向,故A错误;
2 2
B.苯的同系物中,整个分子的对称性越好其沸点越低,所以沸点:邻二甲苯>间二甲苯>对二甲苯沸点,故B
错误;
C.晶体具有自范性,缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的晶体,故C正确;
D.用能层、能级、轨道、自旋状态描述一个电子的运动状态,故D错误;
选C。
16.下列说法中正确的是
A.冰融化时,分子中H—O发生断裂
B.分子晶体熔融时化学键不被破坏
C.分子晶体中,一定存在分子间作用力和共价键
D.分子晶体中,分子间作用力越大,该物质越稳定
【答案】B
【解析】A.冰为分子晶体,熔化时破坏的是分子间作用力,A项错误;
B.分子晶体是通过分子间作用力将分子结合在一起的,所以熔化时,分子内部的化学键未发生变化,破坏的
只是分子间作用力,B项正确;
C.稀有气体在固态时也属于分子晶体,而稀有气体是单原子分子,在分子内部不存在共价键,C项错误;
D.分子晶体熔沸点高低取决于分子间作用力大小,而共价键强弱决定了分子的稳定性强弱,D项错误;
答案选B。
17.填空。
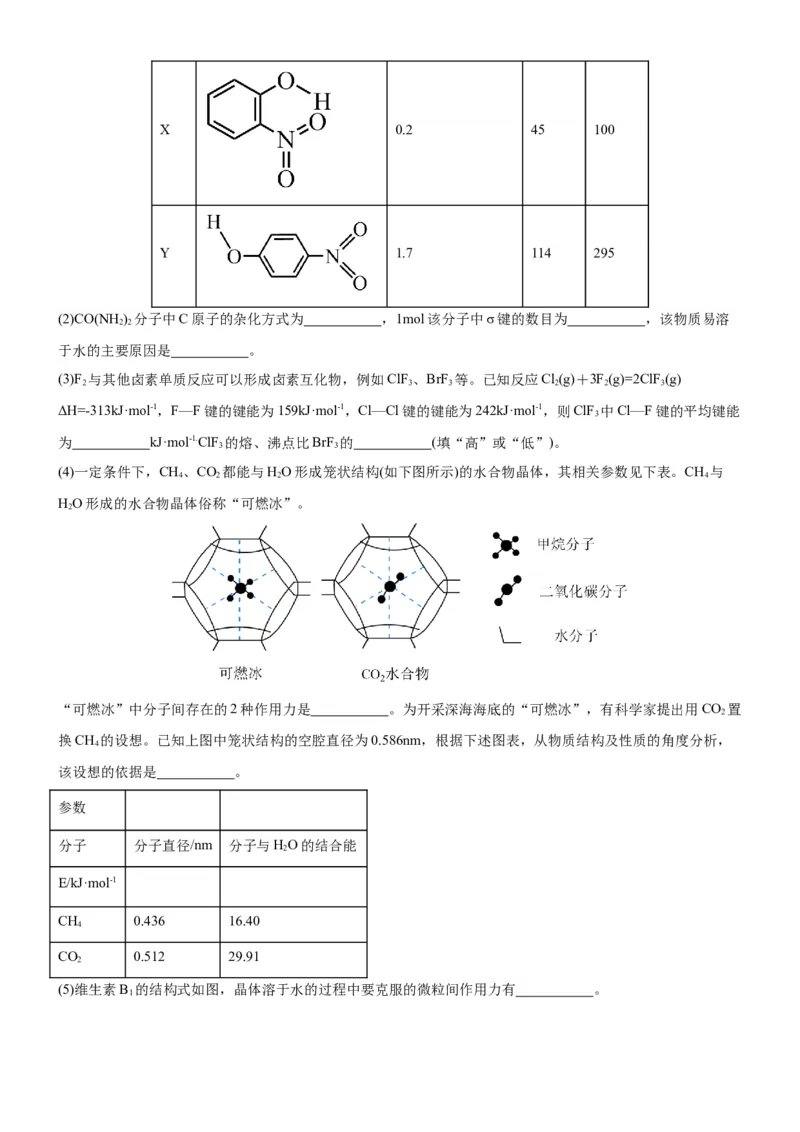
(1)X、Y两者物理性质有差异的主要原因是 。
代
结构简式 水中溶解度/g(25℃) 熔点/℃ 沸点/℃
号X 0.2 45 100
Y 1.7 114 295
(2)CO(NH) 分子中C原子的杂化方式为 ,1mol该分子中σ键的数目为 ,该物质易溶
2 2
于水的主要原因是 。
(3)F 与其他卤素单质反应可以形成卤素互化物,例如ClF 、BrF 等。已知反应Cl(g)+3F(g)=2ClF (g)
2 3 3 2 2 3
ΔH=-313kJ·mol-1,F—F键的键能为159kJ·mol-1,Cl—Cl键的键能为242kJ·mol-1,则ClF 中Cl—F键的平均键能
3
为 kJ·mol-1.ClF 的熔、沸点比BrF 的 (填“高”或“低”)。
3 3
(4)一定条件下,CH、CO 都能与HO形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH 与
4 2 2 4
HO形成的水合物晶体俗称“可燃冰”。
2
“可燃冰”中分子间存在的2种作用力是 。为开采深海海底的“可燃冰”,有科学家提出用CO 置
2
换CH 的设想。已知上图中笼状结构的空腔直径为0.586nm,根据下述图表,从物质结构及性质的角度分析,
4
该设想的依据是 。
参数
分子 分子直径/nm 分子与HO的结合能
2
E/kJ·mol-1
CH 0.436 16.40
4
CO 0.512 29.91
2
(5)维生素B 的结构式如图,晶体溶于水的过程中要克服的微粒间作用力有 。
1【答案】(1)X物质形成分子内氢键,Y物质形成分子间氢键,分子间氢键使分子间作用力增大
(2) sp2 7N CO(NH ) 分子与水分子之间能形成氢键
A 2 2
(3) 172 低
(4) 氢键、范德华力 CO 的分子直径小于笼状结构空腔直径,且与HO的结合能大于CH
2 2 4
(5)离子键、氢键、范德华力
【解析】(1)X、Y两者物理性质有差异的主要原因是X物质形成分子内氢键在水中溶解度低,溶沸点低,Y
物质与水形成分子间氢键水中溶解度高,分子间氢键使分子间作用力增大,溶沸点高,答案为:X物质形成分
子内氢键,Y物质形成分子间氢键,分子间氢键使分子间作用力增大;
(2)CO(NH) 分子的结构简式为: C原子周围3个价层电子对,杂化方式为sp2,1个分
2 2
子中σ键的数目是7个,所以1mol该分子中σ键的数目为7N ,该物质易溶于水的主要原因是CO(NH) 分子与
A 2 2
水分子之间能形成氢键,答案为:sp2,7N ,CO(NH) 分子与水分子之间能形成氢键;
A 2 2
(3)设Cl—F键的平均键能为XkJ·mol-1,根据反应的焓变=反应物的键能总和-生成物的键能总和可知,
VH=242KJ·mol-1+3×159KJ·mol-1-6XJK·mol-1=-313JK·mol-1,解得:X=172JK·mol,ClF 和 BrF 为结构相似的分
3 3
子晶体,相对分子质量越大,其熔、沸点越高,因ClF 相对分子质量小于和BrF,故ClF 熔、沸点低于BrF,
3 3 3 3
答案为:172,低;
(4)“可燃冰”中分子间存在的2种作用力是氢键、范德华力,科学家提出用CO 置换CH 的设想依据是:
2 4
CO 的分子直径小于笼状结构空腔直径,且与HO的结合能大于CH,答案为:氢键、范德华力,CO 的分子
2 2 4 2
直径小于笼状结构空腔直径,且与HO的结合能大于CH;
2 4
(5)维生素B 的结构中存在离子键、氢键、范德华力和共价键,晶体溶于水的过程中要克服的微粒间作用力
1
有:离子键、氢键、范德华力,答案为:离子键、氢键、范德华力。