文档内容
第三章 晶体结构与性质
第二节 分子晶体与共价晶体
第二课时 共价晶体
一.选择题
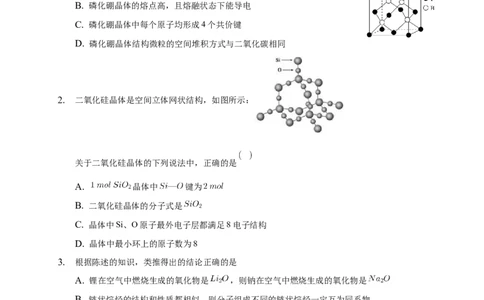
1. 磷化硼是一种超硬耐磨涂层材料。如图为其晶体结构中最小的重复结构单元,其中的每个原子
均满足8电子稳定结构。下列有关说法正确的是
A. 磷化硼晶体的化学式为BP,属于分子晶体
B. 磷化硼晶体的熔点高,且熔融状态下能导电
C. 磷化硼晶体中每个原子均形成4个共价键
D. 磷化硼晶体结构微粒的空间堆积方式与二氧化碳相同
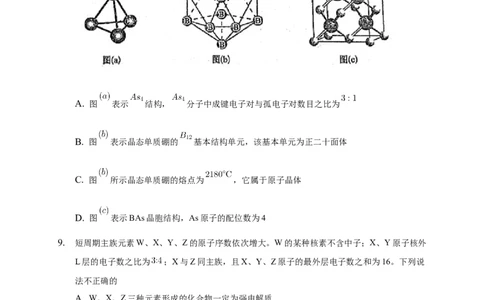
2. 二氧化硅晶体是空间立体网状结构,如图所示:
关于二氧化硅晶体的下列说法中,正确的是
A. 晶体中 键为
B. 二氧化硅晶体的分子式是
C. 晶体中Si、O原子最外电子层都满足8电子结构
D. 晶体中最小环上的原子数为8
3. 根据陈述的知识,类推得出的结论正确的是
A. 锂在空气中燃烧生成的氧化物是 ,则钠在空气中燃烧生成的氧化物是
B. 链状烷烃的结构和性质都相似,则分子组成不同的链状烷烃一定互为同系物
C. 晶体硅熔点高、硬度大,则可用于制作半导体材料
D. 金刚石的硬度大,则 的硬度也大
4. 以 表示阿伏加德罗常数的值,下列说法错误的是A. 18g冰 图 中含 键数目为
B. 28g晶体硅 图 中含有 键数目为
C. 44g干冰 图 中含有 个晶胞结构单元
D. 石墨烯 图 是碳原子单层片状新材料,12g石墨烯中含 键数目为
5. 下列反应只需要破坏共价键的是
A. 晶体硅熔化 B. 碘升华 C. 熔融 D. NaCl溶于水
6. 下列关于原子晶体、分子晶体的叙述中,正确的是
A. 在 晶体中,1个硅原子和2个氧原子形成2个共价键
B. 分子晶体中分子间作用力越大,分子越稳定
C. 金刚石为网状结构,由共价键形成的碳原子环中,最小环上有6个碳原子
D. HI的相对分子质量大于HF,所以HI的沸点高于HF
7. GaAs 晶体的熔点很高,硬度很大,密度为 ,Ga 和 As 的摩尔质量
分别为 和 ,原子半径分别为 和
pm,阿伏加德罗常数值为 ,其晶胞结构如图所示,下列说法错误的是
A. 该晶体为原子晶体
B. 在该晶体中,Ga 和 As 均无孤对电子,Ga 和 As 的配位数均为 4
C. 原子的体积占晶胞体积的百分率为D. 所有原子均满足 8 电子稳定结构
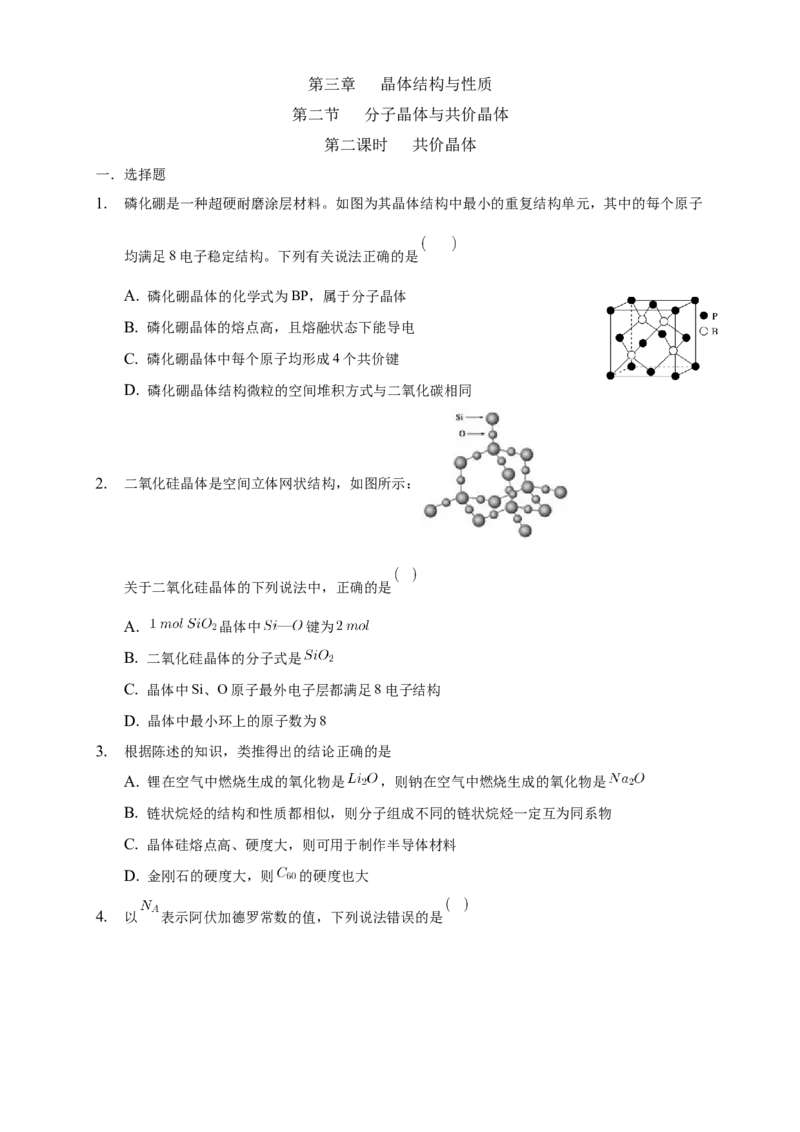
8. 2018年7月5日 科学 杂志在线报道:合成一种新的具有超高热导率半导体材料 砷化
硼 。通过反应 ,晶体 可制备BAs晶体。下
列说法错误的是
A. 图 表示 结构, 分子中成键电子对与孤电子对数目之比为
B. 图 表示晶态单质硼的 基本结构单元,该基本单元为正二十面体
C. 图 所示晶态单质硼的熔点为 ,它属于原子晶体
D. 图 表示BAs晶胞结构,As原子的配位数为4
9. 短周期主族元素W、X、Y、Z的原子序数依次增大。W的某种核素不含中子;X、Y原子核外
L层的电子数之比为 ;X与Z同主族,且X、Y、Z原子的最外层电子数之和为16。下列说
法不正确的
A. W、X、Z三种元素形成的化合物一定为强电解质
B. 简单氢化物的稳定性:
C. X与Y形成晶体的基本结构单元为四面体
D. 原子半径:
10. 氮化硅 是一种新型的耐高温耐磨材料,氮化硅属于
A. 离子晶体 B. 分子晶体 C. 金属晶体 D. 原子晶体
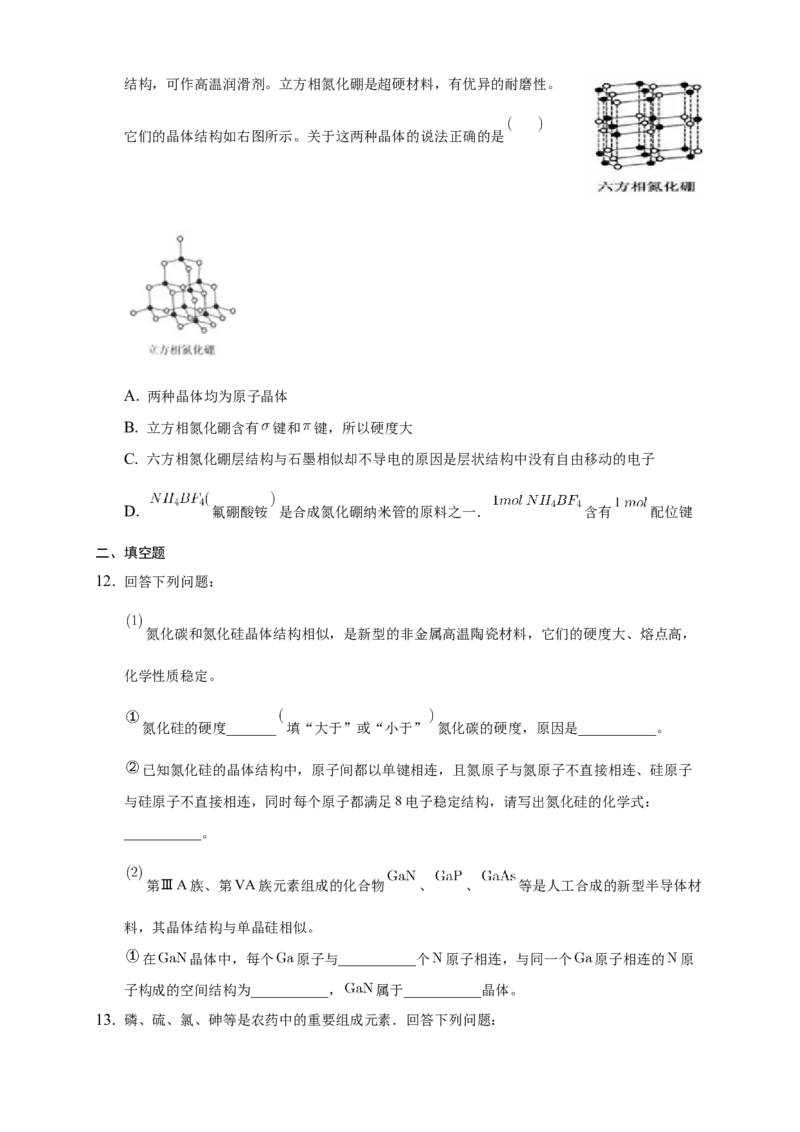
11. 氮化硼 晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。
它们的晶体结构如右图所示。关于这两种晶体的说法正确的是
A. 两种晶体均为原子晶体
B. 立方相氮化硼含有 键和 键,所以硬度大
C. 六方相氮化硼层结构与石墨相似却不导电的原因是层状结构中没有自由移动的电子
D. 氟硼酸铵 是合成氮化硼纳米管的原料之一. 含有 配位键
二、填空题
12. 回答下列问题:
氮化碳和氮化硅晶体结构相似,是新型的非金属高温陶瓷材料,它们的硬度大、熔点高,
化学性质稳定。
氮化硅的硬度_______ 填“大于”或“小于” 氮化碳的硬度,原因是___________。
已知氮化硅的晶体结构中,原子间都以单键相连,且氮原子与氮原子不直接相连、硅原子
与硅原子不直接相连,同时每个原子都满足8电子稳定结构,请写出氮化硅的化学式:
___________。
第ⅢA族、第VA族元素组成的化合物 、 、 等是人工合成的新型半导体材
料,其晶体结构与单晶硅相似。
在 晶体中,每个 原子与___________个 原子相连,与同一个 原子相连的 原
子构成的空间结构为___________, 属于___________晶体。
13. 磷、硫、氯、砷等是农药中的重要组成元素.回答下列问题:基态砷原子价层电子的电子排布式为________,基态砷原子的核外有________个未成对电
子.
生产农药的原料 中P、S、Cl的第一电离能由大到小的顺序为________,电负性:
由大到小的顺序为________.
羰基硫 可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为________,
中含有________ 键和________ 键,与COS键合方式相同且空间构型也相同的微粒
是________ 写出一种即可 .
与 为同族元素的氢化物, 可以形成 或 ,而 几乎不能形成类
似的 或 ,其原因是________.
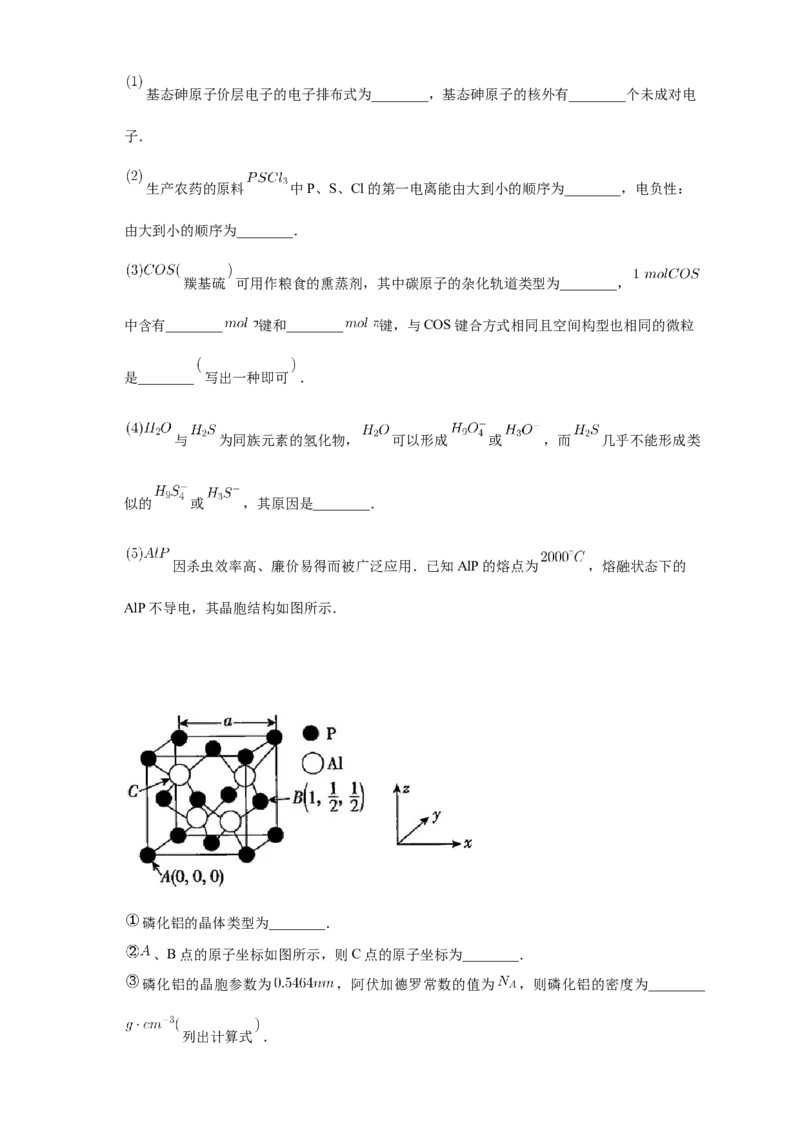
因杀虫效率高、廉价易得而被广泛应用.已知AlP的熔点为 ,熔融状态下的
AlP不导电,其晶胞结构如图所示.
磷化铝的晶体类型为________.
、B点的原子坐标如图所示,则C点的原子坐标为________.
磷化铝的晶胞参数为 ,阿伏加德罗常数的值为 ,则磷化铝的密度为________
列出计算式 .14. 非金属元素虽然种类不多,但是在自然界中的丰度却很大,请回答下列问题:
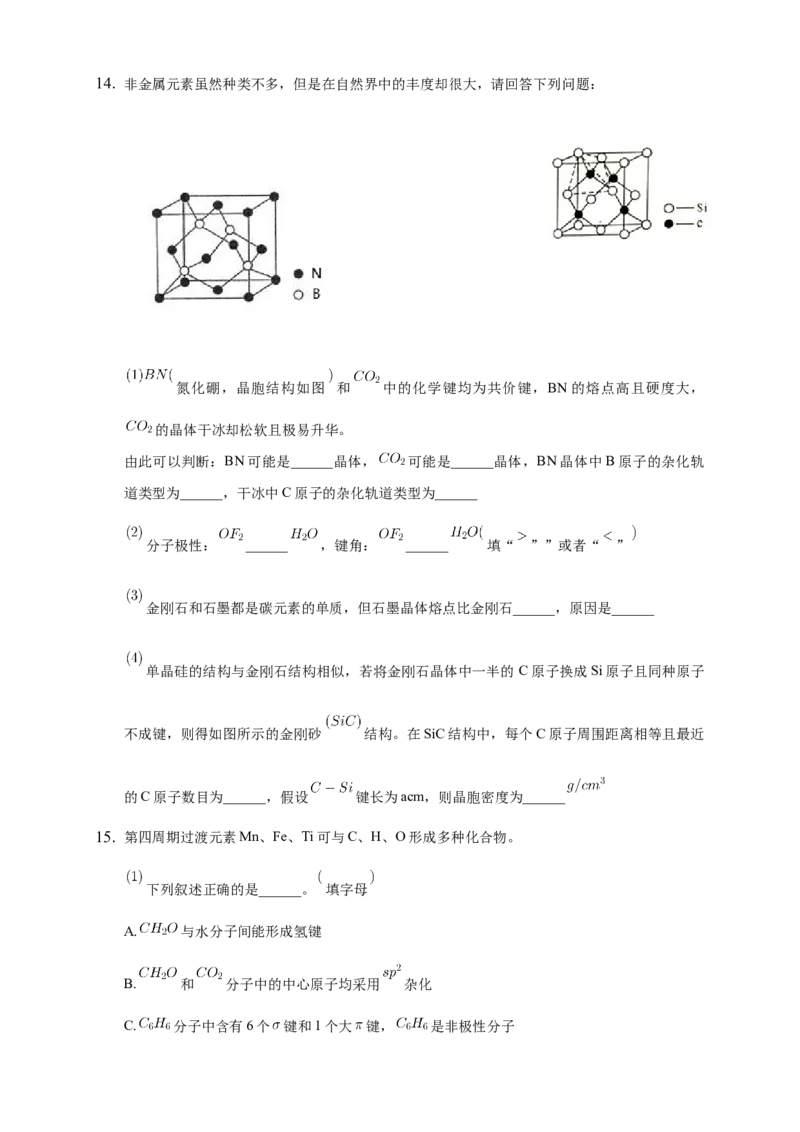
氮化硼,晶胞结构如图 和 中的化学键均为共价键,BN的熔点高且硬度大,
的晶体干冰却松软且极易升华。
由此可以判断:BN可能是______晶体, 可能是______晶体,BN晶体中B原子的杂化轨
道类型为______,干冰中C原子的杂化轨道类型为______
分子极性: ______ ,键角: ______ 填“ ””或者“ ”
金刚石和石墨都是碳元素的单质,但石墨晶体熔点比金刚石______,原因是______
单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的 C原子换成Si原子且同种原子
不成键,则得如图所示的金刚砂 结构。在SiC结构中,每个C原子周围距离相等且最近
的C原子数目为______,假设 键长为acm,则晶胞密度为______
15. 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物。
下列叙述正确的是______。 填字母
A. 与水分子间能形成氢键
B. 和 分子中的中心原子均采用 杂化
C. 分子中含有6个 键和1个大 键, 是非极性分子D. 晶体的熔点、沸点都比二氧化硅晶体的低
和Fe的部分电离能数据如下表:
元素 Mn Fe
717 759
电离能
1509 1561
3248 2957
Mn元素价电子排布式为_________,气态 再失去一个电子比气态 再失去一个电子
难,其原因是_____________________________________。
根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中 Ti属于____
区。
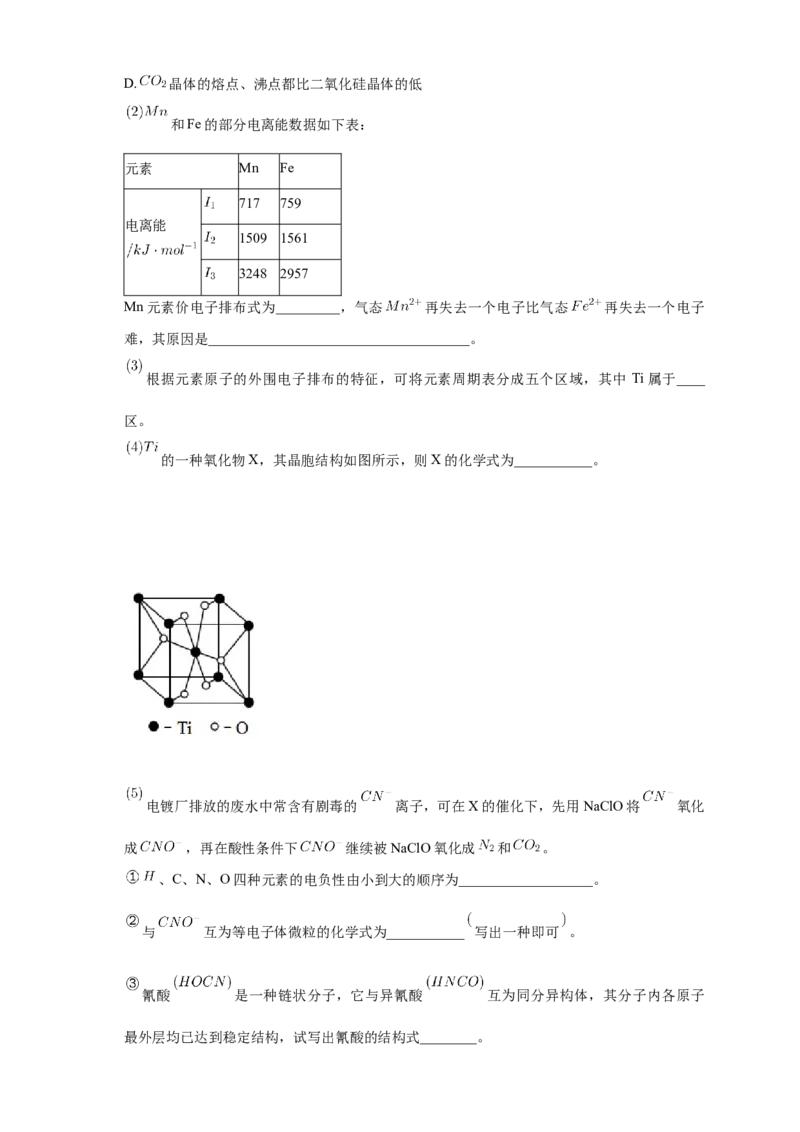
的一种氧化物X,其晶胞结构如图所示,则X的化学式为___________。
电镀厂排放的废水中常含有剧毒的 离子,可在X的催化下,先用NaClO将 氧化
成 ,再在酸性条件下 继续被NaClO氧化成 和 。
、C、N、O四种元素的电负性由小到大的顺序为___________________。
与 互为等电子体微粒的化学式为___________ 写出一种即可 。
氰酸 是一种链状分子,它与异氰酸 互为同分异构体,其分子内各原子
最外层均已达到稳定结构,试写出氰酸的结构式________。16. C和Si元素在化学中占有极其重要的地位。
写出C原子的核外电子排布式_______________________________。
的晶体结构与金刚石相似,SiC晶体中存在的微粒间作用力是______________;
SiC的熔点_________ 金刚石。 填“ ”或“ ”
氧化物MO的电子总数与SiC的相等,则M的原子结构示意图为________;MO是优良的
耐高温材料,其晶体结构与NaCl晶体相似,则每个 周围吸引_____个 ;每个MO晶
胞 中 含 有 _____ 个 ; MO 的 熔 点 比 CaO 的 高 , 其 原 因 是
___________________________________________。
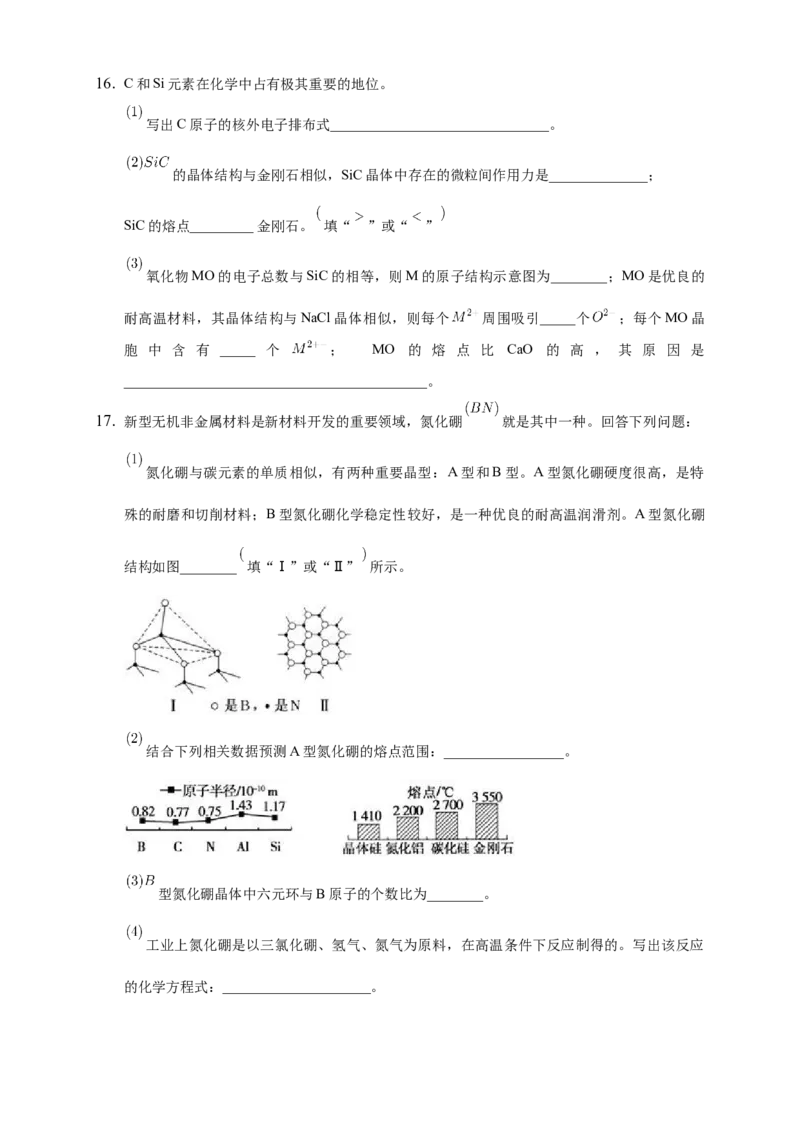
17. 新型无机非金属材料是新材料开发的重要领域,氮化硼 就是其中一种。回答下列问题:
氮化硼与碳元素的单质相似,有两种重要晶型:A型和B型。A型氮化硼硬度很高,是特
殊的耐磨和切削材料;B型氮化硼化学稳定性较好,是一种优良的耐高温润滑剂。A型氮化硼
结构如图________ 填“Ⅰ”或“Ⅱ” 所示。
结合下列相关数据预测A型氮化硼的熔点范围:_________________。
型氮化硼晶体中六元环与B原子的个数比为________。
工业上氮化硼是以三氯化硼、氢气、氮气为原料,在高温条件下反应制得的。写出该反应
的化学方程式:_____________________。