文档内容
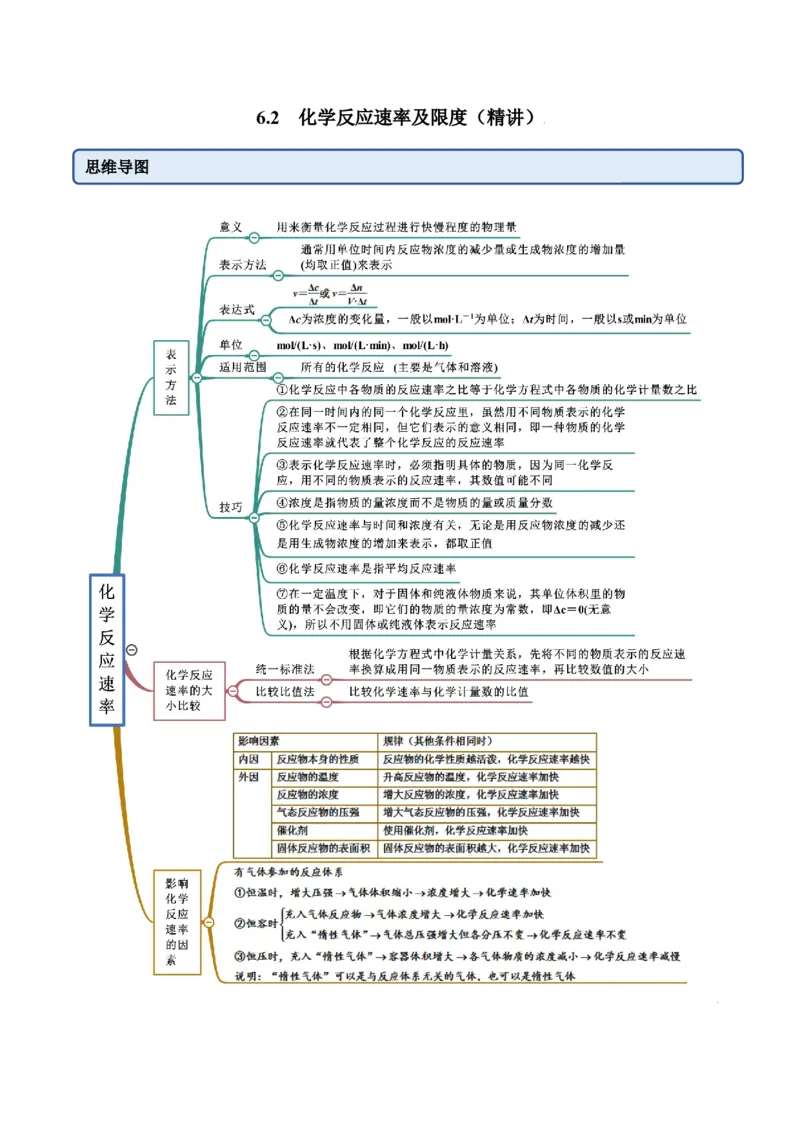
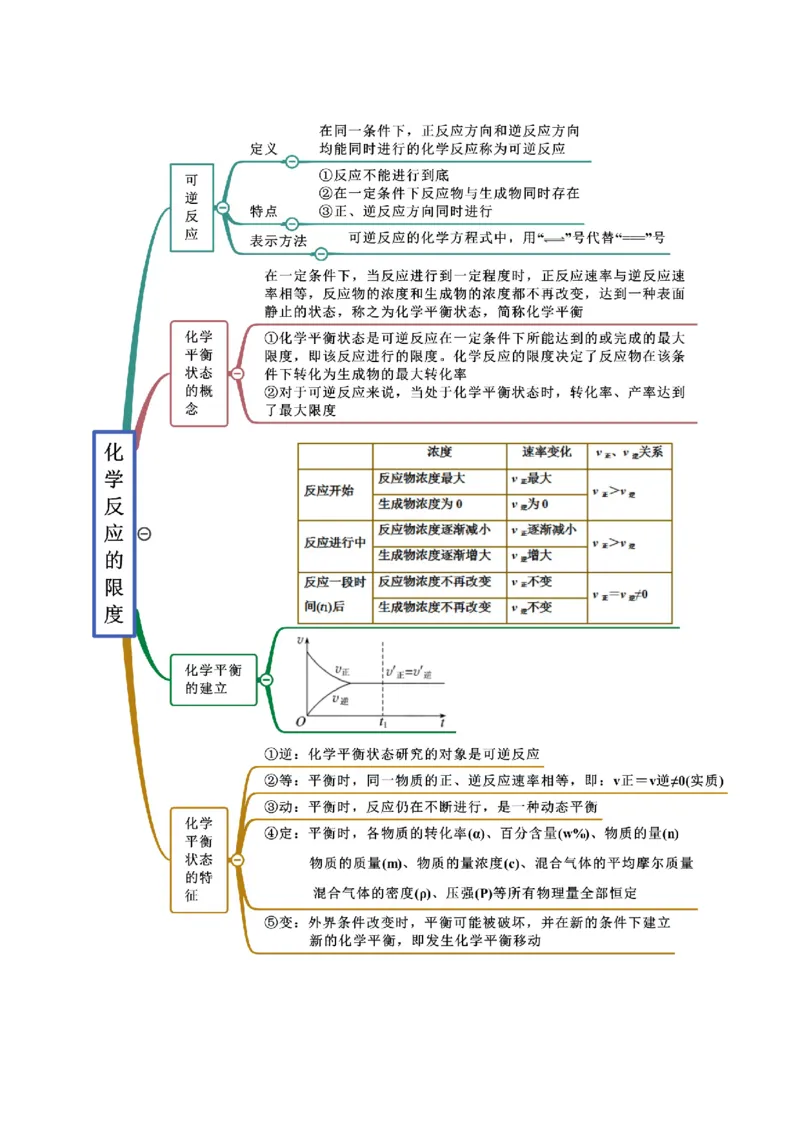
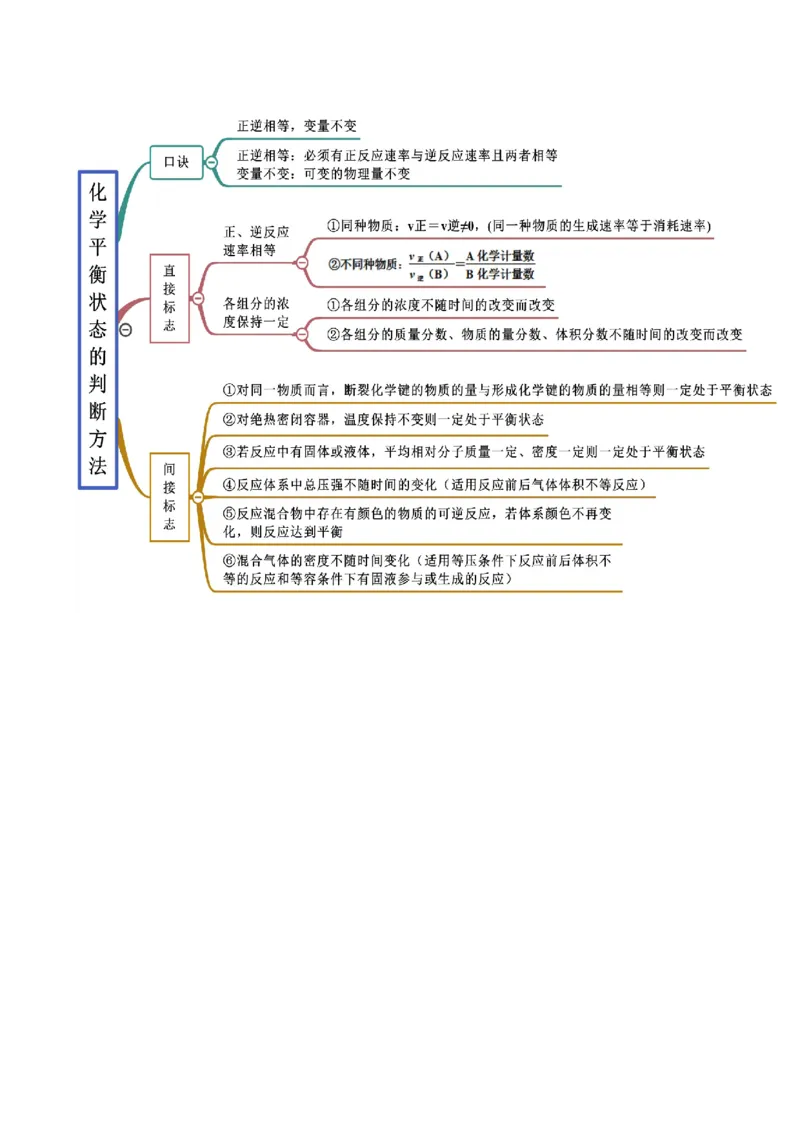
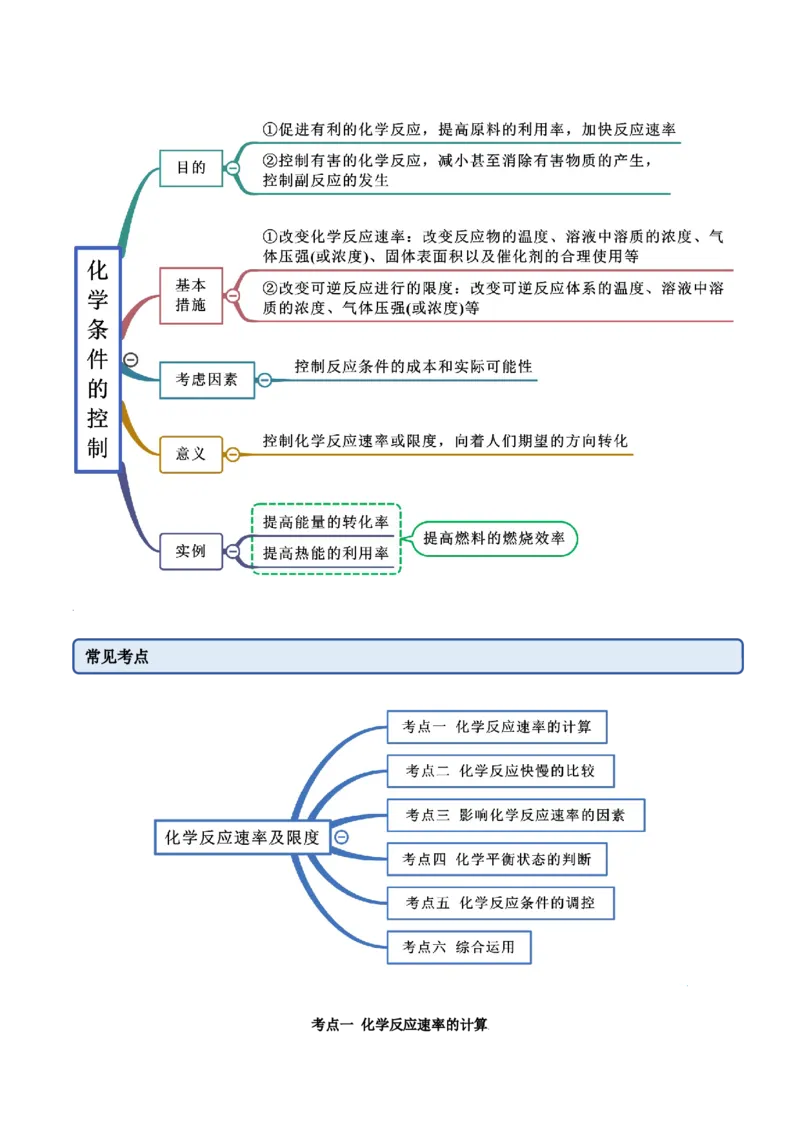
6.2 化学反应速率及限度(精讲)
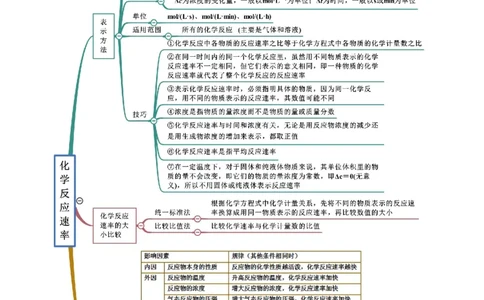
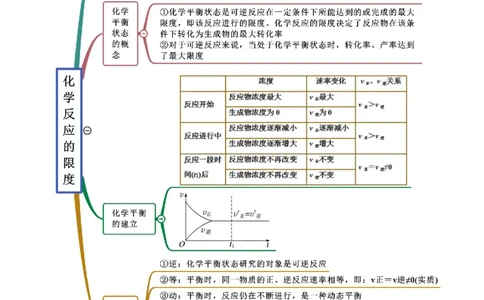
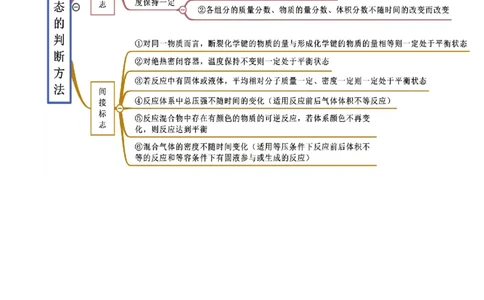
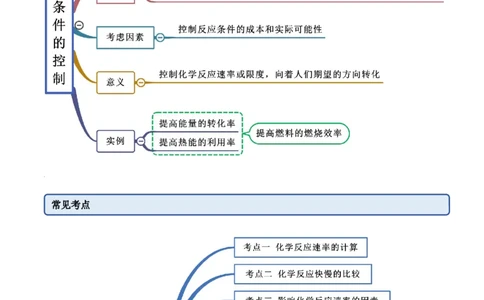
思维导图常见考点
考点一 化学反应速率的计算【例1-1】(2021·广西·桂林十八中)一定条件下,在2L密闭容器中进行反应:C(s)+HO(g) CO(g)
2
+H (g),反应3min时,H 的物质的量增加了0.9mol。则0~3min内以H 表示的平均反应速率为
2 2 2
A.0.60mol/(L•min) B.0.45mol/(L•min)
C.0.30mol/(L•min) D.0.15mol/(L•min)
【例1-2】(2021·全国)已知4NH (g)+5O(g) 4NO(g)+6H O(g),若反应速率分别用
3 2 2
v(NH )、v(O )、v(NO)、v(H O)表示,则正确的关系式为
3 2 2
A.4v(NH )=5v(O) B.5v(O )=6v(HO)
3 2 2 2
C.2v(NH )=3v(HO) D.4v(O )=5v(NO)
3 2 2
【一隅三反】
1.(2021·江苏沭阳)一定条件下,在容积为2 L的密闭容器中发生反应:N(g)+3H(g) 2NH (g),
2 2 3
1min后测得生成0.06 mol NH ,则该段时间内用NH 来表示的化学反应速率为
3 3
A.0.01 mol·L-1·min-1 B.0.02 mol·L-1·min-1
C.0.03 mol·L-1·min-1 D.0.06 mol·L-1·min-1
2(2021·辽宁葫芦岛 )已知:3Cl +2NH=N +6HCl。若反应速率分别用v(Cl )、v(NH ) 、v(N )、v(HCl)
2 3 2 2 3 2
表示,则下列关系式正确的是
A. v(Cl )= v(NH ) B. v (Cl)=v (N )
2 3 2 2
C. v(Cl ) = v(HCl) D. v(NH )=v(HCl)
2 3
3(2021·安徽宿州 )在容积为1L恒容容器内进行反应4A(g)+3B(s) 2C(g)+D(g),经2min后,A的浓
度减少了0.8mol•L-1。下列反应速率的表示正确的是
A.在这2min内,用单位时间内B的物质的量变化表示的平均反应速率是0.3mol•min-1
B.2min末时的反应速率,用A表示为0.2mol•L-1•min-1
C.在这2min内,用B表示的平均反应速率是0.3mol•L-1•min-1
D.在这2min内,用A表示的反应速率的值是减小的,用C表示的反应速率逐渐增大
考点二 化学反应快慢的比较
【例2】(2021·全国 )反应 在四种不同情况下的反应速率分别为:① ②
③ ④
下列有关反应速率的比较中正确的是
A.④<③=②<① B.④>③>②>① C.④>③=②>① D.①>②>③>④
【一隅三反】
1.(2021·浙江 )A(g)+3B(g) 2C(g)+2D(g)在不同情况下测得反应速率,其中反应速率最快的是
A.v(A)=0.5mol/(L•min) B.v(B)=1.2mol/(L•min)
C.v(C)=0.9mol/(L•min) D.v(D)=0.04mol/(L•s)
2.(2021·河南新乡)已知反应 在不同条件下的化学反应速率如下,
其中表示反应速率最快的是
A. B.
C. D.
3.(2021·全国 )在t℃,在4个均为 的密闭容器中分别进行合成氨反应:
。根据在相同时间内测定的结果,判断反应进行快慢的顺序为
a. b.
c. d.
A. B. C. D.
考点三 影响化学反应速率的因素
【例3】(2021·辽宁·清原满族自治县第二高级中学高一期中)对于在一定条件下的密闭容器中进行的反应
C(s)+CO(g) 2CO(g),下列说法不正确的是
2
A.将木炭磨⇌成粉末可以加快反应速率
B.升高温度可以加快反应速率
C.容器体积不变时,向其中充入N,反应速率不变
2
D.增加木炭的量可以加快反应速率【一隅三反】
1.(2021·全国)可使反应C(s)+CO(g)=2CO(g)的反应速率增大的措施是:①增大压强 ②增加碳的用量
2
③通入CO ④恒压下充入N ⑤恒容下充入N ⑥通入CO
2 2 2
A.①③⑤ B.②④⑥ C.①③⑥ D.③⑤⑥
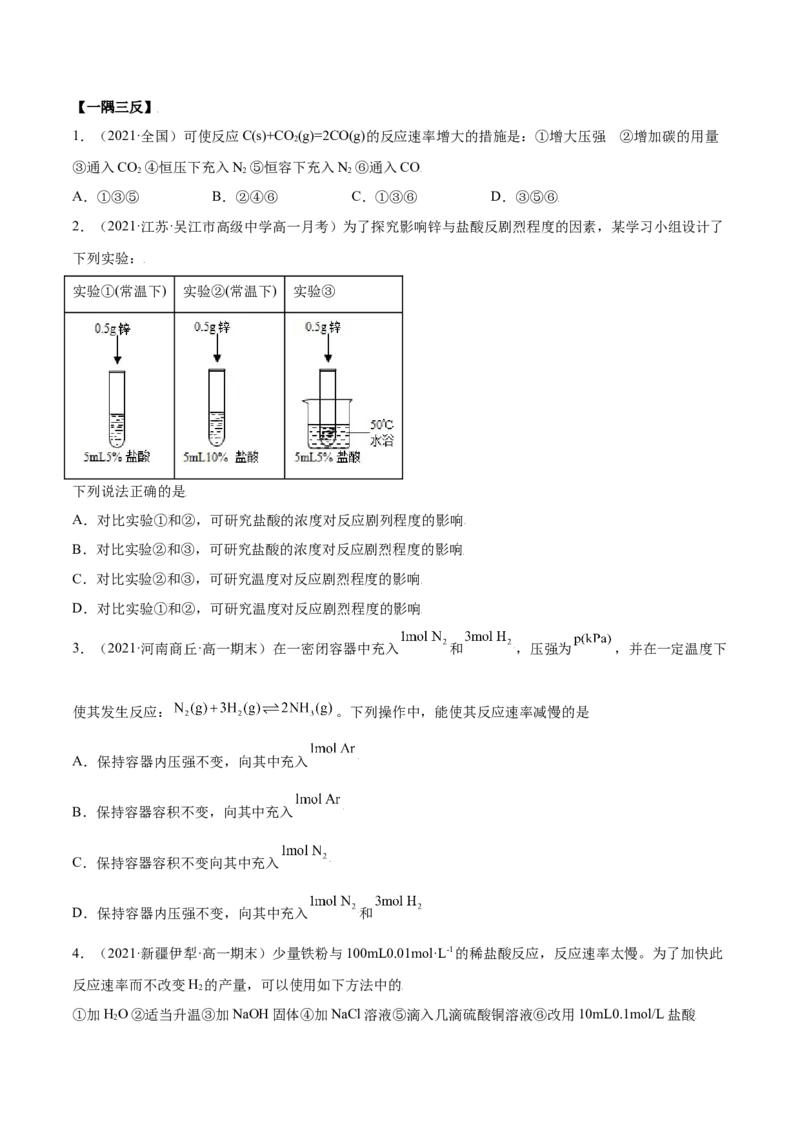
2.(2021·江苏·吴江市高级中学高一月考)为了探究影响锌与盐酸反剧烈程度的因素,某学习小组设计了
下列实验:
实验①(常温下) 实验②(常温下) 实验③
下列说法正确的是
A.对比实验①和②,可研究盐酸的浓度对反应剧列程度的影响
B.对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响
C.对比实验②和③,可研究温度对反应剧烈程度的影响
D.对比实验①和②,可研究温度对反应剧烈程度的影响
3.(2021·河南商丘·高一期末)在一密闭容器中充入 和 ,压强为 ,并在一定温度下
使其发生反应: 。下列操作中,能使其反应速率减慢的是
A.保持容器内压强不变,向其中充入
B.保持容器容积不变,向其中充入
C.保持容器容积不变向其中充入
D.保持容器内压强不变,向其中充入 和
4.(2021·新疆伊犁·高一期末)少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢。为了加快此
反应速率而不改变H 的产量,可以使用如下方法中的
2
①加HO②适当升温③加NaOH固体④加NaCl溶液⑤滴入几滴硫酸铜溶液⑥改用10mL0.1mol/L盐酸
2A.①③⑥ B.②⑥ C.③⑥ D.④⑤⑥
考点四 化学平衡状态的判断
【例4】(2021·四川省内江市第六中学高一期中)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容
器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:HNCOONH (s) 2NH (g)
2 4 3
+CO (g)。能判断该反应已经达到化学平衡的是 ⇌
2
①v(NH ) =2v(CO )
3 正 2 逆
②密闭容器中总压强不变
③密闭容器中混合气体的密度不变
④密闭容器中混合气体的平均相对分子质量不变
⑤密闭容器混合气体的总物质的量不变
⑥密闭容器中 CO 的体积分数不变
2
⑦混合气体总质量不变
A.①②⑤⑦ B.①②③⑤⑦ C.①②③⑤⑥ D.全部
【一隅三反】
1.(2021·山东·高一学业考试)一定条件下,恒容密闭容器中发生反应:
。下列说法能说明该反应一定达到平衡状态的是
A. 、 、 、 在容器中同时存在
B.容器中气体分子总数保持不变
C.容器中氮原子总数保持不变
D. 、 的浓度相等
2.(2021·四川省华蓥中学高一月考)可逆反应2NO (g)=2NO(g)+O(g)在体积固定的密闭容器中,达到平
2 2
衡状态的标志是
①单位时间内生成n molO 的同时生成2n molNO
2 2
②单位时间内生成n molO 的同时生成2n molNO
2
③用NO 、NO、O 表示的反应速率的比为2∶2∶1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态A.①④⑥⑦ B.②③⑤⑦ C.①③④⑤ D.全部
3.(2021·重庆市第七中学校高一期中)下列平衡建立判断依据中,叙述不正确的项有
A.2HI(g) H(g)+I (g)若1molH−H键断裂的同时有2molH−I键断裂,则平衡建立
2 2
B.3Z(s) X(g)+2Y(g)加入Z后,若气体平均摩尔质量不变,则平衡建立
C.N(g)+3H(g) 2NH (g)若恒容条件下装置压强不变,则平衡建立
2 2 3
D.C(s)+HO(g) CO(g)+H(g)若恒容条件下气体密度不变,则平衡建立
2 2
考点五 化学反应条件的调控
【例5】(2021·河北·辛集中学高一期中)下图所示为工业合成氨的流程图。下列有关生产条件的调控作用
分析正确的是
A.①中“净化”可以防止催化剂中毒,③选择高效催化剂可以使原料完全转化成氨
B.②中“加压”可以加快反应速率,因为在该压强下催化剂的活性最大
C.③一般选择控制反应温度为700℃左右
D.④⑤有利于提高原料的利用率,能节约生产成本
【一隅三反】
1(2021·上海市光明中学高一期末)在工业生产硫酸的过程中,发生如下反应:2SO (g)+O(g)
2 2
2SO (g)+Q,下列叙述中不正确的是
3
A.矿石粉碎的目的是使原料充分利用,并增大接触面使反应速率加快
B.接触室中采用常压的主要原因是常压下SO 的转化率已经很高
2
C.沸腾炉中出来的混合气需要洗涤,目的是防止催化剂中毒
D.接触室用450℃的高温,使催化剂活性最佳,更能促进平衡向正反应方向移动
2.(2021·全国·高一课时练习)工业制硫酸中的一步重要反应是SO 在400-500℃和常压下的催化氧化:
2
2SO + O 2SO , 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误
2 2 3
的是A.反应温度选择400-500℃是该反应催化剂的催化活性、反应速率、反应限度等角度综合考虑的结果
B.因为在常压下该反应的速率和SO 的转化率已经很高了,所以选择常压条件主要是从生产成本角度考
2
虑
C.为提高SO 的转化率,应适当提高O 的浓度
2 2
D.使用催化剂是为了加快反应速率,提高SO 产率
3
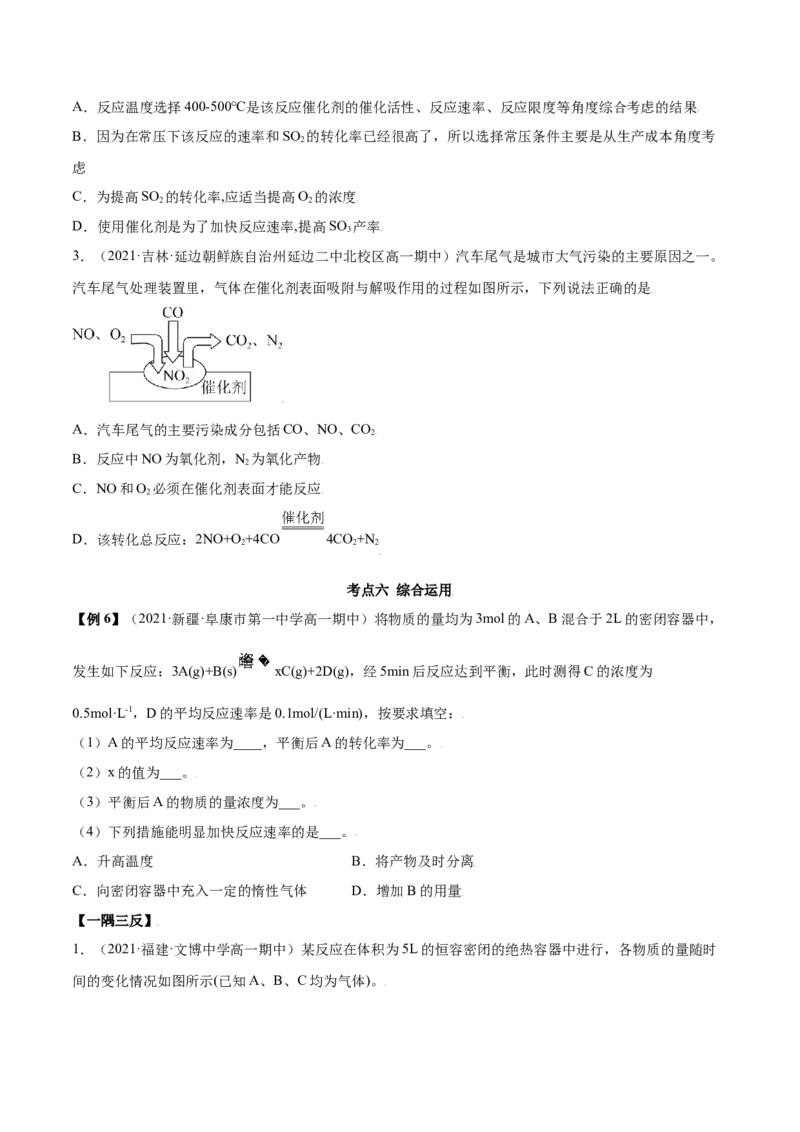
3.(2021·吉林·延边朝鲜族自治州延边二中北校区高一期中)汽车尾气是城市大气污染的主要原因之一。
汽车尾气处理装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是
A.汽车尾气的主要污染成分包括CO、NO、CO
2
B.反应中NO为氧化剂,N 为氧化产物
2
C.NO和O 必须在催化剂表面才能反应
2
D.该转化总反应:2NO+O +4CO 4CO+N
2 2 2
考点六 综合运用
【例6】(2021·新疆·阜康市第一中学高一期中)将物质的量均为3mol的A、B混合于2L的密闭容器中,
发生如下反应:3A(g)+B(s) xC(g)+2D(g),经5min后反应达到平衡,此时测得C的浓度为
0.5mol·L-1,D的平均反应速率是0.1mol/(L·min),按要求填空:
(1)A的平均反应速率为____,平衡后A的转化率为___。
(2)x的值为___。
(3)平衡后A的物质的量浓度为___。
(4)下列措施能明显加快反应速率的是___。
A.升高温度 B.将产物及时分离
C.向密闭容器中充入一定的惰性气体 D.增加B的用量
【一隅三反】
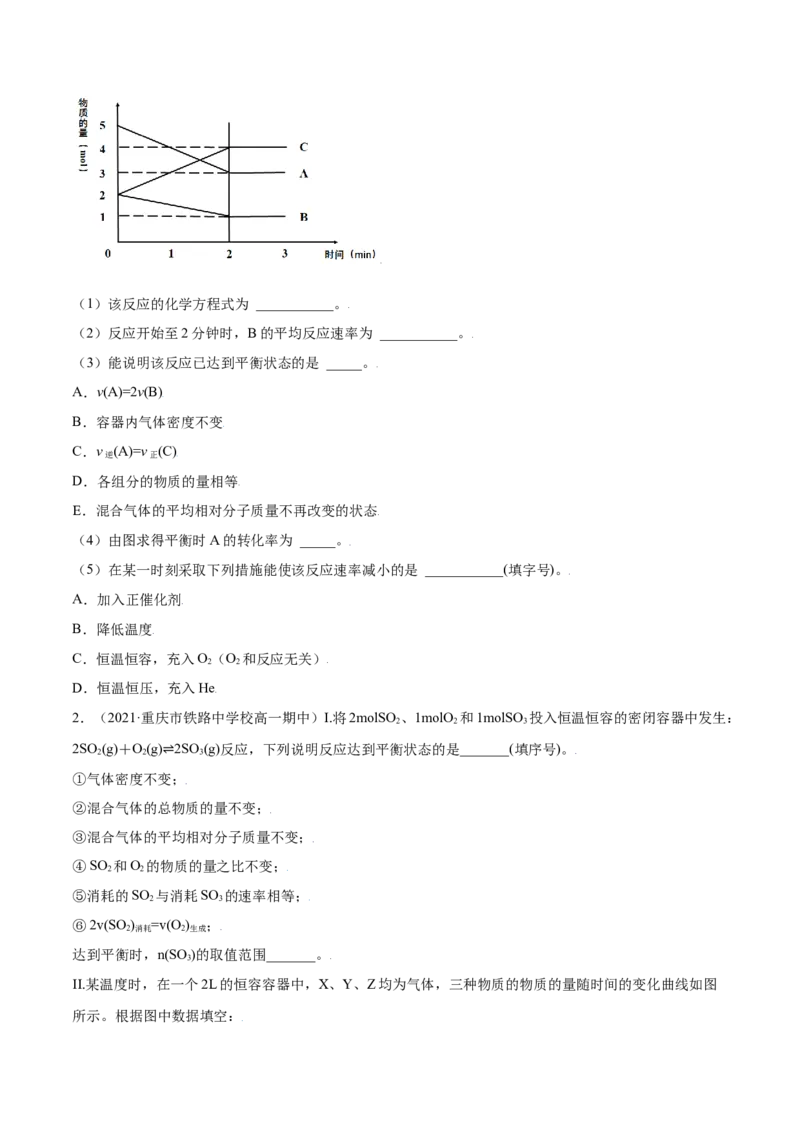
1.(2021·福建·文博中学高一期中)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时
间的变化情况如图所示(已知A、B、C均为气体)。(1)该反应的化学方程式为 ___________。
(2)反应开始至2分钟时,B的平均反应速率为 ___________。
(3)能说明该反应已达到平衡状态的是 _____。
A.v(A)=2v(B)
B.容器内气体密度不变
C.v (A)=v (C)
逆 正
D.各组分的物质的量相等
E.混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为 _____。
(5)在某一时刻采取下列措施能使该反应速率减小的是 ___________(填字号)。
A.加入正催化剂
B.降低温度
C.恒温恒容,充入O(O 和反应无关)
2 2
D.恒温恒压,充入He
2.(2021·重庆市铁路中学校高一期中)I.将2molSO 、1molO 和1molSO 投入恒温恒容的密闭容器中发生:
2 2 3
2SO (g)+O(g) 2SO (g)反应,下列说明反应达到平衡状态的是_______(填序号)。
2 2 3
①气体密度不变⇌;
②混合气体的总物质的量不变;
③混合气体的平均相对分子质量不变;
④SO 和O 的物质的量之比不变;
2 2
⑤消耗的SO 与消耗SO 的速率相等;
2 3
⑥2v(SO ) =v(O ) ;
2 消耗 2 生成
达到平衡时,n(SO )的取值范围_______。
3
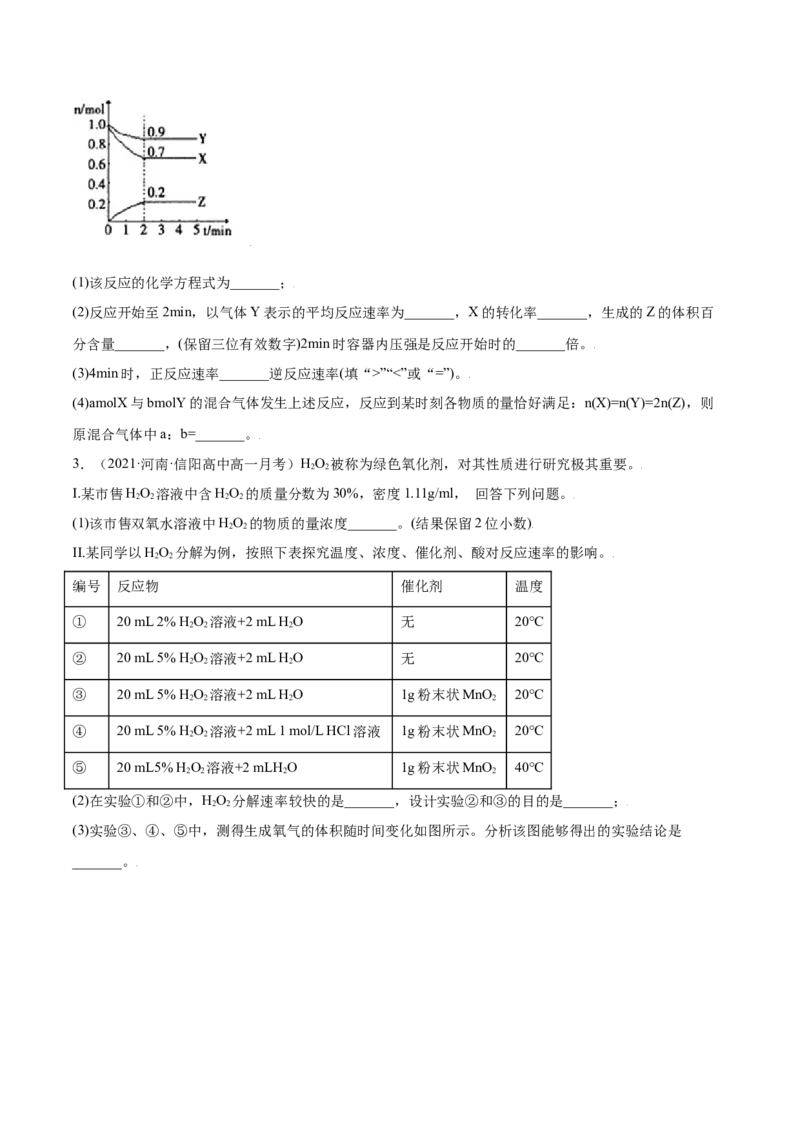
II.某温度时,在一个2L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图
所示。根据图中数据填空:(1)该反应的化学方程式为_______;
(2)反应开始至2min,以气体Y表示的平均反应速率为_______,X的转化率_______,生成的Z的体积百
分含量_______,(保留三位有效数字)2min时容器内压强是反应开始时的_______倍。
(3)4min时,正反应速率_______逆反应速率(填“>”“<”或“=”)。
(4)amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则
原混合气体中a:b=_______。
3.(2021·河南·信阳高中高一月考)HO 被称为绿色氧化剂,对其性质进行研究极其重要。
2 2
I.某市售HO 溶液中含HO 的质量分数为30%,密度1.11g/ml, 回答下列问题。
2 2 2 2
(1)该市售双氧水溶液中HO 的物质的量浓度_______。(结果保留2位小数)
2 2
II.某同学以HO 分解为例,按照下表探究温度、浓度、催化剂、酸对反应速率的影响。
2 2
编号 反应物 催化剂 温度
① 20 mL 2% HO 溶液+2 mL HO 无 20℃
2 2 2
② 20 mL 5% HO 溶液+2 mL HO 无 20℃
2 2 2
③ 20 mL 5% HO 溶液+2 mL HO 1g粉末状MnO 20℃
2 2 2 2
④ 20 mL 5% HO 溶液+2 mL 1 mol/L HCl溶液 1g粉末状MnO 20℃
2 2 2
⑤ 20 mL5% H O 溶液+2 mLH O 1g粉末状MnO 40℃
2 2 2 2
(2)在实验①和②中,HO 分解速率较快的是_______,设计实验②和③的目的是_______;
2 2
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出的实验结论是
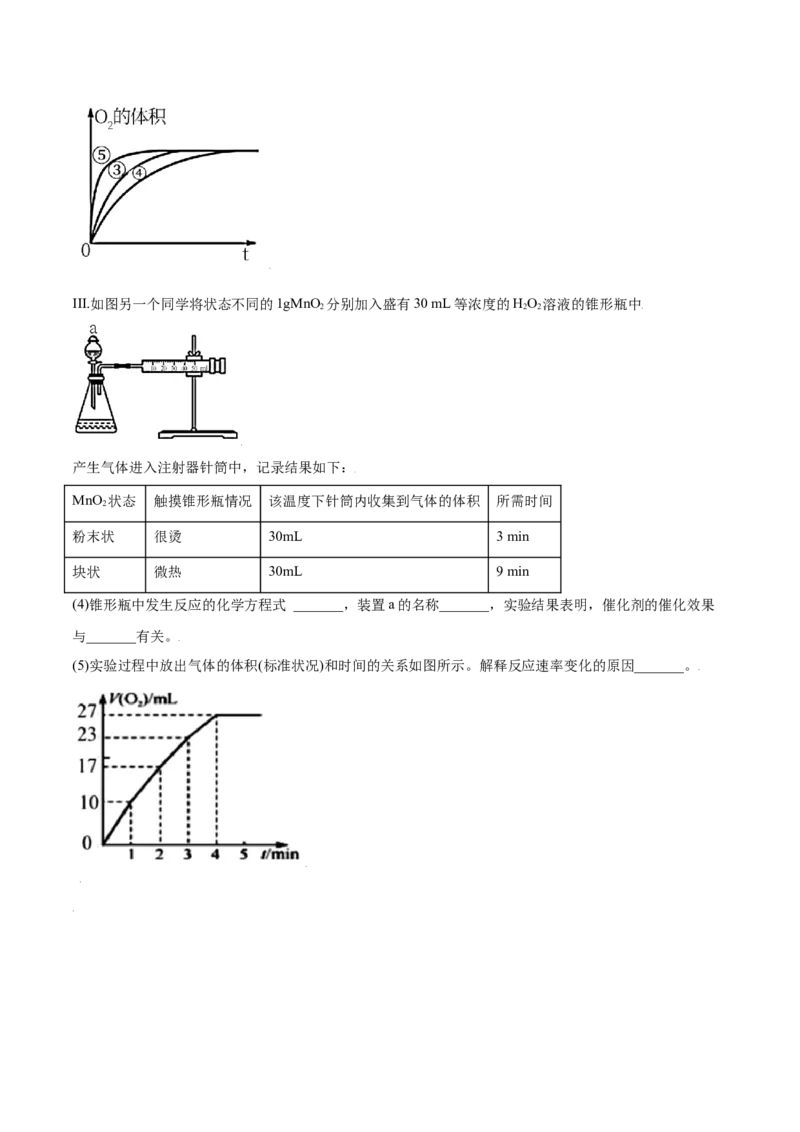
_______。III.如图另一个同学将状态不同的1gMnO 分别加入盛有30 mL等浓度的HO 溶液的锥形瓶中
2 2 2
产生气体进入注射器针筒中,记录结果如下:
MnO 状态 触摸锥形瓶情况 该温度下针筒内收集到气体的体积 所需时间
2
粉末状 很烫 30mL 3 min
块状 微热 30mL 9 min
(4)锥形瓶中发生反应的化学方程式 _______,装置a的名称_______,实验结果表明,催化剂的催化效果
与_______有关。
(5)实验过程中放出气体的体积(标准状况)和时间的关系如图所示。解释反应速率变化的原因_______。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育