文档内容
6.2 化学反应速率及限度(精练)
题组一 化学反应速率的计算
1.(2021·福建·文博中学高一期中)反应4NH (g)+5O(g) 4NO(g)+6H O(g)在恒容密闭容器中进行,
3 2 2
30 s后NH 的物质的量浓度减小了3 mol•L﹣1,则对此反应的速率的表示正确的是
3
A.v(H O)=0.15 mol•(L•s)﹣1 B.v(O )=0.1 mol•(L•s)﹣1
2 2
C.v(NH )=0.2 mol•(L•s)﹣1 D.v(O ):v(NO)=4:5
3 2
2.(2021·吉林·长春市清蒲中学高一期中)一定温度条件中,在密闭容器中,投入一定量 发生2SO (g)
2
+O (g) 2SO (g),5min达到平衡, 的浓度为1mol/L,则用 表示的速率为
2 3
A. B.0.2 mol•L-1•min-1
C. D.
3.(2021·浙江杭州)某温度时,浓度都是 的两种气体 和 ,在密闭容器中发生可逆反应生成
气体Z,充分反应后 的浓度为 , 的浓度为 ,生成的Z的浓度为 ,则
该反应的化学方程式(Z用X、Y表示)是
A. B.
C. D.
4.(2021·湖北宜昌)将气体X、Y置于容积为2L的密闭容器中,发生如下反应: 。
反应进行到4s末,测得X为 0.5 mol,Y为 0.4 mol,Z为 0.2 mol。则用反应物X浓度的减少来表示该反
应速率为
A.0.025 B.0.0125
C.0.05 D.0.1
5.(2021·浙江·嘉兴市第五高级中学 )在一密闭容器中充入一定量的N 和H,经测定反应开始后的2s
2 2内氢气的平均速率:v(H )=0.45mol/(L·s),则2s末NH 的浓度为
2 3
A.0.45mol/L B.0.50mol/L
C.0.55mol/L D.0.60mol/L
6.(2021·河南 )在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知
v(A)、v(B)、v(C)之间有以下关系:2v(B)=3v(A),2v(B)=3v(C),则此反应可表示为
A.2A+3B=2C B.A+2B=C C.3A+2B=2C D.2A+2B=3C
7.(2021·河南·辉县市第一高级中学高一月考)将固体 置于2L的密闭容器中,在恒温的条件下发
生如下反应: , 。2min时测得 的浓度为 ,
HBr的浓度为8 ,则上述反应中0~2min内生成 的速率为
A.0.5 B.2
C.2.5 D.5
8.(2021·新疆伊犁·高一期末)在一定条件下发生反应:N+3H 2NH ,经2min后N 的物质的量浓
2 2 3 2
度减小了0.4mol·L-1,则用H 表示的平均反应速率为
2
A.0.4mol·L-1·s-1 B.0.2mol·L-1·min-1
C.0.6mol·L-1·min-1 D.0.4mol·L-1·min-1
9.(2021·河南9)在2L恒容密闭容器中进行反应: 。已知反应过程中某一
时刻 、 、 物质的量分别为1.0mol、3.0mol、4.0mol,当反应达到平衡时,可能存在的数据是
A. 为 B. 、 均为
C. 为 D. 为
10.(2021·浙江省余姚市第七中学高一月考)某温度下,密闭容器中进行反应:X(g)+4Y(g) 2Z(g)+
3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1,下同),则达⇌平衡时,
各物质的浓度不可能的是
A.c(X)=0.15mol/L B.c(Z)=0.3mol/L C.c(Y)=0.45mol/L D.c(R)=0.6mol/L题组二 化学反应快慢的比较
1.(2021·甘肃·庆阳第六中学高一期中)在 反应中,下列表示的该
反应速率最快的是
A. B.
C. D.
2.(2021·浙江·瑞安市上海新纪元高级中学高一月考)对于可逆反应A(g)+3B(s) 2C(g)+2D(g),在不同
条件下的化学反应速率如下,其中表示的反应速率最快的是
A.v(A)=0.5mol·L-1·min-1 B.v(B)=1.2mol·L-1·s-1
C.v(D)=0.4mol·L-1·min-1 D.v(C)=0.1mol·L-1·s-1
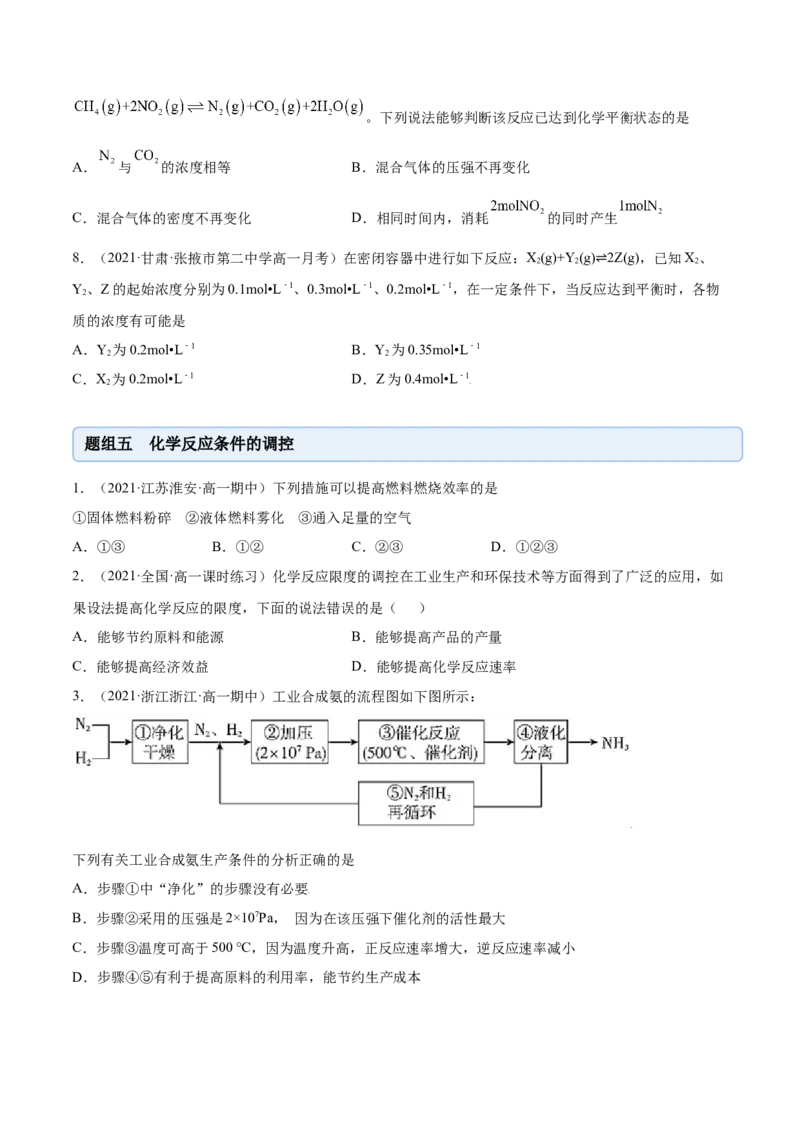
3.(2021·福建·文博中学高一期中)下表中是各组反应的反应物和温度,反应刚开始时,放出H 速率最
2
快的是
金属(粉末状)/mol 酸的浓度及体积 反应温度
A Mg 0.1 6mol•L﹣1硝酸 10mL 60℃
B Mg 0.1 3mol•L﹣1盐酸 10mL 60℃
C Fe 0.1 3mol•L﹣1盐酸 10mL 60℃
D Mg 0.1 3mol•L﹣1硫酸 10mL 60℃
题组三 影响化学反应速率的因素
1.(2021·山东聊城·高一期末)化学在生活中的应用随处可见,下列措施不是为了改变化学反应速率的是
A.将食物存放在冰箱中 B.加工馒头时添加膨松剂
C.糕点包装袋内放置除氧剂 D.冶铁时将铁矿石粉碎
2.(2021·河北衡水·高一期中)对于反应C(s)+HO(g) CO(g)+H(g),现采取下列措施,其中能够使
2 2
反应速率加快的措施是
A.恒容下充入氦气 B.增加碳的质量
C.缩小容器体积,增大压强 D.及时移出生成的CO3.(2021·河北衡水·高一期中)下列措施中,不能加快化学反应速率的是
A.煤作燃料燃烧时,将煤块碾磨成煤粉
B.铝片与稀盐酸反应时,加入少量的蒸馏水
C.HO 分解制取氧气时,加入适量的MnO
2 2 2
D.合成氨厂制备氨气时,适当升高温度
4.(2021·山东·高一学业考试)某密闭容器中发生反应: ,不改变其他
条件,下列措施不能提高反应速率的是
A.升高温度 B.减小容器体积
C.保持容积不变,通入 D.选用合适的催化剂
5.(2021·福建·泉州五中高一期中)现有反应3Fe(s)+4H O(g) Fe O(s)+4H(g),在一体积可调的密闭
2 3 4 2
容器中进行,采取下列措施对其反应速率几乎无影响的是
A.保持容器内压强不变,增加H 的量
2
B.保持容器内压强不变,充入Ar
C.保持容器体积不变,充入Ar
D.将容器体积缩小一半
6.(2021·湖北武汉 )下列有关化学反应速率的说法中,正确的是
A.对化学反应来说,反应速率越大,实验现象越明显
B.升高温度后,吸热反应的速率加快,放热反应的速率减慢
C. 和 可以反应生成 和 ,减小压强反应速率减慢
D.钠和水的反应中,减少水的量,反应速率减慢
7.(2021·江苏·东海县教育局教研室高一期中)已知 溶液和 溶液能发生如下反应:
,下列关于该反应的说法正确的是
A.升高温度会减慢反应速率
B.增大 和 的浓度能加快反应速率
C.当上述可逆反应达到平衡时,溶液中 与 一定相等D.当上述可逆反应达到平衡时, 的转化率为
8.(2021·河北石家庄·高一月考)已知:反应P(g)+Q(g M(g)+N(g)的正反应是放热反应。下列关于该
反应的说法正确的是
A.P(g)的能量一定高于N(g)的
B.M(g)和N(g)的总能量大于P(g)和Q(g)的总能量
C.当反应达到平衡时,正反应速率、逆反应速率均为0
D.当反应达到平衡时,改变反应条件,化学平衡可能会被破坏
9.(2021·吉林·乾安县第四中学高一期中)下列有关说法中是为了减慢化学反应速率的是
A.用冰箱保存食物
B.过氧化氢分解用二氧化锰作催化剂
C.合成氨气时采用高温条件
D.将块状固体药品研细混匀后进行反应
10.(2021·全国·高一课时练习)在一定温度下,某密闭容器中发生反应:2C(g) A(g)+B(s) ΔH
>0,若0~15s内c(C)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是
A.0~15s内用B表示的平均反应速率为v(B)=0.001mol·L-1·s-1
B.c(C)由0.07mol·L-1降到0.05mol·L-1所需的反应时间小于10s
C.升高温度正反应速率加快,逆反应速率减慢
D.减小反应体系的体积,化学反应速率加快
11.(2021·全国·高一课时练习)据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇(CHCHOH)已
3 2
成为现实:2CO(g)+6H(g) CHCHOH(g)+3HO(g)。下列叙述错误的是
2 2 3 2 2
A.使用Cu—Zn—Fe催化剂可大大提高生产效率
B.升高温度,则CHCHOH的产率一定增大
3 2
C.充入大量CO 气体可提高H 的转化率
2 2
D.从平衡混合气体中分离出CHCHOH和HO,可提高CO 和H 的利用率
3 2 2 2 2
题组四 化学平衡状态的判断
1.(2021·河北·沧州市一中高一月考)工业上,在持续加热的条件下用氢气和碘蒸气经铂黑催化合成碘化
氢,化学方程式为:H(g)+I (g) 2HI(g)。在实验室中模拟该反应时,控制反应条件不变,将一定量的氢
2 2
⇌气和碘蒸气充入恒容密闭容器中,反应一段时间后,不能确定该反应已经达到化学平衡状态的是
A.容器中的压强不再变化 B.H 的浓度不再变化
2
C.容器中混合物的颜色不再变化 D.HI的物质的量不再变化
2.(2021·黑龙江·齐齐哈尔市教育局 )某温度下的恒容密闭容器中,发生反应:A(s)+2B(g) C(g)
+D(g)。下列哪些物理量不再发生变化时,表明该反应已达到平衡状态
①混合气体的密度 ②混合气体的压强 ③A的质量 ④气体的总物质的量 ⑤混合气体的平均相对
分子质量
A.①②③ B.②③⑤ C.①③⑤ D.①③④⑤
3.(2021·山东聊城·高一期末)在一定条件下的恒容密闭容器中发生可逆反应2X(g) Y(g)+Z(s),下列不
能说明该反应达到化学平衡状态的是 ⇌
A.2v (X)=v (Y) B.反应容器中Y的质量分数不变
正 逆
C.体系压强不再变化 D.混合气体的密度不再变化
4.(2021·广东惠州·高一期末)一定条件下的恒容密闭容器中,发生可逆反应H(g)+I (g) 2HI(g)。下列情
2 2
况能说明该反应一定达到平衡状态的是 ⇌
A.1 mol氢氢键断裂同时生成2 mol氢碘键
B.H 的百分含量保持不变
2
C.混合气体的密度保持不变
D.H、I 和HI的物质的量之比为1:1:2
2 2
5.(2021·内蒙古赤峰·高一期末)一定温度下,在一容积不变的密闭容器中发生的可逆反应
,不是达到反应限度的标志的是
①Y的消耗速率与Z的生成速率相等
②反应容器中压强不再变化
③X、Y、Z的浓度不再变化
④反应容器中气体平均摩尔质量不再变化
A.①③ B.②③ C.①② D.②④
6(2021·重庆市铁路中学校高一期中)经过化学家长期研究发现高炉中:Fe O(s)+3CO(g) 2Fe(s)+3CO (g)
2 3 2
是可逆反应。一定温度下,在一体积恒定容器中发生上述反应,下列情况能说明达到反应⇌达到平衡的是
A.气体平均摩尔质量不变 B.容器内压强不变
C.容器中n(CO)=n(CO ) D.v(CO)=v(CO )
2 2
7.(2021·山东济南·高一期末)一定温度下,恒容密闭容器中发生反应。下列说法能够判断该反应已达到化学平衡状态的是
A. 与 的浓度相等 B.混合气体的压强不再变化
C.混合气体的密度不再变化 D.相同时间内,消耗 的同时产生
8.(2021·甘肃·张掖市第二中学高一月考)在密闭容器中进行如下反应:X(g)+Y(g) 2Z(g),已知X、
2 2 2
Y、Z的起始浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.2mol•L﹣1,在一定条件下,当反应⇌达到平衡时,各物
2
质的浓度有可能是
A.Y 为0.2mol•L﹣1 B.Y 为0.35mol•L﹣1
2 2
C.X 为0.2mol•L﹣1 D.Z为0.4mol•L﹣1
2
题组五 化学反应条件的调控
1.(2021·江苏淮安·高一期中)下列措施可以提高燃料燃烧效率的是
①固体燃料粉碎 ②液体燃料雾化 ③通入足量的空气
A.①③ B.①② C.②③ D.①②③
2.(2021·全国·高一课时练习)化学反应限度的调控在工业生产和环保技术等方面得到了广泛的应用,如
果设法提高化学反应的限度,下面的说法错误的是( )
A.能够节约原料和能源 B.能够提高产品的产量
C.能够提高经济效益 D.能够提高化学反应速率
3.(2021·浙江浙江·高一期中)工业合成氨的流程图如下图所示:
下列有关工业合成氨生产条件的分析正确的是
A.步骤①中“净化”的步骤没有必要
B.步骤②采用的压强是2×107Pa, 因为在该压强下催化剂的活性最大
C.步骤③温度可高于500 ℃,因为温度升高,正反应速率增大,逆反应速率减小
D.步骤④⑤有利于提高原料的利用率,能节约生产成本题组六 综合运用
1.(2021·陕西金台 )某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间
的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为___________。
(2)反应开始至2min,气体Z的平均反应速率为___________。
(3)①若X、Y、Z均为气体:1min时v _____v (填 、 或者 =,下同),2min时v _____ v
正 逆 正 逆
②若此时将容器的体积缩小到原来的一半,达到平衡时,容器内温度升高(容器不与外界进行热交换),则
该反应的正反应为_____反应(填“放热”或“吸热”)。
(4)若该反应的正反应吸热,则能使该反应的反应速率增大,且平衡向正反应方向移动的是
___________(填序号)。
a.适当升高温度 b.增大X的浓度 c.选择高效催化剂
2.(2021·四川省华蓥中学高一月考)(一)将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g)=xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15
mol·L-1·min-1。
(1)B的反应速率v(B)=_______,x=_______。
(2)A在5 min末的浓度是_______。
(3)此时容器内的压强与开始时之比为_______。
(二)计算下列化学反应的速率:
(4)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物
质B表示此反应的化学反应速率为_______mol·L-1·min-1。
(5)一定温度下,将1 mol N O 充入体积为1 L的密闭容器中,反应3s后,NO 的物质的量为0.6 mol,
2 4 2
则0~3s内的平均反应速率v(NO ) =_______ mol·L-1·s-1。
2
(6)在2 L的密闭容器中,充入2 mol N 和3 mol H ,在一定条件下发生反应,3 s后测得N 为1.9 mol,
2 2 2
则以H 的浓度变化表示的反应速率为_______。
2
3.(2021·陕西陈仓·高一期中)小茗同学所在的化学探究小组用金属铝分别与稀盐酸或稀硫酸反应的方法
研究金属与酸反应的情况及影响反应速率的因素。
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,质量相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g。
(1)小茗同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
反应进程(分钟) 1 2 5 15 20
4.0mol/L盐酸 少量气泡 较多气泡 大量气泡 反应剧烈 反应结束
2.0mol/L硫酸 无明显现象 极少量气泡 少量气泡
4.0mol/L硫酸 无明显现象 少量气泡 有比较连续的气泡
反应1~15min,铝与酸的反应速率逐渐加快,其原因是___________。
(2)小茗同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助小
茗同学完成以下实验设计表(酸均为50.0mL、铝为9.0g):
实
验 金属铝形 盐酸浓度/
实验目的 温度
编 态 mol·L-1
号
① 25˚C 铝片 4. 0
Ⅰ.实验①和②探究盐酸浓度对该反应速率的影响;
② _____ _____ _____
Ⅱ. 实验①和③探究温度对该反应速率的影响;
Ⅲ. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的
③ _____ _____ _____
影响。
④ _____ _____ _____
4.(2021·河南周口·高一月考)碘化钾(KI)是白色半透明的六角形结晶或白色颗粒状粉末,在空气中久置
能被氧化为碘单质。某学校化学课外小组利用该反应原理探究外界条件对化学反应速率的影响。回答下列
问题:
(1)写出酸性KI溶液在空气中被氧化成碘单质的离子方程式:________________。
实验Ⅰ:探究温度对化学反应速率的影响
在四支试管中各加入浓度均为0.5mol·L-1的KI溶液2mL,再滴加3mL同浓度的稀硫酸,同时均滴加2滴指
示剂,用不同温度的水浴进行加热。实验现象记录如下表:
试管组号 ① ② ③ ④
温度/℃ 30 40 50 60
显色时间/s 240 t t t
1 2 3(2)实验中用到的计量仪器除量筒外,还需要___________(写仪器名称)。
(3)滴加的指示剂名称是__________。
(4)该实验结束后,小组成员得出结论:温度每升高10℃,反应速率增大为原来的2倍。
①某同学将 的KI溶液(含指示剂)置于40℃的水浴中加热,80s时溶液开始显色,则c___(填“>”、
“=”或“<”)0.5。
②上表中t=________。
2
实验Ⅱ:探究硫酸浓度对化学反应速率的影响
常温下,取三支试管,先向其中各加入1mL相同浓度的KI溶液(含指示剂),再分别加入2 mol·L-1的硫酸和
一定量蒸馏水,其显色时间如下表所示:
组别 硫酸/mL 蒸馏水/mL 显色时间/s
ⅰ 3 0 120
ⅱ 2 V 140
1
ⅲ 1 V 200
2
(5)实验中加入蒸馏水的目的是___________
(6)通过实验Ⅰ、Ⅱ,本小组得出的实验结论为___________。
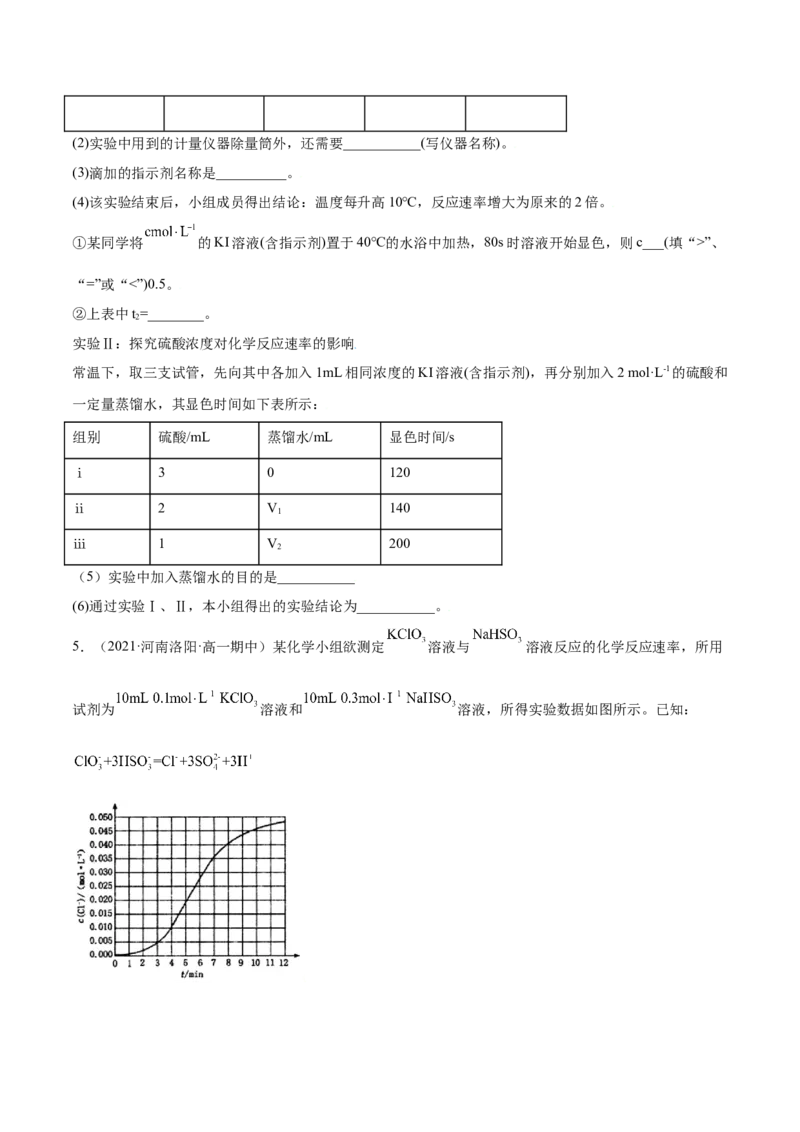
5.(2021·河南洛阳·高一期中)某化学小组欲测定 溶液与 溶液反应的化学反应速率,所用
试剂为 溶液和 溶液,所得实验数据如图所示。已知:(1)该反应在 的化学反应速率 ___________ 。
(2)某同学仔细分析实验数据后发现,在反应过程中该反应的化学反应速率先增大后减小。
Ⅰ.小组同学针对这一现象,通过测定 随时间变化的情况,进一步探究影响因素,具体情况见下表。
方
假设 实验操作
案
该反应放热,使溶液温
向烧杯中加入 溶液和 溶
1 度升高,化学反应速率
提高 液,___________
取 溶液加入烧杯中,向其中加入少量氯化钠固体,
2 ___________
再加入 溶液
分别向标号为①②的两只烧杯中加入 溶液;向烧杯
溶液酸性增强,加快了
3 ①中加入1mL水,向烧杯②中加入 盐酸;然后分别向这两
化学反应速率
只烧杯中加入 溶液
①补全方案1中的实验操作:___________。
②方案2中的假设为___________。
③除方案1、2、3中的假设外,还可以提出的假设是___________。
④在已知方案1的假设不成立的情况下,某同学从控制变量的角度思考,认为方案3中实验操作设计不严
谨,请进行改进:___________。
Ⅱ.反应后期,化学反应速率降低的原因是___________。
6.(2021·浙江省余姚市第七中学高一月考)在一定温度下,在容积为5.0L的密闭容器中发生如下反应:
N(g)+3H(g) 2NH (g),起始时,充入的N 和H 的物质的量分别是3.0mol和6.0mol,2min达化学平衡状
2 2 3 2 2
态,已知2m⇌in内消耗N 平均速率为0.12mol·L‒1·min‒1.试求:
2
(1)达平衡时H 的转化率是___________。
2
(2)平衡时混合气体中N 的体积分数是___________。
2
(3)以下能使此反应速率加快的措施是_______。
①减小容器体积;②升高温度; ③恒容条件通入He ;④恒容条件下通入N
2
(4)下列可以说明该反应达到平衡状态的是____
a.3molH-H键断裂的同时断裂2molN-H键 b.容器内压强保持不变 c.3v (N )=v (H ) d.容器
逆 2 正 2
内混合气体的密度保持不变 e.N 的质量分数保持不变
2倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育