文档内容
第六章 化学反应与能量
第二节 化学反应的速率与限度
第二课时 化学反应的限度及条件控制
【学习目标】1.通过实例分析,体会可逆反应存在限度,理解化学平衡状态的特征,初步学会判断
化学平衡状态,发展“变化观念与平衡思想”的学科核心素养。
2.通过问题探究,发展认识化学的基本角度,能从化学反应限度和快慢的角度解释生产、生活中的
简单化学现象,体会从限度和快慢两各方面去认识和调控化学反应的重要性。
3.通过讨论交流,进一步认识控制反应条件在生产和科学研究中的作用,知道提高燃料的燃烧效率
的重要性和方法,体会化学学科价值,树立将化学知识应用于生产、生活实践的意识。
【学习重点】可逆反应的概念、化学平衡状态的特征及判断、反应条件的控制
【学习难点】可逆反应的理解及化学平衡状态的判断
【课前预习】
旧知回顾:1.除物质本身的性质外,影响化学反应速率的主要因素有哪些?
2.压强对化学反应速率的影响有何特点何规律?
新知预习:1.什么是可逆反应?有何特点?
2.什么是化学平衡状态?有何特征?
【课中探究】
情景导入:观看“炼铁高炉尾气之谜”视频。(视频见PPT)
一、化学反应的限度
活动一、认识可逆反应
任务一、阅读思考:阅读教材P46页内容,结合视频“炼铁高炉尾气之迷”,思考是否所有化学反应都能进行得很完全呢?
任务二、讨论交流:结合教材P 页内容,思考可逆反应的定义是什么?有何特点?
46-47
①定义:
②特点:
注意:
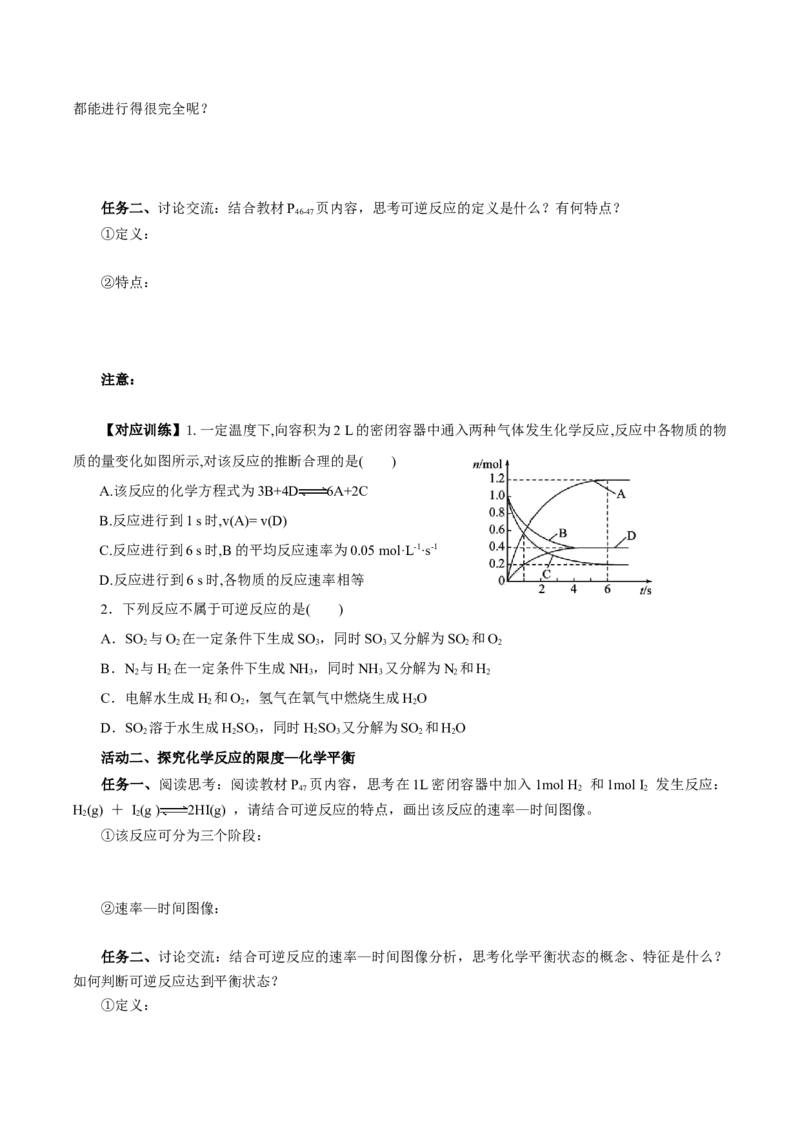
【对应训练】1.一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物
质的量变化如图所示,对该反应的推断合理的是( )
A.该反应的化学方程式为3B+4D 6A+2C
B.反应进行到1 s时,v(A)= v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol·L-1·s-1
D.反应进行到6 s时,各物质的反应速率相等
2.下列反应不属于可逆反应的是( )
A.SO 与O 在一定条件下生成SO ,同时SO 又分解为SO 和O
2 2 3 3 2 2
B.N 与H 在一定条件下生成NH ,同时NH 又分解为N 和H
2 2 3 3 2 2
C.电解水生成H 和O,氢气在氧气中燃烧生成HO
2 2 2
D.SO 溶于水生成HSO ,同时HSO 又分解为SO 和HO
2 2 3 2 3 2 2
活动二、探究化学反应的限度—化学平衡
任务一、阅读思考:阅读教材P 页内容,思考在1L密闭容器中加入1mol H 和1mol I 发生反应:
47 2 2
H(g) + I(g ) 2HI(g) ,请结合可逆反应的特点,画出该反应的速率—时间图像。
2 2
①该反应可分为三个阶段:
②速率—时间图像:
任务二、讨论交流:结合可逆反应的速率—时间图像分析,思考化学平衡状态的概念、特征是什么?
如何判断可逆反应达到平衡状态?
①定义:②建立过程:
③速率—时间图像:
④化学平衡状态的特征概括为:
⑤判断可逆反应已达到平衡状态的依据(标志):
任务三、应用探究:结合教材P 页内容,思考什么是化学反应的限度?研究化学反应的限度有何意
47
义?
【对应训练】1.下列理解错误的是( )
A.化学平衡是一个动态平衡
B.化学反应达到平衡时,正反应速率和逆反应速率相等,是对反应中不同物质而言
C.化学反应速率是研究化学反应进行快慢的问题,化学平衡是研究化学反应进行的限度问题
D.化学平衡研究的对象主要是可逆反应
2.可逆反应:2NO 2NO+O 在体积固定的密闭容器中进行,达到平衡状态的标志是( )
2 2
①单位时间内生成n mol O 的同时生成2n mol NO
2 2
②单位时间内生成n mol O 的同时生成2n mol NO
2
③用NO 、NO、O 表示的反应速率的比为2∶2∶1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦
C.①③④⑤ D.全部
二、化学反应条件的控制
活动一、化学反应条件控制的目的和措施任务一、阅读思考:阅读教材P 最后自然段,思考化学反应条件控制的目的和措施是什么?
47
①目的:
②措施:
任务二、讨论交流:结合教材P48页“思考与讨论”栏目,思考为提高煤的燃烧效率,应如何调控燃
烧反应的条件?
【对应训练】1.生活中家庭常用的燃料气体有三种:天然气、水煤气和液化石油气。天然气和液化石
油气燃烧的主要化学方程式依次为CH+2O CO+2H O,C H+5O 3CO+4H O,现有一套以天然气
4 2 2 2 3 8 2 2 2
为燃料的灶具,今改为烧液化石油气,应采用的正确措施是 ( )
A.减少空气进入量,增大石油气进入量 B.增大空气进入量,减少石油气进入量
C.减少空气进入量,减少石油气进入量 D.增大空气进入量,增大石油气进入量
2.下列措施可以提高燃料燃烧效率的是 ( )
①提高燃料的着火点 ②降低燃料的着火点 ③将固体燃料粉碎 ④将液体燃料雾化处理 ⑤将煤进
行气化处理 ⑥通入适当过量的空气
A.①③④⑤ B.②③⑤⑥
C.③④⑤⑥ D.①②③④
活动二、化工生产中反应条件的调控
任务一、阅读思考:阅读教材P 页第一自然段,思考化工生产(工业合成氨)中理论上该如何调控
48反应条件?
任务二、实例探析:下表的实验数据是在不同温度、压强下,平衡混合物中氨的含量的变化情况(初始
时氮气和氢气的体积比是1:3),根据合成氨反应的数据分析合成氨的适宜条件是什么?
温
氨的含量/%
度/℃
0.1MPa 10MPa 20MPa 30MPa 60MPa 100MPa
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.20 52.0 64.2 71.0 84.2 92.6
400 0.40 25.1 38.2 47.0 65.2 79.8
500 0.10 10.6 19.1 26.4 42.2 57.5
600 0.05 4.50 9.1 13.8 23.1 31.4
理论分析适宜条件:
工业实际适宜条件:
【对应练习】1.工业上合成氨的反应为N(g)+3H(g)========2NH (g),在实际生产中为提高合成氨
2 2 3
的反应速率,下列说法正确的是( )
A.温度越高,反应速率越快,因此采取的温度越高越好
B.压强越大,反应速率越快,因此采取的压强越大越好
C.催化剂能加快反应速率,因此可选用适当的催化剂
D.可向容器中加入一定量的水蒸气,使氨气溶解以提高反应速率
2.硫酸是一种重要的化工产品,目前的重要生产方法是“接触法”,反应原理为:2SO +O
2 2
2SO ,已知该反应为放热反应。则下列说法正确的是
3
A.只要选择适宜的条件,SO 和O 就能全部转化为SO
2 2 3
B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零
C.由反应可知,2mol SO 的能量大于2mol SO 的能量
2 3
D.工业在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和反应速率两方面的问题
【课后巩固】1.下列反应中可判断为可逆反应的是( )
A.氢气在氯气中燃烧生成氯化氢,氯化氢受热分解生成氢气和氯气B.氮气与氢气在高温、高压、催化剂作用下可以生成氨气,同时氨气又分解为氮气和氢气
C.单质溴可以置换出碘,氯气又可以置换出溴
D.氯气和水反应生成盐酸和次氯酸,次氯酸在光照条件下可分解为盐酸和氧气
2.下列关于化学反应限度的说法正确的是( )
A.当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的限度
B.可以通过延长化学反应时间改变化学反应限度
C.平衡状态是一种静止的状态,因为反应物和生成物的浓度不再改变
D.化学反应的限度不可以通过改变条件而发生改变
3.CO和H 在一定条件下可以合成乙醇:2CO(g)+4H(g) CHCHOH(g)+H O(g),下列叙述中能
2 2 3 2 2
说明上述反应在一定条件下已达到最大限度的是 ( )
A.CO全部转化为乙醇
B.正反应和逆反应的化学反应速率均为零
C.CO和H 以1∶2的物质的量之比反应生成乙醇
2
D.反应体系中乙醇的物质的量浓度不再变化
4.将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不
计),在恒定温度下使其达到分解平衡:NH COONH(s) 2NH (g)+CO (g)。可以判断该分解反应已经达
2 4 3 2
到化学平衡状态的是( )
A.2v(NH )=v(CO) B.密闭容器中NH 与CO 的物质的量之比不变
3 2 3 2
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
5.将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧,这样处理的目的是( )
①使煤充分燃烧,提高煤的利用率;②减少SO 的产生,避免造成“酸雨”;③减少有毒CO的产
2
生,避免污染空气;④减少CO 的产生,避免“温室效应”
2
A.①②③ B.②③④
C.①③④ D.①②③④
6.在一定条件下发生反应 2SO (g) 2SO (g)+O(g),将2 mol SO 通入2 L容积恒定的密闭容器甲
3 2 2 3
中,若维持容器内温度不变,5 min末测得SO 的物质的量为0.8 mol。则下列说法正确的是( )
3
A.0~5min,SO 的生成速率v(SO )=0.12mol·L-1·min-1
2 2
B.若起始时充入3 mol SO ,起始时SO 分解速率不变
3 3
C.若某时刻消耗了1 molSO 同时生成了0.5molO,则表明该反应达到了平衡状态
3 2
D.达到平衡时,SO 和SO 的浓度相等
2 3
7.一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g)正反应
为放热反应,经60 s达到平衡,生成0.3 mol Z。下列说法正确的是 ( )A.以X浓度变化表示的反应速率为0.001 mol·L-1·s-1
B.反应经过60 s时一定能达到化学平衡
C.反应放出的热量可用于提高反应速率
D.反应达到平衡时,n(X)∶n(Y)=1∶1
8.在2 L密闭容器内,800 ℃时发生反应:2NO(g)+O(g) 2NO (g),n(NO)随时间的变化如下
2 2
表:
时间/s 0 1 2 3 4 5
n(NO)/mol 0.20 0.1 0.08 0.07 0.07 0.07
(1)上述反应是不是可逆反应 (填“是”或“否”);在3 s时NO的转化率为 。
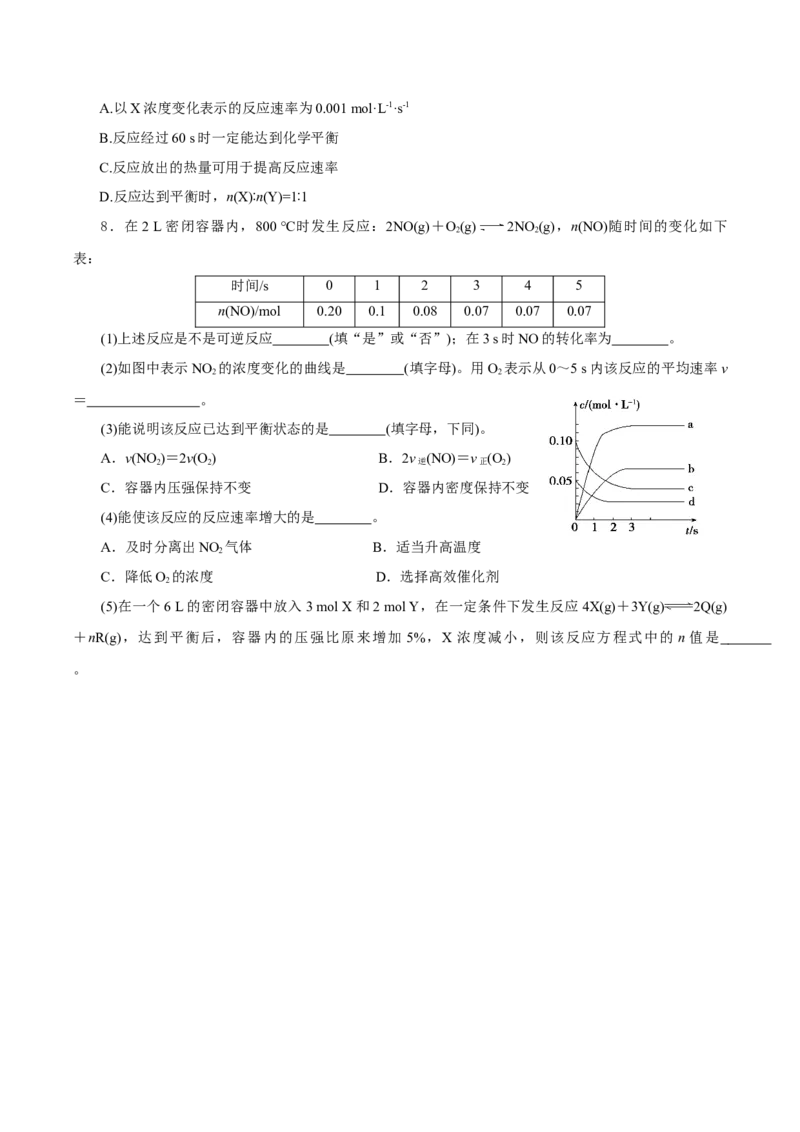
(2)如图中表示NO 的浓度变化的曲线是 (填字母)。用O 表示从0~5 s内该反应的平均速率v
2 2
= 。
(3)能说明该反应已达到平衡状态的是 (填字母,下同)。
A.v(NO )=2v(O ) B.2v (NO)=v (O )
2 2 逆 正 2
C.容器内压强保持不变 D.容器内密度保持不变
(4)能使该反应的反应速率增大的是 。
A.及时分离出NO 气体 B.适当升高温度
2
C.降低O 的浓度 D.选择高效催化剂
2
(5)在一个6 L的密闭容器中放入3 mol X和2 mol Y,在一定条件下发生反应4X(g)+3Y(g) 2Q(g)
+nR(g),达到平衡后,容器内的压强比原来增加 5%,X 浓度减小,则该反应方程式中的 n 值是
。