文档内容
6.2 化学反应速率及限度(精练)
题组一 化学反应速率的计算
1.(2021·福建·文博中学高一期中)反应4NH (g)+5O(g) 4NO(g)+6H O(g)在恒容密闭容器中进行,
3 2 2
30 s后NH 的物质的量浓度减小了3 mol•L﹣1,则对此反应的速率的表示正确的是
3
A.v(H O)=0.15 mol•(L•s)﹣1 B.v(O )=0.1 mol•(L•s)﹣1
2 2
C.v(NH )=0.2 mol•(L•s)﹣1 D.v(O ):v(NO)=4:5
3 2
【答案】A
【解析】A.30 s后NH 的物质的量浓度减小了3 mol•L﹣1,则根据物质反应转化关系可知HO的浓度改变
3 2
了△n(H O)= n(NH )=4.5 mol/L,则v(H O)= ,A正确;
2 3 2
△
B.△n(NH )=3 mol/L,则△n(O )= n(NH )=3.75 mol/L,v(O )= ,B错误;
3 2 3 2
△
C.v(NH )= ,C错误;
3
D.用不同物质化学反应速率时,速率比等于化学方程式中相应物质的化学计量数的比,则v(O ):
2
v(NO)=5:4,故合理选项是A。
2.(2021·吉林·长春市清蒲中学高一期中)一定温度条件中,在密闭容器中,投入一定量 发生2SO (g)
2
+O (g) 2SO (g),5min达到平衡, 的浓度为1mol/L,则用 表示的速率为
2 3
A. B.0.2 mol•L-1•min-1
C. D.
【答案】B
【解析】用 表示的速率为: 0.2 mol•L-1•min-1,故答案为:B。
3.(2021·浙江杭州)某温度时,浓度都是 的两种气体 和 ,在密闭容器中发生可逆反应生成气体Z,充分反应后 的浓度为 , 的浓度为 ,生成的Z的浓度为 ,则
该反应的化学方程式(Z用X、Y表示)是
A. B.
C. D.
【答案】B
【解析】X 浓度变化量为0.6 mol/L,Y 的浓度变化量为0.4mol/L,Z的浓度变化为0.4mol/L,对于同一反
2 2
应,同一时间,浓度变化量之比等于化学计量数之比;故反应为 。
答案选B。
4.(2021·湖北宜昌)将气体X、Y置于容积为2L的密闭容器中,发生如下反应: 。
反应进行到4s末,测得X为 0.5 mol,Y为 0.4 mol,Z为 0.2 mol。则用反应物X浓度的减少来表示该反
应速率为
A.0.025 B.0.0125
C.0.05 D.0.1
【答案】C
【解析】反应进行到4s末,测得Z为 0.2 mol,根据方程式可知消耗X是0.4mol,浓度是0.2mol/L,则用
反应物X浓度的减少来表示该反应速率为0.2mol/L÷4s=0.05 。
答案选C。
5.(2021·浙江·嘉兴市第五高级中学 )在一密闭容器中充入一定量的N 和H,经测定反应开始后的2s
2 2
内氢气的平均速率:v(H )=0.45mol/(L·s),则2s末NH 的浓度为
2 3
A.0.45mol/L B.0.50mol/L
C.0.55mol/L D.0.60mol/L
【答案】D
【解析】v(H )=0.45mol/(L·s),则2s内氢气的浓度减少0.45mol/(L·s)×2s=0.9 mol/L,根据反应方程式
2
,氨气的浓度为0.9 mol/L =0.6 mol/L,选D。6.(2021·河南 )在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知
v(A)、v(B)、v(C)之间有以下关系:2v(B)=3v(A),2v(B)=3v(C),则此反应可表示为
A.2A+3B=2C B.A+2B=C C.3A+2B=2C D.2A+2B=3C
【答案】A
【解析】由2v(B)=3v(A),2v(B)=3v(C)可得出,v(A)=v(C)= v(B),所以v(A):v(B):v(C)=2:3:2,反应的化学
方程式为2A+3B=2C,故选A。
7.(2021·河南·辉县市第一高级中学高一月考)将固体 置于2L的密闭容器中,在恒温的条件下发
生如下反应: , 。2min时测得 的浓度为 ,
HBr的浓度为8 ,则上述反应中0~2min内生成 的速率为
A.0.5 B.2
C.2.5 D.5
【答案】D
【解析】此题为连锁反应,溴化铵分解生成的溴化氢又有一部分分解,故剩余的溴化氢的量为溴化铵分解
生成的溴化氢的量减去分解的溴化氢的量,即c (HBr)=c (HBr)-c (HBr),氢气的浓度为 ,
剩余 生成 分解
则c (HBr)=2mol/L,HBr的的浓度为8 ,则c (HBr)=c (HBr)+c (HBr)=10mol/L,溴化铵分
分解 生成 分解 剩余
解生成的氨气浓度与溴化氢浓度相等,则2min后溴化铵分解生成的氨气的浓度为:c(NH )=c
3 生成
(HBr)=10mol/L,氨气的平均反应速率为: =5 mol/(L•min),答案选D。
8.(2021·新疆伊犁·高一期末)在一定条件下发生反应:N+3H 2NH ,经2min后N 的物质的量浓
2 2 3 2
度减小了0.4mol·L-1,则用H 表示的平均反应速率为
2
A.0.4mol·L-1·s-1 B.0.2mol·L-1·min-1
C.0.6mol·L-1·min-1 D.0.4mol·L-1·min-1【答案】C
【解析】经2min后N 的物质的量浓度减小了0.4mol·L-1,则v(N )= =0.2mol·L-1,不同物质表示
2 2
的反应速率之比等于计量数之比,所以v(H )=3v(N)=0.6mol·L-1;故答案为C。
2 2
9.(2021·河南9)在2L恒容密闭容器中进行反应: 。已知反应过程中某一
时刻 、 、 物质的量分别为1.0mol、3.0mol、4.0mol,当反应达到平衡时,可能存在的数据是
A. 为 B. 、 均为
C. 为 D. 为
【答案】C
【解析】根据极值法讨论假设反应正向进行到底, 、 完全反应生成2molXY ,加上原来的4mol,故
3
XY 的最大浓度为3mol/L;假设反应逆向进行到底,4.0mol 完全反应生成2mol 、6mol ,加上原
3
来的1.0mol 、3.0mol , 的浓度为1.5mol/L、 的浓度为4.5mol/L,由于可逆反应不可能完全进行
到底,故0 = 放热
(4)ab
【解析】(1)反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,,则反应的化学方程式为3X+Y 2Z;
(2)反应开始至2min,气体Z的平均反应速率为 0.05 mol·L-1·min-1;
(3)①若X、Y、Z均为气体:1min后X、Y物质的量继续减少,Z物质的量继续增加,反应正向进行,
所以v >v ,2min时反应达到平衡状态,v =v ;
正 逆 正 逆
②若此时将容器的体积缩小到原来的一半,平衡正向移动,达到平衡时,容器内温度升高(容器不与外界进
行热交换),说明该反应的正反应为放热反应;
(4)a.正反应吸热,适当升高温度,反应的反应速率增大,且平衡向正反应方向移动,故选a;
b.增大X的浓度,反应的反应速率增大,且平衡向正反应方向移动,故选b;
c.选择高效催化剂,平衡不移动,故不选c;选ab。
2.(2021·四川省华蓥中学高一月考)(一)将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g)=xC(g)+2D(g),5 min 后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=1∶2,C的反应速率是 0.15
mol·L-1·min-1。
(1)B的反应速率v(B)=_______,x=_______。
(2)A在5 min末的浓度是_______。
(3)此时容器内的压强与开始时之比为_______。
(二)计算下列化学反应的速率:
(4)在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物
质B表示此反应的化学反应速率为_______mol·L-1·min-1。
(5)一定温度下,将1 mol N O 充入体积为1 L的密闭容器中,反应3s后,NO 的物质的量为0.6 mol,
2 4 2
则0~3s内的平均反应速率v(NO ) =_______ mol·L-1·s-1。
2
(6)在2 L的密闭容器中,充入2 mol N 和3 mol H ,在一定条件下发生反应,3 s后测得N 为1.9 mol,
2 2 2
则以H 的浓度变化表示的反应速率为_______。
2
【答案】
(1) 0.05 mol·L-1·min-1 3
(2)0.5 mol·L-1
(3)11∶10
(4)0.6
(5)0.2
(6)0.05 mol·L-1·s-1
【解析】(1)5 min 后测得c(D)=0.5 mol·L-1,则反应消耗B的浓度△c(B)= c(D)=0.25 mol·L-1,故用B的浓度变化
表示的化学反应速率v(B)= ;
化学反应速率比等于化学方程式中相应物质的化学计量数的比。C的反应速率是 0.15 mol·L-1·min-1,
v(B):v(C)=0.05:0.15=1:3,解得x=3;
(2)假设反应开始时A、B的物质的量都是x mol,5 min时生成D的浓度是0.5 mol/L,则产生D的物质
的量n(D)=0.5 mol/L×2 L=1 mol,根据物质反应转化关系可知反应产生A物质的量是1.5 mol,消耗B物质
的量是0.5 mol,此时A、B的物质的量分别是(x-1.5)mol、(x-0.5) mol,此时c(A)∶c(B)=1∶2,由于容器的
容积相同,物质的浓度比等于物质的量的比,所以(x-1.5):(x-0.5)=1:2,解得x=2.5 mol,则5 min末A的
物质的量是2.5 mol-1.5 mol=1 mol,故A的浓度c(A)= ;
(3)5 min时C的物质的量n(C)=0.15 mol/(L·min)×2 L×5 min=1.5 mol。在同温同体积时,气体的压强之比
等于物质的量之比,反应后气体的物质的量之和为1 mol+ (2.5-0.5) mol+ 1.5 mol+1 mol= 5.5 mol,起始时气
体的物质的量为2.5 mol+ 2.5 mol=5 mol ,则此时容器内的压强与开始时之比为5.5:5=11:10;
(4)用不同物质表示反应速率时,速率比等于化学方程式中相应物质的化学计量数的比。v(A)=0.2
mol/(L·min),则以物质B表示此反应的化学反应速率v(B)=3v(A)=3×0.2 mol/(L·min)=0.6 mol/(L·min);
(5)0~3s内的平均反应速率v(NO )= mol/(L·s);
2
(6)反应开始时n(N )=2 mol,3 s后n(N )=1.9 mol,△n(N )=0.1 mol,则根据物质反应消耗关系可知
2 2 2
△n(H )=0.3 mol,故以H 的浓度变化表示的反应速率v(H )= mol/(L·s)。
2 2 2
3.(2021·陕西陈仓·高一期中)小茗同学所在的化学探究小组用金属铝分别与稀盐酸或稀硫酸反应的方法
研究金属与酸反应的情况及影响反应速率的因素。
实验药品:2.0moL/L盐酸、4.0mol/L盐酸、2.0mol/L硫酸、4.0mol/L硫酸,质量相同的铝片和铝粉(金
属表面氧化膜都已除去);每次实验各种酸的用量均为50.0mL,金属用量均为9.0g。
(1)小茗同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
反应进程(分钟) 1 2 5 15 20
4.0mol/L盐酸 少量气泡 较多气泡 大量气泡 反应剧烈 反应结束2.0mol/L硫酸 无明显现象 极少量气泡 少量气泡
4.0mol/L硫酸 无明显现象 少量气泡 有比较连续的气泡
反应1~15min,铝与酸的反应速率逐渐加快,其原因是___________。
(2)小茗同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助小
茗同学完成以下实验设计表(酸均为50.0mL、铝为9.0g):
实
验 金属铝形 盐酸浓度/
实验目的 温度
编 态 mol·L-1
号
① 25˚C 铝片 4. 0
Ⅰ.实验①和②探究盐酸浓度对该反应速率的影响;
② _____ _____ _____
Ⅱ. 实验①和③探究温度对该反应速率的影响;
Ⅲ. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的
③ _____ _____ _____
影响。
④ _____ _____ _____
【答案】(1)铝与酸反应放热,随反应进行,溶液温度升高,反应速率加快
(2) 25℃ 铝片 2.0mol/L 35℃ 铝片 4.0 mol/L 25℃ 铝粉 4.0 mol/L
【解析】(1)该反应是放热反应,随着反应的进行,放出的能量越多,溶液的温度升高,温度越高反应
速率越快。
(2)②根据题意知,①和②只有盐酸浓度不同,其它完全相同进行实验。
③根据题意,实验①和③只有温度不同,其它完全相同进行实验。
④根据题意,实验①和④只有金属规格不同,其它完全相同进行实验。
4.(2021·河南周口·高一月考)碘化钾(KI)是白色半透明的六角形结晶或白色颗粒状粉末,在空气中久置
能被氧化为碘单质。某学校化学课外小组利用该反应原理探究外界条件对化学反应速率的影响。回答下列
问题:
(1)写出酸性KI溶液在空气中被氧化成碘单质的离子方程式:________________。
实验Ⅰ:探究温度对化学反应速率的影响
在四支试管中各加入浓度均为0.5mol·L-1的KI溶液2mL,再滴加3mL同浓度的稀硫酸,同时均滴加2滴指
示剂,用不同温度的水浴进行加热。实验现象记录如下表:
试管组号 ① ② ③ ④温度/℃ 30 40 50 60
显色时间/s 240 t t t
1 2 3
(2)实验中用到的计量仪器除量筒外,还需要___________(写仪器名称)。
(3)滴加的指示剂名称是__________。
(4)该实验结束后,小组成员得出结论:温度每升高10℃,反应速率增大为原来的2倍。
①某同学将 的KI溶液(含指示剂)置于40℃的水浴中加热,80s时溶液开始显色,则c___(填“>”、
“=”或“<”)0.5。
②上表中t=________。
2
实验Ⅱ:探究硫酸浓度对化学反应速率的影响
常温下,取三支试管,先向其中各加入1mL相同浓度的KI溶液(含指示剂),再分别加入2 mol·L-1的硫酸和
一定量蒸馏水,其显色时间如下表所示:
组别 硫酸/mL 蒸馏水/mL 显色时间/s
ⅰ 3 0 120
ⅱ 2 V 140
1
ⅲ 1 V 200
2
(5)实验中加入蒸馏水的目的是___________
(6)通过实验Ⅰ、Ⅱ,本小组得出的实验结论为___________。
【答案】(1)
(2)秒表(或计时器)、温度计
(3)淀粉溶液
(4)> 60
(5)保持溶液总体积不变
(6)其他条件不变时,升高温度或者增大反应物的浓度,反应速率均增大
【解析】(1) 在空气中被氧气氧化成碘单质,氧气作氧化剂,KI作还原剂,碘单质为氧化产物,则酸性
KI溶液在空气中被氧化,结合酸性、电子守恒、原子守恒、电荷守恒可知反应的离子方程式为:
,故答案为: 。(2)反应中需要控制温度变量,因此需用到温度计调控不同的温度条件,另外需测定反应在不同温度下反应
结束的时间,因此需用到秒表或其他计时器,故答案为:秒表(或计时器)、温度计。
(3)碘离子被氧化成碘单质,碘遇淀粉变蓝色,故可用淀粉作该反应的指示剂,故答案为:淀粉溶液。
(4)①温度每升高10℃,反应速率增大为原来的2倍,则 的 溶液(含指示剂)在40℃的水
浴中加热, t=120s,, 的KI溶液(含指示剂)置于40℃的水浴中加热,80s时溶液开始显色,根据
1
浓度越大反应速率越快,可知c>0.5,故答案为:>。
②根据温度每升高10℃,反应速率增大为原来的2倍,则所需时间缩小1倍,则t=60。
2
实验Ⅱ:(5)由表格数据可知三支试管中所加硫酸的体积不同,而加入的碘化钾是相同的,为了比较硫酸的
浓度对反应速率的影响,因此加入的蒸馏水的目的是使三组硫酸溶液体积相同,硫酸的浓度不同。
(6)通过实验Ⅰ、Ⅱ,本小组得出的实验结论为其他条件不变时,升高温度或者增大反应物的浓度,反应速
率均增大。
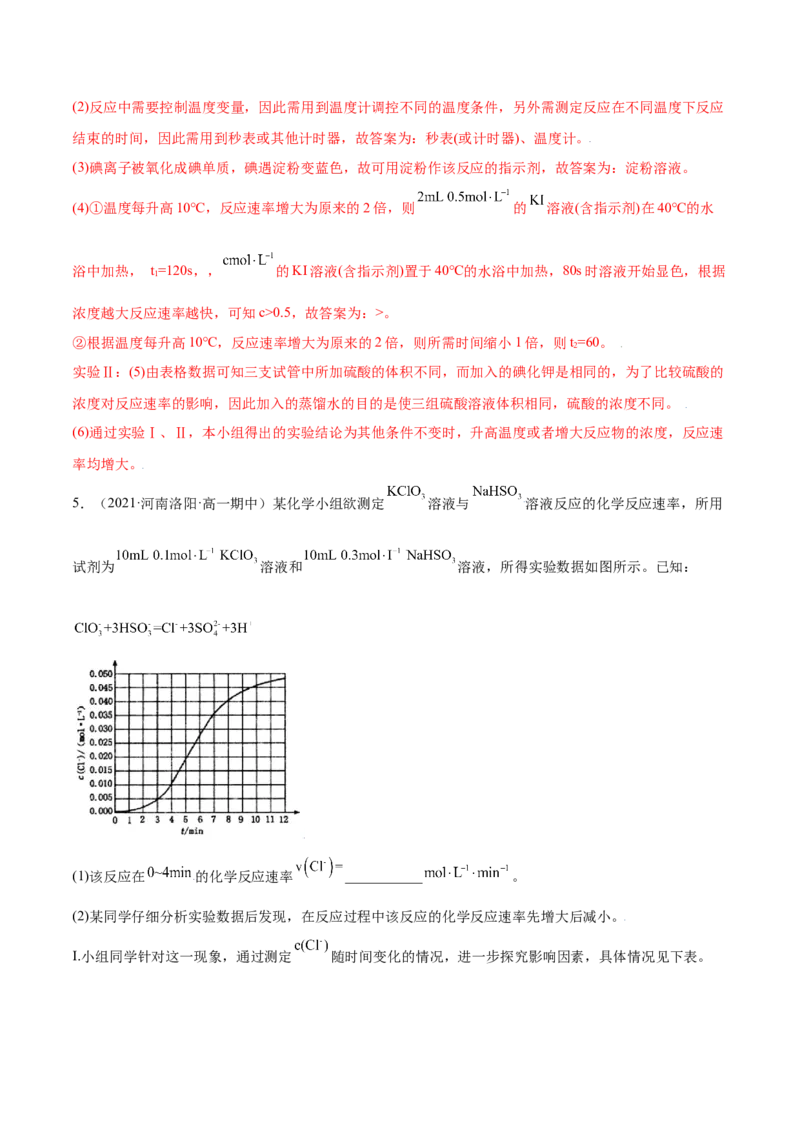
5.(2021·河南洛阳·高一期中)某化学小组欲测定 溶液与 溶液反应的化学反应速率,所用
试剂为 溶液和 溶液,所得实验数据如图所示。已知:
(1)该反应在 的化学反应速率 ___________ 。
(2)某同学仔细分析实验数据后发现,在反应过程中该反应的化学反应速率先增大后减小。
Ⅰ.小组同学针对这一现象,通过测定 随时间变化的情况,进一步探究影响因素,具体情况见下表。方
假设 实验操作
案
该反应放热,使溶液温
向烧杯中加入 溶液和 溶
1 度升高,化学反应速率
液,___________
提高
取 溶液加入烧杯中,向其中加入少量氯化钠固体,
2 ___________
再加入 溶液
分别向标号为①②的两只烧杯中加入 溶液;向烧杯
溶液酸性增强,加快了
3 ①中加入1mL水,向烧杯②中加入 盐酸;然后分别向这两
化学反应速率
只烧杯中加入 溶液
①补全方案1中的实验操作:___________。
②方案2中的假设为___________。
③除方案1、2、3中的假设外,还可以提出的假设是___________。
④在已知方案1的假设不成立的情况下,某同学从控制变量的角度思考,认为方案3中实验操作设计不严
谨,请进行改进:___________。
Ⅱ.反应后期,化学反应速率降低的原因是___________。
【答案】(1)0.0025
(2)① 插入温度计 ② 生成的 加快了化学反应速率 ③生成的 加快了化学反应速率
④将1mL水改为 的NaCl溶液 (II)反应物浓度降低
【解析】(1) 根据实验数据可知,该反应在 0 4min 的平均反应速率:
∼
,故答案为:0.0025
(2) ①假设1提出该反应放热使得速率加快,所以应在一开始就测量温度,测量温度需要温度计;故答案
为:插入温度计;
②方案2的操作中加入了氯化钠固体,则会使生成的氯离子浓度变大,所以假设可以为生成的Cl−加快了化
学反应速率;故答案为:生成的Cl−加快了化学反应速率;
③还可以根据加入含有硫酸根离子的固体物质不同提出假设,即生成的 加快了化学反应速率;故答案
为:生成的 加快了化学反应速率;④方案3中向烧杯①中加入1mL水相当于直接稀释了该溶液,则变量不唯一了,需要保持两只烧杯中除氢
离子外参加反应的各离子浓度不变,所以可以将1mL水改为1mL0.2mol/L NaCl溶液,就能使两溶液中氯
离子浓度也保持一致;故答案为:将1mL水改为1mL0.2mol/L NaCl溶液;
Ⅱ.随着化学反应的进行,体系中的各物质浓度都会逐渐降低,所以反应速率也会逐渐减慢;故答案为:
反应物浓度降低。
6(2021·浙江省余姚市第七中学高一月考)在一定温度下,在容积为5.0L的密闭容器中发生如下反应:
N(g)+3H(g) 2NH (g),起始时,充入的N 和H 的物质的量分别是3.0mol和6.0mol,2min达化学平衡状
2 2 3 2 2
态,已知2m⇌in内消耗N 平均速率为0.12mol·L‒1·min‒1.试求:
2
(1)达平衡时H 的转化率是___________。
2
(2)平衡时混合气体中N 的体积分数是___________。
2
(3)以下能使此反应速率加快的措施是_______。
①减小容器体积;②升高温度; ③恒容条件通入He ;④恒容条件下通入N
2
(4)下列可以说明该反应达到平衡状态的是____
a.3molH-H键断裂的同时断裂2molN-H键 b.容器内压强保持不变 c.3v (N )=v (H ) d.容器
逆 2 正 2
内混合气体的密度保持不变 e.N 的质量分数保持不变
2
【答案】
(1)60
(2)27.3%
(3)①②④
(4)bce
【解析】(1)在一定温度下,在容积为5.0L的密闭容器中发生如下反应: N (g) + 3H (g)= 2NH (g),起始时,
2 2 3
充入的N 和H 的物质的量分别是3.0mol和6.0mol,,2 min达化学平衡状态,此时生成NH 的N 平均速率
2 2 3 2
为0.12mol·L‒1·min‒1.,则N 的变化量为n(N )= 0.12mol·L‒1·min‒1 2 min 5.0L=1.2mol,根据
2 2
N (g) + 3H (g)= 2NH (g)反应,H 的变化量为n(H )= 3.6mol,达平衡时H 的转化率= =60
2 2 3 2 2 2
,故答案:60 。
(2)根据平衡时混合气体中N 的体积分数= =27.3%,故答案:27.3%。
2
(3)根据N (g) + 3H (g)= 2NH (g)反应可知,①减小容器体积相当增大容器压强、②升高温度都可以加快
2 2 3
此反应速率;③恒容条件通入He,对反应速率无影响;④恒容条件下通入N,增加了反应物浓度,可以
2
加快此反应速率。故答案:①②④。
(4)a.根据N (g) + 3H (g)= 2NH (g)反应可知,3molH-H键断裂的同时断裂2molN-H键,反应正向进行,
2 2 3
没有达到平衡,故a不符合题意;
b.根据N (g) + 3H (g)= 2NH (g)反应可知,化学反应两边计量数不等,所以容器内压强保持不变,说明
2 2 3
该反应达到平衡状态,故b符合题意;
c.根据N (g) + 3H (g)= 2NH (g)反应可知,当3v (N )=v (H ) 时,正逆反应速率相等, 说明该反应达
2 2 3 逆 2 正 2
到平衡状态,故c符合题意;
d.根据N (g) + 3H (g)= 2NH (g)反应可知,体积一定时,容器内混合气体的密度是常数,所以容器内混
2 2 3
合气体的密度保持不变,不能作为判断平衡的依据,故d不符合题意;
e.根据N (g) + 3H (g)= 2NH (g)反应可知,当N 的质量分数保持不变,说明N 的浓度保持不变,说明该
2 2 3 2 2
反应达到平衡状态,故e符合题意;
故答案为: bce。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育