文档内容
第七章 有机化合物
第一节 认识有机化合物
第一课时 烷烃的结构
【学习目标】1.通过阅读思考、模型制作、动画演示等,认识甲烷的分子结构特点,掌握甲烷的结
构式、电子式,建立甲烷的立体结构模型,知道甲烷的正四面体结构。
2.通过对比分析、归纳总结,认识烷烃同系物在组成、结构上的共同点,形成同系物的概念,并能对
同系物进行判断。
【学习重点】有机化合物中碳原子的成键特点、烷烃的结构
【学习难点】同系物概念的理解及烷烃同系物的判断
【课前预习】
旧知回顾:1.有机物的定义是什么?元素组成有何特点?
【答案要点】 ①有机物是指 含有C元素 的化合物,但 CO、HCO 及其盐 等除外。
2 2 3
②有机化合物的组成元素:有机物中一定含有碳元素,常含有氢、氧元素,有的还含有氮、硫、磷、
卤素等;含碳元素的化合物不一定都是有机物。如CO、CO、碳酸盐、氰化物等为无机物。
2
2.如何鉴别甲烷、一氧化碳、氢气这三种无色无味的气体?
【答案要点】先分别取样点燃三种气体,再将燃烧后的气体产物分别依次通过无水硫酸铜,澄清石灰
水。如果只有硫酸铜变色就是氢气,只有石灰水变混浊就是一氧化碳,硫酸铜变色石灰水同时变混浊就是
甲烷。
新知预习:1.最简单的有机化合物是什么?其结构有何特点?
【答案要点】 ①最简单的有机化合物是甲烷,甲烷是天然气、沼气 、油田气和 煤矿坑道气的主要成
分。
②甲烷的分子式为CH,分子为 正四面体结构,电子式为 ,结构式为 。
4
2.有机化合物中碳原子的结构及成键有何特点?
【答案要点】①机物中,碳原子可以形成4 个共价键。
②碳原子间成键方式多样:碳碳之间的结合方式有单键、双键、三键;多个碳原子之间可以结合成碳
链,也可以结合成碳环(且可带支链)。
③有机物分子可能只含有一个或几个碳原子,也可能含有成千上万个碳原子;含有相同碳原子数的有
机物分子,可能因为碳原子间成键方式或碳骨架的不同而具有多种结构。
【课中探究】
情景导入:当今社会,清洁、环保的能源成为时代新宠,低碳社会来临,全球能源结构待变。全球都
将目标指向一种储量巨大、清洁环保、前景广阔的“特殊天然气”,它就是“可燃冰”,又称天然气水合
物,其主要成分是甲烷。我国经过十几年艰苦的努力,于2007年5月1日、2009年9月25日先后宣布在南海海域和青海陆域冻土带钻获“可燃冰”实物样品,我国台湾的“可燃冰”研究也处于国际领先水平。
那么,甲烷的分子结构有什么特点?具备什么样的性质?它作为新生代能源又有什么优势呢?我们将在下
面的学习中找到答案。(图片见PPT)
一、有机化合物中碳原子的成键特点
活动一、最简单的有机化合物—甲烷
任务一、阅读教材“前言”相关内容,观察图片,联系生活实际,举例说明什么是有机化合物?与无
机物相比有何特点?
【答案要点】①有机化合物是指含有C元素的化合物,简称有机物,但 CO、HCO 及其盐等除外。
2 2 3
②有机化合物与人类的生活有密切的关系,在衣、食、住、行、医疗、能源、材料、科学技术及工农
业生产等领域中都起着重要作用,迄令为止已经超过2000万种。
③与无机物相比,有机物不仅数量很多,而且分布极广。如常见燃料中的汽油、煤油、柴油;建材中
的木材、黏合剂、涂料、油漆;日用品中的塑料、橡胶、纤维、清洁剂;食物中的营养餐—糖类、油脂、
蛋白质等都是有机化合物。
④有机化合物除一定含有碳元素外,它还可以含有氢、氧、氮、硫、磷、卤素等。
任务二、阅读教材P60页内容,结合教材P62页图7-5,思考甲烷分子结构有哪些表示方法?完成下
表内容。
【答案要点】甲烷结构的表示方法
类别 表示方法 含义
用元素符号表示物质分子组成的式子,可反映一个分子中原子
分子式 CH
4 的种类和数目
用小黑点等符号代替电子,表示原子最外层电子成键情况的式
电子式
子
①具有化学式所能表示的意义,能反映物质的结构;②表示分
结构式
子中原子的结合或排列顺序的式子,但不表示空间构型
小球表示原子,短棍表示价键(单键、双键或三键)(甲烷键角
♦球棍模型
109028′)
♦空间填充模
用不同体积的小球表示不同大小的原子
型
【对应训练】1.下列说法正确的是( )
A.含碳元素的化合物都是有机物
B.易溶于汽油、酒精、苯等有机溶剂的物质一定是有机化合物
C.大多数有机物分子中碳原子与碳原子之间或碳原子与其他原子之间相结合的化学键是非极性共价键或极性共价键
D.有机物完全燃烧只可能生成CO 和HO
2 2
【答案】C
【解析】有机物通常是指含碳元素的化合物,但 CO、CO 、NaCO 等少数物质,虽含有碳元素,但
2 2 3
其性质却跟无机物相似,故一般把它们归为无机物,A项错误;易溶于汽油、酒精、苯等有机溶剂的物质
不一定是有机化合物,如溴单质易溶于有机溶剂,但溴是无机物,B项错误;有机物中碳原子与碳原子之
间不论是形成单键、双键或三键,都是非极性共价键,而碳原子与其他元素原子之间形成的化学键为极性
共价键,C项正确;有些有机物除含碳、氢、氧外,还含有氮、硫、卤素、磷等,它们完全燃烧可能还会
生成SO 、氮的氧化物等物质,D项错误。
2
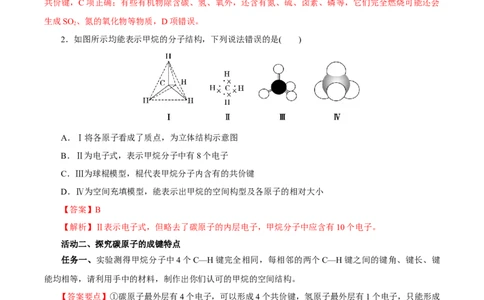
2.如图所示均能表示甲烷的分子结构,下列说法错误的是( )
A.Ⅰ将各原子看成了质点,为立体结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间充填模型,能表示出甲烷的空间构型及各原子的相对大小
【答案】B
【解析】Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
活动二、探究碳原子的成键特点
任务一、实验测得甲烷分子中4个C—H键完全相同,每相邻的两个C—H键之间的键角、键长、键
能均相等,请利用手中的材料,制作出你们认可的甲烷的空间结构。
【答案要点】①碳原子最外层有4个电子,可以形成4个共价键,氢原子最外层有1个电子,只能形成
1个共价键,因此甲烷的分子式为CH。
4
②甲烷分子的空间构型为正四面体,C原子位于正四面体的中心,H原子位于四面体的顶点,四个C-
H键的键长、键能、键角都相同(等价),甲烷分子中最多有3 个原子在同一平面内。
③在上述几种表示甲烷分子结构的方法中,球棍模型及空间填充模型均能反映甲烷分子的空间构型,
但空间填充模型更能形象的表达出H、C的位置及所占比例;电子式只反映原子的最外层电子的成键情
况。
任务二、结合教材P60页及P61页“思考与讨论”内容,观察图7-1和7-3,利用两个或多个碳原子及
多个氢原子制作更多的有机物分子空间模型,分析有机物种类繁多的主要原因是什么?【答案要点】①碳原子所成价键多:有机化合物中,碳原子最外层有4个单电子,可以形成4个共价
键,比氮、氧、氢或卤素原子所成价键都要多。
②碳原子成键方式多样:含有多个碳原子的有机化合物,碳原子间成键方式较多,可以形成单键,也
可以形成双键或叁键。
③碳骨架多样:碳原子间所成骨架有多种,可以是直链,也可以成环,也可以带支链。
④成链原子及种类多而灵活:有机物分子中碳原子可以与一个或若干个碳原子成键,也可以和其他原
子如H、O、N、S等成键,数目不等。
【对应训练】1.只含C、H元素的有机物分子中的碳原子与其他原子的结合方式是( )
A.通过两个共价键 B.通过非极性键
C.形成四对共用电子对 D.通过离子键和共价键
【答案】C
【解析】碳原子核外最外层有四个电子,在形成有机化合物时与其他原子可形成四对共用电子对,C
正确,故选C。
2.有机物种类繁多的原因是( )
A.碳元素在地壳中的含量大,且属于非金属
B.碳原子间能以共价键结合,形成多种链状和环状结构
C.碳元素所形成的化合物性质稳定,且共价键键能大
D.碳原子中质子数和中子数相等
【答案】B
【解析】有机物分子中碳原子间能以共价键结合形成4个共价键,而且可以形成链状或环状等结构,
是导致有机物种类繁多的原因,B正确。
二、认识烷烃
活动一、探究烷烃的结构
任务一、阅读教材P62页内容,结合“思考与讨论”栏目,完成表格填空,根据碳原子的成键规律和
下表中提供的信息,试着写出丁烷的结构烷、丙烷、丁烷等一系列的有机化合物分子式,并归纳出该类有机
物分子式的通式式什么?
【答案要点】
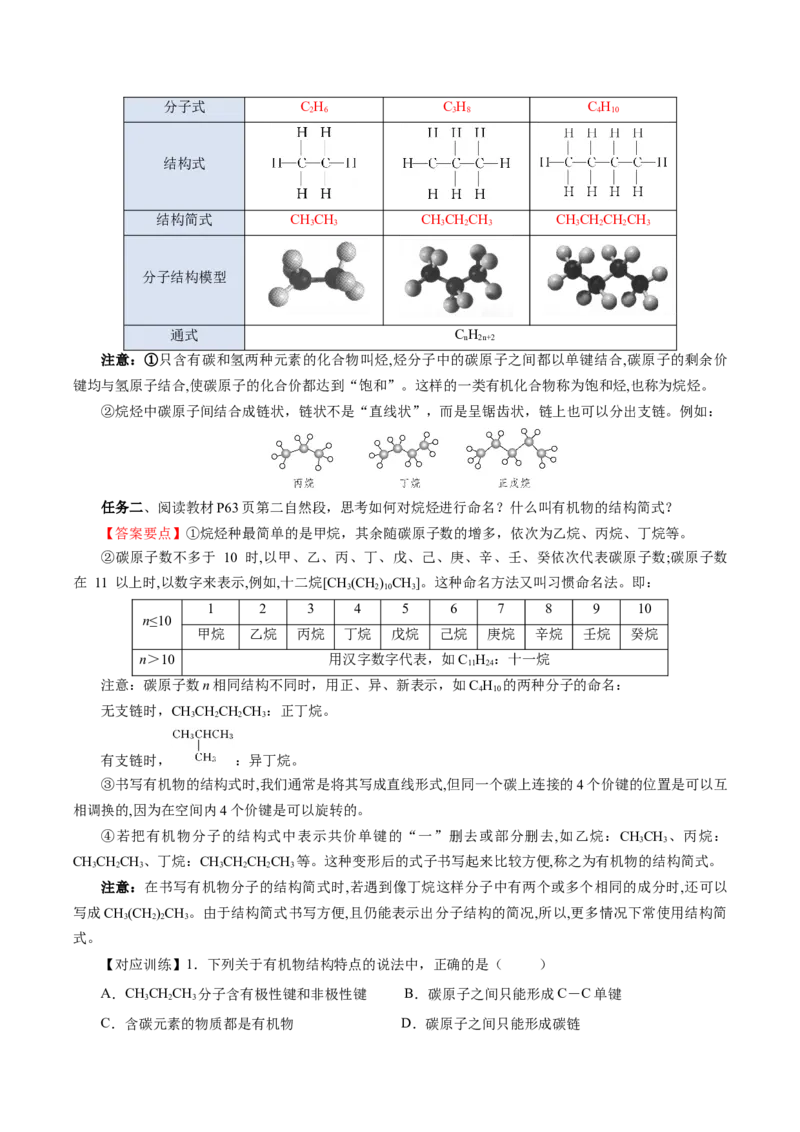
烷烃 乙烷 丙烷 正丁烷
分子中碳原子数 2 3 4分子式 C H C H C H
2 6 3 8 4 10
结构式
结构简式 CHCH CHCHCH CHCHCHCH
3 3 3 2 3 3 2 2 3
分子结构模型
通式 C H
n 2n+2
注意:①只含有碳和氢两种元素的化合物叫烃,烃分子中的碳原子之间都以单键结合,碳原子的剩余价
键均与氢原子结合,使碳原子的化合价都达到“饱和”。这样的一类有机化合物称为饱和烃,也称为烷烃。
②烷烃中碳原子间结合成链状,链状不是“直线状”,而是呈锯齿状,链上也可以分出支链。例如:
任务二、阅读教材P63页第二自然段,思考如何对烷烃进行命名?什么叫有机物的结构简式?
【答案要点】①烷烃种最简单的是甲烷,其余随碳原子数的增多,依次为乙烷、丙烷、丁烷等。
②碳原子数不多于 10 时,以甲、乙、丙、丁、戊、己、庚、辛、壬、癸依次代表碳原子数;碳原子数
在 11 以上时,以数字来表示,例如,十二烷[CH(CH) CH]。这种命名方法又叫习惯命名法。即:
3 2 10 3
1 2 3 4 5 6 7 8 9 10
n≤10
甲烷 乙烷 丙烷 丁烷 戊烷 己烷 庚烷 辛烷 壬烷 癸烷
n>10 用汉字数字代表,如C H :十一烷
11 24
注意:碳原子数n相同结构不同时,用正、异、新表示,如C H 的两种分子的命名:
4 10
无支链时,CHCHCHCH:正丁烷。
3 2 2 3
有支链时, :异丁烷。
③书写有机物的结构式时,我们通常是将其写成直线形式,但同一个碳上连接的4个价键的位置是可以互
相调换的,因为在空间内4个价键是可以旋转的。
④若把有机物分子的结构式中表示共价单键的“一”删去或部分删去,如乙烷:CHCH 、丙烷:
3 3
CHCHCH、丁烷:CHCHCHCH 等。这种变形后的式子书写起来比较方便,称之为有机物的结构简式。
3 2 3 3 2 2 3
注意:在书写有机物分子的结构简式时,若遇到像丁烷这样分子中有两个或多个相同的成分时,还可以
写成CH(CH)CH 。由于结构简式书写方便,且仍能表示出分子结构的简况,所以,更多情况下常使用结构简
3 2 2 3
式。
【对应训练】1.下列关于有机物结构特点的说法中,正确的是( )
A.CHCHCH 分子含有极性键和非极性键 B.碳原子之间只能形成C-C单键
3 2 3
C.含碳元素的物质都是有机物 D.碳原子之间只能形成碳链【答案】A
【解析】A.CHCHCH 中存在C-H极性键和C-C非极性键,故A正确;B.碳原子之间能形成碳碳
3 2 3
单键,碳碳双键,碳碳三键,故B错误;C.含碳元素的物质不一定都是有机物,比如CO,故C错误;
D.碳原子之间能形成碳链,也可以形成碳环,故D错误。故选:A。
2.下列说法正确的是( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合C H 的烃一定是烷烃
n 2n+2
C.正戊烷分子中所有的碳原子均在同一条直线上
D.碳、氢原子个数比为1∶3的烷烃有两种
【答案】B
【解析】A项中环烷烃也符合要求,但它不是链烃,属于环烃;C项中由碳原子的成键方式和键角特
征知,碳原子呈折线方式排列,因此正戊烷中的碳原子不在同一直线上;D项中n(C)∶n(H)=1∶3时必为
C H,一定是乙烷。
2 6
活动二、认识同系物
任务一、阅读教材P63页第三自然段,根据甲烷、乙烷、丙烷、丁烷、十二烷等烷烃分子的结构简
式,思考什么是同系物?
【答案要点】①甲烷、乙烷、丙烷、丁烷、十二烷分子的结构简式分别为:CH 、CHCH 、
4 3 3
CHCHCH、CHCHCHCH、CH(CH) CH。
3 2 3 3 2 2 3 3 2 10 3
②这些分子结构相似—只含C—C键,碳原子的剩余价键均与氢原子结合;分子组成相差一个或若干
个“CH”原子团。
2
③定义:像这些结构相似,在分子组成上相差一个或若干个“CH”原子团的化合物互称为同系物。
2
任务二、讨论交流:同系物有何特点,你是如何理解烷烃同系物概念的?
【答案要点】①)同系物具有以下三个特点:属于同一类物质,且有相同的通式;式量相差一定是14的
倍数;化学性质相似,物理性质随着碳原子数的增加而发生规律性的变化,
②烷烃结构相似是指分子中原子全部以单键相结合,与支链或直链无关,如丙烷(CHCHCH)是直连
3 2 3
结构,异丁烷(CH)(CH) 含支连结构,但二者是同系物,烷烃的组成可以用通式C H 表示。
3 3 n 2n+2
注意:在判断同系物的时候,要严格把握同系物概念的两个方面:一是分子结构相似,二是分子组成上
相差一个或若干个 CH 原子团,二者要联系在一起应用,缺一不可。当然,还应注意,同系物的关系不光是只
2
有烷烃分子之间存在,在其他的有机物内也存在着同系物的关系。
【对应训练】1.下列关于同系物的说法中,错误的是( )
A.同系物具有相同的分子式
B.同系物符合同一通式
C.相邻的同系物在组成上相差一个CH 原子团
2D.同系物的化学性质基本相似
【答案】A
【解析】同系物的结构相似,属于同一类物质,因此符合同一通式,但一定不具有相同的分子式,A
错误,B正确;相邻同系物在分子组成上相差一个CH 原子团,C正确;同系物的结构相似,所以化学性
2
质基本相似,D正确。
2.下列叙述中正确的是( )
A. 含5个碳原子的有机物,每个分子中最多可形成4个C—C键
B. 正丁烷分子中所有碳原子在一条直线上
C. 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定符合通式C H
n 2n+2
D. 分子式为C H 与C H 的两种有机物一定互为同系物
3 8 6 14
【答案】D
【解析】A.如果5个碳原子成环,则碳碳键数量为5。B.碳的4个键是有角度的,故正丁烷的4个碳不
在一条直线上。C.若果是环状,则不满足通式C H 。故答案为D。
n 2n+2
【课后巩固】1.下列说法不正确的是( )
A.有机物分子中一定含有一个或多个碳原子
B.有机物分子中的碳原子可以相互连接成链状或环状
C.有机物分子中的碳原子可以与其它元素的原子连接
D.分子中含有碳原子的化合物一定是有机化合物
【答案】D
【解析】A. 含有碳元素的化合物是有机化合物,有机物分子中一定含有一个或多个碳原子,A正确;
B. 有机物分子中的碳原子可以相互连接成链状或环状,B正确;C. 有机物分子中的碳原子可以与其它元
素的原子连接,C正确;D. 分子中含有碳原子的化合物不一定是有机化合物,例如CO 等,D错误。
2
2.下列关于有机物和无机物的说法错误的是( )
A.有机物一定含有碳元素 B.无机物可能含有碳元素
C.无机物的熔点一般较高 D.常温下有机物都是液体
【答案】D
【解析】A.绝大多数含有碳元素的化合物叫有机化合物简称有机物,有机物都含碳,A正确;B.无
机物也可能是含有碳元素的化合物,如一氧化碳、二氧化碳等含碳化合物属于无机物,B正确;C.有机
物一般都属于分子晶体,大多数熔点较低,一般在400℃以下 ,无机物熔点一般比较高,C正确;D.常
温下有的有机物为液体,如乙醇、乙酸,有的有机物为气体,如甲烷、乙烯,还有一些有机物为固体,如
葡萄糖、淀粉等,D错误。
3.下列关于碳原子的成键特点及成键方式的理解中正确的是( )
A.饱和碳原子不能发生化学反应
B.碳原子只能与碳原子形成不饱和键C.具有六个碳原子的苯与环己烷的结构不同
D.五个碳原子最多只能形成四个碳碳单键
【答案】C
【解析】饱和碳原子可以发生取代反应或裂化反应等,A错;碳原子也可以与氧原子或氮原子等形成
不饱和键,B错;五个碳原子若构成环戊烷,可以形成5个碳碳单键,D错。
4.火炬中燃料的主要成分为丙烷。下列有关丙烷的叙述不正确的是( )
A.丙烷属于烷烃
B.丙烷的球棍模型为
C.丙烷的结构简式为
D.丙烷燃烧时将化学能转化为光能和热能
【答案】C
【解析】丙烷分子中,碳碳之间均为单键,符合通式C H (n为正整数),属于烷烃,A项正确;由
n 2n+2
图可知,丙烷的球棍模型正确,B项正确;丙烷的结构简式为CHCHCH ,C项错误;丙烷燃烧时将化学
3 2 3
能转化为光能和热能,D项正确。
5.如图为含4个碳原子的6种有机物分子模型(氢原子没有画出),下列叙述中正确的是( )
A.与d互为同分异构体的是c
B.b、c、f的分子式均为C H
4 8
C.a和f均为链状烷烃
D.同种物质中只能含碳链或碳环
【答案】B
【解析】d和c的分子式不同,不互为同分异构体,A错误;b、c、f的分子式均为C H ,互为同分异
4 8
构体,B正确;f为环烷烃,C错误;同种物质中可能同时含有碳链和碳环,D错误。
6.下列有关烷烃的说法中正确的是( )
A.烷烃的分子组成都满足C H (n≥1),彼此都是同系物
n 2n+2
B.戊烷(C H )有三种同分异构体
5 12
C.CHCl只有一种结构,说明甲烷是正四面体结构而不是平面结构
3
D.正丁烷的四个碳原子可以在同一条直线上
【答案】B【解析】A.符合通式CnH 的一定是烷烃,但符合通式CnH 的不同物质一定互为同系物,还可
2n+2 2n+2
能是同分异构体,A错误;B.C₅H₁₂的同分异构体一共有三种,分别为正戊烷、异戊烷和新戊烷,B正
确;C.无论甲烷分子是以碳原子为中心的正四面体结构,还是平面正方形结构,CHCl都不存在同分异
3
构体,即CHCl只有一种结构,不能说明甲烷是正四面体结构还是平面结构,C错误;D.烷烃分子中有
3
多个碳原子呈锯齿形连接,碳原子不在一条直线上,D错误; 故选B。
7.下列关于有机物结构特点的说法中,正确的是( )
A.CH 具有正四面体结构 B.碳原子之间只能形成C-C单键
4
C.含碳元素的物质都是有机物 D.碳原子之间只能形成碳链
【答案】A
【解析】A.CH 具有正四面体结构,故A正确;B.碳原子之间能形成碳碳单键,碳碳双键,碳碳三
4
键,故B错误;C.含碳元素的物质不一定都是有机物,比如CO,故C错误;D.碳原子之间能形成碳
链,也可以形成碳环,故D错误。综上所述,答案为A。
8.(1)某些有机化合物的分子模型如图所示。
回答下列问题:
①属于空间填充模型的是__________(填“甲”“乙”“丙”“丁”或“戊”,下同)。
②可表示同一种有机化合物的是______。
③含碳量最低的是__________,含氢量最低的分子中氢元素的质量分数是________(保留一位小
数)。
(2)已知链状烷烃的通式为 C H ,在链状烷烃分子中的基团:—CH 、—CH—、 、
n 2n+2 3 2
中的碳原子,分别称为伯、仲、叔、季碳原子,数目分别用n、n、n、n 表示。
1 2 3 4
例如: 分子中,n =6,n =0,n =2,n =1,在链状烷烃(除甲烷外)分子
1 2 3 4
中,各种类型的碳原子个数之间存在着一定的关系。
①四种碳原子个数之间的关系为n=_________________。
1
②若某链状烷烃分子中n=n=n=1,写出该链状烷烃的分子式:____________________。
2 3 4
【答案】(1)①乙、丙 ②甲、丙 ③甲、丙;16.7%
(2)①n+2n+2 ②C H
3 4 8 18【解析】(1)①乙、丙能表示原子的相对大小及连接形式,属于空间填充模型。②甲、丙分别是甲
烷的球棍模型与空间填充模型,属于同一种有机化合物。③烷烃的通式为C H (n≥1),随n值增大,
n 2n+2
碳元素的质量分数逐渐增大,故含碳量最低的是甲烷,含氢量最低的是戊烷,戊烷中氢元素的质量分数是
1×12
5×12+1×12
×100%≈16.7%。