文档内容
3.2 水的电离和溶液的PH
题组一 水的电离与水的离子积
1.(2022·广东广州·高二期末)能影响水的电离平衡,并使溶液中的c(H+)<c(OH-)措施是
A.将纯水加热煮沸 B.向纯水中通入SO
2
C.向纯水中投入一小块金属钠 D.向纯水中加入NaCl固体
【答案】C
【解析】A.将纯水加热煮沸,水的电离程度增大,但溶液中c(H+)=c(OH-),A不符合题意;
B.向纯水中通入SO ,SO 与水反应生成亚硫酸,亚硫酸电离使溶液显酸性,c(H+)>c(OH-),B不符合题
2 2
意;
C.向纯水中投入一小块金属钠,钠与水电离产生的H+作用,从而促进水电离,溶液呈碱性,c(H+)<
c(OH-),C符合题意;
D.向纯水中加入NaCl固体,对水的电离平衡不产生影响,溶液中c(H+)=c(OH-),D不符合题意;
故选C。
2.(2022·上海市北虹高级中学高二期末)下列措施使得水的电离:HO H++OH-正向移动的是
2
A.滴加盐酸 B.加入 NaOH 固体
C.加热 D.加水
【答案】C
【解析】A.滴加盐酸,氢离子浓度增大,平衡逆向移动,故A不符合题意;
B.加入 NaOH 固体,氢氧根浓度增大,平衡逆向移动,故B不符合题意;
C.水的电离是吸热过程,加热,平衡正向移动,故C符合题意;
D.水的浓度是定值,加水,水的浓度未变,平衡不移动,故D不符合题意。
综上所述,答案为C。
3.(2022·江苏·南京市雨花台中学高二阶段练习)水是最常见的溶剂。下列说法正确的是
A.水的电离方程式为HO H+ + OH—
2
B.升高温度,水的离子积常数增大
C.常温下,由水电离出c(H+)=1×10-12mol/L的溶液呈碱性
D.水是非极性溶剂
【答案】AB【解析】A.水是弱电解质,水的电离方程式为HO H+ + OH-,故A正确;
2
B.水电离吸热,升高温度,电离平衡正向移动,水的离子积常数增大,故B正确;
C.酸、碱抑制水电离,常温下,由水电离出c(H+)=1×10-12mol/L,说明水电离受到抑制,溶液呈碱性或酸
性,故C错误;
D.水分子是极性分子,水是极性溶剂,故D错误;
选AB。
4.(2021·山东·高密三中高二阶段练习)已知25℃时,水存在电离平衡:HO H++OH- ΔH>0。下
2
列叙述中正确的是
A.向水中加入稀氨水,平衡逆向移动,c (OH-)减小
平
B.将水加热,pH减小,溶液显酸性
C.向水中加入少量的CHCOONa固体,平衡逆向移动,c (H+)减小
3 平
D.向水中加入少量的NaHSO 固体,c (H+)增大,K 不变
4 平 w
【答案】D
【解析】A.向水中加入稀氨水,OH-浓度增大,平衡逆向移动,c(H+)减小,故A错误;
B.水的电离吸热,升高温度,水的电离平衡正向移动,K 增大,pH减小,但仍呈中性,故B错误;
w
C.向水中加入少量的CHCOONa固体,CHCOO-和H+结合生成CHCOOH,使c(H+)减小,促进水电离,
3 3 3
平衡正向移动,故C错误;
D.向水中加入少量的固体NaHSO:NaHSO=Na++H++S ,c(H+)增大,但K 不变,故D正确;
4 4 w
答案选D。
5.在常温下,某溶液中由水电离出的 ,下列说法中正确的是
A.该溶液肯定显碱性 B.该溶液肯定显酸性
C.该溶液的 可能是12,也可能是2 D.该溶液的 肯定不是12
【答案】C
【解析】常温下,水电离出的 <1×10-7mol/L,说明抑制了水的电离,该溶液可能为
酸性或者碱性溶液,若为酸性溶液,溶液中氢氧根离子是水电离的,溶液中氢氧根浓度=水电离出的氢离
子浓度为:1×10-12 mol/L,溶液的pH=2;若为碱性溶液,则溶液中氢离子是水电离的,溶液的pH为12。
故选:C。6.(2022·安徽宿州·高二期末)25°C时,某溶液中由水电离出的离子浓度关系为c(H+)· c(OH-)= 1× 10-24,
该溶液的pH可能为
A.3 B.6 C.9 D.12
【答案】D
【解析】水电离出的氢离子和氢氧根离子相等,则c(H+)= c(OH-)= 1× 10-12,酸或碱能抑制水的电离,25°C
时,若为酸,酸电离的氢离子 ,pH=2,若为碱,pH=12,故选:D。
题组二 水电离出的c(H+ )或c(OH- )的计算
1.(2022·新疆·乌鲁木齐市第三十一中学高二期末) 时,由水电离出来的 ,则
关于溶液的pH的说法正确的是
A.一定是 B.一定是 C.一定是 D.可能 或
【答案】D
【解析】由水电离出来的 ,若为碱溶液,碱中水电离出的 ,
则 ,则pH=11,若为酸溶液,则酸中水电离出的 ,酸中氢
离子浓度为 ,则pH=3,因此溶液pH可能3或11,故答案为D。
综上所述,答案为D。
2. 25℃时,在等体积的①pH=0的 HSO 溶液、②0.05 mol/L的Ba(OH) 溶液中,发生电离的水的物质
2 4 2
的量之比是
A.1∶10 B.1∶5 C.1∶20 D.10∶1
【答案】A
【解析】25℃时pH=0的HSO 溶液中氢离子浓度是1mol/L,0.05 mol/L的Ba(OH) 溶液中氢氧根的浓度
2 4 2
是0.1mol/L,酸或碱溶液中氢离子或氢氧根的浓度越大,对水电离的抑制程度越大,因此在等体积两溶液
中发生电离的水的物质的量之比是10-14:10-13=1:10,答案选A。
3.(2021·湖北·黄石市有色第一中学高二期末)在某温度下,水的离子积常数为1×10-12,该温度下等体积
的①pH=0的HSO 溶液、②0.05 mol·L-1的Ba(OH) 溶液、③pH=10的NaS溶液、④pH=5的NH NO 溶
2 4 2 2 4 3
液中,发生电离的水的物质的量之比(①∶②∶③∶④)是A.1∶10∶1010∶107 B.1∶5∶5×109∶5×106
C.1∶20∶1010∶107 D.1∶10∶102∶107
【答案】A
【解析】水的离子积常数 ,因为各溶液体积相等,假设溶液为1L:
①pH=0的HSO 溶液中 ,氢氧根完全来源于水的电离,
2 4
所以电离的水的物质的量为10-12mol;
②0.05 mol·L-1的Ba(OH) 溶液中 ,氢离子完全来源
2
于水的电离,所以电离的水的物质的量为10-11mol;
③pH=10的NaS溶液中, ,氢氧根完全来
2
源于水的电离,所以电离的水的物质的量为10-2mol;
④pH=5的NH NO 溶液中 ,氢离子完全来源于水的电离,所以电离的水的物质的量为
4 3
10-5mol;
所以四种溶液中发生电离的水的物质的量之比是 ,也就等于1∶10∶1010∶107,A正确;
故选A。
4.25 ℃时,在等体积的①pH=0的HSO 溶液,②0.05 mol·L-1的Ba(OH) 溶液中,发生电离的水的物质
2 4 2
的量之比是
A.1∶10 B.1∶5 C.1∶20 D.1∶10
【答案】A
【解析】试题分析:①中水电离出的氢离子浓度为10-14mol/L,②氢氧根离子浓度为0.1mol/L,则水电离出
的氢离子浓度为10-13mol/L。所以二者发生电离的水的物质的量之比为10-14:10-13=1:10,选A。
5.(2021·黑龙江·密山市第四中学高二期中)常温下:
(1)在0.01 mol/LHCl溶液中,c(OH-)=____,由水电离出的c(H+)=____。
(2)在0.01 mol/LNaOH溶液中,c(H+)=____,由水电离出的c(H+)=____。
(3)在pH=2的NH Cl溶液中,水电离出的c(H+)=____。
4
【答案】(1) 10-12 mol/L 10-12 mol/L(2) 10-12 mol/L 10-12 mol/L
(3)10-2 mol/L
【解析】(1)在0.01 mol/LHCl溶液中c(H+)=10-2 mol/L,则该溶液中c(OH-)= ;
溶液中的OH-就是水电离产生的,水电离方程式是:HO H++OH-,所以根据电离产生的离子浓度关系可
2
知:水电离产生的c(H+)=c(OH-)=10-12 mol/L;
(2)在0.01 mol/LNaOH溶液中,c(H+)= ;
溶液中的H+就是水电离产生的,水电离方程式是:HO H++OH-,所以根据电离产生的离子浓度关系可
2
知水电离产生的c(H+)=c(OH-)=10-12 mol/L;
(3)NH Cl是强酸弱碱盐,在溶液中 发生水解反应,消耗水电离产生的OH-变为NH ·H O,同时产生
4 3 2
H+,使水电离平衡正向移动,最终达到平衡时溶液中c(H+)>c(OH-),所以显酸性。在pH=2的NH Cl溶液
4
中,水电离出的c(H+)就是溶液中c(H+)=10-2 mol/L。
6.(2021·河北石家庄·高二阶段练习)25℃时,在①pH=2的盐酸、②pH=3的醋酸、③pH=12的氨水、
④pH=12的NaOH、⑤pH=4的NH Cl溶液、⑥pH=12的CHCOONa溶液。6种溶液中,由水电离出的
4 3
c(H+)大小关系(或顺序)是___。
【答案】⑥>⑤>②>①=③=④
【解析】pH=12的CHCOONa溶液,溶液中c(H+)=1×10-12mol•L-1,按照25℃时 ,求得
3
c(OH-)=1×10-2mol•L-1,OH-是水电离的,故水电离出的c(H+)也为1×10-2mol•L-1;
pH=4的NH Cl溶液,溶液中c(H+)=1×10-4mol•L-1,盐溶液中H+是水电离产生;
4
pH=12的氨水、pH=12的NaOH溶液,这两种碱溶液中的OH-均是溶质电离产生,故抑制水的电离,溶液
中c(H+)=1×10-12mol•L-1全部是由水电离产生;
同理,pH=2的盐酸、pH=3的醋酸,这两种酸溶液中的H+均是溶质电离产生,故抑制水的电离,则盐酸中
c(H+)=1×10-2mol•L-1,按照25℃时 ,求得c(OH-)=1×10-12mol•L-1,则醋酸中c(H+)=1×10-
3mol•L-1,按照25℃时 ,求得c(OH-)=1×10-11mol•L-1,这两种酸溶液中的OH-均是水电离产
生,水电离的H+和OH-一样多,所以盐酸中水电离的c(H+)=1×10-12mol•L-1,醋酸中水电离的c(H+)=1×10-
11mol•L-1故此,六种溶液中水电离的H+浓度由大到小排序应填“⑥>⑤>②>①=③=④”。
题组三 溶液的酸碱性
1.(2021·贵州·高二学业考试)柠檬水溶液的 ,其中的c(H+)是
A. B.
C. D.
【答案】A
【解析】室温下,柠檬水溶液的pH是4,根据pH=-lgc(H+),c(H+)=10-pH=1x10-4mol/L,故选A。
2.下列溶液一定显酸性的是( )
A.溶液中c(OH-)>c(H+)
B.滴加紫色石蕊溶液后变红色的溶液
C.溶液中c(H+)=10-6 mol·L-1
D.常温时,溶液中由水电离的c(H+)=10-9 mol·L-1
【答案】B
【解析】判断溶液酸碱性的关键是看c(H+)和c(OH-)的相对大小,若c(H+)>c(OH-),溶液呈酸性;而
pH<7或c(H+)>10-7 mol·L-1溶液呈酸性,仅适用于常温时,若温度不确定,就不能用来判断溶液的酸碱
性。B项中可使紫色石蕊溶液变红,则该溶液为酸性;D项中水电离的c(H+)<10-7 mol·L-1,说明向水中
加入了抑制水电离的酸或者是碱,溶液的酸碱性不能确定。
3.下列溶液一定显酸性的是( )
A.含H+的溶液
B.c(OH-)7, B错误;
C.稀释后pH >7,C错误;
D.据分析,大量喝水相当于HCl被无效稀释,pH逐渐增大接近于7但小于7,D正确;
答案选D。
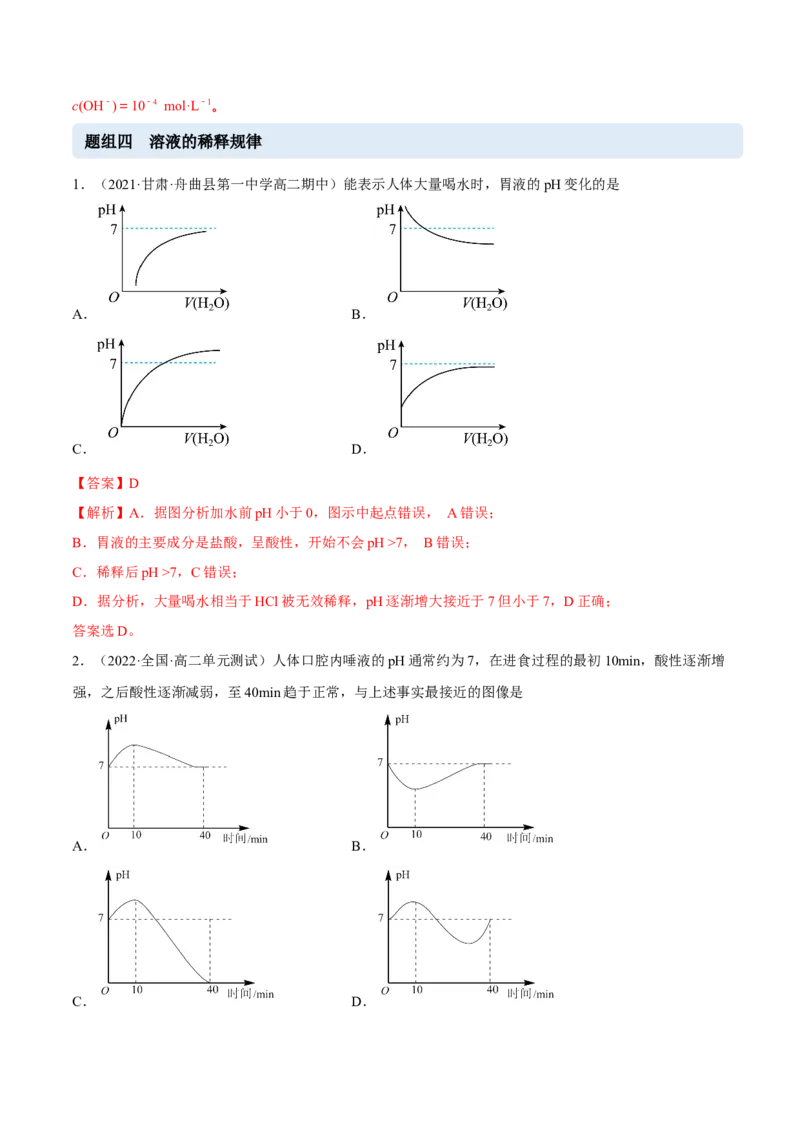
2.(2022·全国·高二单元测试)人体口腔内唾液的pH通常约为7,在进食过程的最初10min,酸性逐渐增
强,之后酸性逐渐减弱,至40min趋于正常,与上述事实最接近的图像是
A. B.
C. D.【答案】B
【解析】在进食过程的最初10分钟,酸性逐渐增强,溶液的pH应该减小,之后酸性逐渐减弱,溶液的
PH应该增大,B图中的曲线变化符合这一情况,综上所述,故选B。
3.下列说法中正确的是
A.100℃时,pH为6的纯水为酸性
B.c(OH一)<c(H+)的水溶液一定呈酸性
C.pH=2的盐酸和醋酸分别加水稀释至原来的100倍,所得溶液中醋酸的pH大
D.常温下,将1mL pH=9的氢氧化钠溶液稀释至1000mL,所得溶液pH=6
【答案】B
【解析】A.100℃时,纯水是呈中性,因此pH为6的纯水也是呈中性的,故A错误;
B.判断溶液酸碱性主要根据c(OH一)、c(H+)的大小关系判断,c(OH一)<c(H+)的水溶液一定呈酸性,故B
正确;
C.pH=2的盐酸和醋酸分别加水稀释至原来的100倍,由于醋酸又电离,因此稀释后醋酸中的氢离子浓度
大于盐酸中氢离子浓度,所以溶液中醋酸的pH小,故C错误;
D.常温下,将1mL pH=9的氢氧化钠溶液稀释至1000mL,由于此时要考虑水电离出的氢氧根离子,因此
所得溶液pH略大于7,故D错误。
综上所述,答案为B。
题组五 (混合)溶液的PH计算
1.(2022·广西河池·高二阶段练习)常温下,下列溶液一定呈酸性的是
A.一定体积 的 溶液加水稀释 倍
B. 的 溶液与 的 溶液等体积混合
C. 氨水和 氯化铵溶液等体积混合
D. 某碱溶液和 盐酸等体积混合
【答案】B
【解析】A.碱溶液无论如何稀释都不会变为中性或酸性,稀释溶液只能接近中性,故A错误;
B.醋酸是弱电解质,氢氧化钠是强电解质, 的醋酸浓度大于 的氢氧化钠浓度,二者等体积混合,醋酸的物质的量大于氢氧化钠,则醋酸过量,混合溶液呈酸性,故B正确;
C.等体积等物质的量浓度的氨水和氯化铵溶液中,一水合氨的电离程度大于铵根离子水解程度,所以混
合溶液呈碱性,故C错误;
D.等浓度、等体积的某碱和盐酸混合,如果碱是一元强碱,则混合溶液呈中性,如果碱是二元强碱,混
合溶液呈碱性,如果碱是一元弱碱,则混合溶液呈酸性,故D错误。
故选B。
2.(2021·全国·高二专题练习)某酸HX稀溶液和某碱YOH稀溶液的物质的量浓度相等,两溶液混合后,
溶液的pH大于7,表中判断合理的是
编号 HX YOH 溶液的体积关系
① 强酸 强碱 V(HX)=V(YOH)
② 强酸 强碱 V(HX)