文档内容
第三章 水溶液中的离子反应与平衡
课题 第三节 盐类的水解
第一、二课时
1、通过实验探究和自主探讨,使学生理解盐类水解的本质和盐类水解对溶液酸碱
知识与技 性的影响及变化规律。
能
2、掌握盐类水解的离子方程式与化学方程式。
3、能够用盐类水解的知识去解释生活、生产中的有关现象和做法。
教 1、通过查阅资料、科学探究等活动培养学生观察能力、思维能力、分析问题和解
学 过程与方 决问题的能力。
目 法 2、通过设计实验方案,进行初步的探究活动,学习科学探究和科学实验的方法,
标 培养学生的实验技能,认识科学探究的基本过程。
1、通过实验数据处理的体验,使学生养成实事求是、尊重事实的科学
情感态度 态度。
与价值观
2、通过学习生产、生活中盐类水解规律的总结,体会自然万物变化的丰
富多彩,对学生进行事物联系和发展的普遍规律的观点的教育。
教学
重点 盐类水解的本质,理解强酸弱碱盐和强碱弱酸盐的水解的规律
教学
难点 盐类水解方程式的书写
教
学科网(北京)股份有限公司
学
设
本课内容是在学习了前一章《化学平衡》和本章的第二节《水的电离和溶液的酸碱性》的基础
教
材 上进一步加深学生对化学平衡和水的电离理论知识的巩固和应用。本节内容重在指导学生利用化学
分
平衡理论知识,了解什么是盐类水解及盐类水解的一般规律。本节是本章教学的重点和难点。
析
高二的学生已经具备独立思考的能力,而且思维活跃。通过前一阶段的学习,学生已经掌握了
学
情 离子方程式书写、化学平衡、电离平衡以及溶液的 pH等知识。但由于知识的前摄效应,又会给本
分
节内容的学习造成一定的困难,比如酸溶液呈酸性,碱溶液呈碱性,盐是中和反应的产物则学生易
析
误解盐溶液一定呈中性等。
教 在教学前讨论教法也是很有必要的。本节课结合教材特点指导学生从已有的知识开展学习活
法
动,结合实验,层层导入,最终让学生懂得盐类水解的本质。这种使学生动口动手动脑动眼的多层
设
计 次教学,让学生真正成为主体,感受到化学学习的乐趣,化难为易,并使知识系统化。
想
意 课
图 件
意图:提高学生的学习兴趣,增加课堂容量
使
用
课件类型:PPT
教学 设计意图
教 学 内 容
环节
教师活动设计 学生活动设计【课前准备】下发导学案,让学生根据导学案内容 学生课前收集资料,并 通过预先布置他们
查找资料 将其制作成幻灯片,幻 预习、查阅盐类水
1、(第一组)在没有洗涤精时,人们为什么用热的 灯片要求内容丰富,必 解的有关资料,旨
纯碱溶液来洗碗? 须有文字、有图片等, 在充分体现学生学
新 2、(第二组)请你查询明矾如何净水?除此之外, 并在幻灯片的最后附上 习的主动性,让学
课 它在我们的生活中还有何作用? 组员分工情况,每个小 生乐于就化学有关
导
3、(第三组)你知道泡沫灭火器里装的是什么药品 组派一名解说员对本组 问题进行交流和作
入
吗?它们接触为什么可以灭火?请你查阅有关资 的幻灯片进行解说。 出判断,并能以开
料,随时准备把你的发现公之于众。 放的态度对待他人
【导入新课】(投影农民施肥图片) 的意见。
设问:俗话说:“灰混粪,粪混灰,灰粪相混损肥 倾听、思考,有些同学
分.” 你想知道肥分损失的原因吗?今天我们所学的内 小声讨论。
容可以帮你解决。
【板书】第三节 盐类的水解
【过渡】要对盐类的水解预先有所了解,你必须在
课前探讨中下点苦功,请问你做到了吗?我们有请
第一组代表解释阿伯遇险之原因及应 【学生汇报】
对方法。
【提示】试用平衡移动原理加以解释
【过渡】好,我们以事实来说话,请大家测试以下
溶液的pH值。
【科学探究】测定食盐(NaCl)、纯碱(Na CO)、小苏
2 3
打(NaHCO )、明矾[KAl(SO)·12H O]、84消毒液 创设问题情景,激
3 4 2 2
(NaClO)、醋酸钠(CHCOONa)的pH, 思考,得出结论:属于 发学习动机,尽量
3
并将实验结果并填表 : 盐类,呈碱性 让学生自主得到知
【板书】结论:①NaCl 中性 识。
② NaCO 碱性 ③NaHCO 碱性④明矾 酸
2 3 3
性 ⑤NaClO 碱性 ⑥CHCOONa 碱性
3
学科网(北京)股份有限公司【讨论】请分析上述实验结果,盐溶液的酸碱性与 实验探索,观察实验,
生成该盐的酸和碱的强弱有什么关系? 纪录、分析,得出结 培养学生操作实
小结:盐的组成与盐溶液酸碱性的关系: 论:呈碱性的溶液: 验,根据实验现象
强碱弱酸盐的水溶液 显碱性 NaCO、NaClO、 进行知识学习的能
2 3
强酸弱碱盐的水溶液 显酸性 NaHCO CHCOONa; 力。
3、 3
强酸强碱盐的水溶液 显中性 呈中性的溶液:
【活动探究】试探究CHCOONa 溶液呈碱性的原 NaCl;
3
因。(要求学生首先提出假设,教师必要提示)
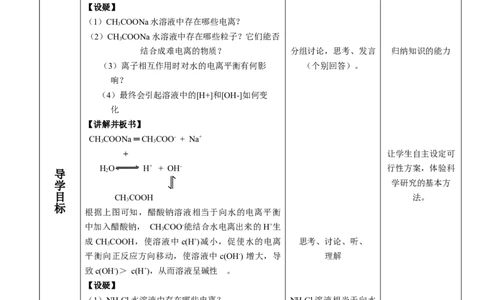
【设疑】
(1)CHCOONa水溶液中存在哪些电离?
3
(2)CHCOONa 水溶液中存在哪些粒子?它们能否
3
结合成难电离的物质? 分组讨论,思考、发言 归纳知识的能力
(3)离子相互作用时对水的电离平衡有何影 (个别回答)。
响?
(4)最终会引起溶液中的[H+]和[OH-]如何变
化
【讲解并板书】
CHCOONa ═ CH COO- + Na+
3 3
+ 让学生自主设定可
H O H+ + OH- 行性方案,体验科
导 2
学 学研究的基本方
目 CH COOH 法。
3
标
根据上图可知,醋酸钠溶液相当于向水的电离平衡
中加入醋酸钠, CHCOO-能结合水电离出来的H+生
3
成CHCOOH,使溶液中c(H+)减小,促使水的电离 思考、讨论、听、
3
平衡向正反应方向移动,使溶液中c(OH-) 增大,导 理解
致c(OH-)> c(H+),从而溶液呈碱性 。
【设疑】
(1)NH Cl水溶液中存在哪些电离? NH Cl溶液相当于向水
4 4
(2)NH Cl水溶液中存在哪些粒子?它们能否结合 的 电 离 平 衡 中 加 入
4
成难电离的物质? NH Cl,NH + 能结合水
4 4
(3)离子相互作用时对水的电离平衡有何影响? 电离出来的 OH-生成
(4)最终会引起溶液中的[H+]和[OH-]如何变化 NH ·H O,使溶液中 创设问题情景,
3 2
c(OH-)减小,促使水的 培养学生分析问题
电离平衡向正反应方向 的能
移动,使溶液中 c(H+)
增 大 , 导 致 c(H+) >
c(OH-),从而溶液呈酸
学科网(北京)股份有限公司【板书】一、盐类的水解
1、定义:在溶液中盐电离出来的离子跟水电离份出
来的H+或OHˉ结合生成弱电解质的反应 归纳总结、听、记 渗透由表及里,由
2、实质:盐中弱酸根离子或弱碱阳离子与水电离出 现象到本质的观点
来的H+或OHˉ 结合生成的分子或离子,破
坏了水的电离。
【提问】是所有的盐都能水解吗?应具备什么条 分析、讨论
件?
【板书】3、条件:一是盐中必须有易结合水中H+或
OHˉ 粒子;二是盐必须溶于水 根据醋酸钠溶液和
【讲述】盐和水反应,生成酸和碱,相当于是酸碱 氯化铵溶液水解的
中和反应的逆反应,所以盐类水解的程度很小 分析过程来推导出
【板书】4、水解方程式的书写规则 一系列问题。培养
一般地说,盐类的水解的程度不大,应用可逆 学生分析问题、解
符号“ ”表示,盐类的水解一般不会产 决问题的能力
生沉淀和气体,所以不用“↓”“↑”
如: CHCOONa + H O CH COOH + NaOH
3 2 3
NHCl + H O NH•H O + HCl
4 2 3 2
【过渡】盐类水解有哪些特点呢? 分析回答
【板书】4、特点
1)、盐类的水解对水的电离是促进
导
2)、盐类的水解一般情况下水解程度较小,且可
学
逆,存在着平衡
目
标 3)、盐类的水解过程是一个吸热过程 归纳总结
【提问】根据盐类水解的相关知识,分析碳酸钠溶
液显碱性、氯化铵溶液显酸性、NaCl溶液显中性的 培养学生利用已学
原因.查阅课本,并试图得出盐类水解的规律。 知识来解决新知识
【板书】4)、盐类的水解规律:谁弱谁水解,不弱 的能力,达到知识
不水解,都弱都水解,越弱越水解,谁强显谁性 加入镁、氢氧化钠溶 的融会贯通
【问题】向氯化铵溶液中别加入镁、盐酸、氢氧化 液、硝酸铵溶液平衡向
钠溶液、硝酸铵溶液,升高温度,利用化学平衡理 正反应方向移动;加入
论平分析平衡是怎么移动的?能否得出影响平衡的 盐酸平衡向逆反应方向
因素? 移动;升高温度平衡向
【板书】5)、影响因素 正反应方向移动 培养学生归纳总结
(1)温度:升温,促进盐类的水解;降温,抑制盐 的能力
类的水解
(2)浓度:盐的浓度越大,盐类水解程度越小;盐
的浓度越小,盐类水解程度越大
(3)酸碱度:加酸或加碱对盐类的水解促进或抑
学科网(北京)股份有限公司【讲述】下面我们来学习几类能水解的盐的水解过
程和水解方程式的书写
【板书】6、水解过程
1)、强酸弱碱盐——水解呈酸性
NH Cl + H O NH •H O + HCl
4 2 3 2
AlCl + 3H O Al(OH) + 3HCl
3 2 3
明确:多元弱碱阳离子中学阶段按一步水解处理 学生活学活用
【练习】书写Fe(NO ) 溶液、CuSO 溶液水解方程式 学生书写 巩固盐类水解方程
3 3 4
【板书】2)、强碱弱酸盐——水解呈碱性 式的书写及会判断
CHCOONa + H O CH COOH + NaOH 盐类水解的酸碱性
3 2 3
Na CO + H O NaHCO + NaOH
2 3 2 3
NaHCO + H O H CO + NaOH
3 2 2 3
明确:(1)多元弱酸根离子水解分步进行,第一步
水解大于第二步,中学阶段无特殊说明只写第一步
水解 学生书写
【练习】书写NaSO 溶液、NaS溶液水解方程式
2 3 2
【板书】(2)特殊: NaHCO 水解程度大于电离程 学生在教师的引导下进
3
度,溶液呈碱性 行分析,归纳总结出规 培养学生归纳总结
HCO ˉ + H O H CO + OH ˉ 律 的能力
3 2 2 3
HCO ˉ CO 2ˉ + H+
导 3 3
学 NaHSO 电离程度大于水解程度,溶液呈酸性
3
目 【板书】3)、弱酸弱碱盐
标
CHCOONH + H O NH•H O + CH COOH
3 4 2 3 2 3
(1)相同条件下,弱酸弱碱盐水解程度比强酸弱碱盐
及强碱弱酸盐的水解程度略大 学生了解,会判断即可
(2)溶液酸碱性的判断方法:根据生成弱酸和弱碱相
对强弱
生成的弱酸强于弱碱,溶液呈酸性;
生成的弱酸弱于弱碱,溶液呈碱性
生成的弱酸几乎等于弱碱,溶液呈中性 如:
CHCOONH
3 4
【板书】7、盐类水解的应用: 学生根据前面所学知识
1)配制某些盐溶液时,要考滤盐类的水解 来讨论分析盐类水解的 设置问题情景,拉
如:配制FeCl 、AlCl 溶液时滴加几滴稀盐酸; 应用 近化学与生活的距
3 3
离,激发学生思考
配制NaCO 溶液滴加几滴NaOH溶液
2 3
问题的兴趣。
2) 实验室贮存试剂时,要考滤盐类的水解
如:NaCO、NaHCO 溶液呈碱性而不能用带玻
2 3 3
璃塞的试剂瓶贮存
学科网(北京)股份有限公司学科网(北京)股份有限公司
【板书】 3)根据水解规律判断盐溶液的酸碱性
如:NH Cl溶液呈酸性;NaCO 溶液呈碱性
4 2 3
巩固所学知识
4)判断盐溶液蒸干、灼烧后所得的产物
如:FeCl 、AlCl 溶液蒸干、灼烧后所得的产 学生根据前面所学知识
3 3
物分别为Fe O 、Al O ;CuSO 、NaCO 溶液蒸干、 来讨论分析盐类水解的
2 3 2 3 4 2 3
灼烧后所得的产物仍分别为CuSO 、NaCO 固体 应用
4 2 3 应用所学知识解释
5)利用FeCl 溶液的水解制Fe(OH) 胶体
3 3 实际问题。
6)解释日常生活中某些事实
如:明矾净水、热的纯碱液除油污,这些即
能解释导学案中的问题
【探究】投影图片:普通泡沫灭火器及其剖图
【设问】泡沫灭火器为什么可以灭火?里面有什么
培养学生的问题意
药品?怎样反应?它的使用范围?我们看一下课前
识、自学能力。
探究的第二组同学为我们带来了什么?有请! 思考、小组讨论、代表
导 【过渡】刚才我们从第二组同学的发言中听到了一 回答问题
学 个新名词——双水解,请问什么样的离子可发生双
目
水解反应?怎样书写?查阅课本及讲义,两分钟内
标
作答。
【讲解】非常不错。能发生双水解反应的特点:阴
阳离子水解产生分别产生酸性和碱性,溶液混合后
酸碱中和而互相促进水解并加深水解程度,称为双
水解(即:弱酸离子和弱碱离子混合相互反应)。
【板书】二、双水解
与教师共同分析讨论双
1、定义:两种不同类型盐水解相互促进,使水解
水解的知识点
程度增大的过程
加深学生对双水解
2、范围:强酸弱碱与强碱弱酸 的发生条件、方程
3、特点:一般水解程度较大,且不可逆,进行到 式书写的认识。
底;表示时用“===”“↑”“↓”
4、 应用:泡沫灭火器:1)药品: Al (SO ) 和
2 4 3
NaHCO 溶液
3
2)原理:Al (SO ) + 6NaHCO == 2Al(OH) ↓ +
2 4 3 3 3
6CO↑ + 3Na SO
2 2 4
3)装置:Al (SO ) 装在塑料桶中;NaHCO 塑料桶
2 4 3 3
与钢桶之间
掌握特殊的知识,不要
5、特例:
混为一谈
1)可溶性铜盐与可溶性的硫化物
如:CuSO + Na S === CuS↓+ Na SO
4 2 2 4
2)可溶性铁盐与可溶性的硫化物如:2FeCl + Na S
3 2
=== 2FeCl + S↓+ 2NaCl
2
【课堂小结】通过本节课的学习,知道盐溶液的酸学科网(北京)股份有限公司
作
导学案中的习题
业
设
计
盐类的水解
一、盐类的水解
1、定义
2、实质
3、条件
板
4、水解方程式的书写规则
书 5、特点
6、水解过程
设
7、应用
计 二、双水解
1、定义
2、范围
3、特点
4、应用
5、特例学科网(北京)股份有限公司