文档内容
第三节 盐类的水解
一、盐类的水解
(一)盐的分类
1、按组成分:正盐:电离时生成的阳离子是金属离子(或铵根),阴离子为酸根离子的盐
酸式盐:电离时生成的阳离子除金属离子(或铵根)外还有氢离子,阴离子为
酸根离子的盐。
碱式盐:电离时生成的阴离子除酸根离子外还有氢氧根离子,阳离子为金属离
子(或NH+)的盐。
4
2、按溶解性:易溶盐(NaCl);微溶盐(CaSO);难溶盐(BaCO )
4 3
3、按形成盐的酸碱的强弱不同:强酸强碱盐(KNO)、强酸弱碱盐(NH Cl)、
3 4
强碱弱酸盐(NaF)、弱酸弱碱盐(CHCOONH)
3 4
(二)盐溶液呈现不同酸碱性的原因——盐类的水解
1、定义:在溶液中,盐电离出来的离子与水电离出来的 H+或OH-结合生成弱电解质的反
应,叫做盐类的水解
2、实质:
→溶液呈酸性或碱性
表示为:盐+HO 酸+碱
2
3、特点:(1)极其微弱,为可逆反应,存在水解平衡
(2)是中和反应的逆反应,水解反应是吸热反应
4、规律:有弱就水解,无弱不水解;越弱越水解,都弱都水解;谁强显谁性,同强显中性
注:(1)组成盐的酸越弱,水解程度越大。例如:水解程度:NaCO >CH COONa,因
2 3 3
为酸性:HCO 0.1mol/L的
2 3
NaHCO
3
(3)弱酸酸式盐的酸碱性,看电离与水解程度大大小。HCO -、HPO 2-、HS- 以水解为
3 4
主→显碱性
HSO -、HPO - 以电离为主→显
3 2 4
酸性
5、盐类水解方程式的书写
(1)一般原则:①必须写“ ”
②不写“↑”“↓”
③HCO、HSO 等不拆开
2 3 2 3
④多元弱酸阴离子分步水解,分步书写,以第一步为主;多元弱碱阳离子
水解方程式一步写完⑤遵守质量守恒、电荷守恒、客观事实
(2)书写模式:盐的离子+ HO 弱酸(或弱碱)+OH-(或H+)
2
举例:CHCOONa溶液:CHCOO-+ HO CHCOOH+OH-
3 3 2 3
NH Cl溶液:NH ++ HO NH ·HO +H+
4 4 2 3 2
NaCO 溶液:CO2-+HO HCO -+ OH-(第一步水解) HCO -+ H O
2 3 3 2 3 3 2
HCO+ OH-(第二步水解)
2 3
FeCl 溶液:Fe3++3HO Fe(OH) +3H+
3 2 3
(3)双水解——阴阳离子都水解
①非彻底型:用“ ”连接
例:CHCOONH :CHCOO-+ NH ++H O CHCOOH+NH·HO(CHCOONH 显
3 4 3 4 2 3 3 2 3 4
中性)
②彻底型:用“=”连接。特点:有“↑”或“↓”生成,能同时离开体系
Al S:2Al3++ 3S2-+6HO=2Al(OH) ↓+3H S↑
2 3 2 3 2
Fe (CO):2Fe3++3CO2-+3HO=2Fe(OH) ↓+3CO ↑
2 3 3 3 2 3 2
二、影响盐类水解的主要因素
(一)内因:反应物的性质。越弱越水解,越水解其酸(或碱)性越强
(二)外因:(1)温度:升高温度,促进水解
(2)浓度:加水稀释→向右移动→水解程度大→酸(或碱)性减弱
盐的浓度越高→向右移动→水解程度小→酸(或碱)性增强
(3)同离子效应:加酸或碱抑制或促进水解
小结:越弱越水解,越热越水解,越稀越水解,加酸或碱抑制或促进水解
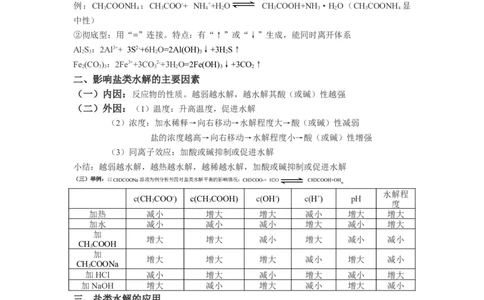
(三)举例:以CH3COONa溶液为例分析外因对盐类水解平衡的影响情况:CH3COO-+ H2O CH3COOH+OH-
水解程
c(CHCOO-) c(CHCOOH) c(OH-) c(H+) pH
3 3 度
加热 减小 增大 增大 减小 增大 增大
加水 减小 减小 减小 增大 减小 增大
加
增大 增大 减小 增大 减小 减小
CHCOOH
3
加
增大 增大 增大 减小 增大 减小
CHCOONa
3
加HCl 减小 增大 减小 增大 减小 增大
加NaOH 增大 减小 增大 减小 增大 减小
三、盐类水解的应用
(一)在化学实验中的应用
1、判断溶液的酸碱性确定pH范围
2、盐溶液中微粒种类的判断
3、配制和贮存易水解的盐溶液
(1)配制强酸弱碱盐溶液时,加强酸抑制水解。例如:配制 FeCl 溶液时,常将FeCl 晶
3 3
体溶于较浓的盐酸中
(2)配制强碱弱酸盐溶液时,加强碱抑制水解
(3)配制Al S 只能在干态条件下把铝粉和硫粉的混合物加热,不能在水溶液中得到
2 3(4)试剂的贮存:NaCO、NaSiO 溶液的试剂瓶不能用磨口玻璃塞;NH F溶液不能用玻
2 3 2 3 4
璃瓶盛放
4、判断盐溶液蒸干产物
(1)不水解不分解的盐(如NaCl、KSO )
2 4
水 解 生 成 不 挥 发 性 酸 的 盐 ( 如 Al (SO ))
2 4 3
( 2 ) 水 解 生 成 挥 发 性 酸 的 盐 ( CuCl 、 Fe(NO ) 、 MgBr )
2 3 3 2
(3)较低温度下受热分解的盐(KMnO 、NaHCO )
4 3
(4)易被氧化的盐 (如:FeSO →Fe (SO ),NaSO →NaSO )
4 2 4 3 2 3 2 4
(5)其他:NaClO溶液
5、活泼金属与强酸弱碱盐反应产生氢气:例:Mg与NH Cl(或FeCl 、AlCl 、CuCl )反
4 3 3 2
应,产生H
2
6、判断离子共存:Al3+、Fe3+、Cu2+与CO2-、HCO -、S2-、HS-、AlO-生成气体或沉淀的双
3 3 2
水解不能共存
7、制备胶体:饱和FeCl 溶液滴入沸水中因水解得到Fe(OH) 胶体。FeCl +3H O Fe(OH)
3 3 3 2 3
(胶体)+3HCl
8、物质的提纯:
(1)KNO(Fe(NO )) 促进Fe(NO ) 水解→除去Fe3+
3 3 3 3 3
( 2 ) MgCl (FeCl )
2 3
促进Fe3+水解→Fe(OH) →除杂
3
9、酸碱中和时指示剂的选择
强碱滴定弱酸时(生成的盐溶液水解呈碱性)常用酚酞做指示剂
强酸滴定弱碱时(生成的盐溶液水解呈酸性)常用甲基橙做指示剂
(二)在日常生活中的应用
1、去污:热的纯碱去污能力强。CO2-+H O HCO -+OH- 温度升高→促进水解
3 2 3
→c(OH-)升高
2、灭火:泡沫灭火器
3 、 食 品 : 炸 油 条 时 加 入注: CO 使油条变得松脆可口
2
4、净水:明矾净水:Al3++3H O Al(OH) +3H+
2 3
铁盐净水:Fe3++3H O Fe(OH) +3H+
2 3
Al(OH) 和Fe(OH) 都具有吸附性
3 3
5、水垢:主要成分是CaCO 和Mg(OH) ,不会生成MgCO ,因为MgCO 微溶,受热水解
3 2 3 3
生成更难溶的Mg(OH)
2
(三)在工农业生产中的应用
1、化肥的合理施用
(1)长期施用(NH )SO 的土壤因 NH +水解,使土壤酸性增强:NH ++H O
4 2 4 4 4 2
NH ·HO+H+
3 2
(2)铵态氮肥与草木灰(KCO )不能混合施用:CO2-+H O HCO -+OH- NH ++OH-
2 3 3 2 3 4
=NH·HO= NH ↑+HO
3 2 3 2
生成NH 降低肥效
3
(3)普钙(或过磷酸钙)(Ca(HPO ) )与草木灰不能混 CaCO
2 4 2 Ca(H PO ) 酸性 3
2 4 2 Ca (PO ) 不能被作物吸收
合施用: K CO 碱性 3 4 2
2 3 CaHPO
4
2、焊接时用NH Cl溶液除锈:利用其水解后溶液显酸性,溶解铁锈
4
3 、 制 备 纳 米 材 料 : 用 TiCl 制 备 TiO : TiCl + ( x+2 ) HO ( 过 量 )
4 2 4 2
TiO·xHO↓+4HCl
2 2
四、盐类水解常数——K
h
(一)表达式:用HA表示酸,MOH表示碱,MA表示由它们生成的盐。若MA为强碱
弱酸盐,则其水解的离子方程式为:A-+H O HA+OH-,该反应的平衡常数可表示为:
2
(二)水解常数与电离常数、水的离子积的关系
(K 是酸的电离平衡常数) (K 是碱的电离平衡常数)
a b
(三)影响因素:
水解平衡常数只受温度的影响,因水解是吸热反应,故水解平衡常数随温度的升高而增大
五、溶液中粒子浓度大小的比较
(一)溶液中的守恒关系
1、电荷守恒:任何电中性溶液中,阴离子所带负电荷总数恒等于阳离子所带正电荷总数例:NaCO:c(Na+)+c(H+)=2c(CO 2-)+c(HCO-)+c(OH-)
2 3 3 3
2、元素质量守恒:即原子个数守恒或质量守恒
例:KS:c(K+)=2[c(S2-)+c(HS-)+c(H S)]
2 2
(二)溶液中粒子浓度大小的比较
1、多元弱酸:根据其分步电离来分析,例:HCO:c(HCO)>c(H+)>c(HCO-)>c(CO 2-)
2 3 2 3 3 3
2 、 多 元 弱 酸 的 正 盐 : 根 据 弱 酸 根 的 分 步 水 解 来 分 析 , 例 : NaS :
2
c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
3、多元弱酸的酸式盐:看其弱酸根离子的电离与水解程度的大小
例:水解>电离:NaHCO :c(Na+)>c(HCO-)>c(OH-)>c(H+)>c(CO 2-)
3 3 3
电离>水解:NaHSO:c(Na+)>c(HSO -)>c(H+)>c(SO2-)>c(OH-)
3 3 3
4、其他单一盐溶液,例:NH Cl:c(Cl-)>c(NH+)>c(H+)>c(OH-)
4 4
5、不同溶液中同一离子浓度的大小:看其他离子对其影响
例:0.1mol/L的NH HSO 、NH Cl、CHCOONH、(NH )SO 中c(NH +)的大小顺序:
4 4 4 3 4 4 2 4 4
(NH )SO > NH HSO > NH Cl > CHCOONH
4 2 4 4 4 4 3 4
6、混合溶液中离子浓度的大小判断
(1)混合前后不反应:
①电离>水解:同浓度的NH Cl与NH ·H O混合:c(NH +)> c(Cl-)> c(OH-)> c(H+)
4 3 2 4
同浓度的CHCOONa与CHCOOH混合:c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3 3 3
②水解>电离:同浓度的NaCN与HCN混合:c(Na+)>c(CN-)> c(OH-)> c(H+)
(2)混合前后反应:
①完全反应形成单一溶液:
②不完全反应形成混合液,看电离与水解的程度大小