文档内容
第三章 《晶体结构与性质》教学设计
第四节 配合物与超分子
课题: 3.4 配合物与超分子 课时 1 授课年级 高二
1.了解配合物应用
课标要求 2.知道简单配合物的制备,如银、铜、铁等金属离子所形成的配合物的制取与性质。
3.知道超分子代表物,了解超分子的发展前景。
本节内容的功能价值(素养功能)主要是培养和发展学生的“宏观辨识与微观探
析”和“实验探究与创新意识”“变化观念与平衡思想”等学科核心素养,能从微观角
度理解配位键的形成条件和表示方法;能判断常见的配合物、配体、中心原子;能利用
配合物的性质及实验现象等去推测配合物的组成结构,从而形成“结构决定性质”的认
知模型。
旧人教版教材(2004年)关于配合物理论这部分内容是插在第2章“分子结构与性
质”的第2节“分子的立体构型”中介绍的;旧人教版中配合物代表实验较少,新人教版
教材
教材(2019年)在章节编排对此做了较大改动,将“配合物与超分子”单独列为一节内
分析
容,放在了第3章“晶体结构与性质”的第4节里介绍,说明现在对配位键及配合物的认
识的重要性有所提高,要求学生对配合物的了解需要更深入一些。另外还增加了一个常
见的简单配合物的制备和应用的演示实验:氯化银沉淀溶于氨水形成一氯二氨合银,让
学生更能体会到配位键的形成可以改变一些物质的原有性质如溶解性、颜色等,配合物
在医药学、生物、化学等领域将有广泛应用。
超分子是新教材新加的内容,体现了科学发展的前沿。内容较难理解,课标的要求
相对较低,但是要知道简单的超分子代表物
1.能知道常见的配合物制备过程。
教学目标 2.能举例说明配合物常见的应用,如配合物在生物、化学等领域的广泛应用。
3.了解超分子概念,知道超分子代表物杯酚和冠醚的应用。
教学重、难 重点:常见配合物实验制备、超分子的代表物及其特点。
点 难点:常见配合物实验制备、超分子的代表物及其特点。
宏观辨识与微观探析:能够从微观角度理解配位键的形成条件和表示方法,以及判
断常见的配合物。
变化观念与平衡思想:能利用配合物的性质去推测配合物的组成,从而形成“结构
核心素养
决定性质”的认知模型。
科学态度与社会责任:通过超分子的学习,培养正确的科学态度和对社会责任的认
识。
在本章的前三节学生已经学习了分子晶体、共价晶体、金属晶体、离子晶体等几类
晶体的结构与性质特点,并且对这几类晶体里存在的微粒间作用力——分子间作用力、
共价键、金属键、离子键也很清楚,对接下来学习配位键奠定了知识基础。
学情分析
配合物的实验是基于上一节配合物第一课时的基础上,学生已经学习了配位化合物
的基本知识,接受配合物实验制备比较简单。而超分子,学生在之前的内容从来没有接
触过,内容难度较大。
教学过程
教学环节 教学活动 设计意图
【视频导入】通过观看《两次获得诺贝尔奖的超分子化学》中一段超分子
的片段,介绍超分子的在化学和医学方面的应用,引起学生的兴趣和好奇心,为后续的知识学习做好铺垫。
环节 导 【教师】提出教材新增超分子在科学领域的重要作用
一、 入
新
情景
知 【学生】体会化学与生活,化学与科研的联系
导入
活 【视频】播放演示实验3-2 回归教
动 材,抓纲
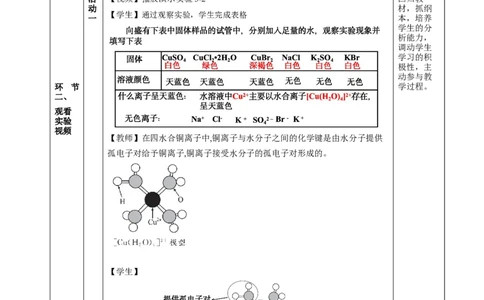
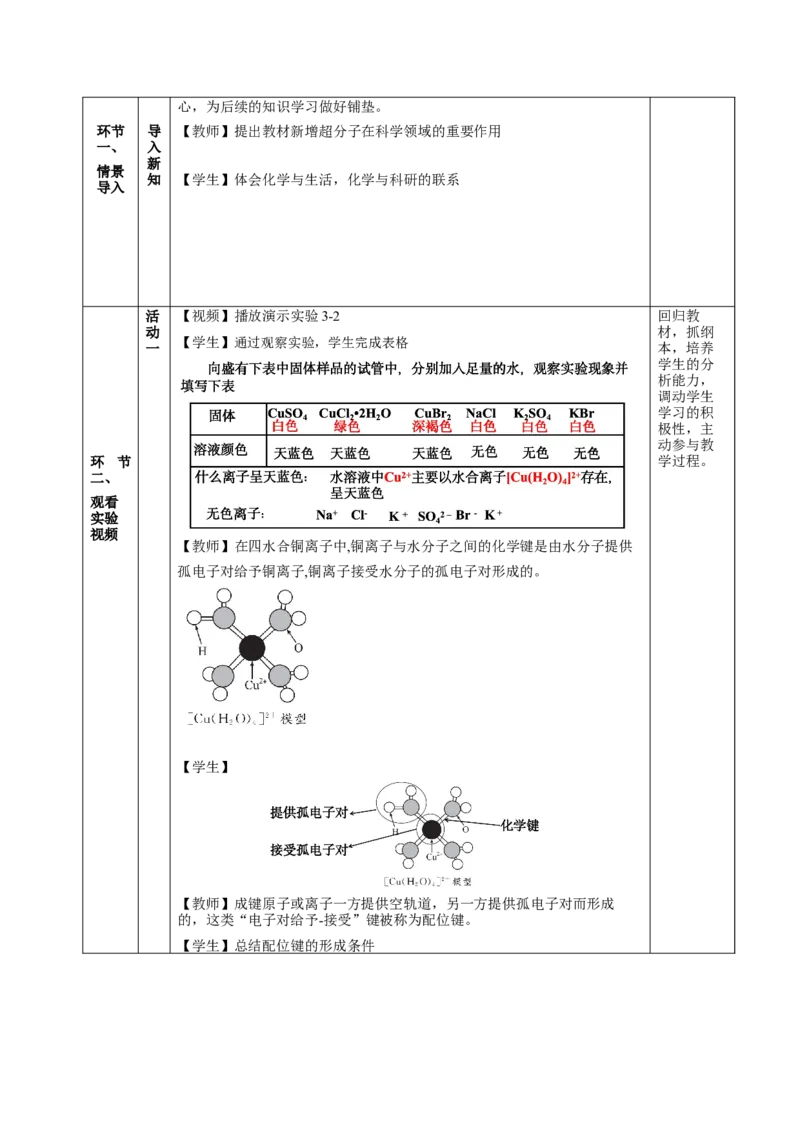
【学生】通过观察实验,学生完成表格
一 本,培养
学生的分
析能力,
调动学生
学习的积
极性,主
动参与教
环 节 学过程。
二、
观看
实验
视频
【教师】在四水合铜离子中,铜离子与水分子之间的化学键是由水分子提供
孤电子对给予铜离子,铜离子接受水分子的孤电子对形成的。
【学生】
【教师】成键原子或离子一方提供空轨道,另一方提供孤电子对而形成
的,这类“电子对给予-接受”键被称为配位键。
【学生】总结配位键的形成条件【教师】通常把金属离子或原子(称为中心离子或原子)与某些分子或离子(称
为配体或配位体)以配位键结合形成的化合物称为配位化合物,简称配合物。
【视频】播放演示实验3-3 促进对知
识的理里
活 【学生】通过观察实验,学生完成表格 解与掌
动 握,实现
二 知识的内
化过程。
知识问题
化,促进
知识的理
解与应
用。创设
问题情
境,促进
对科学研
究的深度
理解。
【视频】播放演示实验3-4
【学生】通过观察实验,学生完成表格
【教师】利用硫氰化铁配离子等颜色,可用于鉴别溶液中存在Fe3+;
又由于硫氰化铁配离子的颜色极似血液,常被用于电影特技和魔术
【视频】播放演示实验3-5
【学生】通过观察实验,学生完成表格【教师】引导学生总结
活 【过渡】学生体会超分子的重要性 作为拓展
学生视见
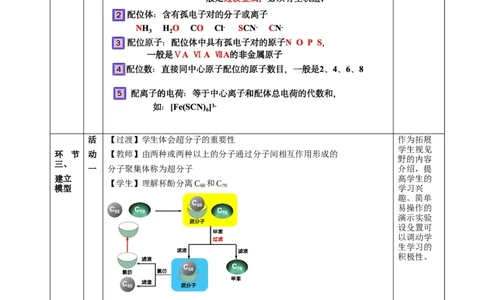
环 节 动 【教师】由两种或两种以上的分子通过分子间相互作用形成的
野的内容
三、
一 分子聚集体称为超分子 介绍,提
建立 高学生的
【学生】理解杯酚分离C 和C
模型 60 70 学习兴
趣。简单
易操作的
演示实验
设殳置可
以调动学
生学习的
积极性。
【问题】石墨性质的特点与其结构之间的关系?石墨晶体的结构特点是什么?
【学生】结合石墨晶体的性质特征思考其具备的晶体类型特点是兼有共价晶
体、分子晶体和金属晶体的一种混合型晶体。
活 【教师】冠醚识别碱金属离子(如K+) 通过教学
动 活动,激
【学生】观察图片
二 发学生对
自然现象
的关心,
培养学生
乐于探索
自然现象的情感,
以及善于
实践和勇
于克服困
难的良好
意志和品
质。
【教师】冠醚是皇冠状的分子,可有不同大小的空穴适配不同大小的碱金
属离子
1.下列说法不正确的是
A.(AlCl ) 中含有配位键
3 2
B.NH 的键角大于HO的键角
3 2
C.SiO 中的O—Si—O键角为120°
作 2
业 D.HBO 是弱酸,HBO 晶体中存在作用力为共价键、氢键和范德华力
3 3 3 3
环节 设
四、 计 【答案】C
课后
【解析】A.双聚氯化铝分子中具有空轨道的铝原子与具有孤电子对的氯原
巩固
子形成配位键,故A正确;
B.氨分子中氮原子的孤电子对数为1、水分子中氧原子的孤电子对数为
2、孤电子对数越多,对成键电子对的斥力越大,键角越小,所以氨分子的
键角大于水分子的键角,故B正确;
C.二氧化硅晶体中硅原子与4个氧原子形成硅氧四面体,所以晶体中O—
Si—O键角小于120°,为109º28',故C错误;
D.硼酸分子能与水分子作用生成四羟基合硼离子和氢离子,所以硼酸是一
元弱酸,硼酸晶体是存在作用力为共价键、氢键和范德华力的分子晶体,
故D正确;
故选C。
2.下列过程与配合物的形成无关的是( )
A.除去Fe粉中的SiO 可用强碱溶液
2
B.向一定量的AgNO 溶液中加入氨水至沉淀消失
3C.向FeCl 溶液中加入KSCN溶液
3
D.向一定量的CuSO 溶液中加入氨水至沉淀消失
4
【答案】 A
【解析】 A项,利用了SiO 可与强碱反应的化学性质,与配合物的形成
2
无关;B项,AgNO 与氨水反应生成了AgOH沉淀,继续反应生成了配离
3
子[Ag(NH)]+;C项,Fe3+与KSCN反应生成了配离子[Fe(SCN) ]3-n(n=1~
3 2 n
6);D项,CuSO 与过量氨水反应生成了配离子[Cu(NH )]2+。
4 3 4
3.0.01 mol氯化铬(CrCl ·6H O)在水溶液中用过量的AgNO 处理,产生0.01
3 2 3
mol AgCl沉淀,此氯化铬最可能是( )
A.[Cr(H O) ]Cl
2 6 3
B.[Cr(H O) Cl]Cl ·H O
2 5 2 2
C.[Cr(H O) Cl]Cl·2HO
2 4 2 2
D.[Cr(H O) Cl]·3H O
2 3 3 2
【答案】 C
【解析】 0.01 mol氯化铬(CrCl ·6H O)在水溶液中用过量的AgNO 处理,
3 2 3
产生0.01 mol AgCl沉淀,说明1 mol氯化铬(CrCl ·6H O)中有1 mol氯离子
3 2
在外界,其余在内界,而正三价铬为六配位,则此氯化铬最可能是
[Cr(H O) Cl]Cl·2HO。
2 4 2 2
4.向硫酸铜溶液中逐渐通入过量氨气,然后加入适量乙醇,溶液中析出深
蓝色的[Cu(NH )]SO ·H O。关于该晶体下列说法中错误的是( )
3 4 4 2
A.加入乙醇的目的是降低溶剂的极性,促使[Cu(NH )]SO ·H O析出
3 4 4 2
B.该配合物晶体中,N是配位原子,NH 为三角锥形,配位数是4
3
C.配离子内N原子排列成为平面正方形,可见Cu2+采取sp3杂化
D.向该晶体的水溶液中加入浓BaCl 溶液有白色沉淀生成
2
【答案】 C
【解析】 配离子内N原子形成平面正方形,Cu2+不为sp3杂化,C错误。
5.某物质的结构如图所示:
下列有关该物质的分析中正确的是( )
A.该物质分子中不存在σ键
B.该物质的分子内只存在共价键和配位
键两种作用力
C.该物质是一种配合物,其中Ni为中心
原子
D.该物质的分子中C、N、O均存在孤电子对
【答案】 C
【解析】 A项,该物质中碳原子之间、碳氢原子间、碳氮原子间等,均存
在σ键;B项,该物质中H、O间存在氢键,C与其他原子间存在共价键,
Ni、N之间存在配位键,所以该物质的分子内存在氢键、共价键、配位键三
种作用力;C项,Ni具有空轨道,接受孤电子对,是配合物的中心原子;D
项,C最外层的4个电子全部参与成键,没有孤电子对。
6.关于化学式为[TiCl(H O) ]Cl ·H O的配合物的下列说法中正确的是( )
2 5 2 2A.配体是Cl-和HO,配位数是9
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中的Cl-的数目比是1∶2
D.加入足量AgNO 溶液,所有Cl-均被完全沉淀
3
【答案】 C
【解析】 配合物[TiCl(H O) ]Cl ·H O中配体是Cl-和HO,配位数是6,A
2 5 2 2 2
错误;中心离子是Ti3+,B错误;加入足量AgNO 溶液,外界离子Cl-与
3
Ag+反应,内界中配位离子Cl-不与Ag+反应,D错误。
7.X、Y、Z、W为原子序数依次增大的短周期元素,基态Y原子的s能级
电子数是p能级的2倍,基态W原子的电子总数是其最高能级电子数的2
倍,XW+是10电子微粒,可形成离子液体[Y XZX]+[ZW ]-。下列说法正确
3 2 5 3 3
的是
A.第一电离能:YO>C,A正确;
1
B.HO+中心原子O价层电子对数:3+ (5-3×1)=4,含1对孤电子对,空间
3 2
1
结构为三角锥形;NO- 中心原子N原子价层电子对数:3+ (6-3×2)=3,为平
3 2
面三角形,B错误;
C.N 中的共价键是三键,键能最大,C错误;
2
D.[Y XZX]+内不存在分子间相互作用力氢键,D错误;
2 5 3
答案选A。
8.利用超分子的某种特性可分离C 和C 。将C 、C 的混合物加入一种
60 70 60 70
空腔大小适配C 的“杯酚”中可发生如图所示变化。下列说法错误的是(
60
)
A.C 和C 互为同素
70 60
异形体
B.“杯酚”分子中存
在大π键
C.“杯酚”与C 之间
60
形成氢键
D.C 不能与“杯酚”形成超分子
70
【答案】 C
【解析】 C 和C 是由碳元素组成的不同单质,互为同素异形体,A正
70 60
确;“杯酚”分子中含有苯环,苯环中存在大π键,B正确;氢键普遍存在
于已经与N、O、F等电负性很大的原子形成共价键的氢原子与另外的N、
O、F等电负性很大的原子之间,“杯酚”与C 之间不能形成氢键,C错
60
误;C 分子比C 分子大,将C 、C 的混合物加入一种空腔大小适配C
70 60 60 70 60的“杯酚”中,“杯酚”能与C 形成超分子,而不能与C 形成超分子,D
60 70
正确。
9.如图是卟啉配合物叶绿素的结构示意图,下列
有关叙述正确的是( )
A.示意图中氧原子的杂化类型无法确定
B.该叶绿素是配合物,中心离子是镁离子
C.该叶绿素是配合物,其配体是N元素
D.该叶绿素不是配合物,而是高分子
【答案】 B
【解析】 Mg的最高化合价为+2价,而化合物
中Mg与4个氮原子形成化学键,由此可以判断该化合物中Mg与N间存在
配位键,该物质为配合物,B正确;因氮原子还与碳原子成键,因此只能说
氮原子是配位原子而不能说是配体,故C错误;该叶绿素是配合物,不是
高分子,故D错误。
10.BF 与一定量的水形成(H O) •BF ,一定条件下(H O) •BF 可发生如图转
3 2 2 3 2 2 3
化,下列说法正确的是
A.BF 和 中B原子均采用sp2杂化轨道成键
3
B.(H O) •BF 分子中存在氢键和配位键
2 2 3
C.(H O) •BF 中的所有元素都位于元素周期表中的p区
2 2 3
D.BF、NF 分子中的原子个数比相同,两者都是极性分子
3 3
【答案】B
【解析】
A.BF 形成3个共价键,采用sp2杂化轨道成键; 中B原子形
3
成4个共价键,采用sp3杂化轨道成键,A错误;
B.分子间的HO与HO之间形成氢键,分子中O原子提供孤电子对,B原
2 2
子提供空轨道,O与B原子之间存在配位键,B正确;
C.H为s区元素,C错误;
D.BF 中B原子采取sp2杂化,分子空间构型为平面三角形,结构对称,正
3
负电荷重心重合,为非极性分子;NF 中N原子采取sp3杂化,分子空间构
3
型为三角锥形,为极性分子,D错误;
故选B。
二、非选择题
11.配位化合物在生产生活中有重要应用,请根据要求回答下列问题:(1)光谱证实单质铝与强碱性溶液反应有[Al(OH) ]-生成,则[Al(OH) ]-中存
4 4
在________(填序号)。
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(2)Co(NH )BrSO 可形成两种钴的配合物,已知Co3+的配位数是6,为确定
3 5 4
钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的
溶液中加BaCl 溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl
2 2
溶液时,则无明显现象。则第一种配合物的结构可表示为
______________________,第二种配合物的结构可表示为
___________________________。若在第二种配合物的溶液中滴加AgNO 溶
3
液,则产生的现象是________________________________
__________。
【答案】 (1)acd (2)[CoBr(NH )]SO [Co(SO )(NH )]Br 生成淡黄色沉
3 5 4 4 3 5
淀
【解析】 (1)光谱证实单质Al与强碱性溶液反应有[Al(OH) ]-生成,可看
4
作铝原子和三个羟基形成三个共用电子对,形成三个极性共价键,形成
Al(OH) ,Al(OH) 溶解在强碱性溶液中,和OH-结合形成[Al(OH) ]-,利用
3 3 4
的是铝原子的空轨道和OH-的孤电子对形成的配位键;共价单键为σ键,
所以[Al(OH) ]-中也形成了σ键。
4
(2) 加入BaCl 溶液时,产生白色沉淀,说明硫酸根离子为配合物的外界,
2
在水溶液中以离子形式存在,所以会与钡离子结合生成白色沉淀,则配合
物的结构为[CoBr(NH )]SO ;若加入BaCl 溶液时无明显现象,说明硫酸根
3 5 4 2
离子在内界,所以配合物的结构为[Co(SO )(NH )]Br;溴离子为配合物的外
4 3 5
界,在水溶液中以离子形式存在,若加入AgNO 溶液,会产生淡黄色沉淀
3
溴化银。
12.蛇纹石是一类含水富镁硅酸盐矿物,主要成分为MgO和SiO,含少量
2
Fe、Ni的氧化物。可用于生产重要无机化工产品碱式碳酸镁
[Mg (OH) CO)。其制备流程如图所示:
2 2 3
(1)①滤渣1的主要成分从性质上来分,属于 氧化物,其用途很
广泛,请写出一种: 。
A.酸性 B.两性 C.碱性
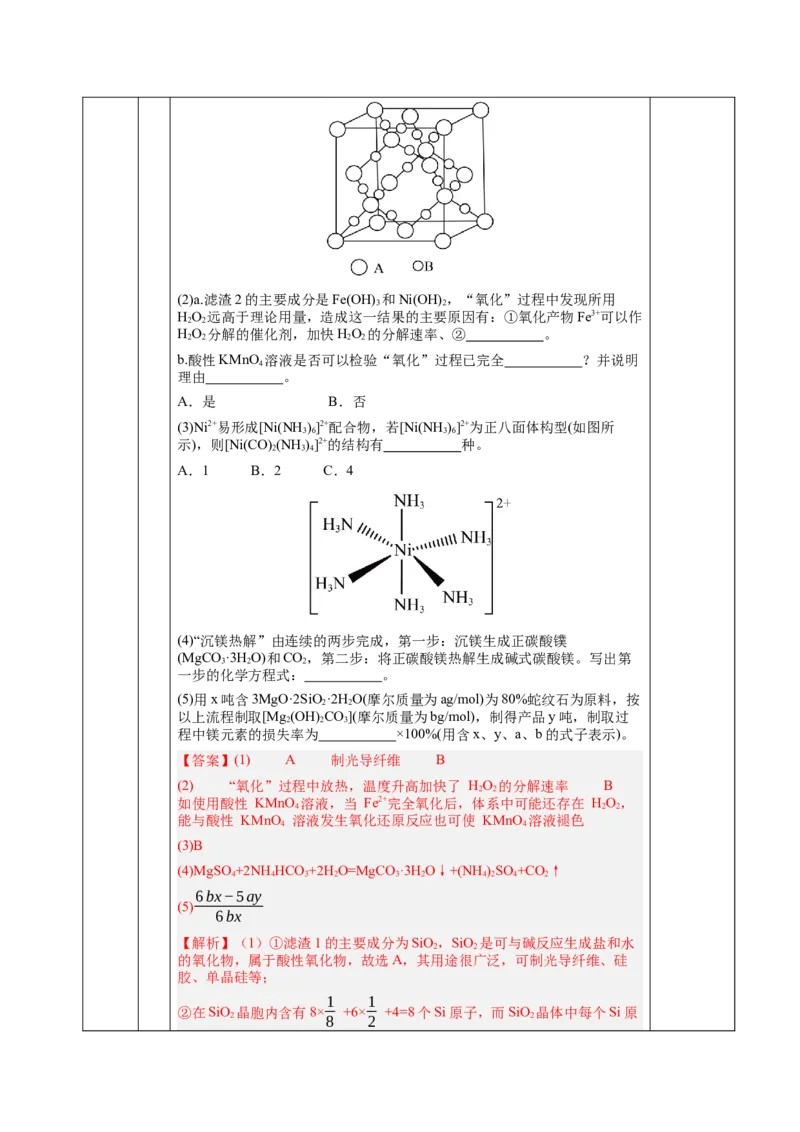
②如图表示该物质晶体的晶胞结构,1个该晶胞中含有 个A-B
键。
A.28 B.32 C.36(2)a.滤渣2的主要成分是Fe(OH) 和Ni(OH) ,“氧化”过程中发现所用
3 2
HO 远高于理论用量,造成这一结果的主要原因有:①氧化产物Fe3+可以作
2 2
HO 分解的催化剂,加快HO 的分解速率、② 。
2 2 2 2
b.酸性KMnO 溶液是否可以检验“氧化”过程已完全 ?并说明
4
理由 。
A.是 B.否
(3)Ni2+易形成[Ni(NH )]2+配合物,若[Ni(NH )]2+为正八面体构型(如图所
3 6 3 6
示),则[Ni(CO) (NH )]2+的结构有 种。
2 3 4
A.1 B.2 C.4
(4)“沉镁热解”由连续的两步完成,第一步:沉镁生成正碳酸镤
(MgCO ·3H O)和CO,第二步:将正碳酸镁热解生成碱式碳酸镁。写出第
3 2 2
一步的化学方程式: 。
(5)用x吨含3MgO·2SiO ·2H O(摩尔质量为ag/mol)为80%蛇纹石为原料,按
2 2
以上流程制取[Mg (OH) CO](摩尔质量为bg/mol),制得产品y吨,制取过
2 2 3
程中镁元素的损失率为 ×100%(用含x、y、a、b的式子表示)。
【答案】(1) A 制光导纤维 B
(2) “氧化”过程中放热,温度升高加快了 HO 的分解速率 B
2 2
如使用酸性 KMnO 溶液,当 Fe2+完全氧化后,体系中可能还存在 HO,
4 2 2
能与酸性 KMnO 溶液发生氧化还原反应也可使 KMnO 溶液褪色
4 4
(3)B
(4)MgSO +2NHHCO +2H O=MgCO ·3H O↓+(NH)SO +CO ↑
4 4 3 2 3 2 4 2 4 2
6bx−5ay
(5)
6bx
【解析】(1)①滤渣1的主要成分为SiO,SiO 是可与碱反应生成盐和水
2 2
的氧化物,属于酸性氧化物,故选A,其用途很广泛,可制光导纤维、硅
胶、单晶硅等;
1 1
②在SiO 晶胞内含有8× +6× +4=8个Si原子,而SiO 晶体中每个Si原
2 8 2 2子与相邻的4个O原子形成4个Si-O共价键,则1个该晶胞中含有的Si-O
共价键数目是8×4=32个,故选B;
(2)a .加入的HO 将Fe2+氧化为Fe3+,因Fe3+可以催化HO 分解,且
2 2 2 2
HO 受热易分解,导致“氧化”过程中所用HO 远高于理论用量,造成这
2 2 2 2
一结果的主要原因有:①氧化产物Fe3+可以作HO 分解的催化剂,加快
2 2
HO 的分解速率、②“氧化”过程中放热,温度升高加快了HO 的分解速
2 2 2 2
率;
b.因HO 也能使酸性KMnO 溶液褪色,则酸性KMnO 溶液不可以检验
2 2 4 4
“氧化”过程已完全,理由是:如使用酸性KMnO 溶液,当 Fe2+完全氧化
4
后,体系中可能还存在HO,能与酸性KMnO 溶液发生氧化还原反应也可
2 2 4
使KMnO 溶液褪色;
4
(3)若[Ni(NH )]2+为正八面体构型,则[Ni(CO) (NH )]2+相当于在正八面体
3 6 2 3 4
上二取代,会产生邻、对位取代,共2种结构,故选B;
(4)第一步:主要含有MgSO 的滤液与NH HCO 发生反应生成正碳酸镁
4 4 3
(MgCO ·3H O)、CO 和(NH )SO ,则反应的化学方程式为:
3 2 2 4 2 4
MgSO +2NHHCO +2H O=MgCO ·3H O↓+(NH)SO +CO ↑;
4 4 3 2 3 2 4 2 4 2
(5)x吨含3MgO·2SiO ·2H O(摩尔质量为ag/mol)为80%蛇纹石中含镁元素
2 2
质量为:
3×24
x×80%× 吨,y吨产品[Mg (OH) CO](摩尔质量为bg/mol)中含镁元素
a 2 2 3
2×24
质量为:y×
b
3×24 2×24
x×80%× −y×
a b
吨,则制取过程中镁元素的损失率为
3×24
x×80%×
a
6bx−5ay
×100%= ×100%。
6bx
两种超分子特征:(1)分子识别 (2)自组装
课堂总结 分子识别两个实例介绍
① “杯酚”分离 C 和 C
60 70
② 冠醚识别碱金属离子
板书
设计由于配合物和配位键的概念较为抽象,教学中可以多运用实验探究和多媒体辅助教
学的方式,让学生直观感受典型配合物的形成过程,以及中心离子和配体间的相互作
用。
教学 通过实验介绍简单配合物的制备和性质,帮助学生建立配合物的认知模型,同时让
学生认识到配位键不仅存在于金属离子与某些分子间,也能存在于金属离子与某些离子
反思
间,加深对配位键本质和配合物理论的理解。引导学生将配位键和配合物的概念纳入到
已有的知识系统中,实现知识的结构化,更新学生的知识结构。在教授超分子的概念
时,重点提升学生的科学精神和社会责任,鼓励学生从微观角度理解配位键的形成条件
和表示方法,以及判断常见的配合物。
随着科学的不断发展,配合物与超分子领域也在不断进步,教师应不断更新教学内
容,引入最新的科学发现和理论。积极听取学生的反馈,了解他们在学习过程中遇到的
困难和疑惑,及时调整教学策略。