文档内容
第三章 水溶液中的离子反应与平衡
课题
第四节 难溶电解质溶解平衡
1、让学生掌握难溶电解质的溶解平衡概念,并运用平衡移动原理分
知识与技
析、解决沉淀的生成、溶解和转化问题。
能
2、培养学生动手实验能力、归纳概括能力、知识迁移能力。
教
1、体验难溶电解质的溶解平衡建立的过程、平衡移动的过程;
学 过程与方
2、让学生掌握科学探究的方法,根据实验现象和已有的知识经验,
目 法
分析推理出新的知识的方法。
标
激发学生学习化学的热情,培养其将化学知识应用于生产、生活
情感态度
实践的能力,认识自然科学中的对立统一的辩证唯物主义,能够对与
与价值观
化学有关的社会和生活问题作出合理的判断。
教学
重点 难溶电解质的溶解平衡的建立和应用
教学
难点 难溶电解质的溶解平衡的建立和应用
教
学科网(北京)股份有限公司
学
设
本节内容是第三章《水溶液中的离子平衡》的最后一部分,包括难溶电解质的
溶解平衡及其应用两个部分。本节应用第二章所学的化学平衡理论,探讨水溶液中
教 离子平衡问题,是化学平衡学习的延伸与拓展,是对中学化学的平衡理论体系的完
材
善和丰富,是中学化学基础理论的一个重要部分,也是学生整个中学阶段的难点。
分
析
通过本章的学习,学生可以感受理论分析的作用,体会相关知识在生产生活中的应
用价值,进一步拓展和巩固前一章所学知识,更为透彻地理解在溶液中发生离子反
应的原理。
高二学生已经具备了独立思考的能力,而且思维活跃;学习自觉性增强,能通
学 过自学主动获取知识。
情
分
高二学生已经了解了AgCl、AgI、Ag
2
S等物质的颜色和溶解性,学习了复分解反
析
应、化学平衡、电离平衡、盐类的水解平衡等知识,并具备应用其解决简单实际问
题的能力。
想
教
法
探究法
设
计
教学 教 学 内 容 设计意图
环节
教师活动 学生活动【投影】情景1龋齿
【回顾】复分解反应发生的条件 化 学 来 源 于 生
【演示实验1】步骤一、二 观看、思考、交流、 活,激发学习兴
引
入 问:在Ag++Cl-== AgCl↓的反应中, 回答。 趣。以学生熟知
新
当溶液中Cl-大量过量时,你认为溶液
学 生 的 回 答 是 :
的 知 识 提 出 问
课
中哪种离子反应完全? + 题,激发思考,
Ag 反应完全。
追问:那反应后所得到的体系中到底 引出新课。
还有没有Ag+呢?
导
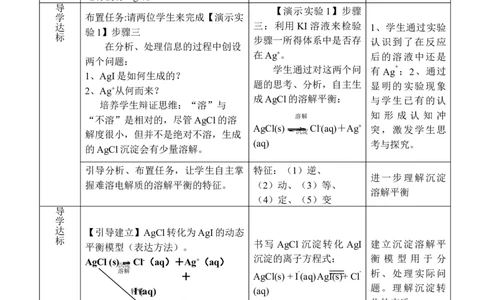
【演示实验 1】步骤
学 布置任务:请两位学生来完成【演示实
达 三:利用 KI 溶液来检验 1、学生通过实验
验1】步骤三
标
步骤一所得体系中是否存 认识到了在反应
在分析、处理信息的过程中创设
在Ag+。 后的溶液中还是
两个问题:
学生通过对这两个问 有 Ag + ;2、通过
1、AgI是如何生成的?
题的思考、分析,自主生 显明的实验现象
2、Ag+从何而来?
成AgCl的溶解平衡: 与学生已有的认
培养学生辩证思维:“溶”与
知 形 成 认 知 冲
“不溶”是相对的,尽管AgCl的溶 溶解
AgCl(s) Cl-(aq)+Ag+ 突,激发学生思
解度很小,但并不是绝对不溶,生成 沉淀
(aq) 考与探究。
的AgCl沉淀会有少量溶解。
引导分析、布置任务,让学生自主掌 特征:(1)逆、
进一步理解沉淀
握难溶电解质的溶解平衡的特征。 (2)动、(3)等、
溶解平衡
(4)定、(5)变
导
学
达 【引导建立】AgCl转化为AgI的动态
标
书写 AgCl 沉淀转化 AgI 建立沉淀溶解平
平衡模型(表达方法)。
沉淀的离子方程式: 衡 模 型 用 于 分
AgCl (s) Cl-(aq)+Ag+(aq)
沉淀
溶解 - - 析、处理实际问
+ AgCl(s) + I(aq)AgI(s)+ Cl
题。理解沉淀转
转 I-化(aq) (aq)
化的实质。
归纳:沉淀转化的实质就
是沉淀溶解平衡的移动。
AgI(s)
导
归纳概括沉淀转化的一般
学
达 【演示实验2】 规律:一般说来,溶解度 学生体验探究过
标
提醒学生对比观察实验现象,指导阅 小的沉淀转化成溶解度更 程,发现规律,
读教材 61 页表 3—4 几种电解质的 小的沉淀容易实现;两者 深化对沉淀转化
溶解度。 的溶解度差别越大转化越 的理解。
容易。
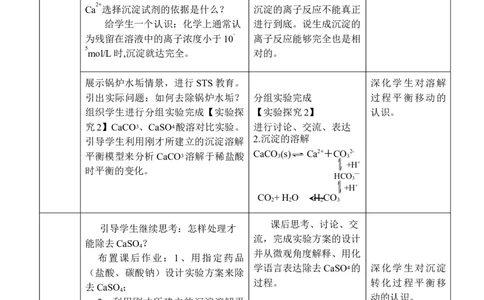
学科网(北京)股份有限公司分组实验完成
创设两个情景:硬水的软化和水 【实验探究1】
垢的处理。组织学生进行分组实验探 1、沉淀的生成。
究。 认识到沉淀试剂的选
首先提出一个实际问题:如何除 择原则:首先要使生成沉
2+
去硬水中的 Ca ?然后组织学生进行 淀的反应能够发生;其次
帮助学生深化认
分组实验完成【实验探究1】1、沉淀 希望沉淀生成的反应进行
识,理解沉淀完
的生成。 得越完全越好。
全的相对性。
引导学生思考:除去水中的 进一步认识到,生成
2+
Ca 选择沉淀试剂的依据是什么? 沉淀的离子反应不能真正
给学生一个认识:化学上通常认 进行到底。说生成沉淀的
-
为残留在溶液中的离子浓度小于10 离子反应能够完全也是相
5
mol/L时,沉淀就达完全。 对的。
展示锅炉水垢情景,进行STS教育。 深化学生对溶解
引出实际问题:如何去除锅炉水垢? 分组实验完成 过程平衡移动的
组织学生进行分组实验完成【实验探 【实验探究2】 认识。
究2】CaCO3、CaSO4酸溶对比实验。 进行讨论、交流、表达
引导学生利用刚才所建立的沉淀溶解
2.沉淀的溶解
平衡模型来分析CaCO3溶解于稀盐酸 CaCO 3 (s) Ca2++CO 3 2-
+H+
时平衡的变化。
HCO —
3
+H+
CO + H O H CO
2 2 2 3
课后思考、讨论、交
引导学生继续思考:怎样处理才
流,完成实验方案的设计
能除去CaSO ?
4
并从微观角度解释、用化
布置课后作业:1、用指定药品
学语言表达除去CaSO4的 深化学生对沉淀
(盐酸、碳酸钠)设计实验方案来除
过程。 转化过程平衡移
去CaSO ;
4
动的认识。
2、利用刚才所建立的沉淀溶解平
衡模型从平衡移动的角度来分析、解
释除去CaSO 的原理。
4
思考、讨论、归纳:
引导学生思考、讨论、归纳:通
拓宽和加深对原
在溶液中进行的复分解反
过上面的探究,你对复分解反应发
有知识的认识
应总是向着反应体系中某
生的条件有什么新的认识?
些离子浓度减小的方向进
行。
学科网(北京)股份有限公司加深理解
展示【随堂练习】,投影含氟牙膏能
思考、回答。
巩固新知
防止龋齿的原因。
作
业
设
计
板 五、难溶电解质的溶解平衡
(一)溶解平衡
书
1、概念:
2、表达式:如: AgCl (s) Cl-(aq)+Ag+(aq)
设
3、特征:动、等、定、变
4、影响溶解平衡的因素:
计
(1)内因:
(2)外因:
(二)沉淀反应的应用
1、沉淀的生成
2、沉淀的溶解
3、沉淀的转化
三、溶度积(平衡常数)——K
sp
对于沉淀溶解平衡:(平衡时) M A (s) mMn+(aq)+ nAmˉ(aq)
m n
K =[ c (Mn+) ]m·[c(Am ˉ)]n
sp
在一定温度下,K 是一个常数,称为溶度积常数,简称溶度积。
sp
若任意时刻有: Qc= [ c (Mn+) ]m·[c(Amˉ )]n
则有: Qc > K 过饱和,析出沉淀,
sp
Qc = K 饱和,平衡状态
sp
Qc < K 未饱和。
sp
学科网(北京)股份有限公司学科网(北京)股份有限公司