文档内容
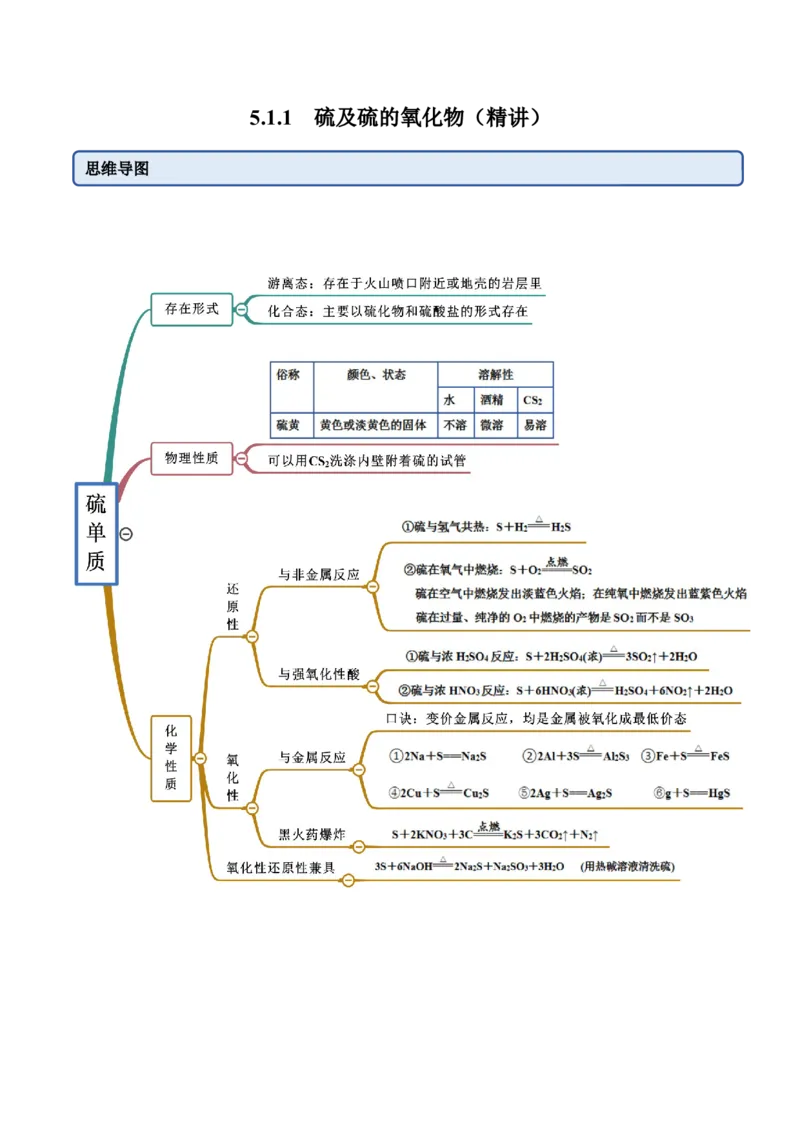
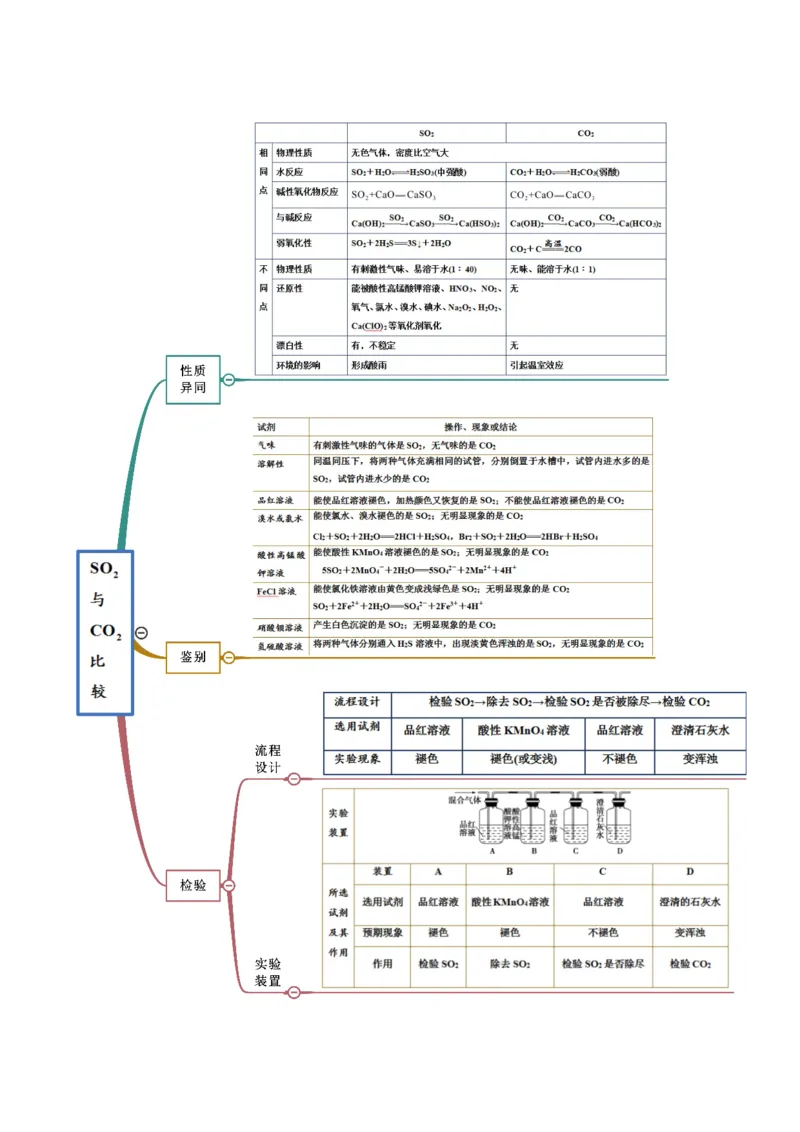
5.1.1 硫及硫的氧化物(精讲)
思维导图常见考点
考点一 硫单质
【例1-1】(2021·辽宁·大连市第一中学高一期中)下列关于硫单质的叙述错误的是
A.硫(俗称硫黄)是一种黄色晶体 B.硫易溶于水,自然界中无单质硫存在
C.硫在空气中燃烧时生成二氧化硫 D.硫质脆,易研成粉末
【答案】B
【解析】A. 硫(俗称硫黄)是一种黄色晶体,故A正确;
B. 硫难溶于水,微溶于酒精,易溶于二硫化碳,自然界中有单质硫和硫的化合物存在,故B错误;
C.硫化学性质比较活泼,在空气中燃烧时生成二氧化硫,故C正确;
D. 硫质脆,易研成粉末,故D正确;故答案为:B
【例1-2】(2021·吉林·高一期中)下列关于硫单质参与反应的化学方程式正确的是
A.与少量铜反应S+Cu CuS
B.与少量铁反应2S+Fe FeS
2
C.与足量纯氧气反应S+O SO
2 2
D.与氢氧化钠溶液反应3S+4NaOH 2NaS+SO↑+2H O
2 2 2
【答案】C【解析】A.与少量铜反应生成硫化亚铜:S+2Cu Cu S,故A错误;
2
B.与少量铁反应生成硫化亚铁:S+Fe FeS,故B错误;
C.与足量纯氧气反应生成二氧化硫:S+O SO ,故C正确;
2 2
D.与氢氧化钠溶液反生成硫化钠和亚硫酸钠:3S+6NaOH 2NaS+Na SO +3H O,故D错误;故选
2 2 3 2
C。
【一隅三反】
1.(2021·北京东城·高一期末)下列关于硫(俗称硫黄)的说法中,正确的是
A.易溶于水 B.与氢气反应生成
C.在氧气中燃烧生成 D.与铁反应生成
【答案】B
【解析】A. 为非极性分子,水是极性分子,难溶于水,A项错误;
B.与氢气反应式: ,B项正确;
C.在氧气中燃烧反应式: ,C项错误;
D.与铁反应式:,D项错误;故选B。
2.(2021·广东梅州·高一期末)中医用药讲究十八反和十九畏,其中有“硫黄原是火中精,朴硝一见便相
争”的说法,硫黄即硫单质。下列关于硫的说法中正确的是
A.硫是一种淡黄色能溶于水的固体 B.过量的硫与铁反应生成Fe S
2 3
C.试管内壁上的硫黄可用二硫化碳清洗 D.硫在过量纯氧中燃烧生成三氧化硫
【答案】C
【解析】A.硫是一种淡黄色的固体,但不溶于水,A项错误;
B.硫与铁反应生成FeS,与硫用的量无关,B项错误;
C.硫黄易溶于二硫化碳,难溶于酒精,试管内壁上的硫黄可用二硫化碳清洗,C项正确;D.硫在过量纯氧中燃烧生成二氧化硫,D项错误;
答案选C。
3(2021·吉林·长春市第二十九中学高一期末)下列说法错误的是
A.硫在自然界的存在形式既有化合态,也有游离态
B.残留在试管内壁上的硫可用CS 溶解除去
2
C.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
D.硫单质与变价金属反应时一般生成低价态的金属硫化物
【答案】C
【解析】A.硫元素在自然界中有化合物和单质形式存在,在自然界中既有游离态,又有化合态,故A正
确;
B.非极性分子易溶于非极性分子,残留在试管内壁上的硫可用CS 溶解除去,S能够与NaOH反应,也可
2
用热的NaOH溶液除去,故B正确;
C.单质硫或含硫物质燃烧时,无论氧气多少,都生成SO ,不能生成SO ,故C错误;
2 3
D.硫单质具有弱氧化性,硫与变价金属反应,一般生成低价态的金属化合物,如加热时Cu与S反应生成
Cu S,故D正确;
2
故选C。
4.(2021·天津滨海新·高一期末)下列关于硫的说法不正确的是
A.游离态的硫存在于火山口附近或地壳的岩层里
B.单质硫既有氧化性,又有还原性
C.试管内壁附着的硫可用二硫化碳溶解除去
D.硫与铁、铜反应,生成FeS、CuS
【答案】D
【解析】A.游离态的硫存在于火山喷口附近和地壳的岩层里,土壤中和空气中的S以化合态形式存在,A
正确;
B.单质硫化合价为0价,既能升高又能降低,所以既有氧化性,又有还原性,B正确;
C.硫易溶于二硫化碳,所以试管内壁附着的硫可用二硫化碳溶解除去,C正确;
D.S的氧化性较弱,铜与S反应生成Cu S,D错误;
2
综上所述答案为D。
5.(2021·山西·盂县第三中学校高一期中)0.1mol某单质与足量硫充分反应,质量增加了1.6g,则组成这
种单质的元素不可能是
A.Ag B.K C.Cu D.Fe【答案】D
【解析】质量增加1.6g是参加反应硫的质量,其物质的量是0.05mol,令金属在硫化物中的化合价是x,根
据得失电子守恒,则0.1x=0.05×2,故x=1,选项中Ag、K、Cu与硫反应都变为+1价,而铁与硫反应生成
硫化亚铁,铁表现为+2价,故答案为D。
6.(2021·吉林·高一期中)下列关于硫单质参与反应的化学方程式正确的是
A.与少量铜反应S+Cu CuS
B.与少量铁反应2S+Fe FeS
2
C.与足量纯氧气反应S+O SO
2 2
D.与氢氧化钠溶液反应3S+4NaOH 2NaS+SO↑+2H O
2 2 2
【答案】C
【解析】A.与少量铜反应生成硫化亚铜:S+2Cu Cu S,故A错误;
2
B.与少量铁反应生成硫化亚铁:S+Fe FeS,故B错误;
C.与足量纯氧气反应生成二氧化硫:S+O SO ,故C正确;
2 2
D.与氢氧化钠溶液反生成硫化钠和亚硫酸钠:3S+6NaOH 2NaS+Na SO +3H O,故D错误;
2 2 3 2
故选C。
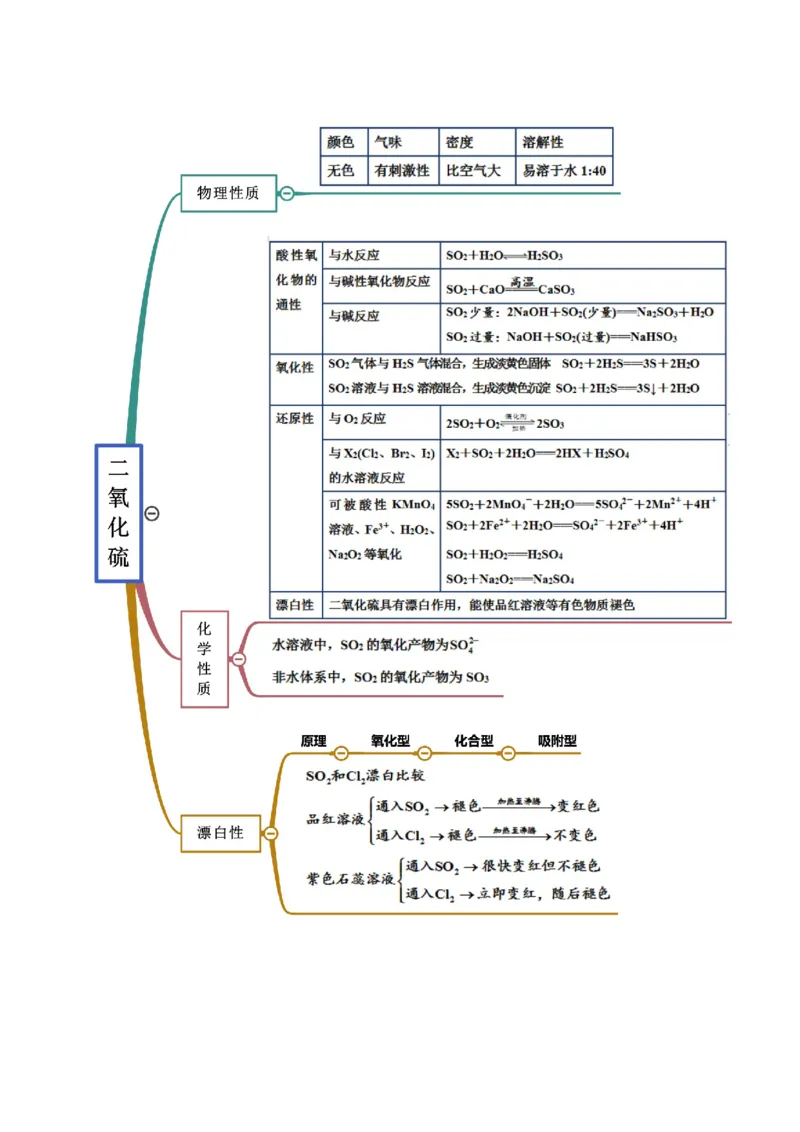
考点二 二氧化硫
【例2-1】(2021·四川·攀枝花市成都外国语学校高一月考)下列有关二氧化硫的性质叙述中,不正确的是
A.工业生产中常用生石灰来吸收废气中的二氧化硫
B.二氧化硫的水溶液能使紫色石蕊溶液变红,说明二氧化硫能与水反应生成酸
C.二氧化硫能使有色物质颜色消失,说明二氧化硫具有氧化性D.二氧化硫能使酸性高锰酸钾溶液褪色,说明二氧化硫具有还原性
【答案】C
【解析】A.CaO+SO=CaSO ,故工业生产中常用生石灰来吸收废气中的二氧化硫,A正确;
2 3
B.二氧化硫的水溶液能使紫色石蕊溶液变红,SO +H O HSO ,说明二氧化硫能与水反应生成酸,B
2 2 2 3
正确;
C.二氧化硫能使有色物质颜色消失,是由于SO 与有色物质直接结合为无色不稳定的化合物,与氧化还
2
原反应无关,C错误;
D.二氧化硫能使酸性高锰酸钾溶液褪色,是SO 将KMnO 还原为无色的Mn2+,自身被氧化为HSO ,则
2 4 2 4
说明二氧化硫具有还原性,D正确;故答案为:C。
【例2-2】(2021·四川·邻水实验学校高一月考)下列实验中能证明某气体为SO 的是
2
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaCl 溶液,有白色沉淀生成,该沉淀溶于稀盐酸
2
⑤通入溴水中,能使溴水褪色,再滴加Ba(NO ) 溶液有白色沉淀产生
3 2
A.都能证明 B.都不能证明
C.③④⑤均能证明 D.只有⑤能证明
【答案】D
【解析】①CO 也能使澄清石灰水变浑浊;
2
②酸性气体均能使湿润的蓝色石蕊试纸变红;
③Cl 也能使品红溶液褪色;④CO 也有此现象;
2 2
⑤二氧化硫具有还原性,能与溴单质发生氧化还原反应而使其褪色,滴加硝酸钡,被硝酸根离子氧化成硫
酸根,硫酸根离子与钡离子反应生产硫酸钡沉淀;因此只有⑤能证明某气体为二氧化硫,D符合题意;
故选答案D。
【例2-3】(2021·四川·攀枝花市成都外国语学校高一月考)某化学兴趣小组为探究SO 的性质,按下图所
2
示装置进行实验。(已知:NaSO +H SO =Na SO +SO↑+H O)
2 3 2 4 2 4 2 2(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是___________、___________。
(2)反应后,装置B中反应的离子方程式为___________;装置C中发生反应的化学方程式为
___________;装置D中发生反应的化学方程式为___________。
(3)装置E的目的是探究SO 与品红作用的可逆性,请写出实验操作及现象_________。
2
(4)F装置的作用是___________,其中漏斗的作用是___________。
【答案】(1)分液漏斗 圆底烧瓶
(2)Cl+SO+2H O=4H⁺+SO +2Cl— 5SO +2KMnO +2H O=KSO +2MnSO +2H SO
2 2 2 2 4 2 2 4 4 2 4
SO +2H S=3S↓+2H O
2 2 2
(3)品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,无色溶液恢复为红色
(4) 吸收二氧化硫,防止污染空气 防倒吸
【解析】(1)由实验装置图可知,装置A中盛放浓硫酸和亚硫酸钠的仪器分别为分液漏斗和圆底烧瓶,
故答案为:分液漏斗;圆底烧瓶;
(2)由分析可知,装置B中发生的反应为通入的二氧化硫与氯水反应生成硫酸和盐酸,使氯水褪色,反
应的离子方程式为Cl+SO+2H O=4H⁺+SO +2Cl—;装置C中发生的反应为通入的二氧化硫与酸性高锰酸
2 2 2
钾溶液反应生成硫酸钾、硫酸锰、硫酸,使酸性高锰酸钾溶液褪色,反应的化学方程式为
5SO +2KMnO +2H O=KSO +2MnSO +2H SO ;装置C中发生的反应为通入的二氧化硫与氢硫酸反应生成
2 4 2 2 4 4 2 4
硫沉淀和水,反应的化学方程式为SO +2H S=3S↓+2H O,故答案为:Cl+SO+2H O=4H++SO +2Cl—;
2 2 2 2 2 2
5SO +2KMnO +2H O=KSO +2MnSO +2H SO ;SO +2H S=3S↓+2H O;
2 4 2 2 4 4 2 4 2 2 2
(3)二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色,则探究二氧化硫与品红作用的可逆性
操作为待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,观察到的现象为无色溶液恢复为红色,故答案为:待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,无色溶液恢复为红色;
(4)由分析可知,装置F中氢氧化钠溶液用于吸收未反应的二氧化硫,防止污染空气,倒置的漏斗用于
防止产生倒吸,故答案为:吸收二氧化硫,防止污染空气;防倒吸。
【一隅三反】
1.(2021·上海市南洋模范中学高一期中)燃煤锅炉的烟囱冒出的浓烟中含有SO 气体,污染空气,消除
2
污染的方法一般是将浓烟通入
A.盐酸 B.碱溶液 C.氯化钠溶液 D.水
【答案】B
【解析】A.SO 气体不能与盐酸反应,不能除去二氧化硫,故A选项错误。
2
B.SO 气体能与碱溶液反应生成盐和水,能除去二氧化硫,故B选项正确。
2
C.SO 气体不能与氯化钠溶液反应,不能除去二氧化硫,故C选项错误。
2
D.SO 气体能与水反应生成亚硫酸,但吸收效果不如碱溶液,故D选项错误。故选B。
2
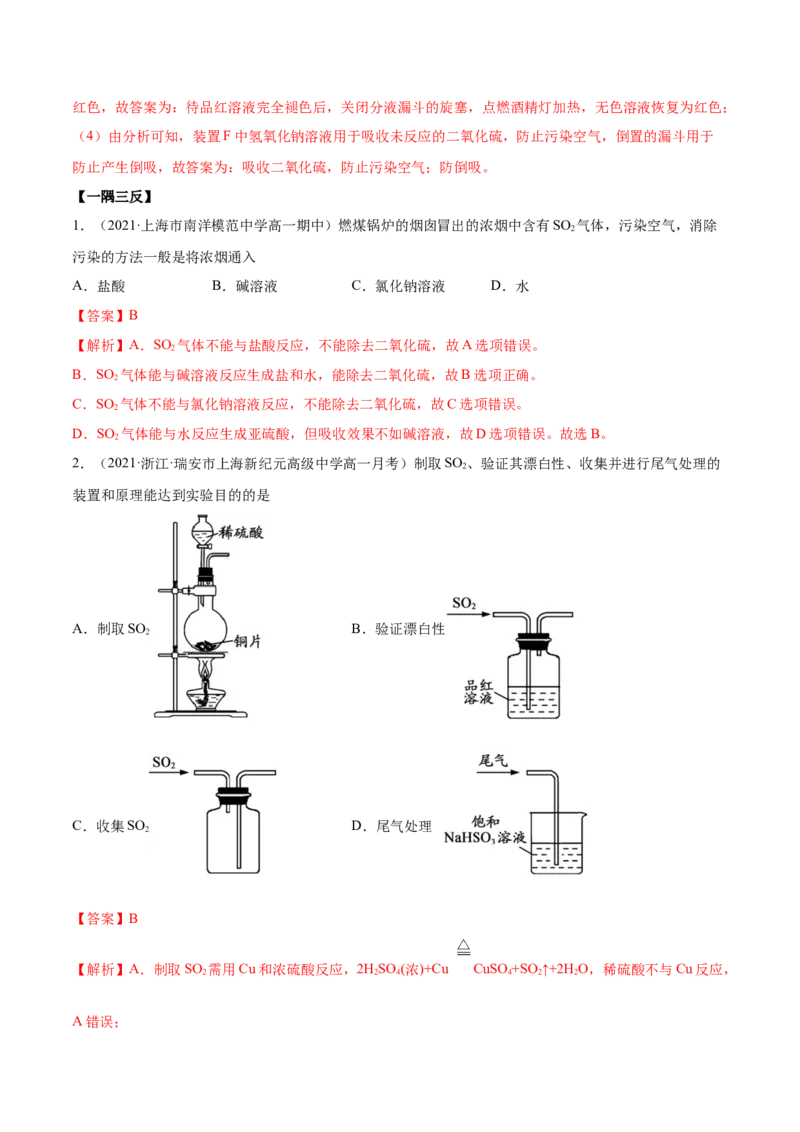
2.(2021·浙江·瑞安市上海新纪元高级中学高一月考)制取SO 、验证其漂白性、收集并进行尾气处理的
2
装置和原理能达到实验目的的是
A.制取SO B.验证漂白性
2
C.收集SO D.尾气处理
2
【答案】B
【解析】A.制取SO 需用Cu和浓硫酸反应,2HSO (浓)+Cu CuSO +SO↑+2H O,稀硫酸不与Cu反应,
2 2 4 4 2 2
A错误;B.SO 可使品红褪色,因此可以用品红验证SO 的漂白性,B正确;
2 2
C.SO 的密度大于空气,应使用向上排空气法收集,瓶中导管应长进短出,C错误;
2
D.SO 需用强碱(如NaOH)等物质吸收,SO 难溶于饱和NaHSO 溶液,即饱和NaHSO 不能吸收SO ,
2 2 3 3 2
D错误;
故选B。
3.(2021·江苏省天一中学高一期中)将足量的SO 通BaCl 溶液中无明显现象,当加入(或通入)某试剂
2 2
(或气体)X后,有沉淀生成。此试剂(或气体)X可能是
①NaOH溶液②NaNO 溶液③KSO 溶液④新制氯水⑤HS⑥CO
3 2 4 2 2
A.①② B.①②③④⑤ C.②③⑤⑥ D.④⑤⑥
【答案】B
【解析】①当加入NaOH溶液时,SO 与NaOH反应可生成NaSO ,与BaCl 溶液不反应生成BaSO 沉淀,
2 2 3 2 3
①项正确;
②当加入NaNO 溶液时,SO 溶于水显酸性,NO -在酸性条件下具有强氧化性,混合溶液中会生成BaSO
3 2 3 4
沉淀,②项正确;
③当加入KSO 溶液会引入SO 2-,与Ba2+会形成BaSO 沉淀,③项正确;
2 4 4 4
④新制氯水可将SO 氧化为SO 2-,进而生成BaSO 沉淀,④项正确;
2 4 4
⑤HS能与SO 反应生成不溶性的S单质,⑤项正确;
2 2
⑥CO 不能与SO 、BaCl 溶液发生反应,⑥项错误;
2 2 2
综上所述,①②③④⑤符合题意,B项正确;答案选B。
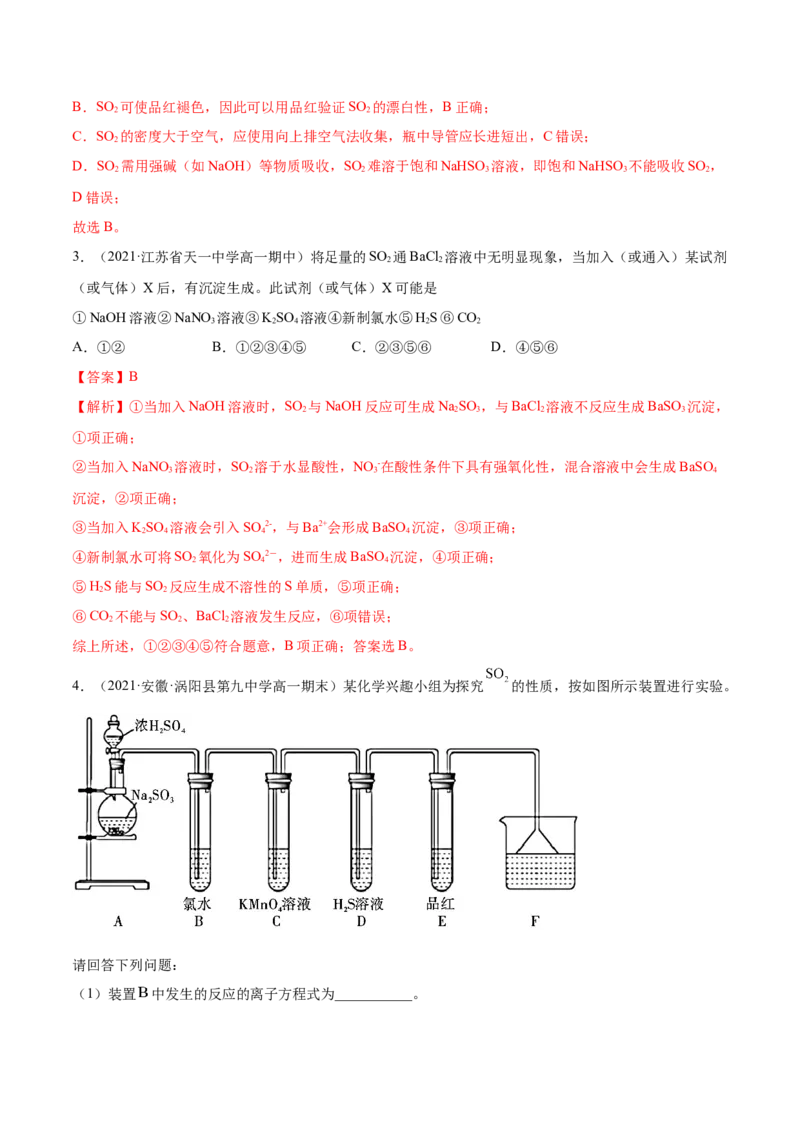
4.(2021·安徽·涡阳县第九中学高一期末)某化学兴趣小组为探究 的性质,按如图所示装置进行实验。
请回答下列问题:
(1)装置 中发生的反应的离子方程式为___________。(2)装置C中的现象是___________,表现了 的___________性。
(3)装置D中发生反应的化学方程式为___________。
(4)装置F中漏斗的作用是___________。
【答案】(1)
(2) 紫色溶液褪色(或颜色变浅) 还原
(3)
(4)防止倒吸
【解析】(1)装置B中氯水具有强氧化性,能将SO 氧化,故反应的离子方程式为
2
,故答案为: ;
(2)高锰酸钾溶液具有强氧化性,能将SO 氧化成硫酸根离子,因此装置C中的现象是紫色褪去,体现
2
了SO 的还原性,故答案为:溶液的紫色褪去或溶液褪色;还原;
2
(3)装置D中SO 与HS发生反应:SO +2H S=3S↓+2H O,观察到的现象是有黄色沉淀生成,故答案为:
2 2 2 2 2
SO +2H S=3S↓+2H O;
2 2 2
(4)SO 有毒,污染环境,需要尾气处理,装置F的作用是吸收多余的SO ,防止污染空气,其中漏斗的
2 2
作用是防止倒吸,故答案为:防止污染空气。
考点三 二氧化硫与三氧化硫
【例3-1】(2021·全国·高一课时练习)将SO 和SO 两种气体的混合物通入BaCl 溶液中,其结果是(
2 3 2
)
A.两种气体都被吸收,并有BaSO 沉淀生成
4
B.只有 BaSO 沉淀,SO 通入溶液中无沉淀生成
3 3
C.生成 BaSO 和BaSO 两种沉淀
3 4
D.只生成BaSO 沉淀,SO 从溶液中逸出
4 2
【答案】D
【解析】将SO 和SO 两种气体的混合物通入BaCl 溶液,由于盐酸的酸性大于亚硫酸,则SO 不反应,但
2 3 2 2
BaSO 不溶于酸,SO 与HO反应产生HSO ,HSO 与BaCl 发生复分解反应生成BaSO 沉淀和HCl,因
4 3 2 2 4 2 4 2 4
此最终结果是:生成BaSO 沉淀,SO 从溶液中逸出,故答案为D。
4 2
【例3-2】(2021·吉林·乾安县第七中学高一月考)已知SO 可与NaSO 溶液发生下列反应:NaSO +SO
2 2 3 2 3 2
+HO=2NaHSO 。欲除去SO 中混有的少量的SO 气体,可使气体通过
2 3 2 3A.澄清石灰水 B.饱和NaHSO 溶液
3
C.水 D.饱和NaHCO 溶液
3
【答案】B
【解析】A.SO 、SO 均属于酸性氧化物,都能与石灰水反应,达不到提纯的目的,故A不选;
2 3
B.SO +2NaHSO=Na SO +HO+2SO ↑,而SO 不与NaHSO 反应,可以除去SO 中混有的少量的SO 气
3 3 2 4 2 2 2 3 2 3
体,故B选;
C.三氧化硫与水反应生成硫酸,而SO 在水中溶解度为1∶40,溶解的太多,不符合物质提纯的要求,故
2
C不选;
D.SO 、SO 都能被饱和NaHCO 溶液吸收,另生成的CO 为新的气体杂质,达不到提纯的目的,故D不
2 3 3 2
选;
故选B。
【一隅三反】
1.(2021·广东·东莞市光明中学高一月考)下列有关SO 的说法中正确的是
3
A.SO 极易溶于水,且与水反应生成HSO
3 2 4
B.SO 是碱性氧化物
3
C.将SO 加入BaCl 溶液无明显现象
3 2
D.SO 、SO 均具有漂白性,能使紫色石蕊试液褪色
2 3
【答案】A
【解析】A.由三氧化硫物理性质可知,SO 极易溶于水,与水反应生成HSO ,故A正确
3 2 4 ;
B.SO 是酸性氧化物,故B错误;
3
C.将SO 加入BaCl 溶液中会生成白色沉淀,故C错误;
3 2
D.SO 有漂白性,但不能使紫色石蕊试液褪色,三氧化硫不具备漂白性,故D错误;故选A。
2
2.(2021·全国·高一课时练习)下列对SO 和SO 的叙述正确的是 ( )
2 3
A.通常条件下,SO 是无色、无味的气体,易溶于水
2
B.都是酸性氧化物,其水溶液都是强酸
C.都可使品红溶液褪色,加热时红色又能再现
D.都能跟碱液反应
【答案】D
【解析】A.二氧化硫是具有刺激性气味的气体,故A错误;B.SO +H O=HSO 、SO +H O=HSO ,二
2 2 2 3 3 2 2 4
氧化硫和三氧化硫都是酸性氧化物,但亚硫酸是弱酸、硫酸是强酸,故B错误;C.三氧化硫没有漂白性,
二氧化硫具有漂白性能使品红溶液褪色,但二氧化硫的漂白性不稳定,在加热条件下易恢复为原来颜色,故C错误;D.二氧化硫和三氧化硫都属于酸性氧化物,能和碱反应生成盐和水,故D正确;故选D。
3(2021·浙江·高一月考)SO 、SO 均为硫的氧化物,请回答下列问题。
2 3
(1)关于SO 和SO ,下列说法正确的是_______(填字母)。
2 3
a.都是酸性氧化物
b.都有氧化性
c.硫在纯氧中燃烧生成SO
3
d.都能使品红溶液褪色
(2)工业尾气中排放的SO 会导致酸雨,请从化合价和物质类别的角度,各列举一种试剂处理尾气中的
2
SO :_______、_______。
2
(3)将SO 通入FeCl 溶液中,下列实验事实能够证实SO 具有还原性的是_______(填字母)。
2 3 2
a.反应后溶液由黄色变为浅绿色
b.取反应后的溶液少许,加入BaCl 溶液,产生白色沉淀
2
c.取反应后的溶液少许,加入Ba(OH) 溶液,产生沉淀,加入足量盐酸后,沉淀部分溶解
2
【答案】(1)a b
(2) 酸性高锰酸钾等氧化剂均可 NaOH溶液、CaO等碱性溶液或碱性氧化物均可
(3) abc
【解析】(1)a.SO 和SO 分别是HSO 和HSO 对应的酸性氧化物,a正确;
2 3 2 3 2 4
b.SO 和SO 中S元素的价态分别为+4、+6价,都能降低,从而表现出氧化性,b正确;
2 3
c.硫在纯氧中燃烧只能生成SO ,不能生成SO ,c不正确;
2 3
d.SO 不能使品红溶液褪色,d不正确;
3
故选a b。答案为:a b;
(2)处理尾气中的SO 时,可利用强氧化剂,通过发生氧化还原反应除去SO ,如酸性高锰酸钾等氧化剂均
2 2
可;也可利用碱性物质,与SO 生成盐除去SO ,如NaOH溶液、CaO等碱性溶液或碱性氧化物均可。答
2 2
案为:酸性高锰酸钾等氧化剂均可;NaOH溶液、CaO等碱性溶液或碱性氧化物均可;
(3)a.反应后溶液由黄色变为浅绿色,表明Fe3+转化为Fe2+,证明SO 具有还原性,a符合题意;
2
b.加入BaCl 溶液,由于SO 不能生成白色沉淀,所以产生的白色沉淀一定是BaSO,则反应后的溶液中
2 2 4
含有HSO ,证明SO 具有还原性,b符合题意;
2 4 2
c.加入Ba(OH) 溶液,产生的沉淀可能是BaSO 也可能是BaSO,加入足量盐酸后,没有溶解的那部分沉
2 3 4
淀为BaSO,则反应后的溶液中含有HSO ,证明SO 具有还原性;
4 2 4 2
综合以上分析,abc都符合题意,故选abc。答案为:abc。
考点四 二氧化硫与二氧化碳【例4-1】(2021·安徽·马鞍山市教育科学研究院高一期末)下列溶液中能够区别SO 和CO 气体的是
2 2
①石灰水②氯水③酸性KMnO 溶液④BaCl 溶液⑤品红溶液
4 2
A.①③⑤ B.②③⑤ C.②④⑤ D.全部
【答案】B
【解析】①SO 和CO 都能使石灰水变浑浊,不能用石灰水鉴别SO 和CO,故不选①;
2 2 2 2
②SO 和氯水反应生成盐酸和硫酸,SO 使氯水褪色,CO 和氯水不反应,氯水能鉴别SO 和CO,故选②;
2 2 2 2 2
③SO 和酸性KMnO 溶液反应,SO 使酸性KMnO 溶液褪色,CO 和酸性KMnO 溶液不反应,酸性
2 4 2 4 2 4
KMnO 溶液能鉴别SO 和CO,故选③;
4 2 2
④SO 和CO 都不与BaCl 溶液反应,BaCl 溶液不能鉴别SO 和CO,故不选④;
2 2 2 2 2 2
⑤SO 能使品红溶液褪色,CO 不能使品红溶液褪色,品红溶液能鉴别SO 和CO,故选⑤;选B。
2 2 2 2
【例4-2】(2021·全国·高三专题练习)欲除去CO 中混有的少量SO 气体,可选用的试剂是
2 2
A.饱和食盐水 B.饱和NaHCO 溶液
3
C.足量澄清石灰水 D.NaOH溶液
【答案】B
【解析】A.SO 、CO 气体都能够在饱和食盐水中溶解,不能达到除杂的目的,A不符合题意;
2 2
B.SO 能够与饱和NaHCO 溶液反应产生CO 气体,能够达到除杂、净化的目的,B符合题意;
2 3 2
C.SO 、CO 气体都是酸性氧化物,二者都能够与足量澄清石灰水反应形成难溶性物质,不能达到除杂、
2 2
净化的目的,C不符合题意;
D.SO 、CO 气体都是酸性氧化物,二者都能够与NaOH水溶液反应形成盐,不能达到除杂、净化的目的,
2 2
D不符合题意;
故合理选项是B。
【例4-3】(2021·广东海丰·高一期中)某同学设计如图实验检验木炭与浓硫酸反应放出的气体是否有SO
2
和CO,下列说法错误的是
2A.木炭与浓硫酸反应,浓硫酸中的S元素被还原
B.当该反应转移4mol电子时,生成标准状况下的气体共67.2L
C.洗气瓶①②中溶液褪色,体现的二氧化硫的性质依次为漂白性、还原性
D.证明二氧化碳存在的现象为洗气瓶①中品红溶液不褪色,澄清石灰水变浑浊
【答案】D
【解析】A.木炭与浓硫酸反应生成CO、SO 和HO,化学方程式为
2 2 2
。在该反应中,C元素的化合价升高,被氧化,S元素的化合
价降低,被还原,A正确;
B.由化学方程式可知,每消耗1molC,转移4mol电子,生成1molCO 和2molSO ,在标准状况下的体积
2 2
为 ,B正确;
C.洗气瓶①中品红溶液褪色,体现了二氧化硫的漂白性,洗气瓶②中酸性高锰酸钾溶液褪色,体现了二
氧化硫的还原性,C正确;
D.当洗气瓶③中品红溶液不褪色时,证明SO 已被除尽,澄清石灰水变浑浊,即可证明有二氧化碳存在,
2
D错误;故选D。
【一隅三反】
1.(2021·重庆·高一期末)能鉴别CO 和SO 的试剂是
2 2
A.氯化钙溶液 B.澄清石灰水 C.紫色石蕊试液 D.溴水
【答案】D
【解析】A.碳酸、亚硫酸的酸性均小于盐酸,根据强酸制备弱酸的规律可知,CO 和SO 与氯化钙溶液均
2 2不发生反应,不能鉴别,故A不选;
B.CO 和SO 均属于酸性氧化物,均能与澄清石灰水反应产生白色沉淀,不能鉴别,故B不选;
2 2
C.CO 和SO 均属于酸性氧化物,溶于水后所得溶液均显酸性,均能使紫色石蕊试液变红,不能鉴别,故
2 2
C不选;
D.二氧化硫具有还原性,能够与溴水发生氧化还原反应,溴水褪色,而二氧化碳与溴水不反应,溴水不
能褪色,可以鉴别两种气体,故D选;故选D。
2.(2021·河北·石家庄市第二十一中学高一期中)检验SO 气体中是否含有CO 气体应用的方法是
2 2
A.通过石灰水
B.先通过酸性KMnO 溶液再通过石灰水
4
C.通过品红溶液
D.先通过小苏打浴液再通过石灰水
【答案】B
【解析】A.因SO 和CO 都能使石灰水变浑浊,所以无法检测出是否含有CO,故A不符合题意;
2 2 2
B.SO 具有还原性,能被酸性高锰酸钾溶液氧化,所以应先通过酸性KMnO 溶液除去SO ,再通过石灰
2 4 2
水,石灰水变浑浊证明含有CO 气体,故B符合题意;
2
C.SO 能使品红溶液褪色,CO 不能,只能检验气体中有SO ,但无法检测出是否含有CO,故C不符合
2 2 2 2
题意;
D.因SO 和碳酸氢钠反应也能生成CO,所以无法检测出是否含有CO,故D不符合题意。
2 2 2
本题答案B。
3.(2021·四川·雅安中学高一期中) 气体中含有少量的 ,欲用如图所示装置得到干燥、纯净的
,则下列叙述正确的是
A.先让混合气体通过盛有 溶液的洗气瓶①,再通过盛有浓 的洗气瓶②
B.先让混合气体通过盛有饱和 溶液的洗气瓶②,再通过盛有浓 的洗气瓶①C.先让混合气体通过盛有 溶液的洗气瓶②,再通过盛有浓 的洗气瓶①
D.先让混合气体通过盛有饱和 溶液的洗气瓶①,再通过盛有浓 的洗气瓶②
【答案】B
【解析】 气体中含有少量的 ,欲用如图所示装置得到干燥、纯净的 ,先用饱和碳酸氢钠溶液
除掉二氧化硫,再浓硫酸干燥,除杂及干燥时都是长进短出,因此先通过盛有饱和碳酸氢钠的洗气瓶②,
再通过盛有浓硫酸的洗气瓶①,故B符合题意。综上所述,答案为B。
4.(2021·云南·玉溪市江川区第二中学高一期末)某同学为了检验浓硫酸与木炭粉在加热条件下反应产生
的所有气体产物,选用了如图所示实验装置。
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式_____。
(2)①装置中观察到的现象是___;该现象证明____。
(3)②中酸性KMnO 溶液的作用是___,②中两次用到品红溶液,它们的作用分别是___。
4
(4)③中反应的离子方程式为____。
(5)上述实验体现SO 的性质有漂白性、还原性和___。
2
【答案】
(1)C+2H SO (浓) CO↑+2SO↑+2H O
2 4 2 2 2
(2) 无水硫酸铜由白色变成蓝色 证明反应中有水生成
(3) 除去气体产物中的SO 检验气体产物中是否有SO 、检验气体产物中的SO 是否除尽
2 2 2
(4)CO+Ca2++2OH-=CaCO ↓+H O
2 3 2
(5)酸性氧化物的通性
【解析】(1)浓硫酸和木炭粉在加热条件下发生反应,产生CO、SO 、HO,该反应的化学方程式为:
2 2 2C+2H SO (浓) CO↑+2SO↑+2H O;
2 4 2 2 2
(2)在装置①中白色无水硫酸铜遇水反应变为蓝色硫酸铜晶体,故①装置中观察到的现象是无水硫酸铜
由白色变成蓝色,这个实验证明C与浓硫酸反应中有水生成;
(3)②由于SO 具有还原性,可以被酸性KMnO 溶液氧化为硫酸而被除去,故②中酸性KMnO 溶液的作
2 4 4
用是除去气体产物中的SO ;
2
在②中两次用到品红溶液,第一次使用品红溶液是为了检验气体产物中是否有SO ;第二次使用品红溶液
2
是检验KMnO 溶液是否将气体产物中的SO 是否除尽;
4 2
(4)在③中CO 与Ca(OH) 反应,产生CaCO 沉淀和水,该反应的离子方程式为:CO+Ca2++2OH-
2 2 3 2
=CaCO ↓+H O;
3 2
(5)SO 能够使酸性KMnO 溶液褪色,体现了它的还原性;SO 使品红溶液褪色,体现了它的漂白性;
2 4 2
SO 能够与碱Ca(OH) 在溶液中发生反应产生CaSO 沉淀而使石灰水变浑浊而干扰CO 气体的检验,因此
2 2 3 2
在使用澄清石灰水检验CO 之前要先将其用酸性KMnO 溶液氧化除去,这又体现了SO 的酸性氧化物的通
2 4 2
性,故上述实验中体现SO 的性质有漂白性、还原性和酸性氧化物的通性。
2倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育