文档内容
第二节 乙烯与有机高分子材料
第 1 课时 乙烯
[核心素养发展目标] 1.掌握乙烯的组成及结构特点,体会结构决定性质的观念,增强“宏
观辨识与微观探析”的能力。2.掌握乙烯的化学性质,认识加成反应的特点,培养“证据推
理与模型认知”能力。3.了解乙烯在生产及生活中的应用,培养“科学态度与社会责任”。
(一)乙烯的分子组成与结构
空间充
分子式 电子式 结构式 结构简式 球棍模型
填模型
C H CH==CH
2 4 2 2
(二)乙烯的性质
1.乙烯的物理性质
颜色 状态 气味 水溶性 密度
无色 气体 稍有气味 难溶于水 比空气略小
2.乙烯的化学性质
(1)氧化反应
①燃烧:现象:火焰明亮,伴有黑烟。
化学方程式:C H+3O――→2CO+2HO。
2 4 2 2 2
②和酸性KMnO 溶液反应
4
现象:酸性KMnO 溶液褪色。
4
结论:乙烯能被酸性KMnO 溶液氧化。
4
(2)加成反应
①将乙烯通入溴的四氯化碳溶液中
现象:溴的四氯化碳溶液褪色。
化学方程式: 。
②加成反应定义:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合
物的反应。
书写下列加成反应的化学方程式:(3)聚合反应
①定义:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。
②乙烯自身加成生成聚乙烯的方程式:
该反应是聚合反应,同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
其中,—CH—CH—称为链节,n称为聚合度,小分子乙烯称为聚乙烯的单体。
2 2
(三)乙烯的用途
1.乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。乙烯的
产量可以用来衡量一个国家的石油化工发展水平。
2.在农业生产中用作植物生长调节剂。
(1)乙烯的结构简式可书写为CHCH( × )
2 2
提示 乙烯分子中含有 ,在书写时,官能团 不能省略,应为CH==CH。
2 2
(2)乙烯是一种无色无味,易溶于水的气体( × )
提示 乙烯是一种稍有气味,难溶于水的气体。
(3)乙烯的化学性质比乙烷活泼( √ )
(4)乙烯能使酸性KMnO 溶液和溴水褪色,反应原理相同( × )
4
提示 乙烯使酸性KMnO 溶液褪色发生的是氧化反应,乙烯使溴水褪色发生的为加成反应。
4
(5)乙烯聚合生成聚乙烯,本质是每个乙烯分子中的碳碳双键的一个键断裂,相互结合生成
聚乙烯,因此也称为加聚反应( √ )
1.已知乙烯分子中两个碳原子和四个氢原子同在一个平面内,推测丙烯(CH==CH—CH )分
2 3
子中最多有几个原子共面?
提示 丙烯可以认为乙烯分子中的一个氢原子被—CH 取代,且碳碳单键可以旋转,故可以
3
将甲基上的一个H原子旋入面内,故丙烯分子中最多有7个原子共面。
2.体育比赛中当运动员肌肉挫伤或扭伤时,队医随时对准运动员受伤部位喷射药剂氯乙烷
(CHCHCl)(沸点为12.27 ℃)进行局部冷却麻醉应急处理,工业上制取氯乙烷有两种方案:
3 2
a.CH CH+Cl――→CHCHCl+HCl
3 3 2 3 2
b.CH ==CH+HCl――→CH—CHCl
2 2 3 2你认为制备氯乙烷的最好方案为________(填“a”或“b”),并说出选择该方案及不选择另
一方案的理由。
提示 最好方案为b。
理由:a方案中CHCH 和Cl 在光照条件下发生取代反应,反应产物中除CHCHCl和HCl
3 3 2 3 2
外,还有很多副产物(如CHCHCl 、 、CHCl CHCl、CHCl CHCl 、CHCl CCl 、
3 2 2 2 2 2 2 3
CCl —CCl 等),产物不纯,产率低。
3 3
b方案中CH==CH 和HCl在一定条件下发生加成反应,产物中只有 CHCHCl,产品纯度
2 2 3 2
高、产率高。
3.某化工厂厂房有两罐失去标识的气体,分别是乙烷和乙烯,怎么用化学方法鉴别哪一罐是
乙烷气体或乙烯气体?请设计出实验方案。
提示 方案一,将两气体分别通入到溴水中,溴水褪色的为乙烯,则不褪色的为乙烷。
方案二,将两气体分别通入到酸性KMnO 溶液,紫红色褪色的为乙烯,不褪色的为乙烷。
4
方案三,将两气体分别在空气中燃烧,火焰明亮,且伴有黑烟的为乙烯,无黑烟的为乙烷。
4.含有碳碳双键的有机物很多,其性质和乙烯相似,写出下列要求的方程式。
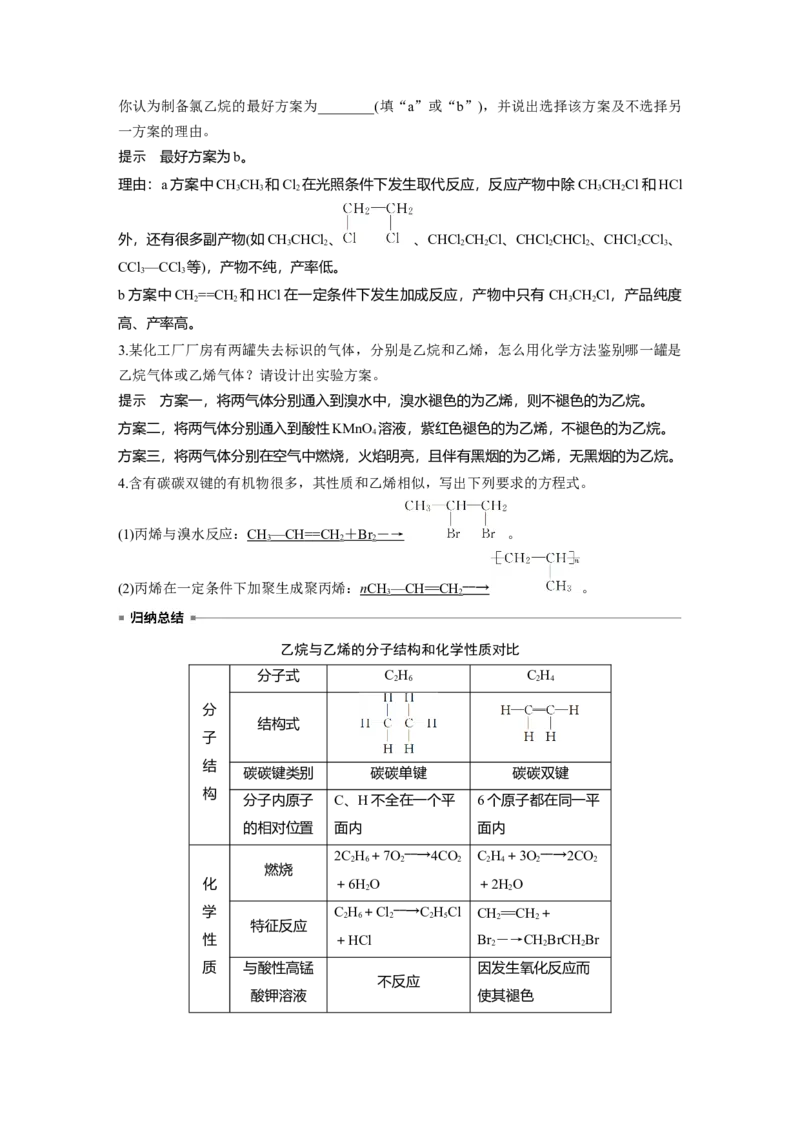
(1)丙烯与溴水反应:CH —CH = = CH + B r ― → 。
3 2 2
(2)丙烯在一定条件下加聚生成聚丙烯: n CH —CH == CH ――→ 。
3 2
乙烷与乙烯的分子结构和化学性质对比
分子式 C H C H
2 6 2 4
分
结构式
子
结
碳碳键类别 碳碳单键 碳碳双键
构
分子内原子 C、H不全在一个平 6个原子都在同一平
的相对位置 面内 面内
2C H+7O――→4CO C H+3O――→2CO
2 6 2 2 2 4 2 2
燃烧
化 +6HO +2HO
2 2
学 C 2 H 6 +Cl 2 ――→C 2 H 5 Cl CH 2 ==CH 2 +
特征反应
性 +HCl Br ―→CHBrCHBr
2 2 2
质 与酸性高锰 因发生氧化反应而
不反应
酸钾溶液 使其褪色1.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅土放置在盛放水果的容器中,其目的是
( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
答案 C
解析 水果释放出的乙烯是催熟剂,用KMnO 溶液来吸收乙烯,防止水果早熟。
4
2.(2019·自贡高一检测)能证明乙烯分子中含有一个碳碳双键的事实是( )
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO 和HO的物质的量相等
2 2
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO 溶液褪色
4
答案 C
解析 分子中的碳氢原子个数比只能说明烃的组成,不能说明其结构特点;燃烧产物的物质
的量相等和被酸性KMnO 溶液氧化,不能说明乙烯分子中含有一个碳碳双键;1 mol乙烯只
4
能与1 mol溴单质加成,说明乙烯分子中含有一个碳碳双键。
3.(2019·武汉高一期中)①②是两种常见烃的球棍模型,则下列叙述正确的是( )
A.都能在空气中燃烧
B.都能使酸性高锰酸钾溶液褪色
C.都能发生加成反应
D.等质量的①②完全燃烧时,产生CO 的量相同
2
答案 A
解析 由题图可知,①为乙烷,②为乙烯。乙烷不能使酸性高锰酸钾溶液褪色,而乙烯能,
B项错误;乙烷不能发生加成反应,而乙烯能,C项错误;乙烷和乙烯的摩尔质量不同,等
质量时二者的物质的量不同,产生CO 的量也不同,D项错误。
2
4.下列物质不可能是乙烯加成产物的是( )
A.CHCH B.CH CHCl
3 3 3 2
B.CH CHOH D.CHCHBr
3 2 3 2
答案 B
解析 A 项 CH==CH 和 H 加成可生成 CHCH ;C 项 CH==CH 和 HO 加成可生成
2 2 2 3 3 2 2 2CHCHOH;D项CH==CH 和HBr加成可生成CHCHBr;C项中两个氯原子在同一个碳上,
3 2 2 2 3 2
CH==CH 和任何含氯物质加成都不能生成,故选B。
2 2
课时对点练
A组 基础对点练
题组一 乙烯的组成与结构
1.下列分子中的各原子均在同一平面上的是( )
A.C H B.CH Cl
2 4 3
C.CH CH==CH D.CHCH
3 2 3 3
答案 A
解析 乙烯分子是一种平面结构,2个碳原子和4个氢原子在同一平面上。因为CH 是正四
4
面体结构,所以只要含有—CH 结构的分子就不可能所有原子在同一平面上。
3
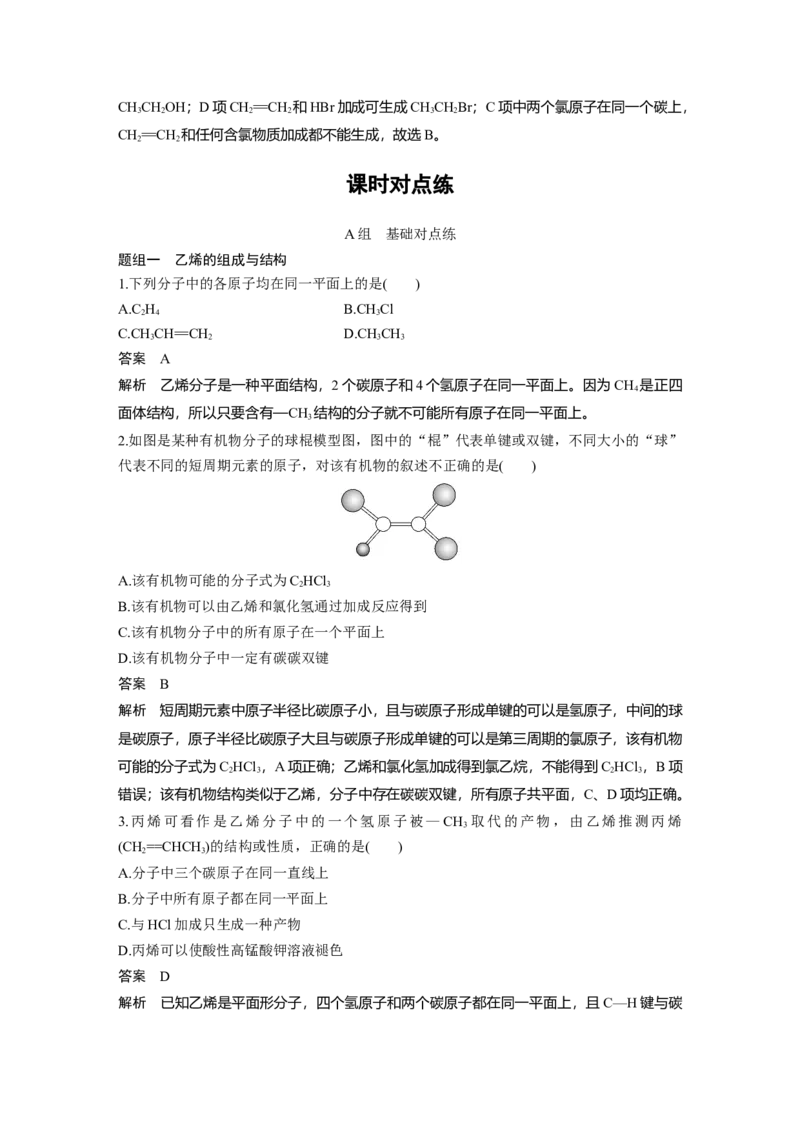
2.如图是某种有机物分子的球棍模型图,图中的“棍”代表单键或双键,不同大小的“球”
代表不同的短周期元素的原子,对该有机物的叙述不正确的是( )
A.该有机物可能的分子式为C HCl
2 3
B.该有机物可以由乙烯和氯化氢通过加成反应得到
C.该有机物分子中的所有原子在一个平面上
D.该有机物分子中一定有碳碳双键
答案 B
解析 短周期元素中原子半径比碳原子小,且与碳原子形成单键的可以是氢原子,中间的球
是碳原子,原子半径比碳原子大且与碳原子形成单键的可以是第三周期的氯原子,该有机物
可能的分子式为C HCl ,A项正确;乙烯和氯化氢加成得到氯乙烷,不能得到C HCl ,B项
2 3 2 3
错误;该有机物结构类似于乙烯,分子中存在碳碳双键,所有原子共平面,C、D项均正确。
3.丙烯可看作是乙烯分子中的一个氢原子被—CH 取代的产物,由乙烯推测丙烯
3
(CH==CHCH )的结构或性质,正确的是( )
2 3
A.分子中三个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.与HCl加成只生成一种产物
D.丙烯可以使酸性高锰酸钾溶液褪色
答案 D
解析 已知乙烯是平面形分子,四个氢原子和两个碳原子都在同一平面上,且C—H键与碳碳双键之间有夹角。丙烯可看作是—CH 取代乙烯分子上的一个氢原子的产物,因而三个碳
3
原子不在同一直线上。因甲基为四面体形,故所有原子一定不在同一平面上。甲基引入后,
双键两侧碳原子所处位置不同,与 HCl 加成产物应有两种情况:CHCHCH—Cl 和
3 2 2
。
题组二 乙烯的性质和用途
4.(2019·济南一中高一月考)有关乙烯的下列叙述:①乙烯溶于水后可得乙醇;②乙烯燃烧时
产生淡蓝色火焰;③乙烯能与溴水发生加成反应;④乙烯是无色、稍有气味、难溶于水的气
体。正确的是( )
A.③④ B.①③
C.②③ D.②③④
答案 A
解析 乙烯和水发生加成反应需要催化剂等条件,①错误;乙烯燃烧时火焰较明亮,并伴有
黑烟,②错误;乙烯分子中有碳碳双键,能与溴水发生加成反应,③正确;乙烯是无色、稍
有气味、难溶于水的气体,④正确;A项正确。
5.(2019·重庆高一月考)以下的说法中错误的是( )
A.无论乙烯的加成,还是乙烷的取代反应都可制得溴乙烷
B.无论使用溴水或酸性KMnO 溶液都可以鉴别乙烯和乙烷
4
C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
答案 C
解析 乙烯与HBr发生加成反应生成溴乙烷,乙烷可与溴蒸气在光照条件下发生取代反应
生成溴乙烷,A正确;溴水或酸性KMnO 溶液均与乙烯反应而褪色,与乙烷均不反应,则
4
溴水或酸性KMnO 溶液都可以鉴别乙烯和乙烷,B正确;相同质量的乙烯和甲烷,含H的
4
质量不同,由H原子守恒可知,完全燃烧后生成的水的质量不同,C错误;乙烯分子中含碳
碳双键,乙烷分子中均为饱和键,则乙烯的化学性质比乙烷的化学性质活泼,D正确。
6.(2019·河南师大附中高一月考)乙烯是重要的工业原料,下列有关乙烯叙述不正确的是(
)
A.常温常压下是稍有气味的气体
B.能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.在一定条件下能够聚合生成聚乙烯
答案 C
解析 A项,乙烯分子中碳原子个数小于5,常温常压下是一种稍有气味的气体,不符合题
意;B项,乙烯能与溴发生加成反应,生成无色的 1,2-二溴乙烷,能使溴的四氯化碳溶液褪色,不符合题意;C项,乙烯含有双键,性质较活泼,能被酸性高锰酸钾溶液氧化而使酸性
高锰酸钾溶液褪色,符合题意;D项,乙烯含有双键,所以在一定条件下能发生加聚反应生
成聚乙烯,不符合题意。
7.由乙烯的结构和性质推测丙烯(CH==CH—CH )的结构或性质错误的是( )
2 3
A.能使酸性高锰酸钾溶液褪色,发生了氧化反应
B.能在空气中燃烧,伴有黑烟
C.能使溴的四氯化碳溶液褪色,发生加成反应
D.与HO在一定条件下能加成并只得到一种产物
2
答案 D
解析 丙烯与乙烯都含有碳碳双键结构,性质有相似之处。丙烯同样能使酸性高锰酸钾溶液
褪色发生氧化反应,A正确;丙烯与乙烯的元素组成是相同的,可以燃烧并伴有黑烟,B正
确;丙烯也能和溴的四氯化碳溶液发生加成反应,C正确。
题组三 加成反应概念理解及判断
8.下列各反应属于加成反应的是( )
A.CH+2O――→CO+2HO
4 2 2 2
B.CH CH==CH+Br ―→CHCHBr—CH Br
3 2 2 3 2
C.CH CHCH+Cl――→CHCHCHCl+HCl
3 2 3 2 3 2 2
D.CHCHCHCH――→CH==CH+CH—CH
3 2 2 3 2 2 3 3
答案 B
解析 CH 在O 中燃烧,是氧化反应,A项错误;CHCH==CH 与Br 发生的是加成反应,
4 2 3 2 2
B项正确;CHCHCH 与Cl 在光照条件下发生取代反应,C项错误;CHCHCHCH 发生
3 2 3 2 3 2 2 3
的是分解反应,D项错误。
9.(2019·广西南宁一中期中)某烯烃与H 加成后的产物为 ,则该烯
2
烃可能的结构简式有( )
A.1种 B.2种 C.3种 D.4种
答案 C
解析 将两个含有氢原子的碳原子之间的单键变双键即可,如 ,在
①②③④处均可使碳碳单键变为碳碳双键,但①②处位置是等效的,所以该烯烃可能的结构
简式有3种。
10.下列是关于有机物A的信息:
①能使溴的四氯化碳溶液褪色;②分子空间充填模型为 ;③能与水在一定条件下反应。
根据上述信息回答下列问题:(1)A与溴的四氯化碳溶液反应的生成物的名称为________________;写出在一定条件下,A
发生聚合反应生成高分子化合物的化学方程式:__________________________。
(2)A具有的性质是________________(填序号)。
①无色、稍有气味的气体 ②有毒 ③难溶于水 ④密度比空气大 ⑤能使酸性KMnO 溶
4
液和溴水褪色 ⑥一定条件下能与氢气反应
答案 (1)1,2-二溴乙烷
nCH==CH――→CH—CH
2 2 2 2
(2)①③⑤⑥
解析 由题给信息,有机物应为乙烯CH==CH ,可以和Br 、H 发生加成反应,也可以被
2 2 2 2
酸性KMnO 溶液氧化,还可以发生加聚反应生成聚乙烯。
4
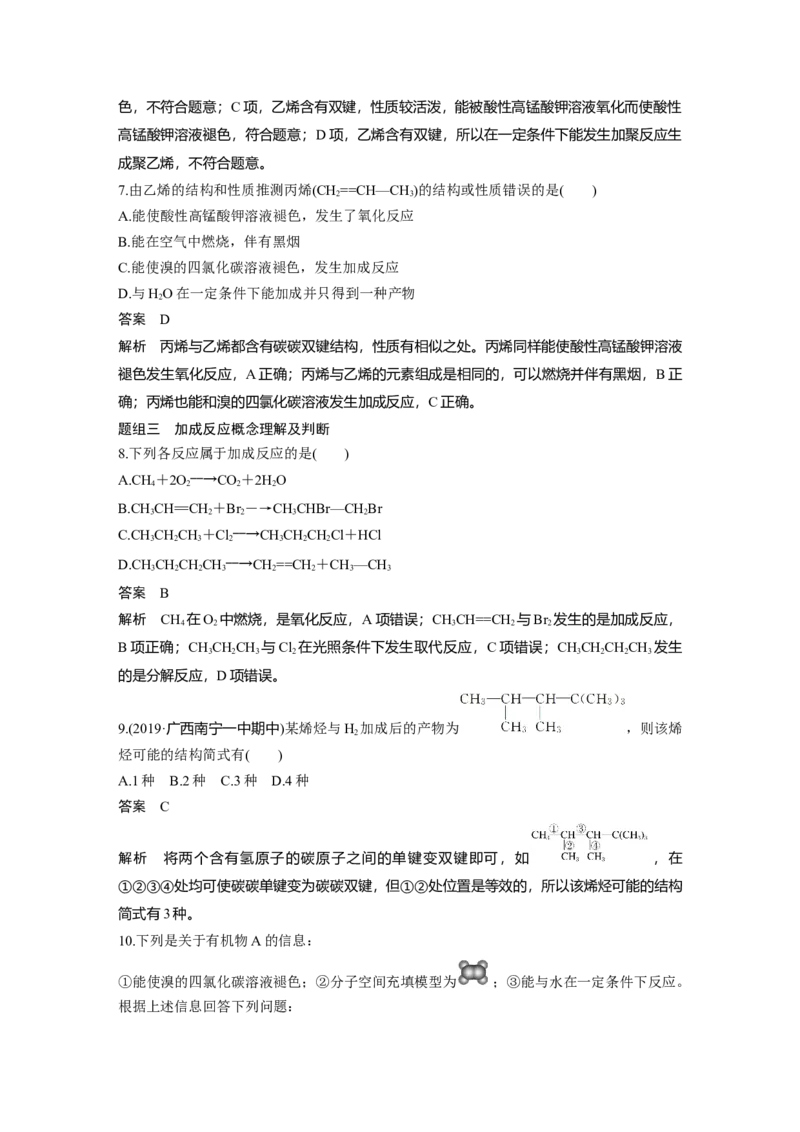
11.(2019·山西太原一中期末)乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙
烯的原理和乙烯的主要化学性质,实验装置如图所示。
(1)用化学反应方程式解释B装置中的实验现象:__________________________________。
(2)C装置中的现象是______________________,其发生反应的类型是________________。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
________(填序号)中的实验现象可判断该资料是否真实。
(4)通过上述实验探究可知,检验甲烷和乙烯的方法是______________(填字母,下同);除去
甲烷中乙烯的方法是____________。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
答案 (1)CH ==CH+Br ―→CHBr—CHBr
2 2 2 2 2
(2)酸性高锰酸钾溶液褪色 氧化还原反应
(3)D (4)BC B
解析 (1)乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,反应方程式为
CH==CH+Br ―→CHBr—CHBr。
2 2 2 2 2
(2)乙烯具有还原性,能够与酸性高锰酸钾溶液发生氧化还原反应而使酸性高锰酸钾溶液褪色。
(3)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙溶液反应生成碳
酸钙沉淀,溶液变浑浊。(4)A项,甲烷、乙烯均不溶于水,且常温下与水都不反应,不能用于鉴别和除杂。B项,乙
烯中含有C==C键,能与溴水发生加成反应生成1,2-二溴乙烷液体,甲烷不与溴水反应,所
以可用溴水除去甲烷中混有的乙烯,也可以鉴别甲烷与乙烯。C项,甲烷与高锰酸钾溶液不
反应,乙烯能够与高锰酸钾溶液反应而使其褪色,可以鉴别甲烷与乙烯;但是乙烯被氧化生
成二氧化碳气体,故不能用于除去甲烷中混有的乙烯杂质。D项,甲烷、乙烯都不溶于氢氧
化钠溶液,不能用来鉴别和除杂。综上所述,可用来鉴别的是B、C项,可用来除杂的是B
项。
B组 综合强化练
1.通常用乙烯的产量来衡量一个国家的石油化工发展水平,你认为其理由是( )
A.乙烯在自然界中大量存在,是一种廉价易得的化工原料
B.通过石油加工可获得乙烯,由乙烯可以合成许多化工产品
C.乙烯易燃烧,释放出的热量用于化工能源
D.乙烯性质活泼,易发生取代反应
答案 B
解析 乙烯主要来源于石油加工,所得乙烯能发生取代、加成等反应,可得到许多有机物,
所以乙烯的产量是一个国家石油化工发展水平的标志。
2.(2019·淄博高一检测)下列关于乙烯和乙烷的各种说法中,错误的是( )
A.乙烯是不饱和烃,乙烷是饱和烃
B.乙烯能使酸性高锰酸钾溶液和溴水褪色,乙烷则不能
C.乙烯分子中碳碳双键的键能是乙烷分子中碳碳单键的键能的两倍,因此乙烯比乙烷稳定
D.乙烯分子为平面结构,乙烷分子为立体结构
答案 C
解析 A项,乙烯含有碳碳双键,属于不饱和烃,乙烷属于饱和烃,正确;B项,乙烯易发
生加成反应,遇某些氧化剂发生氧化反应,正确;C项,乙烯分子中碳碳双键键能小于乙烷
分子中碳碳单键键能的两倍,错误;D项,甲烷是正四面体结构,所有原子不可能在同一平
面上,乙烯为平面结构,正确。
3.下列叙述错误的是( )
A.1 mol CH ==CH 先与HCl发生加成反应,再与Cl 发生取代反应,最多消耗Cl 2.5 mol
2 2 2 2
B.实验室中可用如图所示方法除去CHCH 气体中的CH==CH 气体
3 3 2 2
C.实验室中可用酸性的KMnO 溶液鉴别CHCH 气体和CH==CH 气体
4 3 3 2 2
D.工业上可利用CH==CH 与HCl的加成反应制得纯净的CHCHCl
2 2 3 2
答案 A解析 A项,CH==CH +HCl――→CHCHCl,CHCHCl+5Cl―→CCl CCl +5HCl,最多
2 2 3 2 3 2 2 3 3
消耗Cl 5 mol;B项,CHCH 气体不溶于溴水且不反应,CH==CH 气体在溴水中发生加
2 3 3 2 2
成反应生成液态CHBr—CHBr;C项,CHCH 气体不溶于酸性KMnO 溶液且不反应,
2 2 3 3 4
CH==CH 气体在酸性KMnO 溶液中被氧化,使酸性KMnO 溶液褪色;D项,CH==CH 与
2 2 4 4 2 2
HCl的加成反应生成唯一产物CHCHCl。
3 2
4.(2019·河南师大附中高一期末)下列各组物质在一定条件下反应,可以制得较纯净的 1,2-二
氯乙烷的是( )
A.乙烷与氯气在光照条件下反应
B.乙烯与氯化氢气体混合
C.乙烯与氯气混合
D.乙烯通入浓盐酸
答案 C
解析 乙烷与氯气在光照条件下发生取代反应,产生一氯乙烷、二氯乙烷等多种取代产物,
反应是同时进行的,因此不能制得较纯净的1,2-二氯乙烷,A项错误;乙烯与氯化氢气体混
合,发生加成反应产生一氯乙烷,B项错误;乙烯与氯气混合发生加成反应产生 1,2-二氯乙
烷,C项正确;乙烯通入浓盐酸不能发生反应,D项错误。
5.(2019·南昌一中高一联考)使1 mol乙烯与氯气发生完全加成反应,然后使该加成反应的产
物与氯气在光照的条件下发生完全取代反应,则两个过程中消耗氯气的总物质的量是( )
A.3 mol B.4 mol C.5 mol D.6 mol
答案 C
解析 1 mol乙烯与1 mol氯气发生完全加成反应生成1 mol CH ClCH Cl,1 mol CH ClCH Cl
2 2 2 2
中含有4 mol氢原子,与足量氯气在光照的条件下发生取代反应,要消耗4 mol氯气,即两
个过程中消耗氯气的总物质的量是5 mol。
6.(2019·泰安一中月考)角鲨烯是一种高度不饱和烃类化合物,最初是从鲨鱼的肝脏中发现的,
分子中含有多个双键,分子式为C H ,具有生物氧化还原作用,从而增强机体的耐力与改
30 50
善心脏功能,可用于癌症的防治,是一种无毒性的具有防病治病作用的海洋生物活性物质,
下列叙述中正确的是( )
①角鲨烯能使酸性KMnO 溶液褪色
4
②角鲨烯能与氢气发生加成反应
③角鲨烯只含碳、氢两种元素
④角鲨烯能使溴的CCl 溶液褪色
4
A.①②③ B.①③④
C.②③④ D.①②③④答案 D
解析 ①角鲨烯含双键,能使酸性KMnO 溶液褪色,故正确;②角鲨烯含双键,能与氢气
4
发生加成反应,故正确;③由分子式可知,角鲨烯只含碳、氢两种元素,故正确;④角鲨烯
中含双键,能和Br 发生加成反应,故正确。综上所述,D项正确。
2
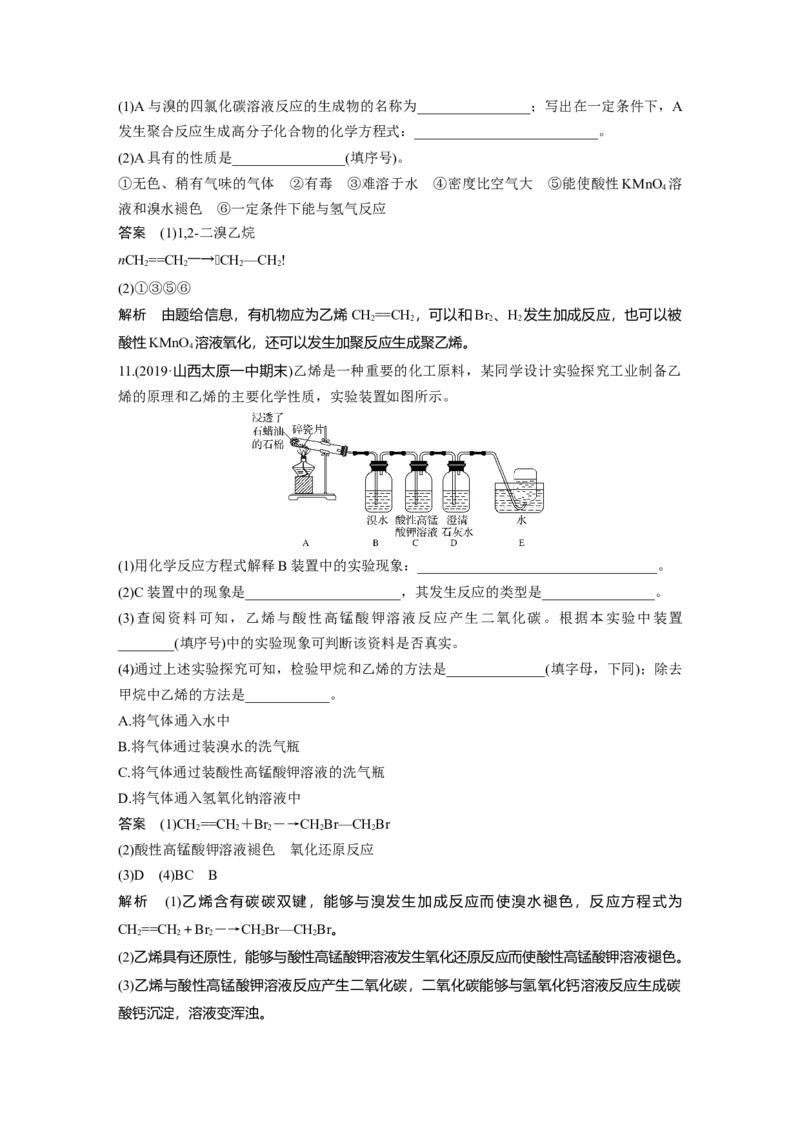
7.有人设计了如图所示实验,以确认某混合气体中含有CH==CH 和SO 。
2 2 2
实验中提供的试剂有:A.品红溶液 B.NaOH溶液
C.浓硫酸 D.酸性KMnO 溶液
4
试回答下列问题:
(1)写出图中①②③④装置盛放试剂的顺序为(将上述有关试剂的序号填入空格
内)________→________→________→________。
(2)能说明混合气体中存在SO 的现象是_________________________________________。
2
(3)能确定混合气体中存在乙烯的现象是_________________________________________。
(4)乙烯与溴水反应的化学方程式为________________________________,该反应的反应类
型为________。
答案 (1)A B A D
(2)①中品红溶液褪色
(3)③中的品红溶液不褪色,④中的酸性KMnO 溶液褪色
4
(4)CH ==CH+Br ―→CHBr—CHBr 加成反应
2 2 2 2 2
解析 检验SO 用品红溶液,检验C H 用酸性KMnO 溶液,C H 和SO 都能使酸性KMnO
2 2 4 4 2 4 2 4
溶液褪色,所以先检验 SO ,然后检验C H ,且在检验C H 之前需要用NaOH溶液除尽
2 2 4 2 4
SO ,再将气体通过品红溶液,若溶液不褪色,则SO 已除干净,最后用酸性KMnO 溶液检
2 2 4
验C H 。(1)装置中盛放试剂的顺序为品红溶液、NaOH溶液、品红溶液、酸性KMnO 溶液。
2 4 4
(2)SO 可使品红溶液褪色,装置①中品红溶液褪色,可证明混合气体中存在SO 。(3)装置③
2 2
中品红溶液不褪色且装置④中酸性KMnO 溶液褪色说明混合气体中存在C H 。(4)C H 和溴
4 2 4 2 4
水中的溴单质发生加成反应:CH==CH+Br ―→ 。
2 2 2
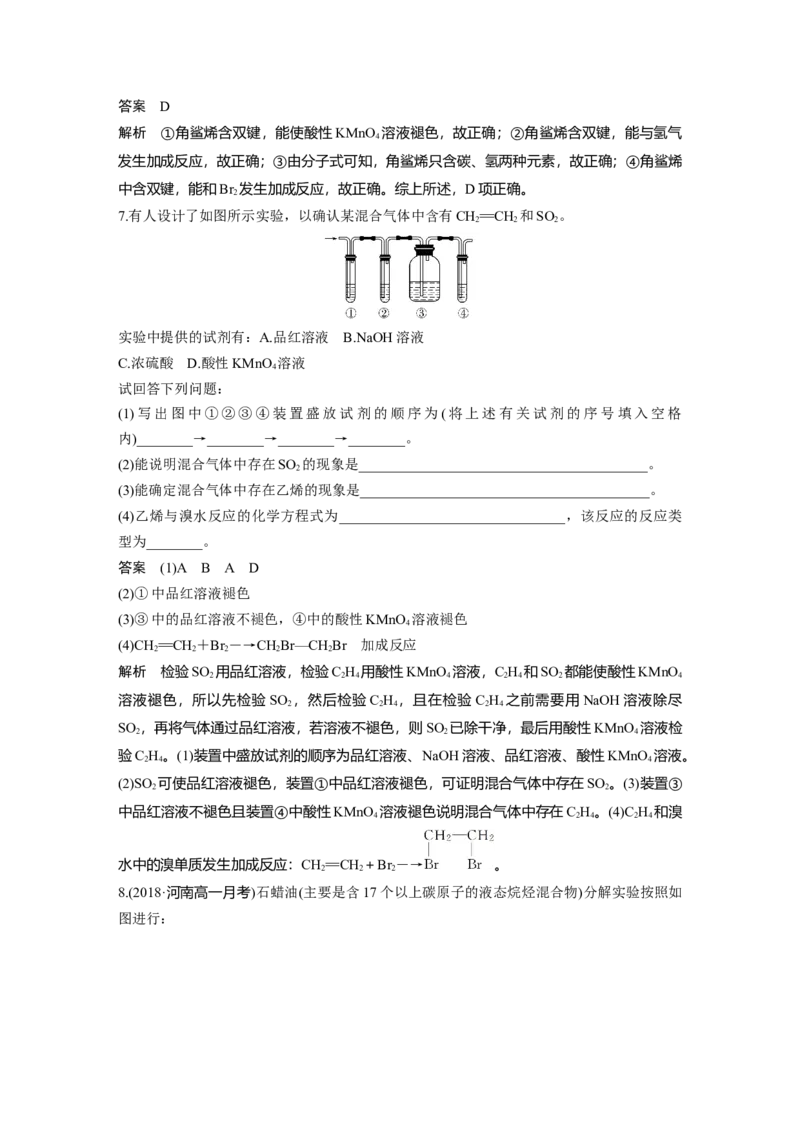
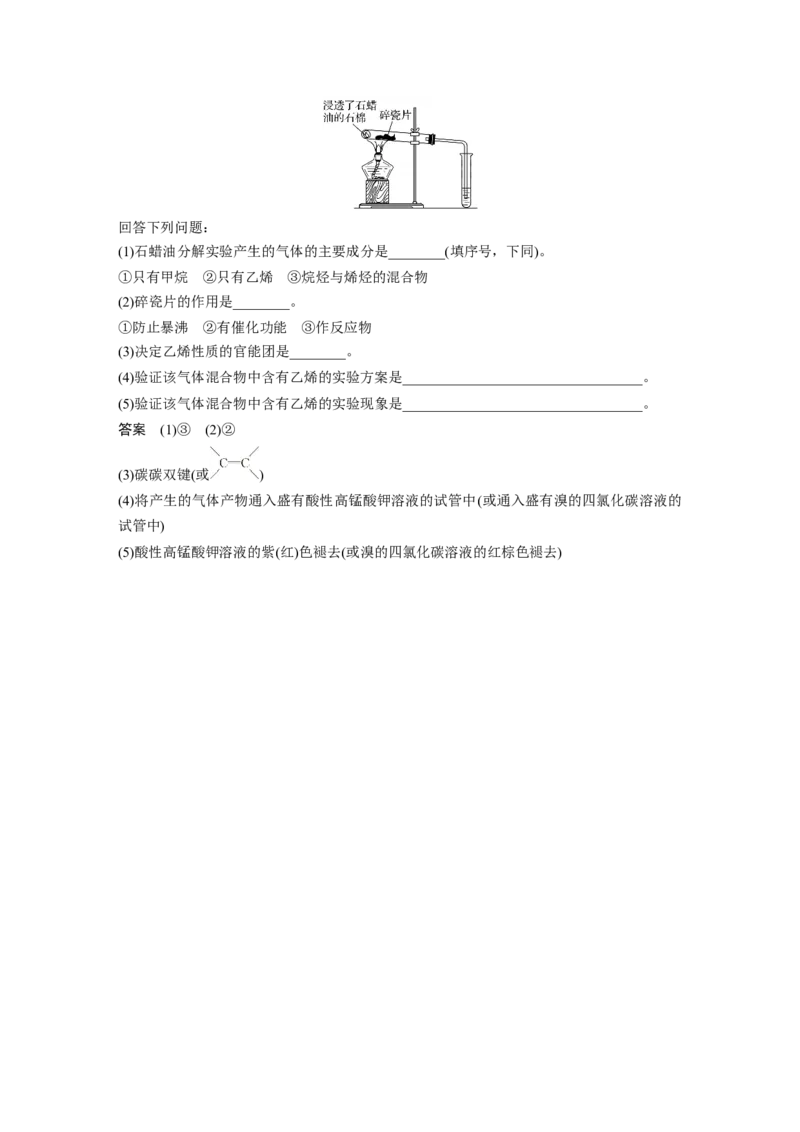
8.(2018·河南高一月考)石蜡油(主要是含17个以上碳原子的液态烷烃混合物)分解实验按照如
图进行:回答下列问题:
(1)石蜡油分解实验产生的气体的主要成分是________(填序号,下同)。
①只有甲烷 ②只有乙烯 ③烷烃与烯烃的混合物
(2)碎瓷片的作用是________。
①防止暴沸 ②有催化功能 ③作反应物
(3)决定乙烯性质的官能团是________。
(4)验证该气体混合物中含有乙烯的实验方案是__________________________________。
(5)验证该气体混合物中含有乙烯的实验现象是__________________________________。
答案 (1)③ (2)②
(3)碳碳双键(或 )
(4)将产生的气体产物通入盛有酸性高锰酸钾溶液的试管中(或通入盛有溴的四氯化碳溶液的
试管中)
(5)酸性高锰酸钾溶液的紫(红)色褪去(或溴的四氯化碳溶液的红棕色褪去)