文档内容
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
2021-2022 学年高二化学重难点专题突破
模块三 晶体结构与性质
专题 09 四类典型晶体的比较及应用
一.选择题
1.下面的排序不正确的是( )
A.熔点由高到低:Na>Mg>Al
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.晶体熔点由低到高:CF碳化硅>硅
答案:A
解析:A项,金属离子的电荷越多、半径越小,其熔点越高,则熔点由高到低为 Al>Mg>Na,错误;
B项,键长越短,共价键越强,硬度越大,键长C—C碳化硅>
晶体硅,正确;C项,组成和结构相似的分子,相对分子质量越大,范德华力越大,晶体的熔点越高,则
晶体熔点由低到高顺序为CF碳化硅>硅,A正确;。
2.下列晶体熔、沸点由高到低的顺序正确的是( )
①SiC ②Si ③HCl ④HBr ⑤HI ⑥CO ⑦N ⑧H
2 2
A.①②③④⑤⑥⑦⑧ B.①②⑤④③⑥⑦⑧
C.①②⑤④③⑦⑥⑧ D.⑥⑤④③②①⑦⑧
答案:B
解析:一般来说,晶体熔、沸点高低顺序是:原子晶体>离子晶体>分子晶体,原子晶体熔、沸点与键
长成反比,分子晶体熔、沸点与相对分子质量成正比,但含有氢键的熔、沸点较高,SiC和Si是原子晶体,
熔、沸点较高,键长Si—CSi;剩余这些物质都是分子晶体,且都不含氢键,
相对分子质量大小顺序是⑤④③⑥⑦⑧,氮气为非极性分子、CO为极性分子,极性分子熔、沸点高于非
极性分子,所以所有物质熔、沸点高低顺序是①②⑤④③⑥⑦⑧。
3.下列物质的熔沸点高低顺序正确的是( )
A.金刚石>晶体硅>二氧化硅>碳化硅
B.CI >CBr >CCl >CH
4 4 4 4
C.MgO>H O>N>O
2 2 2
D.金刚石>生铁>纯铁>钠
答案:B
解析:原子晶体中共价键的键长越短,键能越大,熔沸点越高,则熔沸点为金刚石>二氧化硅>碳化硅
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
>晶体硅,A 错误;结构相似的分子晶体,相对分子质量越大,熔沸点越高,则熔沸点为
CI >CBr >CCl >CH ,B正确;离子晶体的熔沸点大于分子晶体,水中含有氢键,沸点比氮气、氧气的高,
4 4 4 4
则熔沸点为MgO>H O>O>N ,C错误;熔沸点一般为原子晶体>金属晶体,合金的熔点比纯金属的低,则
2 2 2
熔沸点为金刚石>纯铁>生铁>钠,D错误。
4.下列物质性质的变化规律,与共价键的键能大小有关的是( )
A.F、Cl、Br 、I 的熔点、沸点逐渐升高
2 2 2 2
B.HF、HCl、HBr的熔、沸点顺序为HF>HBr>HCl
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
答案:C
解析:A项、B项中分子晶体熔、沸点高低与分子间的作用力有关,含有氢键时会出现反常现象,与
分子内共价键无关。D项离子晶体内存在的是离子键。
5.下列各组物质中,按熔点由低到高的顺序排列正确的是( )
①O、I、Hg ②CO、KCl、SiO
2 2 2
③Na、K、Rb ④Na、Mg、Al
A.①③ B.①④
C.②③ D.②④
答案:D
解析:①中Hg在常温下为液态,而I 为固态,故①错误;②中SiO 为原子晶体,其熔点最高,CO是
2 2
分子晶体,其熔点最低,故②正确;③中Na、K、Rb价电子数相同,其原子半径依次增大,金属键依次
减弱,熔点逐渐降低,故③错误;④中Na、Mg、Al价电子数依次增多,原子半径逐渐减小,金属键依次
增强,熔点逐渐升高,故④正确。
6.下列各物质的晶体中,晶体类型相同的是( )
A.O 和SiO B.NaI和I
2 2 2
C.CO 和HO D.CCl 和NaCl
2 2 4
答案:C
解析:A项,O 是分子晶体,SiO 是原子晶体;B项,NaI是离子晶体,I 是分子晶体;C项,CO 和
2 2 2 2
HO都是分子晶体;D项,CCl 是分子晶体,NaCl是离子晶体。
2 4
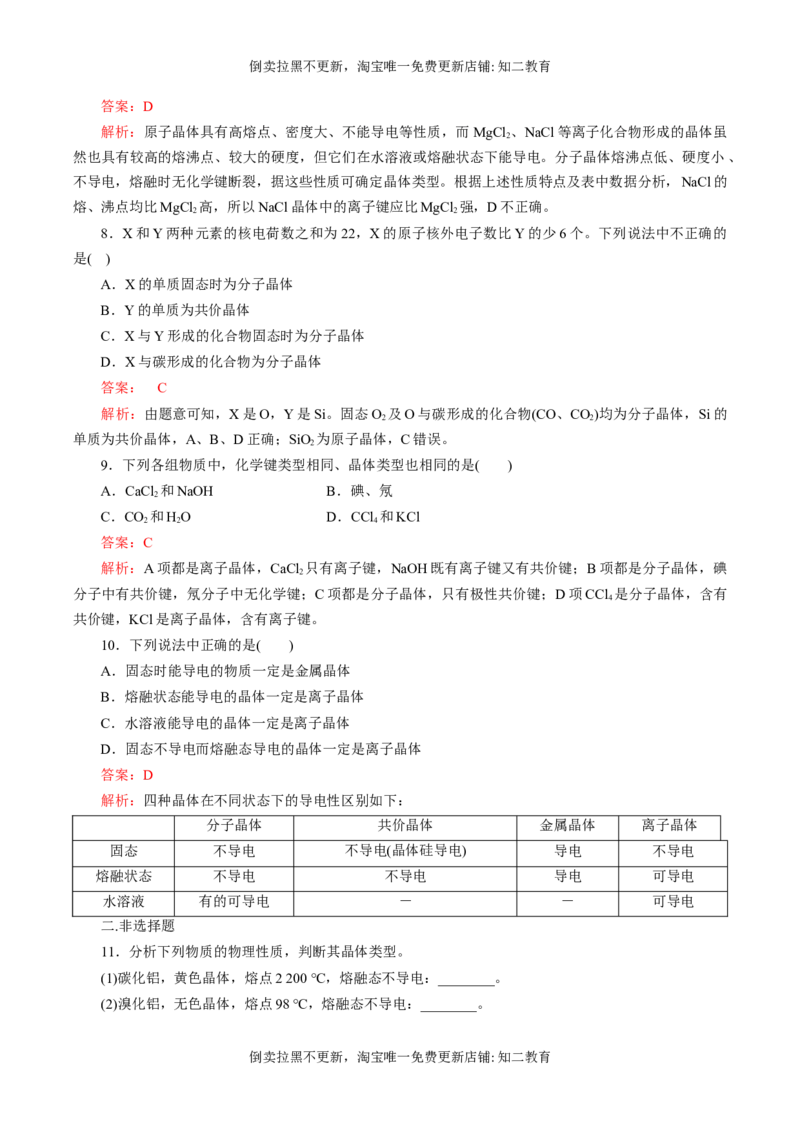
7.根据下列几种物质的熔点和沸点数据,判断下列有关说法中,错误的是( )
NaCl MgCl AlCl SiCl 单质B
2 3 4
熔点/℃ 810 710 190 -68 2 300
沸点/℃ 1 465 1 418 182.7 57 2 500
A.SiCl 是分子晶体
4
B.单质B是原子晶体
C.AlCl 加热能升华
3
D.MgCl 所含离子键的强度比NaCl大
2
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
答案:D
解析:原子晶体具有高熔点、密度大、不能导电等性质,而MgCl 、NaCl等离子化合物形成的晶体虽
2
然也具有较高的熔沸点、较大的硬度,但它们在水溶液或熔融状态下能导电。分子晶体熔沸点低、硬度小、
不导电,熔融时无化学键断裂,据这些性质可确定晶体类型。根据上述性质特点及表中数据分析,NaCl的
熔、沸点均比MgCl 高,所以NaCl晶体中的离子键应比MgCl 强,D不正确。
2 2
8.X和Y两种元素的核电荷数之和为22,X的原子核外电子数比Y的少6个。下列说法中不正确的
是( )
A.X的单质固态时为分子晶体
B.Y的单质为共价晶体
C.X与Y形成的化合物固态时为分子晶体
D.X与碳形成的化合物为分子晶体
答案: C
解析:由题意可知,X是O,Y是Si。固态O 及O与碳形成的化合物(CO、CO)均为分子晶体,Si的
2 2
单质为共价晶体,A、B、D正确;SiO 为原子晶体,C错误。
2
9.下列各组物质中,化学键类型相同、晶体类型也相同的是( )
A.CaCl 和NaOH B.碘、氖
2
C.CO 和HO D.CCl 和KCl
2 2 4
答案:C
解析:A项都是离子晶体,CaCl 只有离子键,NaOH既有离子键又有共价键;B项都是分子晶体,碘
2
分子中有共价键,氖分子中无化学键;C项都是分子晶体,只有极性共价键;D项CCl 是分子晶体,含有
4
共价键,KCl是离子晶体,含有离子键。
10.下列说法中正确的是( )
A.固态时能导电的物质一定是金属晶体
B.熔融状态能导电的晶体一定是离子晶体
C.水溶液能导电的晶体一定是离子晶体
D.固态不导电而熔融态导电的晶体一定是离子晶体
答案:D
解析:四种晶体在不同状态下的导电性区别如下:
分子晶体 共价晶体 金属晶体 离子晶体
固态 不导电 不导电(晶体硅导电) 导电 不导电
熔融状态 不导电 不导电 导电 可导电
水溶液 有的可导电 - - 可导电
二.非选择题
11.分析下列物质的物理性质,判断其晶体类型。
(1)碳化铝,黄色晶体,熔点2 200 ℃,熔融态不导电:________。
(2)溴化铝,无色晶体,熔点98 ℃,熔融态不导电:________。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
(3)五氟化矾,无色晶体,熔点19.5 ℃,易溶于乙醇、氯仿、丙酮等:________。
(4)溴化钾,无色晶体,熔融时或溶于水中都能导电:________。
(5)SiI:熔点120.5 ℃,沸点287.4 ℃,易水解:________。
4
(6)硼:熔点2 300 ℃,沸点2 550 ℃,硬度大:________。
(7)硒:熔点217 ℃,沸点685 ℃,溶于氯仿:________。
(8)锑:熔点630.74 ℃,沸点1 750 ℃,导电:________。
解析:晶体的熔点高低、熔融态能否导电及溶解性等性质相结合是判断晶体类型的重要依据。原子晶
体和离子晶体的熔点都很高或较高,两者最大的差异是熔融态的导电性不同。原子晶体熔融态不导电,离
子晶体熔融时或其水溶液都能导电。原子晶体和分子晶体的区别则主要在于熔、沸点有很大差异。一般原
子晶体和分子晶体熔融态时都不能导电。另外易溶于一些有机溶剂往往也是分子晶体的特征之一。金属晶
体能导电。
答案:(1)原子晶体 (2)分子晶体 (3)分子晶体
(4)离子晶体 (5)分子晶体 (6)原子晶体
(7)分子晶体 (8)金属晶体
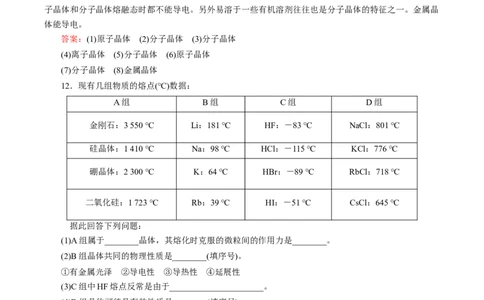
12.现有几组物质的熔点(℃)数据:
A组 B组 C组 D组
金刚石:3 550 ℃ Li:181 ℃ HF:-83 ℃ NaCl:801 ℃
硅晶体:1 410 ℃ Na:98 ℃ HCl:-115 ℃ KCl:776 ℃
硼晶体:2 300 ℃ K:64 ℃ HBr:-89 ℃ RbCl:718 ℃
二氧化硅:1 723 ℃ Rb:39 ℃ HI:-51 ℃ CsCl:645 ℃
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________。
(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于______________________。
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D 组 晶 体 的 熔 点 由 高 到 低 的 顺 序 为 NaCl>KCl>RbCl>CsCl , 其 原 因 为
_______________________________________。
解析:(1)A 组熔点很高,为原子晶体,是由原子通过共价键形成的。(2)B 组为金属晶体,具有
①②③④四条共性。(3)HF中含有分子间氢键,故其熔点反常。(4)D组属于离子晶体,具有②④两条性质。
(5)D组属于离子晶体,其熔点与晶格能有关。
答案:(1)原子 共价键 (2)①②③④
(3)HF分子间能形成氢键,其熔化时需要消耗的能量更多(只要答出HF分子间能形成氢键即可)
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
(4)②④
(5)D组晶体都为离子晶体,r(Na+)氯酸钾>碘
(2)①<⑤<③<②<④<⑥
(3)H 氯酸钾>碘。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
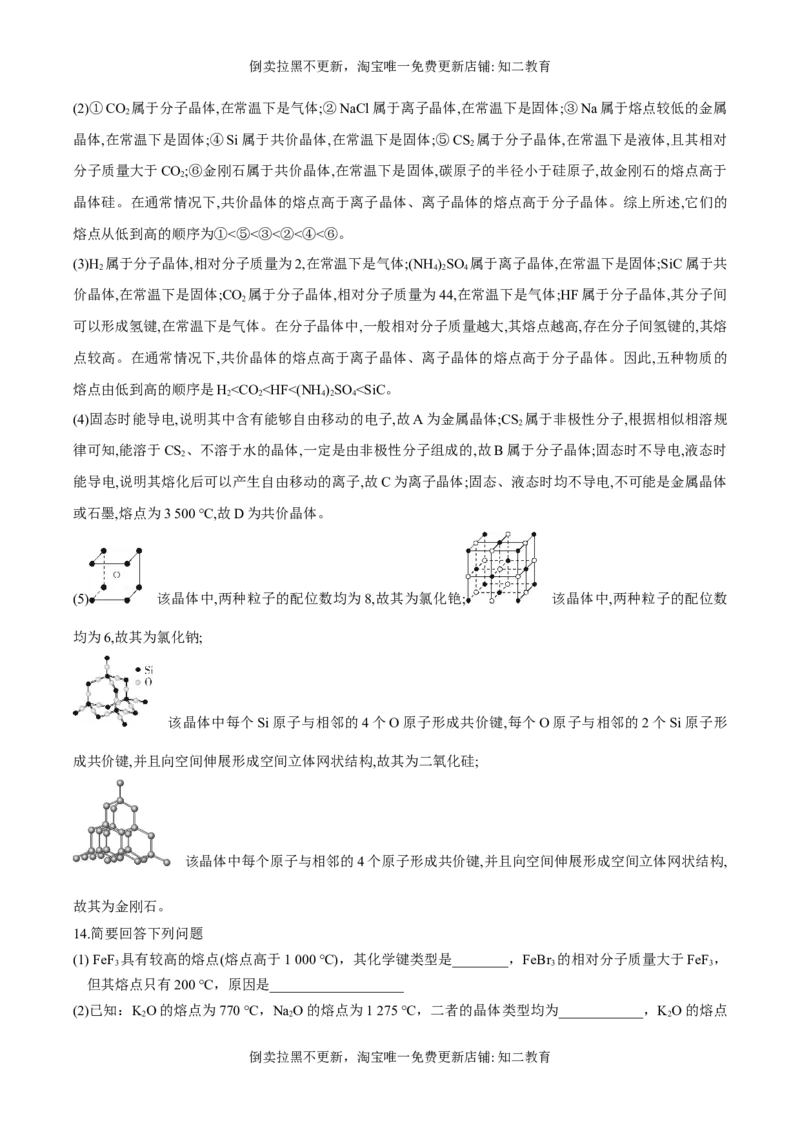
(2)①CO 属于分子晶体,在常温下是气体;②NaCl属于离子晶体,在常温下是固体;③Na属于熔点较低的金属
2
晶体,在常温下是固体;④Si属于共价晶体,在常温下是固体;⑤CS 属于分子晶体,在常温下是液体,且其相对
2
分子质量大于CO;⑥金刚石属于共价晶体,在常温下是固体,碳原子的半径小于硅原子,故金刚石的熔点高于
2
晶体硅。在通常情况下,共价晶体的熔点高于离子晶体、离子晶体的熔点高于分子晶体。综上所述,它们的
熔点从低到高的顺序为①<⑤<③<②<④<⑥。
(3)H 属于分子晶体,相对分子质量为2,在常温下是气体;(NH )SO 属于离子晶体,在常温下是固体;SiC属于共
2 4 2 4
价晶体,在常温下是固体;CO 属于分子晶体,相对分子质量为44,在常温下是气体;HF属于分子晶体,其分子间
2
可以形成氢键,在常温下是气体。在分子晶体中,一般相对分子质量越大,其熔点越高,存在分子间氢键的,其熔
点较高。在通常情况下,共价晶体的熔点高于离子晶体、离子晶体的熔点高于分子晶体。因此,五种物质的
熔点由低到高的顺序是H”“<” 或 “ = ” ) , 理 由 是
___________________________________________________
(4)金属铼的熔点高于锰,试从原子结构的角度加以解释:_________________
(5)Cu O与Cu S比较,熔点较高的是__________,原因是
2 2
(6)砷化镓以第三代半导体著称,熔点为1 230 ℃,具有空间网状结构。已知氮化硼与砷化镓属于同种晶体
类型。则两种晶体熔点较高的是________________(填化学式),其理由是_____________________
(7)判断KCl、NaCl、CaO、BaO四种晶体熔点的高低顺序,并说明原因:
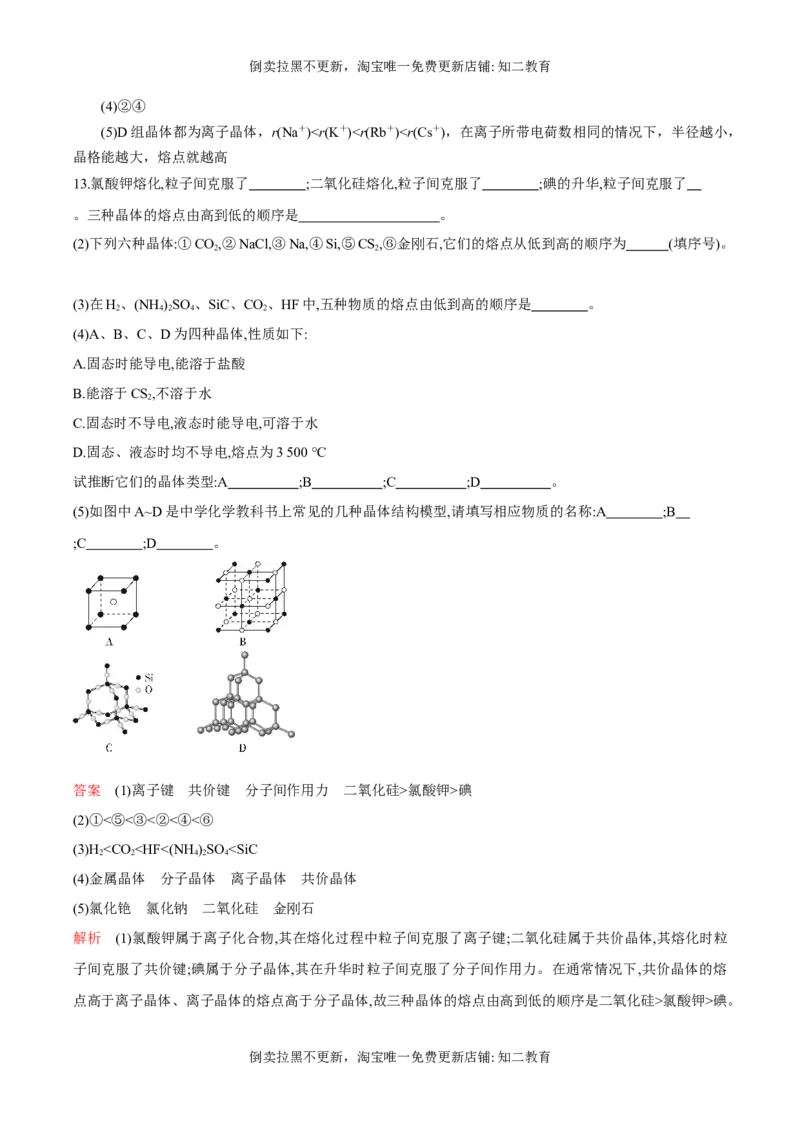
(8人工氮化钛晶体的晶胞与NaCl晶胞相似,如图所示。该晶体的熔点高于NaCl晶体的熔点,其原因是
__________________________________
答案 (1)离子键 FeF 为离子晶体,FeBr 的化学键以共价键为主,属于分子晶体
3 3
(2)离子晶体 K+的半径大于Na+,KO的晶格能小于NaO的
2 2
(3)> Mg2+半径比 Ni2+小, MgO的晶格能比 NiO大
(4)从锰到铼原子序数增大,原子核对外层电子引力增大,电子层数增多,原子核对外层电子引力减小,
但前者占主导,所以铼中的金属键更强,熔点更高
(5)Cu O两物质均为离子化合物,且离子带电荷数相同,O2-半径小于S2-,所以Cu O的晶格能大,熔
2 2
点更高
(6)BN 两种晶体均为原子晶体,N和B原子半径较小,键能较大,熔点更高
(7)CaO>BaO>NaCl>KCl四种物质皆为离子晶体,晶格能越大,晶体熔、沸点越高;离子所带电荷
数越多,半径越小,晶格能越大,因为r(K+)>r(Na+),r(Ba2+)>r(Ca2+),所以熔点的高低顺序为CaO>
BaO>NaCl>KCl
(8)氮化钛晶体中阴阳离子的电荷数均高于氯化钠晶体中阴阳离子的电荷数,氮化钛晶体的晶格能高于
氯化钠晶体的晶格能
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育